Aportaciones originales
Análisis de supervivencia a cinco años en pacientes con cáncer de pene*
Five-year survival analysis in patients with penile cancer
Análisis de supervivencia a cinco años en pacientes con cáncer de pene*
Revista Médica del Instituto Mexicano del Seguro Social, vol. 55, núm. 1, pp. 34-43, 2017
Instituto Mexicano del Seguro Social
Recepción: 15 Abril 2016
Aprobación: 15 Agosto 2016
Resumen:
Introducción: la sobrevida del cáncer de pene es pobre a corto plazo. El objetivo fue describir la supervivencia de pacientes con cáncer de pene a cinco años.
Métodos: estudio de cohorte retrospectivo. Se incluyeron pacientes con cáncer de pene manejados quirúrgicamente durante el periodo de 2010 a 2014. La estadística fue descriptiva y se usó el estimador de Kaplan-Meier para analizar la función de supervivencia.
Resultados: se estudiaron 22 pacientes, con edad media de 64.95 años y tiempo de evolución del cáncer al diagnóstico de 25 meses. El 68.2% era fumador o presentó VPH; todos tuvieron fimosis; 72.7% tuvo dolor en pene e ingle; 81.8% presentó ganglios palpables y 45.5% lesiones ≥ 3 cm. El 86.3% se diagnosticó en estadio clínico mayor de IIIa. Al 59.1% se le realizó penectomía parcial y 86.4% fue de variedad epidermoide. El 40.9% de los pacientes falleció a los seis meses después del tratamiento quirúrgico. El 66.6% de los fumadores presentó metástasis; todos los que presentaban tabaquismo más infección por VPH tuvieron invasión neurovascular y fallecieron. Al 83.3% (n = 6) de los pacientes a los que se les realizó penectomía parcial y disección ganglionar con ganglios positivos por metástasis fallecieron. La mortalidad fue de 40.9% a cinco años.
Conclusión: el tabaquismo y el VPH aumentan la morbimortalidad en pacientes con cáncer de pene; las lesiones mayores de 5 cm se presentan más en fumadores. El tamaño de la lesión aumenta con la demora diagnóstica.
Palabras clave: Cáncer de pene, Epidemiología, Supervivencia, Mortalidad.
Abstract:
Background: Short-term survival of penile cancer is poor. The objective was to describe the 5-years penile cancer survival.
Methods: Retrospective cohort study. We included patients with penile cancer managed surgically from 2010 to 2014. Descriptive statistics were used for socio-demographic variables and the Kaplan-Meier estimator for survival function.
Results: We studied 22 patients with a mean age of 64.95 years and a time of evolution of 25 months after the diagnosis. 68.2% of patients smoked or had human papillomavirus (HPV); they all presented phimosis; 72.7% had pain in the penis and the groin area; 81.8% had palpable lymph nodes and 45.5% lesions ≥ 3 cm; 86.3% were diagnosed in clinical stage IIIa. 59.1% underwent partial penectomy and 86.4% had squamous cell variety. 40.9% of patients died six months after the surgery. 66% of the smokers presented metastasis; all of the patients that smoked and had HPV infection had neurovascular invasion and died; 83.3% of the patients (n = 6) who underwent partial penectomy and positive lymph node dissection due to metastases died. The 5-years mortality of patients with penile cancer was 40.9%.
Conclusion: Tobacco use and HPV increase morbidity and mortality in patients with penile cancer; lesions greater than 5 cm are more common in smokers. The size of the lesion increases with the delay in treatment.
Keywords: Penile cancer, Epidemiology, Survival, Mortality.
Introducción
El cáncer de pene es una patología poco frecuente. En el Registro Histopatológico de Neoplasias Malignas del año 2003 de México se reportan 346 casos, con una incidencia de 0.91 por 100 000 varones, que representó el 0.31% del total de neoplasias malignas de ese año, mientras que la mortalidad ocurrió en 103 casos (tasa de mortalidad de 0.2 por 100 000 varones), representando el 0.17% de las muertes por cáncer en nuestro país.1,2,3En países desarrollados la mortalidad va de 0.1 a 0.7 por 100 000 habitantes y en España la tasa de prevalencia es de 0.7% de los tumores malignos del varón.4
Las lesiones con evolución de más de un año se presentan en pacientes con nivel socioeconómico bajo.4,5 Las guías de la National Comprehensive Cancer Network (NCCN)6 hacen recomendaciones según el estadio clínico y el grado de diferenciación celular. El factor de riesgo más importante para el desarrollo de cáncer de pene es un prepucio intacto, que en algunos pacientes puede o no estar asociado a la presencia de fimosis. Esta se encuentra en un rango que va del 25 al 60% de los pacientes con cáncer de pene.4,7
La presentación clínica varía, desde una lesión pequeña con induración hasta una lesión exofítica, papular, plana, ulcerada; el prurito, las parestesias en la piel del prepucio, la presencia de úlcera en el glande o en el prepucio son los síntomas más comunes. El dolor es inusual, lo que probablemente retrasa la atención médica. Otras formas de presentación son la diseminación linfática superficial y la diseminación profunda inguinal, con ganglios pélvicos que están asociados a la supervivencia de pacientes con cáncer de pene.8,9
La mayoría de las neoplasias de pene son carcinomas de células escamosas. Dentro de esta categoría existen distintos subtipos, cada uno con supervivencia diferente.10 La etapificación de los ganglios linfáticos tiene más relevancia que otros rubros (como el tamaño de la lesión) en la predicción pronóstica de la enfermedad.11,12,13,14,15,16 El examen físico y los métodos de imagen contribuyen al diagnóstico, el cual es confirmado por el estudio histopatológico. Los sistemas de etapificación dan la pauta para el tratamiento; en 1966 Jackson intentó clasificar el cáncer de pene. La clasificación TNM fue introducida en 1968 y posteriormente revisada en los años 1978, 1987 y 2002. La última actualización de la NCCN la hizo la American Joint on Cancer Committee (AJCC) en el 2012.6 En estos pacientes el tratamiento más eficaz es la cirugía.17,18,19,20,21
Debido a que el cáncer de pene es una patología poco común, con un pronóstico malo para la vida y con gran impacto psicológico y funcional para los pacientes con una sobrevida pobre a corto plazo,22,23,24,25,26,27,28 se decidió realizar este estudio cuyo objetivo es presentar las características clínicas y la supervivencia a cinco años en pacientes con cáncer de pene en un hospital de tercer nivel de atención médica.
Métodos
Se estudiaron 22 pacientes con cáncer de pene. La edad media fue 64.95 ± 14.14 años (mínima 30, máxima 93). Las características clínicas de los pacientes se muestran en el cuadro I.
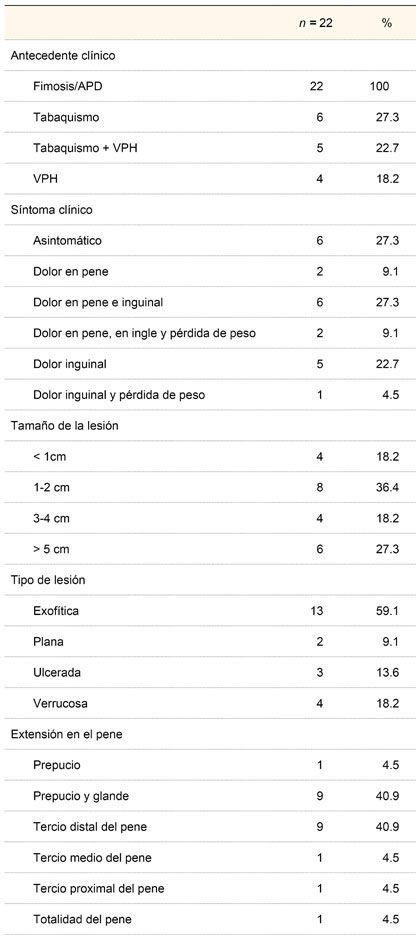
APD = diámetro anteroposterior (del inglés anteroposterior diameter)
La variedad epidermoide correspondió a 19 pacientes (86.4%), la sarcomatoide a 1 (4.5%) y la variedad verrucosa a 2 pacientes (9.1%). El detalle de los resultados histopatológicos y el estadio clínico de los pacientes se muestran en el cuadro II.
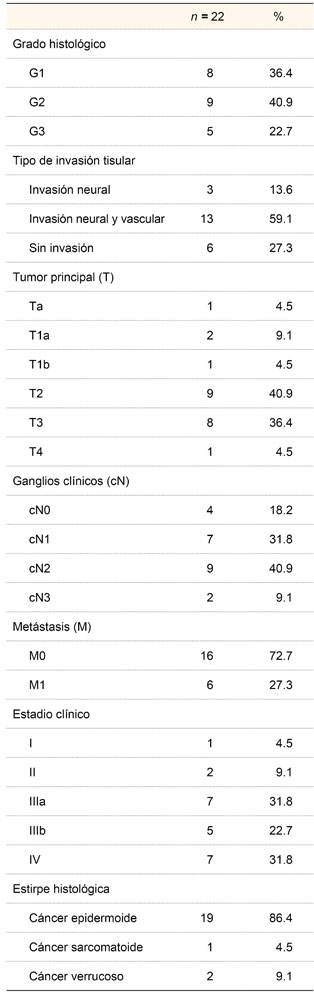
Cuatro pacientes (18.2%) tuvieron metástasis por tomografía, 2 por tomografía y telerradiografía de tórax (9.1%) y 16 (72.7%) no tuvieron evidencia de metástasis ni por tomografía ni por radiografía simple.
A un paciente (4.5%) se le realizó circuncisión ampliada, a 5 (22.7%) penectomía parcial, a 8 (36.4%) penectomía parcial con disección inguinal, a 1 (4.5%) penectomía radical más disección inguinal, a 2 (9.1%) penectomía total y a 5 (22.7%) penectomía total más disección inguinal. Al momento de realizar el estudio 13 pacientes (59.1%) estaban vivos. En los restantes, el motivo de la defunción fue un paciente por metástasis abdominal (4.5%), 7 por metástasis pulmonar (31.8%) y uno (4.5%) por otra causa distinta del cáncer de pene (síndrome de Fournier).
De los seis pacientes que tenían antecedentes clínicos relevantes (tabaquismo, virus del papiloma humano [VPH] y tabaquismo más VPH), se encontró que cinco (83.3%) tenían también lesiones mayores de 5 cm; de los que fumaron y tenían VPH positivo (n = 16), cuatro (25%) no tuvieron evidencia de metástasis; en cuanto al estadio clínico, cuatro tuvieron estadio IV (57.14%) de los pacientes que fumaron y dos (28.57%) de los que fumaron y tenían VPH positivo (n= 7); la invasión tisular se presentó en cinco pacientes que fumaron y tenían VPH positivo (38.46% de n = 13) y el motivo de defunción mayor fue la metástasis pulmonar en seis (85.71% de n= 7) de los pacientes que fumaron y fumaron con VPH positivo. Los detalles se muestran en el cuadro III.
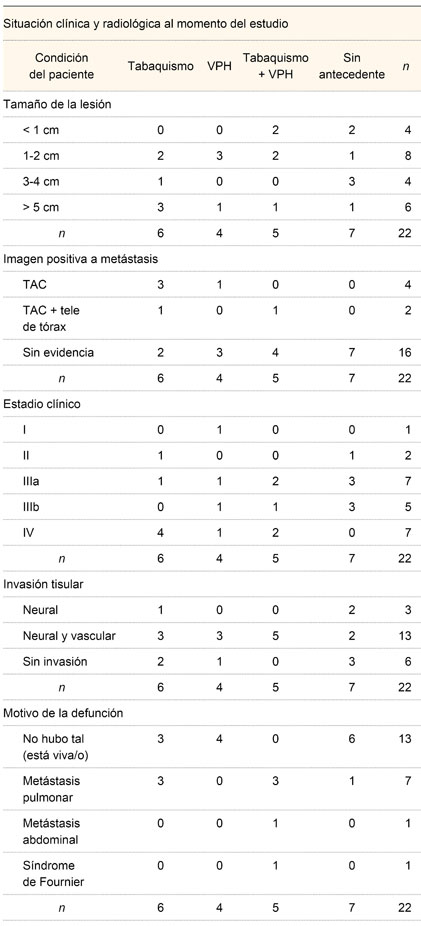
VPH = virus del papiloma humano; TAC = tomografía axial computarizada
La mediana de la supervivencia en los pacientes con cáncer de pene fue de 16 meses (mínima 10.15, máxima 21.84); a 10 meses fue de 95.5%, a 12 meses de 86.4%, a 16 meses de 77.3%, a 18 meses de 68.2%, a los 19 meses de 63.6% y a los 20 meses de 59.1%, la cual se mantuvo hasta los 60 meses (cuadro IV, figura 1).
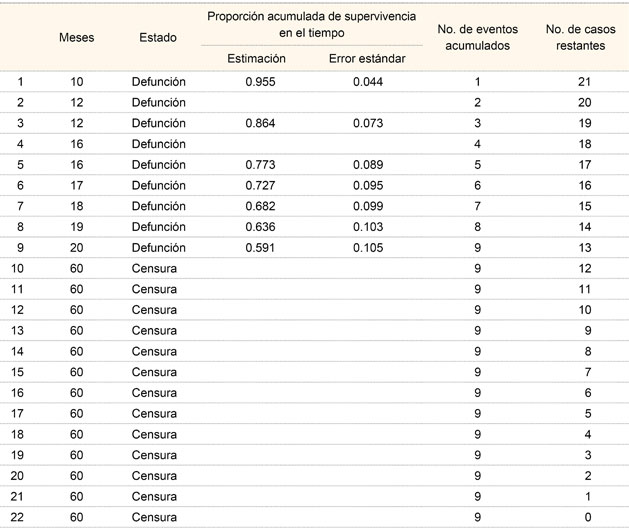
* Hubo trece pacientes censurados (59.1%) y 9 eventos (40.9%); el tiempo de supervivencia promedio fue de 41.818 meses, con un intervalo de confianza al 95% de 32.645-50.991
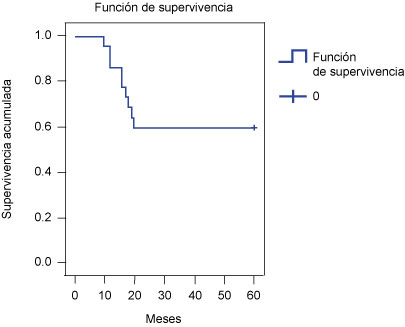
Figura 1
Supervivencia global a 60 meses de los pacientes con cáncer de pene en todos los estadios clínicos
La supervivencia para los estadios clínicos II, IIIa, IIIb y IV disminuyó con el tiempo, pues llegó a ser de 0% a los 18 meses para los pacientes con cáncer de pene EC IV (cuadro V, figura 2).
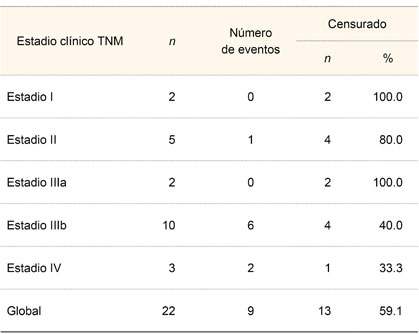
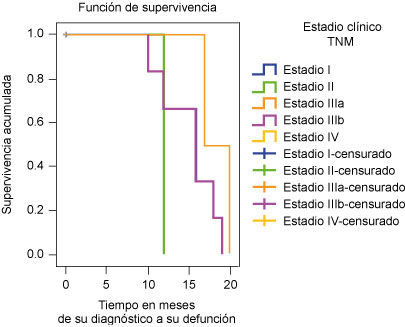
Figura 2
Supervivencia de los pacientes con cáncer de pene por estadio clínico TNM a 60 meses
En cuanto al tiempo en que se diagnosticó el cáncer de pene, la supervivencia en los pacientes a los que se les diagnosticó antes de un año de haber iniciado la patología fue de 84.6% a los 20 meses y a los pacientes a los que se les diagnosticó después de 1 año fue de 22% a los 19 meses (p = 0.002, Mantel-Cox) (figura 3).
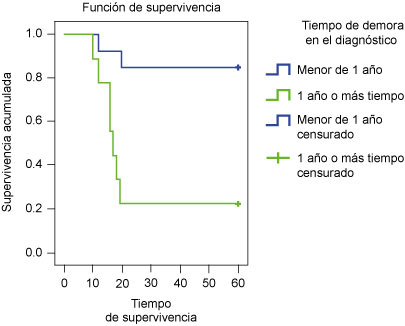
Figura 3
Supervivencia a 60 meses de los pacientes con cáncer de pene de acuerdo con el tiempo de demora en el diagnóstico
Los pacientes con una lesión clínica menor de 1 cm tuvieron una supervivencia de 75% a 12 meses y de 50% a los 16 meses, y los que tuvieron una lesión igual o mayor de 1 cm tuvieron una supervivencia de 61.1% a los 20 meses (p = 0.573, Mantel-Cox) (figura 4).
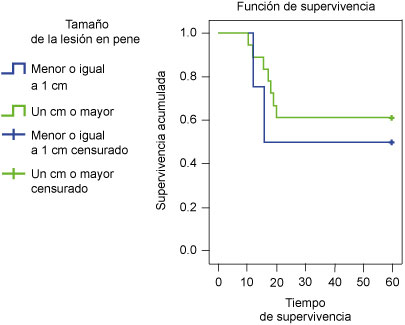
Figura 4
Supervivencia de pacientes con cáncer de pene según el tamaño de la lesión al momento del diagnóstico
La supervivencia fue de 65% a los 20 meses y de 0% a los 19 meses para los que tuvieron bordes quirúrgicos libres de tumor y con tumor, respectivamente, (p = 0.047, Mantel-Cox) (figura 5). Asimismo, los pacientes que no tuvieron invasión mixta (neural y vascular) presentaron una supervivencia de 88.9% a los 17 meses y los que tuvieron una invasión mixta (neural y vascular) presentaron una supervivencia de 38.5% a los 20 meses (p = 0.023, Mantel-Cox) (figura 6).
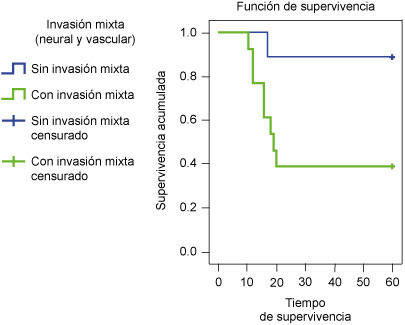
Figura 5
Supervivencia de pacientes con cáncer de pene según los resultados histopatológicos de los bordes quirúrgicos del tumor
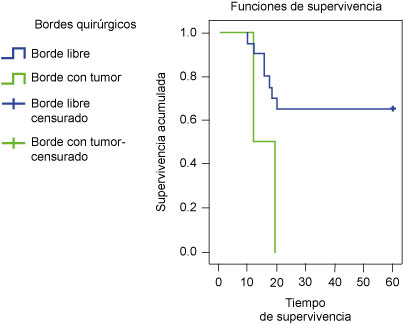
Figura 6
Supervivencia a 60 meses de pacientes con cáncer de pene según la invasión neural y vascular
En cuanto a los ganglios linfáticos, la supervivencia fue del 100% a los 20 meses para los cN0; sin embargo, fue de 0% a los 17, 20 y 12 meses, respectivamente para los cN1, cN2 y cN3 (p = 0.00, Mantel-Cox) (figura 7).
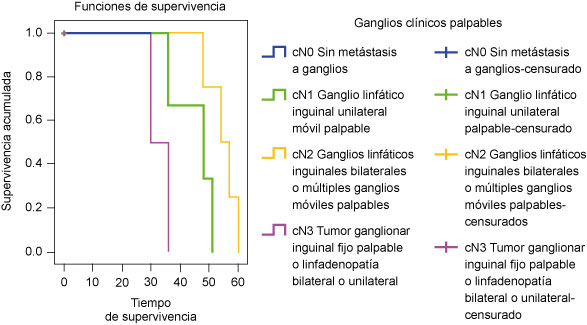
Figura 7
Supervivencia a 60 meses de pacientes con cáncer de pene de acuerdo con los ganglios linfáticos palpables
Para el grado de diferenciación histológica, la supervivencia fue de 0% a los 17, 28 y 20 meses para los grados I, II y III, respectivamente (p = 0.245, Mantel-Cox) (figura 8).
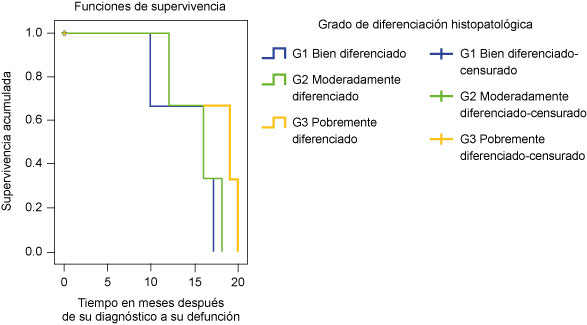
Figura 8
Supervivencia a 60 meses de pacientes con cáncer de pene según el grado de diferenciación histológica
Discusión
El cáncer de pene es una enfermedad rara.1La incidencia en menores de 40 años es de 19 % y del 7% en menores de 30 años; en países en vías de desarrollo se incrementa si la comparamos con países desarrollados.2,22
Se presenta en pacientes mayores de 50 años, lo cual concuerda con estos hallazgos, cuyos pacientes tienen como edad promedio 65 años.2
En México, la tasa de mortalidad en el año 2003 fue de 0.2 por 100 000 varones, que representa el 0.17% del total de las muertes por cáncer.3
El tiempo promedio de evolución desde la aparición de la lesión hasta el momento del diagnóstico fue de 25 meses, lo que concuerda con lo dicho por Lont et al., quienes mencionan que es de más de 12 meses.7
Madsen et al. describen que el prepucio intacto se presenta entre 25 y 60% de los pacientes con cáncer de pene,5 lo cual difiere con estos hallazgos, ya que se encontró prepucio intacto con fimosis en todos los pacientes (100%).
Los antecedentes clínicos de mayor importancia encontrados fueron el uso de tabaco, así como la infección por VPH (n = 15, 68.18%), lo cual concuerda con la literatura que menciona que el consumo de tabaco aumenta el riesgo de padecer cáncer de pene de 3 a 4.5 veces.7,22
La presentación clínica varía desde una lesión con induración hasta una lesión exofítica. Se encontró dolor en pene e ingle (27.3%) y dolor inguinal (22.7%) como síntomas más frecuentes, aunque la literatura menciona que los pacientes pueden cursar también con prurito, ardor en la piel del prepucio y ulceración en el glande o en el prepucio.10,16
De los pacientes que tuvieron lesiones de más de 5 cm, el 83.3% fumaron (n = 6) y de estos algunos casos tuvieron presencia de VPH; además, el 66.6% de los pacientes fumadores presentaron metástasis al momento del diagnóstico y también estaban en estadio clínico avanzado. Al consultar la literatura no se encontró ningún artículo que mencionara estos datos.15
La presentación de la lesión es más frecuente en el glande (48%), prepucio (21%), glande y prepucio (9%), surco coronal en 6% y en el cuerpo del pene en menos del 2%. Los pacientes retrasaron la atención médica y refirieron lesiones con más de un año de evolución antes del diagnóstico.23,24 En el presente estudio 40.9% de la lesión se presentó en prepucio y glande y en 40.9% abarcaba hasta un tercio distal del pene, dato que no es lo habitual a pesar de que el tiempo de evolución en estos pacientes fue de 12 meses, el mismo que el reportado en la literatura.1,10,16,24
El carcinoma de células escamosas de pene es el más frecuente (entre 48 y 65%). En este estudio se encontró que el 86.4% de los cánceres de pene eran de la variedad epidermoide o de células escamosas; otras variedades fueron la verrucosa (9.1%) y la sarcomatoide (4.5%). Se menciona que la variedad sarcomatoide es muy agresiva con una sobrevida corta.10,12 Pues bien, en este estudio el paciente con variedad sarcomatoide estuvo vivo a los 60 meses.
Todos los pacientes que presentaban tabaquismo más infección por VPH tuvieron invasión neurovascular. En la literatura revisada no encontramos ningún artículo sobre la presencia de invasión neurovascular en pacientes con cáncer de pene. Sin embargo, se requieren estudios de seguimiento para ver si hay asociación entre estos factores y el desarrollo de este cáncer.
De los pacientes con metástasis (n = 6) todos eran fumadores y portadores de infección por VPH; todos los pacientes con estadio IV (n = 7) también tenían estos antecedentes presentes; 75% de los pacientes que tuvieron invasión tisular por histopatología (n = 16) eran fumadores o tenían infección por VPH y el 42.85% de los pacientes que fallecieron por metástasis pulmonares (n= 7) también eran fumadores. En la literatura no encontramos asociación entre el cáncer de pene y la morbimortalidad, pero sí con el estadio clínico y el desarrollo de la enfermedad.24,25,26,27
En el carcinoma de pene el pronóstico vendrá determinado por el estadio patológico y en especial por la afectación ganglionar.22,27,28 En este estudio se encontró que la supervivencia global de los pacientes con cáncer de pene a los 60 meses es del 59.1%, como lo muestran el cuadro IV y la figura 1; así, la supervivencia es de 100% a los 11 meses para el EC IIIb de 83% a 10 meses y para el EC IV de 50% a 17 meses. Esto no concuerda con lo descrito en la literatura, en la que se menciona que la función de la supervivencia es inversamente proporcional al EC.20,29,30,31,32,33Consideramos que la discordancia en estos resultados se debe a la población limitada de este estudio. Así, encontramos que la supervivencia es de 100% a 11 meses para el EC II, esto debido a que en ese estadio solo tuvimos un paciente, el cual estaba vivo. También la supervivencia disminuye en el tiempo en todos los estadios, como se puede ver en la figura 2.
Otro factor que hay que tomar en cuenta para la supervivencia en estos pacientes es la demora en el diagnóstico, ya que la supervivencia es mayor en pacientes a los que el diagnóstico se les realiza antes de un año, si la comparamos con aquellos a los que se les realiza después de un año (p = 0.002).
El borde quirúrgico positivo también influye en la supervivencia si se compara con el borde quirúrgico negativo (p = 0.023). Asimismo, para los ganglios linfáticos positivos también la supervivencia es menor comparada con los pacientes que tuvieron ganglios linfáticos negativos (p = 0.000). Respecto al grado de diferenciación histológica del cáncer de pene, la supervivencia fue mayor en los pobremente diferenciados, comparados con los bien diferenciados (p = 0.245), lo cual no concuerda con la literatura.
Podemos concluir que la supervivencia de los pacientes del cáncer de pene a 60 meses es de 59.1%, que el EC más temprano, el borde quirúrgico negativo, el diagnóstico temprano de la patología y la ausencia de ganglios linfáticos positivos disminuyen la supervivencia de estos pacientes.
Referencias
Pettaway C, Lynch D Jr, Davis D. Tumors of the penis. En: Wein AJ, Kavoussi LR, Novick AC, et al., (eds.) Campbell-Walsh Urology 10th Edition. Philadelphia: Saunders; 2011. pp. 959-992.
Pow-Sang MR, Ferreria U, Pow-Sang JM, Nardi AC, Destefano V. Epidemiology and natural history of penile cancer. Urology. 2010; 76(2 Suppl 1):S2-S6.
Jiménez-Ríos MA, Ariza-Villaro P, Solares-Sánchez ME, Martínez-Cervera P. Factores pronósticos de mortalidad en cáncer de pene. Gac Med Oncol. 2011;10(4):191-6.
Di Capua-Sacoto C, Luján-Marco S, Morales-Solchaga G, Budía-Alba A, Pontones-Moreno JL, Jiménez-Cruz JF. Cáncer de pene. Nuestra experiencia en 15 años. Actas Urol Esp. 2009;33(2):143-8.
Madsen BS, van den Brule AJ, Jensen HL, Wohlfahrt J, Frisch M. Risk factors for squamous cell carcinoma of the penis--population-based case-control study in Denmark. Cancer Epidemiol Biomarkers Prev. 2008;17(10):2683-91.
The National Comprehensive Cancer Network. Guidelines Penile Cancer Inc. 2012. Version 1. 2012.
Lont AP, Kroon BK, Horenblas S, Gallee MP, Berkhof J, Meijer CJ, et al. Presence of high-risk human papillomavirus DNA in penile carcinoma predicts favorable outcome in survival. Int J Cancer. 2006;119(5):1078-81.
Misra S, Chaturvedi A, Misra NC. Penile carcinoma: a challenge for the developing world. Lancet Oncol. 2004;5(4):240-7.
Baroas DA, Chang SS. Penile cancer: clinical presentation, diagnosis, and staging. Urol Clin North Am. 2010;37(3):343-52.
Cubilla AL, Reuter V, Velazquez E, Piris A, Saito S, Young RH. Histologic classification of penile carcinoma and its relation to outcome in 61 patients with primary resection. Int J Surg Pathol. 2001;9:111-20.
Eble JN, Sauter G, Epstein JI, Sesterhenn IA. World Health Organization Classification of Tumours: Pathology and Genetics of Tumours of the Urinary System and Male Genital Organs. Lyon: IARC Publishing; 2004: 281-290.
Chaux A, Lezcano C, Cubilla AL, Tamboli P, Ro J, Ayala A. Comparison of subtypes of penile squamous cell carcinoma from high and low incidence geographical regions. Int J Surg Pathol. 2010 Aug;18(4):268-77.
Chaux A, Velazquez EF, Algaba F, Ayala G, Cubilla AL. Developments in the pathology of penile squeamous cell carcinomas. Urology. 2010;76(2 Suppl 1):S7-S14.
Leijte JA, Kirrander P, Antonini N, Windahl T, Horenblas S. Recurrence Patterns of Squamous Cell Carcinoma of the Penis: Recommendations for Follow-Up Based on a Two-Centre Analysis of 700 Patients. Eur Urol. 2008;54(1):161-8.
Novara G, Galfano A, De Marco V, Artibani W, Ficarra V. Prognostic factors in squamous cell carcinoma of the penis. Nat Clin Pract Urol. 2007;4(3):140-6.
Pandey D, Mahajan V, Kannan RR. Prognostic factors in node-positive carcinoma of the penis. J Surg Oncol. 2006;93(2):133-8.
Broders AC. Squamous-cell epithelioma of the skin: a study of 256 cases. Ann Surg. 1921;73(2):141-60.
Solsona E, Bahl A, Brandes SB, Dickerson D, Puras-Baez A, van Poppel H, et al. New developments in the treatment of localized penile cancer. Urology. 2010;76(2 Suppl 1):S36-S42.
Bissada NK, Yakout HH, Fahmy WE, Gayed MS, Touijer AK, Greene GF, et al. Multi-institutional long-term experience with conservative surgery for invasive penile carcinoma. J Urol. 2003;169(2):500-2.
Lont AP, Gallee MP, Meinhardt W, van Tinteren H, Horenblas S. Penis conserving treatment for T1 and T2 penile carcinoma: clinical implications of a local recurrence. J Urol. 2006;176(2):575-80.
Smith Y, Hadway P, Ahmed S, Perry MJ, Corbishley CM, Watkin NA. Penile preserving surgery for male distal urethral carcinoma. BJU Int. 2007;100(1):82-7.
Montiel-Jarquín AJ, Villagómez-Camargo R, Chopin-Gazga M, González-López A, Palmer-Márquez L, Rodríguez-Pérez F, et al. Cáncer de pene en etapas tempranas: expresión negativa de Metaloproteinasa-9 en biopsia. Pren Med Arg. 2015;101(8):444-50.
Korets R, Koppie TM, Snyder ME, Russo P. Partial penectomy for patients with squamous cell carcinoma of the penis: the Memorial Sloan-Kettering experience. Ann Surg Oncol. 2007;14(12):3614-9.
Ficarra V, Akduman B, Bouchot O, Palou J, Tobias-Machado M. Prognostic factors in penile cancer. Urology. 2010;76(2 Suppl 1):S66-73.
Lont AP, Besnard AP, Gallee MP, van Tinteren H, Horenblas S. A comparison of physical examination and imaging in determining the extent of primary penile carcinoma. BJU Int. 2003;91(6):493-5.
Ornellas AA, Seixas AL, Marota A, Wisnescky A, Campos F, de Moraes JR. Surgical treatment of invasive squamous cell carcinoma of the penis: retrospective analysis of 350 cases. J Urol. 1994;151(5):1244-9.
Pietrzak P, Corbishley C, Watkin N. Organ-sparing surgery for invasive penile cancer: early follow-up data. BJU Int. 2004;94(9):1253-7.
Shindel AW, Mann MW, Lev RY, Sengelmann R, Petersen J, Hruza GJ, et al. Mohs micrographic surgery for penile cancer: management and long-term followup. J Urol. 2007;178(5):1980-5.
Villagómez-Camargo R. Experiencia en el manejo del Cáncer de pene en el Hospital General Regional No. 36 del Instituto Mexicano del Seguro Social [tesis de Especialidad]. Puebla: UPAEP-IMSS; 2014.
Horenblas S, van Tinteren H, Delemarre JF, Moonen LM, Lustig V, Kröger R. Squamous cell carcinoma of the penis: accuracy of tumor, nodes and metastasis classification system, and role of lymphangiography, computerized tomography scan and fine needle aspiration cytology. J Urol. 1991;146(5):1279-83.
Scardino E, Villa G, Bonomo G, Matei DV, Verweij F, Rocco B, et al. Magnetic resonance imaging combined with artificial erection for local staging of penile cancer. Urology. 2004;63(6):1158-62.
Minhas S, Kayes O, Hegarty P, Kumar P, Freeman A, Ralph D. What surgical resection margins are required to achieve oncological control in men with primary penile cancer? BJU Int. 2005;96(7):1040-3.
Pontillo H, Fernández A, León H. Experiencia de 15 años en el manejo del cancer de pene. Rev Venez Oncol. 2011;23(1):26-33.
Notas
Notas de autor
dralmoja@hotmail.com
Información adicional
PMID PubMed: 28212473
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/1331/1930 (pdf)