Aportaciones originales
Relación entre la actividad ósea y el metabolismo en el adulto mayor*
Relationship between bone remodeling and metabolism in the elderly
Relación entre la actividad ósea y el metabolismo en el adulto mayor*
Revista Médica del Instituto Mexicano del Seguro Social, vol. 56, 1, pp. 6-11, 2018
Instituto Mexicano del Seguro Social
Recepción: 15 Agosto 2017
Aprobación: 15 Noviembre 2017
Resumen:
diversos estudios sugieren que la osteocalcina (OC) contribuye no solo a la regulación del metabolismo óseo, sino también al metabolismo energético. El objetivo del trabajo fue evaluar la relación entre la concentración sérica de OC y los parámetros metabólicos y la densidad mineral ósea (DMO) en adultos mayores.
Métodos: estudio transversal descriptivo en 122 hombres sanos mayores de 60 años. Se les determinó glucosa, lípidos, insulina, adiponectina y OC. La DMO se analizó por absorciometría de doble fotón.
Resultados: el 42.8% de la muestra presentó síndrome metabólico (SM). Los niveles de OC no difirieron entre el grupo de pacientes con y sin SM. Se observó una correlación negativa entre la concentración de OC y el índice de masa corporal (IMC) (r = −0.226, p = 0.04), circunferencia de cintura (r = −0.261, p = 0.02), glucosa (r = −0.245, p = 0.03), insulina (r = −0.235, p = 0.03) y HOMA-IR (r = −0.211, p = 0.04). Los pacientes con DMO disminuida mostraron una concentración significativamente mayor de OC en comparación con aquellos con DMO normal.
Conclusiones: la OC se asoció inversamente con el IMC, la obesidad abdominal, la glucosa, la insulina y la resistencia a la insulina en hombres mayores de 60 años. Lo anterior confirma la conexión que existe entre el tejido óseo y el metabolismo.
Palabras clave: Osteocalcina, Síndrome Metabólico, Densidad Ósea, Anciano.
Abstract:
Recent studies have shown that osteocalcin (OC) is related to not only bone metabolism but also energy metabolism. The aim of the present study was to investigate whether OC was associated with metabolic factors and bone mineral density (BMD) in elderly men.
Methods: A cross-sectional study was done including 122 healthy men aged 60 years or older. Serum glucose, lipids, insulin, adiponectin and OC were measured and BMD was estimated using dual energy X-ray absorptiometry.
Results: 42.8% of men had metabolic syndrome (MetS). OC levels were not significantly different between men with and without MetS. OC concentrations were inversely associated with body mass index (BMI) (r = −0.226, p = 0.04), waist circumference (r = −0.261, p = 0.02), glucose (r = −0.245, p = 0.03), insulin (r = −0.235, p = 0.03), and HOMA-IR (r = −0.211, p = 0.04). In addition, OC levels were higher in patients with diminished BMD compared with those with normal BMD.
Conclusions: OC levels correlate negatively with BMI, waist circumference, glucose, insulin and HOMA-IR in elderly men, which suggests a connection between bone and energy metabolism.
Keywords: Osteocalcin, Metabolic Syndrome X, Bone Density, Aged.
Introducción
Durante mucho tiempo, el tejido óseo fue considerado solamente como un aparato de sostén. Sin embargo, es un tejido muy activo en el que hay una remodelación constante de su arquitectura, gracias a la actividad de los osteoblastos y los osteoclastos.1, 2, 3
La osteocalcina (OC) es una proteína secretada por los osteoblastos durante el proceso osteogénico. Posee tres residuos de ácido glutámico que por acción de la vitamina K se pueden carboxilar, facilitando así la unión de calcio e hidroxiapatita. Cuando uno de los tres residuos de la OC no se carboxila, se conoce como osteocalcina decarboxilada (ucOC).1 Hace apenas algunos años se demostró que la OC participa en el metabolismo energético.4,5 Lee et al.4 al realizar estudios en ratones carentes del gen de osteocalcina (OC-/-), encontraron una mayor concentración de glucosa en circulación y menor secreción de insulina, comparados con los ratones silvestres. Además, observaron una menor sensibilidad a la insulina, un menor tamaño y número de los islotes de Langerhans y de las células β, así como un incremento de la masa grasa, del número de adipocitos y una menor expresión de niveles séricos de adiponectina (adipocina asociada a sensibilidad a la insulina). Posteriormente, al realizar cultivos celulares de los islotes de Langerhans y de los adipocitos de los ratones OC-/- y adicionarles OC, describieron una mayor producción de insulina y adiponectina. Finalmente, a los ratones OC-/- les administraron una carga de glucosa junto con la administración de OC y observaron una disminución significativa de los niveles de glucosa, así como un incremento de los niveles de insulina y adiponectina.4
Los datos anteriores permitieron proponer la OC, particularmente la ucOC, como una hormona que mejora la tolerancia a la glucosa al incrementar la proliferación de las células β, la expresión y secreción de insulina y la sensibilidad a la insulina en tejidos periféricos.4
Diversos estudios clínicos posteriormente confirmaron estas asociaciones y además señalaron una menor concentración de OC en personas con síndrome metabólico (SM)6, 7, 8, 9, 10, 11, 12 el cual está conformado por un grupo de factores de riesgo que aumentan las probabilidades de sufrir enfermedad cardiovascular y diabetes mellitus tipo 2 (DM2). Sin embargo, los estudios se han enfocado principalmente a la mujer y pocos han evaluado estas asociaciones en el adulto mayor del género masculino, el cual presenta pérdida de masa ósea en una etapa mas tardía que la mujer, además de mayor riesgo cardiovascular, DM2 y fragilidad ósea relacionada a la edad.
Métodos
Estudio transversal descriptivo en el que se seleccionaron 112 hombres, sin diagnóstico previo de SM, mayores de 60 años de edad. A los participantes se les realizó un examen físico completo. Para la medición del peso y de la talla se les solicitó a los participantes vestir ropa ligera y no usar zapatos. Se utilizó una báscula y estadímetro Bame con una escala de precisión de 0.5 kg. El índice de masa corporal (IMC) se calculó como el peso (kg) divido entre la talla (m2). Para fines del análisis, se definieron dos categorías del IMC ≤ 27 kg/m2 y ≥ 27.1 kg/m2.
Fueron excluidos del estudio los sujetos con historia de diabetes, infección crónica, cáncer, enfermedad gastrointestinal, hepática o renal, hábito tabáquico, enfermedades endócrinas y alteraciones hematológicas. Igualmente, fueron excluidos los sujetos con consumo de medicamentos que afectaran el metabolismo óseo o con consumo de alcohol de más de 30 mL por día.
El diagnóstico de SM se definió de acuerdo con los criterios armonizados de la Federación Internacional de Diabetes (IDF, por sus siglas en inglés).13,14 Los criterios fueron circunferencia de cintura ≥ 94 cm, glucosa de ayuno ≥ 100 mg/dL, triglicéridos ≥ 150 mg/ dL, HDL-colesterol < 40 mg/dL o la administración de medicamentos hipolipemiantes, presión arterial sistólica ≥ 130 o diastólica ≥ 85 mmHg, o la administración de medicamentos antihipertensivos.
Este protocolo de estudio fue aprobado por un comité de ética del Instituto Mexicano del Seguro Social (IMSS). Los participantes fueron informados y firmaron la correspondiente carta de consentimiento.
Análisis bioquímico
En condiciones de 10 horas de ayuno se obtuvieron muestras de sangre venosa antecubital entre las 8:00 y las 9:00 a.m. Las muestras se centrifugaron a 2000 rpm durante 20 minutos para separar el suero y preparar fracciones de 500 µl que se mantuvieron en congelación a −70 °C hasta la realización de los ensayos. La glucosa, el colesterol total, las lipoproteínas de alta densidad y los triglicéridos se determinaron en suero por métodos enzimáticos colorimétricos en el analizador químico semiautomatizado Ekem Control Lab. La fracción de lipoproteínas de baja densidad se calculó con base en la fórmula de Friedewald. Asimismo, se utilizó el modelo de HOMA-IR de Matthews et al. para evaluar la resistencia a la insulina.15 Se empleó la técnica de radioinmunoensayo para medir los niveles de adiponectina e insulina. Para la medición de adiponectina se usaron los kits comerciales de Linco Research (St Charles, MO, USA). La sensibilidad del ensayo fue de 0.05 µg/mL y los coeficientes de variación (CV) intraensayo e interensayo fueron 3.9 y 8.5 %, respectivamente. La insulina se midió con estuches comerciales de Millipore (Billerica, MA, USA). La sensibilidad de este ensayo fue de 2 μU/mL y los CV de 4.0 y 8.6%, respectivamente. La osteocalcina se midió por inmunoensayo quimioluminiscente en el analizador Immulite (Diagnostic Products Corporation, Los Angeles, USA). La sensibilidad de este ensayo fue 0.55 ng/mL y los CV de 2.8 y 7.2%.
Densidad mineral ósea
Se obtuvo en la región lumbar y en el cuello femoral mediante absorciometría de doble fotón utilizando un densitómetro Lunar DPX (GE Lunar Corporation, Madison, WI). Todos los participantes fueron evaluados en el mismo equipo y por el mismo operador. La DMO se expresó en términos absolutos con la aplicación de una escala de desviación estándar del promedio de adultos jóvenes, de acuerdo con la escala T, con valores de referencia calculados por el protocolo del equipo. Con base en los criterios de la Organización Mundial de la Salud (OMS) se consideró osteoporosis cuando el valor T fue < -2.5; osteopenia cuando T se encontró entre -1.0 y -2.5; y DMO normal cuando el valor de T fue > -1.0.
Análisis estadístico
Se utilizó la prueba de Kolmogorov-Smirnov, que mostró la distribución no paramétrica de las variables. Los resultados se presentan como media ± DE. La comparación de los resultados entre pacientes con y sin SM se realizó con la prueba U de Mann-Whitney. Se utilizó la prueba de correlación de Rho de Spearman para evaluar la asociación entre la OC y los factores de riesgo metabólico. El análisis de los datos se realizó mediante el programa estadístico para las ciencias sociales SPSS, versión 21.0. La significación estadística se estableció como una p < 0.05.
Resultados
La edad promedio de los participantes fue de 63.1 ± 3.0 años y el IMC de 27.7 ± 3.5, (cuadro I). De los participantes, el 42.8% reunió los criterios diagnósticos del síndrome metabólico. La concentración de OC fue inferior en el grupo de pacientes con SM, en comparación con los participantes sin SM (4.39 ± 1.8 frente a 4.71 ± 2.1 ng/dL), pero sin diferencias significativas. En contraste, se encontró una disminución de insulina (6.8 ± 3.2 frente a 14.1 ± 7.5 mUI/mL, p = 0.03) y una mayor concentración de adiponectina (10.2 ± 4.8 frente a 7.4 ± 3.9 µg/mL, p = 0. 001) en los pacientes sin SM en comparación con los que presentaron SM.
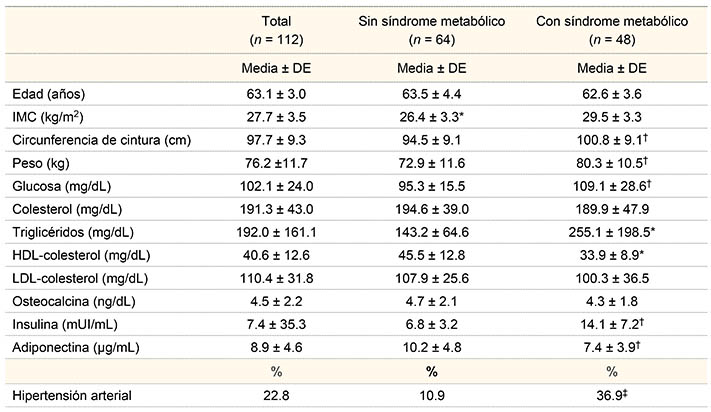
Cuadro I
Características generales de los participantes
DE = desviación estándar; IMC = índice de masa corporal
*p < 0.001, †p < 0.01, ‡p < 0.05
Las comparaciones se establecieron entre el grupo sin y con síndrome metabólicoLa concentración de OC se correlacionó negativamente con la circunferencia de cintura, glucosa, insulina y HOMA-IR. En tanto que no hubo asociación significativa con el resto de los componentes (cuadro II).
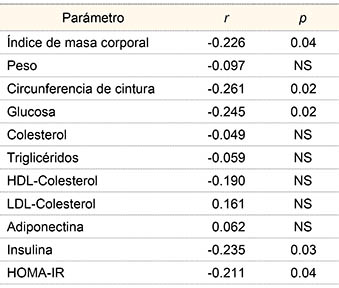
Cuadro II
Correlación entre la osteocalcina y los factores de riesgo metabólico
La significación estadística se estableció con una p < 0.05
Cuando los participantes fueron divididos a partir del IMC, se encontró que en aquellos con IMC ≥ 27 la correlación entre OC y glucosa fue −0.312, p = 0.04, con el peso corporal −0.612, p = 0.03, y con insulina −0.292, p = 0.05.
Según los criterios de la OMS, 53% de los participantes presentaron DMO normal, 43% tenían osteopenia y 4% osteoporosis. La concentración de OC fue menor en aquellos con DMO normal, en comparación con los pacientes con osteopenia y osteoporosis (3.9 ± 1.6, 5.1 ± 2.4, 5.0 ± 1.3 ng/mL respectivamente, p < 0.05). Por el contrario, no hubo diferencias en la glucosa, insulina y lípidos entre estos grupos. Los pacientes con obesidad presentaron mayor DMO tanto lumbar como femoral, en comparación con los pacientes con sobrepeso y peso normal (figura 1).
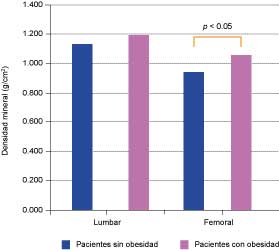
Figura 1
Se presenta la densidad mineral ósea de las regiones lumbar y femoral en pacientes obesos y no obesos
Discusión
En este estudio se encontró una asociación de la concentración de OC con factores de riesgo metabólico, como el IMC, la obesidad abdominal, la concentración de glucosa, la insulina y la resistencia a insulina medida por el modelo HOMA-IR en adultos mexicanos mayores de 60 años. Estos resultados concuerdan con algunos trabajos previos en los que se encontró una relación inversa de la OC con el nivel de glucosa y la resistencia a la insulina.16,17
Cada vez surge más información que apoya el papel del hueso en la regulación de la glucosa y el metabolismo energético. La insulina interviene en la función ósea y estimula la diferenciación del osteoblasto; recientemente, se identificó que la osteocalcina, sintetizada por el osteoblasto, influye en el metabolismo energético, en la adiposidad y en la homeostasis de glucosa.4
En el presente estudio, los niveles de OC no mostraron diferencia entre los pacientes con SM y sin este síndrome; no obstante, se asociaron de manera inversa con algunos de sus componentes. En algunos estudios se han encontrado menores niveles de OC en personas con SM.18
Por otra parte, la frecuencia de SM en el adulto mayor en este estudio fue más elevada que en poblaciones europeas y asiáticas, en las que se describen prevalencias en el rango de 12.7 a 28.8%; sin embargo, fue similar a la de poblaciones americanas en las que inclusive se ha reportado una frecuencia del 50%.7, 8, 9, 10
Uno de los mecanismos fisiopatológicos involucrados al inicio del SM es una mayor resistencia a la insulina. En el presente estudio se observó una relación inversa entre la OC y la resistencia a la insulina, además de asociaciones negativas con glucosa, IMC y circunferencia de cintura de manera similar a lo descrito en ratones y en humanos, lo cual sugiere los efectos endócrinos de la OC en la homeostasis de glucosa y en el tejido adiposo.18 Se ha propuesto que algunos de estos efectos son mediados a través de la acción de la adiponectina.19,20 La ucOC estimula la secreción de esta adiponectina, la cual mejora la sensibilidad a la insulina al incrementar la oxidación de ácidos grasos en músculo, inhibir la gluconeogénesis hepática, reducir el contenido de triglicéridos en músculo e hígado y disminuir los niveles plasmáticos de ácidos grasos.19,20 Sin embargo, en este estudio la asociación entre OC y adiponectina tuvo una significación limítrofe.
El adulto mayor tiene un mayor riesgo de fracturas. En el presente estudio se identificó que solo la mitad de la población evaluada presentaba una DMO normal y que a mayor DMO, menor nivel circulante de OC. Es probable que la pérdida de la DMO durante el envejecimiento se acompañe de un incremento en la actividad de los osteoblastos que tratan de compensar la pérdida de masa ósea.21 Adicionalmente se ha señalado que la activación de la resorción ósea facilita la liberación de OC de la matriz ósea. Por otra parte, en este estudio no se encontraron diferencias entre los parametros metabólicos y la DMO.
En nuestra población se identificó que los adultos mayores obesos presentaban una mayor DMO. Diversos estudios epidemiológicos han mostrado que la osteoporosis es menos frecuente en personas obesas en las que se promueve la formación de hueso para que este pueda cumplir su función de sostén, locomoción y protección de una mayor masa corporal.22,23
La función ósea está regulada por muchos factores, como la hormona paratiroidea, los esteroides sexuales, la vitamina D, el calcio y las fuerzas mecánicas, entre otros. La señal entre osteblasto e insulina representa un mecanismo de retrocontrol de asa corta, el cual regula la formación del hueso y el metabolismo de la glucosa por acción hormonal de la OC. Así, este eje osteoblasto-insulina es una de las vías de comunicación entre el metabolismo óseo y la glucosa.16
Otra observación es que en pacientes con diabetes tipo 2, la resistencia a la insulina y la hiperglucemia reducen la formación ósea por el osteoblasto. Esto conlleva a una menor producción de OC, que puede conducir a su vez a una mayor resistencia a la insulina por disminución de la producción de la adiponectina por el adipocito.5,16 De esta forma se produce un círculo vicioso.
Algunas limitaciones del estudio fueron la medición de la OC total y no la ucOC. Esta fracción se ha señalado como la biológicamente activa; sin embargo, la osteocalcina total medida en este trabajo permitió identificar las asociaciones entre el metabolismo óseo y el energético. Los resultados de este estudio, que se encuentran en el mismo sentido que otros estudios clínicos transversales, deberán ser evaluados con estudios longitudinales.
Conclusiones
En este estudio se confirmó la asociación de OC con índices de adiposidad y de glucosa circulante, insulina y resistencia a la insulina en adultos mayores. Los datos anteriores apoyan el efecto del hueso sobre la regulación del metabolismo.
Agradecimientos
Agradecemos el apoyo financiero brindado por el Fondo de Investigación en Salud del Instituto Mexicano del Seguro Social.
Referencias
1. Hauschka PV, Lian JB, Cole DE, Gundberg CM. Osteocalcin and matrix Gla protein: vitamin K-dependent proteins in bone. Physiol Rev.1989;69(3):990-1047.
2. Karsenty G, Ferron M. The contribution of bone to whole-organism physiology. Nature. 2012;481 (7381):314-20.
3. Ducy P. The role of osteocalcin in the endocrine cross-talk between bone remodelling and energy metabolism. Diabetologia 2011;54(6):1291-7.
4. Lee NK, Sowa H, Hinoi E, Ferron M, Ahn JD, Confavreux C, et al. Endocrine regulation of energy metabolism by the skeleton. Cell. 2007;130(3):456-69.
5. Zárate A, Basurto L, Saucedo R. El tejido óseo se incorpora a la constelación hormonal. Rev Med Inst Mex Seguro Soc. 2010;48(1):1-5.
6. Saleem U, Mosley TH Jr, Kullo IJ. Serum osteocalcin is associated with measures of insulin resistance, adipokine levels, and the presence of metabolic syndrome. Arterioscler Thromb Vasc Biol. 2010;30 (7):1474-8.
7. Tan A, Gao Y, Yang X, Zhang H, Qin X, Mo L, et al. Low serum osteocalcin level is a potential marker for metabolic syndrome: results from a Chinese male population survey. Metabolism. 2011;60(8):1186-92.
8. Yeap BB, Chubb SA, Flicker L, McCaul KA, Ebeling PR, Beilby JP, et al. Reduced serum total osteocalcin is associated with metabolic syndrome in older men via waist circumference, hyperglycemia, and triglyceride levels. Eur J Endocrinol. 2010;163(2):265-72.
9. Confavreux CB, Szulc P, Casey R, Varennes A, Goudable J, Chapurlat RD. Lower serum osteocalcin is associated with more severe metabolic syndrome in elderly men from the MINOS cohort. Eur J Endocrinol. 2014;171(2):275-83.
10. Oosterwerff MM, van Schoor NM, Lips P, Eekhoff EM. Osteocalcin as a predictor of the metabolic syndrome in older persons: a population-based study. Clin Endocrinol (Oxf). 2013;78(2):242-7.
11. Pittas AG, Harris SS, Eliades M, Stark P, Dawson-Hughes B. Association between serum osteocalcin and markers of metabolic phenotype. J Clin Endocrinol Metab. 2009;94(3):827-32.
12. Hwang YC, Jeong IK, Ahn KJ, Chung HY. The uncarboxylated form of osteocalcin is associated with improved glucose tolerance and enhanced beta-cell function in middle-aged male subjects. Diabetes Metab Res Rev. 2009;25(8):768-72.
13. Alberti KG, Zimmet P, Shaw J. The metabolic syndrome a new worldwide definition. Lancet. 2005; 366(9491):1059-62.
14. Alberti KG, Zimmet P, Shaw J. Metabolic syndrome a new world-wide definition. A consensus statement from the international diabetes federation. Diabetic Medicine. 2006;23(5):469-80.
15. Matthews DR, Rudenski AS, Burnett MA, Darling P, Turner RC. The half-life of endogenous insulin and C-peptide in man assessed by somatostatin suppression. Clin Endocrinol (Oxf). 1985; 23(1):71-9.
16. Iki M, Tamaki J, Fujita Y, Kouda K, Yura A, Kadowaki E, et al. Serum undercarboxylated osteocalcin levels are inversely associated with glycemic status and insulin resistance in an elderly Japanese male population: Fujiwara-kyo Osteoporosis Risk in Men (FORMEN) Study. Osteoporos Int. 2012;23(2):761-70.
17. Musso C, Mingote E, Durante C, Brenta G, Gurfinkiel M, Fossati MP et al. Correlación entre osteocalcina, insulinorresistencia, insulinosensibilidad y metabolismo de la glucosa en adultos mayores con síndrome metabólico. Rev Argent Endocrinol y Metab. 2015;52 (1):8-14.
18. Kindblom JM, Ohlsson C, Ljunggren O, Karlsson MK, Tivesten A, Smith U, et al. Plasma osteocalcin is inversely related to fat mass and plasma glucose in elderly Swedish men. J Bone Miner Res 2009;24(5):785-91.
19. Lihn AS, Pedersen SB, Richelsen B. Adiponectin: action, regulation and association to insulin sensitivity. Obes Rev. 2005;6(1):13-21
20. Zhang Y, Zhou P, Kimondo JW. Adiponectin and osteocalcin: relation to insulin sensitivity. Biochem Cell Biol. 2012; 90(5):613-20.
21. Brown JP, Delmas PD, Malaval L, Edouard C, Chapuy MC, Meunier PJ. Serum bone Gla-protein: a specific marker for bone formation in postmenopausal osteoporosis. Lancet.1984;77(3):1091-3.
22. Edelstein SL, Barrett-Connor E. Relation between body size and bone mineral density in elderly men and women. Am J Epidemiol.1993;138(3):160-9.
23. Lindsay R, Cosman F, Herrington BS, Himmelstein S. Bone mass and body composition in normal women. J Bone Miner Res. 2001;7(1):55-63.
Notas
Notas de autor
lbasurtoa@yahoo.com
Información adicional
Link PubMed: https://www.ncbi.nlm.nih.gov/pubmed/29624339
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/2394/2814 (pdf)