Aportaciones originales
Recepción: 22 Mayo 2017
Aprobación: 19 Junio 2017
Resumen:
Introducción: las bronquiectasias (BQs) son dilataciones permanentes de los bronquios. Su prevalencia en pacientes con inmunodeficiencia común variable (IDCV) es alta, sin embargo existe escasa información respecto al tipo y localización de las mismas. El objetivo de este estudio es conocer el tipo y localización de las bronquiectasias en una cohorte de pacientes adultos portadores de IDCV.
Métodos: estudio transversal, observacional y descriptivo que incluyó a 32 pacientes adultos con diagnóstico de IDCV de acuerdo con los criterios de la Sociedad Europea de Inmunodeficiencias. A todos se les realizó tomografía de alta resolución pulmonar, las cuales fueron interpretadas por un médico radiólogo experto. Se reportó la frecuencia, tipo y localización de las bronquiectasias mediante estadística descriptiva.
Resultados: se incluyeron 32 pacientes adultos, diez hombres y 22 mujeres. El 40.6% presentaron bronquiectasias. El 23% tenía afección en un lóbulo, el 15.3% dos lóbulos, 46.1% 3 lóbulos y el 15.3% afectación completa del parénquima; distribuidos de la siguiente manera: tubulares 38.4%, varicosas 23% y las combinaciones quísticas y tubulares 15.3%, quísticas y varicosas 15.3% y quísticas, tubulares y varicosas 7.6%.
Conclusión: nuestros resultados muestran que el 40% de los pacientes adultos con IDCV tienen BQs, suelen afectar tres lóbulos pulmonares, el tipo más común fue el tubular. Su diagnóstico y tratamiento oportuno puede mejorar la supervivencia y reducir los costos para el paciente y las instituciones de salud.
Palabras clave: Bronquiectasia, Agammaglobulinemia, Enfermedades del Sistema Inmune.
Abstract:
Background: Bronchiectasis are permanent dilatations of the bronchi. Its prevalence in patients with variable common immunodeficiency (CVID) is high, however there is little information regarding the type and location of the same; therefore the objective of this study is to know the type and location of bronchiectasis in a cohort of patients with CVID of tertiary level of care.
Methods: It has been made a transversal, observational and descriptive study that included 32 adult patients with diagnosis of CVID according to the criteria of the European Society of Immunodeficiencies (ESID). All patients underwent high resolution pulmonary computed tomography (HRCT), which were interpreted by an expert radiologist. The frequency, type and location of bronchiectasis were reported using descriptive statistics.
Results: Thirty-two adult patients, ten men and 22 women were included. 40.6% had bronchiectasis. 23% had a lobe involvement, 15.3% two lobes, 46.1% 3 lobes and 15.3% complete involvement of the parenchyma. The types of bronchiectasis were distributed as follows: tubular 38.4%, varicose 23% and cystic and tubular combinations 15.3%, cystic and varicose 15.3% and cystic, tubular and varicose 7.6%.
Conclusions: Our results show that 40% of adult patients with CVID have BQs, usually affecting three pulmonary lobes, located mainly in the right and middle lower lobe; The tubular type, is the most common. Their timely diagnosis and treatment can improve survival and reduce costs for patients and health care.
Keywords: Bronchiectasis, Agammaglobulinemia, Immune System Diseases.
Introducción
Las bronquiectasias (BQs) constituyen una enfermedad heterogénea, resultado de factores infecciosos, genéticos, autoinmunes o alérgicos. Se definen como una dilatación permanente de los bronquios. Su prevalencia se estima en 52 pacientes por cada 100 000 habitantes en Estados Unidos, aunque en nuestro país existe escasa información al respecto.1,2
Las BQs generan altos costos directos e indirectos al paciente y al sistema de salud como consecuencia de la tasa de exacerbaciones, hospitalizaciones e incremento de la mortalidad, entre otros factores.1
Se calcula que entre el 20 al 30% de las BQs son postinfecciosas, y en el 53% de los casos no se identifica un factor causal.1
Las inmunodeficiencias primarias (IDPs) son una causa poco común de BQs.3 Un estudio multicéntrico realizado en España incluyó a 2047 pacientes adultos con BQs, con una media de edad de 65 años, mostró que el 9.4% de las mismas se asoció a una inmunodeficiencia primaria (IDP).4 Un estudio similar realizado en hospitales universitarios europeos reveló que el 5.8% de los pacientes con BQs fueron secundarias a IDP.5
La tomografía computarizada de alta resolución (TACAR) es el estudio de elección para el diagnóstico de BQs, con una sensibilidad del 96% y especificidad del 93% con cortes de 1 mm a intervalos de 10 mm, en inspiración máxima.6,7 La TACAR permite valorar la extensión y morfología de las BQs.
Los criterios diagnósticos tomográficos son:
- Signos directos: Dilatación bronquial con una relación broncoarterial mayor de 1-1.5 o también denominado signo en anillo de sello, falta de afilamiento de los bronquios y visualización de bronquios a 1 cm de la pleura.6
- Signos indirectos: Engrosamiento de la pared bronquial, pérdida de volumen lobular, patrón en mosaico, nódulos en árbol en brote y tapones de moco.6
Existen distintos sistemas de clasificación de las BQ, el más reconocido y aceptado es la clasificación de Lynne Reid que las agrupa de acuerdo a la morfología tomográfica.6
- BQs tubulares o cilíndricas: Bronquios de contornos regulares, no se observan en afinamiento normal hacia la periferia y los bronquios “hijos” son iguales a los bronquios “padres”. Los bronquios son más grandes que sus bronquios “hermanos” en un área del pulmón o se aprecian a menos de 1 cm de la superficie pleural. Engrosamiento de la pared bronquial y la luz bronquial ocluida por tapones mucosos.6,8
- BQs varicosas: De apariencia similar al de las venas varicosas, se caracterizan por la presencia de una vía aérea más dilatada y de contornos irregulares por la presencia de constricciones fibrosas localizadas que le dan un aspecto irregular, tipo rosario.6,8
- BQs saculares o quísticas: Presentan dilatación progresiva hacia la periferia de las vías aéreas y terminan en grandes quistes, sacos, o como racimos de uvas, con frecuentes niveles hidroaéreos.6,8
Las BQs también pueden clasificarse de acuerdo a la severidad en leve, moderada o grave. Actualmente se pueden emplear dos herramientas: el score FACED9 y el Bronchiectasis Severity Index (BSI), que contempla parámetros radiológicos, clínicos, de función pulmonar y microbiológicos con una excelente capacidad pronóstica.10,11,12
El tratamiento incluye la identificación y manejo de la causa, suspensión del tabaquismo, vacunación contra influenza y neumococo. Los beneficios de la fisioterapia pulmonar, broncodilatadores y corticoesteroides inhalados son poco claros.1,13
En las exacerbaciones está indicado el uso de antibióticos como macrólidos y antibióticos inhalados como tobramicina o gentamicina, sobre todo cuando se cuenta con cultivos positivos para Pseudomonas aeruginosa, ya que su persistencia es un predictor de mortalidad y está asociado a mayor extensión de la enfermedad y deterioro de la función pulmonar.1,13
En pacientes con BQs localizadas que no respondan a medidas higiénicas y farmacológicas, la lobectomía o segmentectomía debe ser considerada.1
La inmunodeficiencia común variable (IDCV) fue descrita por Janeway en 1953 y es la IDP más sintomática y frecuente en adultos. Su prevalencia es difícil de establecer debido a su subdiagnóstico, no obstante, en regiones como América del Norte y Europa, se reporta una frecuencia de 1:10 000 - 1:50 000 habitantes.14,15 Tiene una presentación bimodal, entre 6-8 años y 20-30 años, no obstante los síntomas pueden presentarse a cualquier edad, sin predominio de género.1,16,17
La definición y los criterios diagnósticos propuestos por la Sociedad Europea de Inmunodeficiencias (ESID) para IDCV son:
- Susceptibilidad a procesos infecciosos, autoinmunidad, enfermedad granulomatosa, trastornos linfoproliferativos policlonales sin explicación o algún familiar con inmunodeficiencia humoral (al menos uno de los anteriores).
- Además, disminución de al menos dos desviaciones estándar para la edad de IgG e IgA con o sin niveles bajos de IgM, medidos en dos ocasiones.
- Pobre respuesta a vacunas y/o isohemaglutininas ausentes.
- Pacientes mayores de 4 años, con exclusión de otras causas de hipogammaglobulinemia.
Puede mostrar un patrón de herencia autosómico dominante o recesivo, sin embargo, la mayor parte de las ocasiones es una enfermedad esporádica.15,18
Los pacientes con IDCV presentan infecciones severas y de repetición, principalmente sino-pulmonares. Tienen mayor susceptibilidad a autoinmunidad y malignidades del sistema reticuloendotelial y tumores sólidos.15
Su tratamiento incluye la sustitución de inmunoglobulina a dosis de 400-800 mg/kg de peso cada 3-4 semanas de acuerdo a los niveles séricos de la IgG y de la respuesta clínica, o bien, inmunoglobulina subcutánea semanal a dosis 100-200 mg/kg/dosis.19
Otras terapias recientes como el trasplante de células madre hematopoyéticas se han utilizado para tratar complicaciones (como linfoma, infecciones severas que no responden al tratamiento convencional y desregulación inmune),15 con una alta mortalidad, por lo que es indispensable contar con la caracterización inmunológica y genética del defecto asociado a IDCV para mejorar los resultados.20,21
La evaluación radiológica de los pulmones de pacientes con IDCV muestra múltiples cambios crónicos, incluyendo atrapamiento de aire, engrosamiento de la pared bronquial, BQs, enfisema, opacidades en vidrio despulido, consolidaciones pulmonares, nódulos pulmonares, y/o cicatrices/fibrosis, que han sido poco estudiados.22
La prevalencia de BQs en pacientes adultos con IDCV varía del 16 al 70%.1,2
Un estudio realizado en el servicio de Alergia e Inmunología Clínica del Hospital Británico de Buenos Aires y el Hospital Dr. Carlos G. Durand, incluyó a 69 pacientes adultos y niños con IDCV, con una prevalencia de BQs del 50%.11
En México, Mogica Martínez et al. reportaron una prevalencia de BQs del 75% en una cohorte pediátrica y de adultos con 24 pacientes, en el que incluyeron diferentes IDPs, en su mayoría secundarias a déficit de anticuerpos.23
Ramírez et al. incluyeron a 52 pacientes niños y adultos con IDCV, con reporte del 51% de BQs.24 En ninguno de los anteriores estudios, se describió el tipo y localización de las BQs.
El objetivo de este estudio fue conocer la prevalencia, el tipo y la localización de las BQs en pacientes de la Clínica de IDPs en adultos.
Material y métodos
Se realizó un estudio transversal, observacional y descriptivo, aprobado por el Comité de Ética Local. Se incluyeron todos los pacientes de la Clínica de IDPs del Hospital de Especialidades “Dr. Bernardo Sepúlveda Gutiérrez” del Centro Médico Nacional Siglo XXI del IMSS con diagnóstico de IDCV, de acuerdo con los criterios de la ESID.
Previo consentimiento informado, se les realizó TACAR en el servicio de Imagenología del mismo hospital, con un equipo General Electric Bright Speed, modelo 2335170-2. Los resultados fueron evaluados por un médico radiólogo experto en interpretación de tomografías pulmonares.
Se determinó el tipo de BQs y su localización tomando en cuenta la língula como un lóbulo independiente para facilitar la clasificación. Los resultados se reportan con estadística descriptiva, utilizando el programa SPSS versión 22.
Resultados
Treinta y dos pacientes fueron incluidos, 10 hombres (31.2%) y 22 mujeres (68.7%), con una media de edad de 42 ± 17 años (cuadro I).
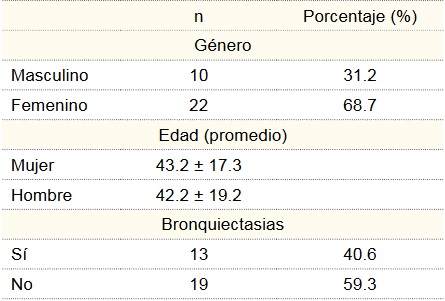
Cuadro I
Características generales de los pacientes con inmunodeficiencia común variable (ICV)
El 40.6% de los pacientes presentó BQs. Su localización fue variable, con predominio del lóbulo inferior derecho y lóbulo medio, solo un paciente presentó BQs exclusivamente en língula y el resto fueron combinaciones de sitios anatómicos, como se muestra en el cuadro II.
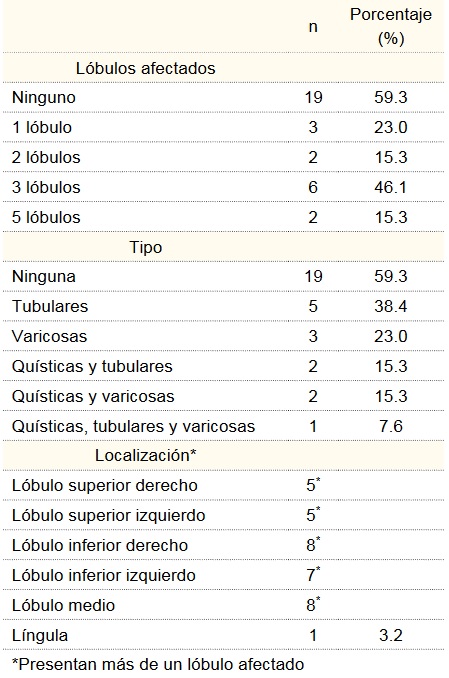
Cuadro II
Localización y tipo de bronquiectasias (BQs)
El tipo de BQs más común fue el tubular, seguido por el varicoso. Las combinaciones quísticas y tubulares se presentaron en el 15.3%, quísticas y varicosas 15.3%. Un paciente (7%) tuvo los tres tipos de BQ. Otros hallazgos tomográficos fueron atelectasias, trayectos de fibrosis, nódulos subsólidos, granulomas calcificantes y adenomegalias.
Del 59% de los pacientes que no tuvieron BQs, los hallazgos tomográficos encontrados por orden de frecuencia fueron: trayectos lineales de fibrosis, granulomas calcificados, engrosamiento intersticial, nódulos subsólidos, bulas y elevación diafragmática.
Discusión
La prevalencia de complicaciones pulmonares crónicas en IDCV es del 27-34%. La presencia de BQs es particularmente importante porque forman parte de los factores pronósticos de sobrevida de los pacientes.
Las BQs secundarias a IDPs se han reportado hasta en un 5.8% de los casos, pero particularmente los pacientes con IDCV las presentan hasta en un 70% de los casos.25
Cunningham et al. reportaron una prevalencia del 21% en una cohorte de 103 pacientes con IDCV, en comparación con los hallazgos de Sole et al. de 15% en su grupo de estudio, conformado únicamente por 15 pacientes.26,27
En el 2014, Kumar reportó un caso de IDCV y BQs difusas bilaterales, con predominio en lóbulos inferiores y lóbulos superiores, similar a lo encontrado en este estudio, sin embargo, es difícil evaluar los hallazgos dado que solo se refiere a un paciente.3
En México se han realizado estudios en poblaciones que incluyen niños y adultos con IDP, con una prevalencia de BQs hasta del 75%, mayor a la encontrada en nuestra cohorte; sin embargo, en ninguno de ellos se reportó la localización, ni el tipo de bronquiectasia, tampoco se específica la cantidad de pacientes incluidos con diagnóstico de IDCV.28
Nuestro grupo de estudio, a diferencia de lo publicado por otros autores, está constituido exclusivamente por adultos.
Conocer la localización y cantidad de lóbulos pulmonares afectados es importante porque repercute en las manifestaciones clínicas de los pacientes, su tratamiento y pronóstico.
Nuestro estudio refiere la prevalencia, tipo y localización de las BQs en una cohorte de pacientes adultos portadores de IDCV, lo que apoya la implementación de tratamientos adecuados para reducir sus complicaciones y realza la importancia de realizar estudios de TACAR en estos pacientes, aún cuando permanezcan asintomáticos. Por el momento, los intervalos para la realización de TACAR, durante su seguimiento, no se han establecido.29
Conclusiones
Este estudio describe las características morfológicas y localización de BQs en población adulta con IDCV, en un hospital de tercer nivel de atención del IMSS.
El porcentaje reportado de BQs en esta cohorte es mayor que el que se ha reportado en la literatura internacional, es importante continuar con esta línea de investigación en el IMSS y en otras instituciones de atención a la salud de nuestro país, que aporte datos sobre la severidad de las BQs, su impacto sobre la calidad de vida, supervivencia de los pacientes y costos para las instituciones de salud.
Referencias
1. Chalmers J, Aliberti S, Blasi F. Managment of bronchiectasias in adults. Eur Respir J. 2015;45(5):1446-1462.
2. Nonas S. Pulmonary manifestations of primary immunodeficiency disorders. Immunol Allergy Clin N Am. 2015;35(4):753-66.
3. Kumar PM. Common variable immunodeficiency disorder - An uncommon cause for bronchiectasis. Lung India. 2014;31(4):394-396.
4. Olveira IC, Padilla A, Martínez GM, De la rosa D, Girón RM. Etiología de las bronquiectasias en una cohorte de 2,047 pacientes. Análisis del registro histórico español. Arch de Bronconeumol. 2017;53(7):366-374.
5. Lonni S, Chalmers J, Goeminne PC, Mcdonnell MJ, Dimakou K. Etiology of non-cystic fibrosis bronchiectasis in adults and its correlation to disease severity. ATS Journals. 2017;12(12):1764-1770.
6. San Roman J, Dovasio F, Kreindel T, Kucharczyk M. Bronquiectasias. Arch Argent Pediatr. 2006;104(4):357-377.
7. Vendrell M, De Gracia J, Olveira C, Martínez MG, Girón R. Diagnosis and Treatment of Bronchiectasis. Arch Bronconeumol. 2008;44(11):629-40.
8. Ocampo ML, Salmon JA, Noguera VD, Zabala OC. Bronquiectasias: Revisión bibliográfica. Revista de Posgrado de la VIa Cátedra de Medicina. 2008;182:16-19.
9. Athanazio R, Corso PM, Gramblicka G, Calvacanti LF, Fernades FM. Latin America validation of FACED score in patients with bronchiectasis: an analysis of six cohorts. BMC Pulmonary Medicine. 2017;17(73):1-9.
10. Martínez GM, Selma FM, Navarro SC. Escalas multidimensionales en bronquiectasias. Medicina Respiratoria. 2015;8(1):31-38.
11. Martínez GM, De García J, Vendrell M, Girón RM, Carro LM. Multidimensional approach to non-cystic fibrosis bronchiectasis: the FACED score. Eur Respir J. 2014;43(5):1357-67.
12. Chalmers JD, Goeminne P, Aliberti S, Mc Donnell MJ, Lonni S. The bronchiectasis severity index. Am J Respir Crit Care Med. 2014;189(5):576-585.
13. Vendrell M, De Gracia J, Olveira C, Martínez MG, Girón R. Diagnosis and Treatment of Bronchiectasis. Arch Bronconeumol. 2008;44(11):629-40.
14. Fernández RD, Juri M, Paolini M, Malbran A. Inmunodeficiencia común variable epidemiología y manifestaciones clínicas en 69 pacientes. Medicina (Buenos Aires). 2013;73(4):315-323.
15. Saika B, Gupta S. Common variable inmunodeficiency. Indian J Pediatr. 2016;83(4):338-334.
16. Lin LJ, Wang YC, Liu XM. Clinical and Immunological Features of Common Variable Immunodeficiency in China. Chin Med J. 2015;128(3):310-315.
17. Marostica PJ, Fisher GB. Non-cystic fibrosis bronquiectasias: a perspective from South America. Pediatric respiratory reviews. 2006;4(4):275-280.
18. Do Amor Divino PH, Carvalho BJ, Alves FR, Polonio BI, Neves FW. Bronchiectasis caused by common variable immunodeficiency. J Bras Pneumol. 2015;41(5):482-483.
19. Zea VA. Bronquiectasias diseminada en un adulto con inmunodeficiencia común variable. Colombia Médica. 2015;46(1):47-50.
20. Cambray GJ, Herrera SD, López PP, Chávez GA, Yamazaki NM. Trasplante de médula ósea en pacientes con inmunodeficiencia común variable, ¿es una opción terapéutica?. Rev Alerg Mex. 2017;64(1): 121-125.
21. Wehr C, Gennery, AR, Lindemans, C, Schulz, A, Hoening, M. Multicenter experience in hematopoietic stem cell transplantation for serious complications of common variable immunodeficiency. J Allergy Blin Immunol. 2015;135(4): 988-997.
22. Maglione PJ, Overbey JR, Radigan L, Bagiella E, Cunningham RC. Pulmonary radiologic findings in CIDV: Clinical and inmunological correlations. Ann Allergy Asthma Immunol. 2014;113(4):452-459.
23. Mogica MM, García LS, Silva VR, Montaño VB, Cruz MA. Neumopatías en pacientes con inmunodeficiencias primarias en tratamiento con gammaglobulina intravenosa. Rev Alerg Mex. 2007;54(1):14-19.
24. Ramírez VN, Arablin OS, Mojica MD, Yamazaki N.M, García CM. Clinical and inmunological features of common variable inmunodeficiency in mexicans patients. Allergol Immunopathol. 2014;42(3):235-240.
25. Buckley RH. Pulmonary complications of primary immunodeficiencies. Paediatr Respir Rev. 2004;5(Suppl. A):225-33.
26. Cunningham-Rundles C. Clinical and immunological analyses of 103 patients with common variable immunodeficiency. J Clin Immunol 1989;9:22-3.
27. Solé D, Leser PG, Hilario MO, Soares FJ, Naspitz CK. Common variable immunodeficiency: a clinical and laboratory evaluation of 15 cases. Rev Paul Med. 1992;110(1):42-48.
28. Dorberker-Azcona R, Mogica-Martinez MD, Becerril-Angeles M, Guevara-Cruz M, Espinosa-Padilla S, Yamazaki-Nakashimada MA, Blancas-Galicia L. Clinical and therapeutic features in patients with common variable immunodeficiency from two third-level care hospitals from México City. Rev Alerg Mex. 2013;60(1):26-30.
29. Touw CM, van de Ven AA, de Jong PA, Terheggen-Lagro S, Beek E, Sanders EA, van Montfrans JM. Deteccion of pulmonary complications in common variable immunodeficiency. Pediatr Allergy Immunol. 2010;21(5):793-805.
Notas
Notas de autor
mhdzo@hotmail.com
Información adicional
PubMed: https://www.ncbi.nlm.nih.gov/pubmed/29799713
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/2524/2885 (pdf)
