Aportaciones originales
Recepción: 22 Mayo 2017
Aprobación: 19 Junio 2017
Resumen:
Introducción: El síndrome de Guillain-Barré (SGB) es una polirradiculoneuropatía aguda caracterizada por debilidad simétrica progresiva de las extremidades con hipo o arreflexia, que progresa en un máximo de 4 semanas y que puede llevar a la falla respiratoria y a discapacidad a largo plazo. El objetivo de este trabajo fue describir las características clínicas, epidemiológicas y neurofisiológicas de pacientes con SGB del Hospital de Especialidades del Centro Médico Nacional Siglo XXI (HECMNSXXI).
Métodos: se realizó un estudio observacional de tipo transversal retrolectivo. Se obtuvieron datos de expedientes clínicos de adultos con diagnóstico de SGB hospitalizados en el HECMNSXXI en el periodo de marzo de 2012 a marzo de 2016. Se registraron variables demográficas, clínicas y neurofisiológicas.
Resultados: se incluyeron 94 pacientes con un promedio de edad de 53 años, en su mayoría hombres, con infección previa en 80%. La fuerza muscular medida con la escala del Medical Research Council (MRC) fue en promedio de 32, la escala de discapacidad del SGB (Hughes) al ingreso tuvo un promedio de 3.63. La variedad axonal se encontró en 68%, la desmielinizante en 29% y en 3% no concluyente.
Conclusiones: se documentan en esta muestra características demográficas y clínicas similares a lo reportado en la literatura, así como la mayor proporción de variedades axonales, las cuales tienen mayor severidad en la presentación clínica así como mal pronóstico.
Palabras clave: Síndrome de Guillain-Barré, Polirradiculoneuropatía, Enfermedades Autoinmunes del Sistema Nervioso.
Abstract:
Background: Guillain-Barré Syndrome (GBS) is an acute polyneuropathy characterized by symmetrical weakness of the limbs with hyporeflexia or areflexia with a maximum progression within four weeks and can impair respiratory function and implies disability at a long. The aim of this paper was to describe the clinical, epidemiological and neurophysiological features of patients with GBS at the Hospital de Especialidades del Centro Medico Nacional Siglo XXI (HECMNSXXI)
Methods: An observational, retrospective cross-sectional study, data were collected form clinical records of adults with GBS hospitalized in HECMNSXXI from March 2012 to March 2016. The recorded variables were demographics, previous infection, clinical presentation, disability scores, prognosis scores and neurophysiological subtypes.
Results: Clinical records of 94 patients were analysed with a mean age of 53 years, 61% male, with previous infection in 80%. Albumin cytologic dissociation was present in 50%. Medical Research Council (MRC) sum scores mean was 32, the SGB disability score at admittance with a mean of 3.63. The axonal subtype was in 68%, and demyelinating in 29%, not conclusive in 3%.
Conclusions: In this study the demographic and clinical features are similar to other previous reports, we documented a greater proportion of axonal subtype, which are related with important disability and worse prognosis.
Keywords: Guillain-Barré Syndrome, Polyradiculoneuropathy, Autoimmune Diseases of the Nervous System.
El síndrome de Guillain-Barré (SGB) es una polirradiculoneuropatía aguda autoinmune, que se caracteriza por debilidad simétrica de las extremidades con hiporreflexia o arreflexia, con progresión máxima de 4 semanas.1,2,3 Dada la eliminación de la poliomielitis, constituye actualmente la causa más importante de parálisis flácida aguda.4 Además de los síntomas motores, con frecuencia se observan síntomas sensitivos, afección de nervios craneales y pueden presentar complicaciones importantes como dificultad respiratoria y disfunción autonómica.2,3
El SGB se considera una enfermedad rara, las incidencias reportadas van de 0.81 a 1.89 casos por cada 100 000 personas.5 Las mujeres son afectadas más frecuentemente; así también se presenta con mayor frecuencia en adultos que en niños.5,6 Existen dos variantes principales: AMAN (Acute motor axonal neurophaty) y AMSAN (Acute motor sensory axonal neurophaty), la primera más frecuente en países europeos y Norteamérica, y las segundas en Asia y América Latina.1,4
Usualmente, es un síndrome postinfeccioso, dos tercios de los paciente reportan antecedente de infección de vías respiratorias o gastrointestinales previo a la instalación del SGB.7 Entre los patógenos identificados en el desarrollo del síndrome están, principalmente: Campylobacter jejuni, citomegalovirus, virus de Epstein-Barr y Mycoplasma pneumoniae entre otros, como causa de Haemophilus influenzae, virus de la influenza tipo A, dengue y recientemente se han documentado casos asociados a Chikunguña y Zika.7,8,9,10,11 En la patogénesis se presenta la generación de anticuerpos que hacen reacción cruzada con gangliósidos específicos.4,12
Es frecuente encontrar en el líquido cefalorraquídeo (LCR) aumento de la concentración de proteínas con el número de células normales, lo que se conoce como disociación albumino-citológica. Los estudios neurofisiológicos de conducción nerviosa son adyuvantes en el diagnóstico y permiten la clasificación en las variedades desmielinizantes o axonales. La presentación clínica, el análisis de LCR y los estudios neurofisiológicos son parte esencial de los criterios diagnósticos.13,14,15
El Hospital de Especialidades del Centro Médico Nacional Siglo XXI (HECMNSXXI) del Instituto Mexicano del Seguro Social es un hospital de referencia en México, en este estudio se muestran los aspectos epidemiológicos y clínicos de pacientes con SGB del servicio de neurología.
Métodos
Se realizó un estudio observacional, descriptivo, retrolectivo, transversal. Los datos se obtuvieron de expedientes clínicos de pacientes adultos, de cualquier género, con el diagnóstico de SGB de acuerdo a los criterios de Brighton, con nivel de certeza de 1-3, que fueron hospitalizados en el periodo de marzo de 2012 a marzo de 2016 en el HECMNSXXI. El diagnóstico clínico fue realizado por especialistas en neurología, y fue complementado con estudios de LCR, conducción nerviosa y pruebas de laboratorio. Los datos analizados fueron: las características demográficas, cuadros infecciosos previos, presentación clínica, grado de discapacidad de SGB (escala de Hughes), pronóstico (a través de las escalas de Erasmus GBS, Respiratory Insufficiency Score [EGRIS] y Erasmus GBS Outcome Score [EGOS]), así como variantes neurofisiológicas. Se utilizó estadística descriptiva de acuerdo al tipo de variable. El estudio fue aprobado por un comité local de investigación.
Resultados
Se revisaron los expedientes clínicos de 94 pacientes, 57 hombres (61%) y 37 mujeres (39%). La media de la edad fue de 53 años (rango 21-82 años). El 50% de los casos se presentaron en los primeros 4 meses del año, siendo abril el mes con más frecuencia con 16% (figura 1). Con antecedente de diabetes mellitus 2 se encontraron 22 pacientes (23%), hipertensión arterial 30 (32%), tabaquismo 35 (37%). Previo al inicio de los síntomas del SGB, 39 pacientes (41%) presentaron infección gastrointestinal, 29 (31%) infección de vías respiratorias, 3 (3%) infección gastrointestinal y de vías respiratorias, 7 (7%) otras infecciones, 1 paciente se vacunó contra la influenza, 1 paciente fue sometido a cirugía y 14 pacientes (15%) no presentaron un cuadro patológico previo (cuadro I). La media de días del cuadro previo a la instalación del SGB fue de 10.9 ±7.
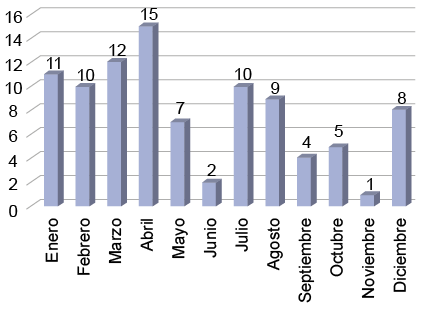
Figura 1
Distribución anual de casos de síndrome de Guillain-Barré en el Hospital de Especialidades del CMNSXXI
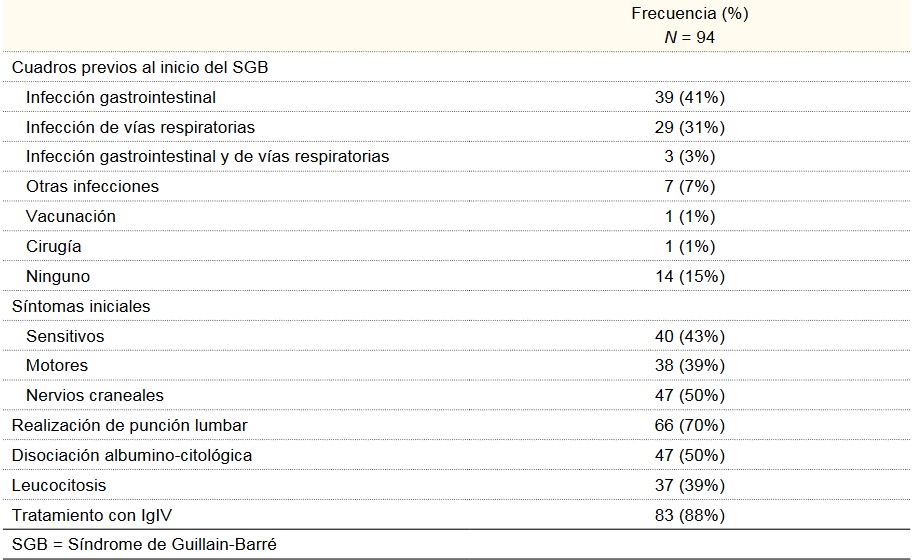
Cuadro I
Datos de pacientes incluidos en el estudio
Con respecto a la presentación clínica, los síntomas iniciales fueron sensitivos en 40 pacientes (43%) y motores en 38 (39%). En 47 pacientes (50%) se documentó afección de nervios craneales, siendo los más frecuentemente afectados: el facial (30%), los oculomotores (28%) y bulbares (16%), 31 pacientes (33%) presentaron disautonomías.
Al ingreso, 25 pacientes (27%) presentaron un SGB disability score (Hughes) de 5, que fueron quienes requirieron ventilación mecánica, la media de Hughes de todos los pacientes fue de 3.63 ± 1.27; mientras que la media de MRC fue de 32 ± 19.5. La media de la escala de EGRIS fue de 3.34 ± 1.9, resultando: con riesgo bajo 32 pacientes (34%), riesgo intermedio 34 (36%) y riesgo alto 28 pacientes (30%). La media en escala de EGOS fue de 5.03 ± 2.8, en la cual 48 pacientes (51%) tuvieron puntaje mayor de 5, lo que augura mal pronóstico (cuadro II). La máxima progresión se alcanzó en el día 9.5 ± 5.4, en 83 pacientes (88%) quienes recibieron tratamiento con inmunoglobulina G intravenosa.
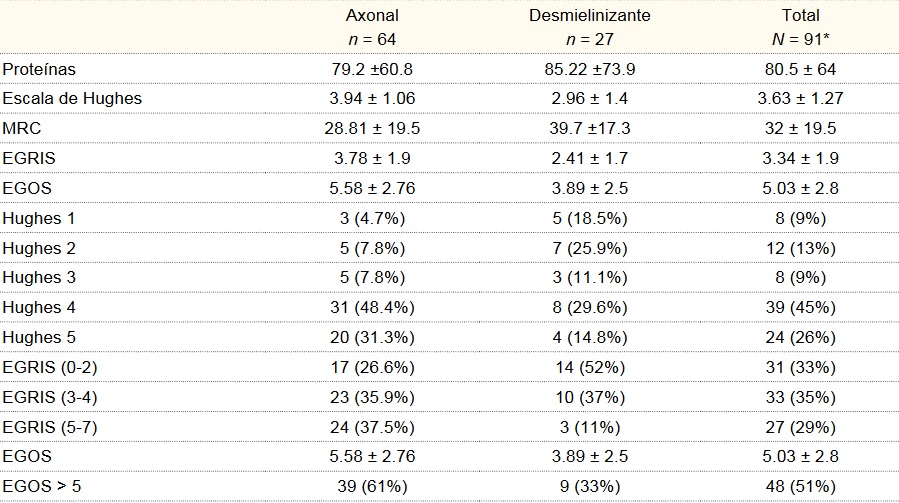
Cuadro II
Valoraciones en los pacientes
* Se presentaron 3 casos no concluyentes; MRC = Medical Research Council (sum score); EGRIS = Erasmus GBS Respiratory Insufficiency Score; EGOS = Erasmus GBS Outcome Score
Se realizó VCN a los 94 pacientes, resultando 64 de ellos con variedad axonal (68%), desmielinizante 27 (29%) y 3 (3%) sin datos concluyentes. En 44 pacientes (46.8%) se obtuvo certeza diagnóstica. Los resultados de escalas como MRC, Hughes, EGRIS y EGOS por variedad neurofisiológica se muestran en el cuadro III.
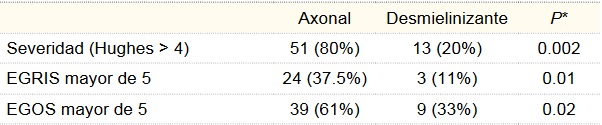
Cuadro III
Resultados de escalas Hughes, EGRIS y EGOS por variedad neurofisiológica
*Chi cuadrada de Pearson o Prueba exacta de Fisher
La media de la cuenta de leucocitos fue de 11512 ± 7414, 37 pacientes (39%) presentaron leucocitosis. La media de glucosa fue de 131 ± 53.9. Se realizó punción lumbar a 66 pacientes (70%), observándose una media de concentración de proteínas de 80.5 ± 64 y cuenta de células de 1.47 ± 2.1, documentándose hiperproteinorraquia y, por ende, disociación albumino-citológica en 47 pacientes (71%); la media del tiempo del inicio de los síntomas a la toma de LCR fue de 8.48 ± 5.4 días.
Discusión
El Síndrome de Guillain-Barré (SGB) es una enfermedad que se observa con frecuencia en nuestro hospital, constituye una urgencia neurológica por el riesgo de falla respiratoria y muerte, además de que se relaciona con discapacidad a largo plazo. Reportamos los hallazgos de 94 casos hospitalizados en un periodo de 4 años, de los cuales se obtuvieron sus características clínicas y neurofisiológicas. La edad promedio de los pacientes fue de 53 años, pero con un rango de 21 a 80 años, con una mayor proporción de hombres con un 61%, lo cual es similar a otras series reportadas en México.16,17,18,19 En lo referente a la frecuencia de aparición de casos con respecto a la época del año, se identificó que el 50% de los casos se presentó en los primeros cuatro meses, lo que coincide con el final del invierno y que puede estar relacionado con las infecciones respiratorias y el inicio de la primavera, probablemente con aumento de infecciones gastrointestinales, lo cual es similar con otras series en el país que reportan más casos en invierno o verano, aunque carecen de datos significativos.17,18 En estudios en otros países también ha sido variable la presencia de casos respecto a la estación del año.6
El 80% de los pacientes tuvo antecedente de infección respiratoria, gastrointestinal u otra, porcentaje que resultó es más alto de lo que se reporta habitualmente (60-70%, dos terceras partes de los casos),7 e incluso con lo reportado por Carrillo et al. de 56% en su estudio en Tabasco, aunque cabe señalar que los pacientes incluidos fueron los que tenían expedientes clínicos con datos completos, por lo que pudo haber un sesgo de selección. Hubo dos pacientes que presentaron cuadro clínico con Chikunguña, pero no se obtuvieron todos los datos para confirmar el diagnóstico, aunque nos parece relevante señalarlo porque entre 2015 y 2016 hubo un brote de casos en algunos estados cuyos pacientes fueron referidos a nuestro hospital. Otros cuadros previos que se relacionaron al SGB fueron un caso de vacunación y un paciente que fue sometido a cirugía.
El cuadro infeccioso precede, en promedio, en 11 días y se alcanza el nadir, en promedio, a los 9 días, similar a lo ya reportado. Con respecto a los síntomas iniciales, hay una alta frecuencia de afección de algún nervio craneal con 50%, síntomas sensitivos en 43% y motor 39%, cabe señalar que respecto a los nervios craneales se incluye cualquier afección, ya sea de oculomotores, facial o bulbares. Las manifestaciones autonómicas, de acuerdo con estudios previos, ocurren en 2 terceras partes de los pacientes,20 en nuestro estudio solo se documentaron en el 33%, lo cual habría que verificar si se debió a un monitoreo no adecuado. Se realizó punción lumbar al 66% de los pacientes, encontrando disociación albumino-citológica en el 71%, también acorde a reportes previos. En nuestro hospital se tiene disponible la IgIV por lo que se otorgó este tratamiento en el 88% de los casos, las razones para no dar tratamiento fueron una escala de Hughes de 1 a 3 y/o evolución sin progresión. El promedio de puntuación de MRC que tiene que ver con la medición de la fuerza muscular fue de 32, de un máximo 60, y con menores calificaciones en las variantes axonales comparadas con las desmielinizantes. Se realizó las escala de EGRIS al ingreso, que establece el riesgo de falla respiratoria en la primera semana, e involucra los días de inicio de síntomas e ingreso hospitalario, debilidad facial o bulbar al ingreso y el puntaje de MRC; 21 el promedio de esta escala fue de 3.34, que se calificó como un riesgo intermedio. También se midió la escala de EGOS que establece el riesgo de la capacidad para caminar a 6 meses e involucra la edad al ingreso, antecedente de diarrea y calificación de la escala de Hughes a las dos semanas de inicio de los síntomas,22 obteniendo un promedio de 5.03, que se calificó como un riesgo alto.
Se realizó estudio neurofisiológico a todos los pacientes de esta serie, con un predominio de la variedad axonal en 68%, desmielinizante 29% y en el 3% de los pacientes el estudio no resultó concluyente para alguna variedad en específico, estos datos son acordes a lo reportado tanto en literatura nacional como internacional del predominio de las variedades axonales en países latinoamericanos y específicamente en México.1,17,18,19,23 Al ver el comportamiento en algunas variables de las variantes axonal y desmielinizante, podemos ver que las variedades axonales tienen mayor proporción de Hughes alto, EGRIS y EGOS con riesgo alto, comparadas con las desmielinizantes, lo cual muestra la mayor severidad en la presentación y un peor pronóstico de la variedad axonal que se ha reportado en la literatura. Este estudio tiene limitaciones evidentes, por estar basado en registros clínicos con los consecuentes sesgos de información y selección, así como por ser transversal. Se requieren seguimientos para poder establecer asociaciones y pronósticos, pero nos permite tener un panorama de la presentación clínica y las diferencias con las que se presentan las variedades axonal y desmielinizante en una muestra importante de pacientes con SGB en México
Conclusión
El SGB es una urgencia neurológica frecuente en nuestro medio, precedida por un proceso infeccioso en la mayoría de los casos, con alteraciones en la función motora, sensitiva y de nervios craneales principalmente; la variedad más frecuente fue la axonal, que se relacionó con una mayor severidad en la presentación clínica y un peor pronóstico tanto en la hospitalización como para la deambulación a los seis meses medida por escalas ya establecidas.
Referencias
1. Hughes RA, Cornblath DR. Guillain-Barré syndrome. Lancet. 2005;366:1653-1666.
2. Willison HJ, Jacobs BC, van Doorn PA. Guillain-Barré syndrome. Lancet. 2016;388:717-727.
3. van den Berg B, Walgaard C, Drenthen J, Fokke C, Jacobs BC, van Doom PA. Guillain-Barré syndrome: pathogenesis, diagnosis, treatment and prognosis. Nat Rev Neurol. 2014;10:469-482.
4. Yuki N, Hans-Peter H. Guillain-Barré syndrome. New Engl J Med. 2012;366: 2294-304.
5. Sejvar JJ, Baughman AL, Wise M, Morgan OW. Population incidence of Guillain-Barré syndrome: A systematic review and meta-analysis. Neuroepidemiology. 2011;36:123-133.
6. McGrogan A, Madle GC, Seaman HE, De Vries CS. The epidemiology of Guillain-Barré syndrome worldwide: A systematic literature review. Neuroepidemiology. 2009;32:150-163.
7. Jacobs BC, Rothbarth PH, van der Meché FG, Herbrink P, Schmitz PI, de Klerk MA, et al. The spectrum of antecedent infections in Guillain-Barré syndrome: a case-control study. Neurology. 1998;51:1110-1115.
8. Caudie C, Quittard-Pinon A, Taravel D, Sivadon-Tardy V, Orlikowsky D, Rozenberg F, et al. Preceding infections and anti-ganglioside antibody profiles assessed by a dot immunoassay in 306 French Guillain-Barré syndrome patients. J Neurol. 2011;258:1958-1964.
9. Brasil P, Sequeira PC, Freitas AD, Zogbi HE, Calvet GA, de Souza RV, et al. Guillain-Barré syndrome associated with Zika virus infection. Lancet. 2016;387:1482.
10. Dirlikov E, Major CG, Mayshack M, Medina N, Matos D, Ryff KR, et al. Guillain-Barré Syndrome During Ongoing Zika Virus Transmission. MMWR. Morb Mortal Wkly Rep. 2016;65(34)910-914.
11. Simon O, Billot S, Guyon D, Daures M, Descloux E, Gourinat AC, et al. Early Guillain-Barré Syndrome associated with acute dengue fever. J Clin Virol. 2016;77:29-31.
12. Uncini A, Kuwabara S. Nodopathies of the peripheral nerve: an emerging concept. J Neurol Neurosurg Psychiatry. 2015;86:1186-1195.
13. Sejvar JJ, Kohl KS, Gidudu J, Amato A, Bakshi N, Baxter R, et al. Guillain-Barré syndrome and Fisher syndrome: Case definitions and guidelines for collection, analysis, and presentation of immunization safety data. Vaccine. 2011;29(3):599-612.
14. Asbury AK, Cornblath DR. Assessment of current diagnostic criteria for Guillain-Barré syndrome. Ann Neurol. 1990;27 (Suppl 1):S21-S24.
15. Fokke C, van den Berg B, Drenthen J, Walgaard C, van Doorn PA, JAcobs BC. Diagnosis of Guillain-Barré syndrome and validation of Brighton criteria. Brain. 2014;137(Pt 1):33-43.
16. Domínguez-Moreno R, Tolosa-Tort P, Patiño-Tamez A, Quintero-Bauman A, Collado-Frías D, Miranda-Rodríguez MG, et al. Mortality associated with a diagnosis of Guillain-Barré syndrome in adults of Mexican health institutions. Rev Neurol. 2014;58:4-10.
17. Zúñiga-González EA, De la Cruz AR, Millán-Padilla J. Subtipos electrofisiológicos del síndrome de Guillain-Barré en adultos mexicanos. Rev Med Inst Mex Seguro Soc. 2007;45:463-468.
18. Carrillo-Pérez DL, García-Ramos G, Ruano-Calderón LÁ, Sosa-Hernández JL, Méndez-Castillo JJ. Síndrome de Guillain-Barré en un hospital de referencia en México. Rev Mex Neurocienc. 2012;13:15-21.
19. De La O-Peña D, Robles-Figueroa M, Chávez-Peña Q, Bedolla-Barajas M. Características del síndrome de Guillain-Barré en adultos: resultados de un hospital universitario. Rev Med Inst Mex Seguro Soc. 2015;53(6):678-85.
20. van Doorn PA, Ruts L, Jacobs BC. Clinical features, pathogenesis and treatment of Guillain-Barré syndrome. Lancet Neurol. 2008;7:939-950.
21. Walgaard C, Lingsma HF, Ruths L, Drenthen J, van Koningsveld R, Garssen MJ, et al. Prediction of respiratory insufficiency in Guillain-Barré syndrome. Ann Neurol. 2010;67(6):781-787.
22. van Koningsveld R, Steyerberg EW, Hughes RA, Swan AV, van Doorn PA, Jacobs BC. A clinical prognostic scoring system for Guillain-Barré syndrome. Lancet Neurol. 2007;6(7):589-594.
23. Nachamkin I, Arzate-Barbosa P, Ung H, Lobato C, González-Rivera A, Rodríguez P, et al. Patterns of Guillain-Barré syndrome in children: Results from a Mexican population. Neurology. 2007;69:1665-1671.
Notas
Notas de autor
neurojgc@gmail.com
Información adicional
PubMed: https://www.ncbi.nlm.nih.gov/pubmed/29799712
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/2525/2886 (pdf)
