Aportación Original
Metaanálisis de pruebas diagnósticas para la detección de COVID-19
Meta-analysis of diagnostic tests for the detection of COVID-19
Metaanálisis de pruebas diagnósticas para la detección de COVID-19
Revista Médica del Instituto Mexicano del Seguro Social, vol. 59, núm. 3, pp. 182-188, 2021
Instituto Mexicano del Seguro Social

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 24 Febrero 2021
Aprobación: 15 Abril 2021
Resumen:
Introducción: la enfermedad COVID-19 surgió a finales de 2019 y se empezó a considerar pandemia a principios de 2020. La metodología de referencia para su diagnóstico es la prueba RT-qPCR.
Objetivo: se evalúo la sensibilidad y la especificidad de kits de pruebas moleculares que se encuentran en la lista de pruebas del Instituto de Diagnóstico y Referencia Epidemiológicos (InDRE).
Material y métodos: a partir del uso de las plataformas PubMed y Google Scholar se realizó una búsqueda de artículos, de los cuales se seleccionaron 14 y se recuperó el número de muestras analizadas y su estado (positivo o negativo) según el método molecular de referencia, el nombre del kit de prueba utilizado, así como las características y los resultados obtenidos, expresados como verdaderos positivos, falsos negativos, verdaderos negativos y falsos positivos. Se calculó la sensibilidad y la especificidad de ocho kits con la compilación de calculadoras estadísticas OpenEpi versión 3.01, mediante el método de puntos de Wilson con un intervalo de confianza de 95%.
Resultados: los kits evaluados tuvieron una sensibilidad y una especificidad superior al 90%.
Conclusiones: las pruebas permiten detectar la presencia o ausencia del virus, pero pueden verse afectadas por condiciones durante las etapas del método.
Palabras clave: Coronavirus, Reacción en Cadena de la Polimerasa, Sensibilidad y Especificidad.
Abstract:
Background: COVID-19 disease emerged at the end of 2019 and it started to be considered a pandemic at the beginning of 2020. The reference methodology for the COVID-19 diagnosis is the RT-qPCR.
Objective: It was assessed the sensitivity and specificity of molecular test kits found on the list of tests of the Instituto de Diagnóstico y Referencia Epidemiológicos (InDRE, Institute for Epidemiologic Diagnosis and Reference).
Material and methods: By using the PubMed and the Google Scholar platforms, a search was carried out for articles, out of which 14 were selected, retrieving the number of samples analyzed and their status (positive or negative), according to the molecular reference method, the name of the test kit used, as well as the characteristics and results obtained, expressed as true positives, false negatives, true negatives and false positives. Sensitivity and specificity of 8 kits were calculated, with compilations of the OpenEpi, version 3.01, statistical calculators, by using the Wilson score with a 95% confidence interval.
Results: The sensitivity and specificity results for the kits were greater than 90%.
Conclusions: Tests evaluated allow the detection of presence or absence of virus, but they can be affected by conditions during the stages of the method.
Keywords: Coronavirus, Polymerase Chain Reaction, Sensitivity and Specificity.
Introducción
La enfermedad denominada COVID-19 surgió a finales del año 2019 en Wuhan, capital de la provincia de Hubei, en China. Inició con el reporte de un brote de neumonía de origen desconocido en ese momento. Posteriormente se realizó la secuenciación genómica del agente causal y se pudo identificar la relación entre este virus y los miembros de una especie denominada coronavirus (CoV), causantes del síndrome respiratorio agudo severo (SARS, por sus siglas en inglés), por lo que el Comité Internacional de Taxonomía de Virus lo nombró SARS-CoV-2.1
El 11 de marzo de 2020, la Organización Mundial de la Salud (OMS) determinó que la COVID-19 puede caracterizarse como una pandemia.2 En México, el primer caso de COVID-19 se registró el día 27 de febrero de 2020 y el 18 de marzo la primera muerte.3
El mecanismo de transmisión de la COVID-19 es de persona a persona; la principal forma de diseminación del virus es por contacto con gotitas de saliva o mucosidad provenientes de personas infectadas, así como mediante aerosoles.4
Estudios muestran que el SARS-CoV-2 tiene lugares optimizados para su unión a los receptores de la enzima convertidora de angiotensina 2 (ACE2) humana, así como espigas virales modificadas en el sector S, donde tiene un sitio de escisión polibásico funcional (furina), específicamente entre las subunidades S1 y S2, por medio de la inserción de 12 nucleótidos que podría aumentar así el potencial infectivo del virus.5
Diagnóstico de laboratorio
Actualmente se cuenta con pruebas de diagnóstico, que detectan al virus causante de COVID-19, y pruebas de anticuerpos contra SARS-CoV-2, que demuestran la respuesta inmunológica después de la infección. En México, el Instituto de Diagnóstico y Referencia Epidemiológicos (InDRE) “Dr. Manuel Martínez Báez” ha evaluado y aprobado 152 kits de pruebas de diagnóstico molecular.6
Detección de material genético del virus mediante PCR
Las pruebas moleculares son altamente sensibles y específicas, rápidas y ampliamente utilizadas para la detección de patógenos.7 La reacción en cadena de la polimerasa con transcriptasa inversa en tiempo real (RT-qPCR, por sus siglas en inglés) es la metodología de referencia para confirmar la presencia del virus SARS-CoV-2.
El tipo de muestra recomendado por la Secretaría de Salud de México es un exudado faríngeo y nasofaríngeo, recolectados en un mismo tubo con el propósito de aumentar la carga viral. En pacientes con enfermedad grave, la muestra puede ser lavado o aspirado nasofaríngeo, bronquioalveolar o broncoaspirado, aspirado traqueal, nasofaríngeo o biopsia de pulmón.8
La Organización Panamericana de la Salud (OPS) recomienda exudados nasofaríngeos y orofaríngeos combinados; aclara que si los hisopos son un factor limitante debe priorizarse la muestra nasofaríngea.9
Detección de antígenos virales
Un tipo de estudio de detección de antígenos son las pruebas rápidas, que son cualitativas y son capaces de emitir un resultado en menos de 30 minutos. Existen kits comerciales, los cuales están disponibles para efectuar este tipo de pruebas; sin embargo, no están recomendadas para diagnóstico clínico debido a que su sensibilidad es fácilmente afectada por factores como el tipo de muestra, la recolección y el transporte.10
Pruebas de anticuerpos contra SARS-CoV-2
Son pruebas que evalúan la respuesta inmunológica humoral de los pacientes y permiten dar seguimiento a la enfermedad y realizar estudios de seroprevalencia. Pueden detectar anticuerpos en sangre venosa y sangre capilar mediante inmunocromatografía, inmunofluorescencia indirecta (IFI) o ensayo de inmunoabsorción ligado a enzimas (ELISA). Estas pruebas de anticuerpos se basan en la detección de inmunoglobulinas IgG e IgM contra SARS-CoV-2.11
Material y métodos
Búsqueda de literatura
Se utilizaron las plataformas PubMed y Google Scholar para buscar artículos con las palabras False positive/negative PCR SARS-CoV-2 COVID-19 y Commercial RT-qPCR diagnostic test for COVID-19 y de esa manera acceder a trabajos que evaluaran kits de pruebas moleculares en muestras clínicas. Todos los resultados obtenidos fueron del año 2020.
Selección de estudios
Los artículos recuperados fueron seleccionados y se descartaron los que se repetían, aquellos que no estaban disponibles en texto completo, los que describían otra prueba diagnóstica o de anticuerpos, así como aquellos cuya metodología no era descrita, que tuvieran una muestra utilizada que no fuera hisopado nasofarígeo o aquellos cuyas pruebas no estuvieran en la lista de pruebas moleculares del InDRE (figura 1).
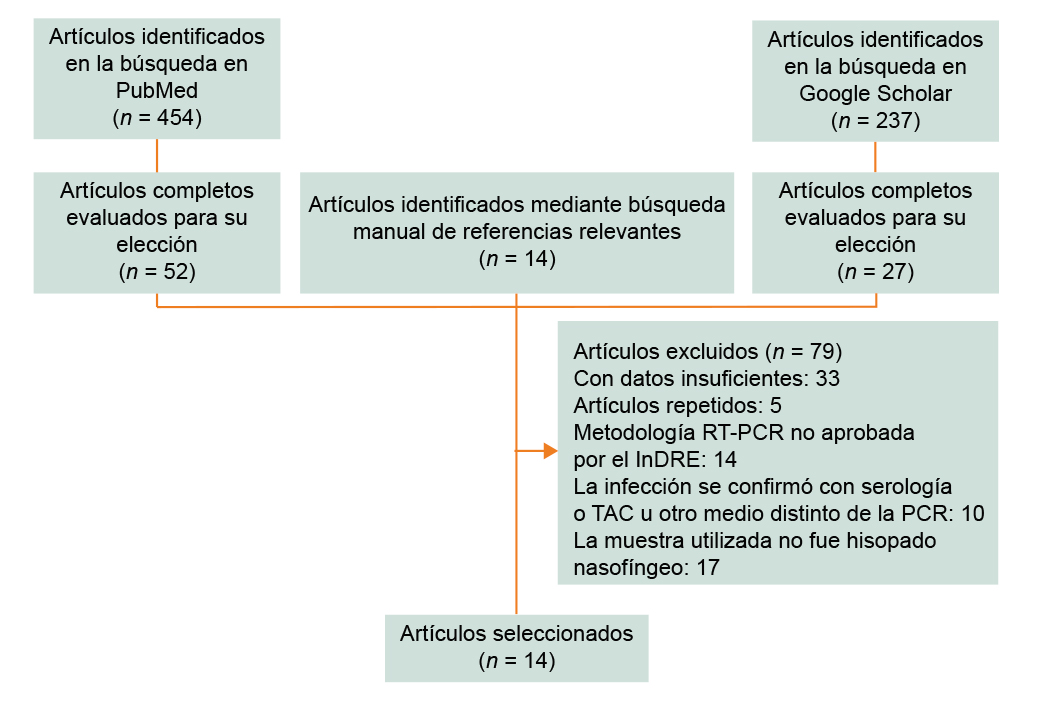
Figura 1
Diagrama del procedimiento de selección de estudios
De cada estudio se recuperaron los datos de los ensayos clínicos realizados con las pruebas moleculares utilizadas. Estos datos son el número de muestras analizadas y su estado (positivo o negativo) según un método molecular de referencia, el nombre del kit de prueba utilizado, así como sus características y resultados obtenidos, expresados como verdaderos positivos (VP), falsos negativos (FN), verdaderos negativos (VN) y falsos positivos (FP).
Análisis estadístico
Se analizaron los datos reportados en los 14 estudios con la compilación de calculadoras estadísticas OpenEpi, versión 3.01. Para cada prueba diagnóstica se calculó, con base en los resultados de VP, FN, VN y FP, sensibilidad y especificidad, con un intervalo de confianza del 95%, mediante el método de puntos de Wilson.
Resultados
Se evaluaron los valores de sensibilidad y especificidad de ocho pruebas moleculares descritas en 14 artículos científicos. Las características de las pruebas analizadas, así como el número de muestras analizadas se encuentran en el cuadro I, mientras que los resultados del análisis de sensibilidad y especificidad de cada prueba se muestran en el cuadro II.
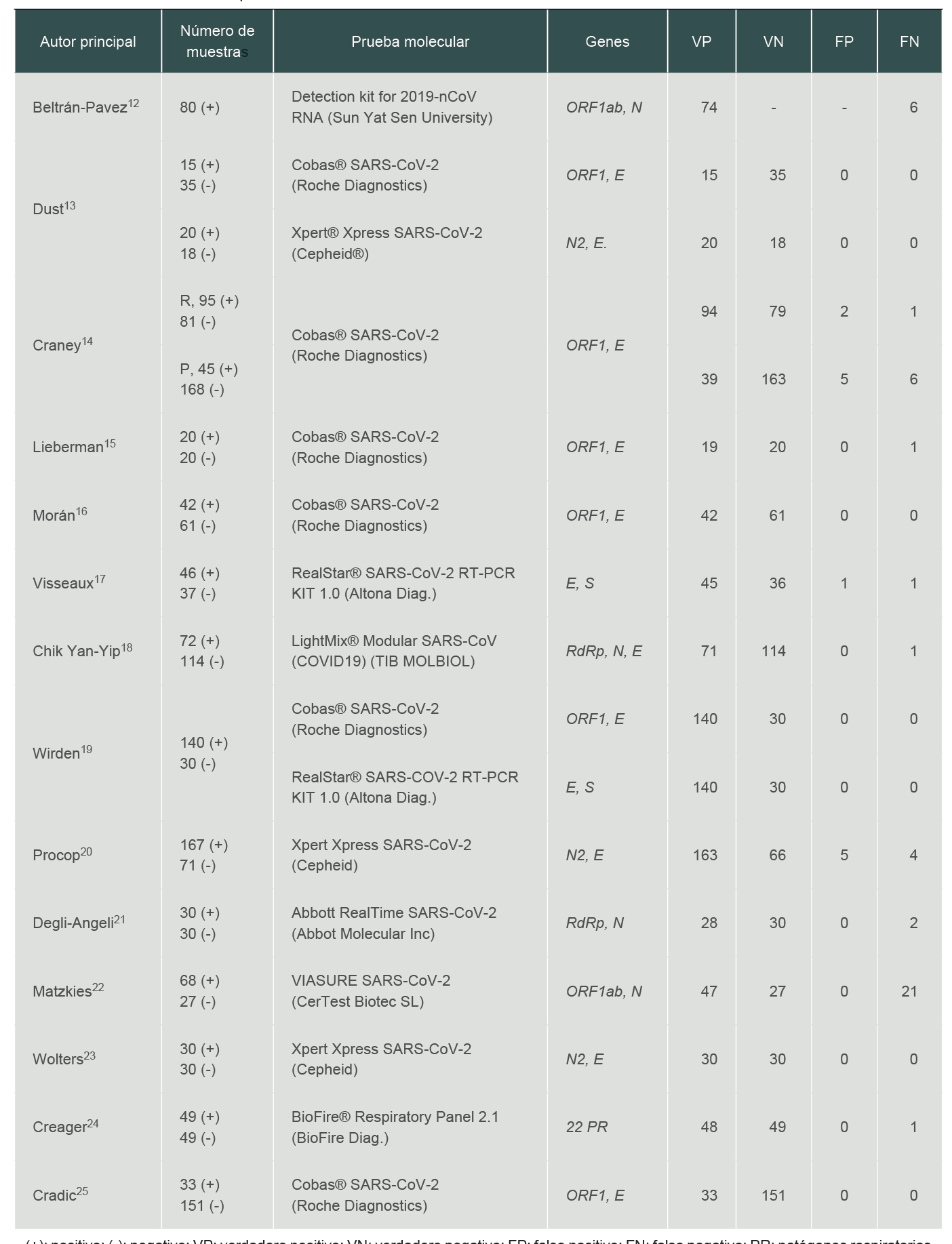
Cuadro I
Características de las pruebas analizadas
(+): positivo; (-): negativo; VP: verdadero positivo; VN: verdadero negativo; FP: falso positivo; FN: falso negativo; PR: patógenos respiratorios. 12,13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25
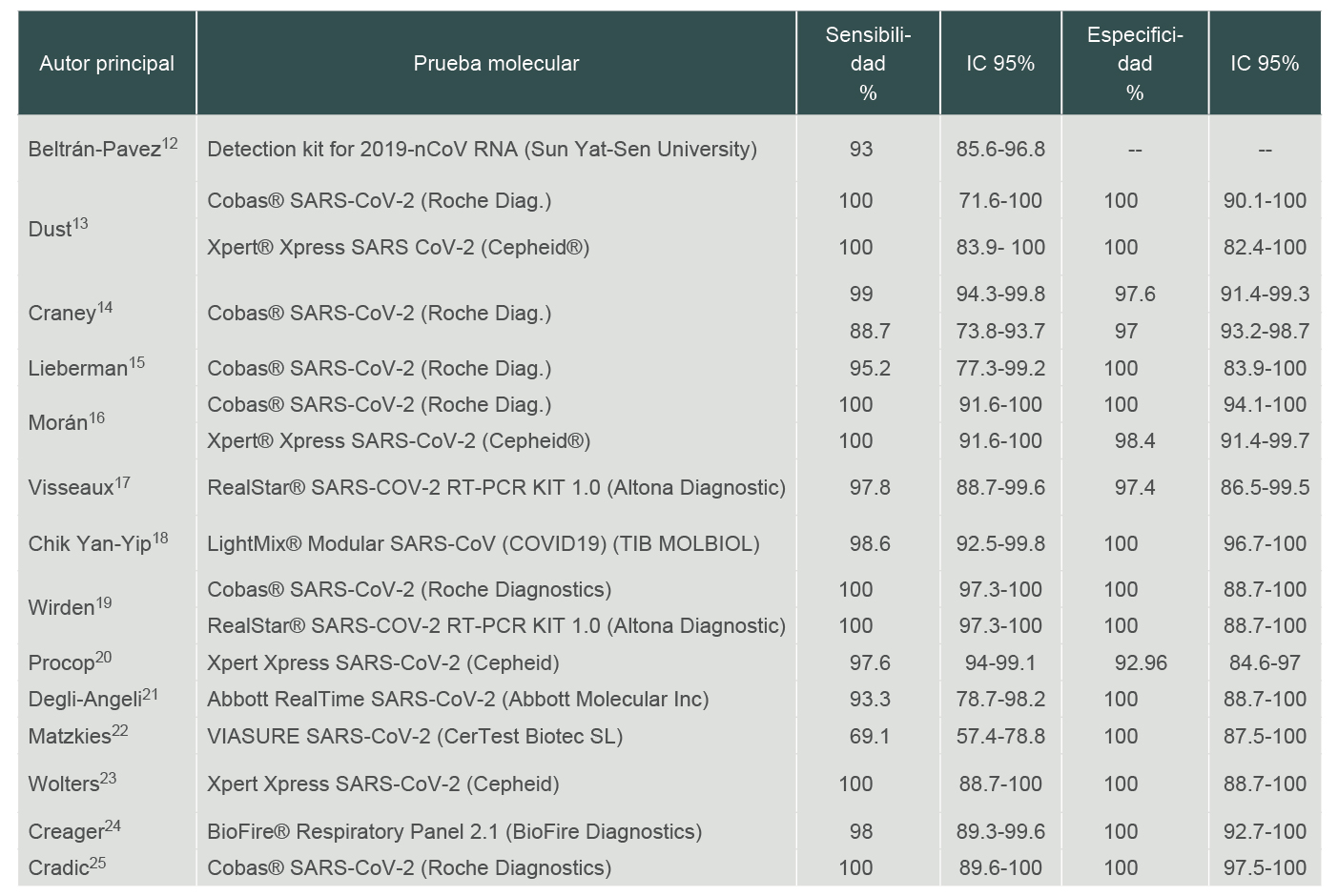
Cuadro II
Resultados de sensibilidad y especificidad de las pruebas moleculares
IC: intervalo de confianza, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25
Los resultados falsos negativos o falsos positivos encontrados en cada ensayo pueden atribuirse a errores durante la metodología, los cuales ocasionan pérdida del material genético del virus o contaminación de las muestras analizadas, con lo que se afecta así la sensibilidad y la especificidad de las pruebas.
Discusión
Desde el inicio de la infección por SARS-CoV-2, a finales de 2019, se han realizado innumerables esfuerzos por desarrollar métodos de diagnóstico de la enfermedad COVID-19, y el método de referencia ha sido la detección de partículas virales mediante RT-qPCR. Las pruebas confirmatorias deben tener validez, fiabilidad y seguridad.
En la práctica clínica, se espera que la sensibilidad y especificidad de las pruebas sean del 100%. Esto no siempre es constante debido a que se encuentran afectadas por las condiciones de realización, así como por el estado de la infección en la que se encuentre la persona a la que se le realiza la prueba.
La toma de muestra es de suma importancia en el método, ya que además de que debe realizarse de manera que se pueda asegurar la recolección de células infectadas por SARS-CoV-2, debe respetarse el “periodo de ventana”, en el que es posible que se obtengan resultados falsos negativos. Se ha demostrado que en el día 3, después de la aparición de los síntomas, la tasa mediana de falsos negativos disminuye al 20% y es el valor más bajo durante los 21 días de la infección.26
Existen variantes genéticas del SARS-CoV-2 con diversas eficiencias de replicación y manifestaciones clínico-patológicas durante el curso de la pandemia, lo cual podría causar variación en la sensibilidad y especificidad de los ensayos RT-qPCR disponibles, debido a que pueden surgir sustituciones de nucleótidos en las regiones de unión del cebador o la sonda y alterar la detección de SARS-CoV-2 en los ensayos.26
En general, las pruebas diagnósticas evaluadas en este metaanálisis muestran buenos resulados de sensibilidad y especificidad. Todos los kits de prueba permitieron identificar la presencia o ausencia de SARS-CoV-2; sin embargo, ninguno de ellos es 100% sensible o específico. El valor de sensibilidad más bajo fue obtenido con la prueba VIASURE SARS-CoV-2 de CerTest Biotec SL. El número elevado de resultados falsos negativos puede atribuírsele, además de a los errores durante el proceso (relacionados con la toma de muestra), a la extracción de ácidos nucleicos, a la eliminación de inhibidores, o a problemas de sensibilidad en la diana del gen ., el cual podría ser menos adecuado para la detección del virus. El kit proporciona un control interno de inhibición de la PCR, pero no cuenta con controles positivos con el gen diana del SARS-CoV-2, lo que impide asegurar la detección de este.22
Respecto a la especificidad, todos los kits obtuvieron valores superiores al 90%, los cuales pueden verse afectados debido a una manipulación incorrecta de muestras, reactivos o controles, así como a una amplificación masiva de ácidos nucleicos (que aunque aumenta la sensibilidad) vuelve los ensayos muy vulnerables a niveles mínimos de contaminación, lo que puede ocasionar resultados falsos positivos.27
Conclusiones
Los kits de prueba de los fabricantes Abbott, BioFire Diagnostics, Roche Diagnostics, Sun Yat-Sen University, TIB MOLBIOL, Altona diagnostics y Cepheid obtuvieron resultados de sensibilidad y especificidad superiores al 90% en los estudios incluidos en el metaanálisis, mientras que la prueba del fabricante CerTest Biotec obtuvo un valor de sensibilidad de menos del 80%
Las pruebas moleculares incluidas en el metaanálisis permiten el diagnóstico de COVID-19, pero es importante que la toma y el procesamiento de la muestra se realicen correctamente.
Referencias
1. Aguilar-Ramírez P, Enríquez-Valencia Y, Quiroz-Carrillo C, Valencia-Ayala E, de León-Delgado J, Pareja-Cruz A. Pruebas diagnósticas para la COVID-19: La importancia del antes y el después. Horiz Med. 2020;20(2): e1231. doi: 10.24265/horizmed.2020.v20n2.14
2. Organización Mundial de la Salud. COVID-19: Cronología de la actuación de la OMS. OMS: 27 de abril de 2020. Disponible en: https://www.who.int/es/news-room/detail/27-04-2020-who-timeline---covid-19 [Consultado el 7 de septiembre de 2020].
3. Gobierno de México. COVID-19 México: Información general. Disponible en: https://coronavirus.gob.mx/datos/ [Consultado el 7 de septiembre de 2020].
4. Quiroz-Carrillo C, Aguilar-Ramírez P, Pareja-Cruz A, Enríquez-Valencia Y, Valencia-Ayala E, De León-Delgado J. Un nuevo coronavirus, una nueva enfermedad: COVID-19. Horiz Med (Lima) 2020;20(2):e1208. doi: 10.24265/horizmed.2020.v20n2.11
5. Pérez-Abreu M, Gómez-Tejeda J, Dieguez-Guach R. Características clínico- epidemiológicas de la COVID-19. Rev Haban Cienc Med. 2020;19(2):e3254. Disponible en: http://www.revhabanera.sld.cu/index.php/rhab/article/view/3254
6. Secretaría de Salud. Instituto de Diagnóstico y Referencia Epidemiológicos Dr. Manuel Martínez Báez. Disponible en: https://www.gob.mx/salud/acciones-y-programas/instituto-de-diagnostico-y-referencia-epidemiologicos-indre [Consultado el 20 de octubre de 2020].
7. Bustin SA, Benes V, Garson JA, Hellemans J, Huggett J, Kubista M, et al. The MIQE guidelines: minimum information for publication of quantitative real-time PCR experiments. Clin Chem. 2009;55(4):611-22. doi: 10.1373/clinchem.2008.112797
8. Secretaría de Salud. Lineamiento estandarizado para la vigilancia epidemiológica y por laboratorio de la enfermedad respiratoria viral. Mayo de 2020. Disponible en: https://coronavirus.gob.mx/wp-content/uploads/2020/06/Lineamiento_VE_Lab_enfermedad_respiratoria_viral-_20052020.pdf [Consultado el 11 de abril de 2021].
9. Organización Panamericana de la Salud. Directrices de laboratorio para la detección y el diagnóstico de la infección por el virus responsable de la COVID-19. 8 de julio de 2020. Disponible en: https://iris.paho.org/bitstream/handle/10665.2/52471/OPSIMSPHECOVID-19200038_spa.pdf?sequence=1&isAllowed=y [Consultado el 11 de abril de 2021].
10. Mohammed-Khairat S, EL Guindy N, Mohammad-Salah E, Salah-Soliman N. Evaluation of Two Rapid Antigen Tests for Detection of SARS-CoV-2 Virus. Int J Microbiol Biotechnol. 2020;5(3):131-4. doi: 10.11648/j.ijmb.20200503.18
11. Gomez-Marin J, Castellanos J, Rodríguez-Morales A, Cardona-Ospina J, Forero-Duarte J, Mattar J et al. Consenso de grupo Ad-hoc sobre recomendaciones para la evaluación y controles de calidad para el diagnóstico molecular y serológico de la infección humana por SARS-CoV-2. Infectio. 2020;24(3):5-10. doi: 10.22354/in.v24i3.868
12. Beltrán-Pavez C, Alonso-Palomares LA, Valiente-Echeverría F, Gaggero A, Soto-Rifo R, Barriga GP. Accuracy of a RT-qPCR SARS-CoV-2 detection assay without prior RNA extraction. J Virol Methods. 2021; 287:113969. doi: 10.1016/j.jviromet.2020.113969
13. Dust K, Hedley A, Nichol K, Stein D, Adam H, Karlowsky J, et al. Comparison of commercial assays and laboratory developed tests for detection of SARS-CoV-2. J Virol Methods. 2020;285:113970. doi: 10.1016/j.jviromet.2020.113970
14. Craney AR, Velu PD, Satlin MJ, Fauntleroy KA, Callan K, Robertson A, et al. Comparison Of Two High-Throughput Reverse Transcription-PCR Systems For The Detection Of Severe Acute Respiratory Syndrome Coronavirus 2. J Clin Microbiol. 2020 Jul 23;58(8):e00890-20. doi: 10.1128/JCM.00890-20
15. Lieberman JA, Pepper G, Naccache SN, Huang ML, Jerome KR, Greninger AL. Comparison of Commercially Available and Laboratory-Developed Assays for In Vitro Detection of SARS-CoV-2 in Clinical Laboratories. J Clin Microbiol. 2020;58(8):e00821-20. doi: 10.1128/JCM.00821-20
16. Moran A, Beavis KG, Matushek SM, Ciaglia C, Francois N, Tesic V, et al. Detection of SARS-CoV-2 by Use of the Cepheid Xpert Xpress SARS-CoV-2 and Roche cobas SARS-CoV-2 Assays. J Clin Microbiol. 2020;58(8):e00772-20. doi: 10.1128/JCM.00772-20
17. Visseaux B, Le Hingrat Q, Collin G, Ferré V, Storto A, Ichou H, et al. Evaluation of the RealStar® SARS-CoV-2 RT-qPCR kit RUO performances and limit of detection. J Clin Virol. 2020; 129:104520. doi: 10.1016/j.jcv.2020.104520
18. Yip CCY, Sridhar S, Cheng AKW, Leung KH, Cho GK, Chen JH, et al. Evaluation of the commercially available LightMix® Modular E-gene kit using clinical and proficiency testing specimens for SARS-CoV-2 detection. J Clin Virol. 2020;129:104476. doi: 10.1016/j.jcv.2020.104476
19. Wirden M, Feghoul L, Bertine M, Nere ML, Le Hingrat Q, Abdi B, et al. Multicenter comparison of the Cobas 6800 system with the RealStar RT-qPCR kit for the detection of SARS-CoV-2. J Clin Virol. 2020;130:104573. doi: 10.1016/j.jcv.2020.104573
20. Procop GW, Brock JE, Reineks EZ, Shrestha NK, Demkowicz R, Cook E, et al. A Comparison of Five SARS-CoV-2 Molecular Assays With Clinical Correlations. Am J Clin Pathol. 2020;155(1):69-78. doi: 10.1093/ajcp/aqaa181
21. Degli-Angeli E, Dragavon J, Huang ML, Lucic D, Cloherty G, Jerome KR, et al. Validation and verification of the Abbott RealTi.e SARS-CoV 2 assay analytical and clinical performance J Clin Virol. 2020;129:104474. doi: 10.1016/j.jcv.2020.104474
22. Matzkies LM, Leitner E, Stelzl E, Assig K, Bozic M, Siebenhofer D, et al. Lack of sensitivity of an IVD/CE-labelled kit targeting the S gene for detection of SARS-CoV-2. Clin Microbiol Infect. 2020;26(10):1417.e1-1417.e4. doi: 10.1016/j.cmi.2020.06.036
23. Loeffelholz MJ, Alland D, Butler-Wu SM, Pandey U, Perno CF, Nava A, et al. Multi-center evaluation of cepheid xpert® xpress SARS-CoV-2 point-of-care test during the SARS-CoV-2 pandemic. J Clin Microbiol. 2020;58(8):e00926-20. doi: 10.1128/JCM.00926-20
24. Creager HM, Cabrera B, Schnaubelt A, Cox JL, Cushman-Vokoun AM, Shakir SM, et al. Clinical evaluation of the BioFire® Respiratory Panel 2.1 and detection of SARS-CoV-2. J Clin Virol. 2020;129:104538. doi: 10.1016/j.jcv.2020.104538
25. Cradic K, Lockhart M, Ozbolt P, Fatica L, Landon L, Lieber M, et al. Clinical Evaluation and Utilization of Multiple Molecular In Vitro Diagnostic Assays for the Detection of SARS-CoV-2. Am J Clin Pathol. 2020;154(2):201-7. doi: 10.1093/ajcp/aqaa097
26. Kucirka LM, Lauer SA, Laeyendecker O, Boon D, Lessler J. Variation in False-Negative Rate of Reverse Transcriptase Polymerase Chain Reaction-Based SARS-CoV-2 Tests by Time Since Exposure. Ann Intern Med. 2020;173(4):262-7. doi: 10.7326/M20-1495
27. Vogels CBF, Brito AF, Wyllie AL, Fauver JR, Ott IM, Kalinich CC, et al. Analytical sensitivity and efficiency comparisons of SARS-CoV-2 RT-qPCR primer-probe sets. Nat Microbiol. 2020 Oct;5(10):1299-305. doi: 10.1038/s41564-020-0761-6
Información adicional
Declaración de conflicto de interés: los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno relacionado con este artículo.
Cómo citar este artículo: Ochoa-Díaz D, Mendoza-Olazarán S, Zarate X, Casillas-Vega N. Metaanálisis de pruebas diagnósticas para la detección de COVID-19. Rev Med Inst Mex Seguro Soc. 2021;59(3):182-8.
PubMed: https://www.ncbi.nlm.nih.gov/pubmed/34357745
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/4016 (html)
