Aportación original

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 16 Abril 2021
Aprobación: 29 Julio 2021
Resumen:
Introducción: la enfermedad del hígado graso no alcohólico (EHGNA) tiene graves implicaciones para la salud y, asociada a la epidemia de obesidad, es una tendencia creciente.
Objetivo: detectar la presencia de hígado graso en niños con sobrepeso y obesidad, así como evaluar los factores asociados con una mayor posibilidad de presentar un resultado positivo en la detección.
Metódos: se realizó un estudio de tipo transversal en una unidad médica del segundo nivel de atención médica en el que fueron reclutados 102 niños. Los niveles séricos de alanina aminotransferasa (ALT) fueron cuantificados y se realizaron ecografías hepáticas. Modelos de regresión logística múltiple fueron utilizados para evaluar los factores asociados con la presencia de EHGNA (infiltración grasa en la ecografía y ALT > 52U/L para niños y > 44 U/L para niñas).
Resultados: la prevalencia de EHGNA fue del 10,8%. En el análisis multivariante, una relación entre cintura y cadera ≥ 1 se asoció con una mayor posibilidad de EHNGA (razón de momios (RM) = 4.96, IC del 95%: 1.17 - 20.90).
Conclusiones: nuestros hallazgos indican que uno de cada diez niños sobrepeso y obesidad tiene datos sugestivos de EHGNA y está en riesgo de presentar sus consecuencias para la salud.
Palabras clave: Sobrepeso, Obesidad, Niño, Enfermedad del Hígado Graso no Alcohólico.
Abstract:
Background: Non-alcoholic fatty liver disease (NAFLD) has serious health implications and upward trends of the disease, accompanied by the obesity epidemic worldwide.
Objective: To screen for fatty liver in overweight and obese children and evaluate the factors associated with an increased likelihood of presenting a positive-screen result.
Methods: In a cross-sectional study, 102 children were recruited at a secondary care medical unit. Serum alanine aminotransferase (ALT) levels were quantified and hepatic ultrasounds were performed; multiple logistic regression models were used to evaluate factors associated with the increased odds of presenting with NAFLD (fatty infiltration on ultrasound and ALT > 52 U/L for boys and > 44 U/L for girls).
Results: The overall prevalence of NAFLD was 10.8%. In multivariate analysis, a waist-to-hip ratio ≥ 1 was associated with increased odds of screening positive for NAFLD (odds ratio (OR) = 4.96, 95% CI 1.17-20.90).
Conclusions: Our findings indicate that one out of ten children with overweight or obesity has data suggestive of NAFLD and is at risk of presenting its consequences on health.
Keywords: Overweight, Obesity, Child, Non-alcoholic Fatty Liver Disease.
Introducción
La enfermedad del hígado graso no alcohólico (EHGNA) es la causa más frecuente de enfermedad hepática crónica en niños y adolescentes en los países desarrollados.1 Los principales factores de riesgo para el desarrollo del hígado graso, así como su incidencia, han aumentado de forma paralela en individuos de todas las edades.2 De acuerdo con proyecciones recientes, la EHGNA será la causa más común de trasplante de hígado en los países industrializados en los próximos diez años.3
El espectro de la enfermedad es amplio y va desde la esteatosis a la esteatohepatitis (caracterizada por inflamación y daño hepatocelular) y, finalmente, a la fibrosis y la cirrosis.4 La EHGNA se asocia de forma independiente con un mayor riesgo de diabetes mellitus tipo 2, neoplasias colorrectales, enfermedad cardiovascular, enfermedad renal crónica y reducción de la densidad mineral ósea en niños con obesidad.5,6,7 Se han documentado frecuencias heterogéneas de hígado graso en diferentes poblaciones y la prevalencia combinada oscila entre el 7.6 y el 34.2%, en población general y en poblaciones clínicamente obesas, respectivamente.8
México se encuentra actualmente en etapas avanzadas de una transición epidemiológica y las enfermedades no transmisibles (relacionadas con el exceso de peso corporal) son las principales causas de discapacidad y muerte prematura.9 Además, en las últimas décadas se han documentado tendencias ascendentes en la prevalencia de sobrepeso y obesidad en niños, especialmente en los que pertenecen a un estrato socioeconómico más bajo.10
De acuerdo con la Encuesta Nacional de Salud y Nutrición (ENSANUT) 2018, más de un tercio de los niños y adolescentes mexicanos presenta sobrepeso/obesidad (5 a 11 años, 35.6%; 12 a 19 años, 35.8%).11 Esas tasas son las más altas documentadas mundialmente en niños en edad escolar y en adolescentes.12
Ubicado en la región occidental del país, el estado de Colima tiene una de las prevalencias combinadas más altas de sobrepeso/obesidad en niños.13 El objetivo del presente estudio fue detectar la EHGNA en niños con sobrepeso y obesidad atendidos en una clínica de obesidad ambulatoria perteneciente a una unidad médica de atención secundaria en México. También evaluamos los factores asociados a una mayor posibilidad de presentar dicha enfermedad hepática.
Material y métodos
Material y métodos
Diseño del estudio
Se realizó un estudio transversal entre julio de 2018 a junio de 2019 en un centro de atención secundaria ubicado en Colima, un estado en el oeste de México. La unidad médica donde se realizó el estudio pertenece al Instituto Mexicano del Seguro Social (IMSS). Los participantes fueron reclutados en el servicio de Endocrinología Pediátrica, que atiende a los niños con sobrepeso y obesidad derivados para manejo médico especializado.
Población de estudio
Los niños de 1 a 15 años de edad con sobrepeso (percentil 85 a < 94% de índice de masa corporal [IMC] para la edad y sexo) u obesidad (percentil 95% o mayor), vistos como pacientes ambulatorios en el servicio de Endocrinología Pediátrica durante el período de estudio, fueron potencialmente elegibles para participar en el estudio. Las tablas de los Centros para el Control y la Prevención de Enfermedades fueron empleadas para realizar la clasificación antes descrita. Fueron excluidos los pacientes con enfermedades hepáticas genéticas o no genéticas concomitantes, distintas a la EHGNA. Los criterios de exclusión también incluyeron la detección positiva del antígeno de superficie del virus de la hepatitis B, anticuerpos del virus de la hepatitis C o anticuerpos antimitocondriales o antinucleares.
No fueron elegibles los infantes con antecedentes personales de hemocromatosis, deficiencia de alfa-1-antitripsina o enfermedad de Wilson, así como aquellos con antecedentes de consumo de alcohol (ya que la edad promedio de inicio del consumo de alcohol en la población mexicana es de 15 años).14 Se excluyeron dos niños (debido a la presencia de antígeno de superficie del virus de la hepatitis B positivo, n = 1; deficiencia de alfa-1-antitripsina, n = 1). Se realizó una selección no aleatoria y todos los niños que cumplieron los criterios de elegibilidad fueron incluidos.
Recopilación de datos
espués de obtener declaraciones escritas de consentimiento informado de todos los padres o tut
Después de obtener declaraciones escritas de consentimiento informado de todos los padres o tutores legales, se entrevistó a los menores (o adultos acompañantes, según correspondiera). Se utilizó un cuestionario con preguntas cerradas para evaluar las variables de interés: edad de la madre al momento del parto (años), si el niño fue amamantado (no/sí) y por cuánto tiempo (meses), así como los antecedentes de diabetes mellitus tipo 2 (DM2, no/sí) o hipertensión arterial (HTA, no/sí) en los padres o tutores legales. Las entrevistas fueron realizadas por un médico de familia cegado al objetivo de esta investigación.
Además, se revisaron los expedientes clínicos y se obtuvieron datos sobre los registros perinatales (peso al nacer, g; talla al nacer, cm), las medidas antropométricas basales (talla, m; peso, kg; circunferencia de cintura, cm; circunferencia de cadera, cm), signos vitales (presión arterial sistólica y diastólica, mmHg) y marcadores de laboratorio (nivel de glucosa en sangre en ayunas, mg/dL; hemoglobina glucosilada, %; colesterol total, mg/dL; triglicéridos, mg/dL; alanina aminotransferasa (ALT), U/L, y gamma-glutamil transferasa (GGT), U/L). Los criterios de la Asociación Americana de Diabetes (American Diabetes Association) fueron utilizados para dicotomizar los niveles de hemoglobina glucosilada (< 6.5% y ≥ 6.5%).15 Por otra parte, los criterios de la Federación Internacional de Diabetes se utilizaron para estimar la prevalencia del síndrome metabólico (MetS) en los niños analizados de 10 años o más.16
Las evaluaciones ultrasonográficas fueron realizadas por un único observador y empleando un equipo SonixTouch Q+ (Ultramedixi; Ciudad de México, México).
Evento de interés
El hígado graso (no/sí) fue el principal evento de interés, y los niveles séricos de alanina aminotransferasa (ALT) se utilizaron para detectar el hígado graso, según lo recomendado por la Sociedad Norteamericana de Gastroenterología, Hepatología y Nutrición Pediátrica (NASPGHAN).17 El nivel de ALT sérico en los niños se consideró alto si era dos veces mayor que los puntos de corte específicos del sexo de > 52 U/L para los niños y > 44 U/L para las niñas.17 Los niños con aumento de ALT e infiltración grasa en la ecografía se clasificaron como positivos para EHGNA, de acuerdo con las recomendaciones publicadas recientemente.18
Métodos de laboratorio
Los participantes proporcionaron una muestra de sangre venosa en ayunas, a partir de la cual se cuantificaron los biomarcadores de interés. Se utilizó el analizador de química clínica ARCHITECT c8000 (Abbott Laboratorios; Chicago, EUA) para evaluar los niveles séricos de ALT y otros marcadores bioquímicos. La cuantificación de la hemoglobina glucosilada se realizó empleando UniCel Synchronn Systems DxC 800 (Beckman Coulter Inc.; Maryfort, O'callaghans Mills, Co. Clare, Ireland), un sistema certificado por el NGSP (National Glycohemoglobin Standardization Program) y siguiendo las instrucciones del fabricante.
Análisis estadístico
Se calcularon estadísticas sumarias. La significación estadística se evaluó mediante las pruebas de Chi cuadrada o t de Student, según fuera apropiado, y el nivel de significación se fijó en 5%. Se emplearon razones de momios (RM) de prevalencia e intervalos de confianza del 95% (IC95%), calculados a través modelos de regresión logística no condicional, para evaluar la asociación de la exposición analizada con la posibilidad de presentar enfermedad hepática. El análisis estadístico se realizó empleando el paquete Stata 15 (StataCorp. 2017. College Station, TX: StataCorp LLC).
Consideraciones éticas
El presente estudio fue revisado y aprobado por el Comité Local de Investigación en Salud 601 (aprobación R-2018-601-005) del IMSS.
Resultados
Se analizaron los datos de 102 niños y las características seleccionadas de la muestra del estudio se presentan en el cuadro I. Más de la mitad de los participantes (52.0%) eran mujeres y la edad media (± desviación estándar) de los individuos inscritos fue de 10.8 ± 3.1 años. Solo el 4.5% (n = 5) de los sujetos analizados tenían cinco años o menos.
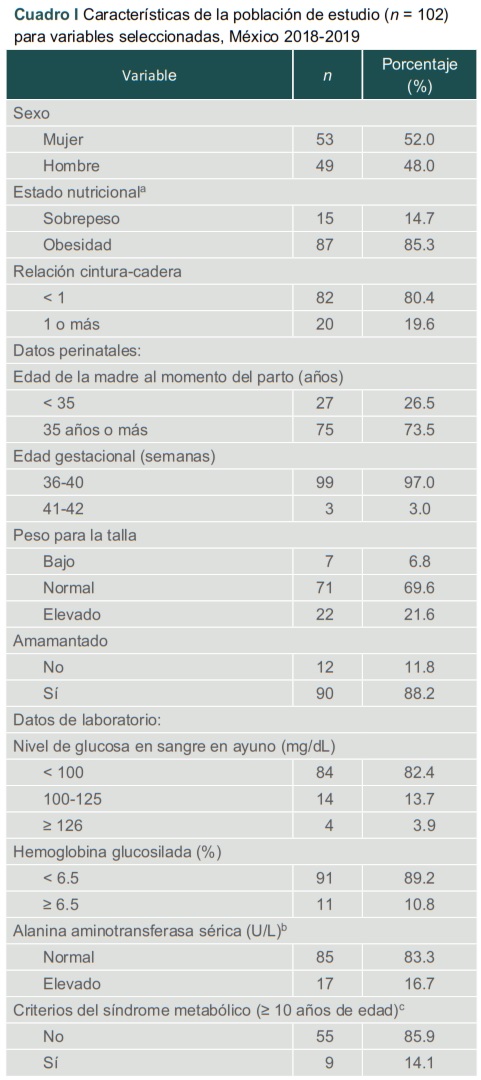
Cuadro I
Cuadro I
Características de la población de estudio
aSe utilizaron tablas de peso para la talla: sobrepeso (del percentil 85 a < percentil 95); obesidad (percentil 95 o superior)
bLos niños con niveles elevados de alanina aminotransferasa sérica fueron aquellos con 2 veces el punto de corte específico del sexo (> 52 U/L para niños y > 44 U/L para niñas)
cSe utilizaron los criterios de la Federación Internacional de Diabetes e incluyeron obesidad central y (≥ 2): triglicéridos elevados (≥ 150 mg/dL), colesterol HDL reducido (niños, <40 mg/dL; niñas, <50 mg/dL), presión arterial elevada (sistólica > 130 mmHg o diastólica > 85 mmHg o tratamiento de hipertensión previamente diagnosticada) o alteración de la glucemia en ayunas (≥ 100 mg/dL). Se presentan datos de niños de 10 años o más de edad
Un nivel elevado de ALT se documentó en 17 niños, de los cuales 11 de ellos también presentaron infiltración grasa en la ecografía. Por lo anterior, la prevalencia de EHGNA en la muestra del estudio fue del 10.8%. Entre los niños de 10 años o más (n = 64), el 14.1% cumplió los criterios de MetS.
En comparación con los pacientes con un resultado negativo de la prueba, los niños con un cribado positivo presentaron más posibilidades de tener una relación cintura-cadera ≥ 1 (54.5% frente a 14.8%) y niveles mayores de GGT en suero (100% frente a 28.2%) (cuadro II).
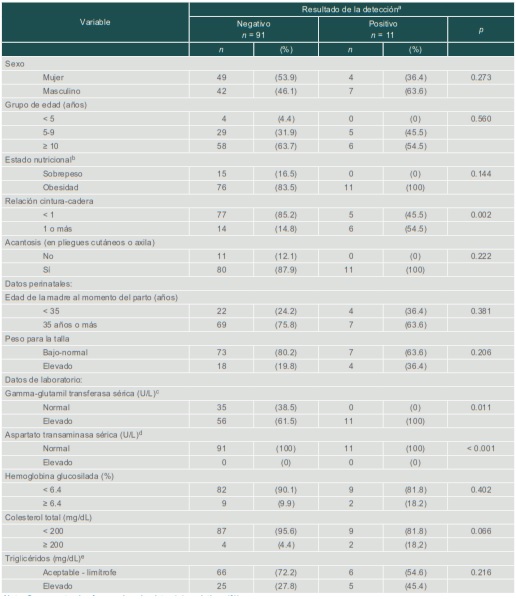
Cuadro II
Cuadro II
Características de los participantes en función del resultado de la prueba de detección, México 2018-2019
aLos niños que resultaron positivos para la enfermedad de hígado graso no alcohólico fueron aquellos con 2 veces el punto de corte específico del sexo de la alanina aminotransferasa sérica (> 52 U/L para niños y > 44 U/L para niñas)
bSe utilizó el índice de masa corporal para los gráficos de edad con el género: exceso de peso (desde el 85 percentil a < el 95 percentil); obesidad (el 95 percentil o superior)
cEn niños < 10 años: Alto > 32 U/L. En los niños de 10-15 años de edad: Alto > 24 U/L
dEn niños ≤ 2 años: Alto > 80 U/L. En niños > 2 años: Mujeres, alto > 35 U/L; Hombres, alto > 40 U/L
eEn niños < 10 años: Aceptable, < 75 mg/dL; Límite, 75-99 mg/dL; Alto, ≥ 100 mg/dL. En niños de 10 a 19 años de edad: Aceptable, < 90 mg/dL; Límite, 90-129 mg/dL; Alto ≥ 130 mg/dL
Nota: Se presentan las frecuencias absolutas (n) y relativas (%).En el análisis multivariado, una relación cintura-cadera ≥ 1 se asoció con un incremento de las probabilidades de que el tamizaje sea positivo para EHGNA (RM = 4.96; IC95%: 1.17-20.90) (cuadro III). No se observaron otras asociaciones significativas en la muestra del estudio.
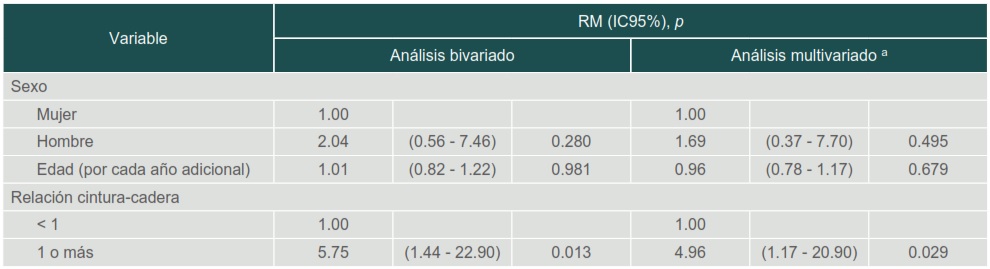
Cuadro III
Cuadro III
Factores asociados con la posibilidad de un resultado positivo en la detección de enfermedad del hígado grado no alcohólico, México 2018-2019
a Estimaciones ajustadas por las variables enumeradas en el cuadro
Notas: 1) Los niños que resultaron positivos para la enfermedad del hígado graso no alcohólico fueron aquellos con 2 veces el punto de corte específico del sexo de la alanina aminotransferasa sérica (> 52 U/L para niños y > 44 U/L para niñas) 2) Las razones de momios (RM) y los intervalos de confianza (IC) del 95% se estimaron mediante modelos de regresión logística incondicionalDiscusión
Los resultados del presente estudio sugieren que el 11% de los niños analizados presenta algún grado de hígado graso. Nuestros resultados deben interpretarse con cautela debido a las limitaciones propias del tamizaje de EHGNA por medio de los niveles de ALT18 y de los hallazgos ecográficos. Nuestros hallazgos destacan la importancia de promover tanto el peso saludable como el examen de detección de EHGNA en niños con sobrepeso u obesidad. Debido a que la carga económica y de salud relacionada con la obesidad en México es alta, dichas estrategias se necesitan con urgencia.
Identificamos que algunos niños pueden beneficiarse de la resonancia magnética y de otras alternativas no invasivas efectivas para el diagnóstico definitivo de EHGNA. Sin embargo, estas técnicas pueden tener un costo prohibitivo en ciertos entornos de atención médica,19 por lo que el cribado mediante ALT y ultrasonido parecen ser una opción plausible.
Nuestra estimación de EHGNA en niños (11%) es muy similar a la prevalencia global esperada, la cual oscila entre el 5 al 10%.20 En un estudio en niños mexicanos que utilizó ALT > 40 U/L como punto de corte, y en comparación con nuestros resultados, se informaron frecuencias más bajas de EHGNA (6.6% frente a 16.7%, respectivamente).21 Nuestra hipótesis es que las variaciones de cohortes relacionadas pueden estar involucradas en tales discrepancias, debido a que los datos del estudio antes mencionado fueron recogidos hace 13-15 años, mientras que los estudios más actuales han informado de las tendencias al alza en la obesidad infantil.10
Con base en lo observado en nuestro estudio, los niños con una relación entre cintura y cadera igual o mayor a 1 se encontraron con una posibilidad incrementada de EHGNA (RM = 4.96, IC95%: 1.17 - 20.90). Esta asociación ha sido descrita previamente.22
Actualmente no existen agentes farmacéuticos aprobados para tratar el hígado graso, pero se ha informado sobre los beneficios de la pérdida de peso: la pérdida de peso > 4% mejora el contenido de grasa hepática, la pérdida de peso ≥ 7% mejora la hepatitis y la pérdida de peso ≥ 10% disminuye la fibrosis hepática.23
La obesidad infantil en México es un problema de salud importante, y comúnmente los esfuerzos preventivos se enfocan en el aumento de la actividad física y la promoción de hábitos alimentarios saludables.24 En general, la eficacia de esas intervenciones se reduce porque ignoran el papel relevante del entorno obesogénico en los estilos de vida de los niños.25
Se han desarrollado varios métodos para el diagnóstico no invasivo de EHGNA, que incluyen la fracción de grasa de densidad de protones basada en imágenes por resonancia magnética (MRI-PDFF). En comparación con el parámetro de atenuación controlada basado en elastografía transitoria fundamentada en ultrasonido (TE-CAP) en casos de HGNA comprobados por biopsia, la MRI-PDFF ha sido más precisa para identificar cualquier grado de esteatosis (área bajo la curva de las características operativas del receptor [AUROC] 0.99, IC95%: 0.98-1.00 frente a 0.85, IC95%: 0.75-0.96).26
El mecanismo patogénico de la EHGNA no se ha dilucidado, pero parece ser multifactorial. La hipótesis de impactos múltiples es ampliamente aceptada e incluye exposiciones múltiples (es decir, sensibilidad a la insulina, factores nutricionales y microbiota intestinal) que interactúan con factores genéticos y epigenéticos.27
Las posibles limitaciones de nuestro estudio incluyen un tamaño de muestra pequeño y el hecho de que se empleó un método de detección de laboratorio y sus variaciones documentadas.28 La biopsia hepática es el estándar de oro en el diagnóstico de EHGNA y es positiva cuando hay esteatosis macrovesicular en al menos el 5% de los hepatocitos. Sin embargo, debido a su naturaleza invasiva, posibles efectos adversos y alto costo, no se recomienda como método de detección. Hoy en día, la cuantificación de ALT sérica y la ecografía (ecografía) del hígado son los métodos más comúnmente empleados en el cribado del hígado graso.8 Sin embargo, se espera que la EHGNA sea infradiagnosticada mediante el uso de cualquiera de esos procedimientos.
En nuestra muestra de estudio, no se documentaron anomalías ecográficas hepáticas en más de un tercio (35.3%) de los niños con niveles de ALT sugestivos de EHGNA. En general, y además de las variaciones dependientes del operador, la ecografía tiene una precisión equitativa en la detección de EHGNA moderada o grave, aunque es menos precisa cuando se evalúa una enfermedad leve.29 Los lactantes analizados que carecían de anomalías en la ecografía hepática, pero mantenían niveles elevados de ALT, y en comparación con aquellos sin hallazgos discrepantes, tenían más probabilidades de ser niñas (p = 0.028).
No se observaron diferencias significativas en cuanto a edad o IMC. Sin embargo, la NASPGHAN no es recomendada en los Estados Unidos como herramienta de detección.17 Dado que los bebés con niveles de ALT de 80 U/L o más corren un mayor riesgo de EHGNA confirmado,17 los sujetos identificados fueron remitidos al servicio de Gastroenterología Pediátrica para un estudio adicional.
En comparación con una fracción de grasa hepática superior al 9% en la resonancia magnética (MRI), la sensibilidad y la especificidad estimadas de los niveles de ALT sérica > 30 U/L para predecir la presencia de EHGNA es del 64 y 81%, respectivamente. Al utilizar niveles de ALT > 40 U/L, la sensibilidad es del 41% y la especificidad es del 89%.30 La sensibilidad baja de la ALT en el cribado podría conducir al subdiagnóstico de la enfermedad de interés.8
La base sanitaria de nuestro estudio es otra de sus limitaciones potenciales, por lo que los niños y adolescentes inscritos pueden no representar a toda la población de origen. La relación de la obesidad/sobrepeso en la muestra fue superior a la media nacional en niños de 5 a 11 años de edad (4.8 frente a 1.2), así como en adolescentes (5.4 frente a 1.6).13 Es factible que los niños remitidos a atención secundaria presenten características indeterminadas (por ejemplo, una masa corporal mayor que los que no son remitidos por unidades médicas de atención primaria), lo que podría conducir a una mayor prevalencia de hígado graso en ese grupo en particular.
Además, se analizó un número relativamente pequeño de individuos. Sin embargo, dada la alta carga relacionada con la obesidad en México y la elevada carga social y económica de la EHGNA, creemos que los resultados de nuestro estudio son muy relevantes desde una perspectiva de salud pública.
Conclusiones
El presente estudio sugiere que uno de cada diez niños con sobrepeso y obesidad analizados tiene un riesgo incrementado de presentar enfermedad hepática por lo que pueden beneficiarse de intervenciones tempranas enfocadas en la reducción de su peso corporal.
Referencias
1. Sarwar R, Pierce N, Koppe S. Obesity and nonalcoholic fatty liver disease: current perspectives. Diabetes Metab Syndr Obes. 2018;11:533-542. doi: 10.2147/DMSO.S146339
2. Divella R, Mazzocca A, Daniele A, Sabbà C, Paradiso A. Obesity, nonalcoholic fatty Liver disease and adipocytokines network in promotion of cancer. Int J Biol Sci. 2019;15(3):610-616. doi: 10.7150/ijbs.29599
3. Neuschwander-Tetri BA. Non-alcoholic fatty liver disease. BMC Med. 2017;15(1):45. doi: 10.1186/s12916-017-0806-8
4. Assunção SNF, Sorte NCB, Alves CD, Mendes PSA, Alves CRB, Silva LR. Nonalcoholic fatty liver disease (NAFLD) pathophysiology in obese children and adolescents: update. Nutr Hosp. 2017;34(3):727-730. doi: 10.20960/nh.723
5. Hecht L, Weiss R. Nonalcoholic fatty liver disease and type 2 diabetes in obese children. Curr Diab Rep. 2014;14(1):448. doi: 10.1007/s11892-013-0448-y
6. Armstrong MJ, Adams LA, Canbay A, Syn WK. Extrahepatic complications of nonalcoholic fatty liver disease. Hepatology. 2014;59(3):1174-97. doi: 10.1002/hep.26717
7. Sun Y, Dai W, Liang Y, Yang P, Yang Q, Liang M, et al. Relationship between nonalcoholic fatty liver disease and bone mineral density in adolescents with obesity: a meta-analysis. Diabetes Metab Syndr Obes. 2019;12:199-207. doi: 10.2147/DMSO.S192256
8. Anderson EL, Howe LD, Jones HE, Higgins JP, Lawlor DA, Fraser A. The prevalence of non-alcoholic fatty liver disease in children and adolescents: A systematic review and meta-analysis. PLoS One. 2015;10(10):e0140908. doi: 10.1371/journal.pone.0140908
9. Institute of Health Metrics and Evaluation. Data of Mexico. Seattle, WA: IHME; 2020. Disponible en: http://www.healthdata.org/mexico
10. Hernández-Cordero S, Cuevas-Nasu L, Morán-Ruán MC, Méndez-Gómez Humarán I, Ávila-Arcos MA, Rivera-Dommarco JA. Overweight and obesity in Mexican children and adolescents during the last 25 years. Nutr Diabetes. 2017;7(3):e247. doi: 10.1038/nutd.2017.29
11. Instituto Nacional de Estadística y Geografía - Instituto Nacional de Salud Pública - Secretaría de Salud. Encuesta Nacional de Salud y Nutrición 2018: Presentación de resultados. Cuernavaca, Morelos: INSP; 2019. Disponible en: https://ensanut.insp.mx/encuestas/ensanut2018/doctos/informes/ensanut_2018_presentacion_resultados.pdf
12. Rivera JÁ, de Cossío TG, Pedraza LS, Aburto TC, Sánchez TG, Martorell R. Childhood and adolescent overweight and obesity in Latin America: a systematic review. Lancet Diabetes Endocrinol. 2014;2(4):321-332. Disponible en: https://doi.org/10.1016/S2213-8587(13)70173-6
13. Instituto Nacional de Estadística y Geografía - Instituto Nacional de Salud Pública - Secretaría de Salud. Encuesta Nacional de Salud y Nutrición 2018-19: Resultados nacionales. Ciudad de México: INEGI: 2019. Disponible en: https://ensanut.insp.mx/encuestas/ensanut2018/doctos/informes/ensanut_2018_informe_final.pdf
14. Strunin L, Díaz-Martínez A, Díaz-Martínez LR, Heeren T, Chen C, Winter M, et al. Age of onset, current use of alcohol, tobacco or marijuana and current polysubstance use among male and female Mexican students. Alcohol and Alcoholism. 2017;52(5):564-571. doi: 10.1093/alcalc/agx027
15. American Diabetes Association. Standards of medical care in diabetes--2011. Diabetes Care. 2011;34(Suppl 1):S11-61.
16. International Diabetes Federation. Consensus definition of metabolic syndrome in children and adolescents. Brussels, Belgium: IDF; 2017. Disponible en: https://www.idf.org/e-library/consensus-statements/61-idf-consensus-definition-of-metabolic-syndrome-in-children-and-adolescents.html
17. Vos MB, Abrams SH, Barlow SE, Caprio S, Daniels SR, Kohli R, et al. NASPGHAN Clinical practice guideline for the diagnosis and treatment of nonalcoholic fatty liver disease in children: Recommendations from the expert committee on NAFLD (ECON) and the North American Society of Pediatric Gastroenterology, Hepatology and Nutrition (NASPGHAN). J Pediatr Gastroenterol Nutr. 2017;64(2):319-334. doi: 10.1097/MPG.0000000000001482h
18. Ezaizi Y, Kabbany MN, Conjeevaram-Selvakumar PK, Sarmini MT, Singh A, Lopez R, et al. Comparison between non-alcoholic fatty liver disease screening guidelines in children and adolescents. JHEP Rep. 2019;1(4):259-264. doi: 10.1016/j.jhepr.2019.06.005
19. Vittorio JM, Lavine JE. Role of Exercise in Mitigating Pediatric Nonalcoholic Fatty Liver Disease. Diabetes Care. 2020;43(2):280-282. doi: 10.2337/dci19-0029
20. Yu EL, Schwimmer JB. Epidemiology of Pediatric Nonalcoholic Fatty Liver Disease. Clin Liver Dis (Hoboken). 2021;17(3):196-199. doi: 10.1002/cld.1027
21. Lin MS, Lin TH, Guo SE, Tsai MH, Chiang MS, Huang TJ, et al. Waist-to-height ratio is a useful index for nonalcoholic fatty liver disease in children and adolescents: a secondary data analysis. BMC Public Health. 2017;17(1):851. doi: 10.1186/s12889-017-4868-5
22. Özhan B, Ersoy B, Özkol M, Kiremitci S, Ergin A. Waist to height ratio: a simple screening tool for nonalcoholic fatty liver disease in obese children. Turk J Pediatr. 2016;58(5):518-523. doi: 10.24953/turkjped.2016.05.009
23. Kenneally S, Sier JH, Moore JB. Efficacy of dietary and physical activity intervention in non-alcoholic fatty liver disease: a systematic review. BMJ Open Gastroenterol. 2017;4(1):e000139. doi: 10.1136/bmjgast-2017-000139
24. Martínez-Andrade GO, Cespedes EM, Rifas-Shiman SL, Romero-Quechol G, González-Unzaga MA, Benítez-Trejo MA, et al. Feasibility and impact of Creciendo Sanos, a clinic-based pilot intervention to prevent obesity among preschool children in Mexico City. BMC Pediatr. 2014;14:77. doi: 10.1186/1471-2431-14-77
25. Egger G, Swinburn B. An "ecological" approach to the obesity pandemic. BMJ. 1997;315(7106):477-80. doi: 10.1136/bmj.315.7106.477
26. Park CC, Nguyen P, Hernandez C, Bettencourt R, Ramirez K, Fortney L, et al. Magnetic Resonance Elastography vs. Transient Elastography in Detection of Fibrosis and Noninvasive Measurement of Steatosis in Patients With Biopsy-Proven Nonalcoholic Fatty Liver Disease. Gastroenterology. 2017;152(3):598-607.e2. doi: 10.1053/j.gastro.2016.10.026
27. Buzzetti E, Pinzani M, Tsochatzis EA. The multiple-hit pathogenesis of non-alcoholic fatty liver disease (NAFLD). Metabolism. 2016;65(8):1038-48. doi: 10.1016/j.metabol.2015.12.012
28. Colantonio DA, Kyriakopoulou L, Chan MK, Daly CH, Brinc D, Venner AA, et al. Closing the gaps in pediatric laboratory reference intervals: a CALIPER database of 40 biochemical markers in a healthy and multiethnic population of children. Clin Chem. 2012;58(5):854-68. doi: 10.1373/clinchem.2011.177741
29. Lee SS, Park SH. Radiologic evaluation of nonalcoholic fatty liver disease. World J Gastroenterol. 2014;20(23):7392-402. doi: 10.3748/wjg.v20.i23.7392
30. Fishbein MH, Miner M, Mogren C, Chalekson J. The spectrum of fatty liver in obese children and the relationship of serum aminotransferases to severity of steatosis. J Pediatr Gastroenterol Nutr. 2003;36(1):54-61. doi: /10.1097/00005176-200301000-00012
Notas de autor
efren.murilloza@imss.gob.mx
Información adicional
Declaración de conflicto de interés: los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno que tuviera relación con este artículo.
Cómo citar este artículo: García-López NA, Jiménez-Álvarez A, Murillo-Zamora E. Detección de hígado graso no alcohólico en niños con sobrepeso y obesidad. Rev Med Inst Mex Seguro Soc. 2021;59(6):465-72.
PubMed: https://pubmed.ncbi.nlm.nih.gov/34905320/
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/4099/4283 (pdf)
