Aportación original
Grupos sanguíneos y SARS-COV-2 en personal de salud de un solo centro
Blood groups and SARS-CoV-2 in health professionals from a single center
Grupos sanguíneos y SARS-COV-2 en personal de salud de un solo centro
Revista Médica del Instituto Mexicano del Seguro Social, vol. 59, núm. 5, 395-403, 2021
Instituto Mexicano del Seguro Social

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 25 Marzo 2021
Aprobación: 21 Junio 2021
Resumen:
Introducción: la posibilidad de que el grupo sanguíneo (GS) predisponga a infección por SARS-CoV-2 es controversial.
Objetivo: comparar prevalencia de GS, anti-IgG SARS-CoV-2 y síntomas más frecuentes, en personal de salud convaleciente frente a controles previo a la vacunación.
Material y métodos: diseño transversal analítico de casos y controles, que incluyó personal de salud, de marzo a junio de 2020, confirmados con reaccion en cadena de la polimerasa (PCR-SARS-CoV-2) y controles negativos con PCR y anti-IgG-SARS-COV-2. Se les interrogó sobre los síntomas y se determinó el GS. Se empleó estadística descriptiva y análisis comparativo con chi cuadrada o prueba exacta de Fisher y . de Student o . de Mann-Whitney.
Resultados: de 218 trabajadores, 102 (46.8%) fueron casos confirmados para SARS-CoV-2 (convalecientes) y 116 controles. La distribución de GS fue similar entre los casos y los controles y el GS-O+ fue el más frecuente (52.9%). El riesgo de infectarse de SARS-CoV-2 para el GS-O, comparado con GS-No-O mostró menor tendencia: razón de momios [RM] 0.725 (intervalo de confianza del 95% [IC 95%] 0.416-1.261; . = ns). El GS-A (28.4%) comparado con GS-No-A (71.6%) mostró tendencia de incremento del riesgo en GS-A, RM 1.523 (IC 95% 0.818-2.837, . = ns). La presencia de anticuerpos IgG de SARS-CoV-2 fue del 85% en el grupo de convalecientes.
Conclusiones: la prevalencia de infectados fue proporcionalmente mayor para GS-A y menor para GS-O. Alrededor de 15% no desarrollaron anticuerpos de SARS-CoV-2 después de recuperarse de COVID-19.
Palabras clave: Infecciones por Coronavirus, Personal de Salud, Sistema del Grupo Sanguíneo ABO.
Abstract:
Background: The possibility that the blood group (BG) predisposes to SARS-CoV-2 infection is controversial.
Objective: To compare the prevalence of BG, anti-IgG SARS-CoV-2, and more frequent symptoms in convalescent health personnel vs controls prior to vaccination.
Material and methods: Analytical cross-sectional design of cases and controls, which included health personnel, from March to June 2020, confirmed with (polymerase chain reaction) PCR-SARS-CoV-2 and negative controls with PCR and anti-IgG-SARS-CoV-2. Participants were questioned concerning symptoms and BG was determined. It was used descriptive statistics and comparative analysis with chi squared, Fisher's exact test, Student's ., and Mann Whitney's . tests.
Results: Of 218 workers, 102 (46.8%) were confirmed cases for SARS-CoV-2 (convalescent) and 116 controls. The distribution of BG was similar between cases and controls, being BG-O + the most frequent (52.9%). The risk of becoming infected by SARS-CoV-2 for BG-O compared to BG-No-O showed a lower trend (odds ratio [OR] 0.725, 95% confidence interval [95% CI] 0.416-1.261, . = ns). The BG-A (28.4%) compared with BG-No-A (71.6%) showed a trend of increased risk in BG-A (OR 1.523, 95% CI 0.818-2.837, . = ns). The presence of SARS-CoV-2 IgG antibodies was 85% in the convalescent group.
Conclusions: The prevalence of infected was proportionally higher for BG-A and lower for BG-O. About 15% did not develop SARS-CoV-2 antibodies after overcoming COVID-19 disease.
Keywords: Coronavirus Infections, Health Personnel, ABO Blood-Group System.
Introducción
En el 2019, la enfermedad del coronavirus 2019 (COVID-19), causada por el agente viral SARS-CoV-2, fue detectada en Wuhan, China. Esta enfermedad se extendió rápidamente por todo el planeta y desde marzo de 2020 ha sido reconocida como pandemia por la Organización Mundial de la Salud (OMS).1,2
Uno de los aspectos más controversiales, motivo de investigación desde el inicio de la pandemia, es la búsqueda de factores de riesgo para enfermar gravemente de COVID-19. En este sentido, durante la pandemia se han detectado factores de gravedad, como ser hombre,3 mayor de 60 años,4 o tener enfermedades crónicas como diabetes mellitus, obesidad, hipertensión arterial, entre otros.5 En relación con el grupo sanguíneo, los estudios han sido controversiales.6 Algunos estudios han asociado los alelos ABO con diferente susceptibilidad a contraer enfermedades infecciosas en general.7,8 En China compararon la distribución del grupo sanguíneo (GS) ABO en 2173 pacientes con COVID-19 con poblaciones locales que no habían enfermado. Encontraron que el GS-A se asoció a un mayor riesgo de infección, mientras que el GS-O se asoció con una disminución del riesgo.9 En otro estudio en 187 pacientes chinos, el riesgo de enfermar de COVID-19 se reportó mayor para los de GS-A que para GSNo-A.10 En China, 33% de la población general son GS-O y 37% son GS-A, 25% son GS-B y 9% son GS-AB. La población mexicana muestra una distribución muy diferente, ya que de cada 10 aproximadamente de 6 a 7 son GS-O y de 2 a 3 son GS-A. Entre 2014 y 2016, al explorar los GS en 271 164 mexicanos, la distribución de GS-O fue de 61.82%; GS-A: 27.44%; GS-B: 8.93%, y GS-AB: 1.81%. Respecto al Rh, el 95.58% de las personas eran Rh (D) O positivo y el 4.42% eran Rh (d) O negativo.11 Por otra parte, la detección de anticuerpos IgG en el personal de salud expuesto a infectarse por SARS-CoV-2 podría ser útil para estudiar quiénes son susceptibles a infectarse nuevamente,12,13 así como detectar al personal asintomático.14 El objetivo de este estudio fue comparar los síntomas más frecuentes, grupos sanguíneos y prevalencia de anticuerpos IgG en una muestra del personal de salud convaleciente de SARS-CoV-2 frente a controles antes de la vacunación.
Material y métodos
El diseño del estudio fue transversal analítico de casos y controles. Se estudiaron 218 individuos del personal de salud que labora en el Hospital de Especialidades “Dr. Antonio Fraga Mouret” del Centro Médico Nacional La Raza. Se incluyó al personal de salud que aceptó ser evaluado acerca de su nivel de anticuerpos IgG contra SARS-CoV-2, al tener la prueba de COVID-19 positiva o ser sospechoso de contagio de SARS-CoV-2.
Se incluyeron todos los casos consecutivos de trabajadores de salud que laboraran con pacientes enfermos de COVID-19, de todas las categorías contractuales del hospital mencionado, entre marzo y junio de 2020, que tuvieran entre 25 y 35 días a partir de los primeros síntomas respiratorios, o también aquellos asintomaticos que hubieran estado en contacto con algún individuo confirmado con COVID-19, con prueba de reacción en cadena de la polimerasa (PCR por sus siglas en inglés) para SARS-CoV-2, determinación de anticuerpos IgG para SARS-CoV-2, que desearan participar de manera voluntaria y firmaran la carta de consentimiento informado. Para su análisis se dividieron en dos grupos: 1. grupo de convalecientes: individuos con PCR positiva o anticuerpos IgG positivo a SARS-CoV-2; 2. grupo control: quienes tuvieron PCR negativo y anticuerpos IgG para SARS-CoV-2 negativos (figura 1). Al momento de entrar al estudio, todos los participantes se encontraban asintomáticos.
Ambos grupos fueron interrogados respecto a los síntomas que presentaron y el tratamiento que recibieron durante el curso de la enfermedad.
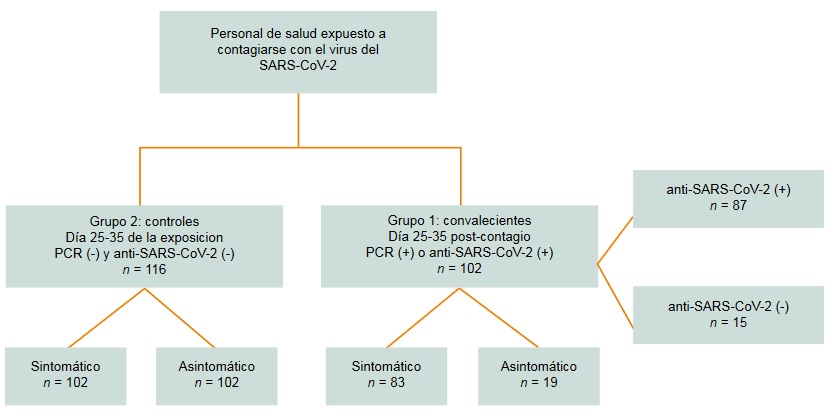
Figura 1
Figura 1
lasificación de pacientes (incluidos en este estudio) en grupos de comparación
PCR: reacción en cadena de la polimerasa; SARS-CoV-2: severe acute respiratory syndrome coronavirus 2; anti-SARS-CoV-2: anticuerpos para SARS-CoV-2Se realizó entrevista directa y exploración física. Entre los datos de la entrevista se incluyeron: comorbilidades, peso, talla, hospitalización, tratamientos utilizados e interrogatorio detallado de cada uno de los síntomas que han sido asociados a COVID-19 en las publicaciones.
Además, se tomaron muestras sanguíneas de laboratorio de rutina, grupo sanguíneo, anticuerpos IgG para SARS-CoV-2, para lo cual los participantes contaron con ayuno de ocho horas y se conservaron alícuotas para estudios paralelos. El análisis de grupos sanguíneos fue procesado en el Laboratorio de Transfusiones del hospital mencionado. La determinación de anticuerpos IgG para SARS-CoV-2 fue procesada con la técnica de Amanat et al., 2020,15 en la Unidad de Desarrollo e Investigación en Bioprocesos (UDIBI) de la Escuela Nacional de Ciencias Biológicas del Instituto Politécnico Nacional (México). Se excluyó el personal de salud no activo que no asistiera al hospital por prevención. Como grupo control se incluyó a personal sospechoso con prueba de PCR negativo. El protocolo fue registrado con el número R-2020-3501-108.
Análisis estadístico
Se llevó a cabo un muestreo de casos consecutivos y se calculó el tamaño de la muestra en 110 individuos con la fórmula de dos proporciones y se tomó en cuenta el porcentaje obtenido del GS-A+ en los controles (21%) y en los casos (28%) en una muestra de 53 pacientes, lo que nos dio un poder estadístico de 25%. Realizamos estadística descriptiva de las variables de interés en número y porcentaje o media y desviación estándar o mediana y rango intercuartil, según la distribución de los datos. Los datos obtenidos de la revisión y entrevista fueron capturados en el programa de Microsoft Excel 2010 y fueron analizados mediante el programa IBM SPSS, versión 20. Se utilizó prueba de chi cuadrada y prueba exacta de Fisher para comparar proporciones, t de Student para variables paramétricas y U de Mann-Whitney para variables no paramétricas.
Resultados
De 218 trabajadores de la salud analizados, 102 (46.8%) fueron “convalecientes” con PCR positiva a SARS-CoV-2 y 116 (53.2%) fueron “controles” negativos tanto a PCR como a anticuerpos IgG para SARS-CoV-2. De los 102 convalecientes, 83 (81%) fueron sintomáticos y 19 (19%) asintomáticos. De los 116 controles, 102 (96%) tuvieron síntomas que hicieron sospechar la presencia de COVID-19 y 14 (4%) solo tuvieron contacto con un enfermo de COVID-19 sin presentar síntomas. La edad media fue 37 ± 10 años; el sobrepeso u obesidad fue de casi 60% en los sintomáticos y alrededor de 80% en los asintomáticos convalecientes.
El GS general predominante fue O+ (59%), luego GS-A+ (24%), después el GS-B+ (9.6%), con menor frecuencia GS-O negativo (4.6%) y el menos frecuente de todos fue el GS-AB+ (2.3%). Específicamente al comparar con los controles, los convalecientes mostraron mayor tendencia a desarrollar anticuerpos en el GS-O+ (52% frente a 73%, p = 0.1682), menor en el GS-A+ (31% frente a 13%, p = 0.2214) y mayor similitud en los otros grupos (GS-B+, p = 0.62; GS-O negativo, p = 0.99, y AB+, p = 0.99) (cuadro I).
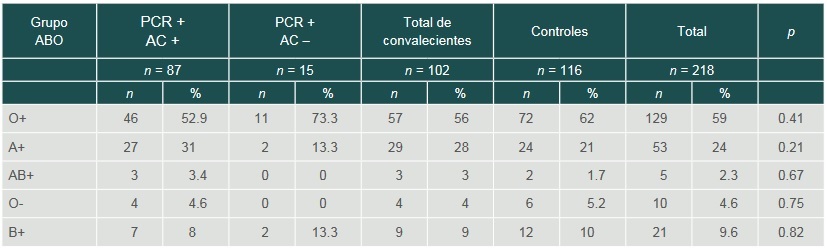
Cuadro I
Cuadro I
Clasificación ABO y RH de convalecientes y controles con o sin anticuerpos IgG para SARS-CoV-2
El análisis estadístico se hizo con chi cuadrada y prueba exacta de Fisher
PCR +: prueba de reacción en cadena de la polimerasa nasofaríngea SARS-CoV-2 positiva; AC +: detección de anticuerpos IgG anti SARS-CoV-2 positiva por ELISA; AC –: no detección de anticuerpos IgG para SARS-CoV-2 a pesar de haber superado la enfermedad > día 30Al comparar GS-O y GS-No-O, el porcentaje de individuos convalecientes del GS-O fue 58.9% y el de GS-No-O 41.1%, sin significación estadística. Con estos datos, el riesgo de infectarse durante el primer trimestre de la pandemia COVID-19 en México para el GS-O mostró menor tendencia (razón de momios [RM] de 0.725, IC 95% 0.416-1.261, p = ns). Por otro lado, el porcentaje de individuos convalecientes del GS-A fue de 28.4% comparado con GS-No-A (71.6%), lo cual mostró una tendencia al incremento del riesgo en GS-A, (RM de 1.523, IC 95% 0.818-2.837, p = ns).
En los casos confirmados para SARS-CoV-2 por PCR, 15/102 (14.7%) fueron asintomáticos. La prevalencia del GS en los pacientes asintomáticos no fue significativa. El personal de salud que enfermó de COVID-19 presentó cefalea y mialgias en más del 70%, en más del 40% astenia, tos, odinofagia y diarrea (cuadro II).
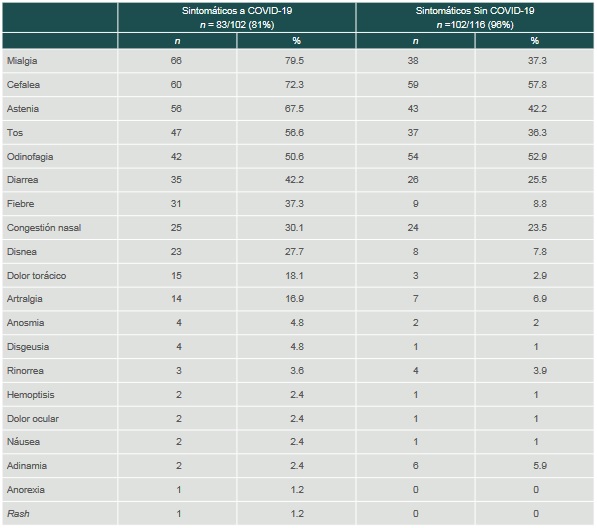
Cuadro II
Clasificación de síntomas en personal de salud (convalecientes no-hospitalizados y controles)
La proporción de pacientes asintomáticos para el GS-O+ fue del 19.3%, para el GS-A+ fue del 13.8%, para el GS-AB+ del 33.3%, para el GS-B+ del 33.3% y para el GS-O negativo del 0%. Las comorbilidades que se encontraron en los pacientes convalecientes fueron diabetes mellitus tipo II e hipertensión y esta última fue la más prevalente en el grupo de convalecientes que presentaron síntomas (cuadro III).
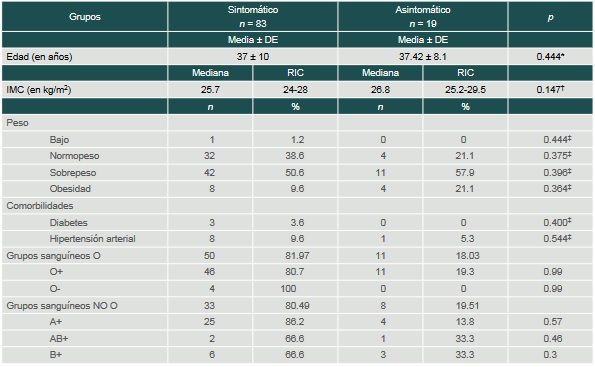
Cuadro III
Cuadro III
Características clínicas y clasificación ABO-RH de sujetos convalecientes (no-hospitalizados previamente) confirmados con PCR (+) y anticuerpos IgG (+) a SARS-CoV-2 que cursaron sintomáticos y asintomáticos
*Prueba t de Student
†Prueba U de Mann-Whitney
‡Prueba de chi cuadrada
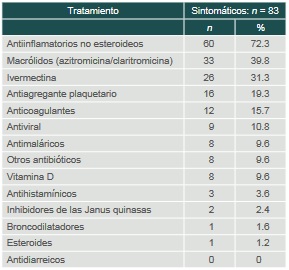
DE: desviación estándar; IMC: índice de masa corporal; RIC: rango intercuartílicoCuatro de los 87 sintomáticos con COVID-19 requirieron ingreso al hospital por enfermedad grave. Ninguno requirió ventilación mecánica ni falleció. De ellos, dos correspondían al GS-O+, uno al GS-A+ y uno al GS-AB+. El tratamiento más frecuente en los que enfermaron de COVID-19 leve o moderado fueron antiinflamatorios no esteoideos (AINE), macrólidos (azitromicina o claritromicina), ivermectina y antiagregantes plaquetarios o anticoagulantes (cuadro IV).
Cuadro IV
Cuadro IV
Clasificación de tratamiento ambulatorio recibido por el personal de salud no-hospitalizado que enfermó de COVID-19
Discusión
Hemos tenido una oportunidad única y trascendental para investigar factores de riesgo de contagiosidad en un padecimiento altamente mortal, al iniciar una evaluación en el debut de la COVID-19. Nuestros resultados sugieren que tener un GS-O pudiera ser un factor protector ante la infección por SARS-CoV-2, en contraste con tener GS-A, que podría incrementar el riesgo. De 218 trabajadores de nuestro hospital de tercer nivel, en poco menos de la mitad (102) fue corroborada la COVID-19 por PCR y anticuerpos IgG a SARS-CoV-2. De ellos, ocho de cada 10 desarrollaron la enfermedad clínica de COVID-19, caracterizada por mialgias y cefalea como síntomas principales y en los controles fue más frecuente cefalea y odinofagia. El tratamiento en COVID-19 leve o moderado fue similar al reportado en la literatura.16,17
Más de la mitad del total de individuos estudiados, sintomáticos o asintomáticos fue O+, alrededor de una cuarta parte GS-A, uno de cada diez GS-B y solo menos de 5% fue AB, lo cual es una representación excelente de la distribución de grupos en población mexicana.11 De los estudios sobre GS como posible factor de riesgo para infectarse con el virus SARS-CoV-2, destaca un metaanálisis donde se incluyeron siete estudios, derivados de 13 subgrupos de casos en comparación con su respectivo grupo control (para un total de 7503 casos y 2 962 160 controles) de China, Estados Unidos, Italia, España y Turquía. En este estudio se sugiere mayor susceptibilidad de los individuos del GS-A (RM 1.23, IC 95%: 1.09-1.40) a la infección por SARS-CoV-2 y el posible efecto protector del GS-O (RM 0.77, IC 95%: 0.67-0.88).18 Al respecto nosotros observamos una predominancia de grupo A (28 frente a 21%) y menor proporción del grupo O (60 frente a 67%) en el grupo de COVID-19 comparado con el control; sin embargo, estadísticamente no fue significativo por el pequeño número de individuos participantes.
Por otro lado, ya con anterioridad se ha cuestionado la relación entre la transmisión de enfermedades infecciosas con los GS para otros agentes virales como el norovirus y rotavirus como causantes de casos de gastroenteritis.19 Por ejemplo, Batool et al.20 encontraron una significante asociación entre la frecuencia de hepatitis B, hepatitis C y VIH en donantes de sangre con los grupos ABO. En este estudio realizado en Pakistán, donde el GS más frecuente fue B+, se encontró en los donantes con hepatitis B positivos una asociación significativa con los GS-A positivos. Por otro lado, en los donantes que resultaron positivos para el VIH, se encontró una asociación significativa en los grupos sanguíneos A positivos. En el estudio encontraron que el GS-O probablemente tiene una influencia protectora contra este tipo de infecciones, en contraparte con el GS-A, grupo que probablemente es más propenso a contraerlas. Por otra parte, Franchini et al.21 sugirieron una ventaja selectiva del alelo O que influye en la susceptibilidad a varios patógenos diferentes responsables de enfermedades, como la malaria grave, las infecciones por Helicobacter pylori y las formas graves de cólera. En nuestra población las personas con GS-O se infectaron más por SARS-CoV-2 en comparación con los demás grupos sanguíneos, debido a la mayor prevalencia de este grupo en la población mexicana, sin alcanzar una diferencia estadísticamente significativa con los controles.
Con respecto a los grupos de menor prevalencia, un estudio retrospectivo encontró que los pacientes con GS-B y AB, en quienes se realizó la prueba confirmatoria para COVID-19, tenían una mayor probabilidad de dar positivo. En contraste, las personas con GS-O tenían menos probabilidades de dar una prueba positiva para COVID-19. En este mismo estudio no se encontró asociación entre la severidad de la progresión en COVID-19 con los GS.22 En nuestro estudio no hubo diferencia significativa, dada la baja prevalencia de estos GS en la población. Algunos autores señalan al grupo sanguíneo ABO como posible marcador biológico de riesgo de COVID-19, y sugieren que personas de grupo O tienen menor probabilidad de infección. Los determinantes antigénicos ABO también se expresan en células de ciertos tejidos endoteliales y epiteliales como el sistema respiratorio. La presencia de antígenos A y B se ha relacionado con mayor susceptibilidad para infecciones, enfermedades cardiovasculares y cáncer, mientras que el grupo O suele asociarse con mayor resistencia a enfermedades.23
Los enfermos de COVID-19 presentan complicaciones inflamatorias, sobreinfecciones y trombosis asociadas a mayor mortalidad, por lo que los biomarcadores de inflamación, procalcitonina y el dímero D se han empleado con frecuencia para predecir riesgos. Otro factor de hemostasia es la glucoproteína del factor de von Willebrand (VWF), en la que se ha observado que individuos del grupo O tienen concentraciones menores de VWF y menor predisposición a complicaciones trombóticas al enfermar de COVID-19 que los del grupo No-O. Adicionalmente el virus de SARS-CoV-2 sintetiza epítopos de carbohidratos ABH en las células pulmonares y digestivas, donde podría unirse la proteína S y favorecer la formación de coágulos.23 En nuestro estudio cuatro individuos del personal de salud requirieron hospitalización, de los cuales dos fueron del GS-O+, 1 del GS-A+ y 1 del GS-AB+. Al ser un estudio de centro único, con alrededor de 2800 trabajadores y muchos de ellos en permiso laboral por alto riesgo de mal pronóstico, una limitación fue incluir una población relativamente reducida, decidido por factibilidad para estudiar los casos que se presentaron durante el primer trimestre de la pandemia en México. La muestra requerida para establecer una diferencia estadística en la mayor susceptibilidad del GS-A+ para infectarse por SARS-CoV-2 es el doble de la que hemos incluido en este estudio, por lo que el poder estadístico es de solo el 25%, lo cual no nos permite asegurar el mayor riesgo de infectocontagiosidad del GS-A+. Otra limitación de este estudio es el posible sesgo de recuerdo y la subjetividad de algunos síntomas. Por otra parte, de acuerdo con nuestro conocimiento, no existen estudios similares en nuestro país durante la época inicial de la pandemia, en la que no contábamos con vacunas, que analice los GS en personal expuesto a SARS-CoV-2.
Adicionalmente observamos que en los casos de enfermos de COVID-19 el GS-A predomina en población europea y china, mientras que en México y Estados Unidos predomina el GS-O (figura 2).
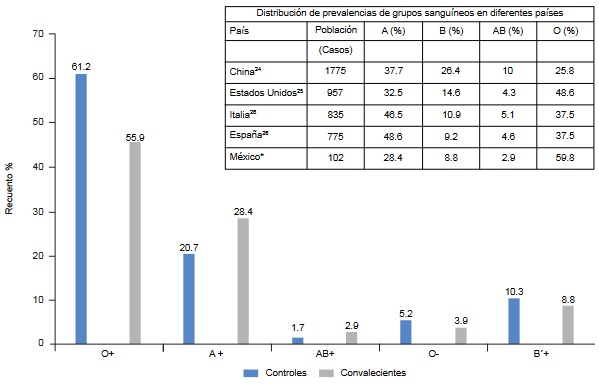
Figura 2
Figura 2
Prevalencia de grupos sanguíneos en COVID-19
Comparacion entre controles y convalecientes: O+: p = 0.41; A+: p = 0.21; AB+: p = 0.67; O-: p = 0.75; B+: p = 0.82. *Resultados que se reportaron en este estudioPor otra parte, en 220 casos en Navarra, España, se encontró una tendencia a una menor susceptibilidad a infectarse en el grupo O y un mayor riesgo de complicarse en el grupo B.23 Resulta de interés que en 2018, antes de la pandemia de COVID-19, un análisis en 271 164 mexicanos reportó una distribución global de los grupos ABO, O: 61.82%; A: 27.44%; B: 8.93%, y AB: 1.81%.11 Esta distribución es muy similar a la distribución de los trabajadores de salud de nuestro centro que se infectaron de SARS-CoV-2 en los primeros seis meses de la pandemia en México. No obstante, en el grupo control de trabajadores que no se infectaron fueron más del grupo O y menos del grupo A, aunque se requiere una mayor muestra para alcanzar significación.
Conclusiones
La prevalencia de contagios por SARS-CoV-2 fue proporcionalmente mayor para GS-A y menor para GS-O que lo esperado por la distribución nacional de GS y lo observado en no contagiados. El personal de salud convaleciente de enfermedad COVID-19 leve presentó manifestaciones clínicas similares a los controles expuestos no contagiados. La prevalencia de anticuerpos IgG en esta muestra del personal de salud confirmado con la prueba de PCR a SARS-COV-2 fue de 85%, lo que sugiere que alrededor de 15% podría no crear anticuerpos.
Referencias
1. Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019. N Engl J Med. 2020;382(8):727-33. doi: 10.1056/NEJMoa2001017
2. Mojica-Crespo R, Morales-Crespo MM. Pandemia COVID-19, la nueva emergencia sanitaria de preocupación internacional: una revisión. Semergen. 2020; 1:65-77. doi:10.1016/j.semerg.2020.05.010
3. Bienvenu LA, Noonan J, Wang X, Peter K. Higher mortality of COVID-19 in males: sex differences in immune response and cardiovascular comorbidities. Cardiovasc Res. 2020;116(14):2197-06. doi:10.1093/cvr/cvaa284
4. Ma Y, Hou L, Yang X, Huang Z, Yang X, Zhao N, et al. The association between frailty and severe disease among COVID-19 patients aged over 60 years in China: a prospective cohort study. BMC Med. 2020;18(1):274. doi: 10.1186/s12916-020-01761-0
5. Ejaz H, Alsrhani A, Zafar A, Javed H, Junaid K, Abdalla AE, et al. COVID-19 and comorbidities: Deleterious impact on infected patients. J Infect Public Health. 2020;13(12):1833-9. doi:10.1016/j.jiph.2020.07.014
6. Chen Y, Klein SL, Garibaldi BT, Li H, Wu C, Osevala NM, et al. Aging in COVID-19: Vulnerability, immunity and intervention. Ageing Res Rev. 2021;65:101205. doi:10.1016/j.arr.2020.101205
7. Lalueza-Fox C, Gigli E, de la Rasilla M, Fortea J, Rosas A, Bertranpetit J, et al. Genetic characterization of the ABO blood group in Neandertals. BMC Evol Biol. 2008;8:342. doi:10.1186/1471-2148-8-342
8. Liu N, Zhang T, Ma L, Zhang H, Wang H, Wei W, et al. The impact of ABO blood group on COVID-19 infection risk and mortality: A systematic review and meta-analysis. Blood Rev. 2020;100785. doi:10.1016/j.blre.2020.100785
9. Muñiz-Diaz E, Llopis J, Parra R, Roig I, Ferrer G, Grifols J, et al. Relationship between the ABO blood group and COVID-19 susceptibility, severity and mortality in two cohorts of patients. Blood Transfus. 2021;19(1):54-63. doi:10.2450/2020.0256-20
10. Wu Y, Feng Z, Peng Li P, Yu Q. Relationship between ABO blood group distribution and clinical characteristics in patients with COVID-19. Clin Chim Acta. 2020;509:220-3. doi: 10.1016/j.cca.2020.06.026
11. Canizalez-Román A, Campos-Romero A, Castro-Sánchez JA, López-Martínez MA, Andrade-Muñoz FJ, Cruz-Zamudio CK, et al. Blood Groups Distribution and Gene Diversity of the ABO and Rh (D) Loci in the Mexican Population. Biomed Res Int. 2018;2018:1-11. doi: 10.1155/2018/1925619
12. Liu X, Wang J, Xu X, Liao G, Chen Y, Hu C. H. Patterns of IgG and IgM antibody response in COVID-19 patients. Emerg Microbes Infect. 2020;9(1):1269-74. doi:10.1080/22221751.2020.1773324
13. Zhao J, Yuan Q, Wang H, Liu W, Liao X, Su Y, et al. Antibody Responses to SARS-CoV-2 in Patients With Novel Coronavirus Disease 2019. Clin Infect Dis. 2020;71(16):2027-34. doi: 10.1093/cid/ciaa344
14. Infantino M, Grossi V, Lari B, Bambi R, Perri A, Manneschi M, et al. Diagnostic accuracy of an automated chemiluminescent immunoassay for anti-SARS-CoV-2 IgM and IgG antibodies: an Italian experience. J Med Virol. 2020;92(9):1671-5. doi:10.1002/jmv.25932
15. Amanat F, Stadlbauer D, Strohmeier S, Nguyen THO, Chromikova V, McMahon M, et al. A serological assay to detect SARS-CoV-2 seroconversion in humans. Nat Med. 2020. https://doi.org/10.1038/s41591-020-0913-5
16. Procter BC, Ross C, Pickard V, Smith E, Hanson C, McCullough PA. Clinical outcomes after early ambulatory multidrug therapy for high-risk SARS-CoV-2 (COVID-19) infection. Rev Cardiovasc Med. 2020;21(4):611-4. doi:10.31083/j.rcm.2020.04.260
17. McCullough PA, Alexander PE, Armstrong R, Arvinte C, Bain AF, Bartlett RP, et al. Multifaceted highly targeted sequential multidrug treatment of early ambulatory high-risk SARS-CoV-2 infection (COVID-19). Rev Cardiovasc Med. 2020;21(4):517-30. doi:10.31083/j.rcm.2020.04.264
18. Golinelli D, Boetto E, Maietti E, Fantini MP. The association between ABO blood group and SARS-CoV-2 infection: A meta-analysis. PLoS One. 2020;15(9):e0239508. doi:10.1371/journal.pone.0239508
19. Pendu JL, Breiman A, Rocher J, Dion M, Ruvoën-Clouet N. ABO Blood Types and COVID-19: Spurious, Anecdotal, or Truly Important Relationships? A Reasoned Review of Available Data. Viruses. 2021;13(2):160. doi:10.3390/v13020160
20. Batool Z, Durrani SH, Tariq S. Association Of ABO And Rh Blood Group Types To Hepatitis B, Hepatitis C, Hiv And Syphilis Infection, A Five Year' Experience In Healthy Blood Donors In A Tertiary Care Hospital. J Ayub Med Coll Abbottabad. 2017;29(1):90-2.
21. Franchini M, Liumbruno GM. ABO blood group: old dogma, new perspectives. Clin Chem Lab Med. 2013;51(8):1545-53. doi:10.1515/cclm-2013-0168
22. Latz CA, DeCarlo C, Boitano L, Png CYM, Patell R, Conrad MF, et al. Blood type and outcomes in patients with COVID-19. Ann Hematol. 2020;99(9):2113-8. doi:10.1007/s00277-020-04169-1
23. Zalba MS, Antelo ML, Galbete A, Etayo M, Ongay E, García-Erce JA. Infection and thrombosis associated with COVID-19: Possible role of the ABO blood group. Med Clin (Barc). 2020;155(8):340-3. doi: 10.1016/j.medcli.2020.06.020
24. Li J, Wang X, Chen J, Cai Y, Deng A, Yang M. Association between ABO blood groups and risk of SARS-CoV-2 pneumonia. Br J Haematol. 2020; 190(1):24-7. doi:10.1111/bjh.16797
25. Dzik S, Eliason K, Morris EB, Kaufman RM, North CM. COVID-19 and ABO blood. Transfusion. 2020; 60(8): 1883-4. doi.org/10.1111/trf.15946
26. Severe Covid-19 GWAS Group. Genomewide Association Study of Severe Covid-19 with Respiratory Failure. N Engl J Med. 2020;383(16):1522-34. doi:10.1056/NEJMoa2020283
Notas de autor
drapilarcd@gmail.com
Información adicional
Declaración de conflicto de interés: los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno relacionado con este artículo.
Cómo citar este artículo: López-Zamora B, Ordoñez-González I, Morales-Montalvo SI, Medina-García G, Velázquez-García JA, Montes-Cortés DH et al. Grupos sanguíneos y SARS-CoV-2 en personal de salud de un solo centro. Rev Med Inst Mex Seguro Soc. 2021;59(5):395-403.
PubMed: https://pubmed.ncbi.nlm.nih.gov/34914348/
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/4071/4273 (pdf)
