Aportación original
Evolución clínica de 31 pacientes adultos con trombocitopenia inmune tratados con rituximab
Clinical evolution of 31 adult patients with immune thrombocytopenia treated with rituximab
Evolución clínica de 31 pacientes adultos con trombocitopenia inmune tratados con rituximab
Revista Médica del Instituto Mexicano del Seguro Social, vol. 61, núm. 1, pp. 21-32, 2023
Instituto Mexicano del Seguro Social

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 28 Febrero 2022
Aprobación: 25 Julio 2022
Resumen:
Introducción: la trombocitopenia inmune primaria (TIP) es una enfermedad autoinmune que puede causar hemorragias de diferente intensidad, las cuales llegan a poner en peligro la vida y alteran la calidad de vida de los pacientes. Puede ser tratada con rituximab como primera o segunda línea y la respuesta global es de 60%. Los mejores resultados se han observado en mujeres jóvenes con tiempo breve de evolución. Objetivo: reportar la respuesta y la evolución clínica con el tratamiento de rituximab usado como un rescate en pacientes adultos con TIP en fase crónica o persistente de la enfermedad. Material y métodos: se le administró rituximab de forma semanal por cuatro dosis a 31 pacientes adultos y se les hizo seguimiento durante un año. Resultados: de los 31 pacientes adultos, se observó respuesta completa (RC, plaquetas ≥ 100 x 109 /L) en 22 pacientes (71%) y respuesta parcial (RP, plaquetas ≥ 30 y ≤ 99x 109 /L) en 5 pacientes (16%); la respuesta global fue de 87%. Tres pacientes recayeron durante el seguimiento y la respuesta sostenida (≥ 12 meses) se mantuvo en 24 pacientes, 21 (67%) con RC y 3 (10%) con RP. Los efectos secundarios fueron de leves a moderados en 13% de los pacientes. Conclusiones: el rituximab demostró su utilidad en pacientes con TIP como tratamiento de rescate en las fases crónica y persistente. La respuesta sostenida ≥ 12 meses fue de 77%, con buena tolerancia y toxicidad aceptable.
Palabras clave: Trombocitopenia Autoinmune, Rituximab.
Abstract:
Background: Primary immune thrombocytopenia (ITP) is an autoimmune disease that could cause different grades of bleeding, which could even threat the patients’ life or make them experience poor quality of life. ITP can be treated with rituximab either as a first or second-line therapy option, resulting in an overall response of 60%. The best results have been observed on young women with a short time of disease evolution. Objective: To report the response and clinical evolution by providing therapy with rituximab, which was used as a rescue in adult patients with either persistent or chronical ITP. Material and methods: 4 weekly doses of rituximab were administered to 31 adult patients and it was made a follow-up with them for a year. Results: Out of the 31 patients, a complete response was observed (CR, platelets ≥ 100 x 109 /L) in 22 patients (71%), and a partial response (PR, platelets ≥ 30 and ≤ 99 x 109 /L) in 5 patients (16%); the global response was of 87%. 3 patients relapsed during follow-up and sustained response after rituximab (≥ 12 months) was held in 24 patients, 21 (67%) with CR and 3 (10%) with PR. Side effects were from low to moderate in 13% of patients. Conclusions: Rituximab showed its effectiveness in patients with ITP as a rescue therapy in both chronical and persistent phases. Sustained response ≥ 12 months was of 77%, with good tolerance and acceptable toxicity.
Keywords: Immune Thrombocytopenia, Rituximab.
Introducción
La trombocitopenia inmune primaria (TIP) es una enfermedad adquirida, la cual se define por una cuenta de plaquetas < 100 x 109 /L en forma transitoria o persistente y dependiendo del grado de trombocitopenia, hay el riesgo de hemorragia.1,2 Se combinan de forma variable: 1) la aparición de autoanticuerpos antiplaquetarios; 2) la remoción de plaquetas sensibilizadas por el sistema retículo-endotelial; 3) la megacariopoyesis disminuida por la acción de los autoanticuerpos y 4) la destrucción de plaquetas mediada por células T.2,3 La formación de autoanticuerpos antiplaquetarios es favorecida por la pérdida de tolerancia inmune con disminución de linfocitos T reguladores (T-reg).4 La enfermedad en los adultos tiene prevalencia en mujeres jóvenes, pero en los adultos > 65 años es muy semejante entre hombres y mujeres.3 En cuanto al tiempo de evolución con la enfermedad, se encuentra la fase de reciente diagnóstico, con menos de tres meses de evolución; la fase persistente, de los tres a los 12 meses, y la fase crónica, con más de 12 meses de evolución.1,2,3
La primera línea de tratamiento en pacientes con TIP de reciente diagnóstico incluye los corticosteroides, como la prednisona por vía oral, o las dosis altas de dexametasona, sola o combinada con otros fármacos como rituximab y agentes trombopoyéticos.5,6,7,8 La segunda línea de tratamiento incluye la esplenectomía, con respuesta del 60-70% a cinco años, y el rituximab, con respuesta global de 60%, respuesta completa de 40% y respuesta sostenida de 15-20% en un lapso de 3 a 5 años.2 Los agonistas de los receptores de trombopoyetina (AR-TPO), con respuesta > 80%, también son otro tratamiento de primera o segunda linea.2,3
El rituximab reduce las células B y la producción de autoanticuerpos en forma reversible, regula también el comportamiento de los linfocitos T y es utilizado en el tratamiento de la TIP solo o combinado con otros fármacos, que es cuando demuestra su eficacia y baja toxicidad.4
El objetivo de este estudio fue presentar los resultados con el tratamiento de rituximab usado como un rescate y el seguimiento durante 12 meses en pacientes con TIP en diferentes fases de la enfermedad, que tuvieran recaída y tratamientos de primera y segunda línea o subsecuentes. Se mencionará la respuesta clínica y la modificación de la cifra de plaquetas de los pacientes, posterior al tratamiento con rituximab.
Material y métodos
El presente estudio derivó de una investigación previa en nuestro hospital, en el año 2013, aprobada por el Comité Local de Investigación y Ética en Investigación en Salud, con número de registro: R-2012-3601-57.
El presente estudio es retrospectivo y se hizo con la captación de pacientes con diagnóstico de TIP que recibieron tratamiento con rituximab durante los años 2017 y 2018, en el Servicio de Hematología del Hospital de Especialidades “Dr. Bernardo Sepúlveda Gutiérrez” del Centro Médico Nacional Siglo XXI. Después del tratamiento con rituximab, los pacientes tuvieron seguimiento por medio de la consulta externa y su expediente clínico durante 12 meses, a fin de informar los resultados del tratamiento y la evolución clínica de los pacientes.
Criterios de inclusión
Se incluyeron en el estudio pacientes adultos con TIP, de cualquier género, que estuvieran en la fase persistente o crónica de la enfermedad, que no tuvieran contraindicaciones para rituximab, que se encontraran en recaída de la enfermedad, que tuvieran trombocitopenia con o sin hemorragia asociada y que fueran dependientes de los corticosteroides.
A todos los pacientes se les solicitó su consentimiento informado para que participaran en el estudio.
Inmunización
De forma profiláctica, todos los pacientes antes de iniciar el tratamiento con rituximab, recibieron vacuna antineumocóccica y debían contar con serología negativa para hepatitis B, como ha sido recomendado en otros estudios.9
Administración del rituximab
Se aplicaron cuatro dosis, cada una de forma semanal. Tomando en cuenta que hasta la fecha no hay un consenso internacional en la dosis de rituximab para esta enfermedad, las dosis se administraron con base en las siguientes modalidades:
a) Una dosis fija de 250 mg en los pacientes mayores de 75 años para, con ello, disminuir el riesgo de toxicidad.
b) Una dosis fija de 500 mg de acuerdo con la presentación farmacéutica de rituximab (frasco ámpula de 500 mg/10 mL), con lo cual se utilizó la totalidad de la dosis del vial y se evitó desechar parte del fármaco.
c) Las dosis calculadas a razón de 375 mg/m2 de superficie corporal fueron asignadas a criterio del médico tratante del paciente. Esta dosis es considerada como estándar en los pacientes con linfomas.
El rituximab se administró por vía intravenosa (IV) y fue diluido en solución salina fisiológica al 0.9%, a razón de 1 mg/mL y se administró en infusión de seis horas. Todos los pacientes fueron premedicados con metilprednisolona 150 mg IV, paracetamol 1 g vía oral y difenhidramina 25 mg IV. En la primera infusión, los pacientes fueron hospitalizados para vigilancia del tratamiento y las siguientes tres dosis se aplicaron de forma ambulatoria. Los pacientes recibieron tratamiento profiláctico a base de fluconazol 100 mg por día vía oral y aciclovir 200 mg cada 12 horas vía oral, después del tratamiento con rituximab, durante ocho semanas.
Tratamiento concomitante con rituximab
Al iniciar el tratamiento con rituximab, el tratamiento para la TIP que los pacientes se encontraban utilizando en ese momento se mantuvo con su administración y posteriormente fue reducido, modificado e incluso se suspendió según la evolución de cada paciente y a criterio de los médicos tratantes.
Criterios de respuesta
De acuerdo con la evolución clínica y la cifra de plaquetas obtenida después de la administración del rituximab, se consideraron los siguientes criterios de respuesta:
a) Respuesta completa (RC): si se alcanzaban plaquetas ≥ 100 x109/L, al menos durante seis meses, si había ausencia de hemorragias.
b) Respuesta parcial (RP): con plaquetas ≥ 30 x 109/L y ≤ 99 x 109/L, al menos durante seis meses y sin evidencia de hemorragias.
c) Respuesta global o general: se consideró a la suma de pacientes con RC y RP.
d) No respuesta (NR): si las plaquetas basales no aumentaban y eran < 30 x 109/L, con o sin hemorragias.
e) Recaída: si durante el seguimiento los pacientes presentaban disminución de sus plaquetas < 100 x 109/L, o < 30 x 109/L, en los pacientes con RC o RP, respectivamente, con o sin hemorragias.
f) Respuesta sostenida: si los pacientes permanecían ≥ 12 meses con RC o RP después del tratamiento.
Efectos secundarios y seguimiento
Los pacientes fueron seguidos mediante la consulta externa, con estudios periódicos de laboratorio, durante 12 meses y se reportaron los efectos secundarios relacionados con el tratamiento con rituximab.
Análisis estadístico
Se hizo el análisis descriptivo estratificado por fase de la enfermedad y posteriormente se evaluó la respuesta al tratamiento. Todas las variables se contrastaron con la prueba de hipótesis que correspondiera: prueba exacta de Fisher, chi cuadrada o t de Student.
Resultados
Se estudiaron un total 31 pacientes adultos, con una mediana de edad de 51 años, siete se encontraban en fase persistente y 24 en fase crónica, con una mediana de tiempo de evolución de 10 y 56 meses, respectivamente. La mediana de plaquetas basales fue de 26 x 109/L. Todos habían recibido tratamientos previos de primera y segunda línea, incluidos rituximab y esplenectomía. Los tratamientos previos fueron aplicados a lo largo de la evolución de la enfermedad de los pacientes y se dieron al diagnosticarse esta y cuando los pacientes tuvieron recaída con trombocitopenia grave, con la presencia o no de hemorragias, y fueron asignados a criterio de los diferentes médicos tratantes en cada ocasión. Algunos pacientes fueron tratados en otros hospitales antes de ser enviados a nuestro servicio. Los tratamientos previos se pueden usar solos o combinados por tiempo variable hasta que las cifras plaquetarias se normalizan o mejoran, tras lo cual dichos tratamientos pueden ser modificados o retirados. Cuando se decidió comenzar a usar rituximab en nuestros pacientes, se encontraban recibiendo algún tratamiento y se decidió continuar con dicho tratamiento de forma concomitante con rituximab; posteriormente, según la evolución, los tratamientos concomitantes fueron reducidos, modificados o retirados de acuerdo con la respuesta observada con rituximab. En el cuadro I se anotan los tratamientos registrados en los expedientes de los pacientes.
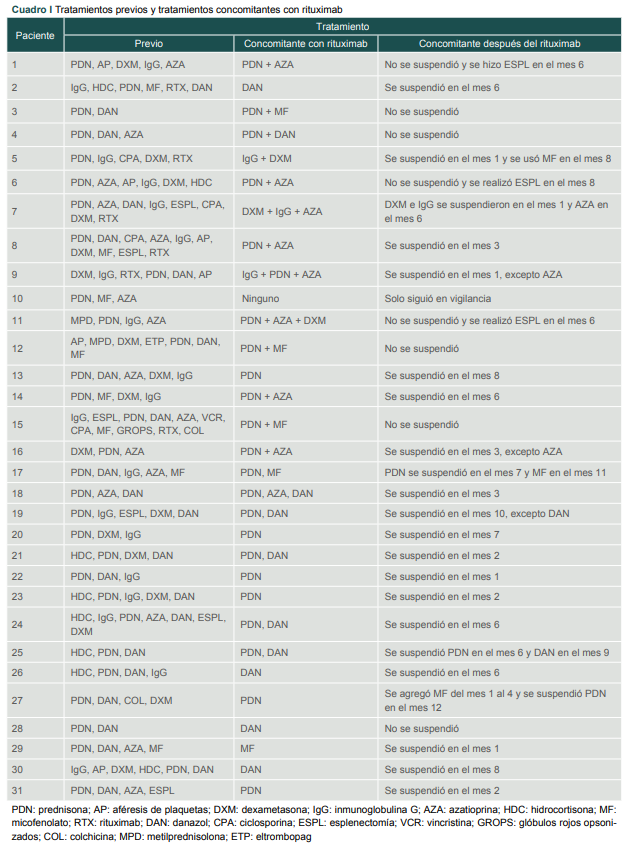
Cuadro I
Tratamientos previos y tratamientos concomitantes con rituximab
PDN: prednisona; AP: aféresis de plaquetas; DXM: dexametasona; IgG: inmunoglobulina G; AZA: azatioprina; HDC: hidrocortisona; MF: micofenolato; RTX: rituximab; DAN: danazol; CPA: ciclosporina; ESPL: esplenectomía; VCR: vincristina; GROPS: glóbulos rojos opsonizados; COL: colchicina; MPD: metilprednisolona; ETP: eltrombopag
No se observaron diferencias entre el género, la edad y los tratamientos previos cuando se compararon los pacientes de las fases persistente y crónica de la TIP (cuadro II).
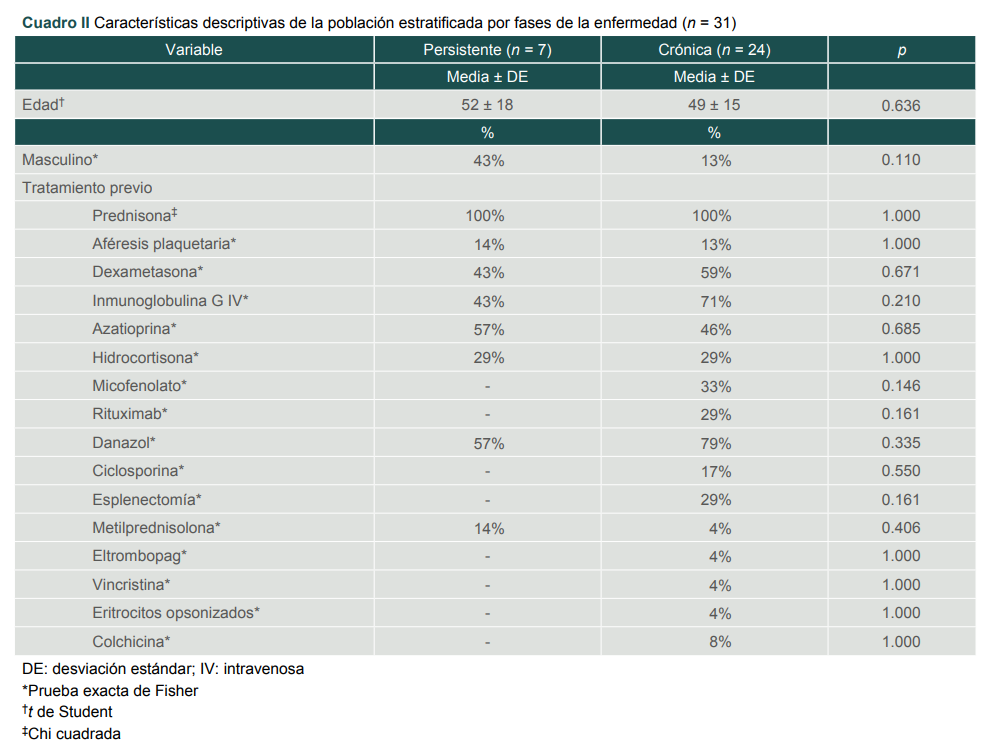
Cuadro II
Características descriptivas de la población estratificada por fases de la enfermedad (n = 31)
DE: desviación estándar; IV: intravenosa
*Prueba exacta de Fisher
† t de Student
‡Chi cuadrada
Al comenzar el tratamiento con el rituximab, las cifras de hemoglobina y leucocitos de todos los pacientes se encontraron dentro de los límites normales y durante el seguimiento no se observó anemia, neutropenia o linfocitopenia en ningún paciente. No fueron evaluados los niveles de inmunoglobulinas. Al iniciar el tratamiento con rituximab, solo 10 pacientes (32%) tenían algún tipo de hemorragia, como equimosis, menorragia, epistaxis y gingivorragia, las cuales se controlaron después del tratamiento con rituximab en los pacientes con RC y RP, cuestión que coincidió con el aumento de sus plaquetas (cuadro III).
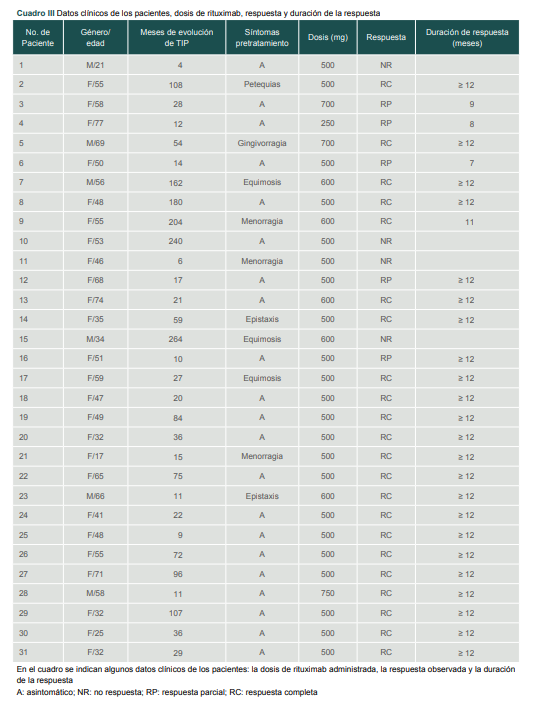
Cuadro III
Datos clínicos de los pacientes, dosis de rituximab, respuesta y duración de la respuesta
En el cuadro se indican algunos datos clínicos de los pacientes: la dosis de rituximab administrada, la respuesta observada y la duración de la respuesta
A: asintomático; NR: no respuesta; RP: respuesta parcial; RC: respuesta completa
En cuatro pacientes (número 6, 8, 12 y 25) se presentaron efectos secundarios (13%) durante la primera infusión de rituximab, como erupción cutánea, hipertensión arterial, dolor torácico, náuseas y disnea; todas estas alteraciones fueron controladas y no fue necesario suspender el tratamiento. Una paciente (la número 12) presentó neumonía de etiología bacteriana después de la primera dosis de rituximab, pero fue controlada y se completó su tratamiento. Otra paciente (la número 25) presentó otitis media aguda y herpes zóster, los cuales se controlaron y se completó el tratamiento.
Durante el seguimiento fue necesario realizar esplenectomía a tres pacientes (los número 1, 6 y 11): en el sexto mes a los pacientes 1 y 11, los cuales no tuvieron respuesta con rituximab, y con la esplenectomía el paciente 1 alcanzó RC y se mantuvo hasta finalizar el seguimiento; la paciente 11 alcanzó RC con la esplenectomía, pero solo por un mes; y la paciente 6 alcanzó respuesta parcial con rituximab, fue intervenida en el mes 8 y alcanzó RC durante dos meses. Se observó trombosis venosa profunda en un paciente (el número 5), en el mes 4 de seguimiento y recibió tratamiento con anticoagulante oral y también se consideró necesario agregar micofenolato ante el riesgo de presentar recaída con trombocitopenia grave y estar en tratamiento anticoagulante. Los tratamientos concomitantes con rituximab fueron reducidos, modificados e incluso se pudieron suspender en la mitad de pacientes (cuadro I).
Del total de pacientes, 22 (71%) tuvieron RC, cinco (16%) tuvieron RP y cuatro pacientes no respondieron. Durante el seguimiento, tres pacientes (el 4, 6 y 9) presentaron recaída (11%), en los meses 8, 7 y 11 respectivamente y al finalizar el seguimiento, 24 pacientes mantuvieron una respuesta sostenida ≥ 12 meses, 21 (67%) con RC y tres (10%) con RP, de los cuales 20 estaban en fase crónica y cuatro en la fase persistente (cuadro IV).
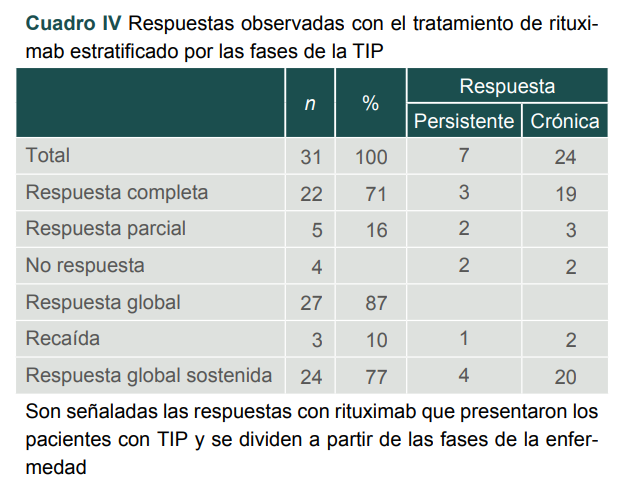
Cuadro IV
Respuestas observadas con el tratamiento de rituximab estratificado por las fases de la TIP
Son señaladas las respuestas con rituximab que presentaron los pacientes con TIP y se dividen a partir de las fases de la enfermedad
No se observaron diferencias en la respuesta entre las diferentes dosis de rituximab y tampoco se observaron diferencias entre las fases crónica y persistente, ni con los tratamientos concomitantes de la TIP (cuadro V).
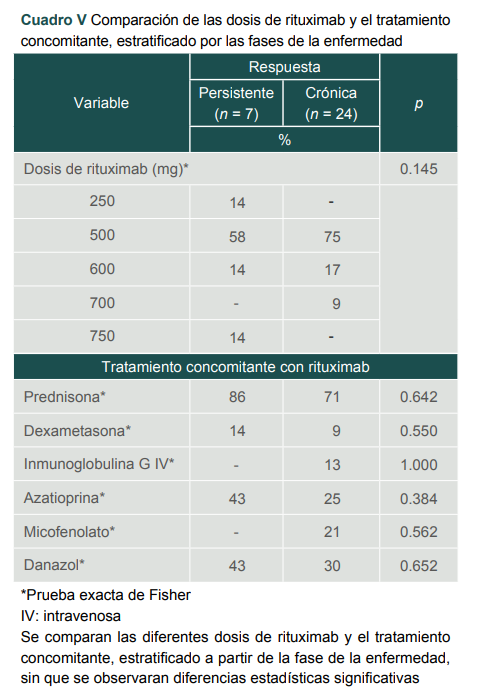
Cuadro V
Comparación de las dosis de rituximab y el tratamiento concomitante, estratificado por las fases de la enfermedad
*Prueba exacta de Fisher
IV: intravenosa
Se comparan las diferentes dosis de rituximab y el tratamiento concomitante, estratificado a partir de la fase de la enfermedad, sin que se observaran diferencias estadísticas significativas
Asimismo, no hubo diferencias en la RC o RP entre los pacientes en fase crónica o persistente, pero es importante señalar que con el tratamiento de rituximab, 92 y 71% de pacientes en fase crónica y persistente, respectivamente, lograron algún tipo de respuesta.
Durante el seguimiento después del tratamiento, se observó que los pacientes respondedores y que estaban en fase crónica tuvieron un aumento significativo de plaquetas al quinto mes, en comparación con los pacientes en fase persistente; este comportamiento puede deberse a que los pacientes respondedores con RC aumentaron sus plaquetas de forma más temprana que los pacientes con RP, pero además es probable que los pacientes con RC y en fase crónica también aumentaran sus plaquetas más tempranamente que los pacientes con RC pero en fase persistente (cuadro VI).
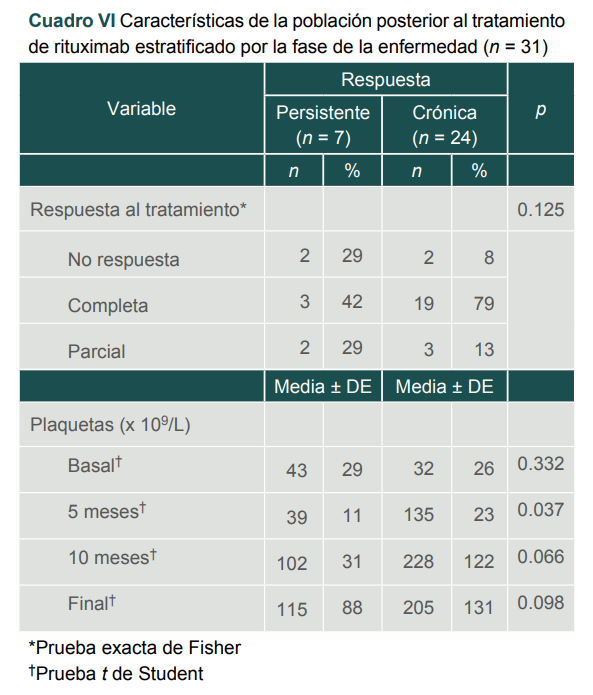
Cuadro VI
Características de la población posterior al tratamiento de rituximab estratificado por la fase de la enfermedad (n = 31)
*Prueba exacta de Fisher
†Prueba t de Student
Otra diferencia estadística observada se notó al comparar la cifra de plaquetas al inicio del tratamiento con rituximab y al final del seguimiento; se observó un incremento de plaquetas independiente del tiempo de evolución con la enfermedad y esto es debido al tratamiento con rituximab (figura 1).
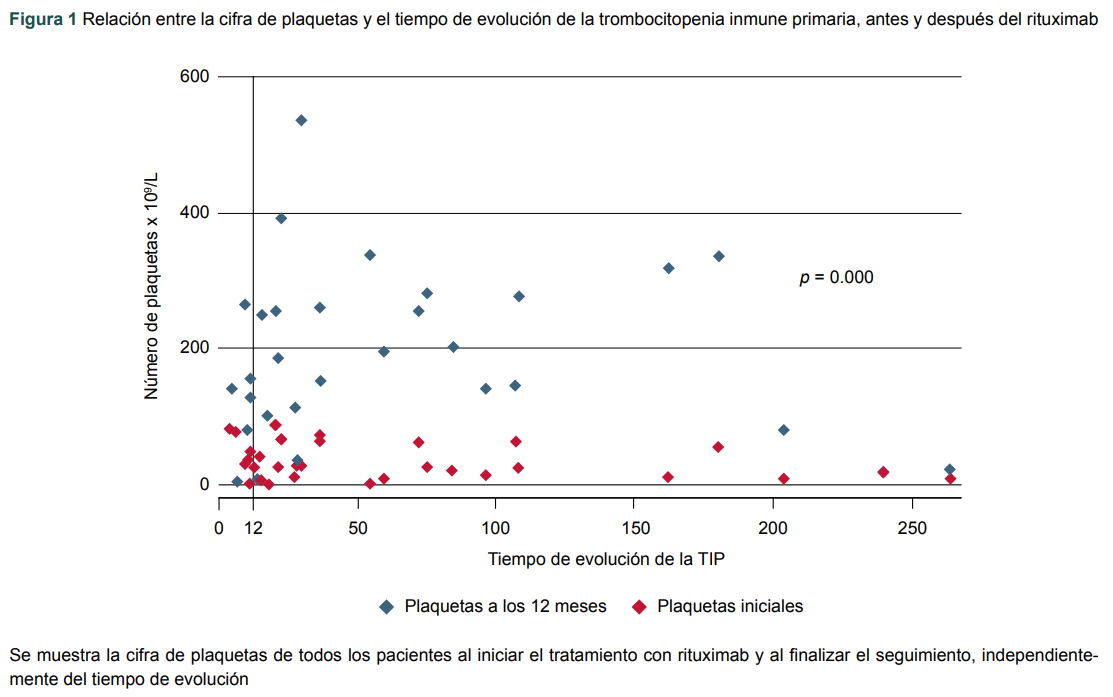
Figura 1
Relación entre la cifra de plaquetas y el tiempo de evolución de la trombocitopenia inmune primaria, antes y después del rituximab
Se muestra la cifra de plaquetas de todos los pacientes al iniciar el tratamiento con rituximab y al finalizar el seguimiento, independientemente del tiempo de evolución
Cuando se comparan los pacientes con RC y RP, se observa un aumento de plaquetas de forma más rápida en los pacientes con RC (figura 2).
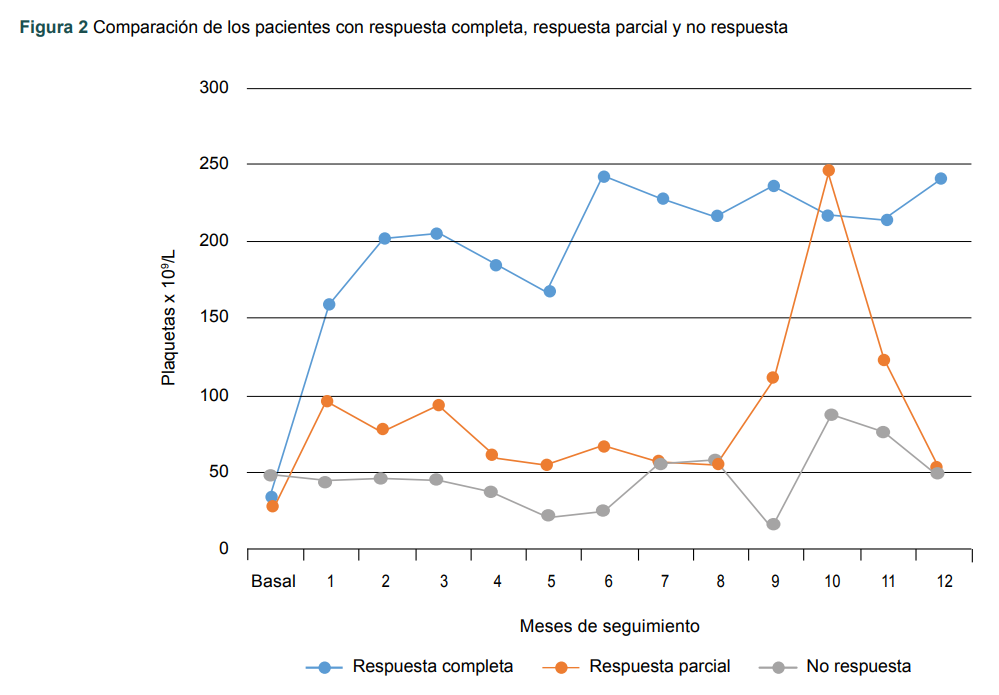
Figura 2
Comparación de los pacientes con respuesta completa, respuesta parcial y no respuesta
Evolución de las cifras plaquetarias durante el seguimiento, según la respuesta obtenida con rituximab. En la curva de respuesta parcial hay una elevación entre el mes 9 y 11, que corresponde al paciente 6, a quien se le realizó esplenectomía y presentó respuesta completa, con recaída a los dos meses
Discusión
Entre los mejores tratamientos de segunda línea para la TIP con respuesta sostenida se encuentra la esplenectomía; no obstante, actualmente esta se trata de evitar y menos de 25% de pacientes son intervenidos por los riesgos de infecciones, trombosis o complicaciones postoperatorias inmediatas.2,3 Los AR-TPO son muy efectivos y seguros, con algunos inconvenientes, como, por ejemplo, su costo y una respuesta dependiente de la administración continua de estos medicamentos.2,10 Sin embargo, otros estudios han observado que una tercera parte de pacientes tratados con romiplostim, un AR-TPO, mantuvieron plaquetas ≥ 50 x 109/L por más de seis meses después de suspender la administración del fármaco.7
Las guías de tratamiento de la Sociedad Americana de Hematología (ASH, por sus siglas en inglés) recomendaron el uso de rituximab en pacientes adultos con TIP y riesgo de hemorragias, quienes habían fallado a otros tratamientos, como los corticosteroides, la IgG-IV o la esplenectomía.11 Posteriormente, estas guías de tratamiento recomendaron el rituximab como un tratamiento de segunda línea para adultos con tres o más meses de evolución que no respondieran a corticosteroides o fueran dependientes de los mismos; también se consideró como una alternativa a la esplenectomía, por las complicaciones potenciales con el procedimiento quirúrgico.12
El rituximab se ha usado como tratamiento de primera línea, combinado con dexametasona (respuesta sostenida > seis meses de 63% frente a dexametasona sola 36%)5 y AR-TPO, pero las guías internacionales recomiendan solamente los corticosteroides como primera línea de tratamiento y en algunos pacientes especiales, la terapia combinada.12 El rituximab también constituye un tratamiento de segunda línea y su respuesta es de 40 a 60%, pero la respuesta sostenida de tres a cinco años solo es de 15-20%, de acuerdo con diferentes reportes.2,3,9,13,14,15,16,17
En un estudio en el que se compararon adultos y niños con TIP > seis meses de evolución, los cuales recibieron dosis de 375 mg/m2 de rituximab, se observó una respuesta de 57% en ambos grupos y la respuesta libre de tratamiento, estimada a cinco años fue de 21 y 26%, respectivamente, sin mayor toxicidad.18
Una revisión sistemática que incluyó a 313 pacientes con TIP que fueron tratados con rituximab reportó una tasa de respuesta global (plaquetas > 50 x 109/L) de 62.5% y una respuesta completa (plaquetas > 150 x 109/L) de 46%. La respuesta se presentó entre dos y 48 meses, con duración promedio de 10.5 meses y la mediana del tiempo de respuesta fue de 5.5 semanas. La limitación de este informe fue la falta de estudios controlados.9,19 Este tratamiento también se aplicó a 26 pacientes con TIP que se encontraban en recaída o refractarios, y se reportó RC en 54% y RP en 15%; el 35% mantuvo la respuesta con una mediana de seguimiento de 57 meses, con un buen perfil de seguridad.10 Otro metaanálisis señaló que la RC fue más probable en pacientes que recibieron rituximab, comparado con el tratamiento de TIP estándar; en 376 pacientes adultos, 38% lograron RC y 19% RP, y mantuvieron la remisión por un año el 38% y por cinco años solo 21%. Los pacientes esplenectomizados tuvieron una tendencia a recaer más tempranamente que los pacientes no esplenectomizados.20
En nuestro estudio con el tratamiento de rituximab se observó RC en 71% y RP en 16%; de los pacientes que estaban en la fase crónica y persistente, el 92 y 71%, respectivamente, tuvieron respuesta al tratamiento. Todos los pacientes con RC y RP que presentaban hemorragias al inicio del tratamiento se controlaron después del tratamiento con rituximab, lo cual coincidió con el incremento de sus plaquetas. De acuerdo con otros estudios, la tasa más alta de pacientes respondedores con rituximab se observa en aquellos con una enfermedad entre 12 y 24 meses de evolución,9 pero en otros estudios solo se menciona como indicador de mejor respuesta un intervalo corto entre el diagnóstico y el comienzo del uso de rituximab.10 En el presente estudio, estar en fase persistente o crónica de la enfermedad no fue una limitante para alcanzar algún tipo de respuesta con rituximab y algunos de nuestros pacientes con una evolución de su enfermedad tan prolongada (de seis a 15 años) alcanzaron RC (cuadro II).
Un estudio con rituximab realizado en nuestro país, en pacientes adultos con TIP crónica y refractaria, reportó una RC (plaquetas > 100 x 109/L) de 28% y una RP (plaquetas > 50 x 109/L) de 28%. En ese mismo estudio, la probabilidad de alcanzar una respuesta de plaquetas > 50 x 109/L en promedio se observó a los cinco meses y la respuesta sostenida a seis meses fue de 67%.21 A diferencia del estudio antes mencionado, en la mayoría de nuestros pacientes respondedores el aumento de plaquetas se observó en las primeras cuatro a ocho semanas después del tratamiento y cuando se compararon los pacientes, hubo un aumento significativo de plaquetas al quinto mes en los pacientes de la fase crónica frente a la fase persistente. No tenemos por ahora una explicación del porqué los pacientes en fase crónica aumentaron sus plaquetas más rápidamente que los pacientes en fase persistente. En respondedores, el aumento de plaquetas es observado rápidamente, usualmente una semana después de la primera dosis de rituximab.22 De acuerdo con estos datos, se puede asumir que es posible que los pacientes que aumentan sus plaquetas de forma temprana logren la RC y de manera sostenida. En algunos estudios se comenta que la intensidad de la respuesta se relaciona directamente con su duración;13,23en otros, se ha encontrado que en los pacientes con un año o más de respuesta, la recaída se presentó en 53 y 31% de pacientes con RP y RC, respectivamente.20
De acuerdo con la velocidad de respuesta con la aplicación de rituximab, se describen tres tipos: rápida, dentro del primer mes; intermedia, hasta los dos meses, y tardía, después de tres meses.23 Según esta observación, la mayoría de nuestros pacientes con respuesta global tuvieron un patrón de respuesta rápida e intermedia.
En cuanto a las dosis de rituximab en esta enfermedad, se han utilizado dosis de 100 mg, dosis estándar de 375 mg/m2, la cual está recomendada en el tratamiento de linfomas, e incluso dosis altas de 1000 mg (dosis utilizadas en pacientes con artritis reumatoide). Zaja et al.24 informaron que la respuesta general fue de 60% y la RC de 29% en pacientes con TIP que recibieron cuatro dosis de 100 mg por semana; sin embargo, la duración de su efecto fue corta.24 Otros autores no han encontrado diferencias significativas entre las dosis bajas y las estándar en cuanto a la respuesta general (62 frente a 64% a los seis meses) y la duración de la respuesta; algunas potenciales ventajas con las dosis bajas serían disminuir los efectos adversos y los costos, así como administrar cursos repetidos.4
En este estudio, la dosis de rituximab en la mayoría de pacientes fue de 500 mg, esto con base en la presentación del producto que se dispone en nuestro hospital. Con esta dosis de 500 mg, se evita desechar rituximab, lo que sucede cuando se utilizan dos viales para completar una dosis más alta; también se evita desechar el medicamento cuando se llegan a emplear dosis más bajas. La dosis de 250 mg se administró solo a una paciente (la 4), ya que tenía 77 años y las dosis de 600, 700 y 750 mg fueron calculadas como dosis estándar de 375 mg/m2 por decisión de los médicos tratantes en ese momento; no se observaron diferencias en la respuesta entre las diferentes dosis; sin embargo, el número de pacientes estudiado es bajo y no se observaron diferencias en la respuesta, entre las dosis y las fases de la enfermedad (cuadros V y VI).
Entre los factores predictivos de respuesta a rituximab, se ha informado que hay mejor respuesta en pacientes jóvenes,10 en especial en mujeres menores de 40 años, con una evolución de la enfermedad entre 12 y 24 meses.4,9,15,22,25,26 En este estudio, la mediana de la edad de nuestros pacientes con respuesta global, fuera que se encontraran en fase crónica o persistente, fue de 51 años y es probable que en nuestros pacientes la edad no fuera una limitante para obtener respuesta con este tratamiento.
El informe de Stasi et al.22 reportó que en cuatro pacientes con respuesta a rituximab y recaída subsecuente, al recibir un nuevo tratamiento con la misma dosis de rituximab dos de ellos nuevamente presentaron respuesta. Posteriormente, en un estudio de 20 pacientes en retratamiento con rituximab a dosis estándar, se observó una respuesta similar al primer tratamiento con rituximab en 75% de los pacientes. En general, la duración de respuesta con el primer y segundo tratamiento de rituximab fueron similares en aquellos pacientes que tuvieron categorías idénticas de respuesta a ambos tratamientos.27 En el presente estudio, observamos que seis/siete pacientes con antecedente de haber recibido tratamiento con rituximab lograron una nueva RC con el retratamiento. Por otro lado, en este estudio seis/siete pacientes que tenían esplenectomía lograron RC con rituximab; no obstante, otros estudios refieren que la esplenectomía no influye en la respuesta a rituximab.9,23
Sobre los efectos adversos con rituximab, su frecuencia está en ~ 19%, de los cuales el más frecuente es la intolerancia a rituximab durante la infusión en 15%, que ocurre principalmente durante la primera dosis, y son menores, como en el caso de la presencia de rash, náuseas, fiebre y escalofríos, entre otros. Las infecciones solo son observadas en 3%, entre dos y 18 meses después de la primera infusión de rituximab.28 En este estudio, solo cuatro pacientes (13%) presentaron reacciones adversas, principalmente durante la primera infusión de rituximab y todas fueron controladas. Con relación a la predisposición de infecciones, se observan con más frecuencia en pacientes inmunocomprometidos, con otras comorbilidades y relacionadas con el uso crónico de corticosteroides.2,28,29 En este estudio, solo dos pacientes (6.4%) presentaron infecciones, pero también fueron controladas; por lo tanto, en nuestro estudio los efectos indeseables, como la intolerancia, fueron parecidos a lo informado en la literatura, aunque la tasa de infecciones fue más alta.
Otros factores relacionados con la respuesta sostenida son la administración de rituximab en la fase persistente de la enfermedad y haber tenido RC con la administración de corticosteroides.28 En este estudio, de 27 pacientes con respuesta global, 24 tuvieron una respuesta sostenida hasta el final de la observación (12 meses), 21 estaban en RC (67%), tres estaban en RP (10%), 20 eran de fase crónica (64%) y cuatro de fase persistente (13%); de acuerdo con lo anterior, nuestros resultados mostraron que a pesar de estar en fase crónica, una buena cantidad de pacientes tuvieron una respuesta sostenida.
Mantenerse con respuesta sostenida permitió la modificación y el retiro de tratamientos concomitantes que eran usados como mantenimiento en los pacientes, lo cual fue muy bueno para ellos, ya que se redujeron los efectos secundarios de diferentes fármacos inmunosupresores y esto mejoró su calidad de vida. El rituximab puede considerarse como una opción terapéutica previa a la esplenectomía9 y en este estudio se pudo comprobar esto, ya que solo en tres pacientes (el 1 y el 11 con NR y el 6 con RP) fue necesario realizar dicha intervención, pero en otros 21 pacientes (68%), 16 en fase crónica y 5 en fase persistente, no fue necesario realizar la esplenectomía, por lo menos hasta la finalización de este estudio. En otros estudios ha sido necesaria la esplenectomía al año siguiente, después de la falta de respuesta al rituximab en un mayor número de pacientes, mientras que una buena respuesta al tratamiento evitó la esplenectomía durante dos años en 33% de pacientes.13
La diferencia de las cifras de plaquetas basales y al final del seguimiento fue muy significativa debido al tratamiento con rituximab, independientemente del tiempo de evolución de la TIP, lo cual refleja la utilidad de este tratamiento (figura 1).
Finalmente, y a propósito de la pandemia de COVID-19, una de nuestras pacientes, diagnosticada en marzo de 2020 (no incluida en este estudio), con TIP de reciente diagnóstico, tenía 54 años de edad, diabetes e hipertensión arterial; no tuvo respuesta al tratamiento de primera línea, por lo que se le empezó a administrar rituximab de forma semanal, cuatro dosis, y se logró la RC, pero dos semanas después de la última dosis de rituximab, tuvo infección por COVID-19, presentó neumonía y falleció. En pacientes con TIP negativos a COVID-19 y que se encuentren recibiendo AR-TPO, como primera línea de tratamiento, puede ser la opción preferida en lugar de los corticosteroides y si es urgente la elevación de plaquetas, la IgG IV, puede ser requerida,30 pero la utilización de AR-TPO en pacientes con TIP positivos a COVID-19 puede aumentar el riesgo de hepatotoxicidad y tromboembolismo, por lo que el tratamiento estándar con corticosteroides puede ser la opción preferida para el tratamiento inicial. Los corticosteroides en pacientes con TIP positivos a COVID-19, ya sea nuevos o en recaída, pueden ser la mejor opción.30
Con el tratamiento de rituximab existe el riesgo de inmunosupresión con la reactivación de algunos virus y también empeora la respuesta inmune humoral secundaria a la vacunación, por ejemplo anti-SARS-CoV-2; por otro lado, los pacientes con TIP también necesitan estar vacunados contra COVID-19; por lo tanto, se recomienda esperar al menos seis meses, después de recibir rituximab, para tener una vacunación efectiva y, si es posible, se debe diferir la terapia con rituximab durante la pandemia, dentro de lo razonable, y utilizarse de preferencia después de que los pacientes con TIP hayan sido vacunados contra COVID-19.30,31
Conclusiones
Nuestros resultados mostraron la utilidad del rituximab utilizado como rescate en pacientes adultos con TIP en fase persistente o crónica, que se encontraban en recaída y con el uso de corticosteroides y otros inmunosupresores. Se observó una respuesta favorable en la mayoría de los pacientes, con diferentes dosis del fármaco. La respuesta favorable con rituximab también se observó en pacientes de diferentes edades y tiempos de evolución de la enfermedad. El tratamiento con rituximab mostró una toxicidad aceptable y controlable; también fue de ayuda para evitar la esplenectomía en la mayoría de los pacientes durante todo el seguimiento. Consideramos que el rituximab usado como rescate es una buena alternativa de tratamiento en pacientes con TIP en fase persistente y crónica, y en los pacientes respondedores fue posible el retiro de tratamientos concomitantes, con sus efectos secundarios potenciales, lo cual mejoró su calidad de vida. En este estudio con pocos pacientes, se observó que el rituximab fue útil como retratamiento, igual a lo mencionado en otros reportes. Es difícil asegurar que la respuesta previa a la esplenectomía también pueda ser un indicador de nueva respuesta con el uso del rituximab, para lo cual se requieren más estudios al respecto. Finalmente, es necesario hacer más estudios controlados con rituximab para conocer las dosis más apropiadas para esta enfermedad y también su posible uso como mantenimiento.
Agradecimientos
A los doctores Natividad Neri y Alejandro Moctezuma por su apoyo en la realización de este trabajo.
Referencias
1. Rodeghiero F, Stasi R, Gernsheimer T, Michel M, Provan D, Arnold DM, et al. Standardization of terminology, definitions and outcome criteria in immune thrombocytopenic purpura of adults and children: report from an international working group. Blood. 2009;113(11):2386-93.
2. Provan D, Stasi R, Newland AC, Blanchette VS, Bolton-Maggs P, Bussel JB, et al. International consensus report on the investigation and management of primary immune thrombocytopenia. Blood. 2010;115(2):168-86.
3. Lambert MP, Gernsheimer TB. Clinical updates in adult immune thrombocytopenia. Blood. 2017;129(21):2829-35.
4. Lucchini E, Zaja F, Bussel J. Rituximab in the Treatment of Immune Thrombocytopenia: What Is the Role of This Agent in 2019? Hematologica. 2019;104(6):1124-35.
5. Zaja F, Baccarani M, Mazza P, Bocchia M, Gugliotta L, Zaccaria A, et al. Dexamethasone plus rituximab yields higher sustained response rates than dexamethasone monotherapy in adults with primary immune thrombocytopenia. Blood. 2010;115(14):2755-62.
6. Gudbrandsdottir S, Birgens HS, Frederiksen H, Jensen BA, Jensen MK, Kjeldsen L, et al. Rituximab and dexamethasone vs dexamethasone monotherapy in newly diagnosed patients with primary immune thrombocytopenia. Blood. 2013;121(11):1976-81.
7. Newland A, Godeau B, Priego V, Viallard JF, López Fernández MF, Orejudos A, et al. Remission and platelet responses with romiplostim in primary immune thrombocytopenia: final results from a phase 2 study. Br J Haematol. 2016;172(2):262-73.
8. Gómez-Almaguer D, Herrera-Rojas MA, Jaime-Pérez JC, Gómez-De León A, Cantú-Rodríguez OG, Gutiérrez-Aguirre CH, et al. Eltrombopag and high-dose dexamethasone as frontline treatment of newly diagnosed immune thrombocytopenia in adults. Blood. 2014;123(25):3906-8.
9. Cuker A, Neunert C. How I treat refractory immune thrombocytopenia. Blood 2016;128(12):1547-54.
10. Medeot M, Zaja F, Vianelli N, Battista M, Baccarani M, Patriarca F, et al. Rituximab therapy in adult patients with relapsed or refractory immune thrombocytopenic purpura: long-term follow-up results. Eur J Haematol. 2008;81(3):165-9.
11. Neunert C, Lim W, Crowther M, Cohen A, Solberg Jr L, Crowther MA; American Society of Hematology. The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia. Blood. 2011;117(16):4190-207.
12. Neunert C, Terrell DR, Arnold DM, Buchanan G, Cines DB, Cooper N, et al. American Society of Hematology 2019 guidelines for immune thrombocytopenia. Blood Adv. 2019;3(23):3829-66. doi: 10.1182/bloodadvances.2019000966.
13. Godeau B, Porcher R, Fain O, Lefrère F, Fenaux P, Cheze S, et al. Rituximab efficacy and safety in adult splenectomy candidates with chronic immune thrombocytopenic purpura: results of a prospective multicenter phase 2 study. Blood. 2008;112(4):999-1004.
14. Ghanima W, Khelif A, Waage A, Michel M, Tjønnfjord GE, Romdhanet NB, et al. Rituximab as second-line treatment for adult immune thrombocytopenia (the RITP trial): a multicentre, randomised, double-blind, placebo-controlled trial. Lancet. 2015;385(9978):1653-61.
15. Marangon M, Vianelli N, Palandri F, Mazzucconi MG, Santoro C, Barcelliniet W, et al. Rituximab in immune thrombocytopenia: gender, age, and response as predictors of long-term response. Eur J Haematol. 2017;98(4):371-7.
16. Zaja F, Vianelli N, Battista M, Sperotto A, Patriarca F, Tomadini V, et al. Earlier administration of rituximab allows higher rate of long-lasting response in adult patients with autoimmune thrombocytopenia. Exp Hematol. 2006;34(5):571-2.
17. Khellaf M, Charles-Nelson A, Fain O, Terriou L, Viallard JF, Cheze S, et al. Safety and efficacy of rituximab in adult immune thrombocytopenia: results from a prospective registry including 248 patients. Blood. 2014;124(22):3228-36.
18. Patel VL, Mahévas M, Lee SY, Stasi R, Cunningham-Rundles S, Godeau B, et al. Outcomes 5 years after response to rituximab therapy in children and adults with immune thrombocytopenia. Blood. 2012; 119(25):5989-95.
19. Arnold DM, Dentali F, Crowther MA, Meyer RM, Cook RJ, Sigouin C, et al. Systematic review: efficacy and safety of rituximab for adults with idiopathic thrombocytopenic purpura. Ann Intern Med. 2007;146(1):25-33.
20. Provan D, Arnold DM, Bussel JB, Chong BH, Cooper N, Gernsheimer T, et al. Update international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Advances 2019; 3 (22): 3780-817. DOI 10.1182/bloodadvances.2019000812.
21. Garcia-Chavez J, Majluf-Cruz A, Montiel-Cervantes L, Esparza MG, Vela-Ojeda J. Rituximab therapy for chonic and refractory immune thrombocytopenic purpura: a long-term follow-up analysis. Ann Hematol. 2007;86(12):871-7.
22. Stasi R, Pagano A, Stipa E, Amadori S. Rituximab chimeric anti-CD20 monoclonal antibody treatment for adults with chronic idiopathic thrombocytopenic purpura. Blood. 2001;98(4):952-7.
23. Cooper N, Stasi R, Cunningham-Rundles S, Feuerstein MA, Leonard JP, Amadori S, et al. The efficacy and safety of B-cell depletion with anti-CD20 monoclonal antibody in adults with chronic immune thrombocytopenic purpura. Br J Haematol. 2004;125(2):232-9.
24. Zaja F, Vianelli N, Volpetti S, Battista ML, Defina M, Palmieri S, et al. Low-dose rituximab in adult patients with primary immune thrombocytopenia. Eur J Haematol. 2010;85(4):329-34. doi: 10.1111/j.1600-0609.2010.01486.x
25. Bussel JB, Lee CS, Seery C, Imahiyerobo AA, Thompson MV, Catellier D, et al. Rituximab and three dexamethasone cycles provide responses similar to splenectomy in women and those with immune thrombocytopenia of less than two years duration. Haematologica. 2014;99(7):1264-71.
26. Chapin J, Lee CS, Zhang H, Zehnder JL, Bussel JB. Gender and duration of disease differentiate responses to rituximab–dexamethasone therapy in adults with immune thrombocytopenia. Am J Hematol. (2016);91(9):907-11.
27. Hasan A, Michel M, Patel V, Cunningham-Rundles S, Leonard JP, Bussel J. Repeated courses of rituximab in chronic ITP: three different regimens. Am J Hematol. 2009;84(10):661-5.
28. Khellaf M, Charles-Nelson A, Fain O, Terriou L, Viallard JF, Cheze S, et al. Safety and efficacy of rituximab in adult immune thrombocytopenia: results from a prospective registry including 248 patients. Blood. 2014;124(22):3228-36.
29. Chugh S, Darvish-Kazem S, Lim W, Crowther MA, Ghanima W, Wang G, et al. Rituximab plus standard of care for treatment of primary immune thrombocytopenia: a systematic review and meta-analysis. Lancet Haematol. 2015;2(2):e75-81.
30. Pavord S, Thachil J, Hunt BJ, Murphy M, Lowe G, Laffan M, et al. Practical guidance for the management of adults with immune thrombocytopenia during the COVID-19 pandemic. Br J Haematol 2020. doi: 10.1111/bjh.16775
31. Houot R, Levy R, Cartron G, Armand P. Could anti-CD20 therapy jeopardise the efficacy of a SARS-CoV-2 vaccine? Eur J Cancer. 2020;136:4‑6. doi: 10.1016/j.ejca.2020.06.017
Notas de autor
Comunicación con: Guillermo Rodolfo Gutiérrez Espíndola Teléfono: 55 5627 6900, extensión 21406
Información adicional
Declaración de conflicto de interés:: los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno relacionado con este artículo.
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/4560/4480 (pdf)
