Investigación
Una aproximación eco hidrológica de un campo experimental de pozos en el karst de Yucatán.
Hydroecological approach for an experimental field of wellsin Yucatan karst
Una aproximación eco hidrológica de un campo experimental de pozos en el karst de Yucatán.
Ingeniería, vol. 23, núm. 1, pp. 24-39, 2019
Universidad Autónoma de Yucatán

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 26 Noviembre 2018
Aprobación: 30 Enero 2019
Resumen: El campo experimental de pozos de la FIUADY es un sistema de pozos de 50 m y hasta 75 m de profundidad. Se construyó con la finalidad de confrontar y consolidar el conocimiento hidrológico del agua subterránea en la planicie kárstica del norte de Yucatán. En este contexto el objetivo de este trabajo es documentar el comportamiento histórico de algunas variables del ambiente físico- químico y biológico del acuífero para bosquejar modelos del hábitat de la microbiota del epikarst en la planicie norte de la península de Yucatán. Se documentó la conformación hidrogeológica con análisis de detritos de la perforación y utilizando video subacuático en los pozos; se hicieron mediciones de temperatura, conductividad eléctrica, pH y oxígeno disuelto en octubre, noviembre, enero, febrero, marzo y abril de diferentes años. Para los análisis estadísticos se agruparon los datos en dos períodos: recarga (octubre y noviembre) y descarga (enero-abril). Los resultados incluyen un perfil hidrogeológico esquemático y los análisis estadísticos de las variables. Los valores mínimos y máximos observados son: temperatura °C (26.64,29.87), conductividad eléctrica µS/cm (465,46800), pH (6.14,8.20) y oxígeno disuelto mg/L (0.01, 7.93); se concluye que: a) en un área de pocos metros cuadrados hay variaciones importantes en las características hidrogeológicas, b) el comportamiento hidrogeológico de los pozos tiene que ver con horizontes kársticos ; sus dimensiones, conectividad, distribución, densidad y la forma como influye ante diversos esfuerzos hidrológicos y finalmente c) la presencia de crustáceos en los pozos y “anomalías” en la concentración de oxígeno puede tener una explicación en procesos biogeoquímicos de ecosistemas oscuros.
Palabras clave: ambiente karstico, hábitat oscuro, planicie kárstica, acuífero de Yucatán.
Abstract: The FIUADY experimental field of wells is a system of 50 m and up to 75 m deep boreholes. It was built with the purpose of confronting and consolidating the hydrological knowledge ofgroundwater in the karst plain of northern Yucatan. In this context, the objective of this work is to document the historical behavior of some variables of the physico-chemical and biological environment of the aquifer to sketch models of the habitat of the microbiota of the epikarst in the northern plain of the Yucatan peninsula. The hydrogeological conformation was documented with drilling debris analysis and using underwater video in the wells; Measurements of temperature, electrical conductivity, pH and dissolved oxygen were made in October, November, January, February, March and April of different years. For the statistical analyzes, the data were grouped into two periods: recharge (October and November) and discharge (January-April). The results include a schematic hydrogeological profile and the statistical analysis of the variables. The minimum and maximum values observed are: temperature ° C (26.64,29.87), electrical conductivity μS/cm (465,46800), pH (6.14,8.20) and dissolved oxygen mg / L (0.01, 7.93); it is concluded that: a) in an area of few square meters there are important variations in the hydrogeological characteristics, b) the hydrogeological behavior of the wells has to do with karst horizons; its dimensions, connectivity, distribution, density and the way it influences various hydrological efforts and finally c) the presence of crustaceans in the wells and "anomalies" in the concentration of oxygen can be explained in biogeochemical processes of dark ecosystems.
Keywords: karst environment, dark habitat, karstic plateou, Yucatan aquifer.
Introducción
En el Karst de la Península de Yucatán tienen lugar hábitats de comunidades biológicas muy diversas: desde los visibles montes (selvas, praderas, humedales) y ciudades que se asientan sobre las planicies y formaciones kársticas, pasando por las asociaciones de animales todavía observables en las cavernas (secas e inundables), hasta grupos prácticamente imperceptibles a la visión humana, ya que habitan dentro de pasajes inaccesibles al hombre y que forman parte de intrincadas redes cavernosas inundadas de origen calcáreo.
La interacción entre estos sistemas biológicos es dinámica, de tal modo que las selvas del karst superficial aportan al subsuelo materia y energía mediante procesos como la infiltración del agua al acuífero (pluvial, riego, etc.) y del subsuelo el monte toma materia y energía: iones y enlaces químicos producto de la actividad biológica. (Pacheco y Cabrera 1997, Pacheco et al. 2000, Pacheco et al. 2001, Cervantes-Martínez et al. 2002, Herrera-Silveira et al. 2002, Xuluc- Tolosa et al. 2003, Hodell et al. 2005, Vargas- Ramos 2007, Hernández-Terrones et al. 2011,Bauer et al. 2011, Pérez et al. 2011, Pérez- Ceballos et al. 2012).
Las formaciones kársticas superficiales (epikarst), visibles (incluyendo cavernas), han sido objeto de estudios desde una perspectiva biológica y ecosistémica (Schmitter-Soto et al. 2002; Bauer-Gottwein et al. 2011, Herrera- Silveira et al. 2002; Pérez et al. 2011, Pérez- Ceballos et al. 2012); sin embargo, existen otras regiones del karst subterráneo que no son accesibles a la exploración directa por el ser humano y que se ha estudiado menos (Bastviken et al. , 2002; Engel 2007, Por 2008, Pronk et al. 2009, Plach et al. , 2011, Staehr et al. 2012, Okafor 2011), porque en su estado natural son inaccesibles a la visión humana, y sólo mediante alguna modificación del espacio físico como la perforación de un pozo y/o la observación con instrumentos, puede generarse conocimiento de estos complejos ecosistemas.
Las comunidades humanas, y particularmente las ciudades, cambian los equilibrios y la dinámica misma de los subsistemas biológicos y ambientales. No solo por la concentración, en espacios reducidos, de agua, alimentos, materia diferente a la que ocurre en los montes o ecosistemas naturales, sino por los desechos y la actividad humana orientada a la máxima productividad económica mediante la industrialización o uso masivo de recursos naturales locales (Hildebrand et al. 1995; Perry et al. 1995, Pope et al. 1996, Graniel- Castro y González-Hita 2002, Hernández- Terrones et al. 2011).
El campo experimental de pozos del Campus de Ingeniería y Ciencias Exactas de la Universidad Autónoma de Yucatán se construyó con el objeto de confrontar y consolidar el conocimiento teórico del comportamiento hidrológico del agua subterránea en la planicie kárstica del norte de Yucatán; en la actualidad ha favorecido la formación académica de estudiantes de ingeniería y ha permitido contribuciones del conocimiento científico del karst yucateco (Sánchez y Pinto et al. 2005). El objetivo de este trabajo es documentar el comportamiento histórico de algunas variables del ambiente físico-químico y biológico del acuífero, a través del monitoreo y análisis de éstas variables medidas y registradas en el campo experimental de pozos del Campus de Ciencias exactas e ingeniería (UADY) para bosquejar modelos del hábitat de la microbiota del epikarst en la planicie norte de la Península de Yucatán y estudiar procesos biogeoquímicos del acuífero kárstico.
Método
1.- Área de estudio
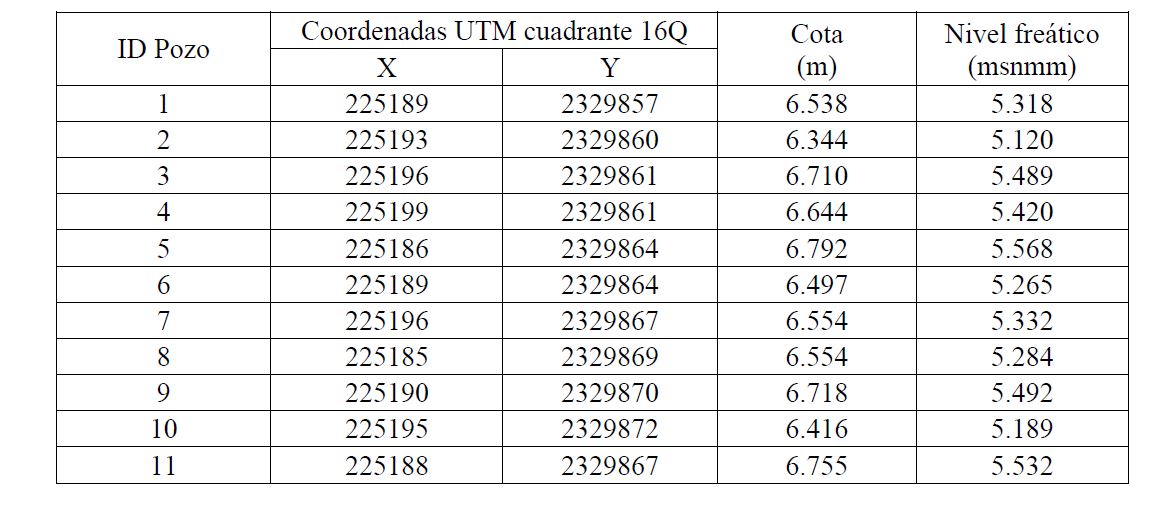
El campo experimental hidrogeológico (CEH) de pozos se encuentra al norte de la ciudad de Mérida, la ubicación geográfica se obtuvo con GPS y mediante levantamientos topográficos con una estación total; localización, cota y altura sobre el nivel medio del mar en metros (modelo de Geoide WGS84) de cada pozo (Tabla 1).
2.- Perfil hidrológico y arquitectura del hábitat físico del epikarst
Para la descripción física y litológica del área de estudio se usaron dos fuentes de información: a) Durante la perforación de los pozos de este campo experimental se tomaron muestras de detritos de los cuales se hicieron inferencias sobre la composición litológica de los diferentes estratos. b) Se tomaron videos con una cámara submarina modelo R-Cam 1000 con registro de la profundidad de las tomas.
3.- Condiciones hidrológicas
Las mediciones de las condiciones atmosféricas se hicieron mediante una estación meteorológica automatizada situada a 50 m del campo experimental de pozos. Las mediciones del ambiente físico químico del agua subterránea en el área del Campo experimental de pozos se realizaron en 2003 (febrero-abril), 2004 (enero), 2008 (noviembre) y 2014 (octubre). Los equipos utilizados fueron sondas multiparamétricas Hidrolab Quantum.
En el mes de noviembre de 2008, se realizaron mediciones de temperatura (°C), conductividad eléctrica (μS/cm), pH, Oxígeno Disuelto(mg/L) y Potencial Rédox (mV). Las mediciones se hicieron en 9 pozos a intervalos de profundidad de 1 m (la primera medición a20 cm por debajo del nivel freático); las mediciones iniciaron a las 9:40 am y finalizaron a las 15:30 (un período de 5:50 h).El estadístico de tendencia central evaluado en las variables observadas en el campo experimental de pozos fue la mediana, y lavariación se registró mediante el registro de mínimos y máximos en el período de medición.
En Octubre de 2014 se realizaron mediciones de temperatura, pH, conductividad eléctrica, oxígeno disuelto, potencial rédox y clorofilas; estas mediciones se hicieron hasta una profundidad de 20 m, entre las 7:30 AM y 12:30 PM.
Los datos fueron agrupados en dos épocas:
-
Recarga que incluye los meses deoctubre y noviembre y
-
Descarga que incluye los meses de enero, febrero, marzo y abril.
Para el análisis estadístico (descriptivo y gráfico) se utilizaron herramientas de EXCEL así como del entorno para análisis estadístico R-Project y StatGraphics CENTURION 18.
Resultados
En la Figura 1 se presentan la distribución de los pozos en un plano horizontal y un corte vertical del campo experimental de pozos (perfil hidrogeológico) en el que se esquematizan las regiones karstificadas del acuífero. En total, 11 son los pozos construidos para experimentación, uno de ellos con una profundidad de 70 m.
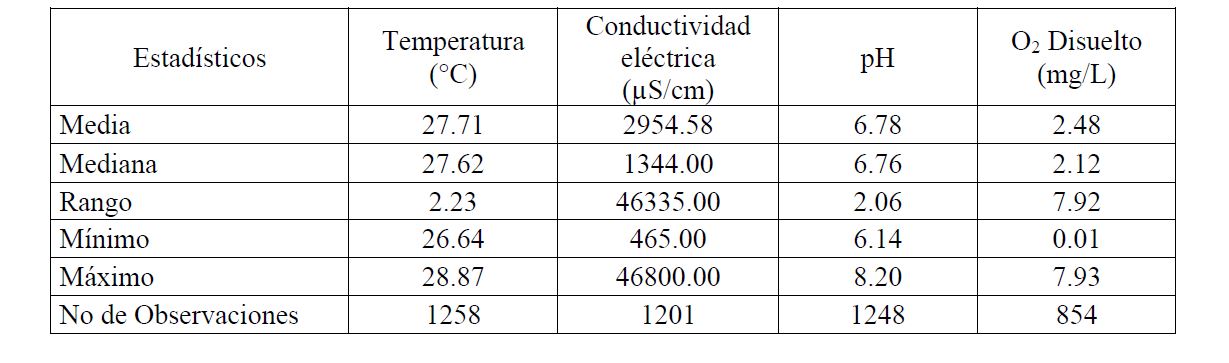
Los valores estadísticos de las variables físico- químicas se presentan en la Tabla 2; los parámetros estadísticos estimados fueron: la Media, Mediana, Rango, Máximo, Mínimo y Número de observaciones realizadas en el Campo experimental de pozos..
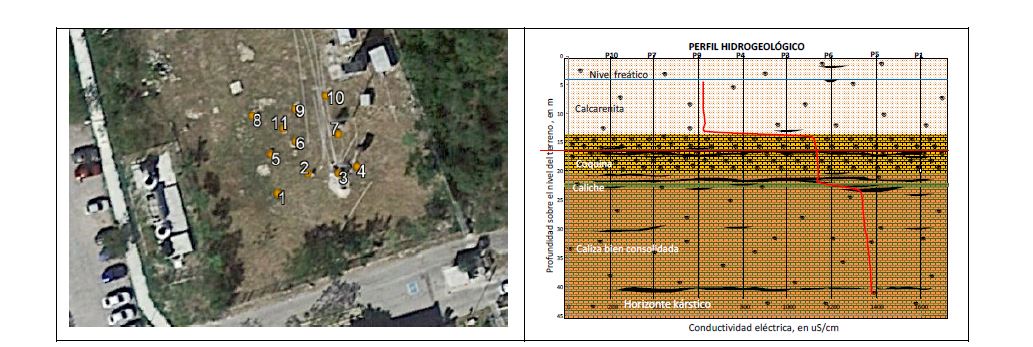
Figura 1
Ubicación de pozos y perfil hidrogeológico del CEH
En la Figura 2, se muestra la estratificación de la Temperatura en mediciones realizadas tanto en épocas de máxima y mínima recarga; es notable la amplia variación de la temperatura en las aguas superficiales y conforme se incrementa la profundidad disminuye la variabilidad; las temperaturas están entre 26.5° C y 29°C.
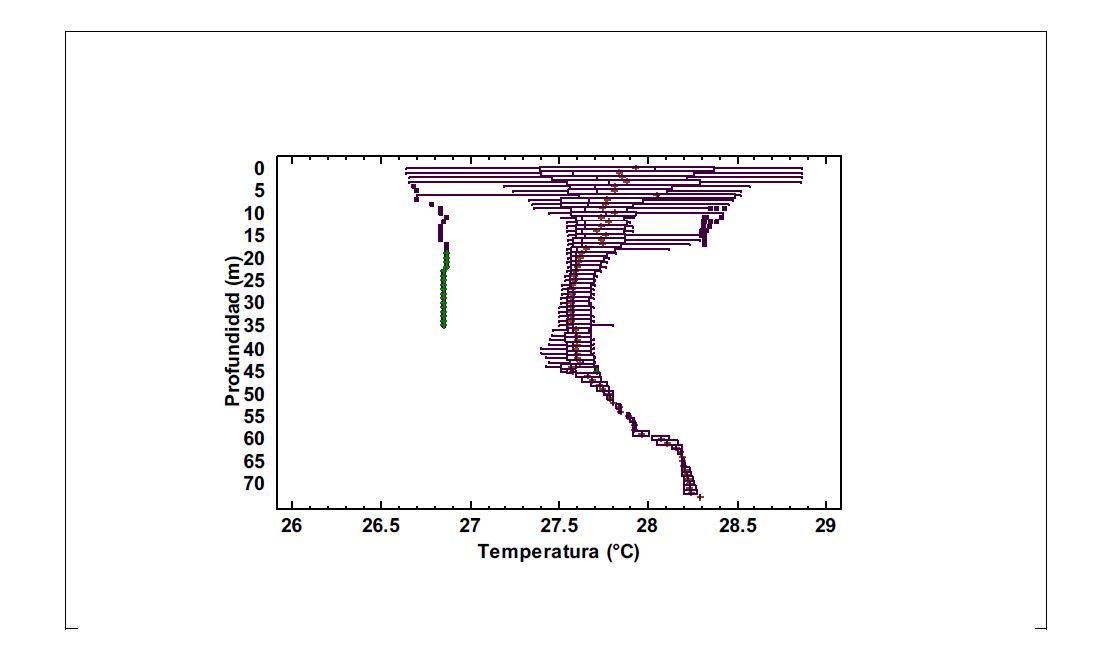
Figura 2
Distribución vertical de la Temperatura medida en °C en el Campo experimental depozos
En la Figura 3 se presenta, mediante un gráfico de cajas y bigotes, la distribución de los valores de temperatura en la época de máxima (recarga) y mínima recarga (descarga) del acuífero; en los meses de recarga (octubre- noviembre) la temperatura es más elevada y con menor dispersión.
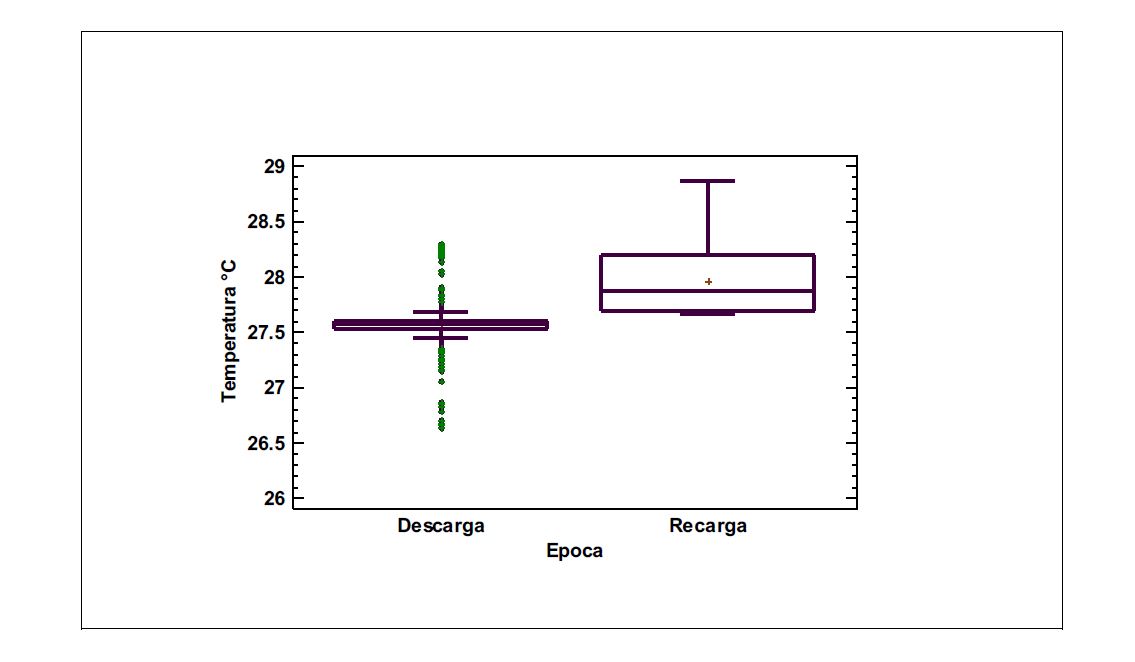
Figura 3
Gráfico de la dispersión de las mediciones de temperatura (°C) en el campo experimental de pozos. La descarga corresponde a los meses de enero a abril y la recarga a octubre y noviembre
La Conductividad eléctrica muestra un arreglo vertical (Figura 4) en el que, en los primeros 10 m de profundidad hay poca variación y los valores se mantienen bajos (465 µS/cm) hasta los 46 m en dónde se presenta una transición hasta alcanzar conductividades eléctricas muy elevadas (>40000 µS/cm).}
En términos generales la conductividad eléctrica es baja (<1500 µS/cm), a excepción de los valores altos que se tienen en aguas por debajo de los 45 m, la Figura 5 muestra la distribución de los valores de conductividad eléctrica de las épocas de descarga y recarga mediante un gráfico de cajas y bigotes.
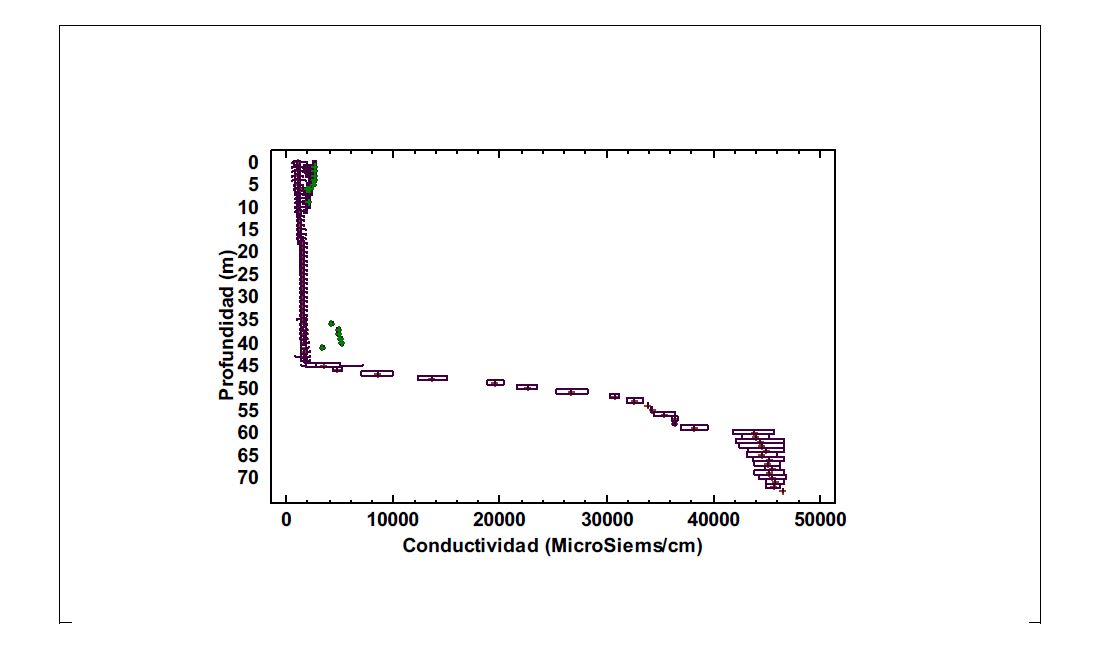
Figura 4
Perfil de conductividad eléctrica en el Campo Experimental de pozos
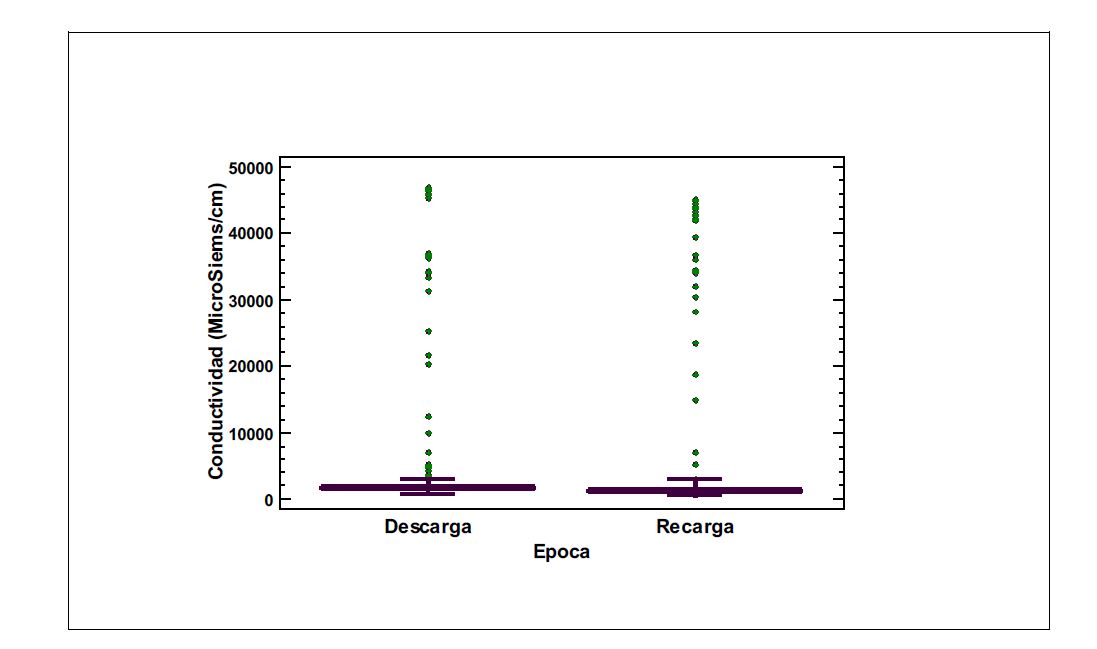
Figura 5
Gráfico de Cajas y Bigotes de las mediciones de Conductividad eléctrica en µS/cm medidas en las épocas de máxima recarga (Recarga) y mínimo nivel del acuífero (Descarga).
El pH del agua del acuífero en el Campo Experimental de pozos muestra una estratificación que se presenta en la Figura 6.
En la Figura 7 se presenta el comparativo de los valores de pH medidos durante la época de descarga y recarga; el pH durante la época de recarga es más ácido y más variable que durante la época de descarga o mínimo nivel del acuífero.
Una Variable importante en el metabolismo de los ecosistemas acuáticos es la concentración de oxígeno disuelto; en la Figura 8 se presenta un perfil vertical en el que son notables los valores altos en la superficie y condiciones de muy bajas concentraciones de oxígeno disuelto a profundidades mayores a los 6 m.
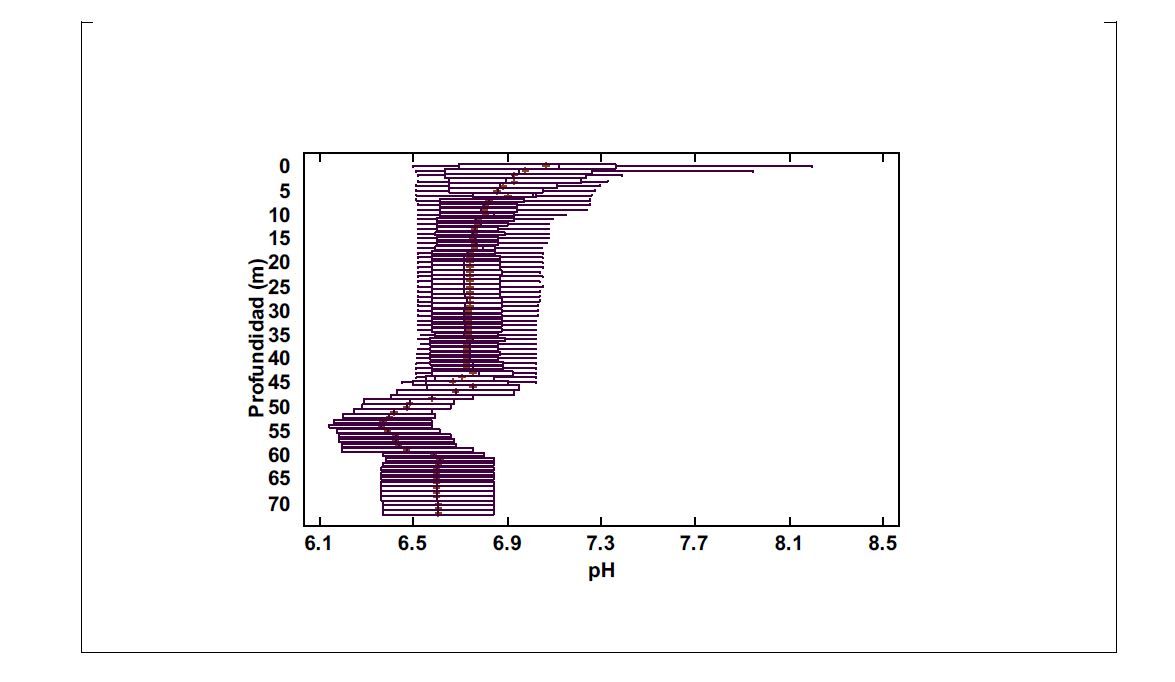
Figura 6
Perfil de mediciones de pH en el que se observa una estratificación con cambios en los15 y 45 m de profundidad
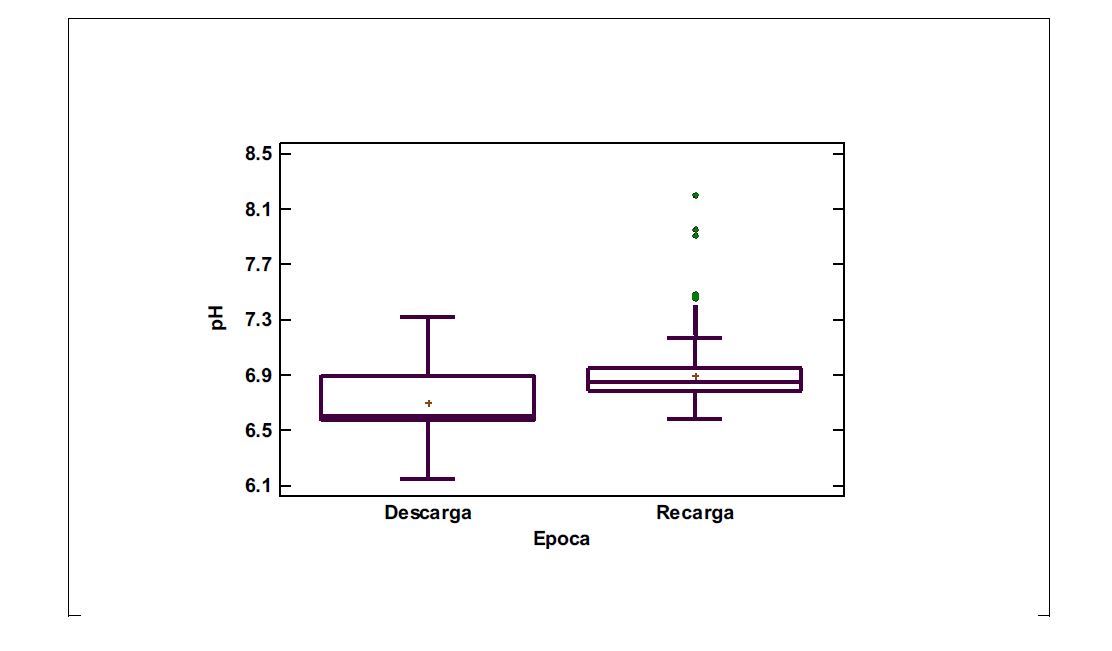
Figura 7
Gráfico comparativo de las mediciones de pH en el Campo Experimental de pozosdurante las épocas de Descarga y Recarga (máximo nivel del acuífero)
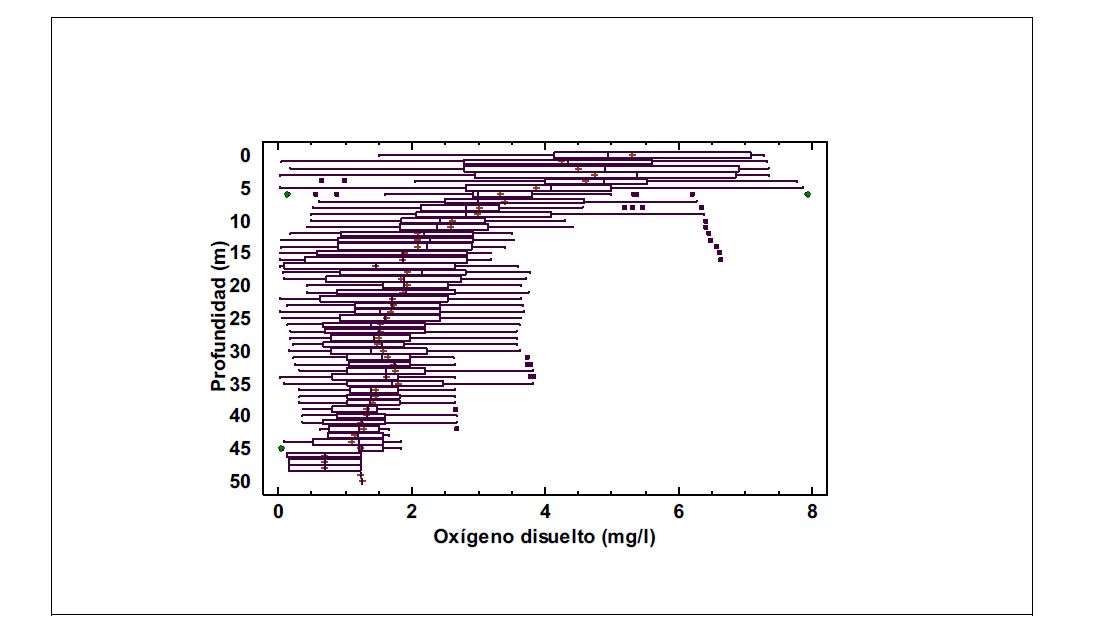
Figura 8
Perfil vertical de las mediciones de oxígeno disuelto en mg/L realizadas en el campoexperimental de pozos
Por otra parte las concentraciones de oxígeno disuelto son menores durante la época derecarga que durante la época de descarga y esto puede apreciarse en la Figura 9.
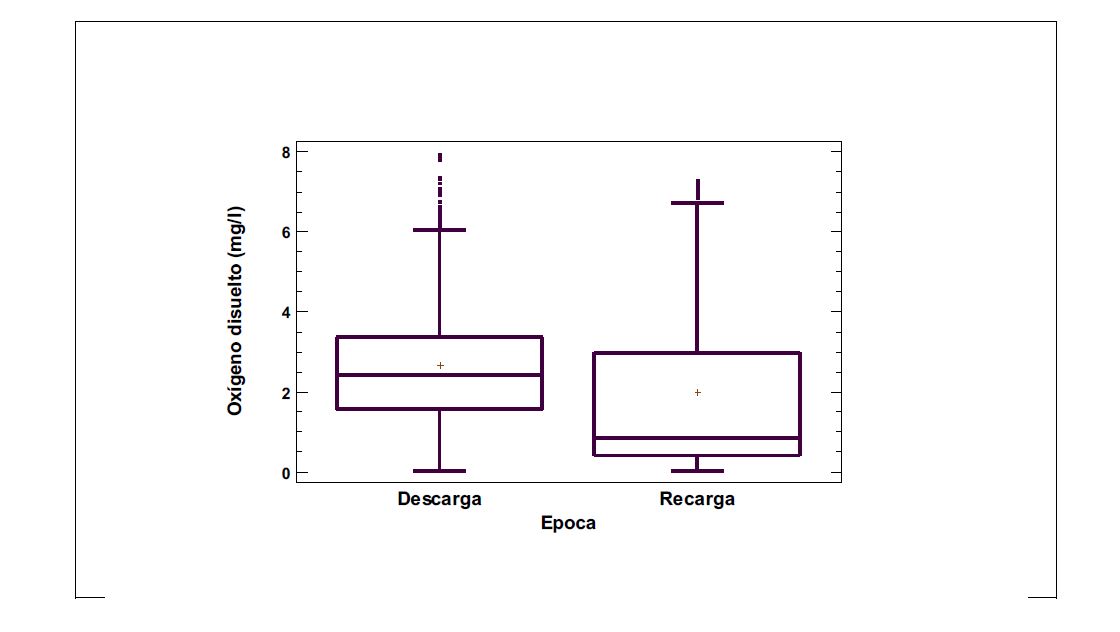
Figura 9
Comparativo de las concentraciones de oxígeno disuelto en el Campo Experimental dePozos durante las épocas de descarga y recarga del acuífero
En los videos subacuáticos se observaron crustáceos a los 42 m a los 43 m y a los 51.6 m de profundidad. La identificación de los organismos sólo permite el nivel de grupo. Sin embargo, los reportes de macrocrustáceos en los sistemas acuáticos epicontinentales de la península de Yucatán incluyen Agostocaris bozanci, Yagerocaris cozumel, Janicea antiguensis, Calliasmata nohochi (Escobar- Briones et al. 1997) Procaris no descrito ( Kornicker e Iliffe 1992) y el ripedia Speleonectes tulumensis (Smitter-Soto et al. 2002). En la Figura 10 se presenta una fotografía extraída de uno de los videos a 42.2 m de profundidad.

Figura 10
Fotografía subacuática de macro crustáceos que habitan el epikarst en lasinmediaciones del campo experimental de pozos de la FIUADY
Discusión
El campo experimental de pozos es una ventana desde la que se puede observar al ecosistema del acuífero que tiene lugar en el epikarst subterráneo; su estructura litológica y la arquitectura de sus expresiones cársticas (cavidades) muestran una gran complejidad y se manifiesta en las observaciones: tanto en los componentes que aparecieron en los detritos (durante la perforación de los pozos) como en las imágenes de video en las que pudieron apreciarse tres horizontes kársticos (estratos horizontales con presencia de cavidades) cuya conectividad horizontal, de alguna manera ha sido evaluada mediante pruebas con trazadores y pruebas de bombeo (Sánchez y Pinto et al. 2005, Zetina-Moguel et al. 2007, Gutiérrez- Díaz 2011).
La construcción de los pozos en el campo experimental conectó verticalmente los diferentes horizontes cársticos y esto de alguna manera encubre los comportamientos hidrogeológicos (combinó las diferentes presiones hidrostáticas correspondientes a los horizontes kársticos), biogeoquímicos (permite el intercambio de componentes químicos y de origen biológico) y biológicos (permite o facilita el paso de organismos entre horizontes cársticos, en migraciones verticales); no obstante brinda la posibilidad de inferir con base en las observaciones sobre los diferentes procesos del ecosistema que se desarrolla en esta zona oscura del karst.
Aunque en el campo experimental de pozos no se han realizado campañas de medición de iones, ni evaluaciones microbiológicas, existen mediciones realizadas en un pozo de monitoreo de la CONAGUA situado en la misma zona de estudio; en este pozo se realizaron determinaciones de iones a dos profundidades (20 y 50 m) y en los meses de Febrero y Octubre (Heise 2013). Algunas de estas determinaciones se presentan en la Tabla 3.
Heise (2013) publica también datos de la composición iónica de pozos situados alrededor de la ciudad de Mérida (25 pozos), incluyendo el pozo de CONAGUA que se encuentra a un lado del Campo Experimental. En la Tabla 4 se presenta un resumen estadístico de estas determinaciones. Y en la Tabla 5 se presenta un resumen estadístico de las determinaciones de coliformes fecales y totales realizadas por Heise (2013) en pozos de la ciudad de Mérida entre 10 y 50 m de profundidad.
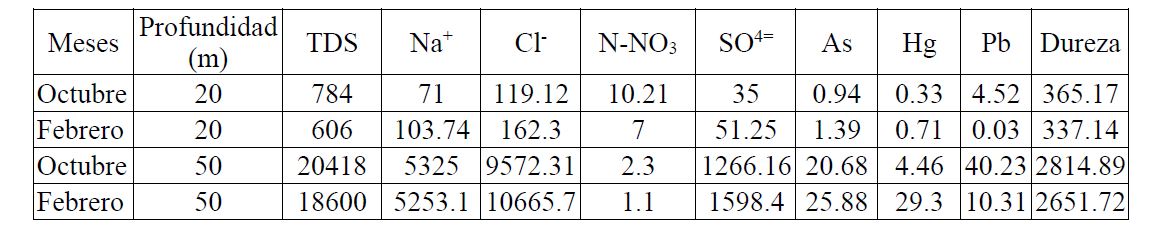
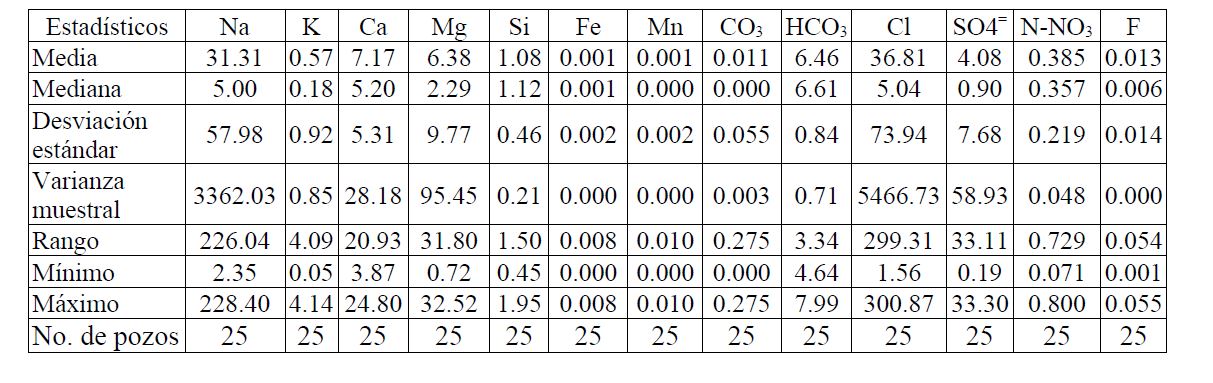
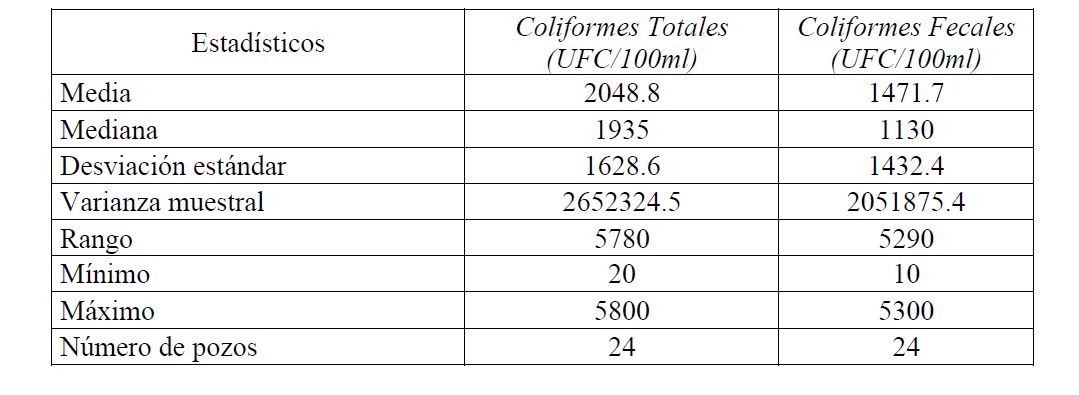
Esta composición química reportada, de alguna manera muestra el ambiente físico-químico (temperatura, conductividad eléctrica, pH, O2) químico (composición iónica: aniones y cationes) y microbiológico (Coliformes: grupos microbiológicos asociados a los organismo homeotermos) que se puede esperar en el campo experimental de pozos. De los datos experimentales previamente publicados relacionados a los sistemas acuáticos del epikarst (Heise 2013 y Moore 2014), se desprende que el análisis de la estratificación vertical en el campo de pozos puede ser de gran importancia (conocimiento y tecnología de gestión del acuífero).
Basta abordar un tema de mediciones en aguas subterráneas (en pozos), y en sistemas abiertos (cenotes): tanto en pozos como en sistemas abiertos se han observado incrementos en la concentración de oxígeno en aguas profundas (40 m y 50 m de profundidad) de 1 mg/L a aproximadamente 3 mg/L (Heise 2013), y aunque la explicación se ha buscado en procesos físicos, hoy se sabe que existe producción de oxígeno por quimiosíntesis en sistemas oscuros (Ettwing et al. 2012) y esta es otra posibilidad de una fuente de oxigenación del acuífero kárstico.
En el campo experimental de pozos de la Facultad de Ingeniería se hicieron observaciones de crustáceos a profundidades de 42.2 m, 43 m y 51.6 m. Los artrópodos son especialmente sensibles a contaminantes antropogénicos, y su existencia a esas profundidades en el campo experimental de pozos (que es un sistema alejado de un cenote u otro ecosistema acuático abierto o expuesto a la luz y los procesos fotosintéticos) sólo puede explicarse por la presencia de materia orgánica alóctona (detritos y desechos de la fotosíntesis) y/o autóctona procedente de quimiosíntesis en los sistemas oscuros del epikarst así como otros procesos que forman parte de los ciclos biogeoquímicos del karst y que han permanecido ocultos a la observación.
Conclusiones
En un área de pocos metros cuadrados (distancia mínima de 3 m y máxima de 16.2 m entre pozos) y una profundidad de 50 y 75 m, pueden encontrarse variaciones importantes en los comportamientos físico-químicos del agua subterránea como resultado de la conexión de los pozos con los horizontes kársticos atravesados, estableciendo así una conexión vertical entre ellos.
El comportamiento hidrogeológico de los pozos tiene que ver con horizontes kársticos de diferente conectividad y en muchos casos permite la presencia y posibilidad de observar microorganismos.
La presencia de crustáceos en los pozos y las “anomalías” en la concentración de oxígeno disuelto con respecto a la profundidad puede tener una explicación en procesos biogeoquímicos de ecosistemas oscuros.
Agradecimientos
Se agradece al Programa de Apoyo y Consolidación de Cuerpos Académicos (PADECCA) de la Coordinación General de Posgrado, Investigación y Vinculación de la Universidad Autónoma de Yucatán por el apoyo brindado para llevar a cabo actividades de investigación por los integrantes del Cuerpo Académico de Hidráulica e Hidrología de la Facultad de Ingeniería.
Referencias
Bastviken D., Ejlertsson J. And L . Tranvik . 2002. Measurement of Methane Oxidation in Lakes: A Comparison of Methods. Environ. Sci. Technol. 36, 3354-3361
Bauer-Gottwein P., B. R. N. Gondwe, G. Charvet, L. E. Marín, M. Rebolledo-Vieyra, G. Merediz- Alonso. 2011. Review: The Yucatán Peninsula karst aquifer, Mexico. Hydrogeology Journal 19: 507–524
Cervantes-Martínez, A., Elías-Gutiéerrez, M. y Suárez.Morales, E. 2002. Limnological and morphometrical data of eight karstic systems “cenotes” of the Yucatan Peninsula, Mexico, during the dry season (February–May, 2001). Hydrobiologia 482: 167-177.
Engel A.S. 2007. Observations on the Biodiversity of Sulfidic Karst Habitats. Journal of Cave and Karst Studies V. 69, no. 1, p. 187–206.
Escobar-Briones, E., M. E. Camacho, and J. Alcocer. 1997. Calliasmata nohochi, new species (Decapoda: Caridea: Hippolytidae), from anchialine cave systems in continental Quintana Roo, Mexico. J. Crust. Bio.17(4):733-744.
Ettwing K.F. , Speth D. R., Reimann J., Wu M.L ., Jetten M.S.M and J. T. Keltjens. 2012. Bacterial oxygen production in the dark. Hypothesis and theory article. Hypothesis and Theory ARTICLE
Graniel-Castro E. y González-Hita 2002. Deterioro de la calidad del agua subterránea por el desarrollo poblacional Cancún Q.Roo. Ingeniería 6 (3): 41-53.
Gutiérrez-Díaz S. 2011. Estudio del coeficiente de dispersión en el acuífero cárstico de porosidad dual de Yucatán. Tesis de Maestría. Facultad de Ingeniería, Universidad Autónoma de Yucatán. Mérida, México.
Heise L. 2013. Dynamics of the coastal karst aquifer in northern Yucatán peninsula. Thesis To Obtain The Degree Of Maestría en Ciencias Ambientales Degree Awarded By Universidad Autónoma de San Luis Potosí And Master Of Science Technology And Resources Management In The Tropics And Subtropics In The Specialization: Resources Management Degree Awarded By Cologne University Of Applied Sciences.
Herrera-Silveira J., Medina-Gomez I. & R. Colli. 2002. Trophic status based on nutrient concentration scales and primary producers community of tropical coastal lagoons influenced by groundwater discharges. Hydrobiologia 475/476: 91–98.
Hildebrand, A.R., Pilkington, M., Connors, M., Ortiz-Aleman, C., Chavez, R.E., 1995. Size and structure of the Chicxulub crater revealed by horizontal gravity gradients and cenotes. Nature 376, 415– 417.
Hodell D.A., Brenner M.,Curtis J.H., Medina-González R., Chan-Can E.I., Albornaz-Pat A. and T.P. Guilderson. 2005. Climate change on the Yucatan Peninsula during the Little Ice Age. Quaternary Research 63: 109– 121
Kornicker, L. S.; Iliffe, T. M. (1992). Ostracoda (Halocypridina, Cladocopina) from anchialine caves in Jamaica, West Indies. Smithsonian Contributions to Zoology. 530, 1-22., available online at https://doi.org/10.5479/si.00810282.530
Moore A. 2014. Characterization of the Native Microbial Communities in the Karst Aquifer of Yucatan Peninsula, Mexico. A DISSERTATION SUBMITTED TO THE GRADUATE SCHOOL IN PARTIAL FULFILLMENT OF THE REQUIREMENTS FOR THE DEGREE DOCTOR OF PHILOSOPHY. NORTHERN ILLINOIS UNIVERSITY DEKALB, ILLINOIS.
Okafor N. 2011. Environmental Microbiology of Aquatic and Waste Systems. Springer Dordrecht Heidelberg London New York.
Pacheco, J., & Cabrera, A. 1997. Groundwater contamination by nitrates in the Yucatan Peninsula, Mexico. Hydrogeology Journal 5, 47–53.
Pacheco, A., Cabrera, J. A., & Marin, L. E. 2000. Bacteriological contamination assessment in the karstic aquifer of Yucatan, Mexico. Geofísica Internacional 39, 285–291.
Pacheco, A., Cabrera, J. A., & Marin, L. E. 2001. Nitrate temporal and spatial patterns in twelve water supply wells, Yucatan, Mexico. Environmental Geology 40, 708–715.
Pérez L., Bugja R., Lorenschat J., Brenner M., Curtis J., Hoelzmann P., Islebe G., Scharf B. and A. Schwalb. 2011. Aquatic ecosystems of the Yucatán Peninsula (Mexico), Belize, and Guatemala. Hydrobiologia 661:407–433.
Pérez-Ceballos, R. Pacheco-Ávila, J. Euán-Ávila, J. I, Hernández-Arana, H. 2012. Regionalization based on water chemistry and physicochemical traits in the ring of cenotes, Yucatan, exico. Journal of Cave and Karst Studies, 74(1), 90-102. doi:10.4311/2011es0222.
Perry, E.C., Marin, L.E., McClain, J., Velazquez, G., 1995. The ring of cenotes (sinkholes) northwest Yucatan, Mexico: its hydrogeologic characteristics and association with the Chicxulub impact crater. Geology 23, 17– 20.
Plach, J.M., Elliott, A.V.C., Droppo, I.G., Warren, L.A., 2011. Physical and ecological controls on freshwater floc trace metal dynamics. Environ. Sci. Technol. 45 (6), 2157–2164.
Por F.D. 2008. Deuterobiosphere the Chemosynthetic Second Biosphere of the Globe. A First Review. Integrative. Zoology 3: 101–114.
Pope, K.O., Ocampo, A.C., Kinsland, G.L., Smith, R., 1996. Surface expression of the Chicxulub crater. Geology 24, 527–530.
Pronk M., Goldscheider N., and J. Zopfi. 2009. Microbial communities in karst groundwater and their potential use for biomonitoring. Hydrogeology Journal 17: 37–48.
Sánchez y Pinto I., González-Herrera R. y E. Perry. 2005. Hidrodinamic behavior of the yucatan aquifer. A perspective on the hydraulic conductivity estimation. Espeleo@digital 2 Ciudad de la Habana, Cuba. Pág. 8-20.
Schmitter-Soto J.J., Comín F.A., Escobar-Briones E., Herrera-Silveira J., Alcocer J., Suárez- Morales E., Elías-Gutiérrez M., Díaz-Arce V., Maín L.E. and B. Steinch. 2002. Hydrogeochemical and biological characteristics of cenotes in the Yucatan Peninsula (SE Mexico). Hydrobiologia 2002;467:215–28.
Staehr, P.A., Testa, J.M., Kemp, W.M., Cole, J.J., Sand-Jensen, K., Smith, S.V., 2012. The metabolism of aquatic ecosysteµS: history, applications, and future challenges. Aquatic Sciences 74, 15–29.
Xuluc-Tolosa F.J., Vester H.F.M., Ramırez-Marcial N., Castellanos-Albores N., and D. Lawrence. 2003. Leaf litter decomposition of tree species in three successional phases of tropical dry secondary forest in Campeche, Mexico. Forest Ecology and Management 174 (2003) 401–412.
Vargas-Ramos R. 2007. Carbon Dynamics in a Seasonally Dry Tropical Forest. A Dissertation submitted in partial satisfaction of the requirements for the degree of Doctor of Philosophy In Environmental Sciences. UNIVERSITY OF CALIFORNIA RIVERSIDE USA.
Zetina-Moguel C., R. Medina-González, I. Sánchez-Molina, L. Chumba-Segura y J. Alonzo- Salomón. 2007. Hacia una Perspectiva Para Definir Criterios de Salud de los Cenotes de Yucatán. Memorias del Primer Encuentro de Investigación Científica y Tecnológica del Sistema Hidrológico de Yucatán 1:23. Mérida.
Hernández-Terrones L., Rebolledo-Vieyra M., Merino-Ibarra M., Soto M, Le-Cossec A. y E. Monroy-Ríos. 2011. Groundwater Pollution in a Karstic Region (NE Yucatan): Baseline Nutrient Content and Flux to Coastal Ecosystems. Water Air Soil Pollution 218:517–528.
Información adicional
*: Este artículo de Investigación es parte de Ingeniería–Revista Académica de la Facultad de Ingeniería, Universidad Autónoma de Yucatán, Vol. 23, No. 1, 2019, ISSN: 2448-8364