Artículo Científico
Propagación invitro de banano (Musa spp.) por embriogénesis somática
In vitro propagation of banana (Musa spp.) by somatic embryogenesis
Propagación invitro de banano (Musa spp.) por embriogénesis somática
La Granja. Revista de Ciencias de la Vida, vol. 43, núm. 1, pp. 132-149, 2026
Universidad Politécnica Salesiana

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 05 Mayo 2022
Revisado: 23 Noviembre 2022
Publicación: 01 Marzo 2026
Resumen: El banano es una fruta de gran consumo a nivel mundial por su alto valor nutritivo y es fuente de ingresos económicos para los países que se dedican a la producción de la fruta. Sin embargo, la susceptibilidad de los cultivares a plagas y enfermedades evidencia la baja producción en el cultivo. Asimismo, los altos niveles de ploidía y esterilidad dificultan el proceso de propagación de plantas. La embriogénesis somática (ES), a través de células embriogénicas, constituye una herramienta eficaz para la propagación masiva de plantas de banano por los altos coeficientes de multiplicación y bajos costos de producción. El presente artículo tiene como finalidad describir los procesos de propagación in vitro de plantas de banano (Musa spp.), mediante una revisión bibliográfica de las aplicaciones de embriogénesis somática en la micropropagación y mejoramiento genético. Para lo cual se realizó una revisión sistemática en buscadores especializados y bases de datos, a través de tres etapas: planificación, ejecución y resumen. Los resultados más relevantes indican que la ES representa una alternativa para la multiplicación de plantas, por el gran potencial para la regeneración de tejidos en un corto periodo de tiempo. Sin embargo, el riesgo de variación somaclonal ha limitado su expansión a escala comercial. Por otro lado, la ES está siendo empleada en estudios relacionados con la transformación genética de plantas. La susceptibilidad del cultivo a enfermedades como M. fijiensis, F. oxysporum f. sp. cubense (Foc R4T) y virus rayado del banano (BSV), ha incentivado el desarrollo de especies resistentes a través del cultivo de células embriogénicas y uso de protoplastos. De igual forma, la aplicación de técnicas de transferencia de genes o edición genética ha permitido obtener nuevas especies con resistencia o tolerancia a las principales enfermedades del cultivo.
Palabras clave: Callos, Embriogénesis somática, In vitro, Musa, Variabilidad genética.
Abstract: The banana is a fruit of great consumption worldwide due to its high nutritional value and is a source of economic income for producing countries. However, the susceptibility of cultivars to pests and diseases, and the complexity of plant regeneration due to high levels of ploidy and sterility, hinder the process of plant propagation. Somatic embryogenesis (SE), through embryogenic cells, constitutes an effective tool for the mass propagation of banana plants due to high multiplication coefficients and low production costs. The purpose of this article is to describe the processes of in vitro propagation of banana plants (Musa spp.) through a bibliographic review of the applications of somatic embryogenesis in micropropagation and genetic improvement. A systematic review was conducted in specialized search engines and databases through three stages: planning, execution, and summary.The most relevant results indicate that SE represents an alternative for plant multiplication due to its enormous potential for tissue regeneration in a short period. However, the risk of somaclonal variation has limited its expansion on a commercial scale. On the other hand, SE is being used in studies related to the genetic transformation of plants. The susceptibility of the crop to diseases such as M. fijiensis, F. oxysporum f. sp. cubense (Foc R4T), and banana streak virus (BSV) has encouraged the development of resistant varieties through embryogenic cell culture and the use of protoplasts. Similarly, the application of gene transfer or gene editing techniques has made it possible to obtain new varieties with resistance or tolerance to the main crop diseases.
Keywords: Callus, Genetic variability, In vitro, Musa, Somatic embryogenesis.
Forma sugerida de citar: (APA)
Lucero-Murillo, J., Manzano-Torres, J., Loaiza-Maldonado, I. y Orellana-García,
Y. (2026). Propagación in vitro de banano (Musa spp.) por embriogénesis somática. La Granja: Revista de Ciencias de la Vida. Vol. 43(1):132-149. https://doi.org/10.17163/lgr.n43.2026.07.
1 Introducción
Las plantas de banano producen frutos muy valorados en los trópicos y subtrópicos en todo el mundo (Tran y cols., 2016). El banano ocupa el segundo lugar entre los cultivos de frutales, con una producción de 115,7 millones de toneladas, y es uno de los cultivos con mayor impacto en la economía de los países exportadores (FAO, 2020). Sin embargo, los métodos de reproducción clásicos de Musa spp. comestibles son complejos por los niveles de ploidía y esterilidad (Simoníková y cols., 2022).
La embriogénesis somática (ES) es una herramienta para la propagación masiva de genotipos de alto rendimiento productivo (Tran y cols., 2016). Esta técnica consiste en seleccionar embriones cigóticos, meristemos proliferantes o escalpos, flores masculinas y flores femeninas (Ahmed y cols., 2014). El material seleccionado inicia un proceso de inducción de callos embriogénicos, seguido del establecimiento de suspensiones celulares embriogénicas, la formación de embriones somáticos, la maduración y germinación; luego las plantas entran al proceso de aclimatización para posteriormente salir a campo abierto (Escobedo-Gracia y cols., 2016; Taco y cols., 2026).
A pesar de la alta capacidad de regeneración de plantas, la especialidad técnica está dirigida al mejoramiento genético y no a la propagación comercial, debido al riesgo de variación somaclonal en comparación con las plantas obtenidas por el método de organogénesis (Galán y cols., 2018). Los cultivos de suspensión de células somáticas constituyen una alternativa para el mejoramiento de plantas de banano (Liu y cols., 2017). Sin embargo, el uso de protoplastos obtenidos por embriogénesis de células en suspensión (ECS) se ha utilizado con frecuencia por tener un alto rendimiento, alta actividad, fácil operación y amplia adaptabilidad (Wuy cols., 2020).
Los métodos de transformación genética actuales incluyen transformación mediada por Agrobacterium (Kovács y cols., 2013), bombardeo de partículas (Vishnevetsky y cols., 2011) y CRISPR/Cas9 (Wu y cols., 2020). Estos procesos han permitido realizar mejoramientos genéticos en cultivares que son susceptibles a enfermedades (Shivani y cols., 2017), como el desarrollo de plantas resistentes al virus rayado del banano (BSV) y Mycosphaerella fijiensis (J. N. Tripathi y cols., 2019; Kovács y cols., 2013).
A pesar del desarrollo de plantas de banano mejoradas y la obtención de la arquitectura ideal, la respuesta inmunitaria sostenida siempre va acompañada de reducciones en el rendimiento (Wang ycols., 2021). Para ello, es necesario realizar estudios del genoma de Musa spp., experimentos de edición genética y el establecimiento de protocolos de cultivos in vitro, que permitan optimizar los procesos de transformación de plantas de banano. Por consiguiente, el presente artículo de revisión pretende describir los procesos de propagación in vitro de plantas de banano (Musa spp.), mediante una revisión bibliográfica de las aplicaciones de embriogénesis somática en la micropropagación y mejoramiento genético.
2 Metodología
La revisión sistemática se llevó a cabo a través de tres etapas (Moreno y cols., 2018): planificación, ejecución y resumen (Figura 1). La información seleccionada corresponde a artículos publicados durante los últimos 10 años, con algunas excepciones consideradas por la relevancia brindada a la revisión bibliográfica.
En la planificación, se elaboró un protocolo a seguir durante todo el proceso de revisión; para ello se empleó información como título del artículo, autores, objetivo, palabras clave, fuentes de investigación, criterios de inclusión/exclusión y tipo de estudio. Para la etapa de ejecución se obtuvo información bibliográfica de bases de datos especializadas como ResearchGate, Semanticscholar, Google Scholar, Springer, SciELO, ScienceDirect, Frontiers y PubMed. Se realizaron búsquedas automatizadas a partir de los títulos, palabras clave y resúmenes (Figura 2). La parte del resumen comprendió la elaboración de figuras, tablas y la redacción del manuscrito.
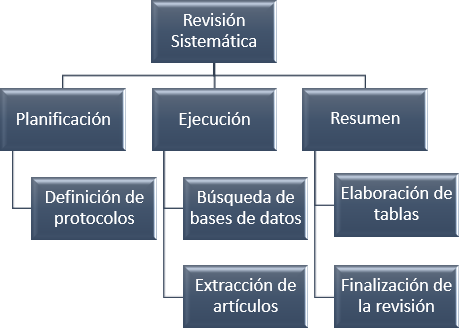
Figura 1.
Proceso metodológico del fichaje crítico de artículos científicos.
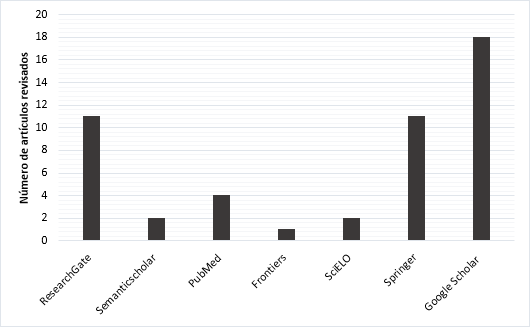
Figura2.
Revisión sistemática en buscadores especializados.
3 Cultivo in vitro en banano
El banano es una monocotiledónea perteneciente al género Musa spp., y se encuentra entre los cultivos más importantes y distribuidos en las regiones tropicales y subtropicales húmedas del mundo (Escobedo-Gracia y cols., 2016). En Ecuador, el cultivo de banano es la actividad agrícola económica de mayor relevancia (Capa Benítez y cols., 2016). Además, el país es el mayor exportador en el mundo, llegando a Europa, EE. UU., Asia, entre otros (MAGAP, 2016).
En la actualidad, se cultivan híbridos diploides y triploides originados de cruces naturales infraespecíficos (2n = 2x = 22 cromosomas), Musa acuminata Colla (genoma A) y Musa balbisiana Colla (genoma B) (Martin y cols., 2020). Sin embargo, una de las limitantes del cultivo de banano es la poliploidía y la partenocarpia vegetativa (Escobedo-Gracia y cols., 2016). La propagación vegetativa mediante brotes naturales conocidos como chupones o yemas procedentes del rizoma no logra satisfacer la demanda de genotipos élites para el establecimiento de cultivos (Lohidas y Sujin, 2015).
Con la propagación in vitro se sustrae un fragmento pequeño de la planta conocido como explante, para cultivarlo en condiciones asépticas con macronutrientes, micronutrientes, carbohidratos, vitaminas, reguladores de crecimiento y, en algunas ocasiones, aminoácidos; todo esto se desarrolla en ambientes controlados (Ahmed y cols., 2014). Esta técnica transita por cuatro etapas, las cuales son: establecimiento, multiplicación, enraizamiento, aclimatación y endurecimiento (Rodríguez, 2013).
En banano, la propagación in vitro se realiza por meristemos apicales extraídos del rizoma, dado que estos presentan un crecimiento longitudinal producto de la totipotencia celular (Ahmed ycols., 2014). Para garantizar el normal desarrollo, los meristemos deben estar establecidos en un medio de cultivo ideal, compuesto por sales inorgánicas, compuestos orgánicos, preparaciones naturales complejas y materiales de apoyo inertes (Anbazhagan y cols., 2014). El medio de cultivo más utilizado para la propagación de plantas in vitro de banano y plátano es el propuesto por Murashige y Skoog (MS). La composición basal de sales y minerales en la formulación MS permite al explante adaptarse a los procesos de micropropagación, aunque muchos laboratorios incorporan ciertas modificaciones basadas en los requerimientos nutricionales específicos de la planta (Galán y cols., 2018). Es necesario considerar que existen otras alternativas como el medio de cultivo de Gamborg (B5), el medio Schenk y Hildebrandt (SH) y Linsmaier y Skoog (LS) (Ngomuo y cols., 2014). Por lo tanto, el empleo de un medio de cultivo con una composición adecuada es importante para garantizar el crecimiento y desarrollo in vitro de cada cultivar.
El proceso de regeneración de plantas se puede realizar por organogénesis y embriogénesis somática (Galán y cols., 2018). La primera técnica se caracteriza por la formación del primordio unipolar a partir de una yema, dando lugar al desarrollo de un brote vegetativo que guarda una relación directa con el tejido materno. Esta tecnología es simple y conocida, se puede realizar a partir de yemas, ápices o meristemos, y ha sido utilizada en procesos sistemáticos para la propagación comercial. La segunda técnica, ES, en cambio, consiste en la formación de un embrión a partir de una célula o un grupo de ellas; los embriones somáticos no poseen una conexión vascular con el tejido materno puesto que no son productos de la fusión de gametos; sin embargo, deben tener la capacidad de crecer y formar toda la estructura de la planta. Este método es considerado el más eficiente para la propagación de plantas in vitro, por los altos coeficientes de multiplicación en periodos cortos de tiempo y la facilidad de automatizar los procesos productivos (Morais-Lino y cols., 2016). Sin embargo, la aplicación en la propagación de bananos y plátanos es un poco limitada debido a la variación somaclonal y la escasez de estudios en campo de plantas obtenidas por estos procesos.
4 Embriogénesis somática
La ES es un proceso que consiste en la formación de un embrión a partir de una célula, sin la necesidad de la fusión de gametos (Quiala y cols., 2021). Las células pasan por ciertos procesos morfológicos y bioquímicos, obteniendo la formación de un embrión somático (Shivani y cols., 2017). Los embriones somáticos son los nuevos individuos y se caracterizan por poseer una estructura bipolar con un polo apical y radical, y tienen la capacidad de dar origen a una planta completa (Horstman y cols., 2017). La ES representa un modelo de totipotencia celular, con redes de señalización y reprogramación de patrones de expresión génica que se regulan de forma específica por acción de los reguladores de crecimiento vegetal o las condiciones ambientales (Nic-Can y Loyola-Vargas, 2016).
Se puede realizar por dos vías: directa e indirecta (Grzyb y cols., 2018). En la ES directa, los embriones en estado de desarrollo avanzado presentan escasa uniformidad; esta técnica es muy utilizada para la regeneración de plantas. En cambio, la ES de forma indirecta produce numerosos embriones somáticos en estado temprano y presentan un desarrollo uniforme; esta técnica es utilizada para realizar suspensiones celulares (Shivani y cols., 2017). El desarrollo de los embriones somáticos en plantas monocotiledóneas pasa por tres etapas: globulares, escutelares y coleoptilares (Yuan y cols., 2016).
El proceso de producción de plantas por ES consta de cinco fases: inducción de embriones, proliferación, maduración, germinación y conservación de plantas (Bradaï y Sánchez-Romero, 2021). La inducción de embriones se inicia con la formación de masas proembriogénicas en medios de cultivos con auxinas para la formación de agregados celulares; luego se transfiere a un medio de cultivo libre de auxinas para promover la división celular y la formación de embriones. El tejido embrionario se multiplica para dar paso a la expansión de las células y acumulación de reservas; las raíces y los brotes se desarrollan en condiciones in vitro; y en la fase final los explantes salen al exterior para la aclimatización y desarrollo completo de la planta (Quiala ycols., 2021).
Es importante considerar que los tejidos donantes, el medio de cultivo y las condiciones de crecimiento influyen en la regeneración de plantas vía ES (Pencik y cols., 2015). Por ello, es necesario comprender los mecanismos fisiológicos y moleculares para inducir la ES (Méndez-Hernández y cols., 2019). La adición de reguladores de crecimiento en diferentes proporciones ayuda a romper la latencia y mejora la formación de los brotes (Márquez-López y cols., 2018). Las citoquininas se encargan de la formación de brotes y el crecimiento de yemas, mientras que las auxinas interfieren en la formación de raíces. La ES utiliza herramientas biotecnológicas con el potencial de realizar mejoramiento y producción masiva de plantas (Zhou y cols., 2016). Asimismo, esta técnica es utilizada en estudios de diferenciación celular, expresión génica y genética molecular (Nic-Can y Loyola-Vargas, 2016). Los cultivos en suspensión de células embriogénicas aceleran la propagación masiva del banano por su gran potencial de regeneración celular y constituyen una herramienta importante para el mejoramiento de plantas de modo no convencional (Escobedo-Graciay cols., 2016).
5 Inicio de la embriogénesis somática en banano
La iniciación de la ES está influenciada por el material vegetal seleccionado (Morais-Lino y cols., 2016) y el equilibrio de los reguladores de crecimiento en el medio de cultivo (Tran y cols., 2016). Uma y cols. (2021) y Morais-Lino y cols. (2016) mencionan que el material vegetal utilizado para la ES en el cultivo de banano son las inflorescencias masculinas y la recolección se debe realizar en la semana 10 después de la emergencia (Natarajan y cols., 2018) (Figura 3).
Los ápices florales inmaduros son cortados capa por capa en dos procesos (Shivani y cols., 2017). Para la eliminación de las brácteas y evitar la contaminación con agentes externos, el material se debe desinfectar con etanol al 70 % (v/v), para reducir la contaminación exógena del material vegetal (Natarajan y cols., 2018). Otro factor clave a considerar es la posición de las manos obtenidas de la inflorescencia; la selección de la sexta a la octava mano permitió obtener el 50, 0 ± 0, 54 % de callos en Grand Naine y 48, 0 ± 1, 67 % en Rasthal. Según Natarajan ycols. (2018), este aspecto influye en la inducción del callo embriogénico.
Los ápices florales se inoculan en un medio MS con sales, vitaminas, sacarosa al 3 % y reguladores de crecimiento exógenos de tipo auxinas, para inducir la formación de agregados celulares (Shivani y cols., 2017). Morais-Lino y cols. (2016) informan que las concentraciones de reguladores de crecimiento de 1 mg/L IAA + 4 mg/L 2,4-D + 1 mg/L NAA suplementado con glutamina inducen la formación de callos en un 50 % (Uma y cols., 2021). En cambio, Youssef y cols. (2010) comunican que el medio MS compuesto por sales y vitaminas suplementadas con 5, 71 µM IAA, 18 µM de 2,4-D, 5, 4 µM NAA, 4, 1 µM biotina y 87 mM sacarosa permiten obtener un 81 % de callos formados en explantes de yemas Williams y el 52,11 % en explantes de yemas Grand Naine. Por lo tanto, los reguladores de crecimiento permiten la formación de callos embriogénicos, siempre que se utilicen en concentraciones óptimas de acuerdo con el tipo de cultivar y especie.
Para inducir la ES se necesita considerar los factores ambientales, por ello los medios de cultivo con el material vegetal deben incubarse a 27 ◦C en condiciones de oscuridad por un tiempo de 12 días (Shivani y cols., 2017) (Tabla 1).
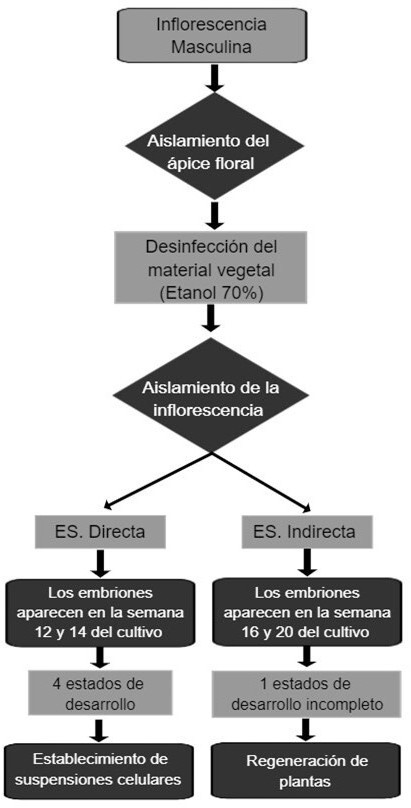
Figura 3.
Proceso de inducción de embriogénesis somática en banano.
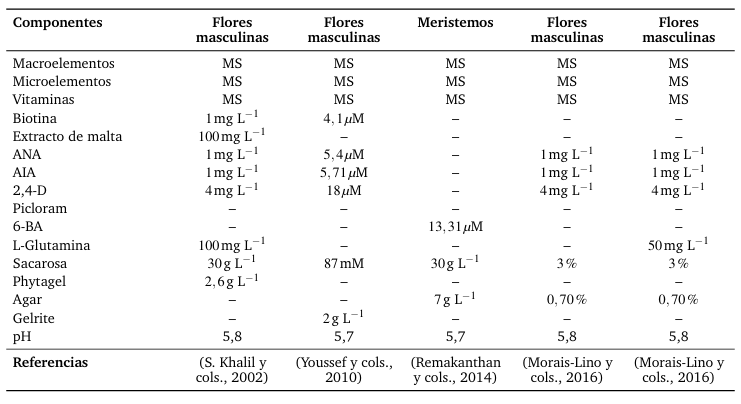
Tabla 1.
Composición de los medios de cultivo para iniciar la ES indirecta en Musa spp.
6 Proliferación e iniciación del callo embriogénico de cultivos en suspensión celular
Después del periodo de incubación (4–6 meses) se inicia la aparición de diferentes tipos de callos, los cuales son evaluados de forma mensual durante los tres primeros meses, seguido de evaluaciones periódicas cada 15 días. Después de los cuatro meses de cultivo se desarrolla el callo embriogénico de naturaleza friable formado por masas proembriogénicas de color blanco-translúcido, y por las características que presenta, el callo es considerado ideal para el establecimiento de suspensiones celulares (Morais-Lino y cols., 2016).
Una vez identificados los callos ideales, se procede al establecimiento de suspensiones celulares embriogénicas. Según Shivani y cols. (2017), los callos embriogénicos de 24 semanas se cultivan en un medio MS suplementado con 2,4-D, incubación a 27 ◦C en oscuridad, con agitación constante a 90 rpm y subcultivos cada 7 días.
En cambio, Strosse y cols. (2003) mencionan que los callos deben transferirse a un medio líquido MS suplementado con 1 mg/L de IAA, 1, 1 mg/L de 2,4-D y 250 µg/L de zeatina; con pH ajustado a 5,8 para la multiplicación de las células embriogénicas.
Por otro lado, Morais-Lino y cols. (2016) exponen que las masas embriogénicas se trasladan a un medio líquido MS suplementado con 1 mg/L de 2,4-D, 100 mg/L de glutamina, 1 mg/L de biotina, 10 mg/L de ácido ascórbico y 44, 5 g/L de sacarosa, en condiciones de oscuridad a 27 ± 2 ◦C, agitación constante a 120 rpm y subcultivos cada 10 días. En cada subcultivo, las suspensiones se filtran a través de un tamiz con la finalidad de eliminar células contaminadas o células que no cumplen con las características para el establecimiento de las suspensiones celulares embriogénicas (SCE) (Morais-Linoy cols., 2016).
Uno de los problemas principales en la inducción de callos es la exudación de compuestos fenólicos en el medio de cultivo, propios de la naturaleza de las musáceas, y que inducen el oscurecimiento, descomposición e hiperhidricidad de los callos. Una alternativa eficaz para disminuir los niveles de fenolización es el empleo de antioxidantes como la melatonina (50 mg/L) y L-glutamina (100 mg/L) en el medio de inducción de callos (Natarajan y cols., 2018).
El análisis de la expresión de genes de callos embriogénicos con aplicación de ácido 2,4diclorofenoxiacético indicó que el regulador de crecimiento actúa como un inductor de la expresión de genes (MaBBM1, MaBBM2, MaWUS2 y MaVP1) (Shivani y cols., 2017). Esta expresión puede ser clave para la regeneración de plantas de banano.
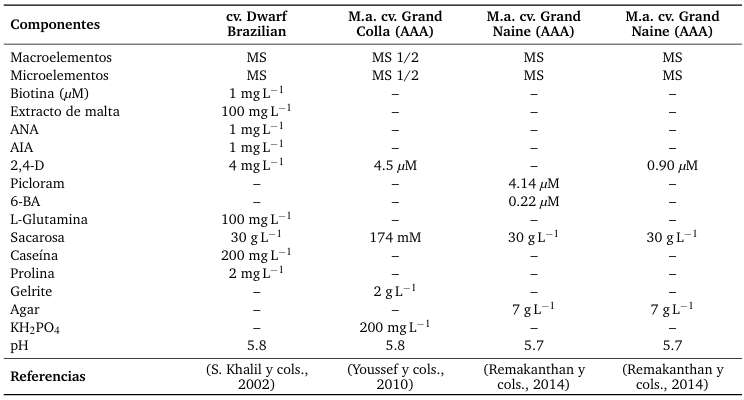
Tabla 2.
Composición de los medios de cultivo para la inducción y proliferación de callos embriogénicos
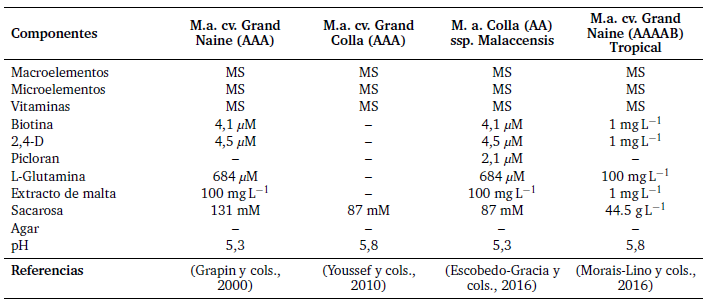
Tabla 3.
Comparación de la composición de medios de cultivo utilizados para el inicio y mantenimiento de la suspensión de células embriogénicas.
7 Desarrollo y maduración del embrión somático
Una vez formado el callo embriogénico (3–5 meses) en un medio de cultivo específico (Escobedo-Graciay cols., 2016), el siguiente paso es la proliferación del tejido embriogénico, el cual se lleva a cabo en un medio MS con sales y vitaminas, suplementado con 87 mM de sacarosa, 4, 52 µM de 2,4-D, 4, 1 µM de biotina, 680 µM de glutamina, 100 mg/L de extracto de malta, pH ajustado a 5,3 y agitación constante a 90 rpm a 27 ◦C en oscuridad. El medio debe ser renovado de forma semanal y las suspensiones celulares deben ajustarse a un volumen determinado (Enríquez, 2019).
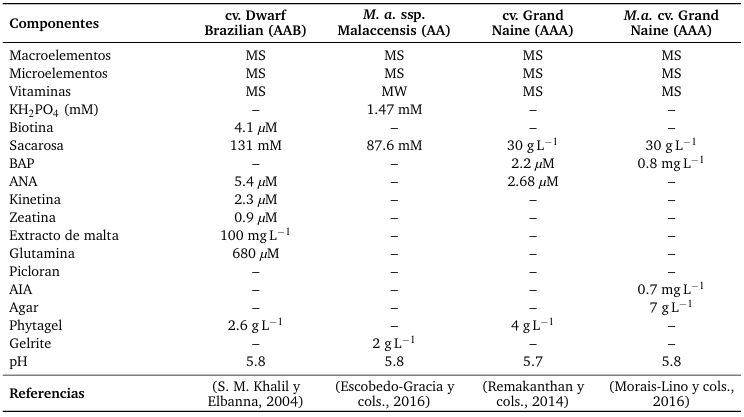
Tabla 4.
Comparación de la composición de medios de cultivo utilizados para el desarrollo y maduración de embriones somáticos de Musa spp.
Para determinar el crecimiento de la ES y definir los tiempos correctos de subcultivo, es necesario establecer la curva de crecimiento de la suspensión celular. Para ello, se toma 1, 5 ml de células somáticas, se determina la concentración de células inicial y se coloca en 50 ml del medio líquido MS. El crecimiento se calcula por el cambio en el volumen celular para el intervalo de evaluación cada 5 días durante 40 días. Asimismo, la calidad de suspensiones celulares embriogénicas se determina mediante la evaluación de la constitución celular (tipos celulares), la coloración, la tasa de multiplicación y el poder de regeneración (Morais-Lino y cols., 2016).
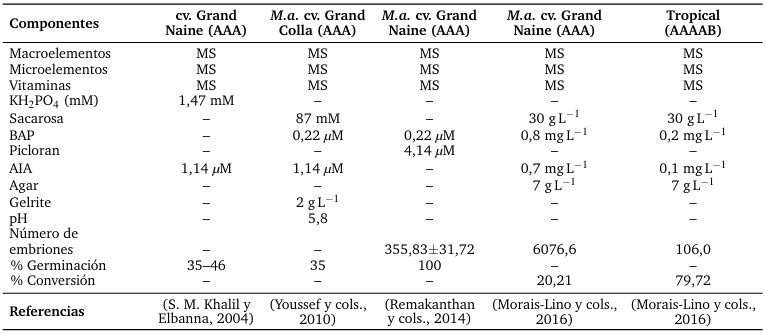
Tabla 5.
Composición media comúnmente utilizada para la germinación de embriones somáticos en Musa spp
8 Plantas derivadas de ES
La obtención de plantas a partir de la germinación de ES con raíces y brotes normales se logra en los sustratos que contengan reguladores de crecimiento (Escobedo-Gracia y cols., 2014). El desarrollo va a depender del genotipo y del procedimiento ejecutado previo y durante el desarrollo del embrión (Morais-Lino y cols., 2016). Después del proceso de aclimatación y endurecimiento, se pueden estimar tasas de conversión que son comparables con los porcentajes de germinación embrionaria.
Estos porcentajes, según el genotipo, fluctúan entre el 3 y el 46 % en bananos triploides Cavendish (AAA), pero cuando los embriones somáticos se obtienen de cultivos de suspensión de células embriogénicas, los valores pueden llegar hasta el 91 % de germinación (Domergue y cols., 2000). La tasa más alta fue encontrada en triploides (AAB) cv. Brasileño Enano y Musa acuminata cv. Grand Naine (AAA); además, tienen en común que el desarrollo del embrión pasa por una fase de diferenciación maduración (Remakanthan y cols., 2014).
Los embriones obtenidos por ES de las puntas de los brotes, como es el caso de Musa acuminata AAA, cv. Grand Naine, presentan de un 2 a 3 % de conversión de embriones (Remakanthan y cols., 2014). Algunos protocolos de ES que han sido descritos para varios genotipos de banano presentan porcentajes de germinación de embriones somáticos y tasas de conversión de embriones diferentes, debido a que los datos presentados no siempre hacen una distinción entre ambas situaciones (Escobedo-Gracia y cols., 2016).
Las tasas de conversión varían desde un 13 % en los comestibles (AA), un 13 a un 25 % para Grand Naine del subgrupo Cavendish (AAA), un 66, 7 % en el plátano africano Highland (AAA) (Namanya ycols., 2004) y un 100 % en la especie silvestre Musa acuminata ssp. (AA) (Escobedo-Gracia y cols., 2016).
En lo que compete al mejoramiento no convencional (transformación genética) para contrarrestar los problemas de plagas y obtener una mayor tasa de germinación, la ES es un proceso esencial en sistemas de regeneración in vitro, lo que permite el desarrollo de variedades resistentes (Ghag y cols., 2014); por esa razón, es importante continuar con el desarrollo y optimización de los protocolos de ES de los diferentes clones cultivados (Escobedo-Gracia y cols., 2016).
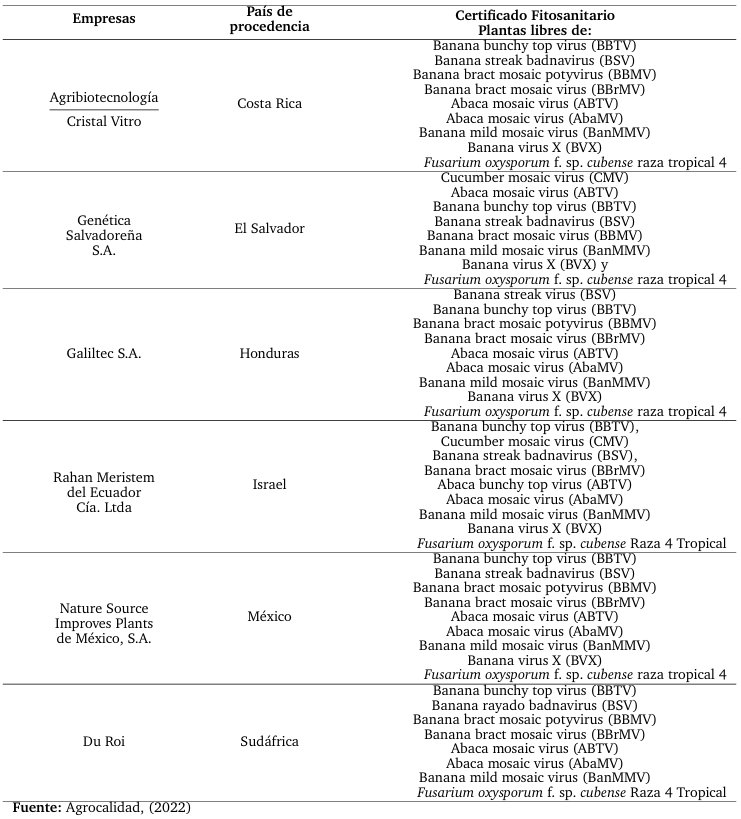
Tabla 6.
Empresas biotecnológicas con certificado fitosanitario para importar plantas in vitro de banano (Musa sapientum) en Ecuador.
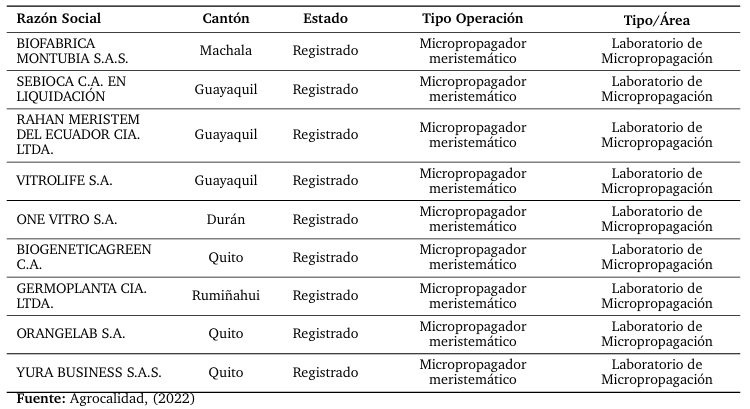
Tabla 7.
Establecimientos registrados para la propagación de material vegetal in vitro de banano (Musa sapientum).
9 Variación somaclonal en ES de plantas regeneradas
Una particularidad en los cultivos in vitro de tejidos vegetales es la aparición de la variación somaclonal, existiendo cambios genéticos en las células y en tejidos cultivados (Nwauzoma y Jaja, 2013). En algunas ocasiones, esta variación es empleada para el mejoramiento genético, permitiendo ampliar la variación genética natural (Wang y cols., 2021); pero cuando se desea realizar una propagación clonal, la variación somaclonal resulta una anomalía no deseada.
El entorno del cultivo in vitro, como son el tipo y la concentración de hormonas reguladoras del crecimiento en plantas, más los antecedentes genéticos del explante, el número total y la duración de los subcultivos, pueden alterar las características que presentan las plantas regeneradas por embriones somáticos (?). Todos estos factores contribuyen a la generación de variación genética y epigenética (Escobedo-Gracia y cols., 2016), que es expresada en el fenotipo y se conoce como variación somaclonal (Youssef y cols., 2010). Esta puede constituir una variación genética preexistente en el explante, debido a cambios en el número de cromosomas, o ser inducida mediante el cultivo in vitro; además, en el ADN también pueden ocurrir mutaciones y cambios epigenéticos a nivel secuencial (Wang y cols., 2021).
También se conoce que la variación somaclonal en el cultivo de banano está asociada con cultivos a largo plazo, cultivos que involucran una fase de callo o altas tasas de tratamientos de multiplicación (Nwauzoma y Jaja, 2013). Por otro lado, la disminución en la capacidad de regeneración de los cultivos provenientes de la suspensión de células embriogénicas se asocia con la inestabilidad citogenética en bananos triploides Cavendish (genoma AAA), regenerados a partir de cultivos en suspensión celular a largo plazo y la subsiguiente pérdida del potencial de regeneración (Wu y cols., 2020).
El proceso de regeneración por ES mostró estabilidad genética en comparación con las plántulas regeneradas de cultivos de largo plazo, donde se encontró una mayor cantidad de ADN (Escobedo-Gracia y cols., 2016). En lo que respecta a la inestabilidad o estabilidad genética, al evaluar los parámetros morfológicos y agronómicos, la variación es de alrededor de 0,3 a 3,6 %; por otra parte, los marcadores moleculares registraron una variación baja, de 1,4 a 1,6 %, dentro de la variación natural encontrada en la planta madre utilizada como fuente de explante (Ghag y cols., 2014).
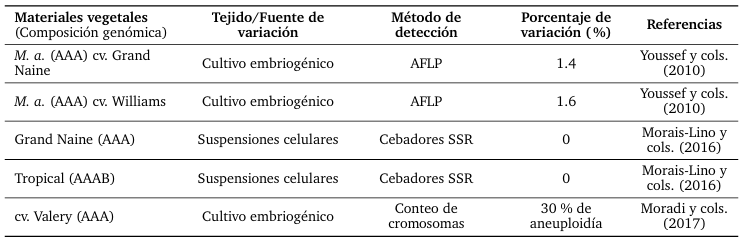
Tabla 8.
Variación somaclonal en plantas de banano regeneradas por embriogénesis somática in vitro.
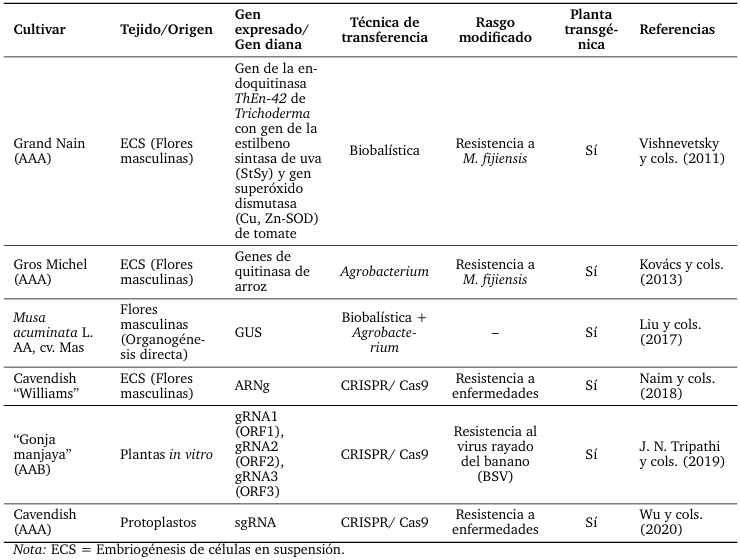
Tabla 9.
Resultados del mejoramiento genético de banano a través de procesos de generación de plantas in vitro.
10 Transformación genética del banano utilizando cultivos de ES
El desarrollo de variedades mejoradas de banano a través de métodos convencionales representa un desafío debido a la baja variabilidad genética, la poliploidía y la esterilidad de los cultivos comerciales (L. Tripathi y cols., 2019). Por tanto, la técnica de embriogénesis somática constituye una alternativa para el mejoramiento de plantas de banano (Liu ycols., 2017).
De igual forma, el uso de protoplastos obtenidos por embriogénesis de células en suspensión (ECS) se utiliza debido a su alto rendimiento, alta actividad, fácil operación y amplia adaptabilidad (Wu y cols., 2020). Los métodos de transformación genética utilizados en el banano incluyen la transformación mediada por Agrobacterium (Kovács ycols., 2013), bombardeo de partículas (Vishnevetskyy cols., 2011) y CRISPR/Cas9 (Wu y cols., 2020).
Las tecnologías de edición del genoma son valiosas para explorar los mecanismos subyacentes de la función y la regulación de los genes, y pueden servir como plataforma para la mejora genética de los cultivos mediante la eliminación del ADN cromosómico indeseable, la regulación positiva o negativa de los genes endógenos y la introducción de secuencias de codificación novedosas (Liu y cols., 2017). En la Tabla 9 se describen los principales resultados obtenidos en la regeneración de plantas de banano.
11 Conclusiones
La propagación de banano por embriogénesis somática representa una alternativa para la multiplicación de plantas, por el gran potencial para la regeneración de tejidos en un corto periodo de tiempo. Sin embargo, el riesgo de variación somaclonal que pueden presentar los explantes ha limitado su expansión a escala comercial. Por ello, es necesario desarrollar protocolos específicos para cada especie, seleccionar el material vegetal adecuado e identificar el tipo de genotipo, para garantizar el éxito de la micropropagación de plantas.
Por otro lado, la variabilidad genética que presentan los explantes sometidos a esta técnica ha sido utilizada para estudios relacionados con la transformación genética de plantas de banano. La susceptibilidad del cultivo a enfermedades como M. fijiensis,F. oxysporum f. sp. cubense (Foc R4T) y virus rayado del banano (BSV), ha incentivado el desarrollo de nuevos protocolos de establecimiento in vitro de especies resistentes.
La propagación a gran escala de plantas a partir de embriogénesis es una alternativa efectiva para los monocultivos de banano en cada renovación, por lo que la trazabilidad en el proceso se hace necesaria para identificar mutaciones. La aplicación de células embriogénicas en suspensión o el uso de protoplastos de forma conjunta con las técnicas de transferencia de genes o edición genética han permitido obtener nuevas especies con resistencia o tolerancia a las principales enfermedades del cultivo.
Contribución de los autores
J.R.L.M.: Conceptualización, curación de datos, análisis formal, adquisición de financiación, investigación, metodología, software, validación, escritura – borrador original, escritura – revisión y edición. J.W.M.T.: Adquisición de financiación, supervisión. I.C.L.M.: Validación, administración de proyecto. Y.A.O.G.: Recursos, visualización.
Referencias
Ahmed, S., Sharma, A., Singh, A. K., Wali, V. K., y Kumari, P. (2014). In vitro multiplication of banana (Musa sp.) cv. Grand Naine. African Journal of Biotechnology, 13(27). Online: https://doi.org/10.5897/AJB2014.13750
K. (2014). In vitro propagation of Musa sp. (banana). International Journal of Current Microbiology and Applied Sciences, 3(7), 399–404. Online: https://tinyurl.com/23lh8gk9
Bradaï, F., y Sánchez-Romero, C. (2021). Effect of Cryopreservation on the Ex-Vitro Establishment of Olive Plants Regenerated via Somatic Embryogenesis. Plants, 10(2), 2223–7747. Online: https://doi.org/10.3390/plants10020396
Capa Benítez, L. B., Alaña Castillo, T. P., y Benítez Narváez, R. M. (2016). Importancia de la producción de banano orgánico: Caso provincia El Oro, Ecuador. Revista Universidad y Sociedad, 8(3), 64–71. Online: https://tinyurl.com/24w794kz
Domergue, F. G. R., Ferrière, N., y Côte, F. X. (2000). Morphohistological study of the different constituents of a banana (Musa AAA, cv. Grande naine) embryogenic cell suspension. Plant Cell Reports, 19, 748–754. Online: https://doi.org/10.1007/ s002999900188
Enríquez, A. (2019). Análisis fisiológico, bioquímico y molecular del desarrollo y maduración del embrión somático (Tesis Doctoral, Tesis doctoral). Online: https://tinyurl.com/yxoqejyq
C. I., y Ku-Cauich, J. R. (2016). Somatic Embryogenesis in Banana, Musa ssp. En V. Loyola-Vargas y N. Ochoa-Alejo (Eds.), Somatic Embryogenesis: Fundamental Aspects and Applications. Cham: Springer. Online: https://doi.org/10.1007/978-3-319-33705-0_21
Escobedo-Gracia, R. M., Maldonado-Borges, J. I., Burgos-Tan, M. J., Valadez-González, N., y KuCauich, J. R. (2014). Using flow cytometry and cytological analyses to assess the genetic stability of somatic embryo-derived plantlets from embryogenic Musa acuminata Colla (AA) ssp. malaccensis cell suspension cultures. Plant Cell, Tissue and Organ Culture (PCTOC), 116, 175–185. Online: https://doi.org/10.1007/s11240-013-0394-z
FAO. (2020). Examen del mercado del banano: resultados preliminares de 2019 (Inf. Téc.). Roma: Food and Agriculture Organization.
Galán, V., Rangel, A., López, J., Hernández, J. B. P., Sandoval, J., y Rocha, H. S. (2018). Propagación del banano: técnicas tradicionales, nuevas tecnologías e innovaciones. Revista Brasileira de Fruticultura, 40(4). Online: https://doi.org/10.1590/ 0100-29452018574
Ghag, S., Shekhawat, U. S., y Ganapathi, T. (2014). Transgenic banana plants expressing a Stellaria media defensin gene (Sm-AMP-D1) demonstrate improved resistance to Fusarium oxysporum. Plant Cell, Tissue and Organ Culture (PCTOC), 119, 247–255. Online: https://doi.org/10.1007/ s11240-014-0529-x
Grapin, A., Ortiz, J. L., Domergue, R., Babeau, J., Monmarson, S., Escalant, J. V., . . . Côte, F. (2000). Establishment of embryogenic callus and initiation and regeneration of embryogenic cell suspensions from female and male immature flowers of Musa. Musalit, 7(1), 13–15. Online: https://www.musalit.org/seeMore.php?id=13956
Grzyb, M., Kalandyk, A., y Mikula, A. (2018). Efecto de TIBA, fluridona y ácido salicílico sobre la embriogénesis somática y el contenido de hormonas y azúcares endógenos en el helecho arborescente Cyathea delgadii Sternb. Acta Physiologiae Plantarum, 40, 1. Online: https://doi.org/10.1007/ s11738-017-2577-4
Horstman, A., Bemer, M., y Boutilier, K. (2017). Una visión transcripcional de la embriogénesis somática. Regeneración, 4(4), 201–216. Online: https://doi.org/10.1002/reg2.91
Khalil, S., Cheah, K., Perez, E., Gaskill, D., y Hu, J. (2002). Regeneration of banana (Musa spp. AAB cv. Dwarf Brazilian) via secondary somatic embryogenesis. Plant Cell Reports, 20(12), 1128– 1134. Online: https://doi.org/10.1007/s00299-002-0461-0
Khalil, S. M., y Elbanna, A. A. M. (2004). Highly efficient somatic embryogenesis and plant regeneration via suspension cultures of banana (Musa ssp.). Arab Journal of Biotechnology, 7, 99–110.
Kovács, G., Sági, L., y Jacon, G. (2013). Expression of a rice chitinase gene in transgenic banana (‘Gros Michel’, AAA genome group) confers resistance to black leaf streak disease. Transgenic Research, 22, 117–130. Online: https://doi.org/ 10.1007/s11248-012-9631-1
Liu, J., Gao, P., Sun, X., Zhang, J., Sun, P., Wang, J., . . . Jin, Z. (2017). Efficient regeneration and genetic transformation platform applicable to five Musa varieties. Electronic Journal of Biotechnology, 25, 33–38. Online: https://doi.org/10.1016/j.ejbt.2016.11.002
Lohidas, J., y Sujin, D. (2015). Effect of growth hormones in the micro propagation of Banana cv. Matti. Plant Archives, 15(1), 307–314. Online: https://tinyurl.com/29hd3t9e
MAGAP. (2016). Análisis Sectorial BANANA (Inf. Téc.). Quito: Pro Ecuador. Online: https://tinyurl.com/y6ywd4pt
Fondi, E., . . . Yahiaoui, N. (2020). Genome ancestry mosaics reveal multiple and cryptic contributors to cultivated banana. The Plant Journal, 102(5), 1008–1025. Online: https://doi.org/ 10.1111/tpj.1468
Moradi, Z., Farahani, F., Sheidai, M., y Nejad Satari, T. (2017). Somaclonal variation in banana (Musa acuminata colla cv. Valery) regenerated plantlets from somatic embryogenesis: histological and cytogenetic approaches. Caryologia, 70(1), 1–6. Online: https://doi.org/10.1080/00087114.2016.1198665
Morais-Lino, L. S., Santos-Serejo, J. A., Amorim, E. P., de Santana, J. R. F., Pasqual, M., y de Oliveira e Silva, S. (2016). Somatic embryogenesis, cell suspension, and genetic stability of banana cultivars. In Vitro Cellular & Developmental Biology-Plant, 52(1), 99–106. Online: https:// doi.org/10.1007/s11627-015-9729-2
Moreno, B., Muñoz, M., Cuellar, J., Domancic, S., y Villanueva, J. (2018). Revisiones sistemáticas: definición y nociones básicas. Revista clínica de periodoncia, implantología y rehabilitación oral, 11(3), 184–186.
V. M. (2018). Localization and transport of indole-3-acetic acid during somatic embryogenesis in Coffea canephora. Protoplasma, 255(2), 695– 708. Online: https://tinyurl.com/y2ugj6mf
Méndez-Hernández, H., Ledezma-Rodríguez, M., Avilez-Montalvo, R., Juárez-Gómez, Y., Skeete, A., Avilez-Montalvo, J., . . . Loyola-Vargas, V. (2019). Signaling overview of plant somatic embryogenesis. Frontiers in Plant Science, 10, 77. Online: https://doi.org/10.3389/fpls.2019.00077
Naim, F., Dugdale, B., Kleidon, J., Brinin, A., Shand, K., Waterhouse, P., y Dale, J. (2018). Gene editing the phytoene desaturase alleles of Cavendish banana using CRISPR/Cas9. Transgenic Research, 27(5), 451–460. Online: https://link.springer.com/ article/10.1007/s11248-018-0083-0
Namanya, P., Magambo, S. M., Mutumba, G., y Tushemereirwe, W. (2004). Somatic embryogenesis from immature male inflorescences of East African highland banana CV ‘Nakyetengu’. African Crop Science Journal, 12(1), 43–49. Online: https://tinyurl.com/y2bknwou
Natarajan, N., Krish, K., Duraialagaraja, S., y Soorianathasundaram, K. (2018). Plant regeneration, developmental pattern and genetic fidelity of somatic embryogenesis derived Musa spp. Journal of Genetic Engineering and Biotechnology, 16(2), 587–598. Online: https://doi.org/10.1016/j.jgeb.2018.10.001
Ngomuo, M., Mneney, E., y Ndakidemi, P. A. (2014). The in vitro propagation techniques for producing banana using shoot tip cultures. American Journal of Plant Sciences. Online: https://doi.org/10.4236/ajps.2014.511175
Nic-Can, G. I., y Loyola-Vargas, V. M. (2016). El papel de las auxinas durante la embriogénesis somática. En V. M. Loyola-Vargas y N. Ochoa-Alejo (Eds.), Embriogénesis somática. Aspectos fundamentales y aplicaciones (pp. 171–181). Cham: Springer. Online: https://doi.org/10.1007/978-3-319-33705-0_10
Nwauzoma, A. B., y Jaja, E. T. (2013). A review of somaclonal variation in plantain (Musa spp): mechanisms and applications. Journal of Applied Biosciences, 67, 5252–5260. Online: https://doi.org/10.4314/jab.v67i0.95046
Pencik, A., Tureková, V., Paulisiç, S., Rolcìk, J., Strnad, M., y Mihaljevic, S. (2015). El amonio regula el potencial embriogénico en Cucurbita pepo a través de cambios mediados por el pH en la auxina endógena y el ácido abscísico. Cultivo de órganos de tejido celular vegetal, 122, 89–100. Online: https://doi.org/10.1007/s11240-015-0752-0
Quiala, E., Barbón, R., Mestanza, S., La O, M., Gardenis, M., Nuñez, J., . . . Noceda, C. (2021). Somatic embryogenesis and plant regeneration from leaf of the interspecific hybrid of mahogany (Swietenia macrophylla King × S. mahagoni (L.) Jacq.). Trees. Online: https://doi.org/10.1007/ s00468-021-02192-x
Remakanthan, A., Menon, T. G., y Soniya, E. V. (2014). Somatic embryogenesis in banana (Musa acuminata AAA cv. Grand Naine): effect of explant and culture conditions. In Vitro Cellular & Developmental Biology Plant, 50(1), 127–136. Online: https://doi.org/10.1007/s11627-013-9546-4
Rodríguez, P. A. (2013). Cultivo de tejidos [Manual de software informático]. Bogotá, Colombia. Online: https://tinyurl.com/y5cuv8z6 (Módulo Escuela de Ciencias Agrícolas Pecuarias y del Medio Ambiente)
Shivani, Awasthi, P., Sharma, V., Kaur, N., Kaur, N., Pandey, P., y Tiwari, S. (2017). Genomewide analysis of transcription factors during somatic embryogenesis in banana (Musa spp.) cv. Grand Naine. PLoS ONE, 12(8), e0182242. Online: https://doi.org/10.1371/journal.pone.0182242
Simoníková, D., Cízková, J., Zoulová, V., Christelová, P., y Hribová, E. (2022). Advances in the Molecular Cytogenetics of Bananas, Family Musaceae. Plants, 11(4), 482. Online: https://doi.org/10.3390/plants11040482
Strosse, H., Domergue, R., Panis, B., Escalant, J. V., y Côte, F. (2003). Banana and plantain embryogenic cell suspensions (Technical Guidelines 8). Montpellier, France: The International Network for the Improvement of Banana and Plantain (INIBAP).
Taco, J., Jiménez, R., y Soto, M. (2026). Valorization of banana peel (Musa paradisiaca) as a raw material for biopolymer production. La Granja: Revista de Ciencias de la Vida, 43(1), 158–169. Online: https://doi.org/10.17163/lgr.n43.2026.09
Tran, T. H., Bui, T. V., y Feng, T. Y. (2016). The role of auxin and cytokinin on somatic embryogenesis from cell suspension cultures of the banana cultivar “Cau Man”. Acta Horticulturae(1114), 219–
Tripathi, J. N., Ntui, V. O., Ron, M., Muiruri, S. K., Britt, A., y Tripathi, L. (2019). CRISPR/Cas9 editing of endogenous banana streak virus in the B genome of Musa spp. overcomes a major challenge in banana breeding. Communications Biology, 2(1), 1–11. Online: https://www.nature.com/articles/s42003-019-0288-7
Tripathi, L., Ntui, V. O., y Tripathi, J. N. (2019). Application of genetic modification and genome editing for developing climate-smart banana. Food and Energy Security, 8(4), 1–16. Online: https://doi.org/10.1002/fes3.168
Uma, S., Kumaravel, M., Backiyarani, S., Saraswathi, M., Durai, P., y Karthic, R. (2021). La embriogénesis somática como herramienta para la reproducción de plantas genéticamente estables en banano y ensayos de campo confirmatorios. Plant Cell, Tissue and Organ Culture (PCTOC), 147, 181–188. Online: https://doi.org/10.1007/ s11240-021-02108-0
Vishnevetsky, J., White, T. L., Palmateer, A. J., Flaishman, M., Cohen, Y., Elad, Y., . . . Perl, A. (2011). Improved tolerance toward fungal diseases in transgenic Cavendish banana (Musa spp. AAA group) cv. Grand Nain. Transgenic Research, 20(1), 61–72. Online: https://tinyurl.com/ y6sjbjed
Wang, X., Yu, R., y Li, J. (2021). Using genetic engineering techniques to develop banana cultivars with fusarium wilt resistance and ideal plant architecture. Frontiers in Plant Science, 11, 617528. Online: https://doi.org/10.3389/ fpls.2020.617528
Yi, G. (2020). Establishment of a PEG-mediated protoplast transformation system based on DNA and CRISPR/Cas9 ribonucleoprotein complexes for banana. BMC Plant Biology, 20(1), 425. Online: https://doi.org/10.1186/s12870-020-02609-8
G. (2010). Influence of genotype and age of explant source on the capacity for somatic embryogenesis of two Cavendish banana cultivars (Musa acuminata Colla, AAA). African Journal of Biotechnology, 9(15), 2216–2223. Online: https://doi.org/10.4314/ajb.v9i15
Yuan, G., Shui-Gen, L., Xiao-Fen, F., y Zhen-Hong, S. (2016). Application of Somatic Embryogenesis in Woody Plants. Frontiers in Plant Science, 7, 938. Online: https://doi.org/10.3389/fpls.2016.00938
Zhou, Q., Wang, M., Yuan, Y., Wang, X., Fu, R., Wan, H., . . . Zhou, Q. (2016). Complete meiosis from embryonic stem cell-derived germ cells in vitro. Cell Stem Cell, 18(3), 330–340. Online: https://doi.org/10.1016/j.stem.2016.01.017
Información adicional
redalyc-journal-id: 4760
Enlace alternativo
https://revistas.ups.edu.ec/index.php/granja/article/view/6197 (html)