Artículo Científico
Efectos del plomo y cromo en la germinación y arquitectura de raíz de plántulas de Typha latifolia (Typhaceae)
Effects of lead and chromium on germination and root architecture of Typha latifolia (Typhaceae) seedlings
Efectos del plomo y cromo en la germinación y arquitectura de raíz de plántulas de Typha latifolia (Typhaceae)
La Granja. Revista de Ciencias de la Vida, vol. 43, núm. 1, pp. 150-165, 2026
Universidad Politécnica Salesiana

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 21 Julio 2021
Revisado: 11 Julio 2023
Publicación: 01 Marzo 2026
Resumen: El presente trabajo evalúa el efecto de diferentes concentraciones de plomo y cromo sobre la arquitectura de raíz y porcentaje de germinación de Typha latifolia. Para ello, se recolectaron semillas viables de dos sitios en la Laguna de Yahuarcocha (Ibarra-Ecuador). Con relación al porcentaje de germinación se trataron las semillas con procesos pregerminativos; posteriormente fueron expuestas a concentraciones de 50, 100 y 200 ppm de plomo y 10, 20, 40 ppm de cromo. Para el análisis de la arquitectura de la raíz se cultivaron plántulas de T. latifolia por cuatro semanas en solución Hoagland al 50 %, luego fueron trasladadas a rizotrones en los que se añadieron los metales pesados en concentraciones similares al ensayo de germinación. Las plántulas se mantuvieron en dichas condiciones por 15 días en los que se registraron variables como el número de raíces, área total, y longitud total. Se realizaron registros fotográficos de los parámetros en estudio y fueron analizados en el programa ImageJ y su extensión SmartRoot. En el porcentaje de germinación se encontró que los dos metales afectan al proceso de germinación, especialmente el cromo, con el que se obtuvo porcentajes de germinación menores al 15 % y con plomo con un 25 %. Con respecto a la arquitectura de raíz el número de raíces y la longitud total no varió entre el control y los tratamientos con metales. Sin embargo, el tratamiento referente al área total de la raíz tratada con cromo presentó diferencias significativas con respecto al control.
Palabras clave: Fisiología vegetal, metales pesados, plantas acuáticas, rizotrón, Yahuarcocha, Typha latifolia, Ecuador.
Abstract: This research evaluates the effect of different concentrations of lead and chromium on root architecture and germination percentage of Typha latifolia. Seeds of Typha latifolia were collected from Yahuarcocha Lagoon (Ibarra-Ecuador). Pre-germinative treatments and exposure to lead concentrations of 50, 100, and 200 ppm, as well as 10, 20, and 40 ppm of chromium concentrations were applied to the seeds to measure the germination percentage. Regarding root architecture analysis, T. latifolia seedlings were grown for four weeks in 50 % Hoagland solution and then transferred to rhizotrons, where the heavy metals were added to concentrations like the germination test. The seedlings were kept in these conditions for 15 days and variables such as number of roots, total area, and total length were recorded. Photographic records of the parameters under study were taken and analyzed in Image J and its SmartRoot extension. It was found that both heavy metals affected (significantly) the germination process, especially chromium. Germination percentages lower than 15 % and 25 % for lead were also obtained. Concerning root architecture, the number of roots and total length from heavy metal treatments were not significantly different from control. However, the total area treatment with chromium showed significant differences with respect to the control.
Keywords: Plant physiology, heavy metals, aquatic plants, rhizotron, Yahuarcocha, Typha latifolia, Ecuador.
Forma sugerida de citar: (APA)
Oquendo, R., Fernández, L., Pabón-Garcés, G. y Vásquez-Hernandez, L. (2026). Efectos del plomo y cromo en la germinación y arquitectura de raíz de plántulas de Typha latifolia (Typhaceae). La Granja: Revista de Ciencias de la Vida. Vol. 43(1):150-165. https://doi.org/10.17163/lgr.n43.2026.08.
1 Introducción
La contaminación ambiental por metales pesados ha aumentado significativamente debido a las actividades antrópicas, en especial las generadas por prácticas industriales. Estos contaminantes, al no ser sustancias biodegradables, producen efectos letales sobre las plantas tales como la reducción de la tasa de transpiración y la división celular (Sharmay cols., 2022). Como respuesta a su exposición, se reduce el porcentaje de germinación de las semillas, hay inactivación de enzimas esenciales, afectando a la fotosíntesis y la regulación hídrica de la planta (Zaidi y cols., 2012); además, pueden causar efectos en su morfología tales como la disminución de su biomasa, diámetro, longitud, área y distribución en el suelo, así como la reducción de raíces laterales y adventicias (Baligar y cols., 1998).
La raíz de las especies vegetales es de vital importancia en su desarrollo y crecimiento, ya que realiza la absorción de agua, nutrientes y minerales del suelo, razón por la cual presenta una plasticidad en su arquitectura que depende de las condiciones y tipo de suelo (Armengaud y cols., 2009; Franco ycols., 2011). Las raíces de plantas tolerantes a metales pesados y estrés abiótico son capaces no sólo de responder a las deficiencias de nutrientes, sino también al exceso de metales en el suelo, lo que provoca la disminución de sus parámetros de crecimiento como la elongación de la raíz, la producción de biomasa y producción de pelos radicales por la toxicidad y alteración de procesos fisiológicos (Barceló y Poschenrieder, 1992; Kahle, 1993).
A pesar del daño inminente de los metales pesados, se conocen ciertas plantas por su tolerancia a estos contaminantes, incluso pues son capaces de incorporar estos compuestos mediante el proceso de absorción, siendo almacenados en la vacuola de la célula y evitando los daños antes mencionados (Pal Singh y cols., 2013). Este es el caso de Typha latifolia, especie acuática que se distribuye en el hemisferio norte y que fue introducida y naturalizada en América del Sur, África Oriental, Australia y Hawái Smith2018, que por su umbral de tolerancia se considera como una hiperacumuladora de metales pesados en sus raíces, pudiendo llegar a tener concentraciones superiores al sustrato circundante (Brankovic´ y cols., 2011).
Sin embargo, a pesar de tolerar los metales también sufre cambios en la arquitectura y un decrecimiento gradual de su raíz, dependiendo de la concentración de metal a la que esté expuesta. Con relación al plomo, se ha reportado un umbral de afectación del crecimiento en un rango de 200–500 ppm y para el cromo en un rango de 10–60 ppm (Sasmazy cols., 2008; Chen y cols., 2014; Han y cols., 2015).
Para cuantificar estos cambios se han utilizado diversas técnicas, entre ellas se destaca el análisis de la arquitectura de la raíz, que consiste en la observación sistemática de una serie de variables medibles en aparatos denominados rizotrones que permiten manipular concentraciones de nutrientes y otros factores externos (Busch y cols., 2006). La descripción del sistema radicular en plantas desarrolladas en rizotrones permite documentar el crecimiento y la forma de las raíces lo que ayuda a conocer su morfología, topología y la interacción entre raíces (Lobet y cols., 2011).
Asimismo, el estudiar la germinación de semillas de plantas de humedales tolerantes a metales pesados, como el caso de Typha latifolia, permitirá determinar el grado de resistencia de sus semillas a la presencia de los contaminantes (Zhang, 2015), lo que tiene gran importancia en proyectos de restauración ecológica y remediación ambiental.
En consideración a lo mencionado, el objetivo de este trabajo es cuantificar el efecto de diferentes concentraciones de plomo y cromo sobre la germinación de semillas y arquitectura de la raíz de plántulas de Typha latifolia en condiciones de laboratorio.
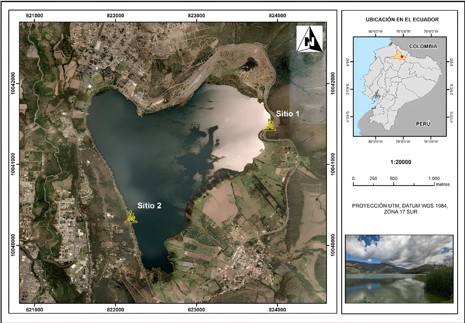
Figura 1.
Sitios de colecta de semillas de T. latifolia en la Laguna de Yahuarcocha. Sitio 1: orilla Noreste de la laguna; Sitio 2: orilla Suroeste. Fecha de colecta: abril–mayo 2021 (época lluviosa).
2 Materiales y Métodos
2.1 Recolección de Semillas
Se emplearon semillas de Typha latifolia, recolectadas de poblaciones de crecimiento espontáneo de la Laguna de Yahuarcocha (2200 msnm), ubicada en la provincia de Imbabura, Ecuador (Figura 1). Se seleccionaron dos sitios de colecta: el primero ubicado en la orilla Noreste de la laguna (Sitio 1), conocido por los lugareños como “la vuelta de la paloma”, y el Sitio 2, ubicado en la orilla Suroeste de la misma, en el sector conocido como “la recta de ingreso al poblado de San Miguel de Yahuarcocha”.
Se procedió a la colecta de una inflorescencia madura por planta (de color marrón oscuro según Smith (2018)), con un total de 20 inflorescencias (diez por cada sitio de muestreo). Se conservaron refrigeradas a 3 ◦C durante siete días. La colecta se realizó en la época lluviosa de abril–mayo de 2021.
2.2 Germinación de las semillas
Las semillas, que se contabilizan entre 20 mil y 700 mil por espiga (Smith, 2018), se desinfectaron con hipoclorito de sodio al 2,5 % (USDA, 2016). Posteriormente se colocaron en placas Petri con agua desionizada con el objetivo de seleccionar las semillas viables (aquellas que se hunden) de las no viables (las que flotan) (Bourgeois y cols., 2012). En total se seleccionaron 600 semillas viables (300 por sitio) que se colocaron en tres cajas Petri (100 por caja).
Cada grupo de semillas se sumergió en agua ligeramente salina (1 % de NaCl) con un pH de entre 6,5 y 7,5 por 24 h, como lo recomienda, para esta especie Semenova (2014). Finalmente, las semillas se sumergieron a una profundidad de 0,5 cm en agua destilada hasta su germinación, con un fotoperíodo de 12 h/12 h y una temperatura promedio de 21 ◦C.
No se realizó tratamiento de escarificación, ya que según el Royal Botanical Gardens, Kew (2016) este reduce la germinación a niveles inferiores al 58 % en Typha latifolia. Los tratamientos control fueron 100 semillas procedentes de los sitios 1 (control 1) y 2 (control 2), hidratadas en agua destilada durante 20 días, con tres repeticiones (Tabla 1).
El efecto del plomo sobre la germinación se evaluó adicionando en cada placa Petri concentraciones de: 50 ppm, 100 ppm y 200 ppm, en forma de Pb(NO3)2, con tres repeticiones (Tabla 2).

Tabla 1.
Condiciones experimentales de los tratamientos en la prueba de germinación de semillas de Typha latifolia
procedentes de dos sitios de muestreo de la Laguna de Yahuarcocha.

Tabla 2.
Condiciones de los tratamientos en la prueba de los efectos de las concentraciones diferentes de plomo (Pb) en la germinación de semillas de Typha latifolia procedentes de la Laguna de Yahuarcocha.
Para evaluar el efecto del cromo sobre la germinación se usaron concentraciones de: 10 ppm, 20 ppm y 40 ppm, en forma de K2Cr2O7, igualmente, con tres repeticiones en cada caso (Tabla 3). En ambos conjuntos los tratamientos de control fueron las semillas hidratadas con agua salina al 1 % de NaCl durante 24 h (como tratamiento pregerminativo), y luego hidratadas con agua destilada.

Tabla 3.
Condiciones de los tratamientos en la prueba de los efectos de las concentraciones diferentes de cromo (Cr) en la germinación de semillas de Typha latifolia procedentes de la Laguna de Yahuarcocha.
En un primer experimento, la variable evaluada fue el porcentaje de germinación de los sitios 1 y 2 respecto al porcentaje de germinación de los tratamientos control (1 y 2). Luego, en un segundo y tercer experimento, se evaluó el porcentaje de germinación en los tratamientos con semillas hidratadas con distintas concentraciones de plomo y cromo, respectivamente, como se explicó anteriormente.
2.3 Arquitectura de raíz
Para estudiar el crecimiento de las raíces se construyó un rizotrón, cuyas medidas fueron: 40 cm de frontal, 8 cm de ancho (lateral) y 40 cm de profundidad (en sentido de la gravedad) (Figura 2). El rizotrón se acondicionó con doble vidrio frontal de 5 mm de ancho, lo que permitió realizar un seguimiento temporal del crecimiento de las raíces, mediante un registro fotográfico.
En la superficie del medio de cultivo (solución Hoagland estándar al 50 %) se colocó una lámina de corcho de 4 mm y sobre esta se colocaron las plántulas obtenidas a partir de semillas del tratamiento control del experimento de germinación. En total se trasplantaron 3 plántulas en cada rizotrón (45 días después de su germinación), con un total de 21 plántulas.
El registro fotográfico se realizó a los 0 (cero), 5, 10, y 15 días después del trasplante (ddt). Los rizotrones se colocaron al aire libre con presencia de sol a una altitud aproximada de 2220 msnm y una temperatura promedio de 20 ◦C.
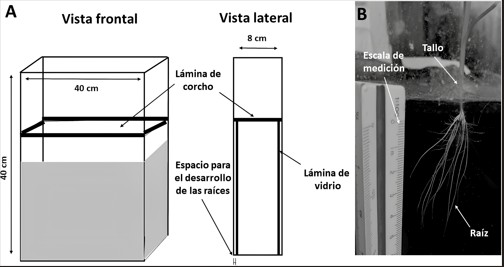
Figura 2.
Características del rizotrón construido. A. Dimensiones del recipiente tanto de la vista frontal y lateral. B. Vista frontal de plántula de Typha creciendo en el rizotrón.
2.4 Condiciones de crecimiento
Cada rizotrón se llenó con 8 L de solución Hoagland 1/2 de fuerza para simular las condiciones naturales con las que crecen en el sitio de colecta (Hoagland y Arnon, 1938), a los que se adicionaron soluciones hasta obtener concentraciones de 50, 100 y 200 ppm de plomo y 10, 20, 40 ppm de cromo.
Las concentraciones de las soluciones de los metales se eligieron de acuerdo con la tolerancia de la especie reportada en la bibliografía y con los rangos encontrados de los metales en los estudios previos de caracterización de agua, suelo, sedimento y raíz de Typha latifolia en la Laguna de Yahuarcocha (Oquendo y cols., 2020).
Se utilizaron como tratamiento control aquellas plántulas que crecieron únicamente en solución Hoagland estándar al 50 %. Los experimentos de germinación y arquitectura de raíz de Typha latifolia se realizaron en el laboratorio de investigaciones ambientales de la Universidad Técnica del Norte (LABINAM).
2.5 Análisis de las imágenes
Las fotografías secuenciales de todas las raíces en los tiempos especificados de registro (0, 5, 10 y 15 días de trasplante) se procesaron en el programa ImageJ y su extensión SmartRoot. Las variables evaluadas fueron: Número de Raíces, Área Total (cm2) y Longitud Total (cm) del sistema radical de las plántulas.
2.6 Análisis estadístico
Con los datos obtenidos del porcentaje de germinación de las semillas de Typha latifolia, los efectos de plomo y cromo en la germinación y los efectos de estos metales pesados sobre crecimiento de las raíces (en rizotrón), se realizaron tres análisis de varianza de clasificación simple.
El primero comparó la germinación de semillas en agua destilada (Control 1 y 2) respecto a la germinación con tratamiento pregerminativo —semillas hidratadas en agua salina (1 % de NaCl) por 24 h—, tanto en el sitio 1 como en el sitio 2. El segundo y tercer análisis de varianza determinó el efecto de las diferentes concentraciones de metales pesados (plomo y cromo) sobre las variables porcentaje de germinación de semillas (en el caso del segundo análisis de varianza) y número de raíces, área y longitud de la raíz (para el tercer análisis de varianza).
Posteriormente, se realizó una prueba de Tukey para cada análisis de varianza. Los datos se sometieron a la verificación del cumplimiento de las premisas de normalidad y homogeneidad de varianzas, mediante las pruebas de Shapiro-Wilk y Levene, respectivamente. El nivel de significancia usado fue de 0,05 y el programa informático empleado fue Statistica versión 10.
3 Resultados y Discusión
3.1 Germinación
Las semillas de Typha latifolia sometidas a tratamiento pregerminativo, es decir aquellas que se hidrataron en agua salina (1 % de NaCl) por 24 h, y posteriormente se hidrataron con agua destilada por 20 días, procedentes del Sitio 1 germinaron en un 86, 5 % ± 9, 2 % de desviación estándar; mientras que aquellas semillas procedentes del Sitio 2 presentaron porcentajes de germinación similares de 81, 4 % ± 5, 9 % de desviación estándar.
Si se compara con las semillas que solo se hidrataron en agua destilada por 20 días, cuyos valores de germinación disminuyeron hasta 60, 4 % (±5, 7 % de desviación estándar) para el Control 1 y hasta 57, 2 % (±5, 5 % de desviación estándar) para el Control 2 (Figura 3).
No se evidenciaron diferencias significativas entre los porcentajes de germinación de las semillas procedentes de los dos sitios seleccionados, pero sí se observaron diferencias significativas de las semillas provenientes de estos dos sitios (columnas a) respecto a sus respectivos controles (1 y 2) cuyas semillas no recibieron tratamiento pregerminativo (columnas b).
En relación con los porcentajes de germinación bajo los efectos de diferentes concentraciones de metales pesados durante su fase de hidratación (Figura 4A), los resultados (que presentan sus respectivas desviaciones estándar) respecto a la adición de plomo fueron de 47, 4 ± 8, 7 % de germinación en concentraciones de 50 ppm, de 40, 7 ± 8, 0 % en 100 ppm, y disminuyeron hasta los 22, 1 ± 4, 8 % en 200 ppm de plomo.
El porcentaje de germinación del tratamiento control (tratamiento pregerminativo + hidratación) fue de 84, 0 ± 9, 2 %. Se evidencian diferencias estadísticamente significativas entre el tratamiento control (a), las concentraciones de 50 y 100 ppm (b) y la concentración de 200 ppm de plomo (c) (Figura 4A).
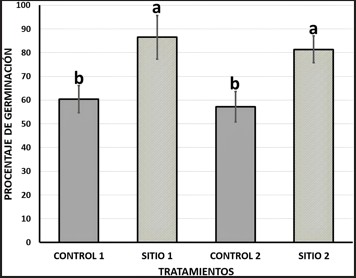
Figura 3.
Porcentaje de germinación de semillas de Typha latifolia de la Laguna de Yahuarcocha. Las semillas control (1 y 2, columnas señaladas por b) se hidrataron durante 20 días, mientras que las semillas de los sitios 1 y 2 (señaladas con a) se sometieron a hidratación previa con agua salina (1 % de NaCl) por 24 h, como tratamiento pregerminativo.
Las letras distintas representan diferencias significativas entre los tratamientos (p < 0, 05).
La germinación en 10 ppm de cromo fue baja, alcanzando valores de 25, 4 ± 7, 3 %. Con 20 ppm de cromo, el porcentaje disminuyó hasta los 18, 2 ± 5, 3 %. Finalmente, en concentraciones de 40 ppm de cromo la germinación fue 13, 2 ± 4, 9 %.
El porcentaje de germinación del tratamiento control (tratamiento pregerminativo + hidratación) fue de 84, 0 ± 9, 2 % (Figura 4B). En este caso, las diferencias significativas detectadas se presentaron entre el tratamiento control (a) y las tres concentraciones de cromo usadas en el experimento (b): 10, 20 y 40 ppm.
3.2 Arquitectura de la raíz
Dentro del experimento del efecto del plomo sobre el número de raíces de las plántulas que crecieron en el rizotrón, no se detectaron diferencias estadísticamente significativas (ns), aunque en números absolutos se incrementó la cantidad de raíces desde el día del trasplante (cero ddt) hasta los 15 ddt que culminó la evaluación (Figura 5A).
Los resultados (en todos los casos se presentan con los respectivos datos de desviación estándar) muestran que el tratamiento control incrementó ligeramente el número de raíces de 8, 3 ± 0, 6 raíces hasta los 9, 3 ± 2, 3 raíces a los 15 ddt. El mayor incremento ocurrió en concentraciones de 50 ppm de plomo, desde las 9, 0 ± 1, 0 raíces (a los cero ddt) hasta las 14, 7 ± 4, 0 raíces a los 15 ddt. En concentraciones de 100 ppm de plomo, el número promedio de raíces no experimentó variación (7, 7 ± 0, 9 raíces) durante todo el experimento. No se evidenciaron diferencias significativas en cuanto al número de raíces entre los distintos tratamientos (50, 100 y 200 ppm de plomo), incluyendo la comparación de estos con el tratamiento control (Figura 5A).
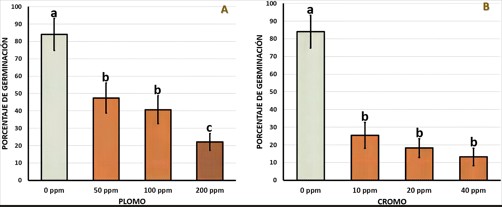
Figura 4.
Porcentaje de semillas germinadas de T. latifolia con los tratamientos: A plomo, B cromo. Se muestran los valores medios y la desviación estándar. Las letras distintas muestran diferencias significativas según la prueba de Tukey (p < 0, 05). El experimento se replicó tres veces (n = 3).
De manera similar, se registró un ligero incremento del número de raíces en presencia de cromo añadido al medio de cultivo, sin embargo, a diferencia del caso del plomo, el mayor incremento se identificó en la mayor concentración de cromo (40 ppm), donde el número de raíces varió ligeramente, aunque sin diferencias significativas, desde las 9, 0 ± 1, 7 hasta las 13, 7 ± 1, 5 al final del experimento (15 ddt). En este caso tampoco se evidenciaron diferencias estadísticas en cuanto al número de raíces entre los distintos tratamientos (10, 20 y 40 ppm de cromo), incluyendo la comparación de estos con el tratamiento control (Figura 5B).
El promedio del área total de la raíz (cm2) se incrementó entre aproximadamente tres y seis veces en los 15 días de evaluación, tanto en el tratamiento control, como en los tratamientos de 50, 100 y 200 ppm de plomo añadido. El mayor incremento del área total de la raíz se evidenció en concentraciones de 100 ppm de plomo, donde los valores pasaron de 4, 00 ± 2, 1 cm2 hasta los 24, 8 ± 7, 8 cm2.
Por el contrario, el menor incremento se presentó en concentraciones de 200 ppm de plomo, con valores iniciales de 6, 5 ± 3, 3 cm2 y finales de 13, 4 ± 7, 7 cm2. Sin embargo, no se detectaron diferencias significativas entre los cuatro tratamientos (Figura 6A).
En presencia de cromo añadido al medio de cultivo, no se registró incremento en el área total de las raíces a ninguna concentración de cromo (10, 20 y 40 ppm), ya que los valores permanecieron constantes (Figura 6B). Solo el promedio del área total de las raíces del tratamiento control incrementó su valor desde los 5, 4 ± 3, 7 cm2, hasta los 18, 0 ± 2, 9 cm2, por lo que se detectaron diferencias significativas entre el control (a) y cada uno de los tres tratamientos experimentales con 10, 20 y 40 ppm y cromo (b).
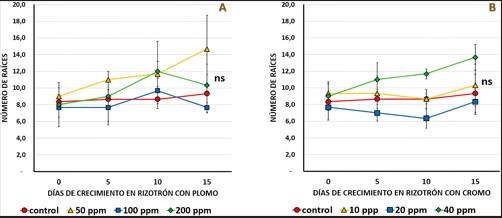
Figura 5.
Variación en el número de raíces de T. latifolia en presencia de diferentes concentraciones de plomo (A) y cromo (B) en el medio de cultivo. Se muestran los valores medios y la desviación estándar. No se presentan diferencias significativas según la prueba de Tukey al 0, 05; n = 3.
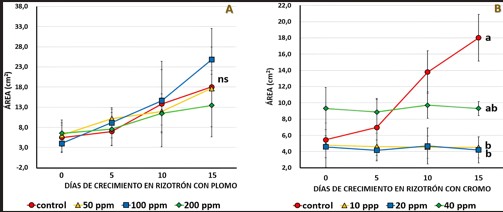
Figura 6.
Variación del área de la raíz de T. latifolia en presencia de diferentes concentraciones de plomo (A) y cromo
(B). Se muestran los valores medios y desviación estándar. Letras diferentes muestran diferencias significativas según la prueba de Tukey al 0, 05; n = 3.
La longitud total de la raíz (cm) ante concentraciones diferenciales de plomo en el medio de cultivo presentó un incremento constante a lo largo del experimento en todos los tratamientos, que fue ligeramente mayor en las concentraciones de 50 ppm y 100 ppm de plomo, con valores de 22, 4 ± 2, 2 cm al inicio y 52, 9 ± 16, 4 cm al final; y 19, 2 ± 3, 5 cm al inicio y 51, 1 ± 16, 7 cm, respectivamente, al finalizar el experimento. No se identificó la existencia de diferencias significativas entre los tratamientos (Figura 7A).
Por otra parte, la adición de distintas concentraciones de cromo a la solución Hoagland produjo un incremento de los valores de la longitud total de la raíz en concentraciones de 40 ppm de cromo (de 27, 4 ± 5, 7 cm hasta 35, 4 ± 6, 8 cm), y un ligero incremento de la longitud de la raíz en concentraciones de 10 ppm de cromo (de 16, 5 ± 3, 6 cm hasta 20, 4 ± 6, 1 cm).
Por el contrario, en concentraciones de 20 ppm de cromo la longitud de la raíz disminuyó de 17, 4 ± 4, 9 a 15, 0 ± 1, 9 cm, durante los 15 días de evaluación, producto de la muerte de las raíces laterales antes contabilizadas, que determinaron que el promedio de la longitud final sea menor. El mayor incremento se midió en el tratamiento control que pasó desde los 25, 0 ± 11, 9 cm hasta los 42, 6 ± 21, 2 cm de longitud en 15 días de crecimiento (Figura 7B).
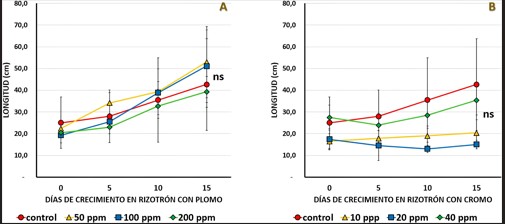
Figura 7.
Variación de la longitud de la raíz de T. latifolia en presencia de diferentes concentraciones de plomo (A) y cromo (B); se muestran los valores medios y desviación estándar. No se observan diferencias significativas según la prueba de Tukey al 0, 05; n = 3.
3.3 Discusión
Varios factores pueden afectar a la planta madre durante el desarrollo de la semilla y provocar cambios en las características de germinación (Baskin y Baskin, 2014). En este sentido, la plasticidad fenotípica se considera uno de los principales medios de adaptación de las semillas a las condiciones ambientales cambiantes a las que se ven expuestas (Gratani, 2014).
Por ejemplo, en semillas maduras de Typha latifolia, la germinación tradicional se realizaba únicamente hidratándose en agua destilada; sin embargo, el tratamiento pregerminativo de hidratación en solución de NaCl al 1 % por 24 h incrementó significativamente la germinación en comparación con el tratamiento tradicional, en un promedio de 25, 2 %, coincidiendo con los incrementos en la germinación descritos por Semenova (2014). Posiblemente esta solución podría actuar neutralizando el efecto de inhibidores potenciales de la germinación y así retardar el crecimiento de microorganismos que afectan negativamente a la germinación (Lorenzeny cols., 2000).
Según USDA (2016), las semillas de T. latifolia alcanzan porcentajes altos de germinación si se siguen los procedimientos correctos, descartándose la escarificación mecánica que según Royal Botanical Gardens, Kew (2016) no incide en el incremento de la germinación, ya que las semillas de la espadaña son lo suficientemente permeables al agua como para desencadenar la germinación. El alto porcentaje de germinación de sus semillas podría deberse a que esta especie no presenta ningún tipo de latencia (Stewart y cols., 1997); aunque Nishihiro y cols. (2004) mencionan que en Typha angustifolia, una especie muy similar a T. latifolia, se han observado mecanismos de latencia fisiológica que podrían ser comunes para todo el género Typha (Baskin y Baskin, 2014).
La germinación con semillas procedentes de los dos sitios analizados no presenta diferencias significativas ya que la Laguna de Yahuarcocha es de tipo no estratificado, en el que sus aguas están mezcladas a lo largo de todo el año, ya sea por influencia de los vientos o por los afluentes que descargan en la laguna, como consta en el Plan de Manejo de la Laguna Yahuarcocha; por lo que con base en la germinación de T. latifolia, los dos sitios corresponden a una población única ubicada dentro de la laguna.
Con relación al efecto de los metales pesados sobre la germinación, los resultados (Figuras 4A y 4B) muestran que tanto el plomo como el cromo, en las concentraciones analizadas, disminuyeron significativamente la germinación. A menudo estos metales pesados tienen efectos inhibidores sobre este proceso, como lo demostró ? y Pandey y cols. (2008). El plomo, por ejemplo, en concentraciones de 50 ppm disminuyó un 43 % la germinación, y a la mayor concentración analizada (200 ppm) la disminución fue del 74 %.
La marcada disminución en la germinación podría deberse a que el plomo (Pb), un metal no esencial, causa toxicidad en las plantas durante mucho tiempo, con cambios adversos en la morfología y germinación de semillas, así como en actividades enzimáticas (Nas y Ali, 2018). Estos efectos son más prominentes con el aumento de la concentración y una exposición más prolongada. Después de reaccionar con el grupo sulfhidrilo, el plomo inhibe las actividades de las enzimas al producir especies reactivas de oxígeno (ROS) que provocan estallidos oxidativos (Zulfiqar y cols., 2019). Gautam y cols. (2010) determinaron que en semillas de Oryza sativa la disminución de la germinación se debió a la inhibición de la producción de actividad de α-amilasa, lo que a su vez inhibe el proceso de degradación del almidón, lo que también podría presentarse en plantas gramíneas y graminoides (Sharma y cols., 2022) como en el caso de las especies de Typhaceae.
La disminución de la germinación es mucho mayor en presencia de cromo, ya que con solo 10 ppm la germinación se redujo en un 70 %, y con 40 ppm de cromo la germinación decayó en un 85 %. Los efectos tóxicos del cromo comprometen la fisiología de la germinación de las semillas (Zaranyikay Nyati, 2017). Sin embargo, Rout y cols. (2000) demostraron que, pese a la disminución de la germinación inicial, las semillas pueden alcanzar tolerancia y aclimatación al cromo, sobre todo cuando las plantas madre provienen de sitios contaminados en relación con sitios no contaminados, características propias de las especies conocidas como hiperacumuladoras.
Por otra parte, la tolerancia a los metales pesados también depende de condiciones genéticas de cada planta. En el estudio publicado por Chengy cols. (2008) en 12 genotipos de Oryza sativa y de Zhang (2015) en especies acuáticas y palustres como: Phragmites australis, Arundo donax, Cyperus alternifolius y Alisma plantago-aquatica, los resultados mostraron una gran variabilidad de respuestas adaptativas, aunque en general el índice de germinación disminuyó significativamente con el aumento de las concentraciones de cromo. Pan y cols. (2008) mencionan que las respuestas sin patrones predecibles frente a mayores niveles de cadmio, cromo, mercurio, son respuestas que dependen de la constitución genética de dichas plantas.
En relación con la arquitectura de la raíz, el crecimiento del sistema radical de T. latifolia en los rizotrones permitió establecer cambios en la estructura de la raíz como respuesta a diferentes concentraciones de plomo y cromo. La solución de Hoagland, utilizada como medio para determinar la estructura de la raíz, a su vez permitió recrear las condiciones fisicoquímicas nutricionales de la Laguna de Yahuarcocha.
Las raíces post embrionarias se formaron dentro de los 5 días posteriores al trasplante y continuaron creciendo 15 y 20 días después, estableciendo un sistema de raíces altamente ramificadas y funcionales.
Con respecto a las plántulas expuestas a concentraciones diferentes de plomo, el número promedio de raíces no sufrió una disminución, incluso en concentraciones de 200 ppm (Figura 5A), mostrando gran tolerancia a este metal. Buta y cols. (2011) reportaron resultados similares en ensayos con plantas de Eichhornia crassipes expuestas a plomo, en las que no se evidenció un decrecimiento en el desarrollo de la raíz por la presencia de plomo, concluyendo que se trata de una especie acuática tolerante, que se utiliza en procesos de depuración de aguas residuales.
En contraste, estudios realizados en Hydrocotyle umbellata una especie acuática, reportan que la exposición a los metales cromo y plomo, en diferentes concentraciones, provocaron disminución en la productividad total de la biomasa. También se observó que en concentraciones altas de cromo el sistema radical cambió de color a marrón oscuro, además de producir necrosis foliar (Yongpisanphop y cols., 2005). De igual forma, estudios realizados en Fagus sylvatica mostraron que la elongación y biomasa de la raíz fueron significativamente reducidas en suelos con concentraciones de 44 ppm de plomo; además, la arquitectura de la raíz tuvo una morfología anormal, con un desarrollo de pelos radicales fuertemente inhibidos (Breckle y Kahle, 1992; Kumar Yadav y cols., 2021).
Los resultados de los tratamientos de las plántulas de T. latifolia expuestas a cromo no evidenciaron una disminución del número promedio de raíces, mostrando tolerancia de T. latifolia a este metal pesado. Sin embargo, muchas plántulas tuvieron un crecimiento anómalo (aspecto raquítico) de la raíz y un marcado amarillamiento de las hojas al final del experimento. En un estudio similar, en el que se colocaron plántulas de Arabidopsis thaliana en diferentes concentraciones de cromo, estas fueron más tolerantes al estrés por el metal en concentraciones menores; sin embargo, el incremento gradual de la concentración de cromo generó inhibición del crecimiento (Martínez-Trujillo y cols., 2013). Es así como Ortiz-Castro y cols. (2007) reportan que el cromo en el sistema radicular y arquitectura en plántulas de Arabidopsis thaliana en concentraciones mayores a 200 µM (60 ppm) —concentración mayor a la del presente experimento— detuvo el crecimiento de raíces, produciendo el amarillamiento de las hojas (clorosis), afectación similar a la detectada la presente investigación.
El cromo está reportado como un metal muy tóxico para las plántulas, que causa deficiencia en la absorción de metales y nutrientes del suelo y su posterior transporte y así lo evidencia la literatura científica. Por ejemplo, en el caso de Pistia stratiotes la exposición de cromo causó un efecto tóxico de inhibición del crecimiento, elongación y estructura anómala de la raíz (Mufarrege y cols., 2010); mientras que en la especie Cicer arietinum, la exposición al cromo causó una disminución gradual de la longitud de la raíz mientras se iba incrementando la concentración de 20 a 100 ppm (Medda yKumar Mondal, 2017).
El área de la raíz (Figura 6A) y la longitud total de la raíz (Figura 7A), se incrementaron ligeramente ante la presencia de plomo, sin diferencias significativas entre los tratamientos (incluyendo el control), lo que confirma la alta tolerancia de T. latifolia al plomo y ratifica el uso ecológico que se le da a esta planta, como es la remoción de nutrientes y contaminantes en sistemas naturales o artificiales de tratamiento de aguas.
Por otra parte, la presencia de concentraciones de cromo detuvo el crecimiento de las plántulas en el rizotrón a lo largo de los 15 días de evaluación, ocasionando que el área total de la raíz (Figura 6B) y su longitud total (Figura 7B) permanecieran constantes. El tratamiento control, mientras tanto, presentó un incremento significativo del área de la raíz, lo que demuestra que el crecimiento es normal cuando el cromo no está presente en la solución nutritiva.
En el presente estudio se pudo evidenciar que tanto la germinación de las semillas de T. latifolia como el crecimiento del sistema radical de las plántulas expuestas al plomo, presentaron germinación y crecimiento, por lo que se pueden considerar tolerantes, al menos para estos dos aspectos, permitiéndoles sobrevivir en ambientes contaminados por este metal pesado (Brankovic´ y cols., 2011). Las semillas y plántulas expuestas a cromo fueron menos tolerantes (en la germinación y el crecimiento radical), sin embargo, esta tolerancia podría incrementar cuando las plantas se desarrollen en ambientes con mayores concentraciones de cromo (tolerancia por aclimatación). Las características mencionadas de T. latifolia brindan a esta especie los atributos para ser usada en sistemas de tratamiento de remediación ambiental de aguas contaminadas.
4 Conclusiones
La aplicación de algunos tratamientos pregerminativos aumenta significativamente el porcentaje de germinación en comparación con las semillas colocadas simplemente en agua destilada. Se asume que las poblaciones de Typha latifolia pertenecen a una misma población ecológica por su porcentaje de germinación con los tratamientos aplicados. Asimismo, la exposición a plomo y cromo causa una disminución del porcentaje de germinación, especialmente este último.
El uso sistemático de rizotrones permitió evidenciar el desarrollo secuencial de la raíz fuera de su hábitat natural y controlar variables para el análisis. Las concentraciones de metales a los que fueron expuestas las plantas no evidenciaron cambios en el número de las raíces y longitud de estas, sin embargo, la exposición al cromo sí afectó el área total de las raíces de esta especie con respecto al control, lo que causó la muerte de varias plántulas, probablemente al ver reducida su área radical en procesos como absorción de agua y nutrientes.
Agradecimientos
Al personal del Laboratorio de Fisiología Vegetal de la Universidad de La Habana, y a la Universidad Técnica del Norte.
Contribución de los autores
M.A.G.: Conceptualización, análisis formal, investigación, metodología, visualización, escritura – borrador original, escritura – revisión y edición. A.V.S.: Conceptualización, análisis formal, investigación, metodología, visualización, escritura – borrador original, escritura – revisión y edición. V.P.V.: Conceptualización, análisis formal, metodología, visualización, escritura – borrador original, escritura – revisión y edición.
Referencias
Armengaud, P., Zambaux, K., Hills, A., Sulpice, R., Pattison, R. J., Blatt, M. R., y Amtmann, A. (2009). Ez-rhizo: Integrated software for the fast and accurate measurement of root system architecture. Plant Journal, 57(5), 945–956. Online: https:// h7.cl/1nP4q
Baligar, V. C., Fageria, N. K., y Elrashidi, M. A. (1998). Toxicity and nutrient constraints on root growth. HortScience, 33(6), 960–965. Online: https://h7.cl/1nP4t
Barceló, J., y Poschenrieder, C. (1992, January). Respuestas de las plantas a los contaminantes: “la fitorremediación”. Suelo y Planta, 2, 345–361. Online: https://h7.cl/1nP4a
Baskin, C. C., y Baskin, J. M. (2014). Seeds: Ecology, biogeography, and evolution of dormancy and germination. Academic Press.
Bourgeois, B., Hugron, S., y Poulin, M. (2012). Establishing a moss cover inhibits the germination of Typha latifolia, an invasive species, in restored peatlands. Aquatic Botany, 100, 76–79. Online: https://h7.cl/1iOuV
Brankovic´, S., Pavlovic´-Muratspahic´, D., Topuzovic´, M., Glišic´, R., Bankovic´, D., y Stankovic´, M. (2011). Environmental study of some metals on several aquatic macrophytes. African Journal of Biotechnology, 10(56), 11956–11965. Online: https://h7.cl/1iOv0
Breckle, S.-W., y Kahle, H. (1992). Effects of toxic heavy metals (cd, pb) on growth and mineral nutrition of beech (Fagus sylvatica l.). Vegetatio, 101, 43–53. Online: https://h7.cl/1iOv6
Busch, J., Mendelssohn, I. A., Lorenzen, B., Brix, H., y Miao, S. (2006). A rhizotron to study root growth under flooded conditions tested with two wetland cyperaceae. Flora: Morphology, Distribution, Functional Ecology of Plants, 201(6), 429–439. Online: https://h7.cl/1iOv7
Buta, E., Paulette, L., Miha˘iescu, T., Buta, M., y Cantor, M. (2011). The influence of heavy metals on growth and development of Eichhornia crassipes species, cultivated in contaminated water. Notulae Botanicae Horti Agrobotanici Cluj-Napoca, 39(2), 135–141. Online: https://h7.cl/1nP4O
Chen, Y.-L., Hong, X.-Q., He, H., Luo, H.-W., Qian, T.-T., Li, R.-Z., . . . Yu, H.-Q. (2014). Biosorption of cr (vi) by Typha angustifolia: Mechanism and responses to heavy metal stress. Bioresource Technology, 160, 89–92. Online: https://h7.cl/1nP4S
Cheng, W., Zhang, G., Yao, H., y Zhang, H. (2008). Genotypic difference of germination and early seedling growth in response to cd stress and its relation to cd accumulation. Journal of Plant Nutrition, 31(4), 702–715. Online: https://h7.cl/1iOvh
Franco, J. A., Bañón, S., Vicente, M. J., Miralles, J., y Martínez-Sánchez, J. J. (2011). Root development in horticultural plants grown under abiotic stress conditions a review. Journal of Horticultural Science and Biotechnology, 86(6), 543–556. Online: https://h7.cl/1iOvm
Gautam, M., Sengar, R. S., Chaudhary, R., Sengar, K., y Garg, S. (2010). Possible cause of inhibition of seed germination in two rice cultivars by heavy metals pb2+ and hg2+. Toxicological and Environmental Chemistry, 92(6), 1111–1119. Online: https://h7.cl/1nP50
Gratani, L. (2014). Plant phenotypic plasticity in response to environmental factors. Advances in Botany, 2014, 1–17. Online: https://h7.cl/1iOvt
Han, J., Chen, F., Zhou, Y., y Wang, C. (2015). High pb concentration stress on Typha latifolia growth and pb removal in microcosm wetlands. Water Science and Technology, 71(11), 1734–1741. Online: https://h7.cl/1iOvw
Hoagland, D. R., y Arnon, D. I. (1938). Preparing the nutrient solution. The Water-Culture Method for Growing Plants Without Soil, 347, 29–31.
Kahle, H. (1993). Response of roots of trees to heavy metals. Environmental and Experimental Botany, 33(1), 99–119. Online: https://h7.cl/1iOvE
Kumar Yadav, V., Santos-González, J., y Köhler, C. (2021). Int-hi-c reveals distinct chromatin architecture in endosperm and leaf tissues of Arabidopsis. Nucleic Acids Research, 49(8), 4371–4385. Online: https://h7.cl/1nP5k
Lobet, G., Pagès, L., y Draye, X. (2011). A novel image-analysis toolbox enabling quantitative analysis of root system architecture. Plant Physiology, 157(1), 29–39. Online: https://h7.cl/1iOvM
Lorenzen, B., Tinerella, P. P., Newman, S., y Steward, K. K. (2000). Seed germination of two everglades species, Cladium jamaicense and Typha domingensis. Aquatic Botany, 66(3), 169–180. Online: https://h7.cl/1iOvU
Martínez-Trujillo, M., Cárdenas-González, J. F., González-Morales, S., y Flores-Hernández, A. (2013). Respuestas morfogénicas de las raíces de Arabidopsis thaliana al estrés de cr(vi). Revista Chilena de Historia Natural, 86, 207–219. Online: https://h7.cl/1iOvZ
Medda, S., y Kumar Mondal, N. (2017). Chromium toxicity and ultrastructural deformation of Cicer arietinum with special reference of root elongation and coleoptile growth. Annals of Agrarian Science, 15(3), 396–401. Online: https://h7.cl/1iOw2
Mufarrege, M. M., Hadad, H. R., y Maine, M. A. (2010). Response of Pistia stratiotes to heavy metals (cr, ni, and zn) and phosphorous. Archives of Environmental Contamination and Toxicology, 58(1), 53–61. Online: https://h7.cl/1iOwh
Nas, F., y Ali, M. (2018). The effect of lead on plants in terms of growing and biochemical parameters: A review. MOJ Ecology & Environmental Sciences, 3(4), 265–268. Online: https://h7.cl/1nP62
Nishihiro, J., Teramura, A., Hosomi, M., y Nakagawa, M. (2004). Germination characteristics of lakeshore plants under an artificially stabilized water regime. Aquatic Botany, 79(4), 333–343. Online: https://h7.cl/1iOwI
Oquendo, R., Fernández, L., y Pérez, L. (2020). Concentración de plomo y cromo en poblaciones de Typha latifolia l. (typhaceae) en el lago yahuarcocha; imbabura. Revista Cubana de Ciencias Biológicas, 8, 1–12. Online: https://h7.cl/1iOwR
Ortiz-Castro, R., Contreras-Cornejo, H. A., MacíasRodríguez, L., y López-Bucio, J. (2007). Effects of dichromate on growth and root system architecture of Arabidopsis thaliana seedlings. Plant Science, 172(4), 684–691. Online: https://h7.cl/1nP6B
Pal Singh, H., Du, J., y Verma, S. K. (2013). Chromium toxicity and tolerance in plants. Environmental Chemistry Letters, 11(3), 229–254. Online: https://h7.cl/1iOwZ
Pan, X. B., Zhu, C., y Cheng, C. (2008). Assessment of techniques for screening alfalfa cultivars for aluminum tolerance. Euphytica, 164(2), 541–549. Online: https://h7.cl/1iOx0
Pandey, S. N., Nautiyal, B. D., y Sharma, C. P. (2008). Pollution level in distillery effluent and its phytotoxic effect on seed germination and early growth of maize and rice. Journal of Environmental Biology, 29(2), 267–270. Online: https://h7.cl/1iOx5
Rout, G. R., Samantaray, S., y Das, P. (2000). Effects of chromium and nickel on germination and growth in tolerant and non-tolerant populations of Echinochloa. Chemosphere, 40, 855–859. Online: https://h7.cl/1nP6N
Royal Botanical Gardens, Kew. (2016). Seed information database. Online: http://data.kew.org/sid/
Sasmaz, A., Obek, E., y Hasar, H. (2008). The accumulation of heavy metals in Typha latifolia grown in a stream carrying secondary effluent. Ecological Engineering, 33(3-4), 278–284. Online: https:// h7.cl/1nP6T
Semenova, A. (2014). Method for producing aquatic plants for the purification of contaminated water (EP: PCT n.o WO131930 A1).
Sharma, A., Singh, H., Kaur, N., Singh, N., Singh, P., y Bhardwaj, R. (2022). Heavy metal induced regulation of plant biology: Recent insights. Physiologia Plantarum, 174(e13688). Online: https://h7.cl/1nP6Z
Smith, P. P. (2018). The book of seeds: A life-size guide to six hundred species from around the world. The University of Chicago Press.
Stewart, H., Miao, S. L., Colbert, M., y Carraher, C. E. (1997). Seed germination of two cattail (Typha) species as a function of everglades nutrient levels. Wetlands, 17, 116–122. Online: https://h7.cl/1nP72
USDA. (2016). Plants database | usda plants guide. Online: http://plants.usda.gov/java/
Yongpisanphop, J., Kruatrachue, M., y Pokethitiyook, P. (2005). Toxicity and accumulation of lead and chromium in Hydrocotyle umbellata. Journal of Environmental Biology, 26(1), 79–89. Online: https://h7.cl/1iOxs
Zaidi, A., Ahmad-Wani, P., y Saghir-Khan, M. (2012). Toxicity of heavy metals to legumes and bioremediation. Springer.
Zaranyika, M. F., y Nyati, W. (2017). Uptake of heavy metals by Typha capensis from wetland sites polluted by effluent from mineral processing plants: implications of metal–metal interactions. 3 Biotech, 7(5), 1–11. Online: https://h7.cl/1nP7a
Zhang, G. (2015). Influence of heavy metal wastewater on seed germination of different wetland plants. Journal of China Agricultural University, 20, 167–178. Online: https://h7.cl/1nP7c
Zulfiqar, U., Farooq, M., Hussain, S., Maqsood, M., Hussain, M., Ishfaq, M., . . . Anjum, M. Z. (2019). Lead toxicity in plants: impacts and remediation. Journal of Environmental Management, 250, 109557. Online: https://h7.cl/1nP7j
Información adicional
redalyc-journal-id: 4760
Enlace alternativo
https://revistas.ups.edu.ec/index.php/granja/article/view/6441 (html)