Artículo Científico
Valorización de la cáscara de banano (Musaparadisiaca) como materia prima para la producción de biopolímeros
Valorization of banana peel (Musa paradisiaca) as a raw material for biopolymer production
Valorización de la cáscara de banano (Musaparadisiaca) como materia prima para la producción de biopolímeros
La Granja. Revista de Ciencias de la Vida, vol. 43, núm. 1, pp. 166-177, 2026
Universidad Politécnica Salesiana

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 10 Agosto 2022
Revisado: 12 Diciembre 2022
Publicación: 01 Marzo 2026
Resumen:
El uso de materiales plásticos y sus efectos negativos en la sociedad ha incrementado los estudios acerca de biomateriales como material sustituto. Durante la presente investigación se desarrolló una biopelícula obtenida a partir de cáscara de plátano (PBCP) y posteriormente se evaluaron varias propiedades. Mediante centrifugado se extrajo pulverizado de plátano variando el número de revoluciones por minuto (rpm) 900, 1500 y 3000. Para la formación de la PBCP se utilizó glicerol en concentraciones de 30 % y 50 %, adicionalmente se controlaron las temperaturas de calenta- miento en 70, 80, y 90 ◦C. Los resultados mostraron que debido a la baja cantidad proteica del pulverizado de plátano los tratamientos no muestran desnaturalización térmica, y los tratamientos sometidos a 3000 rpm y 90 ◦C muestran mayores valores de viscosidad (57570 Pa·s). Por el contrario, en el análisis de cinética de absorción de humedad se determinó que las variables de temperatura y de rpm no influyen en los resultados obtenidos; no obstante, mientras mayor es el porcentaje de glicerol en la película, mayor es la tasa de absorción de humedad pasando de (3, 1 × 10−10 a 3, 7 × 10−10) cm2/s y de (3, 9 × 10−10 a 4, 9 × 10−10) cm2/s, respectivamente. En la permeabilidad de vapor de agua se evidencia una diferencia significativa en los niveles de glicerol. Los valores de PVA de las PBCP en las diferentes condiciones oscilaron entre (2, 8 a 5, 0) g·mm/(kPa·h·m2). Por lo expuesto anteriormente se determina que es posible realizar PBCP y para mejorar los resultados de viscosidad se recomienda usar un emulsionante para evitar la reaglomeración de las moléculas.
Palabras clave: Biodegradabilidad, biopolímero, plastificante, producción, reología.
Abstract:
The use of plastic materials and their negative effects on society has increased the studies about biomaterials as substitute material; during the present research, a biofilm obtained from banana peel (PBCP) was developed and subsequently several properties were evaluated. By means of centrifugation, banana pulverized was extracted by varying the number of revolutions per minute (rpm) 900, 1500, and 3000. Glycerol was used for the formation of PBCP at concentrations of 30 % and 50 %; additionally, the heating temperatures were controlled at 70, 80, and 90 ◦C. The results showed that due to the low protein content of the banana pulverized, the treatments did not show thermal dena- turation; the treatments subjected to 3000 rpm and 90 ◦C denoted higher viscosity values (57570 Pa·s). On the other hand, in the analysis of moisture absorption kinetics, it was determined that the temperature and rpm variables do not influence the results obtained; however, the higher the percentage of glycerol in the film, the higher the rate of moisture absorption, going from (3.1 × 10−10 to 3.7 × 10−10) cm2/s and (3.9 × 10−10 to 4.9 × 10−10) cm2/s, respectively. In the water vapor permeability, a significant difference in the levels of glycerol is evidenced; the PVA values of the PBCP in the different conditions ranged between (2.8 to 5.0) g·mm/(kPa·h·m2). From the above, it is determined that it is possible to perform PBCP, and to improve the viscosity results it is recommended to use an emulsifier to avoid the reagglomeration of the molecules.
Keywords: Biodegradability, biopolymer, plasticizer, production, rheology.
Forma sugerida de citar: (APA)
Taco, J., Jiménez, R. y Soto, M. (2026). Valorización de la cáscara de banano (Musa paradisiaca) como materia prima para la producción de biopolímeros. La Granja: Revista de Ciencias de la Vida. Vol. 43(1):166-177. https://doi.org/10.17163/lgr.n43.2026.09.
1 Introducción
Los mercados globalizados y las exigencias de los consumidores por productos de calidad, no solo higiénico-sanitarios sino amigables con el ambiente, han llevado a la industria de alimentos a un cambio de paradigma de producción a fin de adaptarse a las necesidades de sus clientes (Ramos y cols., 2020). Una de las estrategias que la agroindustria usa para cumplir este propósito es la producción más limpia (PML), que permite el reciclaje interno o externo de los residuos para aumentar la eficiencia en los procesos y reducir riesgos ambientales (Hoofy cols., 2018; Lucero-Murillo y cols., 2026).
Otra problemática relacionada con la producción y consumo de alimentos es el uso progresivo de empaques desechables que, pese a sus ventajas como precio económico, resistencia a la oxidación, especificidad de función y versatilidad, causa grave impacto al medio ambiente (Mejía Osorio, 2020). Además, según Tuárez y cols. (2022), los aditivos adicionados para mejorar las propiedades funcionales de los polímeros usados en envases migran a los alimentos, generando potenciales riesgos en la salud humana. En este contexto, actualmente los investigadores trabajan en la búsqueda de sustitutos de empaques no biodegradables, y los esfuerzos combinados han dado como resultado la obtención de empaques biodegradables que se producen a partir de los biopolímeros (Ospina, 2015).
Por otra parte, la escala de desechos es amplia en el sector agrícola; por ejemplo, los residuos de cultivos y los desechos de las plantas que permanecen en el campo posterior a la cosecha (Mikus y Galus, 2022). Por ello, los principales biopolímeros degradables usados para el desarrollo de películas comestibles, recubrimientos, envases y empaques de alimentos son los polisacáridos, con especial énfasis a los derivados de residuos orgánicos (Eixenberger y cols., 2022).
Por ejemplo, Taghavi Kevij y cols. (2021) desarrollaron películas comestibles funcionales utilizando gelatina y diferentes concentraciones (0, 3, 6, 9, 12 y 15)% de pulverizado de cáscara de naranja (PCN). El espesor, el porcentaje de humedad y la permeabilidad al vapor de agua de las películas de la gelatina incrementaron a medida que aumentaba el contenido de PCN en la formulación. Las películas con mayor contenido de PCN mostraron mayor resistencia y menor elongación. Además, sus resultados demuestran que el contenido de antioxidantes, especialmente de compuestos fenólicos, mejoró significativamente al incorporar PCN. En cuanto a la actividad antimicrobiana de las películas de gelatina contra Staphylococcus aureus y Escherichia coli, mejoró en películas con mayor incorporación de PCN. Por los resultados anteriormente descritos se evidencia que la piel de naranja tiene un potencial para producir biopelículas.
Otra investigación referente al tema la desarrolló Dao y cols. (2022), en la cual se extrajo pectina de las cerezas de café, la cual, pese a formar aproximadamente el 50 % de la pulpa de café no es aprovechada, convirtiéndose en uno de los desechos agrícolas más abundantes en la industria de alimentos. La variedad seleccionada para esta investigación fue Coffea arabica L., del cual se utilizó el método ecológico para obtener pectina y celulosa. Los resultados evidenciaron que el procedimiento de extracción con solvente acidificado a un pH de 3,1 y a 84,3 ◦C durante 4,3 h permite recuperar 16,7 % de pectina de las pulpas de café. Por otro lado, si se aplica un procedimiento de dos pasos que incluye un pretratamiento con vapor a 170 ◦C durante 30 min y un blanqueo utilizando H2O2 a 40 ◦C durante 10 h, contribuye a obtener el 54 % de rendimiento de celulosa de pulpas de café. Las biopelículas que se obtuvieron a partir de mezclas de pectina de café y celulosa microcristalina presentaron una superficie lisa, transparencia elevada, resistencia a la tracción de 3 MPa y alargamiento del 4 %.
Con base a lo anteriormente expuesto se ha definido que es posible obtener biopolímeros a partir de desechos orgánicos, y considerando la alta producción de plátano en el Ecuador (Pacheco y cols., 2021), se seleccionó la cáscara de plátano (Musa paradisiaca) para esta investigación que plantea como objetivo el desarrollo y evaluación de un biopolímero a partir de un residuo de la industria de alimentos.
2 Materiales y Métodos
2.1 Obtención del almidón de cáscara de plátano
El residuo orgánico seleccionado para la investigación fue la cáscara de plátano debido a su alto contenido de carbohidratos (Anhwange y cols., 2009). Para lo cual la cáscara de plátano se obtuvo en la ciudad de Santo Domingo – Ecuador, recolectadas de varios comerciantes que se dedican a la elaboración y expendio de chifles. Luego se lavaron cuidadosamente con agua tibia para eliminar todos los materiales extraños, se rebanaron y picaron. Una vez finalizado el pretratamiento se realizó una hidrólisis ácida utilizando ácido clorhídrico. Posteriormente, se agregó agua desionizada a un vaso de precipitados que contenía la pulpa hidrolizada, dejando reposar durante unas 8 horas.
El proceso de extracción se llevó a cabo utilizando una centrífuga (DM0412P con capacidad de 100 a 4500 rpm), seleccionando 3 niveles de rpm (900, 1500, 3000) según la investigación de Altemimi (2018) quien además estandarizó el tiempo de centrifugación en 15 minutos. Las muestras centrifugadas se filtraron a través de un tamiz de 180 µm. A continuación, se dejó sedimentar el filtrado y se añadió sosa cáustica para separar el contenido de proteínas del almidón e igualmente para neutralizar la acidez del almidón restante. Después de esto, se agregó agua desionizada varias veces para eliminar el exceso de sosa cáustica mediante un proceso de lavado.
El almidón húmedo resultante se secó en un deshidratador de bandejas (DESHI 10); la temperatura de secado se estandarizó a 55 ◦C durante 6 h con base a la investigación de Juárez Chunga (2022), luego se pulverizó (PULVERIZER 10, motor de 1,5 HP) hasta que el 95 % del pulverizado pasara por un tamiz de 120 µm, según la norma técnica ecuatoriana para harina de trigo NTE INEN 612 (NTE INEN 612, 2006).
Seguidamente se almacenó el pulverizado empacado al vacío para mantener el 10 % de humedad.
2.2 Preparación de película biopolimérica de la cáscara de plátano (PBCP)
La preparación de las películas biopoliméricas de la cáscara de plátano (PBCP) se llevó a cabo en condiciones atmosféricas. Según el método usado por Kim y Min (2012), la solución formada por el pulverizado extraído a diferentes rpm (900, 1500, 3000) y el 30% o 50%(p/p) de glicerol se calentó a 70, 80 o 90 ◦C durante 45 minutos. Las películas se moldearon pipeteando la mezcla sobre placas de teflón (14 cm × 10 cm) que descansaban sobre una superficie nivelada de cerámica; la cantidad de solución formadora de película se seleccionó para producir películas con espesor entre 0,2 a 0,3 mm. Transcurrida una hora, la película se colocó en una cámara de temperatura/humedad 23 ± 2◦C y 50 % HR durante 48 horas.
2.3 Análisis de reología
Las propiedades reológicas de las películas se determinaron siguiendo el método de Hendrix y cols. (2012) utilizando un reómetro rotacional (RheolabQC) y una placa paralela de acero inoxidable
(304) de 45 mm. Las soluciones formadoras de película se depositaron en una placa Peltier, se colocó agua desionizada en la trampa de disolvente y se extendió una capa de aceite en los bordes exteriores de las suspensiones para limitar la evaporación del agua.
Se determinaron los módulos elásticos (G′) y la viscosidad (G′′) mientras se elevaba gradualmente la temperatura desde 20 ◦C hasta 90 ◦C con una velocidad de rampa de 1 ◦C/min. Todas las mediciones
fueron realizadas en condiciones de frecuencia de 1 rad/s y deformación del 2 %.
2.4 Análisis de cinética de absorción de humedad
Se aplicó el método de Talja, Helen, y cols. (2008) con algunas modificaciones. Las muestras de película se prepararon con medidas de 5 cm por 15 cm, manteniendo un espesor de 0, 2 ± 0, 03 mm, las cuales posteriormente fueron sometidas a 45 ± 2◦C en horno secador sobre gel de sílice hasta que las muestras mantuvieron un peso constante. A continuación, se acondicionaron a 23 ± 2◦C en un desecador con solución saturada de nitrato de potasio para garantizar HR del 94 %. Paso seguido se calculó la absorción de humedad (AH) mediante la siguiente fórmula:
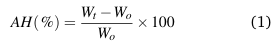
Donde Wo y Wt fueron los pesos de las muestras secas y las muestras en el tiempo t, respectivamente. Posteriormente, según el método de Talja, Peura, y cols. (2008) se calculó el coeficiente de difusión (D) para el agua en las muestras de película, a partir de la pendiente de Wt/Wα mediante la siguiente ecuación:
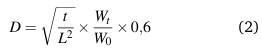
Donde L es la mitad del espesor de la película y Wα es el peso del agua absorbida en el equilibrio.
2.5 Permeabilidad al vapor de agua
La permeabilidad al vapor de agua (PVA) de la película se midió según el método E96-92 de la Sociedad Americana de Pruebas y Materiales (McHughy Krochta, 1994). Brevemente, se agregaron 6 mL de agua destilada a una copa de muestra de poliacrilato de metilo (diámetro interno: 46 mm, diámetro externo: 87 mm, longitud: 21 mm), y se cubrió herméticamente la copa con la película de biopolímero de cáscara de plátano (PBCP). Las copas de muestra se colocaron en una cámara estática de temperatura 23 ± 2◦C equipada con ventiladores ajustados a una velocidad de aire de 152 m/min. Adicionalmente, la HR se registró con un higrómetro (Modelo THDx).
2.6 Prueba de biodegradabilidad
La biodegradabilidad de las películas de biopolímeros se realizó a temperatura ambiente con una duración de 30 días de acuerdo con el procedimiento aplicado por Iguardia (2013). Las pruebas aplicadas fueron degradabilidad en intemperie y degradabilidad por agua de río.
Para el primer ensayo se procedió a pesar las muestras y colocarlas en recipientes de vidrio sin tapa para que reposaran al aire libre por 30 días. Para la prueba de biodegradabilidad por agua se pesaron las muestras y se sumergieron en un recipiente de vidrio con agua, se taparon los recipientes y se dejaron en reposo por 30 días. Transcurrido el tiempo en ambos ensayos se pesaron las muestras y se procedió a calcular el porcentaje de biodegradabilidad mediante la Ecuación 3.
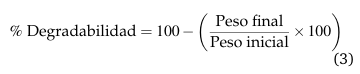
2.7 Análisis estadístico
Todas las medidas se calcularon utilizando el promedio de los tres valores. Los factores de tratamiento en este trabajo fueron: factor A con los diferentes rpm (900, 1500, 3000) a las cuales se obtuvo el pulverizado de cáscara de plátano; factor B al 30 % o 50 % (p/p) de glicerol añadido en la formulación; factor C la temperatura de calentamiento de la película 80, 90 y 100 ◦C, por lo que se aplicó un diseño completamente al azar con arreglo factorial A × B × C, con 18 tratamientos y 3 repeticiones, cada uno arrojando un total de 54 unidades experimentales.
3 Resultados y Discusión
3.1 Análisis de reología
Para el análisis, la temperatura inicial de las suspensiones fue de 20 ± 2◦C y las temperaturas durante las pruebas reológicas oscilaron entre 20 ◦C a 90 ◦C, con rangos de temperatura aumentada (∆T ) de 20 ± 1, 25 ± 2 y ±25◦C y un tiempo aproximado de 50 segundos.
Los valores G′ de las suspensiones de PBCP homogeneizadas a 1 atm se presentan en la Figura 1. Los valores de G′ disminuyeron a medida que la temperatura aumentaba de 20 ◦C hasta llegar a 90 ◦C. La
temperatura modifica la distribución de tamaños de los agregados/partículas de biopolímeros, así como la estructura de agregación (Sanchez y cols., 1999). Las suspensiones formuladas a partir del almidón centrifugado a 3000 rpm exhibieron valores de G′ más altos que los otros tratamientos. Al respecto, Tatirat y Charoenrein (2011) mencionan que la hidrólisis ácida y la centrifugación acelerada pueden provocar la descomposición de los biopolímeros.
El patrón descendente de los valores de G′ para las suspensiones podría explicarse por la pérdida de estructura de red dentro de los polímeros de PBCP. Un mayor número de rpm en el proceso de extracción del biopolímero de la cáscara del plátano puede dar como resultado la pérdida de la red de biopolímero y consecuentemente una disminución, debido al alto potencial de energía. Sin embargo, las tasas de disminución de las suspensiones tratadas con 900, 1500 y 3000 rpm fueron relativamente pequeñas (Figura 1) y presentan mejores resultados de G′ con un 30% de glicerol.
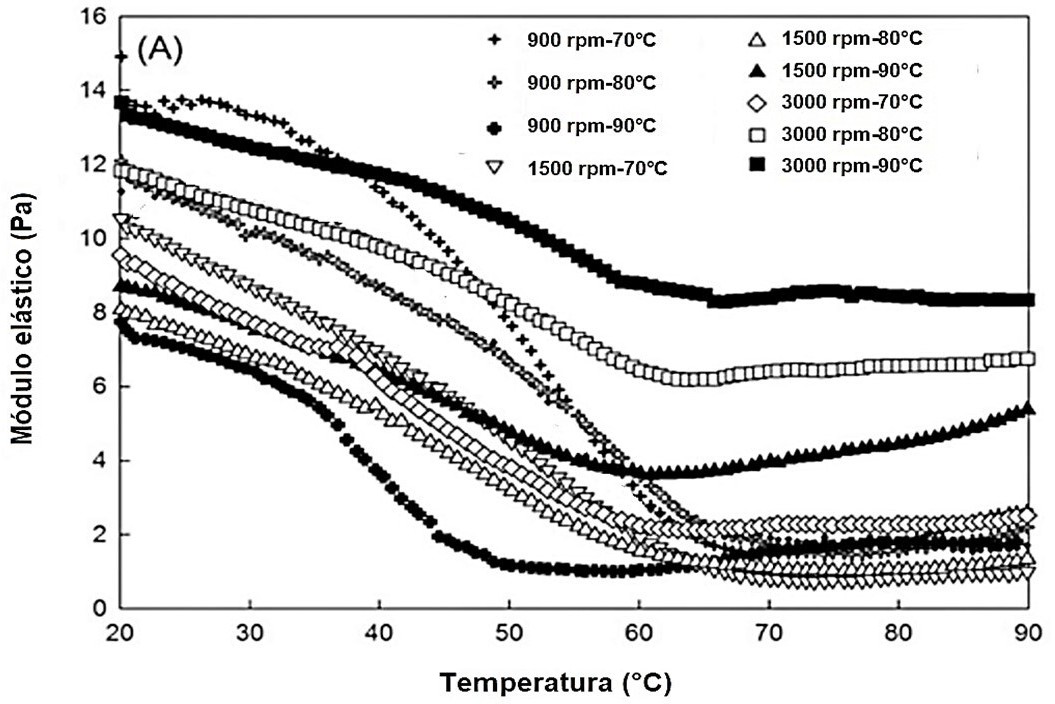
Figura 1.
Módulo elástico (G′) de las suspensiones filmógenas preparadas con pulverizado centrifugado de diferentes revoluciones por minuto (900, 1500, 3000) y calentado a diferentes temperaturas de 70, 80, 90 ◦C.
Según lo manifestado por Sanchez y cols. (1999) y posteriormente por Hendrix y cols. (2012), la reagrupación de las pequeñas partículas ralentizó la tasa de pérdida de la red de biopolímeros debido a que inmediatamente después del tratamiento, los biopolímeros en las suspensiones homogeneizadas fueron muy pequeños. Sin embargo, estas pequeñas partículas de biopolímero podrían reagruparse rápidamente y formar redes a través de enlaces de hidrógeno, interacciones hidrofóbicas e interacciones carga-carga, especialmente si el plastificante utilizado es el glicerol.
En el presente estudio, la temperatura de prueba de reología aumentó gradualmente de 20 ◦C a 90 ◦C; se seleccionó este rango de temperaturas porque las PBCP se calientan a esta temperatura durante la preparación. El calentamiento puede causar la desnaturalización de las proteínas en las suspensiones, aumentando las interacciones proteína-proteína y reduciendo la movilidad segmentaria de las mismas (Pérez-Gago, 2012). Sin embargo, la influencia de la desnaturalización de la proteína, que normalmente ocurre a altas temperaturas manifestándose con un aumento de G′, no se observó en el presente experimento de reología y esto podría deberse a una baja concentración de proteína (∼ 0, 43 %) en la suspensión. Los resultados sugieren que calentar las muestras entre 70 ◦C a 90 ◦C durante 45 min puede incitar la desnaturalización térmica de las proteínas en las suspensiones filmógenas, pero en esta experimentación no fue difícil obtener las propiedades físicas que se esperan.
Los valores de G′ para todas las suspensiones se mantuvieron relativamente constantes entre 4 a 8 Pa en todo el rango de temperatura evaluado. Se reportaron resultados similares por Sablani y cols. (2009) y Hendrix y cols. (2012) durante estudios previos para la formación de películas, utilizando suspensiones de biopolímeros de cáscaras de manzana y harina de mostaza desgrasada, respectivamente.
Respecto a las suspensiones elaboradas con pulverizado a 3000 rpm y a temperatura de homogenización de película de 90 ◦C, estas presentaron valores de viscosidad superiores a los demás tratamientos (Figura 2). Por otra parte, las suspensiones trabajadas a 1500 rpm con 90 ◦C tienen un perfil de viscosidad semejante a las elaboradas a 3000 rpm y 90 ◦C; no obstante, la medida de la viscosidad fue significativamente mayor en estas últimas suspensiones.
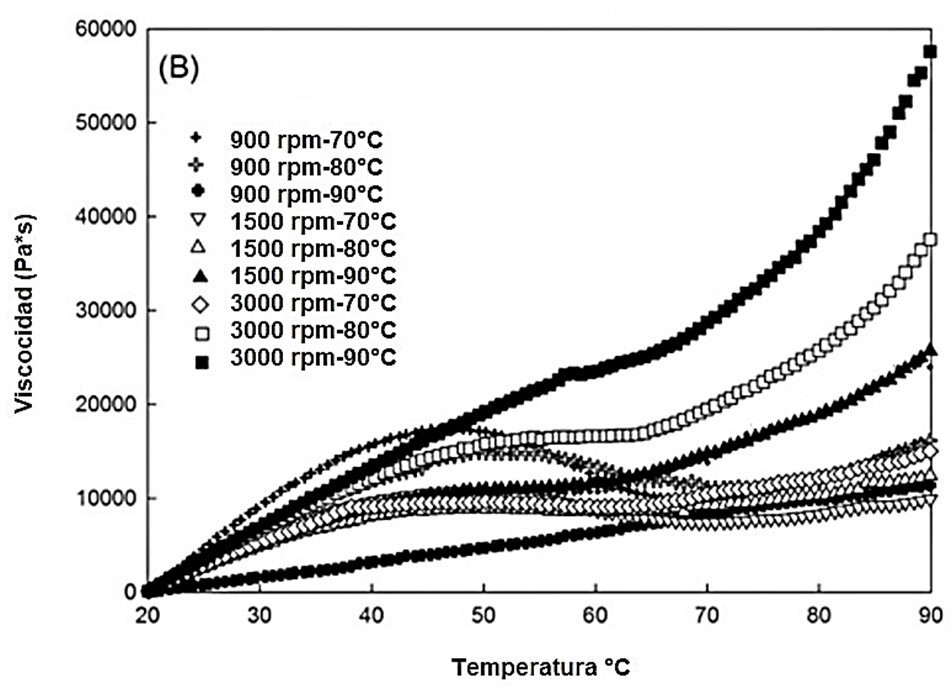
Figura 2.
Viscosidad (G′′) de las suspensiones filmógenas preparadas con pulverizado centrifugado de diferentes revoluciones por minuto (900, 1500, 3000) y calentado a diferentes temperaturas de 70, 80, 90 ◦C.
Además, en el análisis se evidencia que mientras más alta es la temperatura del ensayo, mayor es la viscosidad de las muestras. Se obtuvo la viscosidad 57 570 Pa·s en las suspensiones sometidas a temperatura de 90 ◦C, siendo el mayor valor presentado. Esto podría deberse a aumentos en la reticulación intermolecular entre los polímeros como la celulosa presente en la PBCP en temperaturas bajas, lo que da como resultado la formación de un gel (Coma ycols., 2003).
3.2 Análisis de cinética de absorción de humedad
En cuanto a los resultados sobre absorción de agua, las muestras acondicionadas a 94 % HR y 23 ◦C en función del tiempo (Figura 3) revelan que la absorción de agua fue mayor en las PBCP que contenían 50 % de glicerol, es decir, estas películas presentan un mayor rango de hidratación. La inclusión de moléculas de glicerol polares e hidrofílicas, que pueden actuar como centros hidrofílicos fuertes que se unen fácilmente y con fuerza al agua, probablemente dará como resultado un aumento en la hidrofilia en la superficie y facilitará la absorción de moléculas de agua (Kang y cols., 2015).
Además, las características polares e hidrófilas semejantes de las moléculas de agua y las matrices de la película de biopolímero pueden conducir a una fuerte cohesión entre las moléculas y las matrices debido a los enlaces de hidrógeno (Kang y cols., 2015).
Los resultados de absorción de agua se vieron fuertemente afectados por la concentración de glicerol, pero no por los parámetros de temperatura de calentamiento y número de rpm de centrifugación previa a la obtención del pulverizado (Figura 3). Este hallazgo está de acuerdo con un estudio anterior que demostró que la absorción de agua de las películas de biopolímero hechas de cáscaras de manzana no estuvo afectada por niveles variados de presión HPH (138–207 MPa) ni temperatura (Sablani y cols., 2009).
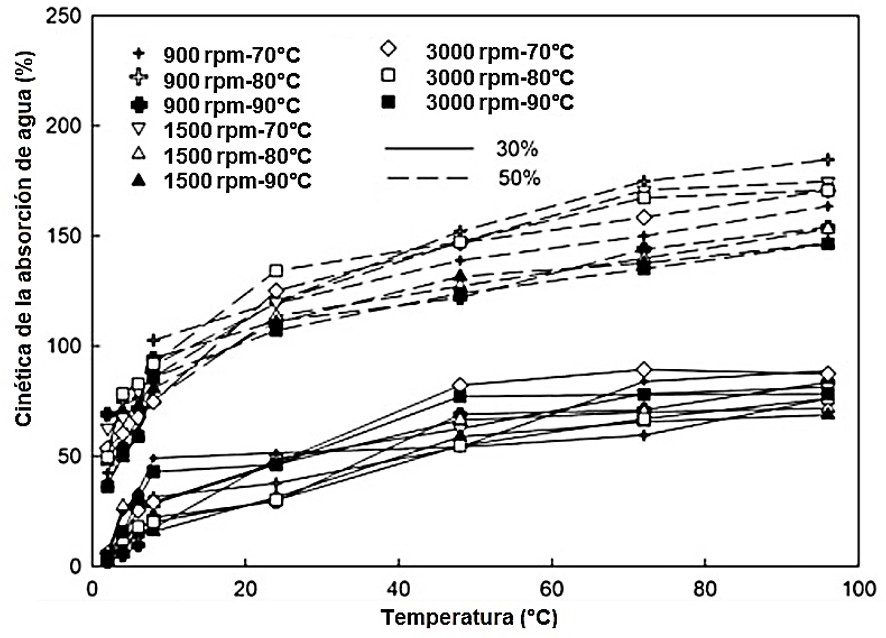
Figura 3.
Cinética de la absorción de agua de películas a base de cáscara de plátano plastificadas con glicerol formadas a partir de las suspensiones filmógenas.
Los valores D para las películas estudiadas acondicionadas al 94 % de HR que contenían 30 % y 50 % de glicerol fueron de 3, 1 × 10−10 a 3, 7 × 10−10 cm2/s y de 3, 9 × 10−10 a 4, 9 × 10−10 cm2/s, respectivamente. El volumen disponible para la expansión de moléculas de agua en la matriz de la película aumenta a medida que incrementa la cantidad de glicerol como plastificante. Los presentes hallazgos indican que las películas de PBCP se pueden formular para proporcionar una tasa de migración de humedad deseada cambiando la cantidad de glicerol.
Se compararon los valores D calculados en esta investigación con los de otras investigaciones en las cuales se desarrollaron películas de biopolímeros, por ejemplo, las películas basadas en cáscara de manzana (0, 82–2, 62 × 10−10 cm2/s) realizada por Sablani y cols. (2009), pero estos valores son inferiores a las de las películas de celulosa microfibrilada (6, 8 × 10−10 cm2/s) desarrollada por Minelli y cols. (2010), o a los datos 12, 6–31, 8 × 10−10 cm2/s presentados por Taghavi Kevij y cols. (2021) en una película de queratina, que también difieren con los valores D 36, 3 × 10−10 cm2/s calculados en películas de almidón de amilosa en la investigación de Muscat ycols. (2014).
3.3 Prueba de permeabilidad al vapor de agua
Los resultados de PVA de las películas se muestran en la Tabla 1.
Los espesores de las películas que contenían 30 % y 50 % de glicerol fueron de 0, 2 ± 0, 03 mm y no difirieron significativamente (p > 0, 05). La PVA fue generalmente más alta en películas con 50 % de glicerol (Tabla 1); esto podría explicarse debido a que la transmisión de vapor de agua a través de una
película hidrófila depende tanto de la difusividad como de la solubilidad de las moléculas de agua en la matriz de la película (Pak y cols., 2020).
La mayor PVA en las películas con 50 % de glicerol en comparación con aquellas con 30 % de glicerol puede ser el resultado de una disminución en las atracciones intermoleculares, un mayor espacio entre cadenas moleculares y una movilidad más alta en la matriz de la película debido a la inclusión de más moléculas de glicerol entre las cadenas poliméricas (Caicedo y cols., 2022). Esta inclusión de glicerol podría suscitar la difusividad del agua mediante el sistema compuesto de la película de PBCP a través de una disminución en la cantidad de obstáculos que bloquean las moléculas de agua a medida que pasan a través de la red de biopolímeros (Sothornvit y Krochta, 2005).
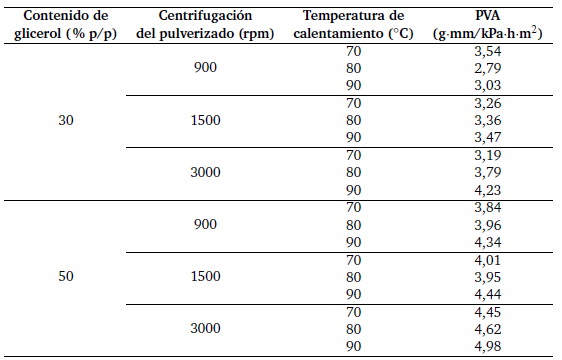
Tabla 1.
Permeabilidad del vapor de agua (PVA) de películas a base de cáscara de plátano.
La elevada hidrofilia de las moléculas de glicerol, y las diferentes temperaturas de calentamiento y rpm, no influyeron en la PVA en ninguna de las concentraciones de glicerol (p > 0, 05). Como se describió anteriormente, se puede suponer que hay una reducción en el tamaño de partícula a medida que aumentan las revoluciones por minuto y la temperatura. Un tamaño de partícula reducido podría disminuir la PVA, lo que podría explicar por qué en estas circunstancias es más difícil la formación de un camino que las moléculas de agua deben cruzar para difundirse a través de la matriz (Dangarany cols., 2006). Sin embargo, en el presente estudio, con el aumento de la temperatura o el número de revoluciones por minuto no se observó tal efecto en la PVA sobre las películas, probablemente debido a la reaglomeración de pequeñas partículas de biopolímero durante la formación de la película (Garcíay cols., 2020). Se sugiere el uso de un emulsionante para evitar la reaglomeración.
Los valores de PVA de las películas de PBCP en las diferentes condiciones oscilaron entre 2,8 y 5,0 g·mm/kPa·h·m2 (Tabla 1), que es comparable con los hallazgos de estudios anteriores que utilizaron aislado de proteína de soya, harina de mostaza desgrasada, gelatina de pescado y cáscara de manzana realizados por Sablani y cols. (2009), Hendrixy cols. (2012), Cho y Rhee (2004) y Kim y Min (2012), respectivamente.
Sin embargo, los resultados de PVA en las películas de PBCP fueron superiores comparados con los estudios que incluyeron metilcelulosa (6,8 g·mm/kPa·h·m2), gelatina de piel de cerdo (0, 1–6, 3 g·mm/kPa·h·m2), caseinato de sodio (4,0 g·mm/kPa·h·m2) y cera de abejas (3, 8–7, 0 g·mm/kPa·h·m2), datos referenciales con base a las investigaciones de Talja, Helen, y cols. (2008) y Avena-Bustillos y cols. (2006). Por otro lado, Vargas y cols. (2008) reportaron valores más altos de PVA en estudios que usaron almidón de papa (8,0 g·mm/kPa·h·m2) y alginato de algas pardas (14,0 g·mm/kPa·h·m2).
La PVA alta en el presente estudio se puede atribuir a la naturaleza hidrófila de los polímeros de PBCP y la naturaleza polar del glicerol. Un PVA alto podría limitar el uso de estas películas para alimentos con niveles de humedad bajos o intermedios (Valero-Valdivieso y cols., 2013). Por lo tanto, se sugiere más investigación para desarrollar métodos para la producción de películas con sensibilidad reducida a la humedad que se puedan aplicar a alimentos con altos niveles de humedad.
3.4 Prueba de biodegradabilidad
De acuerdo a los datos obtenidos se determina que la película de 3000 rpm, calentamiento de 90 ◦C y 50 % de glicerina presenta mayor degradabilidad tanto a la intemperie como en medio acuoso, con un porcentaje de 47 % y 55 %, respectivamente, lo cual es equiparable con la investigación realizada por Garcia (2019) que determinó porcentajes de biodegradabilidad en películas de biopolímero de 43 % a 47 % en un lapso de un mes.
4 Conclusiones
La absorción de agua en el equilibrio fue mayor y la barrera contra la humedad fue menor en las películas con 50 % de glicerol. Por lo tanto, debido a que la sensibilidad a la humedad de las películas de PBCP estuvo fuertemente influenciada por la concentración de glicerol, la sensibilidad de la película se puede modular variando la concentración de glicerol.
Referente a la biodegradabilidad, las PBCP presentan valores similares a los de otras investigaciones, pero se debe medir su eficiencia en condiciones de anaerobiosis. Además, se recomienda utilizar un emulsificante para mejorar la reaglomeración y posteriormente realizar nuevas mediciones para identificar con mayor precisión el efecto de las temperaturas de calentamiento en las propiedades de las películas de biopolímeros de cáscara de plátano.
Contribución de los autores
J.T.: Conceptualización, investigación, metodología, recursos, supervisión, validación, escritura – revisión y edición. R.J.: Curación de datos, adquisición de financiación, administración del proyecto. M.S.: Análisis formal, visualización, escritura – borrador original.
Referencias
Altemimi, A. B. (2018). Extraction and optimization of potato starch and its application as a stabilizer in yogurt manufacturing. Foods, 7(2), 2. Online: https://doi.org/10.3390/foods7020014
Anhwange, B. A., Ugye, T. J., y Nyiaatagher, T. D. (2009). Chemical composition of musa sapientum (banana) peels. Electronic Journal of Environmental, Agricultural and Food Chemistry, 8(6), 437–442. Online: https://n9.cl/kpc56
Avena-Bustillos, R. j., Olsen, C. w., Olson, D. a., Chiou, B., Yee, E., Bechtel, P. j., y McHugh, T. h. (2006). Water vapor permeability of mammalian and fish gelatin films. Journal of Food Science, 71(4), E202–E207. Online: https://doi.org/10.1111/j.1750-3841.2006.00016.x
Caicedo, C., Díaz-Cruz, C. A., Jiménez-Regalado, E. J., y Aguirre-Loredo, R. Y. (2022). Effect of plasticizer content on mechanical and water vapor permeability of maize starch/pvoh/chitosan composite films. Materials, 15(4), 1274. Online: https://doi.org/10.3390/ma15041274
Cho, S. Y., y Rhee, C. (2004). Mechanical properties and water vapor permeability of edible films made from fractionated soy proteins with ultrafiltration. Lebensmittel-Wissenschaft Und Technologie. Food Science and Technology. Online: https:// n9.cl/lpztv0
Coma, V., Sebti, I., Pardon, P., Pichavant, F. H., y Deschamps, A. (2003). Film properties from crosslinking of cellulosic derivatives with a polyfunctional carboxylic acid. Carbohydrate Polymers, 51(3), 265–271. Online: https://doi.org/10.1016/ S0144-8617(02)00191-1
Dangaran, K. L., Cooke, P., y Tomasula, P. M. (2006). Effect of protein particle size reduction on the physical properties of co2-precipitated casein films. Journal of Food Science. Online: http://hdl.handle.net/10113/1840
Dao, D. N., Le, P. H., Do, D. X., Dang, T. M. Q., Nguyen, S. K., y Nguyen, V. (2022). Pectin and cellulose extracted from coffee pulps and their potential in formulating biopolymer films. Biomass Conversion and Biorefinery. Online: https://doi.org/ 10.1007/s13399-022-02339-x
Eixenberger, D., Carballo-Arce, A.-F., Vega-Baudrit, J.-R., Trimino-Vazquez, H., Villegas-Peñaranda, L. R., Stöbener, A., . . . Liese, A. (2022). Tropical agroindustrial biowaste revalorization through integrative biorefineries—review part ii: Pineapple, sugarcane and banana by-products in costa rica. Biomass Conversion and Biorefinery. Online: https://doi.org/10.1007/s13399-022-02721-9
Garcia, G. (2019). Obtención de un biopolímero a partir de harina de plátano de desecho (musa x paradisiaca). Online: https://n9.cl/gkcpd (70.)
García, M. A., Rodríguez, M., Castro, C., y de la Paz, N. (2020). Water vapor permeability of chitosan/zeolite composite films as affected by biopolymer and zeolite microparticle concentrations. Journal of Packaging Technology and Research, 4(2), 157–169. Online: https://doi.org/10.1007/ s41783-020-00092-y
Hendrix, K. M., Morra, M. J., Lee, H.-B., y Min, S. C. (2012). Defatted mustard seed meal-based biopolymer film development. Food Hydrocolloids, 26(1), 118–125. Online: https://doi.org/10.1016/j.foodhyd.2011.04.013
Hoof, B. V., Monroy, N., y Saer, A. (2018). Producción más limpia: Paradigma de gestión ambiental. (Primera edición. Universidad de los Andes. ISBN 9786077073598)
Iguardia, C. (2013). Síntesis y caracterización de bioplástico a partir de almidón de banano verd | iica catálogo bioeconomía. Online: https://n9.cl/84drei
Juárez Chunga, A. S. (2022). Efecto del recubrimiento de almidón de maíz nativo (zea mays l.) y de la temperatura de secado sobre características fisicoquímicas y sensoriales de snack de tiras de pimiento morrón rojo (capsicum annuum l.). Online: https://n9.cl/ 4yy9pg (Universidad Privada Antenor Orrego UPAO)
Kang, H. J., Won, M. Y., Lee, S. J., y Min, S. C. (2015). Plasticization and moisture sensitivity of potato peel-based biopolymer films. Food Science and Biotechnology, 24(5), 1703–1710. Online: https://doi.org/10.1007/s10068-015-0221-x
Kim, D., y Min, S. C. (2012). Trout skin gelatin-based edible film development. Journal of Food Science, 77(9), E240–E246. Online: https://doi.org/10.1111/j.1750-3841.2012.02880.x
Lucero-Murillo, J., Manzano-Torres, J., LoaizaMaldonado, I., y Orellana-García, Y. (2026). In vitro propagation of banana (musa spp.) by somatic embryogenesis. La Granja: Revista de Ciencias de la Vida, 43(1), 127–143. doi: https://doi.org/10.17163/lgr.n43.2026.09https://doi.org/10.17163/lgr.n43.2026.07
McHugh, T. H., y Krochta, J. M. (1994). Sorbitolvs glycerol-plasticized whey protein edible films: Integrated oxygen permeability and tensile property evaluation. Journal of Agricultural and Food Chemistry, 42(4), 841–845. Online: https://doi.org/10.1021/jf00040a001
Mejía Osorio, D. C. (2020). Estudio del manejo de residuos plásticos en colombia. Online: https://n9.cl/ d69tg8
Mikus, M., y Galus, S. (2022). Biopolymers from agriculture waste and by-products. En Biopolymers: Recent updates, challenges and opportunities (pp. 111–128). Springer International Publishing. Online: https://doi.org/10.1007/978-3-030-98392-5_6
Minelli, M., Baschetti, M. G., Doghieri, F., Ankerfors, M., Lindström, T., Siró, I., y Plackett, D. (2010). Investigation of mass transport properties of microfibrillated cellulose (mfc) films. Journal of Membrane Science, 358(1–2), 67–75. Online: https://doi.org/10.1016/j.memsci.2010.04.030
Muscat, D., Adhikari, R., Tobin, M. J., McKnight, S., Wakeling, L., y Adhikari, B. (2014). Effect of spatial distribution of wax and peg-isocyanate on the morphology and hydrophobicity of starch films. Carbohydrate Polymers, 111, 333–347. Online: https://doi.org/10.1016/j.carbpol.2014.04.072
NTE INEN 612. (2006). Harina de trigo. requisitos. Online: https://n9.cl/o3mir
Ospina, S. (2015). Biopolímeros y su aplicación en medio ambiente. Revista Colombiana de Biotecnología, 17(2), 2. Online: https://doi.org/10.15446/rev.colomb.biote.v17n2.54295
Pacheco, M. A. M., Montealegre, V. J. G., Romero, H. R. C., y Campoverde, J. M. Q. (2021). Análisis de la participación del banano en las exportaciones agropecuarias del ecuador periodo 2015-2019. Revista Metropolitana de Ciencias Aplicadas, 4(2), 2. Online: https://n9.cl/yaaidr
Pak, E. S., Ghaghelestani, S. N., y Najafi, M. A. (2020). Preparation and characterization of a new edible film based on persian gum with glycerol plasticizer. Journal of Food Science and Technology, 57(9), 3284–3294. Online: https://doi.org/ 10.1007/s13197-020-04361-1
Pérez-Gago, M. B. (2012). Protein-based films and coatings. Online: https://doi.org/10.3390/ polym13050769 (Impreso, 13–77.)
Ramos, T. P., Guevara-Llerena, D. J., SarduyPereira, L. B., y Diéguez-Santana, K. (2020). Producción más limpia y ecoeficiencia en el procesado del cacao: Un caso de estudio en ecuador. Investigación & Desarrollo, 20(1), 135–146. Online: https://doi.org/10.23881/idupbo.020.1-10i
Sablani, S. S., Dasse, F., Bastarrachea, L., Dhawan, S., Hendrix, K. M., y Min, S. C. (2009). Apple peel-based edible film development using a highpressure homogenization. Journal of Food Science, 74(7), E372–E381. Online: https://doi.org/10.1111/j.1750-3841.2009.01273.x
Sanchez, C., Pouliot, M., Renard, D., y Paquin, P. (1999). Uniaxial compression of thermal gels based on microfluidized blends of wpi and heatdenatured wpi. Journal of Agricultural and Food Chemistry, 47(3), 1162–1167. Online: https://doi.org/10.1021/jf980577o
Sothornvit, R., y Krochta, J. M. (2005). 23— plasticizers in edible films and coatings. En Innovations in food packaging (pp. 403–433). Academic Press. Online: https://doi.org/10.1016/ B978-012311632-1/50055-3
Taghavi Kevij, H., Salami, M., Mohammadian, M., Khodadadi, M., y Emam-Djomeh, Z. (2021). Mechanical, physical, and bio-functional properties of biopolymer films based on gelatin as affected by enriching with orange peel powder. Polymer Bulletin, 78(8), 4387–4402. Online: https:// doi.org/10.1007/s00289-020-03319-9
Talja, R. A., Helen, H., Roos, Y. H., y Jouppila, K. (2008). Effect of type and content of binary polyol mixtures on physical and mechanical properties of starch-based edible films. Carbohydrate Polymers. Online: http://dx.doi.org/10.1016/j.carbpol.2007.05.037
Talja, R. A., Peura, M., Serimaa, R., y Jouppila, K. (2008). Effect of amylose content on physical and mechanical properties of potato-starch-based edible films. Biomacromolecules, 9(2), 658–663. Online: https://doi.org/10.1021/bm700654h
Tatirat, O., y Charoenrein, S. (2011). Physicochemical properties of konjac glucomannan extracted from konjac flour by a simple centrifugation process. LWT Food Science and Technology, 44(10), 2059–2063. Online: https://doi.org/10.1016/j.lwt.2011.07.019
Tuárez, M. A., Laz, M. L., Córdova, R. A., y Conforme, J. V. (2022). Migración química desde envases fabricados con polipropileno hacia alimentos grasos. Revista ESPAMCIENCIA ISSN 13908103, 13(1), 1. Online: https://doi.org/10.51260/ revista_espamciencia.v13i1.286
Valero-Valdivieso, M. F., Ortegón, Y., y Uscategui, Y. (2013). BiopolÍmeros: Avances y perspectivas.
Vargas, M., Pastor, C., Chiralt, A., McClements, D. J., y González-Martínez, C. (2008). Recent advances in edible coatings for fresh and minimally processed fruits. Critical Reviews in Food Science and Nutrition, 48(6), 496–511. Online: https://doi.org/ 10.1080/10408390701537344
Información adicional
redalyc-journal-id: 4760
Enlace alternativo
https://revistas.ups.edu.ec/index.php/granja/article/view/6551 (html)