Resumen: La biomasa es una alternativa estudiada para proporcionar fuentes de energía que reemplacen a los combustibles fósiles. El objetivo de esta investigación es optimizar las condiciones de la reacción de hidrólisis ácida para la obtención de glucosa a partir de la biomasa procedente de los residuos de banano, cacao, bagazo de caña de azúcar y palma africana. Las condiciones fueron evaluadas a través de un diseño experimental 2k . Los factores estudiados fueron la temperatura, el tiempo y la concentración de ácido; los niveles mínimo y máximo corresponden a 70 a 120 ◦C, 20 a 150 min y 1 % al 5 % v/v, respectivamente. Además, se realizaron dos réplicas al centro. Las mejores condiciones encontradas para la obtención de glucosa fueron: 120 ◦C, 150 min y 1 % de ácido sulfúrico. El bagazo de caña de azúcar y el raquis de palma africana fueron las biomasas de las que se obtuvo el mayor contenido de glucosa 9 936,48 y 7 745,14, respectivamente. Se discute la influencia de la composición de la biomasa en la cantidad de glucosa obtenida.
Palabras clave: Hidrólisis ácida, biomasa, glucosa, caracterización estructural.
Abstract: Biomass is an alternative to provide energy sources that replace fossil fuels. The objective of this investigation is to optimize the conditions of the acid hydrolysis reaction for obtaining glucose from biomass: banana rachis, cacao pod, African palm rachis, and sugarcane bagasse. The conditions were evaluated through a 2k experimental design. The factors studied were temperature, time, and acid concentration; the minimum and maximum levels correspond to 70 to 120 ◦C, 20 to 150 min, and 1 % to 5 % v/v, respectively. In addition, two replicates were made to the center. The best conditions for obtaining glucose were: 120 ◦C, 150 min and 1 % v/v sulfuric acid. Sugarcane bagasse and African palm rachis were the biomasses from which the highest glucose content was obtained, 9 936.48 and 7 745.14 mg/L, respectively. The influence of biomass composition on the amount of glucose obtained is discussed.
Keywords: Acid hydrolysis, biomass, glucose, structural characterization.
Artículo Científico
Optimización de los factores de hidrólisis ácida para obtener glucosa de los residuos de banano, cacao, palma africana y bagazo de caña de azúcar
Optimization of the acid hydrolysis factors for obtaining glucose from banana, cacao, African palm, and sugarcane bagasse residues
Universidad Politécnica Salesiana

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 14 Diciembre 2021
Revisado: 01 Agosto 2022
Publicación: 01 Marzo 2026
Abril-González, M. F., Vele-Salto, A. M. y Pinos-Vélez, V. (2026). Optimización de los factores de hidrólisis ácida para obtener glucosa de los residuos de banano, cacao, palma africana y bagazo de caña de azúcar. La Granja: Revista de Ciencias de la Vida. Vol. 43(1):178-190. https://doi.org/10.17163/lgr.n43.2026.10.
El cambio en las fuentes de energía constituye un desafío real. Con el objetivo de reducir el consumo de petróleo, la búsqueda de materiales más sostenibles y con menor impacto ambiental a lo largo de su ciclo de vida conduce a la selección de materias primas renovables o a la mejora de los procesos utilizados para obtener los productos finales. El uso de biomasa lignocelulósica, principalmente derivada de residuos agrícolas, ha aumentado en los últimos años debido a que estos residuos son renovables en comparación con las materias primas de origen fósil (Thompson y cols., 2017; Yánez-Iñiguez ycols., 2020). Sin embargo, el principal obstáculo para su utilización es la ausencia de una tecnología de bajo costo capaz de degradar los polisacáridos presentes en la biomasa, de manera que el material lignocelulósico pueda transformarse en azúcares solubles (Adsul y cols., 2020; Loow y cols., 2015; Fabay cols., 2014). En Ecuador, existe una amplia disponibilidad de materia prima renovable derivada de los principales cultivos permanentes del país, como se indica en los datos presentados en el Atlas Bioenergético del Ecuador (2014) (Ministerio de Electricidad y Energía Renovable del Ecuador, 2014), y los cuatro principales se resumen en la Tabla 1.

Tabla 1.
Residuos generados por cultivos permanentes en el Ecuador.
Los residuos indicados en la Tabla 1 pueden provenir tanto del campo como del procesamiento, y es posible obtener biocombustibles de segunda generación que no implican un riesgo para las fuentes alimentarias. El material lignocelulósico está compuesto por celulosa, hemicelulosa y lignina. Estos polímeros contienen numerosos grupos funcionales activos capaces de reaccionar (Odalanowska y cols., 2021; Yogalakshmi y cols., 2022). Los polímeros de celulosa son unidades glicosídicas unidas mediante enlaces β-1,4-glucosídicos, que son muy estables y difíciles de hidrolizar por vía química o enzimática. La hemicelulosa se hidroliza con mayor facilidad que la celulosa y produce pentosas de alto valor, como xilosa y arabinosa. La lignina, por su parte, presenta una estructura polimérica muy compleja (Sun y cols., 2016; Okolie y cols., 2021).
Una de las principales y más comunes tecnologías de tratamiento de biomasa es la hidrólisis ácida; este método es preferido por su bajo costo y su efectividad en el fraccionamiento de las hemicelulosas hasta obtener monómeros, a la vez que induce cambios estructurales en las fracciones (Loow y cols., 2016). En general, se utilizan ácidos sulfúrico, clorhídrico y nítrico, aunque los dos últimos en menor medida. Los tratamientos con altas concentraciones de ácido generan problemas de corrosividad y su manipulación resulta peligrosa; por ello, es más común la aplicación de tratamientos con ácido diluido (Hoang y cols., 2021; Yuan y cols., 2022).
A nivel industrial, la hidrólisis de biomasa constituye una etapa fundamental para la obtención de biocombustibles de segunda generación, como en el caso específico del bioetanol. Por tanto, la mejora del rendimiento hacia monosacáridos, especialmente glucosa, influirá de manera positiva en los procesos de manufactura posteriores (Duque y cols., 2021).
La glucosa es la molécula más abundante de la biomasa en la naturaleza. Al ser la unidad monomérica del biopolímero celulosa, considerado el más abundante, constituye una materia prima sostenible para la producción de combustibles para el transporte, productos químicos y polímeros a base de carbono (Dutta y Bhat, 2022). Su propiedad de solubilidad en agua la convierte en una alternativa prometedora para producir de manera eficiente compuestos químicos y biocombustibles de alto valor. Los productos C6 obtenidos a partir de glucosa son particularmente adecuados, ya que sus síntesis presentan una economía de carbono del 100 % (Liuy cols., 2015).
La Tabla 2 presenta algunos resultados de diferentes investigaciones, verificando que el ácido sulfúrico diluido es el más utilizado; sin embargo, los factores que intervienen en la reacción, tanto la temperatura como el tiempo, suelen ser elevados, lo que implica un mayor consumo energético.
El objetivo de esta investigación es aprovechar la biomasa residual obtenida en grandes cantidades en el Ecuador, principalmente generada a partir de cultivos de banano, cacao, palma africana y caña de azúcar, y proporcionar alternativas para su uso en la producción de biocombustibles u otros productos derivados. Esto contribuirá positivamente al desarrollo de la industria energética en el país, de manera económica, técnica y ambientalmente sostenible. Para ello, se estudia el proceso de hidrólisis ácida diluida mediante un diseño experimental que optimiza los valores de temperatura, tiempo y concentración de ácido, con el fin de maximizar la conversión de glucosa. Además, se analizan estadísticamente las interacciones entre los factores para determinar su influencia, lo que también favorece la toma de decisiones respecto a las condiciones de reacción. Asimismo, se caracterizó cada biomasa estructuralmente para generar una base de datos que permita conocer su composición y sus posibles aplicaciones en la industria, así como su efecto en la conversión a glucosa.
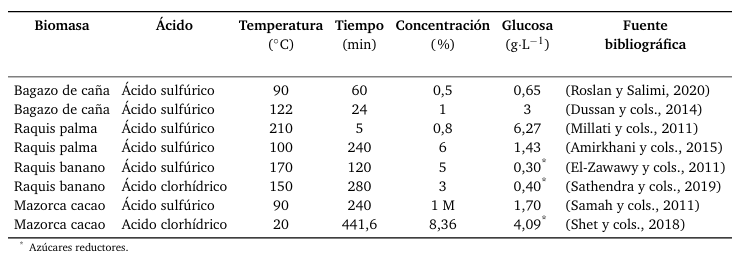
Tabla 2.
Resultados obtenidos de procesos de hidrólisis de biomasa.
2.1 Reactivos
El ácido sulfúrico de grado analítico se adquirió de Fisher Chemical (Center Valley, PA, EE. UU.). La glucosa estándar analítica y el clorito de sodio se adquirieron de Sigma-Aldrich (St. Louis, MO, EE. UU.). El etanol, el tolueno, el ácido acético glacial y el hidróxido de sodio de grado analítico fueron adquiridos de Merck (Darmstadt, Alemania). El agua destilada se obtuvo mediante un destilador Water Still WS 8000 (Boeco, Alemania). El agua tipo I se obtuvo de un sistema de purificación Barnstead Water (Thermo Fisher Scientific, Kansas, EE. UU.).
2.2 Material vegetal y preparación de muestras
La biomasa de banano, cacao y palma aceitera se obtuvo de los cultivos de la “Hacienda San José”, ubicada en la provincia de Los Ríos – Ecuador, km 8,5 Babahoyo Febres Cordero, en las coordenadas 1◦53′15,7′′S, 79◦29′18,8′′W. La variedad de banano utilizada fue Musa acuminata, subgrupo Cavendish del Grupo AAA; la variedad de cacao fue CC N51, y la palma africana pertenecía a la familia Arecaceae, subgrupo Commelinidae.
El bagazo de caña de azúcar se obtuvo en una finca del valle de Yunguilla, al suroeste de Cuenca, en las coordenadas 3◦17′58,843′′S, 79◦17′59,497′′W, siendo la variedad Canalpoa. Las plantas fueron cortadas para recolectar el racimo durante la cosecha. El área de cosecha fue delimitada y los residuos se recolectaron de doce plantas de banano distribuidas aleatoriamente en el terreno. Cada planta se separó en sus diferentes partes: raquis de banano, mazorca de cacao, raquis de palma africana y bagazo de caña, de acuerdo con sus características físicoquímicas, por lo que se esperaban distintas concentraciones de monosacáridos.
Se tomaron muestras de aproximadamente 300 g de cada parte, las cuales fueron almacenadas en bolsas plásticas herméticamente selladas para su transporte al laboratorio, donde se lavaron con agua pura para eliminar residuos químicos (p. ej., pesticidas o insecticidas). Posteriormente, las muestras se cortaron en secciones de aproximadamente 5 mm y se secaron en estufa (marca Innotech, modelo BJPXSummer) a 105 ◦C hasta peso constante, por aproximadamente 24 horas. Luego se trituraron en un molino de corte (ALQUIMIA, modelo MC002) y se tamizaron para obtener un tamaño de partícula máximo de 5 µm. Las muestras preparadas se almacenaron en bolsas plásticas a 2 ◦C hasta su análisis.
2.3 Caracterización estructural
En primer lugar, se eliminó de la biomasa el material extractivo y no estructural para evitar interferencias en los pasos analíticos posteriores (NationalRenewable Energy Laboratory, 2008). Los extractivos se eliminaron de acuerdo con la norma ASTM D1107, utilizando etanol-tolueno como solvente y un equipo de extracción Soxhlet. Se colocaron 7 g de muestra en el cartucho y se añadieron 150 mL de solvente, manteniendo el líquido en ebullición durante 7 horas, tras lo cual la muestra se secó hasta peso constante (ASTM International, 2021).
Una vez eliminados los extractos, se determinó el contenido de lignina insoluble en ácido siguiendo la norma TAPPI 222 (TAPPI, 2006). Se utilizó 1 g de muestra libre de extractos y se le añadieron gradualmente 15 mL de ácido sulfúrico al 72 %. Los carbohidratos fueron hidrolizados y solubilizados por el ácido, mientras que la lignina insoluble se filtró, secó y pesó.
Para determinar el porcentaje de holocelulosa (celulosa y hemicelulosa), se aplicó la norma ASTM D1104, que se obtiene a través de un proceso de cloración para eliminar la lignina. Se emplearon 2,5 g de muestra libre de extractos, 80 mL de agua destilada caliente, seguidos de 0,5 mL de ácido acético y 1 g de clorito de sodio, con cuatro repeticiones de esta adición (ASTM International, 1956). La celulosa se obtuvo a partir de la fracción de holocelulosa mediante la norma TAPPI 212, que consiste en tratar 2 g de holocelulosa libre de extractos con 10 mL de hidróxido de sodio al 17,5 % para degradar la hemicelulosa; su contenido se determinó por diferencia entre holocelulosa y celulosa (TAPPI, 2002).
2.4 Diseño experimental para la reacción de hidrólisis ácida
La hidrólisis ácida se llevó a cabo en un reactor por lotes (THR 250 de alta presión) con capacidad de 50 mL, equipado con manómetro, sensores de temperatura y sistema de agitación mecánica. El material de construcción fue acero inoxidable SS304L recubierto de teflón para reducir la corrosión por ataque ácido.
Se obtuvieron monosacáridos a partir de 3 g de biomasa usando 60 mL de solución acuosa ácida (v/v). Para estudiar la influencia de la concentración de ácido, la temperatura y el tiempo de reacción sobre la cantidad de glucosa recuperada, se aplicó un diseño factorial 2k para cada biomasa. La Tabla 3 presenta el diseño de tres factores con dos niveles por factor aplicado a cada biomasa. Se realizaron dos réplicas en el punto central. Los factores temperatura, tiempo de reacción y concentración de ácido se evaluaron en intervalos de 70–120 ◦C, 20– 150 min y 1–5 % v/v H2SO4, respectivamente. Estas condiciones se aplican a distintas biomasas (raquis de banano, mazorca de cacao, raquis de palma africana y bagazo de caña), y las soluciones obtenidas se filtraron con papel Whatman N°54 y se neutralizaron con solución de hidróxido de sodio al 30 % (p/p). Posteriormente, las muestras fueron analizadas inmediatamente en HPLC.
2.5 Análisis cromatográfico
La concentración de glucosa en los residuos vegetales hidrolizados se analizó en un sistema HPLC (Jasco LC4000) equipado con un termostato (Jasco CO4061), un detector de índice de refracción (IR4030), una bomba cuaternaria (PU4180) y un inyector manual. El volumen de inyección fue de 10 µL. La columna utilizada fue VA 300 / 7,8 Nucleogel, Sugar 810 Ca, (300 × 7,8 mm) (MachereyNagel, Alemania). La temperatura de la columna, el caudal y la concentración de ácido sulfúrico (fase móvil) fueron de 85 ◦C, 0,5 mL/min y 0,01 % v/v de ácido sulfúrico, respectivamente. La cuantificación se realizó utilizando curvas de calibración de soluciones mixtas de los monosacáridos ensayados en concentraciones de 500 a 5 000 mg/L. La operación del instrumento y el procesamiento de datos se llevaron a cabo con ChromNAV Ver. 2.1.0 (Jasco Corporation, Tokio, Japón).
2.6 Análisis estadístico
Para determinar los efectos y las interacciones significativas se utilizó el gráfico de efectos normales, considerando significativos aquellos efectos situados fuera de la línea. Los efectos individuales y de interacción se determinaron gráficamente. Para obtener los modelos lineales de cada biomasa, se verificaron los supuestos de homocedasticidad y normalidad mediante gráficos cuantil-cuantil normales, boxplots y las pruebas de Shapiro-Wilk y Levene (resultados no mostrados); en todos los casos los supuestos se cumplieron. Para determinar la diferencia de medias entre biomasas se aplicó un ANOVA de una vía. Cuando se obtuvieron diferencias significativas con un nivel de significancia de 0,05, se aplicó una prueba post hoc de diferencia de medias con la corrección de Bonferroni. El error se calculó a partir de las réplicas en el punto central. Para todos los análisis se empleó el programa R versión
4.0.4 con la interfaz RStudio.
3 Resultados y Discusión3.1 Caracterización estructural de la biomasa
El material lignocelulósico está compuesto principalmente por celulosa, hemicelulosa, lignina, cenizas y compuestos extractivos solubles en diferentes disolventes, además de impurezas. Para este estudio, se determinaron los componentes más relevantes en la obtención de monosacáridos. La Tabla 3 presenta los resultados obtenidos para α-celulosa, hemicelulosa, lignina insoluble y extractivos etanoltolueno de cada tipo de biomasa. Todos los análisis se realizaron por triplicado.
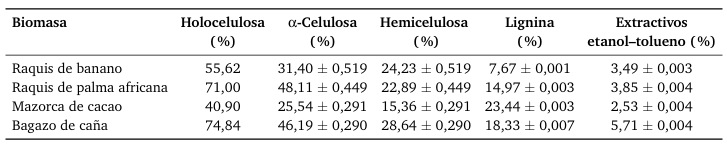
Tabla 3.
Caracterización estructural del raquis de banano, raquis de palma africana, mazorca de cacao y bagazo de caña de azúcar.
Como se observa en la Tabla 3, al caracterizar estructuralmente la biomasa se obtuvo un mayor contenido de α-celulosa en la palma africana con 48,11 %, seguida del bagazo de caña con 46,19 % y el raquis de banano con 31,40 %. Estos resultados son similares a los obtenidos por Kumneadklang ycols. (2019) quienes reportaron 42,67 % para la palma africana, mientras que en los estudios presentados por Oliveira para el raquis de banano se alcanzó un 28,4 % (Oliveira y cols., 2007). En cuanto a la hemicelulosa, el bagazo predomina con 28,64 %, valor semejante al reportado en las investigaciones de Moraes Rocha con 27,6 % (Dussan y cols., 2014). El mayor contenido de lignina se presenta en la mazorca de cacao, con 23,44 %, valor que se encuentra dentro del rango de 14–28 % establecido en los estudios de Lu y cols. (2018). El raquis de banano, en cambio, presentó el valor mínimo de 7,67 %, frente al 9,6 % reportado en los estudios de Oliveira. Estos porcentajes reflejan que cada biomasa presenta un predominio en distintos componentes, lo cual influirá en el proceso de conversión hacia glucosa. Aquellas biomasas con altos contenidos de celulosa y hemicelulosa tendrán un mejor rendimiento en la conversión a monosacáridos.
3.2 Hidrólisis ácida
En los resultados presentados en la Tabla 4, la mayor cantidad de glucosa se obtuvo con el bagazo de caña de azúcar y la menor con el raquis de banano. Roslan et al. (2006) utilizaron biomasa de bagazo de caña con una concentración de 1 % de ácido sulfúrico, a una temperatura de 122 ◦C durante 24 minutos de reacción, obteniendo un rendimiento de 3 g de glucosa/L (Roslan y Salimi, 2020).
Dussan et al. (2014) también experimentaron con bagazo de caña, bajo condiciones de reacción de 90 ◦C, 60 minutos y una concentración de ácido sulfúrico de 0,5 %, obteniendo un rendimiento máximo de azúcares totales de 0,65 g/L (Dussany cols., 2014). Las condiciones de reacción de esas investigaciones son similares a las del presente estudio en cuanto a temperatura y concentración; sin embargo, la variable de tiempo es mayor, alcanzando 150 minutos, lo cual podría influir en el incremento del rendimiento obtenido en este trabajo.
Esta cantidad de glucosa puede ser utilizada para la obtención de diversos compuestos químicos de valor agregado y biocombustibles, tales como alcoholes, ácido glucónico, 5-hidroximetilfurfural (HMF), ácido láctico, ésteres de ácido pentanoico y 2,5-dimetilfurano (2,5-DMF). El HMF puede transformarse en productos químicos de interés industrial como furano y sus derivados, ácido levulínico y ácido fórmico, los cuales actualmente se producen a partir de recursos derivados del petróleo (Liuy cols., 2015; Bali y cols., 2012).
El análisis de la interacción de las variables se describe en la sección 3.3.
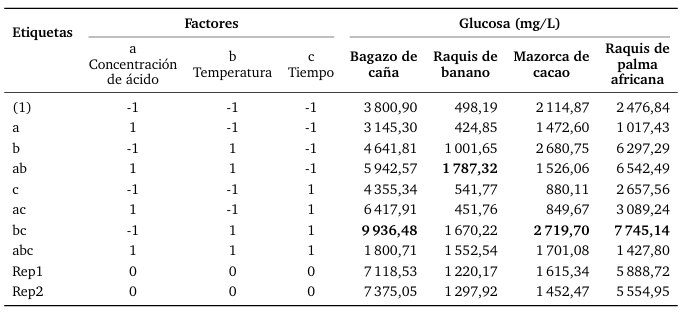
Tabla 4.
Diseño factorial 23 con dos réplicas en el punto central.
Al comparar los resultados de glucosa obtenidos con la caracterización estructural de cada biomasa, tanto el bagazo de caña de azúcar como el raquis de palma africana presentan el mayor contenido de holocelulosa, lo cual se refleja en una mayor conversión a glucosa. Sin embargo, esto no se replica en el caso del raquis de banano y la mazorca de cacao, ya que, aunque la mazorca de cacao presenta un mayor contenido de holocelulosa, su conversión a glucosa es menor. Esto podría deberse a diferentes factores en la composición de estas biomasas, por lo que deben realizarse estudios adicionales para identificarlos. En la actualidad, se investigan diferentes procesos de pretratamiento para mejorar el rendimiento en la hidrólisis ácida, entre los cuales el uso de líquidos iónicos se encuentra entre los más prometedores. Esta técnica ha demostrado facilitar la descomposición de los biopolímeros al eliminar la protección estructural de los centros de hidrólisis. La segunda parte de esta investigación considerará el uso de dichos líquidos con el fin de mejorar los rendimientos y reducir los requerimientos energéticos.
3.3 Análisis estadístico
En los resultados presentados en la Tabla 5, la mayor cantidad de glucosa se obtuvo con el bagazo de caña de azúcar y la menor con el raquis de banano. Existen diferencias estadísticamente significativas entre la cantidad de glucosa obtenida por cada biomasa, p(2,47e-06) < 0, 001. Las diferencias se encuentran entre el valor de glucosa obtenido en el bagazo de caña y el raquis de banano, así como entre la mazorca de cacao y el bagazo de caña, con p(0, 000) < 0, 001 en ambos casos. Asimismo, se encontraron diferencias significativas entre el raquis de palma africana y el raquis de banano, y entre el raquis de palma africana y la mazorca de cacao, con p(0, 001) < 0, 01 y p(0, 013) < 0, 05, respectivamente.
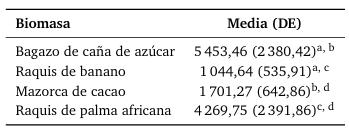
Tabla 5.
ANOVA de una vía y prueba post hoc.
Para el bagazo de caña de azúcar (Figura 1a), únicamente el factor tiempo resultó estadísticamente significativo, y ninguna interacción fue significativa. Al analizar los efectos, la obtención de glucosa se ve favorecida con los niveles altos de temperatura y tiempo, y con el nivel más bajo de concentración de ácido (véase Apéndice S1).
En cuanto a las interacciones dobles, estas se observaron entre concentración y temperatura, donde la mayor cantidad de glucosa obtenida se presentó a baja concentración de ácido y alta temperatura. También se encontró interacción entre tiempo y concentración, donde se repitió el mismo caso anterior; los gráficos de interacción doble se muestran en S2. La concentración de ácido y la interacción triple presentan coeficientes negativos (véase Tabla 6). Como puede observarse, la concentración en un nivel alto de ácido reduce el rendimiento, el cual aumenta con mayor temperatura y/o tiempo de reacción.
Para el raquis de banano (Figura 1b), únicamente el factor temperatura fue significativo. Al analizar los efectos, la obtención de glucosa se ve favorecida con los niveles altos de los tres factores, principalmente con el factor temperatura, ya que los otros dos no muestran gran variación en su respuesta entre niveles (véase Apéndice S1). Se encontraron interacciones débiles entre concentración-tiempo y entre temperatura-tiempo; en ambos casos, los mejores resultados se obtuvieron con alta temperatura, mientras que los niveles de los otros factores no tuvieron influencia significativa. La concentración de ácido, la interacción concentración-tiempo y la interacción triple presentaron coeficientes negativos (véase Tabla 6).
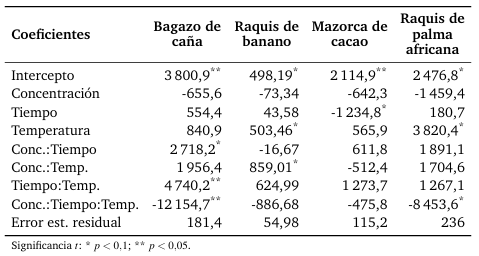
Tabla6.
Coeficientes del modelo.
Para la mazorca de cacao (Figura 1c), ni los factores ni las interacciones fueron significativos. Los efectos simples muestran que la obtención de glucosa se favorece con el nivel alto del factor temperatura y con los niveles bajos de los factores concentración de ácido y tiempo (véase Apéndice S1). Se observaron interacciones dobles entre tiempo y temperatura, donde la mayor glucosa obtenida se presentó al nivel alto de temperatura, sin diferencias en el factor tiempo (véase Apéndice S2). Finalmente, la concentración de ácido, la temperatura, la interacción concentración-temperatura y la interacción triple presentaron coeficientes negativos (véase Tabla 6).
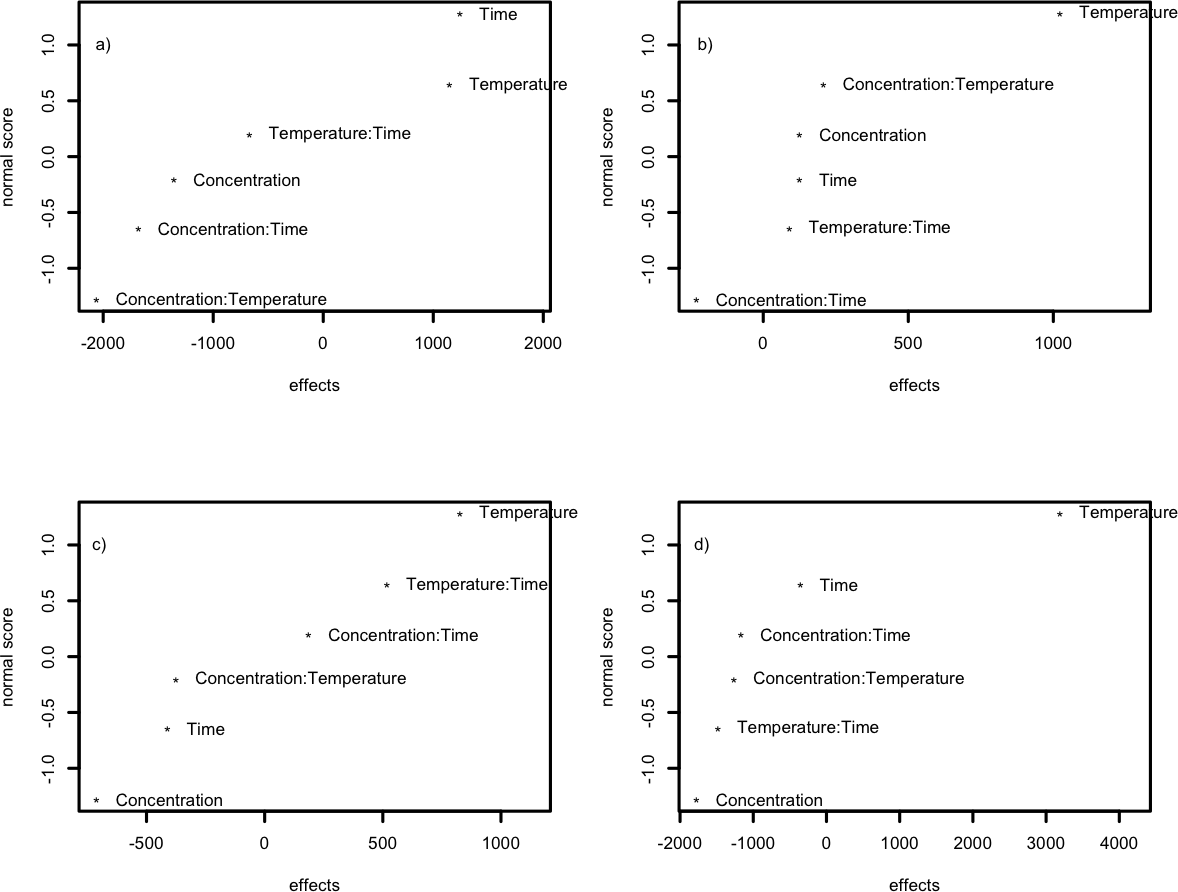
Figura 1.
Gráfico de probabilidad normal de efectos estandarizados (a, b, c, d).
A partir de los resultados obtenidos, se puede concluir que, en el caso de la mazorca de cacao, el raquis de palma africana y el bagazo de caña de azúcar, una temperatura de 120 °C, un tiempo de reacción de 150 min y una concentración de 1 % de ácido sulfúrico fueron las condiciones que presentaron los mejores rendimientos de reacción. En estas condiciones, para el raquis de banano se obtuvo un valor de 1 670,22 mg/L de glucosa, mientras que el mejor rendimiento se alcanzó a una temperatura de 120 °C, un tiempo de reacción de 20 minutos y una concentración de ácido del 5 %, obteniéndose un valor de 1 787,32 mg/L, con una diferencia de 117,1 mg/L.
Además, se evidencia que la composición estructural de cada tipo de biomasa influye en la obtención de glucosa; en este caso, el bagazo de caña de azúcar y el raquis de palma africana fueron los que presentaron mayor contenido de celulosa y hemicelulosa. En el análisis estadístico, para el bagazo de caña de azúcar únicamente el factor tiempo resultó significativo, mientras que la concentración de ácido en niveles altos redujo el rendimiento. En el caso del raquis de banano y del raquis de palma africana, el factor temperatura fue significativo. Para la mazorca de cacao, ni los factores ni las interacciones fueron significativos.
Finalmente, se alcanzó el objetivo de esta investigación, obteniéndose altos rendimientos de conversión a glucosa que permiten mejorar los procesos posteriores de fabricación de biocombustibles. Se recomienda realizar un estudio de factibilidad técnica y económica que permita lograr un equilibrio entre la cantidad de glucosa obtenida y los costos de producción, de manera que el proceso resulte rentable y pueda aplicarse a gran escala.
Financiamiento
Esta investigación fue financiada por la DIUC – Universidad de Cuenca en el proyecto “Optimización de la reacción de hidrólisis ácida con líquidos iónicos para la obtención de monosacáridos de la biomasa generada por los principales cultivos del Ecuador”.
Contribución de los autores
M.A.G.: Conceptualización, análisis formal, investigación, metodología, visualización, escritura – borrador original, escritura – revisión y edición. A.V.S.: Conceptualización, análisis formal, investigación, metodología, visualización, escritura – borrador original, escritura – revisión y edición. V.P.V.: Conceptualización, análisis formal, metodología, visualización, escritura – borrador original, escritura – revisión y edición.
redalyc-journal-id: 4760
https://revistas.ups.edu.ec/index.php/granja/article/view/5647 (html)

Tabla 1.
Residuos generados por cultivos permanentes en el Ecuador.

Tabla 2.
Resultados obtenidos de procesos de hidrólisis de biomasa.

Tabla 3.
Caracterización estructural del raquis de banano, raquis de palma africana, mazorca de cacao y bagazo de caña de azúcar.

Tabla 4.
Diseño factorial 23 con dos réplicas en el punto central.

Tabla 5.
ANOVA de una vía y prueba post hoc.

Tabla6.
Coeficientes del modelo.

Figura 1.
Gráfico de probabilidad normal de efectos estandarizados (a, b, c, d).
