El año 2015 en cardiología: arritmias y tratamiento con dispositivos
El año 2015 en cardiología: arritmias y tratamiento con dispositivos
Revista Uruguaya de Cardiología, vol. 31, núm. 3, pp. 452-460, 2016
Sociedad Uruguaya de Cardiología
Recepción: 26 Octubre 2015
Aprobación: 18 Noviembre 2015
Preámbulo
Nuevamente el año 2015 estuvo cargado de novedades interesantes y de gran importancia en el campo de la electrofisiología intervencionista y los dispositivos cardíacos implantables. Los avances incluyen innovaciones técnicas, novedosas perspectivas moleculares y celulares, y la presentación de grandes ensayos clínicos aleatorizados, así como la publicación de importantes registros del “mundo real”. Además, en 2015 aparecieron una serie de guías, por ejemplo aquellas destinadas al tratamiento de las arritmias ventriculares y la prevención de la muerte súbita cardíaca. Es virtualmente imposible cubrir todas las novedades que ameritarían análisis en este tipo de reseña general, por lo que los autores tuvieron que hacer una selección, concentrándose en varios avances importantes que tienen implicancias directas en la práctica clínica diaria.
Arritmias cardíacas y ablación por catéter Fibrilación auricular
La ablación por catéter de la fibrilación auricular (FA) sigue siendo motivo de estudios clínicos y ensayos en gran escala. El uso de tecnologías de ablación con catéteres con sensores de contacto parece mejorar la creación de lesiones auriculares duraderas; un metaanálisis fundamentalmente compuesto de ensayos no aleatorizados(1) demostró una reducción significativa de la aparición de FA luego de la ablación por catéter. En el futuro, esta tecnología será la norma para la ablación con catéter de la FA. Hay que advertir que va surgiendo cada vez mayor evidencia que muestra que la ampliación de la ablación a nivel auricular de por sí no mejora la evolución del ritmo luego de la ablación. El ensayo Minimax comparó dos estrategias de ablación para el aislamiento de las venas pulmonares (AVP) en 234 pacientes sometidos a ablación con catéter de FA paroxística: AVP antral circunferencial sola (mínima) vs AVP con ablación endovenosa del reborde para lograr una AVP individual (máxima). Luego de una media de seguimiento de 17 ± 8 meses, la ausencia de FA tras una ablación limitada mínima no resultó peor que la ablación más amplia máxima (70 vs 62%; p = 0,25)(2). Información que surge de estudios anteriores indica que la detección con adenosina de una reconducción quiescente de la vena pulmonar y el ulterior reaislamiento de las venas mejoran el resultado de la ablación de la FA con catéter(3). Sin embargo, un ensayo aleatorizado mucho mayor publicado en el European Heart Journal ahora cuestiona la utilidad de las pruebas con adenosina: en el ensayo japonés UNDER de estimulación antitaquicardia (ATP, por su sigla en inglés) se distribuyeron aleatoriamente 2.113 pacientes a un brazo con provocación con adenosina o un brazo control, y no se mostró ninguna diferencia en cuanto a la tasa de recidivas de la FA al cabo del primer año(4). A la fecha no hay explicación para los resultados contradictorios de estos dos ensayos multicéntricos aleatorizados, y el tema amerita una mayor investigación. En el ensayo EAST AF se demostró que el tratamiento con fármacos antiarrítmicos después de la ablación por catéter reducía la recidiva de la FA 90 días después de la ablación por catéter; sin embargo, un año después no hubo diferencia en la recurrencia de las arritmias entre el grupo control y el grupo con tratamiento(5). Estos resultados concuerdan en gran medida con los datos del ensayo AmioCat(6). En AmioCat los pacientes fueron aleatorizados a amiodarona o placebo durante ocho semanas después de la ablación de la FA con catéter. Si bien la amiodarona redujo las internaciones y las cardioversiones en el período de blanqueo de tres meses luego de la ablación, en el seguimiento a los seis meses no hubo diferencia en la tasa de recidivas de la FA (39 vs 48%; p = 0,18). Por lo tanto, los fármacos antiarrítmicos pueden evitar las recidivas tempranas de la FA luego de una ablación, pero tal vez no promuevan una mejor remodelación auricular que determine una mayor frecuencia de ritmo sinusal durante el seguimiento. Durante el congreso ESC en Londres se comunicaron los datos del seguimiento a cinco años del ensayo MANTRA-PAF; este comparó los efectos de la ablación de FA como primera opción terapéutica versus tratamiento antiarrítmico farmacológico. A los dos años de seguimiento no hubo diferencia en la carga acumulada de FA entre el grupo sometido a ablación y el grupo con antiarrítmicos, mientras que la carga de FA fue significativamente más baja en el grupo sometido a ablación (percentil 90,9 vs 18%; p = 0,007)(7). Sin embargo, en el seguimiento a los cinco años hubo una tasa significativa- mente superior de pacientes sin FA en el grupo sometido a ablación comparado con el que recibió terapia medicamentosa antiarrítmica (86 vs 71%; p = 0,001). Además, la carga de FA fue menor en el grupo sometido a ablación comparado con el grupo que recibió fármacos (p = 0,003). Es interesante destacar que los efectos sobre la calidad de vida fueron similares en ambos grupos. Estos datos indican que el beneficio sobre el ritmo que otorga la ablación por catéter puede aumentar con el tiempo; sin embargo, es importante comprender que el ensayo MANTRA-PAF fue demasiado pequeño como para evaluar el efecto de la ablación o de los fármacos antiarrítmicos sobre los parámetros de resultados duros tales como el accidente cerebrovascular o la mortalidad. Estas interrogantes permanecerán sin respuesta hasta que se publiquen los datos del ensayo EAST (punto final compuesto de muerte, accidente cerebrovascular e insuficiencia cardíaca) y el ensayo CABANA (punto final compuesto de muerte, sangrado grave, accidente cerebrovascular invalidante y paro cardíaco)(8,9). La estrategia de ablación de la FA persistente nunca ha tenido la madurez suficiente como para que surgiera un consenso, ni en el pasado ni en el año 2015. La ablación de los rotores por mapeos de fase de contacto ha sido cuestionada(10), y la ablación los CAFE (complex atrial fractionated electro- grams) no es suficientemente específica como para resultar convincente, tal como surge de un gran metaanálisis(11). En contraste, la modificación del estilo de vida, como el adelgazamiento, es claramente muy eficaz en reducir la carga de la FA (un adelgazamiento del 10% se traduce en una reducción de seis veces la carga de la FA) y en reducir la remodelación inversa del tamaño de la aurícula izquierda y el grosor del tabique del ventrículo izquierdo(12).
Prevención de los accidentes cerebrovasculares
Debido a los resultados de los ensayos clínicos a gran escala, los anticoagulantes orales no antagonistas de la vitamina K (NOAC, por su sigla en inglés) son el tratamiento de elección para la prevención de los accidentes cerebrovasculares en la FA no valvular, tal como reflejan las actuales guías de ESC(13). El cuarto NOAC –edoxabán– fue aprobado en 2015 en muchos países europeos, Estados Unidos y Suiza, sobre la base de los resultados del ensayo ENGAGE AF-TIMI 48(14). En el curso de 2015 surgieron varios análisis de subgrupos de los grandes ensayos con NOAC, como el manejo de los sangrados y los resultados con apixabán(15), el manejo de rivaroxabán en torno a la ablación por catéter para FA (VENTURE-AF)(16), y el resultado de la medicación conjunta con amiodarona en pacientes que recibían edoxabán, por mencionar algunos(17). Prácticamente todos los subgrupos de los grandes ensayos con NOAC arrojan un firme beneficio y muestran que estos fármacos son más seguros que la warfarina, subrayando además su superioridad general. Esto queda avalado por importantes datos del mundo real (incluyendo aquellos de un registro prospectivo con rivaroxabán, XANTUS)(18), lo que indica eficacia y seguridad, y concuerda con lo observado en los ensayos clínicos aleatorizados.
Tal vez la novedad más interesante con respecto a los NOAC proviene del desarrollo de agentes que revierten su acción específicamente (antídotos). En un estudio fase 1 en hombres sanos, el anticuerpo monoclonal idarucizumab (específico para dabigatrán) fue bien tolerado y no aparecieron problemas inesperados o de seguridad clínicamente relevantes, y se asoció con la reversión inmediata completa y sostenida de la anticoagulación inducida por dabigatrán(19). Además, en un estudio fase 3 se demostró que idarucizumab era efectivo y que provocaba la reversión inmediata del efecto anticoagulante del dabigatrán en pacientes que se presentaban con sangrado grave o que requerían un procedimiento urgente(20). Como resultado, la Administración de Alimentos y Medicamentos de Estados Unidos aprobó el fármaco en octubre del 2015; asimismo, el Comité para Productos Medicinales para uso Humano de la Agencia Europea del Medicamento también recientemente emitió un dictamen positivo, y se espera que lo apruebe antes de fin de año o a principios del 2016. Es importante destacar que idarucizumab no es efectivo contra los inhibidores del factor Xa. Se están desarrollando diferentes antídotos que actúan directamente, incluyendo andexanet alfa y PER977. Los primeros resultados también son positivos con estos agentes y se prevé realizar ensayos clínicos a mayor escala en el correr del año 2016. Mientras que estas drogas claramente representan un agregado importante a nuestra cartera de productos, todavía quedan muchos aspectos por determinarse en el uso práctico, como el tipo de pacientes, las condiciones a revertir y el momento de reinstitución de la anticoagulación. Estos y otros te- mas están elegantemente descritos en la versión actualizada del 2015 de la guía práctica de la Asociación Europea del Ritmo Cardíaco(21), luego del gran éxito de la primera versión publicada en 2013(22).
¿La ablación de la FA con catéter incidirá sobre el riesgo de accidente cerebrovascular? Nuevos datos de un gran registro danés sugieren un muy bajo riesgo de accidente cerebrovascular en los pacientes que han sido sometidos a una ablación por catéter(23). Sin embargo, antes de poder cambiar la práctica clínica para la anticoagulación oral de los pa- cientes sometidos a ablación por catéter, estos datos deben validarse en un ensayo aleatorizado prospectivo(24).
Arritmias ventriculares y muerte súbita cardíaca
La ablación por catéter de la taquicardia ventricular (TV) es uno de los campos de más rápido crecimiento en la electrofisiología intervencionista(25); la importancia de diagnosticar y clasificar correctamente la severidad de las TV, particularmente aquellas fácilmente pasibles de ablación por catéter (figura 1), es un desafío habitual que enfrentan los cardiólogos. En los últimos 12 meses se han comunicado varios estudios importantes que reflejan la importancia y la creciente utilización de la ablación de las TV. Pese a varias mejoras e innovaciones técnicas y tecnológicas notorias tales como el uso de la integración de imágenes(26), nuevos electrodos de ablación(27,28), tecnologías de sensores de contacto(29), o mapeo de ultraalta densidad(30), la tasa de recidivas de cualquiera de las TV luego de la ablación por catéter en pacientes con TV y cardiopatía estructural sigue siendo relativamente alta y constituye un importante desafío. Tal como surge de datos multicéntricos recientes, la imposibilidad de inducir una TV al terminar la ablación es probablemente el mejor punto final del procedimiento y esa debería ser la meta(31). Además, cuando se logra eliminar los potenciales anómalos, la imposibilidad de inducir una TV también podría reflejarse en la supervivencia (32,33). Lo más fascinante es el informe de la “ablación” exitosa del síndrome de Brugada. En un informe reciente de Brugada y colaboradores(34) los autores analizan en mayor detalle la idea de tratar a los pacientes con Brugada en riesgo de muerte súbita cardíaca con un procedimiento intervencionista de ablación. En su serie sometieron a 13 pacientes a mapeo epicárdico y en todos ellos identificaron electrogramas anómalos en el ventrículo derecho. La ablación por catéter de estos potenciales logró normalizar el electrocardiograma (ECG) y abolir los cambios electrocardiográficos típicos preexistentes inducidos por la flecainida. Sin embargo, pese al entusiasmo por esos resultados, no queda claro si los efectos de la ablación inciden o no en la TV espontánea, la fibrilación ventricular (FV) o el riesgo de muerte súbita cardíaca. En el congreso ESC en Londres se presentaron las nuevas guías de ESC para el tratamiento de las arritmias ventriculares y la prevención de la muerte súbita cardíaca(35). Estas guías ofrecen un resumen actualizado de lo más nuevo del conocimiento y de las mejores prácticas en este campo.
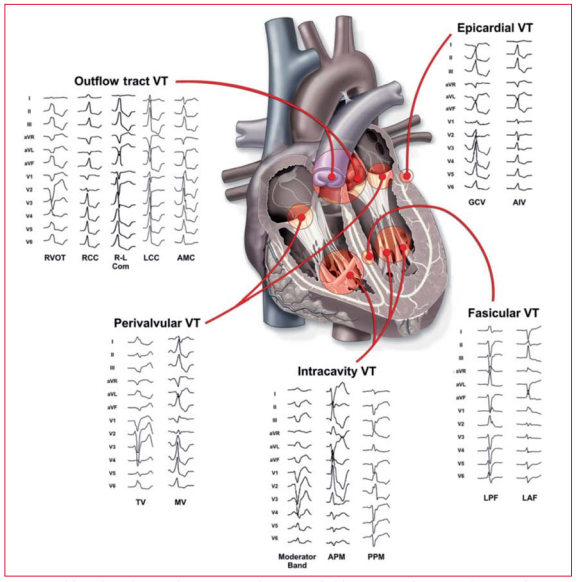
Figura 1
Morfología de un electrocardiograma con 12 derivaciones de diferentes sitios de origen en la taquicardia ventricular idiopática. RVOT, tracto de salida del ventrículo derecho; RCC, cúspide de la coronaria derecha; R–L COM comisura de la cúspide de la coronaria derecha-izquierda; CC, cúspide de la coronaria izquierda; AMC, continuidad aortomitral; TV, anillo tricuspídeo; MV, anillo mitral; APM, PAP anterior; PPM, PAP posterior; LPF, fascículo posterior izquierdo; LAF, fascículo anterior izquierdo; GCV, vena cardíaca magna; AIV, vena interventricular anterior. Reproducido de Tanawuttiwat y colaboradores, reimpreso gracias a la generosidad de Tanawuttiwat y colaboradores(25)
Dispositivos electrónicos cardíacos Marcapasos sin cables
Una de las principales tendencias en dispositivos cardíacos en el año 2015 fue el gradual abandono de los cables endovasculares. Luego de una tórpida introducción, los marcapasos monocamerales sin cables finalmente han llegado a la práctica clínica diaria. Los primeros resultados de los 140 pacientes a los que se les colocó el sistema de marcapasos sin cables MICRA de Medtronic demostraron un perfil de eficacia y seguridad favorables(36). Durante una media de seguimiento de 1,9 ± 1,8 meses (que cubría fundamentalmente el período perioperatorio y el posoperatorio temprano), no se observaron eventos adversos graves no previstos; no hubo desplaza- mientos del dispositivo y solo se informó un derrame pericárdico pero sin taponamiento (este caso dio lugar a una hospitalización prolongada). Es de destacar que este último episodio tuvo lugar en un paciente que requirió varios reposicionamientos del dispositivo (18×). Sin embargo, en la mayoría de los pacientes (81%) el dispositivo se colocó correctamente sin que hubiera que reposicionarlo nunca o requiriendo solo un reposicionamiento. Durante el seguimiento los parámetros eléctricos (umbrales de estimulación, impedancia y sensores) se mantuvieron estables y favorables, gracias a lo cual se estimó que las baterías puedan durar 12,6 años (rango 8,6-14,4)(36). Como resultado de estos hallazgos se le adjudicó a MICRA la marca CE en el verano del 2015, y se introdujo cuidadosamente el sistema en ciertos centros y con operadores seleccionados tras una amplia capacitación in vivo y ex vivo. Luego de estos primeros resultados positivos se logró replicar los resultados en un grupo de mayor tamaño (725 pacientes), 719 (99,2%) de los cuales recibieron implantes con éxito(37). Los valores eléctricos (umbral, sensores e impedancia) fueron favorables en 292 de 297 pacientes con datos apareados para seis meses. Hubo 28 complicaciones mayores en 25 de los 725 pacientes (4,0%, incluyendo 11 [1,9%] perforacio- nes cardíacas traumáticas o derrames pericárdicos y una muerte [0,1%]). Estas cifras se compararon favorablemente con controles históricos de pacientes sometidos a implantes de marcapasos por vía venosa. Es importante destacar que ningún dispositivo migró de su lugar(37). Este año también se presentaron y publicaron los resultados del segundo sistema de estimulación monocameral transcatéter, el Nanostim (St Jude Medical)(38). De los primeros 526 pacientes, la implantación del sistema fue exitosa en 504 (95,8%). De los 300 pacientes controlados durante seis meses se alcanzó el resultado primario de eficacia (valores eléctricos aceptables) en 90%. De la cohorte total de 526 pacientes, aparecieron eventos adversos graves vinculados al dispositivo en 6,5% de los pacientes, incluyendo taponamiento cardíaco en cinco (1,0%), desplazamiento del dispositivo en seis (1,5%), y migración del dispositivo durante el implante debido a fijación inadecuada en dos pacientes (0,4%). Se necesita más experiencia para comparar ambos sistemas de estimulación sin cables en poblaciones aún más grandes y en la práctica clínica diaria.
Los pacientes con indicación de marcapasos monocamerales típicos representan actualmente la po- blación con indicación primaria para marcapasos sin cable; por ejemplo, FA permanente con bradicardia sintomática o bloqueo auriculoventricular. .studios futuros y la experiencia de la vida real permitirán ver el comportamiento de estos dispositivos a largo plazo (incluyendo el novedoso sistema de sensor adaptado a la frecuencia), pero las primeras experiencias personales son alentadoras. Se están desarrollando sistemas más avanzados, como mar- capasos bicamerales, terapia de resincronización cardíaca y comunicación con el desfibrilador cardio- versor implantable subcutáneo (ICD, por su sigla en inglés).
Desfibriladores cardioversores implantables y teleseguimiento basado en el implante
Ya no se necesitan tests para probar el desfibrila- dor cardioversor implantable en los implantes de rutina y no complicados de ICD: en el ensayo Nordic ICD se asignaron 1.077 pacientes aleatoriamente para colocación de ICD por primera vez con (n = 540) o sin (n = 537) tests para detección del umbral de desfibrilación(39). La eficacia de la desfi- brilación no difirió entre ambos grupos durante el seguimiento. De similar manera, en el ensayo SIMPLE, en el que se estudiaron 2.500 pacientes, las pruebas de desfibrilación de rutina no redujeron las muertes por arritmia durante un segui- miento medio de 3,1 años(40).
Casi todos los marcapasos y desfibriladores disponibles actualmente ofrecen la opción técnica de monitoreo a distancia(41). Los primeros resultados de los ensayos clínicos aleatorizados y el análisis de los conjuntos de grandes bases de datos indican que–bien aplicada– esta tecnología puede tener efectos beneficiosos(42). Sin embargo, en el Congreso de ESC en Londres se mostraron resultados decepcionantes del ensayo Optilink HF: en el ensayo se dis- tribuyó aleatoriamente a 1.002 pacientes con insu- ficiencia cardíaca e indicación de implante de ICD, a algunos se les mantuvo la alerta a distancia de congestión pulmonar automatizada encendida –‘on’– (n = 505) y al resto apagada –‘off’– (n = 497). Luego de 18 meses de seguimiento no hubo diferencias sig- nificativas entre los grupos en el punto final primario, que fue una combinación de muerte por todas las causas y de internación por motivos cardiovasculares. El informe de seguimiento del ensayo CHAMPION, que valoró la eficacia de la medición automáticade la presión pulmonar en pacientes con insuficiencia cardíaca para guiar y optimizar el tratamiento de la insuficiencia cardíaca, mostró resultados más promisorios(43). La superioridad del grupo de tratamiento con respecto al grupo control se mantuvo 13 meses más hasta el final del período de acceso aleatorizado, con una reducción significativa (33%) de las internaciones relacionadas con la insuficiencia cardíaca y una disminución del 16% de las internaciones por todas las causas. En segundo lugar, los buenos resultados del grupo de tratamiento se mantuvieron durante un período de acceso abierto de 12 meses más, durante los cuales no se observó aumento de las hospitalizaciones. Lo más importante es que las hospitalizaciones por insuficiencia cardíaca y las hospitalizaciones por todas las causas en el que había sido el grupo control se redujeron significativamente (48% y 21%, respectivamente) al disponerse de la información de la presión de la arteria pulmonar para guiar el tratamiento durante el período de acceso abierto. Por ende, el telemonitoreo del dispositivo a distancia parece ser sumamente promisorio para apoyar el tratamiento de la insuficiencia cardíaca, y será solo cuestión de tiempo para que se combinen los sensores hemodinámicos con los marcapasos, los desfibriladores y los dispositivos de resincronización.
Desfibriladores cardioversores implantables subcutáneos
Desde su aprobación en 2009, la atención y la atracción por el sistema de ICD subcutáneo (S-ICD) han ido aumentando. Ciertamente, al no colocarse electrodos por vía intravascular podría lograrse una importante reducción de la morbilidad (y mortalidad) que responden a complicaciones de los electrodos utilizados con los sistemas actuales de ICD transvenosos clásicos. En 2015 se aprobó la nueva generación del sistema EMBLEMS-ICD, cuya principal característica es que son 20% más delgados y tienen una expectativa de vida 40% mayor que el sistema S-ICD anterior. Paralelamente, se están desarrollando nuevos algoritmos para resolver el problema de descargas eléctricas inadecuadas(44,45). Según surge de registros publicados recientemente, al ir aumentando la experiencia y el volumen se disminuiría el riesgo de complicaciones, de programación subóptima, y (en menor grado) de descargas indebidas(46). Además, los mismos registros demostraron una alta eficacia para la terminación de la TV y FV; 90,1% de los eventos (100/111) terminaron con una descarga y 98,5% (109/111) fueron interrumpidos con los cinco choques disponibles(47) . Como resulta- do de estos datos favorables, por primera vez se ha incorporado el uso de S-ICD en las guías para la pre- vención de la muerte súbita cardíaca como una indicación IIa (nivel de evidencia [NE] C) como alternativa al ICD estándar en pacientes que no tienen indicación para estimulación por bradicardia, resin- cronización cardíaca o ATP(35). Además, se puede considerar el S-ICD (IIb, NE C) en pacientes con difícil acceso venoso, luego de remoción de ICD transvenosos debido a infecciones o en pacientes jóvenes con indicación prolongada de terapia ICD(35). Ciertamente la falta de una posibilidad de administrar ATP o estimulación por bradicardia sigue siendo la principal desventaja de los dispositivos S-ICD actuales. La combinación de S-ICD con marcapasos sin cables sería claramente una de las soluciones más obvias para este problema. Sin embargo, si se aplica programación basada en la evidencia (zonas en que se detecta alta frecuencia o larga duración), es posible que la cantidad de ATP disminuya como resultado tanto de la terminación espontánea de la TV como de las TV que se dan por debajo del límite de detección. Se encuentra en curso un ensayo prospectivo, aleatorizado (PRAETORIAN) que compara los ICD transvenosos y subcutáneos (sin posibilidad de ATP) disponibles actualmente.
Desfibrilador cardioversor portátil (Wearable Cardioverter Defibrillator)
Además, por primera vez las nuevas guías de 2015 para la prevención de la muerte súbita cardíaca recomiendan el uso de los desfibriladores cardioversores portátiles (WCD, por su sigla en inglés; figura 2). Con una recomendación clase IIa (NE C), se consideraría el WCD durante un período de tiempo limitado para pacientes con reducción de la fracción de eyección del ventrículo izquierdo (FEVI) que están en riesgo de muerte súbita cardíaca, pero que actualmente no pueden recibir un ICD, incluyendo pacientes a los que se les ha retirado el sistema por infección, pacientes con miocarditis activa, y pacientes con arritmias en la fase temprana posinfarto de miocardio(35). Al no haber ensayos clínicos aleatorizados, esta recomendación se basó fundamentalmente en grandes registros, tales como uno prospectivo publicado recientemente de pacientes que usaban un desfibrilador portátil (WEARIT-II). En este estudio se siguió a 2.000 pacientes con WCD cuya mediana de uso fue 90 días(48). En este registro se observaron en total 120 taquiarritmias ventriculares sostenidas (TV/FV) en 41 pacientes. De estos pacientes, en 54% las descargas del WCD fueron apropiadas, mientras que solo en 10 pacientes (0,5%) fueron inapropiadas.
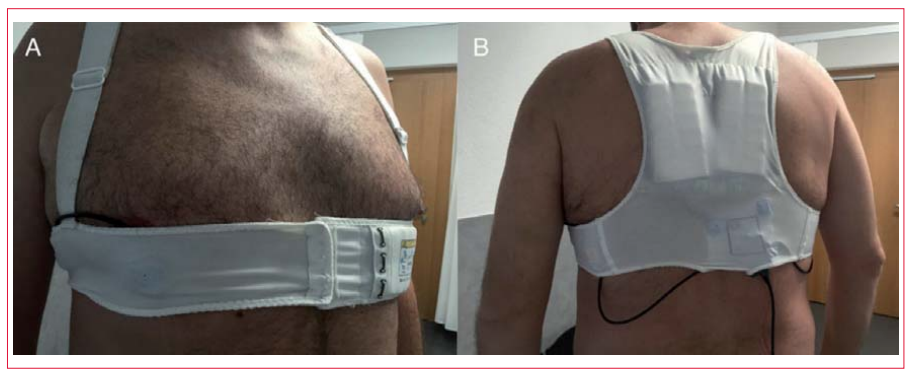
Figura 2
Desfibrilador cardioversor portátil. Modelo de desfibrilador cardioversor portátil. Imágenes cortesía de IS, reimpreso con el generoso permiso y consentimiento del paciente.
Es importante destacar que al final del período de tiempo en que cada individuo llevó puesto elWCD, se implantó solo un ICD en 840 pacientes (42%), siendo la mejora de la FEVI la causa más frecuente, por lo que se decidió no implantar el ICD. Dado el posible ahorro de costos de implantación de un ICD de novo, así como los (posibles) costos de seguimiento asociados y los costos de las complicaciones, esta estrategia puede también resultar conveniente desde el punto de vista de los costos, aunque aún faltan análisis completos en ese sentido.
Reflexiones finales
En el año 2015 aparecieron muchos estudios interesantes en el campo de la electrofisiología invasiva y los dispositivos cardíacos, la mayoría de los cuales pueden tener (o ya tienen) importantes implicancias para la práctica clínica diaria. Será crucial disponer de una confirmación y ampliación de estos datos con experiencias del mundo real para sustanciar su eficacia y seguridad en ese “mundo real”. Es imposible cubrir todas las novedades importantes en una revisión muy concisa, por lo que hubo que omitir varios métodos y tecnologías, como los resultados primarios sobre el uso de la estimulación en múltiples sitios y la comparación entre la ablación punto por punto y la ablación en un único punto. Si se mantienen el ritmo y la calidad de las innovaciones, no hay duda que el año 2016 será igualmente exitoso en el campo de las arritmias.
Bibliografía
1. Shurrab M, Di Biase L, Briceno DF, Kaouts- kaia A, Haj-Yahia S, Newman D, et al. Impact of contact force technology on atrial fibrillation ablation: a meta-analysis. J Am Heart Assoc 2015; 4:e002476.
2. McLellan AJ, Ling LH, Azzopardi S, Lee GA, Lee G, Kumar S, et al. A minimal or maximal ablation strategy to achieve pulmonary vein isolation for paroxysmal atrial fibrillation: a prospective mul- ti-centre randomized controlled trial (the MINIMAX study). Eur Heart J 2015;36:1812–21.
3. Macle L, Khairy P, Weerasooriya R, Novak P, Verma A, Willems S, et al; ADVICE trial investigators. Adenosine-guided pulmonary vein isolation for the treatment of paroxysmal atrial fibrillation: an international, multicentre, randomised superiority trial. Lancet 2015;386:672–9.
4. Kobori A, Shizuta S, Inoue K, Kaitani K, Morimoto T, Nakazawa Y, et al; UNDER-ATP Trial Investigators. Adenosine triphosphate-guided pulmonary vein isolation for atrial fibrillation: the unmasking dormant electrical reconduction by adenosi- ne triphosphate (under-ATP) trial. Eur Heart J 2015;36:3276–87.
5. Kaitani K, Inoue K, Kobori A, Nakazawa Y, Ozawa T, Kurotobi T, et al; EAST-AF Trial Investigators. Efficacy of antiarrhythmic drugs short-term use after catheter ablation for atrial fibrillation (EASTAF) trial. Eur Heart J 2016;37:610-8.
6. Darkner S, Chen X, Hansen J, Pehrson S, Johannessen A, Nielsen JB, et al. Recurrence of arrhythmia following shortterm oral amiodarone after catheter ablation for atrial fibrillation: a double-blind, randomized, placebo-controlled study (AMIO-CAT trial). Eur Heart J 2014;35:3356–64.
7. Cosedis Nielsen J, Johannessen A, Raatikainen P, Hindricks G, Walfridsson H, Kongstad O, et al. Radiofrequency ablation as initial therapy in paroxysmal atrial fibrillation. N Engl J Med 2012;367:1587–95.
8. Aliot E, Brandes A, Eckardt L, Elvan A, Gulizia M, Heidbuchel H, et al. The EAST study: redefining the role of rhythm control therapy in atrial fibrillation: EAST, the early treatment of atrial fibrillation for stroke prevention trial. Eur Heart J 2015;36:255–6.
9. Moreno J, Zamorano JL. The CABANA trial. Eur Heart J 2014;35:1908–9.
10. Benharash P, Buch E, Frank P, Share M, Tung R, Shivkumar K, et al. Quantitative analysis of localized sources identified by focal impulse and rotor modulation mapping in atrial fibrillation. Circ Arrhythm Electrophysiol 2015;8:554–61.
11. Providencia R, Lambiase PD, Srinivasan N, Ganesh Babu G, Bronis K, Ahsan S, et al. Is there still a role for complex fractionated atrial electrogram ablation in addition to pulmonary vein isolation in patients with paroxysmal and persistent atrial fibrillation? Meta-analysis of 1415 patients. Circ Arrhythm Electrophysiol 2015;8:1017–29.
12. Pathak RK, Middeldorp ME, Meredith M, Meh- ta AB, Mahajan R, Wong CX, et al. Longterm effect of goal-directed weight management in an atrial fibrillation cohort: a long-term follow-up study (LEGACY). J Am Coll Cardiol 2015;65:2159–69.
13. Camm AJ, Lip GY, De Caterina R, Savelieva I, Atar D, Hohnloser SH, et al. 2012 focused update of the ESC guidelines for the management of atrial fibrillation: an update of the 2010 ESC guidelines for the management of atrial fibrillation developed with the special contribution of the European Heart Rhythm Association. Europace 2012;14:1385–413.
14. Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al; the EAFTI. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2013;386:2093–104.
15. Held C, Hylek EM, Alexander JH, Hanna M, Lo- pes RD, Wojdyla DM, et al. Clinical outcomes and management associated with major bleeding in patients with atrial fibrillation treated with apixaban or warfarin: insights from the ARISTOTLE trial. Eur Heart J 2015;36: 1264–72.
16. Cappato R, Marchlinski FE, Hohnloser SH, Naccarelli GV, Xiang J, Wilber DJ, et al; VENTURE-AF Investigators. Uninterrupted rivaroxaban vs. uninterrupted vitamin K antagonists for catheter ablation in non-valvular atrial fibrillation. Eur Heart J 2015;36:1805–1811.
17. Steffel J, Giugliano RP, Braunwald E, Murphy SA, Atar D, Heidbuchel H, et al. Edoxaban vs. warfarin in patients with atrial fibrillation on amiodarone: a subgroup analysis of the engage AF-TIMI 48 trial. Eur Heart J 2015; 36:2239–45.
18. Camm AJ, Amarenco P, Haas S, Hess S, Kirchhof P, Kuhls S, et al; Investigators X. XANTUS: a real-world, prospective, observational study of patients treated with rivaroxaban for stroke prevention in atrial fibrillation. Eur Heart J 2015; doi:10.1093/eurheartj/ehv466. Published online ahead of print 1 September 2015.
19. Glund S, Stangier J, Schmohl M, Gansser D, Norris S, van Ryn J, et al. Safety, tolerability, and efficacy of idarucizumab for the reversal of the anticoagulant effect of dabigatran in healthy male volunteers: a randomised, placebo-controlled,dou- ble-blindphase1trial.Lancet 2015; 386:680–90.
20. Pollack CV Jr, Reilly PA, Eikelboom J, Glund S, Verhamme P, Bernstein RA, et al. Idarucizumab for dabigatran reversal. N Engl J Med 2015;373:511–20.
21. Heidbuchel H, Verhamme P, Alings M, Antz M, Diener HC, Hacke W, et al. Updated European Heart Rhythm Association practical guide on the use of non-vitamin K antagonist anticoagulants in pa- tients with non-valvular atrial fibrillation. Europace 2015;17:1467–507.
22. Heidbuchel H, Verhamme P, Alings M, Antz M, Hacke W, Oldgren J, et al. EHRA practical guide on the use of new oral anticoagulants in patients with non-valvular atrial fibrillation: executive summary. EurHeartJ2013; 34:2094–106.
23. Karasoy D, Gislason GH, Hansen J, Johannessen A, Kober L, Hvidtfeldt M, et al. Oral anticoagulation therapy after radiofrequency ablation of atrial fibrillation and the risk of thromboembolism and serious bleeding: long-term follow-up in nation- wide cohort of Denmark. Eur Heart J 2015;36: 307–314a.
24. Kirchhof P, Purmah Y, Verma A. Oral anticoagulation after catheter ablation of atrial fibrillation: caught in the attribution trap? Eur Heart J 2015;36:267–9.
25. Tanawuttiwat T, Nazarian S, Calkins H. The role of catheter ablation in the management of ventricular tachycardia. Eur Heart J 2016;37:594–609.
26. Andreu D, Ortiz-Perez JT, Fernandez-Armenta J, Guiu E, Acosta J, Prat Gonzalez S, et al. 3D delayed-enhanced magnetic resonance sequences improve conducting channel delineation prior to ven- tricular tachycardia ablation. Europace 2015; 17:938-45.
27. Berte B, Cochet H, Magat J, Naulin J, Ghidoli D, Pillois X, et al. Irrigated needle ablation creates larger and more transmural ventricular lesions compared to standard unipolar ablation in an ovine mo- del. Circ Arrhythm Electrophysiol 2015;8:1498–506.
28. Berte B, Relan J, Sacher F, Pillois X, Appetiti A, Yamashita S, et al. Impact of electrode type on mapping of scar-related VT. J Cardiovasc Electrophysiol 2015; doi:10.1111/jce.12761.
29. Jesel L, Sacher F, Komatsu Y, Daly M, Zellerhoff S, Lim HS, et al. Characterization of contact force during endocardial and epicardial ventricular mapping. Circ Arrhythm Electrophysiol 2014;7:1168-73.
30. Hooks DA, Yamashita S, Capellino S, Cochet H, Jais P, Sacher F. Ultrarapidepicardial activation mapping during ventricular tachycardia using continuous sampling from a high-density basket (ORION(TM)) catheter. J Cardiovasc Electrophysiol 2015;26:1153-4.
31. Yokokawa M, Kim HM, Baser K, Stevenson W, Nagashima K, Della Bella P, et al. Predictive value of programmed ventricular stimulation after catheter ablation of post-infarction ventricular tach- ycardia. J Am Coll Cardiol 2015;65: 1954–9.
32. Komatsu Y, Maury P, Sacher F, Khairy P, Daly M, Lim HS, et al. Impact of substrate-based ablation of ventricular tachycardia on cardiac mortality in patients with implantable cardioverter-defibrilla- tors. J Cardiovasc Electrophysiol 2015; doi:10.1111/jce.12825.
33. Dinov B, Arya A, Schratter A, Schirripa V, Fiedler L, Sommer P, et al. Catheter ablation of ventricular tachycardia and mortality in patients with non ischemic dilated cardiomyopathy: cannon inducibility after ablation be a predictor for reduced mortality? Circ Arrhythm Electrophysiol 2015;8: 598–605.
34. Brugada J, Pappone C, Berruezo A, Vicedomini G, Manguso F, Ciconte G, et al. Brugada syndrome phenotype elimination by epicardial sub- strate ablation. Circ Arrhythm Electrophysiol 2015; 8:1373–81.
35. Authors/Task Force M, Priori SG, Bloms- trom-Lundqvist C, Mazzanti A, Blom N, Borg- grefe M, et al. 2015 ESC guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: the task for- ce for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death of the European Society of Cardiology (ESC) endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC). Eur Heart J 2015; doi:10.1093/eurheartj/ehv316. Published onli- ne ahead of print 29 August 2015.
36. Ritter P, Duray GZ, Steinwender C, Soejima K, Omar R, Mont L, et al; Micra Transcatheter Pa- cing Study Group. Early performance of a miniatu- rized leadless cardiac pacemaker: the MICRA Trans- catheter Pacing Study.EurHeartJ2015;36:2510–9
37. Reynolds D, Duray GZ, Omar R, Soejima K, Neuzil P, Zhang S, et al; Micra Transcatheter Pacing Study Group. A leadless intracardiac transcatheter pacing system. N Engl J Med2015. [Epub ahead of print].
38. Reddy VY, Exner DV, Cantillon DJ, Doshi R, Bunch TJ, Tomassoni GF, et al; LEADLESS II Study Investigators. Percutaneous implantation of an entirely intracardiac leadless pacemaker. N Engl J Med 2015;373:1125–35.
39. Bansch D, Bonnemeier H, Brandt J, Bode F, Svendsen JH, Taborsky M, et al; NORDIC ICD Trial Investigators. Intra-operative defibrillation testing and clinical shock efficacy in patients with implantable cardioverter-defibrillators: the NORDIC ICD randomized clinical trial. Eur Heart J 2015;36:2500–7.
40. Healey JS, Hohnloser SH, Glikson M, Neuzner J, Mabo P, Vinolas X, et al; Shockless IMPLant Evaluation [SIMPLE] Investigators. Cardioverter defibrillator implantation without induction of ventricular fibrillation: a single-blind, noninferio- rity, randomised controlled trial (SIMPLE). Lancet 2015;385:785–91.
41. Varma N, Ricci RP. Telemedicine and cardiac implants: what is the benefit? Eur Heart J 2013;34: 1885-95.
42. Varma N, Piccini JP, Snell J, Fischer A, Dalal N, Mittal S. The relationship between level of adherence to automatic wireless remote monitoring and survival in pacemaker and defibrillator patients. J Am Coll Cardiol 2015;65:2601–10.
43. Abraham WT, Stevenson LW, Bourge RC, Lindenfeld JA, Bauman JG, Adamson PB; CHAMPION Trial Study Group. Sustained efficacy of pulmonary artery pressure to guide adjustment of chronic heart failure therapy: complete follow-up results from the CHAMPION randomised trial. Lancet 2015. [Epub ahead of print].
44. Brisben AJ, Burke MC, Knight BP, Hahn SJ, Herrmann KL, Allavatam V, et al. A new algorithm to reduce inappropriate therapy in the S-ICD system. J Cardiovasc Electrophysiol 2015;26:417–23.
45. Lambiase PD, Barr C, Theuns DA, Knops R, Neuzil P, Johansen JB, et al; Investigators E. Worldwide experience with a totally subcutaneous implantable defibrillator: early results from the ef- fortless S-ICD registry. Eur Heart J 2014;35: 1657– 65.
46. Knops RE, Brouwer TF, Barr CS, Theuns DA, Boersma L, Weiss R, et al; Investigators E. The learning curve associated with the introduction of the subcutaneous implantable defibrillator. Europace 2015; doi:10.1093/europace/euv299.
47. Burke MC, Gold MR, Knight BP, Barr CS, Theuns DA, Boersma LV, et al. Safety and efficacy of the totally subcutaneous implantable defibrillator: 2-year results from a pooled analysis of the IDE study and effortless registry. J Am Coll Cardiol 2015;65: 1605–15.
48. Kutyifa V, Moss AJ, Klein H, Biton Y, McNitt S, MacKecknie B, et el. Use of the wearable cardioverter defibrillator in high-risk cardiac patients: data from the prospective registry of patients using the wearable cardioverter defibrillator (WEARIT-II registry). Circulation 2015;132:1613-9.