Almanac 2015: Investigación sobre fibrilación auricular en Heart
Almanac 2015: Investigación sobre fibrilación auricular en Heart
Revista Uruguaya de Cardiología, vol. 31, núm. 3, pp. 461-473, 2016
Sociedad Uruguaya de Cardiología
Recepción: 01 Octubre 2015
Aprobación: 26 Noviembre 2015
Financiamiento
Fuente: Charite Berlin (MonDAFIS), BHF
Nº de contrato: FS/13/32/30324
Beneficiario: Almanac 2015: Investigación sobre fibrilación auricular en Heart
Fuente: Fundación Leducq
Resumen: La fibrilación auricular sigue generando interés en la comunidad cardiovascular y en Heart. Más de 60 trabajos origina- les de investigación y revisiones fueron publicados en Heart en 2014-2015 abarcando diferentes aspectos de la fibrilación auricular, desde las condiciones asociadas y los factores precipitantes hasta nuevos enfoques del tratamiento. Aquí se presenta una reseña general de los artículos sobre fibrilación auricular publicados en Heart en 2014-2015, destacando lo nuevo, los conceptos que van surgiendo y los enfoques de tratamiento novedosos.
Introducción
Los años 2014 y 2015 han sido muy activos en la investigación de la fibrilación auricular (FA), y los aportes de Heart en este tema han sido muy importantes. Los artículos reflejan la naturaleza diversa de los problemas que aquejan a los pacientes con FA y sus médicos, que van desde factores que permiten estimar el riego de complicaciones cardiovasculares y nuevas hipótesis sobre la relación de la FA con biomarcadores, hasta perspectivas sobre la mejor manera de enfocar la anticoagulación, control de la frecuencia y tratamiento de control del ritmo. En el presente artículo resumimos algunos de los hallazgos más interesantes sobre FA comunicados en Heart en los años 2014 y 2015.
Factores de riesgo para el desarrollo y progresión de la fibrilación auricular
ECG basal, frecuencia cardíaca y edad
Un registro estadounidense (ORBIT - AF Outcomes Registry for Better Informed Treatment of Atrial Fibrillation) analizó a más de 6.000 pacientes, investigando el riesgo que la FA pasara de ser paroxística a persistente y luego a permanente(1). Se encontró que un aumento de la edad en diez años (OR 1,16) y la presencia de FA en el electrocardiograma (ECG) basal (OR 2,30) eran fuertes predictores de progresión de la FA. Entretanto, una disminución de la frecuencia cardíaca a menos de 80 (OR 0,84) surgió como un elemento de protección contra la progresión de la FA.
Disfunción diastólica
Los resultados del subanálisis del estudio Tromsø en Noruega mostraron que el tamaño auricular severamente aumentado como marcador de disfunción diastólica solo constituía un marcador ecocardiográfico asociado con el riesgo de presentar FA (HR 4,2)(3). Ese hallazgo fue independiente de otros índices de Doppler de disfunción diastólica de la válvula mitral. El tamaño de la aurícula izquierda (AI) aumenta al incrementarse la disfunción diastólica como consecuencia de cambios prolongados de la dinámica de flujo del corazón izquierdo.
Ivabradina
Un importante metaanálisis identificó un riesgo pequeño (riesgo relativo [RR] 1,15) pero relevante de desarrollar FA en pacientes tratados con ivabradina(2). Este efecto se observa incidentalmente en el mismo grupo de pacientes (frecuencia cardíaca basal >70) que se benefician más de la ivabradina por su disminución de las internaciones. Este RR de desarrollar FA podría atribuirse a cambios en la corriente I. inducidos por ivabradina, una modificación del potencial de membrana de reposo auricular, o a posibles efectos pro arrítmicos de la bradicardia. Se necesitaría contar con estudios mecanicistas para identificar los mecanismos de inducción de la FA provocada por ivabradina (figura 1).
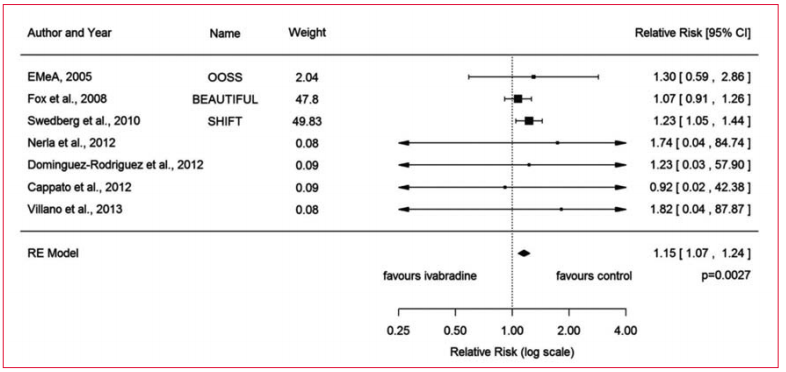
Figura 1
Gráfico: fibrilación auricular con ivabradina(2). RR: riesgo relativo.
Hemodiálisis
Un análisis “generador de hipótesis” de una cohorte de pacientes en diálisis con implante de marcapasos o desfibrilador sugirió que el procedimiento de hemodiálisis de por sí podría desencadenar FA(4). La aparición de episodios de eventos auriculares de al- ta frecuencia (AHRE, por su sigla en inglés) cercanos al momento de la diálisis puede considerarse co- mo una medida sustituta de FA. Se considera que la asociación entre un mayor volumen extraído y una menor concentración de potasio dializado son un desencadenante de FA. Comparativamente los pacientes sometidos a diálisis peritoneal tienen menos episodios de FA. Estos hallazgos concuerdan con lo hallado en otros estudios, en los que se incluyen edad, sexo, enfermedad arterial coronaria y dimen- siones auriculares como riesgos adicionales de presentar FA en pacientes sometidos a hemodiálisis (figura 2)(5,6).
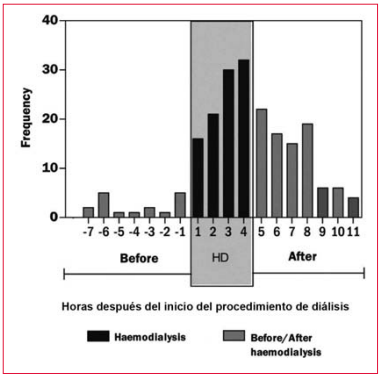
Figura 2
Aparición de episodios de fibrilación auricular en relación con el inicio de hemodiálisis(4).
Ejercicio
Varios trabajos han valorado el impacto del ejercicio físico sobre el riesgo de presentar AF(7,8). Un intere sante estudio sueco que registró más de 44.000 hombres adultos sanos demostró una relación en forma de U entre el ejercicio y el riesgo de FA(9). Los autores encontraron que un ejercicio de moderado a intenso en momentos de ocio, andar en bicicleta o caminar durante más de 60 minutos en un día se acompañaba de un RR de 1,17 y 1,04 de desarrollar FA más adelante en la vida. Es interesante destacar que esta tendencia se revierte al avanzar la edad, con una reducción del RR pese a niveles similares de ejercicio. Se observan tendencias favorables similares del ejercicio para las mujeres de edad mediana y avanzada(10) .
Es un hecho bien establecido que la capacidad de ejercicio se reduce en la FA, con o sin la presencia de deterioro de la función sistólica del ventrículo izquierdo(11,12). Se sugiere que la FA paroxística (FAP) podría agregarse al interjuego entre el ejercicio y las patologías heredadas tales como la miocardiopatía hipertrófica(13). Los pacientes con FAP tienen una tolerancia sustancialmente menor al ejercicio, aun manteniéndose en ritmo sinusal (RS) durante las pruebas de ejercicio. Luego de ajustar para edad, sexo e índice de masa corporal, la FAP siguió teniendo un RR independiente de 4,65 para reducción de la tolerancia al ejercicio.
Ausencia de beneficios por el cierre de una comunicación interauricular
Un estudio danés sobre pacientes adultos con diagnóstico de comunicación interauricular (CIA) muestra que el cierre de la CIA aumenta el riesgo de nueva FA (HR 8,4) comparado con una cohorte apareada para edad y sexo con una incidencia acumulada a los 10 años de 11%(14). El riesgo de accidente cerebrovascular fue más alto en los pacientes con CIA con o sin cierre de la misma (HR 2 y 2,6 respectivamente), sugiriendo que el cierre de la CIA no evita la FA. Esta observación sugiere que hay otros factores aparte de la función hemodinámica alterada que determinan la aparición de FA en pacientes con CIA. Alternativamente, un cierre de la CIA más tempra- no quizá sea necesario para prevenir esta arritmia.
Otras asociaciones con fibrilación auricular generadoras de hipótesis
En 2014 se publicó un análisis de la base de datos del Proyecto de Auditoría Nacional de Isquemia Miocárdica que cubre todos los procedimientos de intervención coronaria percutánea (ICP) en Inglaterra y Gales para ver los efectos a corto plazo de la contaminación aérea sobre los eventos cardiovasculares en esos dos países(15). Este estudio mostró un aumento del riesgo de ingresos hospitalarios debido a FA y arritmias con altos niveles de NO2. Un alto contenido de partículas en suspensión de menos de 2,5 mm de diámetro se acompañó de un aumento de la mortalidad secundaria a FA, arritmia y embolia pulmonar.
Un estudio observacional para determinar el riesgo de presentar aleteo y FA en pacientes ingresados con pericarditis mostró una tasa de incidencia de 4,3%, y más de 90% presentaban un episodio de FA en las primeras 24 horas(16). Todos ellos revirtieron al ritmo sinusal. Sin embargo, en los pacientes que presentaron FA al inicio hubo una tasa de recurrencia de 35% a los tres meses. Los autores plantearon anticoagular a los pacientes de alto riesgo. No se demostró un aumento del riesgo de taponamiento pericárdico con la terapia anticoagulante.
Biomarcadores en fibrilación auricular
En los últimos tiempos los biomarcadores han generado mucho interés para la predicción, el diagnóstico y la estratificación de riesgo pronóstico de FA(17-20).
Niveles de troponina I, péptidos natriuréticos y noradrenalina
Un subestudio del RE-LY (Randomized Evaluation of Longterm anticoagulant TherapY) sobre el valor pronóstico y la estratificación de riesgo de biomarcadores en la FA ha señalado un uso interesante de biomarcadores cardíacos(21). El estudio indica que los niveles seriados elevados de troponina I cardíaca (cTnI) y el propéptido natriurético cerebral N terminal (NT-proBNP) están asociados con una mayor incidencia de accidentes cerebrovasculares, embolia sistémica (HR 4,54) y muerte vascular (HR 8,62). Otros encontraron ya antes una similar asociación entre estos biomarcadores y el pronóstico de FA(22-25). Un estudio japonés mostró niveles más elevados de péptido natriurético auricular, péptido natriurético cerebral y noradrenalina (NA) en la FA persistente comparado con la FAP(26). Únicamente los niveles elevados de NA mostraron una asociación con el síndrome del disfunción sinusal (figura 3).
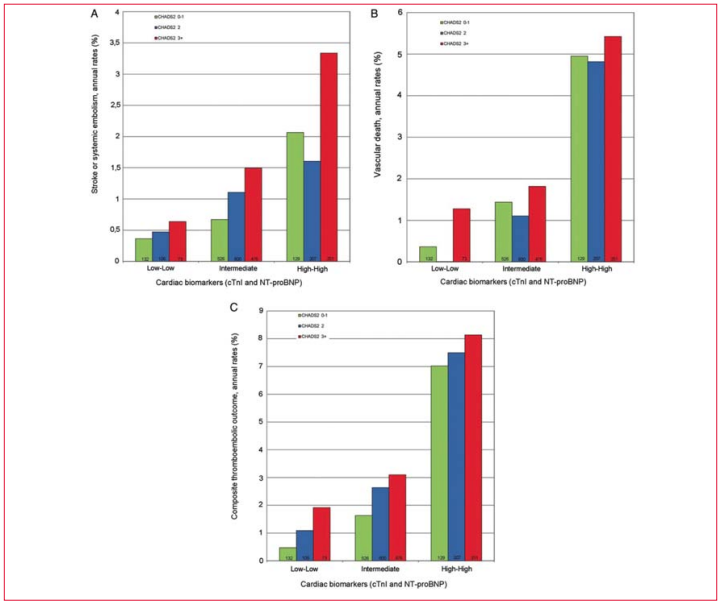
Figura 3
Variables evaluables del estudio en relación con los niveles combinados de los biomarcadores cardíacos y la puntuación CHADS2. Accidente cerebrovascular o embolia sistémica (A), muerte vascular (B), y resultados tromboembólicos compuestos que consisten en accidente cerebrovascular isquémico, embolia sistémica, infarto miocárdico, embolia pulmonar y muerte vascular(C)(21). cTnI: troponina cardíaca. NT-pro BNP: N propéptido natriuretico cerebral N terminal. CHADS2: puntuación de accidente cerebro vascular (basado en un punto cada uno para insuficiencia cardíaca Congestiva, Hipertensión, Edad (Age) mayor a 75, Diabetes mellitus y dos puntos por antecedentes de accidente cerebrovascular o AIT).
Enzimas hepáticas
En un gran estudio de cohorte comunitario prospectivo de más de 15.000 sujetos se encontró que un aumento de los niveles circulantes de enzimas hepáticas tiene una asociación moderadamente fuerte con un aumento de la incidencia de FA(27). La asociación fue lineal y más fuerte para la gama glutamil transferasa (GGT), viéndose que la duplicación de los niveles de GGT llevaban a un aumento de 20% del riesgo de FA luego de ajustar por factores de confusión. La asociación de la incidencia de FA y la aspartamo amino transferasa (AST) y en menor grado la alanino amino transferasa (ALT) mostraron una curva en U, con una incidencia máxima en los dos extremos. Esto se puede explicar por insuficiencia cardíaca derecha, la que provoca congestión hepáti- ca o enfermedad de hígado graso no alcohólica que aumenta el riesgo cardiovascular debido a su efecto sobre el metabolismo de la glucosa y los lípidos(28-30). En un subanálisis del estudio de Framingham(31) se publicó también una correlación entre las alteraciones de las pruebas de funcionalidad hepática y el riesgo de enfermedad cardiovascular.
Adiponectina
Se observó una asociación entre la elevación de los niveles circulantes de adiponectina y el riesgo de presentar FA en función del aumento de la edad(32). Esto se contrapone a la creencia contemporánea de que los niveles elevados de adiponectina resultan cardioprotectores. Se necesita más trabajo en este terreno para identificar una clara asociación con este nuevo biomarcador.
Epidemiología y factores de riesgo
Aumento de la incidencia de fibrilación auricular en el Reino Unido
Un gran estudio de cohorte poblacional analizó los registros de altas de 2,2 millones de individuos de 45 años y mayores, del Datalink de Investigación de Práctica Clínica del Reino Unido(33). Encontraron más de 91.000 casos incidentes de FA. La incidencia de FA ha aumentado de 5,9/1.000 personas-años en 2001 a 6,9/1.000 personas-años en 2013. La incidencia general en términos de 1.000 personas-años aumenta con la edad (25,1 para pacientes entre 80 y 89 años), es más alto para caucásicos (8,1) comparado con asiáticos (5,4) y afroamericanos (4,6).
Valor predictivo de las puntuaciones CHADS. y CHA.DS2Vasc para eventos cardiovasculares en pacientes sin fibrilación auricular
Las puntuaciones CHADS. y CHA.DS.Vasc han sido validadas para predecir el riesgo de accidente cerebrovascular en pacientes con FA(34,35). En un estudio se utilizaron estas puntuaciones para evaluar el riesgo de nuevo accidente cerebrovascular/accidente isquémico transitorio (AIT) en ausencia de FA en pacientes con síndrome coronario agudo (SCA)(36). Ambas puntuaciones mostraron una razonable asociación entre el riesgo anual predicho de accidente cerebrovascular/AIT con una incidencia anual absoluta de 1% con CHADS. S3 y CHA.DS.Vasc S 4. Esto concuerda con los resultados de otro estudio realizado por Poci y colaboradores(37), que encontraron asociación de CHADS. con mortalidad y accidente cerebrovascular. Otros autores han demostrado asociación de estas puntuaciones con mortalidad tras accidente cerebrovascular, riesgo de presentar nueva FA y riesgo de accidente cerebrovascular o muerte después de cirugía de revascularización coronaria(38-40).
Fibrilación auricular e insuficiencia cardíaca
La FA y la insuficiencia cardíaca a menudo son “malas compañeras” y cada condición puede empeorar a la otra. Un estudio en Tanzania mostró que se atribuía a la FA al menos el 16% de los casos de insuficiencia cardíaca clínica que se presentaban en el hospital de cuidados terciario(41). Este es un hallazgo interesante si se compara con el estudio EPOCH (Epidemiology, Practice, Outcomes, and Costs of Heart Failure) realizado en Estados Unidos en 2004 que comparó las características epidemiológicas de los pacientes hospitalizados con insuficiencia cardíaca y la asociación de diversas comorbilidades con diferentes etnias, que mostraron una prevalencia de FA de 19,7% en afroamericanos con insuficiencia cardíaca, comparado con 38,3% en pacientes caucásicos con insuficiencia cardíaca(42). El informe ilustra el impacto global de la FA y de la insuficiencia cardíaca.
Fibrilación auricular como predictor de mortalidad aumentada en la estenosis aórtica de bajo gradiente
La FA resultó ser un predictor independiente de mortalidad (HR 1,74) en pacientes con estenosis aórtica (EA) en un gran estudio observacional en un único centro, que registró pacientes con EA severa que recibieron tratamiento médico, reemplazo quirúrgico de válvula aórtica o implante transcatéter de válvula aórtica(43). En general el grupo que recibió tratamiento médico tuvo peor pronóstico, con una mortalidad por todas las causas de 81% a 3,9 años de seguimiento. Un estudio mostró a la FA como un determinante de estado de bajo flujo en la EA severa (OR 4,17)(44). En otro estudio los pacientes con EA severa de bajo gradiente, la FA también se asoció con mal pronóstico y un aumento de la mortalidad(45). Estas observaciones destacan la importancia de diagnosticar FA en pacientes con EA.
Prevalencia general de fibrilación auricular en pacientes internados
Una interesante encuesta transversal realizada en un único día en un hospital belga de atención terciaria identificó una prevalencia total de FA de 16,8%(46). La presencia de FA se acompañó de mayor edad, hipertensión arterial y cardiopatía valvular. Es interesante destacar que solo el 51% estaba siendo correctamente tratado con anticoagulación oral.
Pronóstico de fibrilación auricular silente luego de infarto de miocardio
Un estudio observacional realizado por Stamboul y colaboradores muestra un peor pronóstico al año, con un aumento de los ingresos hospitalarios y empeoramiento de la insuficiencia cardíaca en los pacientes en los que se halló FA silente dentro de los primeros dos días del ingreso por infarto agudo de miocardio (IAM)(47). Previamente se ha sugerido que la FA silente era tres veces más frecuente que la FA sintomática luego de IMA(48). Esto destaca la importancia de un monitoreo continuo de ECG en todos los pacientes con IAM para detectar FA.
Tamizaje para la fibrilación auricular silente
El diagnóstico temprano de FA es altamente deseable, ya que permite iniciar el tratamiento antes de la primera complicación(49). Un artículo de revisión arroja luz sobre técnicas emergentes para el tamizaje de la FA(50). Los monitores electrocardiográficos manejados por los propios pacientes o sensores con teléfonos celulares inteligentes pueden ser herramientas adecuadas para la detección de FA(51-54). En algunos pacientes seleccionados el tamizaje a largo plazo con registrador de eventos implantable permite detectar más episodios de FA(55). Queda mucho por comprender sobre la necesidad de programas de tamizaje de FA, su óptimo diseño y el mejor uso del tratamiento (fundamentalmente de la anticoagulación oral). Hay estudios en curso que evalúan cuándo iniciar la anticoagulación en pacientes con episodios de alta frecuencia auricular (por ejemplo, ARTESiA o NOAH- AFNET 6) y los programas de tamizaje en la comunidad tales como STROKESTOP(56,57) seguramente brindarán más información en el futuro.
Imagenología en fibrilación auricular
Factores pronósticos basados en parámetros imagenológicos
Un artículo de revisión destaca varias características pronósticas adversas en la imagenología para la FA(58). En la ecocardiografía bidimensional convencional la dilatación de la AI y la función sistólica del ventrículo izquierdo demostraron estar asociadas con un aumento del riesgo de accidente cerebrovas- cular, insuficiencia cardíaca y mortalidad por todas las causas. La estenosis mitral y la miocardiopatía hipertrófica (MCH) también aumentan fuertemente el riesgo de accidente cerebrovascular en FA. En la ecocardiografía transesofágica (ETE), el contraste espontáneo, los trombos en la AI y las placas complejas en la válvula aórtica (VA) predicen un aumento del riesgo de tromboembolismo sistémico y accidente cerebrovascular. En la resonancia nuclear magnética (RNM) cardíaca (CMRI) los parámetros favorables se acompañaron de una disminución del riesgo de accidente cerebrovascular (OR 0,2). Además, la función de conducción de la AI medida por CMRI fue una importante medida de éxito luego de ablación por catéter (figura 4).
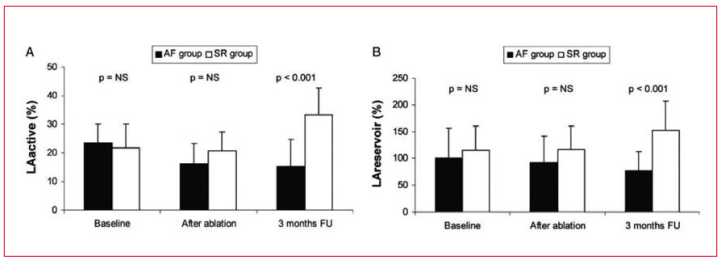
Figura 4
Cambios en la función de la aurícula izquierda tras ablación con catéter. El grupo RS muestra una mejora en la función de reservorio de la aurícula izquierda. AF: fibrilación auricular; LA: aurícula izquierda; NS: no significativo.
RNM cerebral para adaptar la anticoagulación
Otro artículo de revisión analizó el valor de la imagenología cerebral con RNM para adaptar la terapia anticoagulante(59). Se encontró que es frecuente observar infartos cerebrales silentes en pacientes con FA(60,61), dependiendo de la edad del paciente y del tipo de FA. La presencia de microsangrados cerebrales (MSC), que se hallan fre- cuentemente en pacientes con FA sin antecedentes de accidente cerebrovascular, deben ser considerados como un riesgo de sangrado intracraneano en caso de anticoagular al paciente. Sin embargo, se necesitan estudios de gran tamaño para confirmar esta observación. El número y la ubicación de los MSC se ven afectados por las puntuaciones de CHADS2 y CHA2DS2Vasc. Esto es fundamentalmente debido al efecto de los factores de riesgo vascular (figura 5)(62).
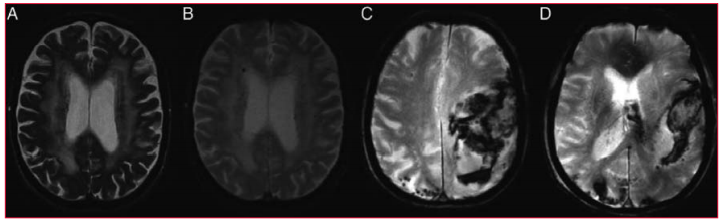
Figura 5
Pacientes con fibrilación auricular considerados como no adecuados para anticoagulación oral T2 (A) y T2* (B) imagen a 1,5 T que demuestra la confluencia de hiperintensidades de sustancia blanca y microsangrados cerebrales en un paciente con fibrilación auricular con imágenes (C/D) de accidente isquémico transitorio reciente en 3,0 T, demostrando una hemorragia lobar aguda y múltiples microsangrados cerebrales en un paciente con fibrilación auricular con sospecha de angiopatía amiloide cerebral(59).
Mapeo de potenciales en superficie corporal e imagenología ECG en la fibrilación auricular También se destacó el uso de imagenología ECG, una modalidad imagenológica novedosa de la fibrilación en la que se utiliza ECG de superficie combinado con TC/RNM cardíaca para evaluar la anatomía auricular y la complejidad de la FA(63). Más recientemente, el mapeo de potenciales de superficie corporal ha demostrado identificar fuentes de alta frecuencia en las aurículas sin una modalidad imagenológica que se midiera previamente con métodos cruentos(64). Tal vez esto permita seleccionar mejor a los pacientes previo al procedimiento de ablación de la FA basado en una mejor predicción de la respuesta a esta terapia.
Anticoagulación para prevención del accidente cerebrovascular
¿Qué terapia antitrombótica utilizar: NOAC, antagonistas de la vitamina K, terapia combinada?
Un gran metaanálisis de una red de 20 estudios que combinaban más de 78.000 pacientes demostró que los nuevos anticoagulantes orales (NOAC, por su sigla en inglés) daban mejores resultados en la reducción del riesgo de accidente cerebrovascular o de embolismo venoso. Otro metaanálisis con más de 100.000 pacientes mostró una reducción de las probabilidades de riesgo de 47% y 64% de sangrado fatal con NOAC comparado con antagonistas de la vitamina K (AVK) y heparina de bajo peso molecular (HBPM)(66).
Está bien establecido que la terapia antiplaquetaria combinada y la anticoagulación aumentan el riesgo de sangrado y que dicha “triple terapia” debería confinarse a períodos breves de tiempo en pacientes seleccionados con SCA o ICP reciente(67,68). Un análisis de un gran conjunto de datos europeos identificó un error común en la terapia antitrombótica en pacientes con FA, es decir, la continuación de la terapia con aspirina en pacientes con enfermedad vascular estable(69). Mucho más de la mitad de los pacientes sometidos a terapia de combinación con aspirina y anticoagulación oral no tenían indicación de terapia de combinación, poniéndolos en un riesgo innecesario de sangrado.
El ensayo TIARA comparó la aspirina y anticoagulación en una cohorte de 238 pacientes con FA con riesgo moderado de accidente cerebrovascular y características imagenológicas “favorables” en la ETE, y sugirió que algunos pacientes pueden marchar bien sin anticoagulación(70). Encontraron que en ausencia de trombos en la AI en la ETE, la aspirina no fue inferior a AVK para la mortalidad por todas las causas, accidente cerebrovascular, síndrome coronario agudo y sangrado mayor. Es interesante destacar que no se incluyeron los AIT como punto final primario, y en el grupo de aspirina hubo siete pacientes que presentaron AIT. Esto destaca las dificultades cuando se considera una terapia de anticoagulación individualizada en pacientes con riesgo de bajo a moderado de presentar accidente cerebrovascular. Los resultados de este estudio piloto necesitan validación para un ensayo a mayor escala.
Anticoagulación en el flutter auricular
Un artículo de revisión publicado en 2015, que consideró 52 artículos publicados, indicó que el flutter auricular entraña un mayor riesgo de complicaciones tromboembólicas(71). Las imágenes en el aleteo auricular también revelan alta prevalencia de contraste espontáneo y trombos en la orejuela de la aurícula izquierda (OAI). Pese a las limitaciones debidas a los pocos datos publicados, este análisis subraya la práctica actual de ofrecer anticoagulación a los pacientes con flutter auricular.
Ablación de fibrilación auricular
Ablación quirúrgica
Se ha publicado un metaanálisis que resume la in- formación disponible sobre la ablación quirúrgica para FA(72). Este metaanálisis amplio y primero de su tipo sugiere que la ablación quirúrgica de la AI es un método seguro y eficaz de mantener el ritmo sinusal durante más de un año en pacientes con FA y sometidos a cirugía cardíaca concomitante comparado con la cirugía cardíaca sola.
NOAC o warfarina en la ablación por catéter
Un metaanálisis de 14 conjuntos de datos observacionales comparó dabigatrán y warfarina en cuanto a los riesgos de eventos tromboembólicos y sangrados mayores(73). No hubo una diferencia significativa entre los grupos para ninguna de las dos variables evaluables. Sin embargo, se observó una diferencia numérica de más eventos tromboembólicos en el grupo de dabigatrán comparado con warfarina (0,55% para dabigatrán contra 0,17% para warfarina, RR 1,78, IC 95% 0,66 a 4,80, p=0,26).
Otro metaanálisis de estudios observacionales también mostró una tendencia no significativa pero superior de peores resultados neurológicos con dabigatrán comparado con warfarina(74). No se encontró diferencia significativa entre dabigatrán y warfarina en otros metaanálisis(75). Se necesitan ensayos controlados de esquemas de anticoagulación ininterrumpidos en pacientes sometidos a ablación de FA.
Cambios en la función renal asociados con la recurrencia de arritmia
Un estudio alemán con una cohorte de 783 pacientes encontró una asociación entre la recurrencia de la FA y un empeoramiento de la función renal (VFG)(76). Se encontró que los pacientes con recurrencia tenían peor VFG a nivel basal y en el seguimiento. Cuanto más altos los puntajes de CHADS2 y CHA2DS2Vasc, peores eran las funciones renales. Finalmente, aquellos pacientes que tenían una declinación de su VFG tenían mayores recurrencias de FA. Este efecto fue independiente del tipo de ACO utilizado. Se sabe que la FA disminuye la función renal(77). Esto podría ser debido al fenómeno embólico o a los mecanismos hemodinámicos vinculados con la FA. La ablación y restauración del ritmo sinusal generalmente mejoran la función renal(78). Sin embargo, un deterioro de la función renal puede contribuir a la recurrencia de FA. Claramente se necesitan otros estudios para validar esta novedosa observación (figura 6).
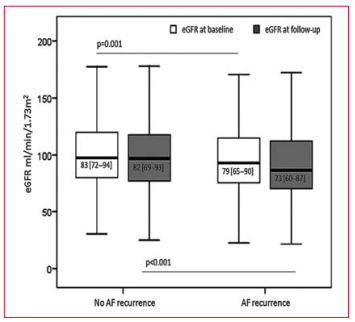
Figura 6
VFG estimado en pacientes con y sin recurrencias a nivel basal y en el seguimiento. FA: fibrilación auricular.
La imagenología periprocedimiento en la ablación por catéter
Un estudio observacional halló una asociación entre la imagenología cardíaca periprocedimiento, tal como ETE, ecocardiografía intracardíaca (ECI), TC cardíaca y RNM, y mejores resultados en pacientes sometidos a ablación de la FA por catéter(79). Encontraron que el uso de TC/MR cardíaca previo al procedimiento se acompañó de un menor riesgo de AIT/accidente cerebrovascular a los seis meses (0,4% vs 0,9%, HR ajustado 0,46). El uso de ECI resultó asociarse con un mayor riesgo de sangrado (1,1% vs 0,7%, HR ajustado 1,76), pero también con una menor incidencia de repetición de la ablación (5,7% vs 8,5%, HR ajustado 0,68). Es interesante destacar que no se halló que ETE afectara los resultados del procedimiento. Otros estudios(80,81) confirmaron la utilidad de la TC cardíaca y RNM para identificar trombos en la AI en pacientes sometidos a ablación, además de su beneficio para evaluar la anatomía cardíaca, el tamaño y ubicación de la vena pulmonar (82-84) y las probabilidades de resultados exitosos (figura 7)(85).
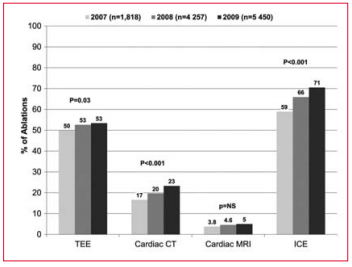
Figura 7
Tendencias temporales de imagenología utilizadas antes de la ablación (CT: tomografía computada; MRI: resonancia magnética nuclear; TEE: ecocardiografía transesofágica) y durante la ablación(79) (ICE: ecocardiografía intracardíaca).
Descargas inapropiadas vinculadas con la fibrilación auricular en pacientes con CDI Se sabe que el monitoreo prolongado del ECG con marcapasos o CRT-D tienen mayores tasas de detección de episodios de alta frecuencia auricular (EAFA)(86,87), especialmente aquellos que monito- rean al paciente en el hogar y que disminuyen el tiempo para detectar EAFA(88). La mayoría, pero no todos estos episodios, reflejan FA paroxísticas a menudo no diagnosticadas (silentes). En un estudio de 1.404 pacientes, se encontró que en un cuarto de los pacientes que recibieron CRT-D se detecta FA de más de 10 minutos de duración(89). En términos generales, tres cuartos de todas las detecciones inapropiadas de arritmia fueron debidas a FA, habiendo 60 pacientes (4% del total) que recibieron descargas inapropiadas debido a FA (2,69 pacientes/100 pacientes-años). La reprogramación de los criterios de descarga podría haber evitado muchas de estas descargas inapropiadas. Otro estudio francés de informe de casos también explica el uso del monitoreo en domicilio para evitar las descargas inapropiadas vinculadas a FA (figura 8)(90).
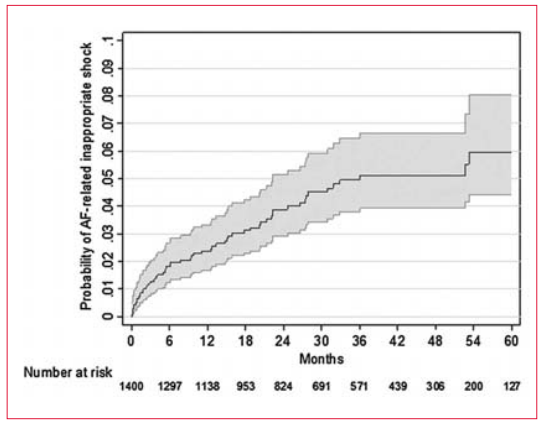
Figura 8
En resumen, la FA sigue siendo uno de los principales temas de la investigación publicada en Heart. Si bien es verdad que hemos aprendido mucho, todavía queda mucho por aprender y estudiar para mejorar los resultados de los pacientes con FA en el futuro.
Agradecimientos
Fondos. La preparación de este artículo fue en parte apoyada por fondos de Charite Berlin (MonDAFIS), BHF (FS/13/32/30324), y la Fundación Leducq.
Bibliografía
1. Holmqvist F, Kim 5, Steinberg BA, et al. Heart rate is associated with progression of atrial fibrillation, independent of rhythm. Heart 2015;101:894-9.
2. Martin RI, Pogoryelova O, Koref MS, et al. Atrial fibrillation associated with ivabradine treatment: meta-analysis of randomised controlled trials. Heart 2014;100:1506-10.
3. Tiwari S, Schirmer H, Jacobsen BK, et al. Association between diastolic dysfunction and future atrial fibrillation in the Tromso Study from 1994 to 2010. Heart 2015;101:1302-8.
4. Buiten MS, de Bie MK, Rotmans II, et al. The dialysis procedure as a trigger for atrial fibrillation: new insights in the development of atrial fibrillation in dialysis patients. Heart 2014;100:685-90.
5. Zimmerman D, Sood MM, Rigatto C, et al. Systematic review and meta-analysis of incidence, prevalence and outcomes of atrial fibrillation in pa- tients on dialysis. Nephrol Dial Transplant 2012;27:3816-22.
6. Atar I, Konas D, Acikel S, et al. Frequency of atrial fibrillation and factors related to its develop- ment in dialysis patients. Intl Cardiol 2006;106: 47-51.
7. Elosua R, Arguer A, Mont L, et al. Sport practice and the risk of lone atrial fibrillation: a case-control study. Intl Cardiol 2006;108:332-7.
8. Mont L, Tamborero D, Elosua R, et al. Physical activity, height, and left atrial size are independent risk factors for lone atrial fibrillation in middle-aged healthy individuals. Europace 2008;10:15-20.
9. Drca N, Wolk A, Jensen-Urstad M, et al. Atrial fibrillation is associated with different levels of physical activity levels at different ages in men. Heart 2014;100:1037-42.
10. Drca N, Wolk A, Jensen-Urstad M, et al. Physical activity is associated with a reduced risk of atrial fibrillation in middle-aged and elderly women. Heart 2015;101:1627-30.
11. Lee SH, Jung IH, Choi SH, et al. Exercise intolerance in patients with atrial fibrillation: clinical and echocardiographic determinants of exercise capacity. J Am Soc Echocardiogr 2005;18:1349-54.
12. Atwood JE, Myers IN, Tang XC, et al. Exercise capacity in atrial fibrillation: a substudy of the Sotalol-Amiodarone Atrial Fibrillation Efficacy Trial (SAFE-T). Am Heart 12007;153:566-72.
13. Azarbal F, Singh M, Finocchiaro G, et al. Exer- cise capacity and paroxysmal atrial fibrillation in patients with hypertrophic cardiomyopathy. Heart 2014;100:624-30.
14. Nyboe C, Olsen MS, Nielsen-Kudsk JE, et al. Atrial fibrillation and stroke in adult patients with atrial septa! defect and the long-term effect of closure. Heart 2015;101:706-11.
15. Milojevic A, Wilkinson P, Armstrong B, et al. Short-term effects of air pollution on a range of cardiovascular events in England and Wales: case-crossover analysis of the MINAP database, hospital ad- missions and mortality. Heart 2014;100:1093-8.
16. Imazio M, Lazaros G, Picardi E, et al. Incidence and prognostic significance of new onset atrial fibrillation/flutter in acute pericarditis. Heart 2015;101: 1463-7.
17. Schnabel RB, Wild PS, Wilde S, et al. Multiple biomarkers and atrial fibrillation in the general population. PLoS ONE 2014;9:e112486.
18. Rosenberg MA, Maziarz M, Tan AY, et al. Circulating fibrosis biomarkers and risk of atrial fibrillation: The Cardiovascular Health Study (CHS). Am Heart J 2014;167:723-8.e2.
19. Hijazi Z, Oldgren J, Siegbahn A, et al. Biomarkers in atrial fibrillation: a clinical review. Eur Heart J 2013;34:1475-80.
20. Howlett PJ, Hatch FS, Alexeenko V, et al. Diagnosing paroxysmal atrial fibrillation: are biomarkers the solution to this elusive arrhythmia? Biomed Res Int 2015;2015:910267.
21. Hijazi Z, Oldgren J, Andersson U, et al. Importance of persistent elevation of cardiac biomarkers in atrial fibrillation: a RE-LY substudy. Heart 2014;100: 1193-200.
22. Roldan V, Marin F, Diaz J, et al. High sensitivity cardiac troponin T and interleukin-6 predict adverse cardiovascular events and mortality in anticoagulated patients with atrial fibrillation. 1 Thromb Haemost 2012;10:1500-7.
23. Smith JG, Newton-Cheh C, Almgren P, et al. Assessment of conventional cardiovascular risk factors and multiple biomarkers for the prediction of incident heart failure and atrial fibrillation. 1 Am Coll Cardiol 2010;56:1712-19.
24. Psychari SN, Chatzopoulos D, Iliodromitis EK, et al. C-reactive protein, interleukin 6, and N-terminal probrain natriuretic peptide following cardioversion of atrial fibrillation: is there a role of biomar- kers in arrhythmia recurrence? Angiology 2011;62:310-16.
25. Hijazi Z, Oldgren J, Andersson U, et al. Cardiac biomarkers are associated with an increased risk of stroke and death in patients with atrial fibrillation: a Randomized Evaluation of Long-term Anticoagula- tion Therapy (RE-LY) substudy. Circulation 2012;125:1605-16.
26. Yoshida K, Kaneshiro T, Ito Y, et al. Elevated plasma norepinephrine level and sick sinus syndrome in patients with lone atrial fibrillation. Heart 2015;101: 1133-8.
27. Alonso A, Misialek JR, Amiin MA, et al. Circula- ting levels of liver enzymes and incidence of atrial fibrillation: the Atherosclerosis Risk in Communities cohort. Heart 2014;100:1511-16.
28. Naschitz JE, Slobodin G, Lewis RJ, et al. Heart diseases affecting the liver and liver diseases affecting the heart. Am Heart 1 2000;140:111-20.
29. Targher G, Bertolini L, Poli F, et al. Nonalcoholic fatty liver disease and risk of future cardiovascular events among type 2 diabetic patients. Diabetes 2005;54:3541-6.
30. Mikolasevic I, Racki 5, Zaputovic L, et al. No-nalcoholic fatty liver disease (NAFLD): a new risk factor for adverse cardiovascular events in dialysis patients. Med Hypotheses 2014;82:205-8.
31. Targher G, Day CP, Bonora E. Risk of cardiovascular disease in patients with nonalcoholic fatty liver disease. N Engl J Med 2010;363:1341-50.
32. Macheret F, Bartz TM, Djousse L, et al. Higher circulating adiponectin levels are associated with increased risk of atrial fibrillation in older adults. Heart 2015;101:1368-74.
33. Martinez C, Katholing A, Wallenhorst C, et al. Increasing incidence of non-valvular atrial fibrillation in the UK from 2001 to 2013. Heart 2015;101:1748-54.
34. Gage BF, Waterman AD, Shannon W, et al. Validation of clinical classification schemes for predicting stroke: results from the National Registry of Atrial Fibrillation. JAMA 2001;285:2864-70.
35. Lip GY, Nieuwlaat R, Pisters R, et al. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest 2010;137:263-72.
36. Mitchell LB, Southern DA, Galbraith D, et al. Prediction of stroke or TIA in patients without atrial fibrillation using CHADS2 and CHA2DS2-VASc scores. Heart 2014;100:1524-30.
37. Poci D, Hartford M, Karlsson T, et al. Role of the CHADS2 score in acute coronary syndromes: risk of subsequent death or stroke in patients with and without atrial fibrillation. Chest 2012;141:1431-40.
38. Henriksson KM, Farahmand B, Johansson S, et al. Survival after stroke-the impact of CHADS2 score and atrial fibrillation. Intl Cardiol 2010;141: 18-23.
39. Chao TF, Liu CJ, Chen ST, et al. CHAIM score and risk of new-onset atrial fibrillation: a nationwide cohort study in Taiwan. Intl Cardiol 2013;168: 1360-3.
40. Hornero F, Martin E, Paredes F, et al. Stroke after coronary artery bypass grafting: preoperative predictive accuracies of CHAIM and CHA2DS2VASc stroke risk stratification schemes. 1 Thorac Cardiovasc Surg 2012;144:1428-35.
41. Makubi A, Hage C, Lwakatare J, et al. Contemporary aetiology, clinical characteristics and prognosis of adults with heart failure observed in a tertiary hospital in Tanzania: the prospective Tanzania Heart Failure (TaHeF) study. Heart 2014;100: 1235-41.
42. Ruo B, Capra AM, Jensvold NG, et al. Racial variation in the prevalence of atrial fibrillation among patients with heart failure: the Epidemiology, Practice, Outcomes, and Costs of Heart Failure (EPOCH) study. J Am Coll Cardiol 2004;43:429-35.
43. Pilgrim T, Englberger L, Rothenbuhler M, et al. Long-term outcome of elderly patients with severe aortic stenosis as a function of treatment modality. Heart 2015;101:30-6.
44. Magne J, Mohty D, Boulogne C, et al. Prognosis importance of low flow in aortic stenosis with preserved LVEF. Heart 2015;101:781-7.
45. Moretti M, Fabris E, Morosin M, et al. Prognostic significance of atrial fibrillation and severity of symptoms of heart failure in patients with low gradient aortic stenosis and preserved left ventricular ejection fraction. Am J Cardiol 2014;114:1722-8.
46. Berti D, Moors E, Moons P, et al. Prevalence and antithrombotic management of atrial fibrillation in hospitalised patients. Heart 2015;101:884-93.
47. Stamboul K, Zeller M, Fauchier L, et al. Prognosis of silent atrial fibrillation after acute myocardial infarction at 1-year follow-up. Heart 2015;101:864-9.
48. Stamboul K, Zeller M, Fauchier L, et al. Incidence and prognostic significance of silent atrial fibrillation in acute myocardial infarction. Int J Cardiol 2014;174:611–17. doi:10.1016/j.ijcard.2014.04.158
49. Sanna T, Diener HC, Passman RS, et al. Cryptogenic stroke and underlying atrial fibrillation. N Engl J Med 2014;370:2478–86. doi:10.1056/NEJMoa1313600
50. Lankveld TA, Zeemering S, Crijns HJ, et al. The ECG as a tool to determine atrial fibrillation complexity. Heart 2014;100:1077–84.
51. Samol A, Masin M, Gellner R, et al. Prevalence of unknown atrial fibrillation in patients with risk factors. Europace 2013;15:657–62. doi:10.1093/europa- ce/eus366
52. McManus DD, Lee J, Maitas O, et al. A novel application for the detection of an irregular pulse using an iPhone 4S in patients with atrial fibrillation. Heart Rhythm 2013;10:315–19. doi:10.1016/j.hrthm.2012.12.001
53. Lee J, Reyes BA, McManus DD, et al. Atrial fibrillation detection using an iPhone 4S. IEEE Trans Biomed Eng 2013;60:203–6. doi:10.1109/TBME.2012.2208112
54. Lau JK, Lowres N, Neubeck L, et al. iPhone ECG application for community screening to detect silent atrial fibrillation: a novel technology to prevent stroke. Int J Cardiol 2013;165:193–4. doi:10.1016/j.ijcard.2013.01.220
55. Keach JW, Bradley SM, Turakhia MP, et al. Early detection of occult atrial fibrillation and stroke prevention. Heart 2015;101:1097–102. doi:10.1136/heartjnl-2015-307588
56. Svennberg E, Engdahl J, Al-Khalili F, et al. Mass screening for untreated atrial fibrillation: the STROKESTOP study. Circulation 2015;131:2176–84. doi:10.1161/CIRCULATIONAHA.114.014343
57. Aronsson M, Svennberg E, Rosenqvist M, et al. Cost-effectiveness of mass screening for untreated atrial fibrillation using intermittent ECG recording. Europace 2015;17:1023–9. doi:10.1093/europace/euv083
58. Bax JJ, Marsan NA, Delgado V. Non-invasive imaging in atrial fibrillation: focus on prognosis and catheter ablation. Heart 2015;101:94–100. doi:10.1136/heartjnl-2013-305150
59. Haeusler KG, Wilson D, Fiebach JB, et al. Brain MRI to personalise atrial fibrillation therapy: current evidence and perspectives. Heart 2014;100:1408–13.
60. Kobayashi A, Iguchi M, Shimizu S, et al. Silent cerebral infarcts and cerebral white matter lesions in patients with nonvalvular atrial fibrillation. J Stroke Cerebrovasc Dis 2012;21:310–17. doi:10.1016/j.jstro-kecerebrovasdis.2010.09.004
61. Cha MJ, Park HE, Lee MH, et al. Prevalence of and risk factors for silent ischemic stroke in patients with atrial fibrillation as determined by brain magnetic resonance imaging. Am J Cardiol 2014;113:655–61. doi:10.1016/j.amjcard.2013.11.011
62. Ovbiagele B, Saver JL, Sanossian N, et al. Predictors of cerebral microbleeds in acute ischemic stroke and TIA patients. Cerebrovasc Dis 2006;22:378–83. doi:10.1159/000094855
63. Cuculich PS, Wang Y, Lindsay BD, et al. Noninvasive characterization of epicardial activation in humans with diverse atrial fibrillation patterns. Circulation 2010;122:1364–72. doi:10.1161/CIRCULATIONAHA.110.945709
64. Guillem MS, Climent AM, Millet J, et al. Noninvasive localization of maximal frequency sites of atrial fibrillation by body surface potential mapping. Cir Arrhythm Electrophysiol 2013;6:294–301. doi:10.1161/CIRCEP.112.000167
65. Dogliotti A, Paolasso E, Giugliano RP. Current and new oral antithrombotics in non-valvular atrial fibrillation: a network meta-analysis of 79 808 pa- tients. Heart 2014;100:396–405. doi:10.1136/heartjnl-2013-304347
66. Caldeira D, Rodrigues FB, Barra M, et al. Non-vitamin K antagonist oral anticoagulants and major bleeding-related fatality in patients with atrial fibrillation and venous thromboembolism: a systematic review and meta-analysis. Heart 2015;101:1204–11. doi:10.1136/heartjnl-2015-307489
67. Camm AJ, Lip GY, De Caterina R, et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the Euro- pean Heart Rhythm Association. Eur Heart J 2012;33: 2719–47. doi:10.1093/eurheartj/ehs253
68. January CT, Wann LS, Alpert JS, et al. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines and the Heart Rhythm Society. Circulation 2014;130:e199–267. doi:10.1161/CIR.0000000000000041
69. De Caterina R, Ammentorp B, Darius H, et al. Frequent and possibly inappropriate use of combination therapy with an oral anticoagulant and antiplatelet agents in patients with atrial fibrillation in Europe. Heart 2014;100:1625–35.
70. Dinh T, Baur LH, Pisters R, et al. Aspirin versus vitamin K antagonist treatment guided by transoe-sophageal echocardiography in patients with atrial fibrillation: a pilot study. Heart 2014;100:563–8. doi:10.1136/heartjnl-2013-305017
71. Vadmann H, Nielsen PB, Hjortshoj SP, et al. Atrial flutter and thromboembolic risk: a systematic review. Heart 2015;101:1446–55. doi:10.1136/heartjnl-2015-307550
72. Phan K, Xie A, La Meir M, et al. Surgical ablation for treatment of atrial fibrillation in cardiac surgery: a cumulative meta-analysis of randomised controlled trials. Heart 2014;100:722–30.
73. Providencia R, Albenque JP, Combes S, et al. Safety and efficacy of dabigatran versus warfarin in patients undergoing catheter ablation of atrial fibrillation: a systematic review and meta-analysis. Heart 2014; 100:324–35.
74. Steinberg BA, Hasselblad V, Atwater BD, et al. Dabigatran for periprocedural anticoagulation following radiofrequency ablation for atrial fibrillation: a meta-analysis of observational studies. J Interv Card Electrophysiol 2013;37:213–21.
75. Bin Abdulhak AA, Khan AR, Tleyjeh IM, et al. Safety and efficacy of interrupted dabigatran for peri-procedural anticoagulation in catheter ablation of atrial fibrillation: a systematic review and meta-analysis. Europace 2013;15:1412–20. doi:10.1093/europace/eut239
76. Kornej J, Hindricks G, Banerjee A, et al. Changes in renal function after catheter ablation of atrial fibrillation are associated with CHADS2 and CHA2DS2-VASc scores and arrhythmia recurrences. Heart 2015;101:126–31.
77. Bohm M, Ezekowitz MD, Connolly SJ, et al. Changes in renal function in patients with atrial fibrillation: an analysis from the RE-LY trial. J Am Coll Cardiol 2015;65:2481–93. doi:10.1016/j.jacc.2015.03.577
78. Takahashi Y, Takahashi A, Kuwahara T, et al. Renal function after catheter ablation of atrial fibrillation. Circulation 2011;124:2380–7. doi:10.1161/CIRCULATIONAHA.111.047266
79. Steinberg BA, Hammill BG, Daubert JP, et al. Periprocedural imaging and outcomes after catheter ablation of atrial fibrillation. Heart 2014;100:1 871–7. doi:10.1136/heartjnl-2014-306067
80. Kapa S, Martinez MW, Williamson EE, et al. ECG-gated dual-source CT for detection of left atrial appendage thrombus in patients undergoing catheter ablation for atrial fibrillation. J Interv Card Electroph- ysiol 2010;29:75–81. doi:10.1007/s10840-010-9505-5
81. Kettering K, Greil GF, Fenchel M, et al. Catheter ablation of atrial fibrillation using the Navx-/Ensite-system and a CT-/MRI-guided approach. Clin Res Cardiol 2009;98:285–96. doi:10.1007/s00392-009-0001-9
82. Ang R, Hunter RJ, Baker V, et al. Pulmonary vein measurements on pre-procedural CT/MR imaging can predict difficult pulmonary vein isolation and phrenic nerve injury during cryoballoon ablation for paroxysmal atrial fibrillation. Int J Cardiol 2015;195:253–8. doi:10.1016/j.ijcard.2015.05.089
83. Shigenaga Y, Kiuchi K, Okajima K, et al. Acquisition of the pulmonary venous and left atrial anatomy with non-contrast-enhanced MRI for catheter ablation of atrial fibrillation: Usefulness of two-dimensional ba- lanced steady-state free precession. J Arrhythm 2015;31:189–95. doi:10.1016/j.joa.2014.11.006
84. Shigenaga Y, Okajima K, Ikeuchi K, et al. Use-fulness of non-contrast-enhanced MRI with two-dimensional balanced steady-state free precession for the acquisition of the pulmonary venous and left atrial anatomy pre catheter ablation of atrial fibrillation: comparison with contrast enhanced CT in clinical cases. J Magn Reson Imaging 2015. doi:10.1002/jmri.24990doi:10.1002/jmri.24990
85. McGann C, Akoum N, Patel A, et al. Atrial fibrillation ablation outcome is predicted by left atrial remodeling on MRI. Circ Arrhythm Electrophysiol 2014;7:23–30. doi:10.1161/CIRCEP.113.000689
86. Hohnloser SH, Capucci A, Fain E, et al. ASymptomatic atrial fibrillation and Stroke Evaluation in pacemaker patients and the atrial fibrillation Reduction atrial pacing Trial (ASSERT). Am Heart J 2006;152:442–7. doi:10.1016/j.ahj.2006.02.016
87. Healey JS, Martin JL, Duncan A, et al. Pacema- ker-detected atrial fibrillation in patients with pacemakers: prevalence, predictors, and current use of oral anticoagulation. Can J Cardiol 2013;29:224–8. doi:10.1016/j.cjca.2012.08.019
88. Lima C, Martinelli M, Peixoto GL, et al. Silent atrial fibrillation in elderly pacemaker users: a ran-domized trial using home monitoring. Ann Noninvasive Electrocardiol 2015. doi:10.1111/anec.12294
89. Ricci RP, Pignalberi C, Landolina M, et al. Ventricular rate monitoring as a tool to predict and prevent atrial fibrillation-related inappropriate shocks in heart failure patients treated with cardiac resynchronisation therapy defibrillators. Heart 2014;100:848–54. doi:10.1136/heartjnl-2013-305259
90. Amara W. [ICD inappropriate shock for atrial fibrillation: use of home-monitoring for the prevention]. Ann Cardiol Angeiol (Paris) 2014;63:389–93. doi:10.1111/anec.12294doi:10.1111/anec.12294