020 Trabajo cientifico
La deriva de glifosato inhibe la fotosíntesis y produce estrés oxidativo en Eucalyptuscamaldulensis
Glyphosate drift inhibes photosynthesis and produces oxidative stress to Eucalyptus camaldulensis
La deriva de glifosato inhibe la fotosíntesis y produce estrés oxidativo en Eucalyptuscamaldulensis
Quebracho - Revista de Ciencias Forestales, vol. 27, núm. 1, pp. 5-12, 2019
Universidad Nacional de Santiago del Estero

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 01 Marzo 2019
Aprobación: 01 Septiembre 2019
Resumen: El desarrollo de plantaciones de Eucalyptus camaldulensis tiene un gran potencial en el noroeste argentino, ya que puede producir madera con características físicas y mecánicas adecuadas para su uso industrial. El manejo de las plantaciones forestales requiere del uso de herbicidas, siendo el glifosato el más frecuente. Este trabajo tuvo como objetivo poner a prueba la hipótesis que la deriva de glifosato inhibe la fotosíntesis, y produce estrés oxidativo en hojas de E. camaldulensis. Se realizaron ensayos en invernáculo, con plantines E. camaldulensis de un año de edad. Se aplicaron dos dosis de herbicida: 3 y 6 L de glifosato ha-1, y un testigo sin tratar. Diez días después de la aplicación del herbicida, se realizaron mediciones de emisión de fluorescencia modulada e intercambio gaseoso, y se cuantificó la concentración de malondialdehído (MDA), y las actividades de las enzimas superóxido dismutasa (SOD), y peroxidadas (POD). Se utilizó un diseño experimental completamente aleatorizado, con 10 repeticiones, y los resultados se analizaron con ANOVA y Test de Fisher. Ambas dosis de glifosato disminuyeron el número de centros de reacción activos, e incrementaron la disipación de energía como calor; la mayor dosis produjo fotoinhibición. Hubo una disminución en la tasa fotosintética; como consecuencia de la inhibición en la etapa fotoquímica, y por cierre estomático. El herbicida produjo peroxidación de lípidos, pese a incremento en las actividades SOD y POD. Se confirmó la hipótesis propuesta.
Palabras clave: eucalipto rojo, fluorescencia modulada, intercambio gaseoso, herbicidas.
Abstract: Developing plantations of Eucalyptus camaldulensis has high potential in north-west Argentina since wood of physical and mechanical features appropriated for industrial use can be obtained. Managing forest plantations demands using herbicides, being glyphosate the most frequently employed. This work aimed to test the hypothesis that glyphosate drift inhibes photosynthesis and produces oxidative stress to E. camaldulensis. Tests were carried out in a greenhouse by applying doses of 3 and 6 L ha-1 of glyphosate on one-year old E. camaldulensis seedlings and a control left untreated. Ten days later, the emissions of modulated fluorescence and gas exchange were measured, and the concentration of malondialdehyde (MDA) besides the activities superoxide dismutase (SOD) and peroxidase (POD) were quantified. A 10- replicate completely randomized experimental design was utilized and the results analyzed using ANOVA and the Fisher’s Test. Both doses of glyphosate lowered the number of centers of reaction active and increased energy dissipation as heat; the highest dose brought about photoinhibition. A decrease of the photosynthetic rate occurred due to the inhibition of the photochemical stage and stomate closure. The herbicide caused lipid peroxidation despite the increase of the SOD and POD activities. The hypothesis was confirmed.
Keywords: red eucalyptus, modulated fluorescence, gas exchange, herbicides.
1. INTRODUCCIÓN
El desarrollo de plantaciones de Eucalyptus camaldulensis Dehnh. (“eucalipto rojo”) tiene un gran potencial en el noroeste argentino, ya que puede producir madera con características físicas y mecánicas adecuadas para su uso industrial. Esta especie posee una gran plasticidad, y es muy tolerante al estrés hídrico (Moglia et al., 2008).
El control de malezas es una de las prácticas silvícolas más importantes en viveros y plantaciones forestales. Se realiza mediante métodos mecánicos, químicos, o la combinación de ambos. El uso de herbicidas es una práctica común, siendo el glifosato el herbicida más utilizado en viveros y plantaciones de Eucalyptus (Tuffi Santos et al, 2009). Sin embargo el uso de glifosato a lo largo del ciclo de desarrollo del Eucalyptus puede ser perjudicial para el propio cultivo, debido a las derivas accidentales que se producen durante las aplicaciones manuales o mecanizadas (Velini et al., 2010; Costa et al., 2012).
El glifosato actúa inhibiendo la enzima 5-enolpiruvil-shikimato-3-fosfato sintasa (EPSPS), responsable de la síntesis del corismato, un intermediario en la ruta del ácido shikímico, que conduce a la síntesis de aminoácidos aromáticos (Alcántara de la Cruz et al., 2016). Pese a que se conoce el mecanismo de acción del glifosato; existen pocas referencias sobre el impacto de este herbicida en la fisiología de especies forestales.
Los herbicidas pueden disminuir la tasa fotosintética, y por ende la síntesis de carbohidratos (Powles y Yu, 2010;). El análisis de la fluorescencia de la clorofila a, constituye un método sensible y no destructivo para la evaluación de los cambios producidos en la etapa fotoquímica de la fotosíntesis. Recientemente ha sido utilizado para evaluar el grado de daño del aparato fotosintético, bajo diferentes condiciones de estreses ambientales, tales como temperaturas extremas (Zushi et al., 2012), sequía (Gomes et al., 2012), salinidad (Meloni et. al., 2017) y herbicidas (Sousa et al., 2014).
Bajo condiciones de estrés, la energía absorbida por los pigmentos fotosintéticos, que no es utilizada para producir ATP y NADPH, suele conducir a la formación de especies reactivas de oxígeno, EROs (Sousa et al., 2014). Las EROs pueden producir peroxidación de lípidos, alteraciones en las membranas celulares, y degradación de proteínas y clorofilas (Paiva et al., 2019).
Las células vegetales están protegidas de las EROs por un sistema antioxidante, que incluye componentes enzimáticos y no enzimáticos (Meloni et al., 2010). Las especies vegetales más tolerantes a estreses abióticos poseen una mayor concentración de antioxidantes, y enzimas involucradas en las rutas metabólicas de detoxificación de especies reactivas de oxígeno (Naliwajski y Skłodowska, 2014).
Este trabajo tuvo como objetivo poner a prueba la hipótesis que la deriva de glifosato inhibe la fotosíntesis, y produce estrés oxidativo en hojas de E. camaldulensis.
2. MATERIALES Y MÉTODOS
Material vegetal: se realizaron ensayos con plantines Eucalyptus camaldulensis de un año de edad, crecidos en macetas plásticas, conteniendo suelo franco, y fertilizadas con N-P-K (20:5:20). Las macetas se dispusieron en invernáculo, recibiendo irrigación manual diaria, para asegurar adecuada disponibilidad de agua.
Se aplicaron dos dosis de herbicida: 3 y 6 L de glifosato ha-1 (Roundup®, sal isopropanilamina al 48 % p/v) utilizando un pulverizador manual, y un testigo sin tratar. Durante la aplicación del herbicida, la temperatura fue de 18 °C, y la humedad relativa del 45 %. Diez días después de la aplicación del herbicida, se realizaron mediciones de emisión de fluorescencia modulada e intercambio gaseoso y se tomaron muestras para la realización de determinaciones químicas.
Fotosíntesis: la emisión de fluorescencia modulada se midió mediante el uso de un fluorómetro portátil (Walz GmbH Eichenring, 691090 Effeltrich, Germany). Los valores de las variables quenching fotoquímico (qP), quenching no fotoquímico (NPQ), y relación fluorescencia variable/fluorescencia máxima (Fv/Fm), se calcularon de acuerdo a Maxwell y Johnson (2000).
Las mediciones de intercambio gaseoso y asimilación neta de CO2, se realizaron en las mismas hojas en las que se midieron las variables de fluorescencia. Para ello se utilizó una analizador de gases infrarrojo en un sistema abierto (IRGA-LCpro+ System ADC, BioScientific Ltd.), con cámara para hojas de Arabidopsis, en condiciones de luz artificial saturante (1000 μmol m-2 s-1) y concentración de CO2 ambiental. Se midieron las siguientes variables: fotosíntesis neta (A), transpiración (E), conductancia estomática (gs), y concentración intercelular de CO2 (Ci). A partir de estas variables se calculó la eficiencia de la carboxilación (A/Ci) y eficiencia en el uso del agua (A/E). Se realizaron 10 mediciones en cada hoja.
Determinaciones químicas: se cuantificó el impacto de la aplicación de glifosato sobre el estrés oxidativo, mediante la determinación de la concentración de malondialdehído (Hendry et al., 1993). Se determinaron las actividades de las enzimas superóxido dismutasa (SOD) y peroxidasas, a través de los métodos descriptos por Giannopolitis y Ries (1977) y Maehly y Chance (1954), respectivamente.
Análisis estadístico y diseño experimental: se utilizó un diseño experimental completamente aleatorizado, con 10 repeticiones, y los resultados se analizaron con ANOVA y Test de Fisher (Fisher p<0,05).
3. RESULTADOS Y DISCUSIÓN
El glifosato produjo una disminución en el quenching fotoquímico, y un aumento en quenching no fotoquímico, respectivamente (Figura 1 A, B). La respuesta al glifosato fue más acentuada en el quenching no fotoquímico que en el quenching fotoquímico, coincidiendo con lo observado en otras especies sometidas a estreses ambientales. Frankart et al. (2003) sugieren que el quenching no fotoquímico es el marcador biológico más apropiado para detectar daños por herbicidas tanto a campo como en laboratorio. Estos resultados indican que el glifosato disminuyó la proporción de centros de reacción activos en el fotosistema II, e incrementó la pérdida de energía absorbida a través de su disipación como calor.
Mientras 3 L ha-1 de glifosato no afectaron la relación Fv/Fm, 6 L ha-1 produjeron una disminución significativa en dicha relación (Figura 1C). Este resultado indica que altas dosis de glifosato producen fotoinhibición, o sea daños en las proteínas D1 y D2 del fotosistema II (Tounekti et al., 2018).
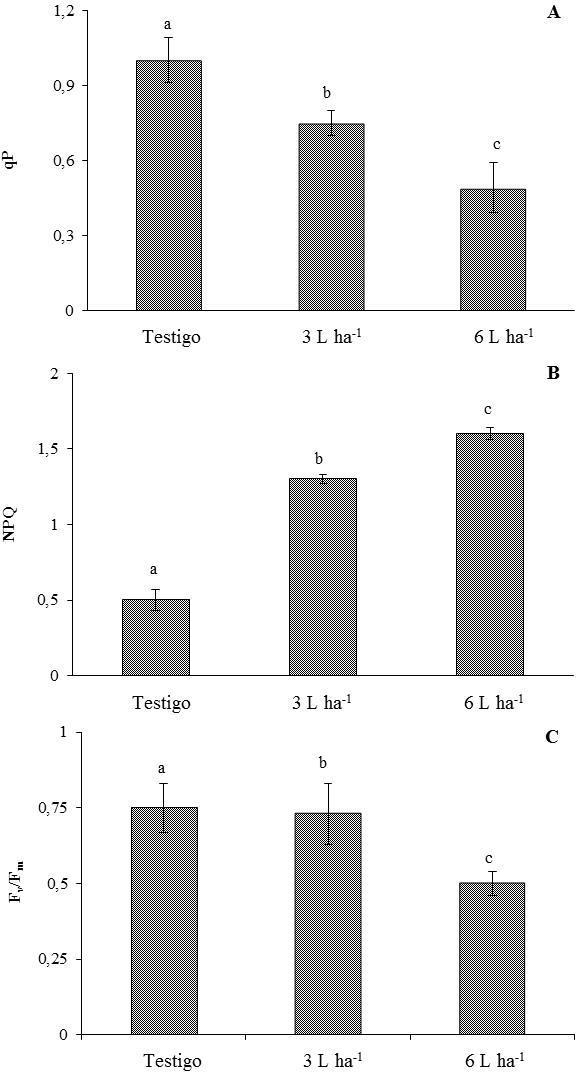
Figura 1.
Variables de fluorescencia modulada en hojas de E. camaldulensis tratadas agua destilada (testigo), o dosis de 3 y 6 L ha-1 de glifosato. qP: quenching fotoquímico (A), NPQ: quenching no fotoquímico (B), Fv/Fm: relación fluorescencia variable, fluorescencia máxima (C). Letras diferentes indican diferencias significativas por el Test de Fisher (p < 0,05).
La relación Fv/Fm solo manifiesta alteraciones en casos de estrés severo, y su disminución en los de plantines de E. camaldulensis coincidió con la aparición de necrosis pronunciada en la mayoría de las hojas. El estrés generado por el glifosato en E. camaldulensis fue más severo que el producido por Bentazona en soja, donde no se detectaron cambios en la relación Fv/Fm pese a que se registró una inhibición en la etapa fotoquímica de la fotosíntesis (Sousa et al., 2014).
Ambas dosis de glifosato produjeron una disminución significativa en la fotosíntesis neta, siendo el efecto más notorio en el tratamiento de 6 L de glifosato ha-1 (Tabla 1). Esta tendencia coincidió con una disminución en la conductancia estomática, la tasa transpiratoria, y la eficiencia en el uso del agua (A/E). Pese a ello, la dosis de 3 L de glifosato ha-1, no afectó la concentración intercelular de CO2, lo que indica que en dicha dosis la fotosíntesis no estuvo limitada por el CO2. Concordando con este resultado se observó una disminución en la eficiencia de la carboxilación en todos los tratamientos con herbicidas.

1 Para cada variable, letras diferentes indican diferencias significativas por el test de Fisher al 5%.
Machado et al. (2010) obtuvieron resultados similares, estudiando el efecto de la aplicación de glifosato sobre variables de intercambio gaseoso, en clones de Eucalyptus grandis. Estos autores determinaron que el glifosato no inhibió la fotosíntesis de E. grandis, luego de 7 días de aplicación. Sin embargo, al cabo de 21 días de aplicación del herbicida, todas las dosis ensayadas inhibieron la fotosíntesis neta, como consecuencia de una disminución en la conductancia estomática.
Los resultados obtenidos sugieren que la inhibición de la fotosíntesis a 3 L de glifosato ha-1 se debió a una inhibición en la etapa fotoquímica, como demuestran las variables de fluorescencia de la clorofila. En la dosis de 6 g de glifosato ha-1, la fotosíntesis fue inhibida tanto en la etapa fotoquímica, como en a nivel estomático con una concomitante disminución en la concentración interna de CO2.
Radwan y Fayez (2016) obtuvieron resultados similares en plantas de en Arachis hypogaea tratadas con 360 y 720 g de glifosato ha-1, y atribuyeron la disminución en la tasa fotosintética a una menor disponibilidad de ATP y NADPH, provenientes de la etapa fotoquímica. Yanniccari et al. (2012) reportaron que en Lolium perenne, el glifosato produjo como primera respuesta cierre estomático, y luego alteraciones en las variables de emisión de fluorescencia.
Los resultados obtenidos difieren con los observados en Phaseolus vulgaris. En dicha especie el glifosato produjo una inhibición de la fotosíntesis, como consecuencia del cierre estomático, mientras que la etapa fotoquímica no fue alterada (Olesen y Cedergreen, 2010). Dichos autores cuestionan el uso de variables de fluorescencia como marcador de estrés por herbicidas, y sugieren utilizar variables de intercambio gaseoso.
Ambas dosis de glifosato ocasionaron incrementos en la concentración de malondialdehído, producto de la peroxidación de lípidos (Figura 2A). Esto indica que el glifosato produjo un importante estrés oxidativo en hojas. Ahsan et al, (2008) observaron una respuesta similar en hojas de Oryza sativa tratadas con glifosato, con una importante producción de H2O2, resultando en peroxidación de lípidos.
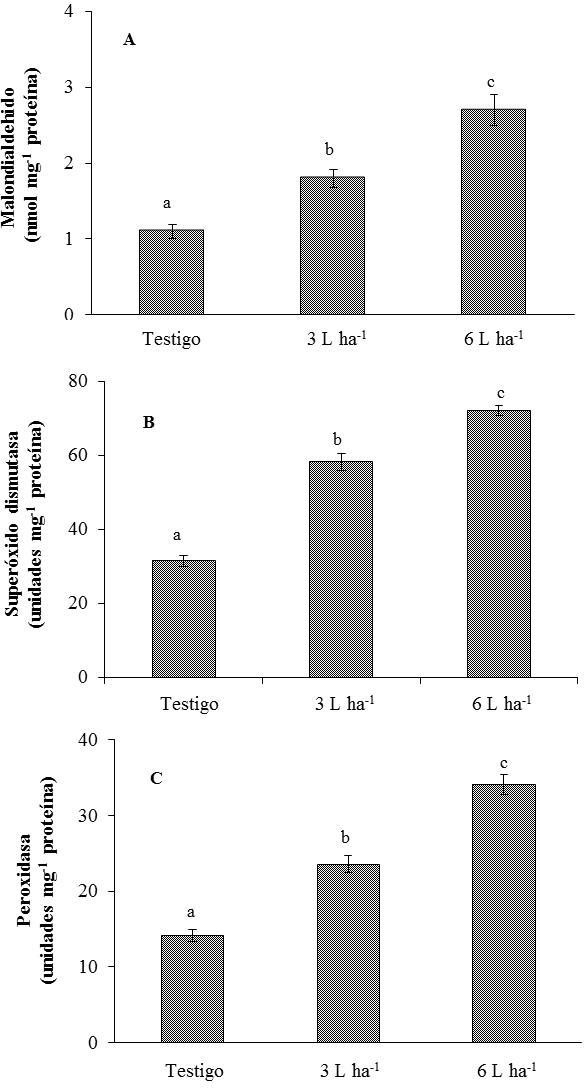
Figura 2.
Concentración malondialdehído (A), y actividades superóxido dismutasa (B), y peroxidasa (C), en hojas de E. camaldulensis tratadas agua destilada (testigo), o dosis de 3 y 6 L ha-1 de glifosato. Letras diferentes indican diferencias significativas por el Test de Fisher (p < 0,05).
Radwan y Fayez (2016) también observaron acumulación de malondialdehído, e incremento en las actividades de SOD y POD en hojas de Arachis hypogaea tratadas con glifosato. Song et al. (2007) reportaron un incremento de la actividad POD en plantas de trigo tratadas clorotoluron, y propusieron su uso como marcador en plantas sometidas a contaminantes.
4. CONCLUSIONES
La deriva de glifosato inhibe la fotosíntesis en E. camaldulensis, a nivel de la etapa fotoquímica, y por cierre estomático. También produce estrés oxidativo, pese a que incrementa la actividad de las enzimas antioxidantes SOD y POD.
5. REFERENCIAS BIBLIOGRÁFICAS
Ahsan, N.; D. G. Lee.; K. W. Lee; I. Alam; S. H. Lee; J. D. Bahk y B. H. Lee. 2008. Glyphosate-induced oxidative stress in rice leaves revealed by proteomic approach. Plant Physiology and Biochemistry 46: 1062-1070.
Alcántara de la Cruz, R.; F. Barro y J. A. Domínguez Valenzuela. 2016. Physiological, morphological and biochemical studies of glyphosate tolerance in Mexican Cologania (Cologania broussonetii (Balb.) DC.). Plant Physiology and Biochemistry 98: 72-80.
Costa, P. R.; A. C. Costa; N. Vilanova; R. M. R. Pereira y D. Martins. 2012. Efeito da deriva simulada de glyphosate em diferentes partes da planta de Eucalyptus grandis. Ciências Agrarias 33: 1663-1672.
Frankart, C; P. Eullaffroy y G. Vernet.2003. Comparative effects of four herbicides on non-photochemical fluorescence quenching in Lemna minor. Environmental and Experimental Botany 49:159-168
Giannopolitis, N. y S. K. Ries. 1977. Superoxide dismutase. I. Occurrence in higher plants. Plant Physiology 59: 309-314.
Gomes, M. T.G.; A. C. Luz; M. R. Dos Santos; M. C. P. Batitucci; D. M. Silva y A. R. Falqueto. 2012. Drought tolerance of passion fruit plants assessed by the OJIP cholophyll a fluorescence transient. Scientia Horticulturae 142: 49-56.
Hendry, G. A. F.; P. C. Thorpe y M. N. Merzlyak. 1993. Stress indicators- lipid peroxidation. In: G.A.F. Hendry, J.P. Grime (Eds.), Methods in Comparative Plant Ecology, Chapman and Hall, London, pp. 154-156.
Maehly, P. C. y M. Chance. 1954. The assay of catalase and peroxidases. In: Gluck, D. (ed.) Methods of Biochemical Analysis pp. 357-424. Interscience Publishers, New York.
Machado, A. F. L.; L. R. Ferreira; L. D. T. Santos; F. A. Ferreira; R. G. Viana; M. S. Machado y F. C. L. Freitas 2010. Eficiência fotossintética e uso da água em plantas de eucalipto pulverizadas com glyfosate. Planta Daninha 28: 319-327.
Maxwell, K. y G. N. Johnson. 2000. Chlorophyll fluorescence practical guide. Journal of Experimental Botany 51: 659-668.
Meloni, D. A.; L. Fornés.; M. R. Gulotta y D. Moura Silva. 2010. Tolerancia de Cedrela lilloi a bajas temperaturas: cambios metabólicos. Revista de Ciencias Forestales Quebracho 18: 16- 23.
Meloni, D. A. 2017. Fisiologia Vegetal: Respuestas de especies leñosas al estrés salino. Editorial Universidad Nacional de Santiago del Estero.
Meloni, D. A.; D. M. Silva; R. Ledesma y G. I. Bolzón. 2017. Nutrición mineral y fotosíntesis en plántulas de algarrobo blanco, Prosopis alba (Fabaceae) bajo estrés salino. UNED Research Journal 9: 297-304.
Moglia, J. G.; S. Bravo y R. Gerez. 2008. Anatomía comparada del leño de Eucalyptus camaldulensis (Myrtaceae) de dos orígenes, ensayados en Santiago del Estero. Boletín de la Sociedad Argentina de Botánica 43: 239-246.
Naliwajski, M. R. y M. Skłodowska. 2014. The oxidative stress and antioxidant systems in cucumber cells during acclimation to salinity. Biologia Plantarum 58: 47-54.
Olesen, C. F. y N. Cedergreen 2010. Glyphosate uncoples gas exchange and chlorophyll fluorescence. Pest Management Science 66: 536-542.
Paiva, A. L.; G. Passaia; A. K. M. Lobos; D. J. Messeder; J. A. G. Silveira y M. M. Pinheiro. 2019. Mitochondrial glutathione peroxidase (OsGPX3) has a crucial role in rice protection against salt stress. Environmental and Experimental Botany 158: 12-21.
Powles, S. B. y Q. Yu. 2010. Evolution in action: plants resistant to herbicides. Annual Review of Plant Biology 61: 317-347.
Radwan, D. E. M. y K. A. Fayez 2016. Photosynthesis, antioxidant status and gas-exchange are altered by glyphosate application in peanut leaves. Photosynthetica 54: 307-316.
Song, N. H.; X. LeYin; G.F. Chen y H. Yang. 2007. Biological responses of wheat (Triticum aestivum) plants to herbicide chlorotoluron in soils. Chemosphere 68, 1779-1787.
Sousa, C. P.; M. E. Farías; A. A. Shock y M. A. Bacarin.2014. Photosynthesis of soybean under the action of a photosystem II-inhibiting herbicide. Acta Physiologiae Plantarum 36: 3051-3062.
Tounekti, T; M. Mahdhi.; T. A. Al-Turki y H. Khemira. 2018. Water relations and photo-protection mechanisms during drought stress in four coffee (Coffea arabica) cultivars from southwestern Saudi Arabia. South African Journal of Botany 117: 17-25.
Tuffi Santos, L. D.; B. F. Santanna-Santos; R. M. S. A Meira; F. A. Ferreira, R. A. S. Tiburcio y A. F. L. Machado. 2009. Leaf anatomy and morphometry in three eucalyt clones treated with glyphosate”. Brazilian Journal of Biology 69: 129-136.
Velini, E. D.; L. B. Trindade; L. R. M. Barberis y F. Duke 2010 Growth regulation and other secondary effects of herbicides. Weed Science 58: 351-354.
Yanniccari, M.; E. Tambussi; C. Istilart y A.M. Castro. 2012. Glyphosate effects on gas exchange and chlorophyll fluorescence responses of two Lolium perenne L. biotypes with differential herbicide sensitivity. Plant Physiology and Biochemistry 57: 210-217.
Zushi, K.; S. Kajiwara y M. Naotaka. 2012. Chlorophyll a fluorescence OJIP transient as a tool to characterize and evaluate response to heat and chilling stress in tomato leaf and fruit”. Scientia Horticulturae 148: 39-46.
Notas de autor
dmeloniunse@gmail.com