Análisis de producción gonadal del pez Grundulus quitoensis Román-Valencia, Ruiz-C. y Barriga, 2005 (Characiformes: Characidae) en la laguna altoandina “El Voladero”, provincia El Carchi, Ecuador
Analysis of gonad production of Grundulus quitoensis Román-Valencia, Ruiz-C. & Barriga, 2005 (Characiformes: Characidae) in the “El Voladero” high Andean lake, Carchi province, Ecuador
Análisis de producción gonadal del pez Grundulus quitoensis Román-Valencia, Ruiz-C. y Barriga, 2005 (Characiformes: Characidae) en la laguna altoandina “El Voladero”, provincia El Carchi, Ecuador
Biota Colombiana, vol. 17, núm. 2, pp. 89-97, 2016
Instituto de Investigación de Recursos Biológicos "Alexander von Humboldt"
Recepción: 16 Agosto 2016
Publicación: 07 Octubre 2016
Resumen: La fecundidad relativa en peces es la estimación de la cantidad de ovocitos de una hembra por desove. Este aspecto se investigó en especímenes topotipos de Grundulus quitoensis de la laguna altoandina El Voladero, Ecuador. Se identificó el estadio de madurez gonadal (maduro e inmaduro) a través de la observación directa, se calculó la fecundidad relativa al peso (FRP) y a la longitud total (LT). Las hembras estudiadas tuvieron en promedio una LT de 63,9 mm. El rango de ovocitos varió entre 75 y 716 por hembra y en total se contaron 5691 ovocitos para 16 hembras. El peso total (PT) varió entre 0,5 g y 4,7 g; mientras que la LT varió entre 36,7 mm a 63,9 mm. La fecundidad relativa se observó comprendida entre 1,6 y 14,3 ovocitos por mm de LT del animal (X- = 6,9 ± 3,6 mm-1) y entre 47,2 y 319,1 ovocitos por g de peso total (X- = 148,9 ± 74,9 g-1). Es importante conocer el ciclo de vida e historia natural de una especie, porque contribuyen al conocimiento ecológico de los peces que habitan las lagunas altoandinas, como es el caso del estudio aquí desarrollado en G. quitoensis.
Palabras clave: Fecundidad relativa, Ovocitos, Pez neotropical, Peso total.
Abstract: Relative fecundity in fishes is the estimated number of oocytes of a female during spawning. This aspect was investigated in Grundulus quitoensis topotypic specimens from the “El Voladero”, a high Andean lake in Ecuador. Gonad maturation stages (mature and immature) were identified by means of direct observation, subsequently, the relative fertility (FRP) as function of the weight and the total length (TL) were calculated. Average TL of females was 63.9 mm. The numbers of oocytes ranged from 75 to 716 per female, in total 5691 oocytes were counted from 16 females. Total weight (TW) ranged from 0.5 to 4.7 g, whereas TL ranged from 36.7 to 63.9 mm. Relative fecundity ranged from 1.6 to 14.3 oocytes per mm TL (X- = 6.9 ± 3.6 mm-1) and from 47.2 to 319.1 oocytes per g of TW (X- = 148.9 ± 74.9 g-1). lt is important to know the life cycle and natural history of a species, since they contribute to the ecological knowledge of the fishes that inhabit the high Andean lakes, as is the case of this study of G. quitoensis.
Keywords: Neotropical fish, Oocytes, Relative fecundity, Total weight.
Introducción
La fecundidad en peces es la estimación de la cantidad de ovocitos que una hembra podría expulsar en un desove, constituyéndose en uno de los indicadores más utilizados para evaluar el potencial reproductivo de una especie, además de ser de interés en la producción piscícola (Villamil y Arias 2011).
Huaquín et al. (2002) mencionaron que el conocimiento de la estructura ovárica permite analizar la capacidad desovante, su duración, su temporalidad y la forma en que se realiza. Por su parte Claramunt et al. (2009) señalaron que los estudios reproductivos en peces, tales como la determinación de la talla de madurez inicial, la duración de la estación de desove y la fecundidad, requieren el conocimiento del estado de desarrollo gonadal de cada individuo, el cual debe ser siempre considerado como parte del estudio de la biología reproductiva de un pez. Los métodos utilizados para el estudio reproductivo de peces varían desde el histológico, como el más detallado pero a su vez el que más tarda en dar resultados, hasta la inspección visual macroscópica, dentro del cual, se encuentran la medición del tamaño ovocitario y la forma y estructura de los ovocitos, además del tipo y disposición del vitelo y el índice gonádico (utilizado para determinar la fase de madurez de los órganos reproductores) (West 1990).
En Ecuador, la historia natural y biología de Grundulus quitoensis (Figura 1) han sido poco estudiadas debido a que esta especie permaneció desconocida durante mucho tiempo para la ciencia (Román-Valencia et al. 2005). Sobre Grundulus hay disponibles estudios morfológicos, taxonómicos y filogenéticos (Barriga et al. 2005, Román-Valencia et al. 2005, Román- Valencia et al. 2010), sin embargo, ninguno de estos estudios ha investigado aspectos ecológicos. Para Grundulus se han descrito tres especies: G. bogotensis (Humboldt 1821), cuyas poblaciones están distribuidas en el altiplano cundiboyacense de la región transandina colombiana; G. cochae Román- Valencia, Paepke y Pantoja, 2003, registrada en la laguna La Cocha, ubicada en la región cisandina colombiana, y G. quitoensis Román-Valencia, Ruiz-C. y Barriga, 2005, conocida para la laguna El Voladero, dentro de la Reserva Ecológica El Ángel en Ecuador. Las observaciones en campo hacen asumir que estas especies pueden estar organizadas en metapoblaciones que presentan tamaños poblacionales pequeños y una alta especificidad en su hábitat. La población de G. quitoensis, que se identificó inicialmente como G. cf. bogotensis (Barriga y Terneus 2005), para la laguna el Voladero, parece estar asociada a la vegetación acuática de Scirpus californicus y Utricularia sp., a pesar de que dicha asociación es muy rara en las lagunas del Ecuador.
Dada la ausencia de literatura publicada sobre la biología reproductiva de G. quitoensis, el presente trabajo estudió la fecundidad relativa, a través del análisis de madurez de los ovarios de hembras colectadas en su medio natural, para inferir el potencial de subsistencia de esta especie, que en la actualidad está altamente amenazada por un depredador potencial, la trucha (Onchorhynchus), pez introducido en Ecuador.
Material y métodos
Área de estudio
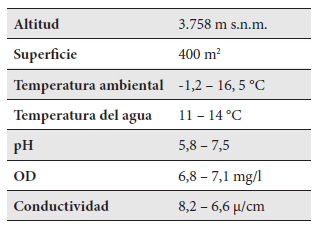
La Reserva Ecológica El Ángel (REEA) se ubica en la provincia del Carchi, en los cantones Espejo, Tulcán y Mira. La superficie actual de la REEA es de 16541 ha y se encuentra entre los 3400 y 4200 m s.n.m. Esta reserva alberga un sin número de lagunas, entre ellas la laguna El Voladero (LEV) (Figura 2), situada geográficamente entre las coordenadas 0º41’22.60”N y 77º52’58.09”O (WGS84), y cuyas características abióticas se presentan en la tabla 1.
El entorno paisajístico donde habita G. quitoensis es abundante en vegetación acuática emergente de totora (Scirpus californicus) y en la zona litoral, donde se capturaron los especímenes estudiados, se identificaron ejemplares de Utricularia sp., una planta acuática sumergida que solo ha sido registrada para la laguna El Voladero (Terneus 2002) y que podría estar asociada al ciclo de vida de esta especie.

Figura 1.
Grundulus quitoensis, topotipo, hembra, 6,5 cm LT, MECN-DP 3052. Ejemplar preservado. © MECN-INB/ Jonathan Valdiviezo R.
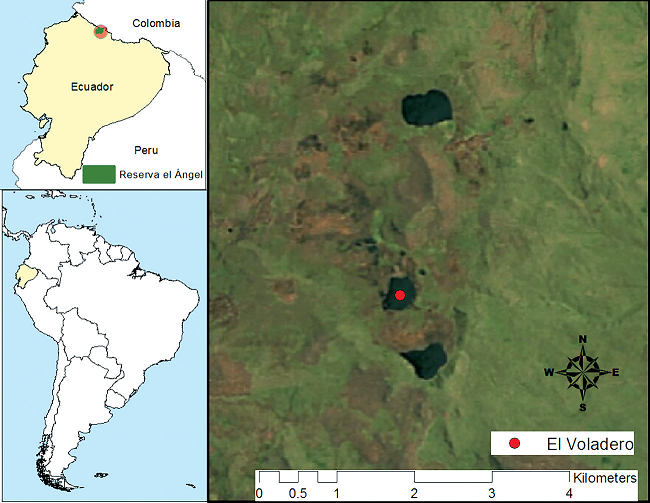
Figura 2.
Ubicación geográfica de la laguna El Voladero en Ecuador. © Gianina Brichetto.
Estaciones de muestreo
Las estaciones se seleccionaron in situ, muestreándose la mayor variabilidad de microambientes potenciales para la especie. Se muestrearon tres estaciones, distribuidas al sur de la laguna, en su zona litoral donde las aguas bajas usualmente forman durante todo el año áreas pantanosas y acumulación de materia orgánica rica en nutrientes (Figura 3).
En cada estación, se tomaron la altitud y las coordenadas geográficas por medio de un GPS (Garmin). Los peces se recolectaron a través de diferentes artes de pesca: redes de arrastre, nasas, redes de mano y atarraya. Los ejemplares capturados se fijaron en una solución de formaldehído al 10 %, se preservaron en etanol al 70 % y luego se depositaron en la Colección de Peces del Museo Ecuatoriano de Ciencias Naturales del Instituto Nacional de Biodiversidad (MECN-INB) en Quito, Ecuador.

Figura 3.
Zona litoral de aguas pantanosas, ambiente natural de Grundulus quitoensis. © UIDE/Esteban Terneus.
Mediciones
En el laboratorio, se registró el peso total de cada uno de los especímenes con la ayuda de una balanza digital (PT, g) y las longitudes estándar (LE, mm) y total (LT, mm) con un calibrador digital. Además, se determinó el sexo y se clasificaron los estadios de maduración de las gónadas macroscópicamente en tres estadios, según la escala de maduración sexual propuesta por Núñez y Duponchelle (2009): 1-inmadura (Figura 4A), 2-en maduración (Figura 4B) y 3-madura (Figura 4C). Todas las medidas y estadios fueron tomadas con base en especímenes en líquido conservante.
Posteriormente se extrajeron los ovarios de los individuos preservados, los cuales se cambiaron a una solución de alcohol al 75 % en tubos Eppendorf. Para eliminar el exceso de agua del tejido gonádico, los ovarios se desecaron encima de cartones durante 50 minutos.
Cada muestra de tejido gonadal deshidratado se dividió en tres submuestras para determinar la fecundidad parcial. Se siguió el procedimiento de Hunter y Leong (1985) que usa tres submuestras provenientes de la región anterior, media y posterior. Luego, se efectuó el conteo de ovocitos, a través del uso de microscopios ópticos y estereoscopios. Los conteos de ovocitos se hicieron por medio de un contador manual de la siguiente manera: se utilizaron 12 cajas de Petri, cada una señalada con una cuadrícula en su parte externa, y se usó un fondo oscuro en la base del microscopio y estereoscopio.
Análisis estadísticos
Se efectuó un análisis de regresión para estimar la relación entre la fecundidad parcial y la longitud total de cada individuo. La fecundidad relativa al peso (FRP) se calculó a partir de la fórmula FRP = F / P (g) expresada como ovocitos por gramos de peso corporal (Chaves y Vazzoler 1984, Araya et al. 2003), donde F es fecundidad y P el peso. La FRP se acompañó de su media (X- ) y su respectiva desviación estándar (DE). Valor de significancia usado fue a = 0,05.

Figura 4.
Fotografías de los ovocitos de Grundulus quitoensis en cada uno de los estadios. A) inmadura, B) en maduración, C) madura.
Resultados
En un total de 25 individuos eviscerados, se identificaron tres machos y 22 hembras de las cuales 16 presentaron características informativas para estimar su fecundidad (ovocitos hidratados y sin folículos postovulatorios), encontrando frecuencias de gónadas maduras (estadio 3) en un 40,91 %; gónadas en maduración (estadio 2) en 31,82 % y gónadas inmaduras (estadio 1) 27,27 % (Tabla 2). Las hembras estudiadas presentaron una LT que varió entre 36,9 y 63,9 mm y un PT entre 0,5 y 4,7 g. El conteo de ovocitos varió entre 75 a 716 ovocitos/ hembra con un promedio de 356, para un total de 5691 ovocitos/16 hembras. La fecundidad relativa se obtuvo entre 1,6 y 14,3 ovocitos por mm LT (X = 6,9 ± 3,6 mm-1 ovocitos de desviación estándar) y entre 47,2 y 319,1 ovocitos por g PT (X = 148 +- 74,9 g-1 ovocitos de desviación estándar).
La regresión lineal calculada entre el número de ovocitos en función del peso total reveló que el número de ovocitos aumenta, aunque no en relación completamente lineal, con el tamaño del pez.
El coeficiente de determinación R2 (0,251) muestra una relación parcial entre el número de ovocitos y el peso de los animales, lo que permite pronosticar en un 25 % que el peso de los animales determina el número de ovocitos producidos; además, el parámetro p (0,04808) de esta relación fue estadísticamente significativa (Figura 5).
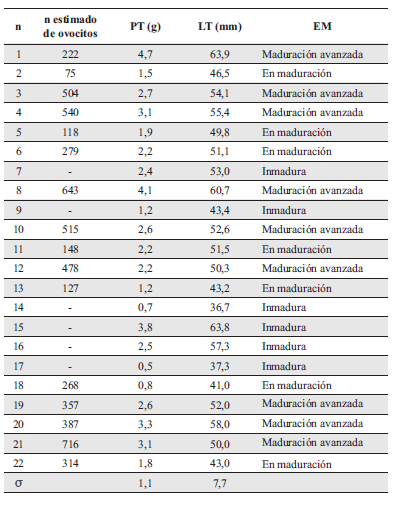
Número total de ovocitos estimados para 22 hembras analizadas de Grundulus quitoensis en la localidad de la laguna El Voladero. Se presentan el peso total (PT), longitud total (LT) y estado de maduración (EM) de cada individuo.
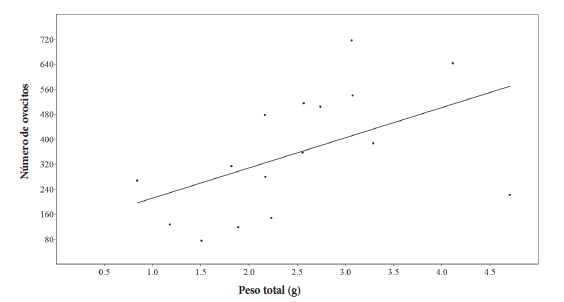
Figura 5.
Regresión lineal entre el número de ovocitos en función del peso total (R2 =0,251; p= 0,04808; y = 96,602x + 114,72) para Grundulus quitoensis en la laguna El Voladero.
Discusión
El promedio de la fecundidad encontrada en G. quitoensis se ajusta al valor más bajo del intervalo reportado para una de las restantes dos especies del género, Grundulus bogotensis (Álvarez-León et al. 2002: F = 293-3458), pero contrasta con un número más bajo de lo reportado para Bryconamericus caucanus y Hemibrycon boquiae, con un promedio de 1965 ovocitos (53-6506) y 376 ovocitos (54-1165) por hembra en estado de predesove, respectivamente (Román-Valencia et al. 2008) y con lo descrito para Bryconamericus iheringii (370-1600 ovocitos) (Lampert et al. 2004) y Bryconamericus stramineus (98 a 1100 ovocitos) (Lampert et al. 2007). El reporte de Román-Valencia et al. (2008) registran un número mayor de machos que hembras en los ejemplares sexados de B. caucanus y H. boquiae, estos resultados no coinciden con la presente investigación, donde el número de hembras fue mayor.
Se ha encontrado una relación directa entre el tamaño de la hembra y el número de ovocitos que esta puede madurar, además en algunas especies de peces es muy común que las hembras pequeñas presenten fecundidades bajas (Nakatani et al. 2001), lo cual coincidió en este caso, con la baja fecundidad relativa encontrada respecto al peso de las hembras tomado.
La relación hallada entre los ovocitos y el peso en G. quitoensis sugiere que especímenes más grandes producen mayor cantidad de ovocitos, aunque sus proporciones no son muy elevadas, lo que concuerda con lo propuesto por Vazzoler (1996), quien indicó que la fecundidad se incrementa con el aumento de la talla y la edad; además coincide con lo reportado por Ferriz et al. (2007) para Pseudocorynopoma doriai donde su modelo de regresión lineal reveló una relación positiva y significativa.
En otras especies de Characiformes, también se ha establecido la existencia de una relación positiva entre la fecundidad y el peso, como por ejemplo en la sardina Cheirodon interruptus (Ferriz et al. 2011) y en los sábalos Prochilodus scrofa (Hirt de Kunkel y Flores 1994). Este escenario da un factor de condición (“k”), el cual se manifiesta positivamente en función de aquellos peces que tienen mayor longitud y peso, catalogándolas como poblaciones ecológicamente saludables, dado que se ha detectado que en algunas poblaciones la relación entre el peso y la longitud, no tienen el mismo efecto positivo comparativamente con aquellas poblaciones sujetas a presiones antrópicas (Cifuentes et al. 2012). Sin embargo, este factor de condición puede variar por distintos factores como disponibilidad de alimento, estacionalidad, e inclusive la interrelación con otras especies de peces, condicionando el potencial de fecundidad (Cifuentes et al. 2012).
Malabarba y Weitzman (2003) mencionan la presencia de espinas en los radios, de las aletas anal y pélvica, a menudo en la aleta caudal y rara vez en la dorsal y aletas pectorales en machos de las familias Gasteropelecidae, Serrasalminae y en varias especies de Characidae; estos ganchos se conocen como “órganos de contacto” y se han considerado apéndices para estimular el cortejo, el desove y defensa del territorio (Wiley y Collette 1970, Azevedo 2000). Este patrón no se evidenció en G. quitoensis. Sin embargo, no se descarta su presencia, ya que esta podría estar condicionada a la época de colecta (julio) ya que Mojica et al. (2012) mencionaron que el ciclo reproductivo de G.bogotensis es permanente, con dos picos de desove al año, uno durante marzo y abril y otro entre septiembre y noviembre. Además Lampert et al. (2004), plantean que la frecuencia de ocurrencia de espinas en las aletas pélvicas y anal de B. iheringii está relacionada con los estadios de maduración gonadal de los machos.
Una última característica reproductiva correlacionada con la fecundidad es la incubación y cuidado parental de la progenie. Se ha reportado una fecundidad baja en especies de peces que incuban sus huevos y cuidan sus crías para garantizar efectivamente la mayor sobrevivencia posible, caso contrario si la fecundidad fuese alta (Villamil y Arias 2011). Para G. bogotensis se ha reportado cuidado parental mediante la construcción de nidos cerca de la vegetación (Álvarez- León et al. 2002). Es posible que G. quitoensis tenga un comportamiento parecido al de G. bogotensis (obs. pers.), razón por la cual el cuidado parental podría explicar la baja fecundidad encontrada aquí. Adicionalmente, habría que evaluar cuál es el efecto negativo de las truchas sobre la dinámica poblacional de las especies de Grundulus (Palma et al. 2002, Vehanen et al. 1998), lo que también influiría en el estado de conservación de esta especie.
Conclusiones
La cantidad de ovocitos estimados para Grundulus quitoensis y el tamaño de los individuos reveló que es una especie con baja fecundidad. Esto conllevaría a sugerir que las medidas de manejo que se hagan sobre la especie a partir de evaluaciones de su dinámica poblacional necesariamente deben contemplar la estrategia reproductiva. La presencia de ejemplares con gónadas maduras encontrada durante el periodo estudiado(épocalluviosa), sugirióque G. quitoensis en El Voladero se reproduce todo el año. Investigaciones futuras en diferentes épocas determinarían los picos de mayor actividad reproductiva.
En G. quitoensis se encontró una talla pequeña que no supera los 10 cm de longitud estándar, en relación a otras especies del grupo (p. e. Astyanax, Bryconamericus o Moenkhausia), y esto podría determinar que el incremento de las gónadas se exprese mejor con el aumento corporal total de cada individuo.
Agradecimientos
Queremos hacer extensivo nuestro agradecimiento a Cecilia Puertas, por sus valiosos aportes a la revisión del manuscrito y a Gianina Brichetto, quien colaboró con la realización del mapa de estudio.
Referencias
Álvarez-León, R., J. A. González y J. E. Forero. 2002. Grundulus bogotensis. Pp: 200-202. En: Mojica, J. I., C. Castellanos, S. Usma y R. Álvarez (Eds.). Libro Rojo de Peces Dulceacuícolas de Colombia. La Serie Libro Rojos de Especies Amenazadas de Colombia. Instituto de Ciencias Naturales, Universidad Nacional de Colombia, Ministerio del Medio Ambiente, Bogotá.
Araya, P., L. Hirt y S. Flores. 2003. Biología reproductiva y crecimiento de Pimelodus clarias maculatus (Lac. 1803) (Pisces, Pimelodidae), en la zona de influencia del embalse Yacyretá. Ecología Austral 13: 83-95.
Azevedo, M. A. 2000. Biologia reprodutiva de dois glandulocaudíneos com inseminação, Mimagoniates microlepis e Mimagoniates rheocharis (Teleostei: Characidae), e características de seus ambientes. Unpublished M. Sc. Dissertation, Universidade Federal do Rio Grande do Sul, Porto Alegre, Brazil. 84 pp.
Barriga, R. S. y E. Terneus. 2005. Primer hallazgo de una población paleoendémica del pez Grundulus cf. bogotensis (Humboldt, 1821) en los altos Andes del Ecuador. Politécnica 26: 1-13.
Cifuentes, R., J. González, G. Montoya, A. Jara, N. Ortíz, P. Piedra y E. Habit. 2012. Relación longitud - peso y factor de condición de los peces nativos del río San Pedro (cuenca del río Valdivia, Chiles). Gayana Especial 75 (02): 101-110.
Claramunt, G., G. Herrera, M. Donoso y E. Acuña. 2009. Período de desove y fecundidad del pez espada (Xiphias gladius) capturado en el Pacífico suroriental. Latin American Journal of Aquatic Research 37 (1): 29-41.
Chaves, P. y G. Vazzoler. 1984. Aspectos biológicos dos peixes amazônicos. II. Anatomia microscópica de ovários, escala de maturidade e tipo de desova das espécies do genero Semaprochilodus. Revista Brasileira de Biologia 44 (3): 347-359.
Ferriz, R., E. M. Fernández, C. A. Bentos y G. R. López. 2007. Reproductive biology of Pseudocorynopoma doriai (Pisces: Characidae) in the High Basin of the Samborombón River, province of Buenos Aires, Argentina. Journal of Applied Ichthyology 23: 226-230.
Ferriz, R., C. Bentos, E. Fernández y G. López. 2011. Reproducción y dinámica poblacional de Cheirodon interruptus (Ostariophysi: Characidae) en el arroyo El Portugués, alta cuenca del río Samborombón, Argentina. Latin American Journal of Aquatic Research 39 (1): 151-160.
Hirt de Kunkel, L. M. y S. A. Flores. 1994. Reproducción de Prochilodus scrofa (Steindachner, 1881) Osteichthyes, Prochilondontidae: histología y escala de maduración de ovarios. Boletim do Instituto de Pesca 21: 83-94.
Huaquín, L., D. Veliz y G. Arratia. 2002. Estudio comparativo de ovarios y cubiertas ovocitarias en peces Siluriformes de aguas continentales de Chile. Gayana 66: 269-274.
Humboldt, F. H. y A. Valenciennes. 1821. Recherches sur les poissons fluviatiles de l’Amérique Équinoxiale. A Voyage de Humboldt et Bonpland, Deuxième partie. Observations de Zoologie et d’Anatomie comparée»; Voyage de Humboldt et Bonpland. Deuxième partie 2: 145-216.
Hunter, N. y R. J. Leong. 1985. Batch fecundity in multiple spawning fishes. Pp: 67 - 77. En: Lasker, R. (Ed.). An egg production method for estimating spawning-biomass of pelagic fish: application to the northern anchovy, Engraulis mordax. U.S. Dep. Commer. NOAA Tech. Rep. NMFS.
Lampert, V., M. Azevedo y C. Bernhardt. 2004. Reproductive biology of Bryconamericus iheringii (Ostariophysi: Characidae) from rio Vacacaí, RS, Brazil. Neotropical Ichthyology 2 (4): 209-215.
Lampert, V., M. Azevedo y C. Bernhardt. 2007. Reproductive biology of Bryconamericus stramineus (Ostariophysi: Characidae) from Rio Ibicuí, RS, Brazil. Brazilian Archives of Biology and Technology 50 (6): 995-1004.
Malabarba, L. R. y S. H. Weitzman. 2003. Description of a new genus with six new species from southern Brazil, Uruguay and Argentina, with a discussion of a putative Characid clade (Teleostei: Characiformes: Characidae). Comunicacoes do Museu de Ciencia e Tecnologia da PUCRS, Série Zoologia 16 (1): 67-151.
Mojica, J. I., J. S. Usma, R. Álvarez-León y C. A. Lasso (Eds.). 2012. Libro rojo de peces dulceacuícolas de Colombia. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Instituto de Ciencias Naturales de la Universidad Nacional de Colombia, WWF Colombia y Universidad de Manizales. Bogotá, D. C., 319 pp.
Nakatani, K., A. Agostino, A. Bialetzki, S. Vanderlei, P. Cavicchioli, M. Makrakis y C. Pavanelli 2001. Ovos e larvas de peixes de água doce: Desenvolvimento e manual de identificacao. Maringá. EDUEM, 378 pp.
Núñez, J. y F. Duponchelle. 2009. Towards a universal scale to assess sexual maturation and relation life history traits in oviparous teleost fishes. Fish Physiology and Biochemistry 35: 167-180.
Palma, A., R. Figueroa, V. Ruíz, E. Araya y P. Berrios. 2002. Composición de la dieta de Oncorhynchus mykiss (Walbaum 1792) (Pisces: Salmonidae) en un sistema fluvial de baja intervención antrópica: Estero Nonguen, VIII región, Chile. Gayana 66 (2): 129-139.
Román-Valencia, C., H. Paepkey, F. Pantoja. 2003. Una especie nueva de Grundulus (Teleostei: Ostariophysi: Characidae) para Colombia y redescripción de Grundulus bogotensis (Humboldt y Valenciennes, 1833). Memoria de la Fundación La Salle de Ciencias Naturales 155: 51-72.
Román-Valencia, C., R. Ruíz y R. Barriga. 2005. Una nueva especie ecuatoriana del género de peces andinos Grundulus (Characiformes: Characidae). Revista de Biología Tropical 53: 537-544.
Román-Valencia, C., R. Ruíz y A. Giraldo. 2008. Dieta y reproducción de dos especies sintópicas: Hemibrycon boquiae y Bryconamericus caucanus (Pisces: Characidae) en la quebrada Boquía, río Quindío, Alto Cauca, Colombia. Revista del Museo Argentino de Ciencias Naturales, n. s. 10 (1): 55-62.
Román-Valencia, C., J. A. Vanegas y R. Ruíz. 2010. Phylogenetic and biogeographic study of the Andean genus Grundulus (Teleostei: Characiformes: Characidae). Vertebrate Zoology 60 (2): 107-122.
Terneus, E. 2002. Estructura y composición florística de las plantas acuáticas vasculares en 70 lagunas altoandinas del Ecuador. Tesis de doctorado. Pontificia Universidad Católica del Ecuador, Facultad de Ciencias Exactas y Naturales, Escuela de Biología. Quito, 120 pp.
Vazzoler, A. E. A. 1996. Biología da reprodução de peixes Teleósteos: teoría e prática. Editora da Universidade Estadual de Maringa, Maringa, Brasil, 169 pp.
Vehanen, T., P. Hyvarinen y A. Huusko. 1998. Food consumption and prey orientation of piscivorus brown trout (Salmo trutta) and pikeperch (Stizostedion lucioperca) in a large regulated lake. Journal of Applied Ichthyology 14: 15-22.
Valdiviezo-Rivera, 2016. Características ambientales del hábitat de Grundulus quitoensis, para generar las bases de un programa de conservación. Tesis de Maestría. Universidad Internacional SEK-Ecuador, Facultad de Ciencias Naturales y Ambientales. Quito, 66 pp.
Villamil, L. y J. Arias. 2011. Fecundidad de Otocinclus spectabilis. Revista Orinoquia 15 (1): 41-47.
West, G. 1990. Methods of assessing ovarian development in fishes: a review. Australian Journal of Marine & Freshwater Research 41: 199-222.
Wiley, M. L. y B. B. Collette. 1970. Breeding tubercles and contact organs in fishes, their occurrence, structure, and significance. Bulletin of the American Museum of Natural History ١٤٣ (٣): ١٤٥-٢١٦.
Información adicional
Citación del artículo: Valdiviezo-Rivera, J., E. Terneus, D. Vera y A. Urbina. 2016. Análisis de producción gonadal del pez Grundulus quitoensis Román-Valencia, Ruiz-C. y Barriga, 2005 (Characiformes: Characidae) en la laguna altoandina “El Voladero”, provincia El Carchi, Ecuador. Biota Colombiana 17 (2): 89-97. DOI: 10.21068/c2016.v17n02a07