Forestación de bosques en sabanas de la altillanura colombiana: relevancia de las condiciones ambientales para el establecimiento de plántulas
Afforestation of savanna forests of the Colombian altillanura: relevance of the environmental conditions for the establishment of seedlings.
Forestación de bosques en sabanas de la altillanura colombiana: relevancia de las condiciones ambientales para el establecimiento de plántulas
Biota Colombiana, vol. 18, 1, pp. 99-109, 2017
Instituto de Investigación de Recursos Biológicos "Alexander von Humboldt"
Recepción: 23 Agosto 2014
Aprobación: 31 Enero 2017
Resumen: Una forma de contrarrestar el cambio climático es la generación de bosques con alta capacidad de almacenamiento de carbono. En este trabajo se reportan los resultados de una iniciativa de reforestación de bosque en sabanas de la rserva Tomogrande. Se crearon barreras contra el fuego en seis áreas: dos inundables y dos no inundables, para sembrar plántulas de bosques de la Orinoquia, y manteniendo dos más como control sin adición de plántulas. De 200 plántulas sembradas en sabanas no inundables, únicamente el 17 % de ellas sobrevivieron por más de dos años (33 % para las especies de bosques aledaños y 12 % para las de otros lugares de la Orinoquia). Ninguna de las 182 plántulas trasplantadas a zonas inundables sobrevivió por más de dos años. La principal causa de mortalidad en sabanas bien drenadas fue el marchitamiento. Se concluye que a pesar de que la ausencia de fuego puede ayudar al establecimiento de árboles, las condiciones climáticas y lumínicas de la sabana disminuyen las probabilidades de que las plantas de bosque se establezcan y las que logran mayor probabilidad de supervivencia son las especies que viven en los bosques de galería aledaños (especialmente en bordes de bosque).
Palabras clave: Barreras de establecimiento, Bosques de galería en Colombia, Sabanas inundables, Supervivencia de plántulas.
Abstract: One way to counteract climate change is to plant forests with high carbon storage capacity. In this study we report the results of a reforestation project in savannas of the Tomogrande Reserve, in Vichada Department, Colombia. We restricted fire in six one-hectare plots: in two seasonally inundated and two highland savannas we planted seedlings of trees found in the Orinoco Basin and nearby gallery forests and in two of them we did not plant seedlings (control plots). Out of 200 seedlings planted in well-drained savannas, only 17 % survived after two and a half years (33 % came from nearby forest and 12 % from other areas). None of the 182 seedlings planted in flooded savannas survived at the end of the study. The main mortality cause in well-drained savannas was wilting. We concluded that in addition to the control of fire, seedling establishment of forest trees in savannas is highly affected by climatic and light conditions and for this reason the trees with highest potential for restoration are the ones already found at the site in the same ecological conditions (e.g. forest edge).
Keywords: Flooded savannas, Gallery forests in Colombia, Plant establishment barriers, Plant survival.
Introducción
El cambio climático global es un fenómeno bien documentado (Karl y Trenbenth 2003, Meehl et al. 2005) que puede tener fuertes implicaciones en los patrones de diversidad del planeta. Este fenómeno se genera principalmente por el aumento en la concentración de gases de invernadero en la atmósfera y por los efectos de evaporación de la superficie de la tierra (Bonan 2008). Se ha documentado que una de las estrategias para mitigar estos problemas es manteniendo bosques, ya que las plantas por procesos de fotosíntesis pueden fijar CO2 de la atmósfera (Nemani et al. 2000). Sin embargo, es claro que las tendencias actuales en el uso de la tierra son de eliminar bosques para generar zonas productivas (Foley et al. 2005), los cuales tienen una menor capacidad de acumulación de carbono a largo plazo. Ante esta tendencia y otros servicios ambientales que ofrecen los bosques, se ha sugerido que la reforestación y restauración de estos puede ser una alternativa para mitigar los problemas asociados al cambio climático global, que incluyen amenazas a humanos y muchas otras especies (Meehl et al. 2005).
El establecimiento, la supervivencia y crecimiento de las plántulas limitan la regeneración de bosques tropicales (Holl et al. 2000). Por ello es necesario conocer su impacto para evaluar las estrategias más adecuadas para restablecer ambientes degradados o propiciar el establecimiento de árboles en zonas de poca acumulación de biomasa. Entre los factores que influyen en estos procesos están: disponibilidad de semillas, calidad de la dispersión, características edáficas, depredación de semillas, competencia con especies establecidas, disturbios y herbivoría (Holl et al. 2000, Duncan y Chapman 2002).
Uno de los principales factores que afectan el establecimiento de especies vegetales en las sabanas es el régimen de fuegos, el cual ha sido reconocido como una fuerza evolutiva importante para las plantas logrando determinar su distribución, estructura filogenética y procesos de desarrollo (Howe 1995, Silva y Batalha 2010). Las sabanas colombianas por ejemplo, presentan entre el 3 % y el 6 % de los eventos de fuego a nivel mundial (Romero-Ruiz et al 2010) y aunque se considera que tales ecosistemas, han sido sometidos a este tipo de perturbaciones por millones de años, el incremento de fuegos de origen antropogénico ha sido considerable en los últimos tiempos. Lo anterior ha limitado la expansión de los bosques y generado cambios en su estructura y composición; dados los efectos negativos sobre la reproducción y establecimiento de aquellas especies no tolerantes al fuego (Hoffmann et al. 2003).
Se ha propuesto el uso de plantaciones de especies locales como herramienta para atenuar las barreras que limitan la regeneración de los bosques. Entre los beneficios que las plantaciones podrían brindar se encuentran: generar una mayor complejidad estructural y mayor cantidad de recursos. Si se presenta una mayor disponibilidad de recursos, los ecosistemas atraerían mayor cantidad de animales dispersores y aumentaría la lluvia de semillas. Adicionalmente, cuando se establecen bosques mejoran las condiciones microclimáticas del sotobosque que favorecen el reclutamiento de plántulas de árboles de sucesión tardía (Bazzas y Pickett 1980), que requieren distintas condiciones de temperatura, humedad y sombrío. Por otra parte, se mejora la estructura y fertilidad del suelo al crear capas de materia orgánica por la hojarasca de los árboles; se disminuye la competencia de las plántulas bajo el dosel, especialmente con aquellas competidoras como gramíneas y helechos; y se disminuye la probabilidad de disturbios como fuegos (Lugo 1997, Parrota et al. 1997).
Por las razones nombradas anteriormente, las plantaciones de madera han sido una de las estrategias más utilizadas para recuperar áreas degradadas o abandonadas, especialmente por el atractivo económico de las especies maderables. Sin embargo, algunos estudios han probado que bajo ciertas condiciones la regeneración natural puede ser una mejor estrategia para una restauración ecológica, ya que las plantaciones usualmente sólo ayudan a recuperar la capacidad productiva y poco hacen por el restablecimiento de la biodiversidad (Lamb 1998). Las características que más se debaten acerca del uso de las plantaciones están relacionadas con los efectos negativos de los monocultivos: una baja biodiversidad, una menor estabilidad ecológica, una menor eficiencia en el uso de los recursos, un mayor desgaste de los componentes edáficos e hídricos, y el uso de especies exóticas (Lugo 1997). Es por esto que se ha propuesto el uso de plantaciones como herramientas de forestación sólo bajo ciertas condiciones de alteración de los ecosistemas: zonas muy degradadas, muy extensas, muy alejadas de remanentes de vegetación o dominadas por pastos (Murcia 1997, Lamb 1998).
De cualquier forma, el papel que juegan los cultivos en los procesos de regeneración debe ser evaluado para poder dar apoyo científico a los planes de forestación, tratando de identificar las particularidades propias de cada área geográfica y de cada cultivo usado como estrategia de regeneración. Si se logra un mejor entendimiento de los procesos y los limitantes que gobiernan la regeneración de un bosque intervenido se pueden proponer prácticas que atenúen las barreras, y que agilicen y mejoren la regeneración de los bosques. Teniendo en cuenta el anterior marco conceptual, en este trabajo se quiso realizar un proyecto piloto de forestación de bosques en sabanas de la altillanura en la reserva Tomogrande (Vichada, Orinoquia colombiana). En particular, se centró en evaluar la posibilidad de establecer bosques en sabanas del Orinoco, mediante el control de fuego y forestación asistida mediante la adición de plántulas y plantones.
Material y métodos
La reserva Tomogrande se encuentra ubicada en el departamento del Vichada en el municipio de Santa Rosalía (4°51´0,97”N, 70°16´15,35”W) a 100 m s.n.m. entre los ríos Tomo y caño Grande. La región presenta un régimen climático unimodal, con un intervalo de pluviosidad de anual entre 2.323 y 2.673 mm (Correa-Gómez y Stevenson 2010), con una época seca de diciembre a marzo y una época de lluvias el resto del año. Sin embargo, para el único año en que se estimó la precipitación anual en el lugar de estudio se obtuvo un valor cercano a los 2.900 mm, correspondiente a un año muy lluvioso.
La temperatura promedio anual es de 26 ºC, con mínimas de 20 ºC y máximas de 34,5 ºC. La topografía presenta leves ondulaciones, con algunas corazas petroférricas de carácter erosivo, y el bioma es considerado en su mayoría peinobioma de sabanas altas (Romero et al. 2004). Así, la zona corresponde a las sabanas de altillanura del Orinoco, que están ubicadas sobre una placa elevada topográficamente que cubre la mayor parte del departamento del Vichada y buena parte del Meta (Castro-Lima et al. 2017), donde ocurren elementos bióticos del escudo Guyanés.
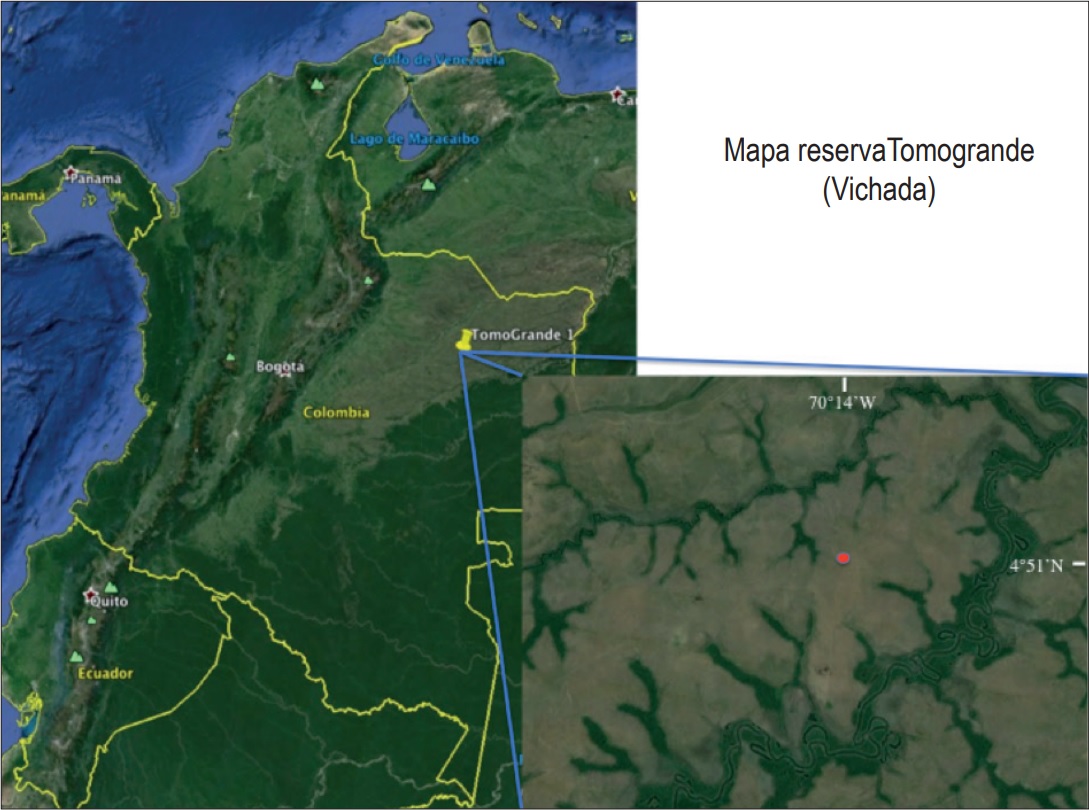
Figura 1.
Ubicación geográfica la reserva Tomogrande (Vichada), Orinoquia colombiana. Datos del mapa ©2015 Google, Landsat, Copernicus.
Se instalaron seis parcelas permanentes de vegetación cada una de 1 ha (100x100 m). Dos de ellas se ubicaron en sabanas de pastos con buen drenaje y cuatro en sabanas arboladas sujetas a inundaciones estacionales (dos sembradas y dos controles). Las parcelas fueron delimitadas con tubos de PVC ubicados cada 10 m con ayuda de un clinómetro laser con medidor de distancia. Todos los árboles de más de 10 cm de diámetro a la altura del pecho (DAP) fueron marcados y determinados. También se revisó la presencia de juveniles en 25 subparcelas de 5x5 m, y cobertura de plántulas y herbáceas en 25 subparcelas de 2x2 m. Para clasificar los individuos se siguieron los siguientes criterios: plántulas con altura menor a 1,3 m ó mayores a 1,3 m en altura pero con un DAP menor a mayor a 1 cm; juveniles se consideraron plantas con DAP entre 1 y 5 cm (Stevenson 2011). Las parcelas en sabanas bien drenadas se ubicaron hacia el costado occidental de un bosque de galería a un par de metros de la vegetación leñosa, pues están más protegidas de los vientos y los fuegos. El control del fuego se hizo evitando incendiar las zonas de las parcelas y se instalaron guardarrayas bordeando las zonas a proteger. En estas regiones se cortó la vegetación mediante guadañadora, para mantener una franja de cerca de 5 m libre de vegetación (Figura 2).
Para la reforestación asistida se compraron 250 plantones de vivero con alturas entre 30 y 60 cm de altura. El criterio de selección se centró en que fueran especies de la Orinoquia, con énfasis en plantas de frutos carnosos y/o maderables. Sin embargo, también dependió de la disponibilidad en el vivero. De estas se sembraron 200 en julio de 2011 en las parcelas de sabana bien drenada (Tabla 1). Estas plantas fueron sembradas en julio de 2011. En cada esquina se clavó un tubo de PVC y se sembraron tres individuos separados cerca de 50 cm del tubo. Cada plántula fue marcada con una plaqueta metálica, que fue amarrada con un hilo de nylon para asegurar su monitoreo. Las plántulas se sembraron en las tres líneas más próximas al bosque de galería de la parcela de 100x 100 m, con el fin de reducir el tiempo de exposición al sol directo y a una posible desecación. Se realizó un monitoreo al mes del sembrado y luego una vez al año, revisando la supervivencia y el crecimiento de las plantas hasta el 2013.

Figura 2.
Vista A) sabana inundable, B) sabana no inundable, C) sabana inundable arbolada y D) plántula sembrada.
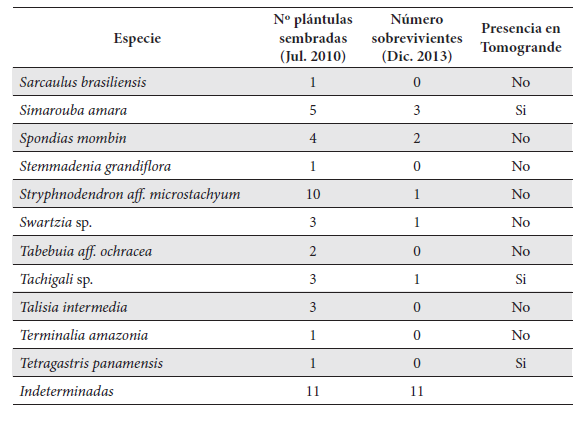
Plantas sembradas en sabanas no inundables en la reserva Tomogrande, Vichada, Colombia. Se incluyen nombres científicos, cantidad de individuos sembrados y sobrevivientes. La última columna indica si la especie ha sido detectada en los boques de la reserva.
Adicionalmente, se utilizaron plántulas del interior de los bosques de galería. Para este efecto se ubicaron plantas creciendo sobre el sistema de trochas de la estación. Estas plántulas fueron removidas cuidadosamente, con el fin de evitar daños en la raíz y fueron trasplantadas inmediatamente a sabanas inundables. Se escogieron este tipo de sabanas, dado que la humedad del suelo podría ayudar a su establecimiento, asumiendo que el requerimiento de agua para estas plantas puede ser muy alto si se encuentran expuestas a sol directo.
Resultados
Las cuatro parcelas de vegetación de zonas inundables donde se realizó la siembra se caracterizaron por la dominancia del saladillo (Caraipa llanorum), con un máximo de 67 individuos por hectárea (Tabla 2). Esta especie estuvo acompañada de unos pocos individuos esparcidos en la sabana, e incluyendo individuos de chaparro (Curatella americana) y peralejo (Byrsonima crassifolia). La diversidad de las cuatro parcelas fue muy baja, incluyendo apenas entre 3 y 4 especies diferentes por hectárea. En dos de estas parcelas se sembraron plántulas en áreas donde la cobertura de árboles varió entre un 20 y un 50 % (Figura 2). Las parcelas de sabanas bien drenadas no incluyeron ningún individuo de más de 10 cm de DAP, y tan solo unos pocos individuos esparcidos de chaparro y peralejo. La cobertura de hierbas (principalmente Poaceae) fue mayor al 80 %, excepto debajo de agrupaciones densas de saladillo. Las plantas más abundantes en las sabanas bien drenadas fueron: Trachypogon spicatus, T. vestitus, Andropogon selloanus, A. leucostachyus y Axonopus purpusii; mientras que las de sabanas inundables fueron: A. anceps, Echinolaena inflexa y Coleataenia caricoides.
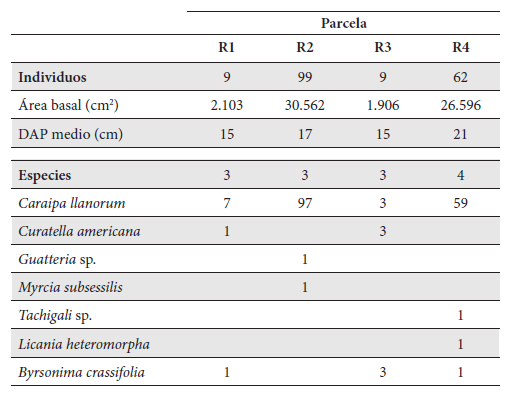
Número de individuos, área basal y DAP de especies arborescentes en parcelas de sabanas inundables.
De las 200 plántulas sembradas en sabanas no inundables, únicamente el 17 % de las plántulas sobrevivió hasta los dos años y medio (última revisión). Las especies que lograron mayor número de sobrevivientes fueron Simarouba amara, Tapirira guianensis, Caraipa llanorum, Acosmium nitens y Spondias mombin. Las tasas de supervivencia más altas fueron S. amara (60 % en dos años y medio), A. nitens y S. mombin (50 %) y Caraipa llanorum (40 %). Todas las especies con números altos de supervivientes están presentes en los bosques aledaños (Correa-Gómez y Stevenson 2012). S. mombin sería una excepción, pero igualmente es común en bosques de várzea de la Orinoquia. Al realizar un análisis de contingencia, mediante una prueba G de independencia, resulta claro que hay una asociación estadísticamente significativa (G = 6,52, gl.= 1, p = 0,011), la cual indica que la probabilidad de sobrevivir es más alta para las especies que crecen en los bosques de la reserva, que para las que no han sido reportadas. Se estima que la tasa de supervivencia de las especies que se encuentran en bosques de galería aledaños fue casi del 33 %, y las de otros lugares de la Orinoquia tan solo del 12 % (Tabla 1).
El crecimiento de las plántulas sobrevivientes fue muy bajo. De hecho, en promedio la tasa de crecimiento relativo y su variación (altura inicial – altura final / altura inicial), en muchos de los supervivientes fue negativa. Esto ocurrió pues en varios casos las plantas se desecaron, pero lograron producir nuevas yemas en las partes bajas del tronco, decreciendo así en altura las estructuras vivas. En las sabanas bien drenadas, la principal causa de mortalidad fue justamente el marchitamiento.
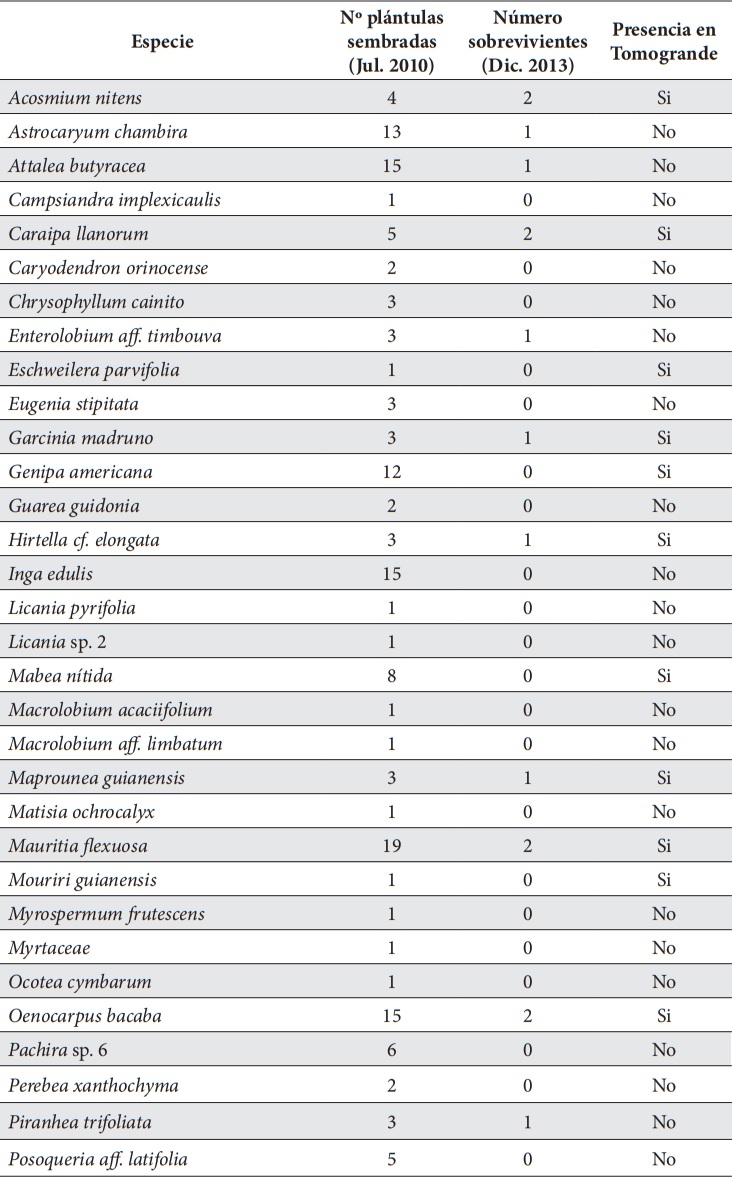
La supervivencia en zonas inundables fue tan sólo de 14 % durante el primer mes de establecimiento. Las especies que mostraron un mejor establecimiento en la sabana luego del trasplante fueron Goupia glabra, Xylopia aromatica y algunos individuos de Tapirira guianensis. Sin embargo, estas murieron cuando el nivel de las aguas aumentó y las plántulas se vieron sujetas a la inundación. En estas parcelas, muchas de las plántulas botaron sus hojas durante el primer mes de establecimiento, y lograron rebrotar hasta la siguiente creciente de las lluvias. Ninguna de las 182 plántulas sobrevivió por más de dos años, lo que sugiere que ninguna de las especies trasplantadas desde las trochas del bosque está adaptada a las condiciones de inundación (Tabla 3).
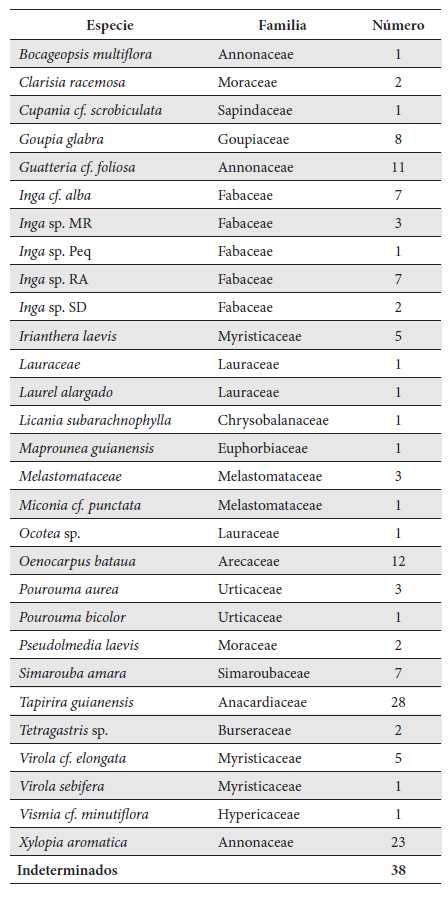
Especies utilizadas en la forestación de sabanas inundables. Las siglas corresponden a morfoespecies.
Discusión y conclusiones
Algunos estudios indican que buena parte de las sabanas de la Orinoquia colombiana podrían tener una vegetación arbórea continua, de acuerdo a los patrones de pluviosidad y temperatura de la región y que la presencia de sabanas dependería más de factores antrópicos relacionados con la ocurrencia de fuegos (Henriques y Hoffmann 2011). Si esto fuera cierto, es de esperase que la supresión de fuegos podría ser la principal herramienta para facilitar el establecimiento de especies de árboles que ocurren en la región. En este trabajo, sin embargo, se encontró tanto en los tratamientos de sabanas bien drenadas, como en saladillales inundables, que las tasas de supervivencia fueron muy bajas a pesar de haber realizado un esfuerzo por controlar el efecto del fuego.
Las tasas bajas de establecimiento de plántulas sugiere que las condiciones climáticas son relevantes para tener éxito en planes de generación de bosques en zonas de altillanura; en particular, la altísima mortalidad de plántulas no típicas de la región (88 % en dos años), en comparación con la alta mortalidad encontrada para las que sí están reportadas para la zona (67 %). Lo anterior sugiere que las especies presentes en la región son el resultado de adaptación a condiciones abióticas particulares y no sólo del resultado de procesos azarosos de migración y establecimiento (Hubbell 2001).
De manera similar, la alta mortalidad encontrada en períodos de inundación en las zonas bajas, sugiere que debe tenerse en cuenta especies que posean adaptaciones particulares para soportar este tipo de filtro ecológico (Parolin y Wittmann 2010). La suposición sobre la posibilidad de que especies de interior de bosques de galería podrían verse beneficiadas con la humedad del suelo en sabanas bajas no estuvo soportada por los datos, pues la mortalidad fue del 100 % y del 83 % teniendo en cuenta también sabanas bien drenadas (Tabla 1). Para sabanas inundables, la posibilidad de crecer bajo la sombra de parentales no conllevó a una alta supervivencia, probablemente por las características del drenaje. Sin embargo, no se descarta que para sabanas bien drenadas, la presencia de otras plantas o de especies nodrizas puede ser adecuado para que logren establecerse especies típicas de bosques de galería sobre las sabanas.
Las especies que tuvieron el mayor éxito fueron en su mayoría especies presentes en la zona o especies que crecen bien en condiciones de abundante irradiación, como es el caso de los hobos (Spondias mombin) (Stevenson 2007). Las otras especies con relativo éxito de supervivencia fueron quienes regeneran de manera abundante en bordes de bosque de galería, y por lo tanto, también parecen estar adaptadas a condiciones de alta luminosidad y alto potencial de pérdida de agua en la altillanura colombiana (Stevenson, observaciones personales). Por lo tanto, los resultados aquí obtenidos son consistentes con la idea de que las sabanas de la Orinoquia tienen una larga historia (Behling y Hooghiemstra 1999), durante la cual las poblaciones de árboles han desarrollado adaptaciones a ambientes particulares.
Dado que la causa de muerte más común para las plántulas sembradas en la sabana bien drenada fue el marchitamiento, se recomienda que en futuros trabajos de forestación o restauración se debe procurar que las plántulas puedan superar la barrera de la desecación. Las sabanas bien drenadas no tienen períodos de más de un día de inundación (se pueden inundar parcialmente durante una gran lluvia), pero en épocas secas se genera un alto estrés hídrico para las plantas, que pareció ser la principal causa de mortalidad. A pesar de que otros autores han resaltado que la competencia con pastos (Hanan y Lehmann 2010) y la escasez de nutrientes en este tipo de sabanas (Medina y Silva 1990) son factores importantes en el establecimiento de plántulas de árboles, se considera que la aplicación de plantas nodriza y especialmente el suministro de agua son claves para el éxito de establecimiento en sabanas.
De este proyecto piloto, las principales conclusiones indican que los planes de forestación de las sabanas del Orinoco deben tener en cuenta especies adaptadas a ambientes particulares. Aunque se considera que el proyecto fue poco exitoso, esperamos que la experiencia pueda aportar para futuros trabajos de forestación en este tipo de ecosistemas, dado que es muy poco lo que se ha publicado al respecto (Mendez et al. 2012). A partir de esta experiencia, se sugiere que la principal barrera para el establecimiento (una vez controlado el fuego), parece ser la posibilidad de marchitamiento por falta de agua o el exceso de ella en sabanas inundables. Se cree que futuros trabajos deben incluir suministro de agua en períodos de escasez o disminución de la radiación por medio de especies nodriza, propias de la región.
Agradecimientos
Queremos agradecer a Nelson Galvis, María Fernanda Torres, Sofía Argüello y David Góngora por su colaboración en el trabajo de campo. También a John y Luz Dary, por la colaboración manteniendo los guarda-rayas. A Francisco Castro por el aporte del material vegetal, por sus determinaciones y por los comentarios sobre el documento final. Este estudio fue financiado por un proyecto semilla de la Facultad de Ciencias de la Universidad de Los Andes.
Referencias
Bazzaz, F. A. y S. T. A. Pickett. 1980. Physiological ecology of tropical succession: a comparative review. Annual review of ecology and systematics 11: 287-310.
Behling, H. y H. Hooghiemstra. 1999. Environmental history of the Colombian savannas of the Llanos Orientales since the Last Glacial Maximum from lake records El Pinal and Carimagua. Journal of Paleolimnology 21: 461–476.
Bonan, G. B. 2008. Forests and climate change: Forcings, feedbacks, and the climate benefits of forests. Science 320 (5882): 1444-1449.
Castro-Lima, F., R. Antelo-Albertos, P. R. Stevenson y M. González-Caballero. 2016. Ecosistémas estratégicos. Pp: 33-56. En: Trujillo, F., R. Antelo y S. Usma (Ed). Biodiversidad de la cuenca baja y media del río Meta. Fundación Omacha, Fundación Palmarito y WWF. Bogotá.
Correa-Gomez, D. F. y P. R. Stevenson. 2010. Estructura y diversidad de bosques de galería de una sabana estacional de los llanos orientales colombianos (Reserva Tomo Grande, Vichada). Revista Orinoquia 14 (1): 31-48.
Duncan, S. y C. Chapman. 2002. Limitations of animal seed dispersal for enhancing forest succession on degraded lands. Pp: 437-450. En: Levey, D., W. Silva y M. Galetti. (Ed.). Seed Dispersal and Frugivory: Ecology, Evolution and Conservation. CAB International, Wallingford, UK.
Foley, J. A., R. Defries, G. P. Asner, C. Barford, G. Bonan, S. R. Carpenter, F. S. Chapin, M. T. Coe, G. C. Daily, H. K. Gibbs, J. H. Helkowski, T. Holloway, E. A. Howard, C. J. Kucharik, C. Monfreda, J. A. Patz, I. C. Prentice, N. Ramankutty y P. Snyder. 2005. Global consequences of land use. Science 309 (5734): 570-574.
Hanan, N. y C. Lehmann. 2010. Tree-Grass Interactions in Savannas: Paradigms, Contradictions, and Conceptual Models. Taylor and Francis Group: Boca Raton, FL, USA. 56 pp.
Henriques, R. P. B. y W. A. Hoffmann. 2011. Tree increase in fire-protected cerrado savanna: dynamics and implications to disequilibrium hypothesis. Abstract. ATBC & SCB Africa, meeting program Arusha, Tanzania.74 pp.
Holl, K., M. Loik, E. Lin e I. Samuels. 2000. Tropical Montane Forest Restoration in Costa Rica: Overcoming Barriers to Dispersal and Establishment. Restoration Ecology 8 (4): 339-349.
Howe, H. F. 1995. Succession and fire season in experimental prairie plantings. Ecology 76 (6): 1917-1925.
Karl, T. R. y K. E. Trenberth. 2003. Modern global climate change. Science 302 (5651): 1719-1723.
Lamb, D. 1998. Large-scale ecological restoration of degraded tropical forest lands: The potential role of timber plantations. Restoration Ecology 6 (3): 271-279.
Lugo, A. 1997. The Apparent Paradox or Reestablishing Species Richness on Degraded Lands on Tree Monocultures. Forest Ecology and Management 99: 9-19.
Medina, E. y J. F. Silva. 1990. Savannas of northern South America: a steady state regulated by water-fire interactions on a background of low nutrient availability. Journal of Biogeography 17: 403-413.
Méndez, F. F., Y. K. C. Martínez y M. B.Sarmiento. 2012. Biodiversidad vegetal asociada a plantaciones forestales de Pinus caribaea Morelet y Eucalyptus pellita F. Muell establecidas en Villanueva, Casanare, Colombia. Revista Facultad Nacional de Agronomía, Medellín 65 (2): 6749-6764.
Meehl, G. A., W. M. Washington, W. D. Collins, J. M. Arblaster, A. X. Hu, L. E. Buja, W. G. Strand y H. Y. Teng. 2005. How much more global warming and sea level rise? Science 307 (5716): 1769-1772.
Murcia, C. 1997. Evaluation of Andean Alder as a catalyst for the recovery of tropical cloud forests in Colombia. Forest Ecology and Management 99: 163-170.
Nemani, R. R., C. D. Keeling, H. Hashimoto, W. M. Jolly, S. C. Piper, C. J. Tucker, R. B. Myneni y S. W. Running. 2003. Climate-driven increases in global terrestrial net primary production from 1982 to 1999. Science 300 (5625): 1560-1563.
Parolin, P. y F. Wittmann. 2010. Struggle in the flood: tree responses to flooding stress in four tropical floodplain systems. AoB plants: plq003. doi: 10.1093/aobpla/plq003.
Parrota, J., J. Turnbull y N. Jones. 1997. Catalyzing native forest regeneration on degraded tropical lands. Forest Ecology and Management 99: 1-7.
Romero, M., G. Galindo, J. Otero y D. Armenteras. 2004. Ecosistemas de la cuenca del Orinoco colombiano. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt. Bogotá. Colombia. 189 pp.
Romero-Ruiz, M., A. Etter, A. Sarmiento y K. Tansey. 2010. Spatial and temporal variability of fires in relation to ecosystems, land tenure and rainfall in savannas of northern South America. Global Change Biology 16: 2013–2023. doi: 10.1111/j.1365-2486.2009.02081.x
Silva, I. A. y M. A. Batalha. 2010. Phylogenetic structure of Brazilian savannas under different fire regimes. Journal of Vegetation Science 21 (6): 1003-1013.
Stevenson, P. R. 2007. A test of the escape and colonization hypotheses for zoochorous tree species in a Western Amazonian forest. Plant Ecology 190 (2): 245-258.
Sevenson, P. R. 2011. The abundance of large ateline monkeys is positively associated with the diversity of plants regenerating in Neotropical Forests. Biotropica 43 (4): 512-519.
Información adicional
Citación del artículo: Stevenson, P. R., M. A. Ramírez, L. F. Casas y F. Henao-Díaz. 2017. Forestación de bosques en sabanas de la altillanura colombiana: relevancia de las condiciones ambientales para el establecimiento de plántulas. Biota Colombiana 18 (Suplemento 1): 99-109. DOI: 10.21068/c2017.v18s01a06