Efecto del CaCl2 sobre el contenido de proteínas, prolina, acidez titulable, clorofila y contenido relativo de agua de Aloe vera expuesta a salinidad por NaCl
CaCl2 effect on protein, proline, titratable acidity, chlorophyll and relative water content from Aloe vera exposed to salinity by NaCl
Efecto del CaCl2 sobre el contenido de proteínas, prolina, acidez titulable, clorofila y contenido relativo de agua de Aloe vera expuesta a salinidad por NaCl
Biota Colombiana, vol. 18, núm. 2, pp. 29-40, 2017
Instituto de Investigación de Recursos Biológicos "Alexander von Humboldt"
Recepción: 16 Noviembre 2015
Aprobación: 01 Febrero 2017
Resumen: Con el fin de determinar el efecto del calcio sobre la fisiología de Aloe vera sometida a dos niveles salinos (100 y 150 mmol.m-3 de NaCl), se determinó el contenido relativo de agua del clorénquima (CRA), acidez titulable, pigmentos, proteínas y prolina (Pro) clorenquimática a 25 plantas jóvenes de dicha especie. Ninguno de los tratamientos salinos con o sin adición de calcio (NaCl+CaCl2) presentó diferencias estadísticamente significativas sobre variables como el CRA y pigmentos (clorofilas a y b, clorofila total y carotenoides). El tratamiento con NaCl provocó la disminución en los valores de acidez titulable, contenido de proteínas y prolina. No obstante, al ser suplementadas con calcio y tratadas con las mismas concentraciones salinas, se alivian los síntomas causados por tal estrés. Estos resultados indican que a una osmolaridad de 100 mmol.m-3 de NaCl, presente en medio radical, al ser suplementado con 10 mmol.m-3 de CaCl2 resulta propicio para el cultivo de sábila en una zona donde se hallen problemas de sales disueltas en el suelo.
Palabras clave: Calcio, Fijación de CO2, Plantas MAC, Prolina, Proteínas.
Abstract: To determine the effect of calcium on the physiology of Aloe vera subjected to two salinity levels (100 and 150 mmol m-3), the relative water content chlorenchyma (CRA), acidity, pigments, and proteins was determined proline (Pro) clorenquimática 25 young plants of this species. None of the saline treatments with or without addition of calcium (CaCl2+NaCl) showed statistically significant differences on variables such as CRA and pigments (chlorophyll a and b, the total chlorophyll and carotenoids). Treatment with NaCl caused a decrease in the values of acidity, protein and proline. However, when supplemented with calcium and treated with the same salt concentrations, such symptoms caused by stress are relieved. These results indicate that an osmolarity of 100 mmol m-3 NaCl, present in radical medium being supplemented with 10 mmol m-3 CaCl2 is suitable for growing aloe in an area where there are problems of dissolved salts in the soil.
Keywords: Calcium, CAM plants, CO2 fixation, Proline, Proteins.
Introducción
La salinidad es un factor que limita la productividad de los cultivos y la distribución de las plantas, en el caso de las glicófitas (plantas no resistentes a la sal). Los efectos negativos causados por este factor perjudican el crecimiento, la morfología y anatomía de la planta y, provoca también la disminución del contenido de agua, azúcares y minerales (Prat y Fathi 1990, Serrano et al. 1999).
Hasegawa y Bressan (2000) señalan que en ambientes salinos, algunas glicófitas evitan los efectos de las sales limitando la absorción de iones tanto en las raíces como en los tallos, mediante la biosíntesis de osmolitos (prolina, betaína, trealosa, polioles, entre otros) o controlando el flujo de agua y transporte de iones a través de la membrana y su compartimentalización, lo cual les permite mantener y/o restablecer la homeostasis iónica.
La sequía es otro factor que limita el crecimiento vegetal y esta es propia de los ambientes secos, pero también es ocasionada por el efecto osmótico de los iones, producto del exceso de sales en los suelos secos y costeros. No obstante, las plantas MAC (metabolismo ácido de las crasuláceas) son resistentes a la sequía, dado que su apertura estomática y fijación de CO2 ocurre durante la noche. En este tipo de metabolismo, el CO2 es incorporado a una molécula de tres átomos de carbono para formar malato durante la noche, este es almacenado en la vacuola de las células clorenquimáticas, acidificando el tejido progresivamente y, posteriormente, durante la mañana, el CO2 es liberado del malato haciendo que la acidez disminuya (Lüttge 2004). Todo esto le permite a las plantas con metabolismo MAC evitar la evapotranspiración durante el día, cuando las altas temperaturas podrían ocasionar la deshidratación. Por otra parte, la presencia de un gran hidroparénquima en la anatomía de la hoja, el cual acumula gran cantidad de agua, bien puede suplir los requerimientos hídricos de la planta cuando esta así lo necesite.
Aloe vera es una planta MAC documentada como una especie altamente resistente a la sequía, la misma no escapa a los efectos adversos de la salinidad (Franco-Salazar et al. 2012). García (2008) demostró que al cultivar a A. vera en varios niveles de salinidad (50, 100, 150, 200, 250, y 300 mmol m-3 de NaCl) dicha especie experimenta desbalance iónico: disminución en la absorción de K+ y aumento en la absorción del Na+, Cl-, Mg2+ y Ca2+. En concordancia, Franco-Salazar et al. (2012) demostraron que la absorción de iones esenciales disminuye ante el estrés salino.
Fisiológicamente, el calcio es un nutriente esencial para las plantas y como catión divalente, Ca2+, es requerido para roles estructurales en las paredes y membranas celulares. El calcio también juega un papel como mensajero secundario en concordancia con numerosos tipos de estrés ambientales (White y Broadley 2003). Fuentes-Carvajal et al. (2006) examinando el efecto de la deficiencia de Ca2+ sobre Aloe vera, lo señalan como un elemento que puede estar relacionado con la fotosíntesis y formación de nuevos tejidos, debido a la escasa formación y necrosis en hojas nuevas.
El Ca2+ alivia los efectos causados por el estrés salino, ya que disminuye la inhibición del crecimiento a nivel de la raíz y el vástago y mejora la absorción del K+ sobre el Na+ en la zona de crecimiento de la raíz, quizás como resultado de que el Ca2+ es esencial en la regulación del trasporte de K+ y Na+ en la membrana plasmática de las células (Epstein 1961, Rains y Epstein 1967, Lauchli y Grattan 2007). Shah et al. (1990) demostraron que la suplementación con Ca2+ tiende a mejorar la acumulación de prolina en callos de alfalfa (Medicago sativa) cultivados bajo salinidad. También, Colmer et al. (1996) sugieren que la acumulación de prolina en sorgo (Sorghum bicolor) está relacionada con el mantenimiento de una relación más favorable hacia K+ que al Na+ en los ápices radiculares de plantas tratadas con NaCl y adicionalmente suplementadas con Ca2+. Los mismos autores indican que la incapacidad de mantener una relación favorable entre K+ y Na+ puede inhibir las funciones enzimáticas, que a su vez puede inhibir la síntesis de prolina en los ápices radicales con un suministro menor de Ca2+. También se ha señalado que la aplicación del calcio tiene efectos benéficos en plantas cultivadas bajo estrés por sequía. En la especie Lonicera japonica, se demostró que la aplicación exógena de calcio mejoró la tasa fotosintética, evitó el daño a la estructura del cloroplasto e incrementó el contenido de clorofila (Li et al. 2012).
Aloe vera es una especie importante desde el punto de vista agrícola e industrial, cuyos productos (gel y acíbar) tienen propiedades farmacológicas, medicinales y cosméticas; sin embargo, la salinidad afecta adversamente su productividad. En vista de que se ha señalado al calcio como un elemento que alivia los efectos de la salinidad en vegetales, en el presente trabajo se indagó acerca de los efectos de la aplicación externa de Ca2+ en plantas de A. vera sometidas a estrés salino con la finalidad de comprobar si este mejora su adaptación a la salinidad como se ha observado en otros cultivos.
Material y métodos
Material vegetal, acondicionamiento y selección
Se colectaron 30 hijuelos (plantas jóvenes de origen asexual) de plantas adultas de Aloe vera (L.) Burm. f. (Asphodelaceae) en la localidad de Guayacán, península de Araya (10°36’34’’N y 64°07’18’’O), estado Sucre, Venezuela.
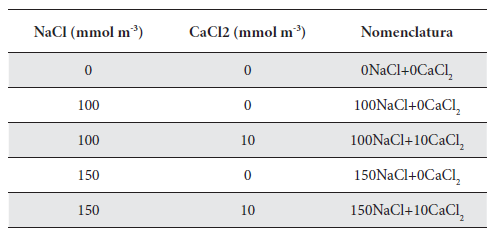
A los hijuelos se les eliminó los restos de tejidos secos, fueron desinfectados con hipoclorito de sodio al 1 % y lavados con agua de grifo. Posteriormente, se dejaron cicatrizar en sombra durante tres días, luego fueron sembrados en bolsas individuales que contenían arena de río, previamente lavada durante dos días, esterilizada en autoclave por 90 minutos y secada en la estufa a 80 ºC durante tres días, y regados con solución nutritiva para su enraizamiento y aclimatación. Se seleccionaron 25 hijuelos para el experimento, a los cuales se les regó diariamente con solución nutritiva Hoagland, según Ross (1974) durante dos meses. Luego de 15 días, se aplicaron los tratamientos (preparados en solución nutritiva) durante tres meses (Tabla 1). Las plantas se cultivaron bajo condiciones de vivero a temperatura ambiente (29 ºC).
Contenido relativo de agua
Al final del experimento se extrajeron secciones de la región media de una hoja basal. Las muestras fueron pesadas inmediatamente para determinar su biomasa fresca y seca. El contenido relativo de agua se determinó siguiendo la metodología de Ghoulam et al. (2002) y Franco-Salazar y Véliz (2007).
Ácidos orgánicos
Se utilizaron tres secciones de tejido previamente extraídas de una hoja basal cosechada a las 6:00 am para la determinación de ácidos orgánicos siguiendo la metodología descrita por Ball et al. (1991).
Pigmentos
Se obtuvieron tres discos de clorénquima de una hoja basal por cada tratamiento, y el contenido de pigmentos (clorofilas a, b, total y carotenoides) se determinó de acuerdo metodología descrita por Takemoto et al. (1988).
Proteínas y prolina
Se prepararon extractos a partir de 0,5 g de clorénquima y de raíces, macerándolos cada uno por separado. El contenido de proteínas se determinó usando el método de Lowry et al. (1951), empleando una curva estándar de suero albúmina bovina (0,25 Mg.mL-1).
Siguiendo el método descrito por Ghoulam et al. (2002), se determinó el contenido de prolina utilizando 0,6 mL del sobrenadante empleado para la determinación de proteínas.
Diseño experimental y análisis estadístico
Se realizó un diseño de bloques completos al azar, con cinco plantas por tratamiento y cinco tratamientos, para un total de 25 plantas. Los datos fueron analizados a través del programa StatGraphics Centurión XV mediante un análisis de varianza y las diferencias significativas entre tratamientos (en el caso de los ácidos orgánicos), fueron sometidos a la prueba a posteriori de Duncan para la separación de grupos (Sokal y Rohlf 1979).
Resultados y discusión
El contenido relativo de agua (CRA) del clorénquima de A. vera (Figura 1) no fue estadísticamente diferente entre tratamientos (Fs=0,99; p>0,05), evidenciando que todas las plantas, cultivadas o no con NaCl+CaCl2, mantuvieron un CRA similar entre tratamientos y superior al 80 %.
Los resultados indican que la adaptación anatómica, propia de las especies suculentas, como lo es un tejido interno voluminoso almacenador de agua o hidroparénquima rodeado por el tejido fotosintetizador o clorénquima, permitió que esta especie evitara la pérdida de agua de este último tejido tan fundamental para la realización de la fotosíntesis, al movilizarla y proporcionársela desde el hidroparénquima, como ha sido señalado para especies MAC, como Opuntia ficus-indica e Hylocereus undatus (Goldstein et al. 1991, Nobel 2006). De allí que se estime que la pérdida de agua propiciada por los tratamientos salinos quizás ocurrió sólo en el hidroparénquima para evitar la deshidratación del tejido fotosintético.
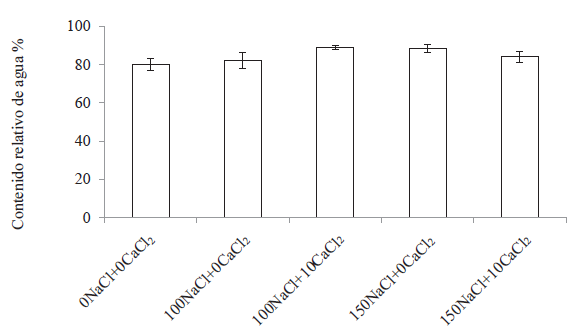
Figura 1.
Contenido relativo de agua clorenquimático de Aloe vera cultivada durante tres meses a diferentes concentraciones de NaCl+CaCl2. Los valores son los promedios ± EE (n=5).
Levent et al. (2007), en plantas de tomate, encontraron que al combinar 75 mmol.m-3 NaCl+5 mmol.m-3 CaCl2, el estrés salino impuesto disminuyó su efecto sobre el CRA. Asimismo, Nedjimi y Daoud (2009) demostraron en dos especies halófitas del género Atriplex cultivadas bajo 400 mmol.m-3 NaCl más 40 mmol.m-3 CaCl2, que los efectos de la salinidad sobre la misma variable son aliviados. En el presente estudio, más que la suplementación con calcio, pareciera que la anatomía suculenta de este tipo de plantas MAC le permitió en todos los tratamientos, hacer uso de algún mecanismo de movilización de agua (acumulación de prolina, por ejemplo) desde el tejido almacenador de agua para mantener hidratado el clorénquima, durante el tiempo que duró el estrés salino, evitando así el daño a las estructuras necesarias para la realización de la fotosíntesis.
La acidez titulable en A. vera, producto de la fijación nocturna de CO2, disminuyó (Fs=3,19; p=0,007) a medida que aumentó la salinidad, sin la adición de calcio (100NaCl+0CaCl2 y 150NaCl+0CaCl2), en comparación con el tratamiento 0NaCl+0CaCl2 (Figura 2). En plantas de sábila cultivadas con 100 mmol.m-3 NaCl y 10 mmol.m-3 CaCl2 (100NaCl+10CaCl2), la acidez titulable se incrementó con respecto al tratamiento correspondiente sólo con NaCl (100NaCl+0CaCl2), llegando a tener un valor cercano al tratamiento 0NaCl+0CaCl2. Para aquellas plantas tratadas con 150 mmol.m-3 NaCl, la suplementación con 10 mmol.m-3 de CaCl2 mejoró un poco el efecto del estrés salino, con respecto a aquel tratamiento donde sólo se aplicó 150NaCl+0CaCl2.
Se ha demostrado que los niveles de ácidos vacuolares durante el período nocturno, en plantas estresadas por sequía y/o salinidad, llegan a ser mayores (Hanscom y Ting 1978, Rayder y Ting 1981, Dodd et al. 2002, Pimienta et al. 2002, Franco-Salazar y Véliz 2008, Franco-Salazar et al. 2012). Sin embargo, en el presente estudio se evidenció que las plantas no estresadas (0NaCl+0CaCl2) y aquellas tratadas con 100NaCl+10CaCl2 fueron las que presentaron los mayores niveles de ácidos vacuolares (Figura 2); posiblemente en el resto de los tratamientos, donde resultó menor la acidez, pudo haber un cierre estomático nocturno más prolongado producto del estrés salino.
Iwasaki et al. (1992) describieron los canales de vacuolas de la planta MAC, Graptopetalum paraguayense, como canales tipo-SV que se abren a altas concentraciones de Ca2+, lo cual puede ser uno de los factores necesarios para la entrada de malato a la vacuola. Por otra parte, Schomburg (1994) midió los niveles de citrato, isocitrato, Ca2+ y Mg2+, además de los cambios diurnos/nocturnos del pH y los niveles de malato en la savia de Kalanchoe daigremontiana, y al calcular las concentraciones de Ca2+ libre, encontró que había una oscilación diurna/nocturna del Ca2+ y los mayores valores se obtuvieron al final de la fase oscura (mañana), cuando la acumulación de malato es máxima. El mismo autor asegura que el Ca2+ es capaz de unirse a los grupos cargados negativamente de proteínas y lípidos y disminuir la fluidez de la membrana, aunque esto puede cambiar diurnamente durante el ciclo MAC, en relación a los niveles cambiantes de Ca2+ unido a ácidos orgánicos y puede estar involucrado en la regulación de la activación entre la acumulación neta de ácido en la vacuola y su removilización (Kluge y Schomburg 1996), aunque no hay suficiente evidencia de tal mecanismo, cosa que parece estar alterada en las plantas tratadas con NaCl+CaCl2, por la menor acumulación de ácidos observada (Figura 2).
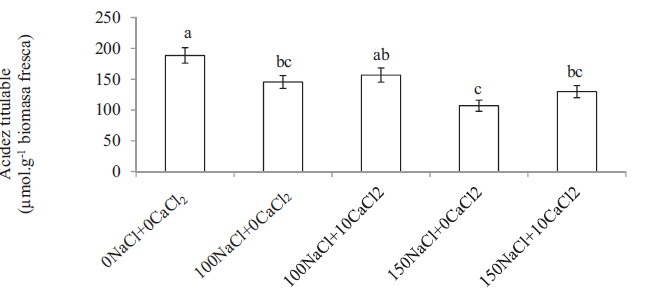
Figura 2.
Acidez titulable de Aloe vera cultivada durante tres meses a diferentes concentraciones de NaCl+CaCl2. Los valores son los promedios ± EE (n=5). Las letras sobre las barras indican diferencias entre tratamientos según Duncan.
El contenido de pigmentos (clorofilas y carotenoides) resultó estadísticamente igual entre tratamientos (p>0,05); evidenciando que las plantas protegieron el clorénquima y dichos pigmentos de los efectos de la salinidad (Figura 3). El déficit hídrico ocasionado por el NaCl no afectó el funcionamiento de una parte del aparato fotosintético, debido al posible movimiento de agua desde el hidroparénquima hacia el clorénquima (Goldstein et al. 1991, Nobel 2006) y al aumento en la concentración de prolina en dicho tejido como se verá más adelante.
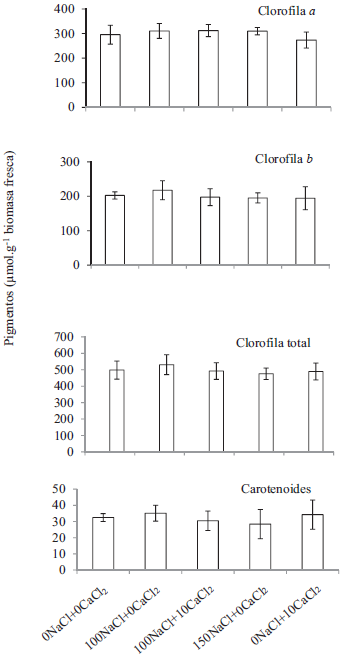
Figura 3.
Contenido de pigmentos (A-D) de Aloe vera cultivada durante tres meses a diferentes concentraciones de NaCl+CaCl2. Los valores son los promedios ± EE (n=5).
Contrario a los resultados obtenidos en la presente investigación, en plantas no suculentas como Phaseolus vulgaris, la salinidad redujo la síntesis y acumulación de clorofila, relacionándose esto con la inhibición de enzimas específicas responsables de la síntesis de estos pigmentos y con la destrucción de los mismos y/o cloroplastos (García et al. 1997). Sin embargo, al igual que en el presente estudio, Franco-Salazar y Véliz (2008) demostraron en la especie suculenta O. ficus-indica, cultivada hidropónicamente bajo salinidad (50, 100 y 150 mmol.m-3 NaCl), que el contenido de pigmentos no se vio afectado a causa del estrés salino. Esto evidencia que las plantas suculentas cultivadas a tales salinidades, entre ellas A. vera, pueden sobrellevar el estrés, posiblemente movilizando agua desde el hidroparénquima.
En la figura 4A y B, se observa que tanto en el clorénquima como en la raíz de A. vera, el contenido de proteínas (Fs=4,19; p=0,007 y Fs=3,58; p<0,001) fue mayor cuando las plantas fueron tratadas con NaCl, con o sin la adición de CaCl2, sugiriendo que en ellas se sintetizan nuevas proteínas para sobrellevar el estrés ocasionado por la sal. Para el caso de las proteínas del clorénquima (Figura 4A), se puede observar que el tratamiento 100NaCl+10CaCl2 propició un resultado superior al tratamiento control (0NaCl+0CaCl2), evidenciando los efectos positivos de la adición de 10 mmol.m-3 de CaCl2 para aliviar los efectos del NaCl en esta variable y en muchas de las mostradas anteriormente; mientras que bajo 150 mmol.m-3 NaCl, la suplementación con 10 mmol.m-3 de CaCl2 (150NaCl+10CaCl2) propició el mayor contenido de proteínas clorenquimáticas para sobrellevar dicho estrés salino (Figura 4A). Por su parte, a nivel radical todos los tratamientos salinos, con o sin cloruro de calcio, tuvieron contenidos parecidos entre tratamientos pero superior al de las plantas cultivadas con 0NaCl+0CaCl2 (Figura 4B).
Es posible que el aumento mostrado en la acumulación de proteínas ante la salinidad encontrado en Aloe vera, se relacione con la osmoprotección, de acuerdo a lo señalado por Franco-Salazar y Veliz (2007). Otros autores aseguran que ante el estrés salino o sequía, algunas plantas activan el metabolismo y la síntesis de proteínas (Ashraf 1989, García et al. 1997), para compensar las proteínas desnaturalizadas, mantener la integridad celular o reparar daños, sintetizando solutos osmoprotectores (García et al. 1997). En contraste, Lüttge et al. (1993) afirman que existen ciertas proteínas estimuladas por la salinidad, que desempeñan funciones enzimáticas relacionadas con la síntesis de prolina. García et al. (1997) plantean que algunas de estas proteínas son capaces de prevenir la entrada de los iones tóxicos a partes vulnerables de la planta o incrementar la excreción de los mismos.
Por su parte, el aumento en las concentraciones de proteínas obtenidas en el presente estudio (Figura 4A y 4B) lleva a inferir que el tratamiento salino, y particularmente la combinación del mismo con el aporte extra de calcio, induce de alguna manera, la síntesis de proteínas para sobrellevar o contrarrestar los efectos de la salinidad.
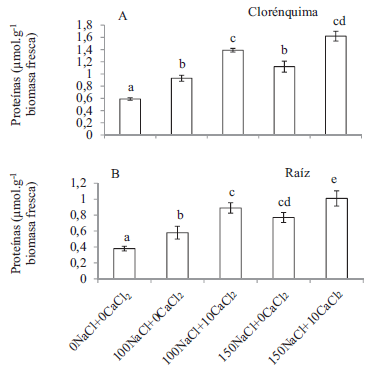
Figura 4.
Contenido de proteínas en clorénquima (A) y raíz (B) de Aloe vera cultivada durante tres meses a diferentes concentraciones de NaCl+CaCl2 (n=5)
En la figura 5 se observa que tanto en el clorénquima como en la raíz de A. vera, el contenido de prolina (Fs=5,78; p<0,001) fue mayor cuando las plantas fueron tratadas con NaCl, con o sin la adición de CaCl2, sugiriendo que estas sintetizan prolina para sobrellevar el estrés ocasionado por la sal. En cuanto a la prolina clorenquimática (Figura 5A), la adición de 10 mmol.m-3 de CaCl2 a plantas cultivadas con 150 mmol.m-3 NaCl conllevó a un mayor contenido de prolina; mientras que en las raíces, las plantas cultivadas con 100NaCl+10CaCl2, 150NaCl+0CaCl2 y 150NaCl+10CaCl2, fueron las que mostraron los mayores contenidos de dicho aminoácido (Figura 5B). Este aumento es aparentemente requerido para tolerar el estrés salino, ya que se ha señalado (Ashraf 1989, Lüttge et al. 1993, García et al. 1997, Franco-Salazar y Véliz 2007) que el estrés ocasiona en la planta el incremento del contenido de prolina u otros osmolitos orgánicos para aliviar dicho estrés y para realizar el ajuste osmótico.
Franco-Salazar y Véliz (2007) demostraron que un aumento de la salinidad (NaCl) en O. ficus-indica provoca un incremento en el contenido de prolina tanto en clorénquima como en hidroparénquima de cladodios basales y apicales y a nivel de las raíces, hecho que también ha sido comprobado en plantas con distintos metabolismos, como Vigna mungo, planta con metabolismo fotosintético C3 (Ashraf 1989) y en plantas con metabolismo fotosintético C4, como Sorghum bicolor (Colmer et al. 1996). De manera similar, en el presente estudio se produjo un incremento de la concentración de prolina en el clorénquima y en las raíces de A. vera ante el aumento de la salinidad en el medio radical (Figura 5).
Por otra parte, García y Medina (2009), en caña de azúcar cultivada bajo estrés salino y suplementada con CaCl2, reportaron que al adicionar Ca2+ se redujo de manera significativa la acumulación de prolina. Por lo contrario, Colmer et al. (1996) y Meloni (2012) en Sorghum bicolor y Prosopis ruscifolia, respectivamente, reportaron aumentos significativos en las concentraciones del soluto en cuestión a nivel foliar.
En concordancia con Colmer et al. (1996) y Meloni (2012), en el presente estudio, la acumulación de prolina clorenquimática fue mucho mayor (Figura 5A) en el tratamiento salino más alto al adicionarle 10 mmol.m-3 de CaCl2 (150NaCl+10CaCl2), pero en líneas generales todos los tratamientos salinos, con o sin la adición de CaCl2, propiciaron el aumento en el contenido de prolina (Figura 5A y 5B).
La prolina se la ha documentado como un soluto citoplasmático que compensa osmóticamente los iones secuestrados en la vacuola o a la osmolaridad externa (Poljakoff-Mayber et al. 1994) permitiendo, por ejemplo, el movimiento de agua desde el medio radical hasta el interior de las raíces, o desde el hidroparénquima hacia el clorénquima, hecho que puede tener implicaciones relevantes en lo alusivo al mantenimiento de la actividad metabólica del clorénquima en plantas MAC y al mantenimiento de la turgencia celular (Goldstein et al. 1991). Asimismo, se ha señalado que la prolina no contribuye al ajuste osmótico a nivel celular sino como un protector de enzimas y un estabilizador de estructuras, organelos y macromoléculas. También actúa como una reserva de energía y nitrógeno, para ser utilizada luego de la exposición a la salinidad (Meloni 2012), lo que explica tales incrementos en su concentración en el presente estudio.
Una de las propiedades atribuidas al calcio es la capacidad de contribuir al ajuste osmótico incrementando la acumulación de solutos osmocompatibles (García y Medina 2009, Meloni 2012). Por su parte, la acumulación de prolina en el clorénquima y raíces (Figura 5) se incrementó en los tratamientos salinos con respecto al tratamiento no salino, llegando a sus niveles más altos en el clorénquima al suplementar con CaCl2 plantas tratadas con 150 mmol.m-3 NaCl (Figura 5A), lo que confirma tal contribución del calcio en la producción de prolina para el ajuste osmótico.
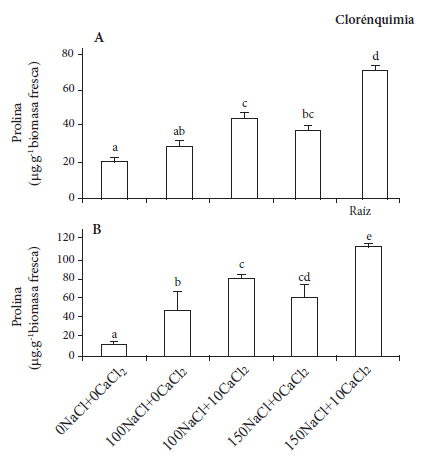
Figura 5.
Contenido de prolina en clorénquima (A) y raíz (B) de Aloe vera cultivada durante tres meses a diferentes concentraciones de NaCl+CaCl2 (n=5).
Conclusión
En general, el aumento de la salinidad (NaCl) afectó de manera negativa los parámetros bioquímicos-fisiológicos de A. vera; sin embargo, la suplementación con 10 mmol.m-3 CaCl2 al medio radical de plantas tratadas con 100 mmol.m-3 de NaCl, tuvo efectos posi-tivos sobre las variables estudiadas, aumentando, en muchos casos, los parámetros disminuidos por la salinidad.
Agradecimientos
El autor agradece a los miembros del laboratorio del laboratorio de Fisiología Vegetal, Universidad de Oriente, estado Sucre, José A. Véliz y Víctor A. Franco, a la profesora Sinatra Salazar del Instituto Oceanográfico de Venezuela y a la profesora Isabel Mimbela.
Referencias
Ashraf, M. 1989. The effect of NaCl on water relations, chlorophyll, and proline contents of two cultivars of blackgram (Vigna Mungo L.). Plant and Soil 119: 205-210.
Ball, E., J. Hann, M. Klug, H. Lee, U. Lüttge, B. Orthen, M. Popp, A. Schimitt e I. Ting. 1991. Ecophysiological comportment of tropical CAM tree Clusia in the field. New Physiology 117: 473-481.
Colmer, T., T. Fan, R. Higashi y A. Läuchli. 1996. Interactive effects of Ca2+ and NaCl salinity on the ionic relations and proline accumulation in the primary root tip of Sorghum bicolour.Physiologia Plantarum 97: 421-424.
Dodd, A., A. Borland, R. Hanslam, H. Griffiths y K. Maxwell. 2002. Crassulacean acid metabolism: plastic, fantastic. Journal of Experimental Botany 53 (369): 569-580.
Epstein, E. 1961. The essential role of calcium in selective cation transport by plant cells. Plant Physiology 36: 47-444.
Franco-Salazar, V. y J. Véliz. 2007. Respuestas de la tuna [Opuntia ficus-indica (L.) Mill.] al NaCl. Interciencia 32 (2): 125-130.
Franco-Salazar, V. y J. Véliz. 2008. Efectos de la salinidad sobre el crecimiento, acidez titulable y concentración de clorofila en Opuntia ficus-indica (L.) Mill. Saber 20 (1): 12-17.
Franco-Salazar, V., J. Véliz y L. Astudillo. 2012. Ecofisiología de Aloe vera (L.) Burm. f. en Guayacán, Península de Araya, estado Sucre, Venezuela. Interciencia 37 (6): 444-450.
Fuentes-Carvajal, A., J. Véliz y J. Imery. 2006. Efectos de la deficiencia de macronutrientes en el desarrollo vegetativo de Aloe vera. Interciencia 31 (2): 116-124.
García, O. 2008. Crecimiento y desarrollo de Aloe vera bajo diferentes condiciones de salinidad. Trabajo de grado. Universidad de Oriente, escuela de Ciencias, Departamento de Biología. Cumaná, 38 pp.
García, M. y E. Medina. 2009. Acumulación de iones y solutos orgánicos en dos genotipos de caña de azúcares estresados con sales simples o suplementadas con calcio. Bioagro 21: 3-14.
García, A., J. Engler, S. Lyer, T. Gerats, M. Van Montagu y A. Caplan. 1997. Effects of osmoprotectans upon NaCl stress in rice. Plant Physiology 115: 159-169.
Ghoulam, C., A. Foursy y K. Fares. 2002. Effects of salt stress on growth, inorganic ions and proline accumulation in relation to osmotic adjustment in five sugar beet cultivars. Environmental and Experimental Botany 47: 39-50.
Goldstein, G., J. Ortega, A. Nerd y P. Nobel. 1991. Diel patterns of water potencial components for the Crassulacean acid metabolism plant Opuntia ficus-indica when well-watared or droughted. Plant Physiology 95: 274-288.
Hasegawa, P. y R. Bressan. 2000. Plant cellular and molecular responses to high salinity. Annual Review of Plant Physiology 51: 463-499.
Hanscom, Z. y I. Ting. 1978. Responses of succulents to plant water stress. Plant Physiology 61: 327-330.
Iwasaki, I., H. Arata, H. Kijima y M. Nishimura. 1992. Two types of channels involved in the malate ion transport across the tonoplast of a crassulacean acid metabolism plant. Plant Physiology 98: 1492-1497.
Kluge, M. y M. Schomburg. 1996. The tonoplast as a target of temperature effects in Crassulacean acid metabolism. Pp: 72-77. En: Winter, K. y J. A. C. Smith. (Eds.). Crassulacean acid metabolism. Bioshemistry, ecophysiology and evolution. Ecological Studies, vol 114. Berlin, Heidelberg, New York: Spriger-Velarg.
Lauchli, A. y S. Grattan. 2007. Plant growth and development under salinity stress. Pp: 1-32. En: Matthew A., J., P. M. Hasegawa y J. S. Mohan (Eds.). Advances in Molecular Breedling Toward Drought and Salt Tolerant Crops. Springer. California. U.S.A.
Levent, A., K. Cengiz, A. Muhammad, A. Hakan, Y. Ibrahim y Y. Bulent. 2007. The effects of calcium sulphate on growth, membrane stability and nutrient uptake of tomato plants grown under salt stress. Environmental and Experimental Botany 59: 173-178.
Li, Q., J. Cao, L. Yu, M. Li, J. Liao y L. Gan. 2012. Effects on physiological characteristics of Honeysuckle (Lonicera japonica Thunb) and the role exogenous calcium under drought stress. Plant Omics Journal 5 (1): 1-5.
Lowry, O., N. Rosebrough, A. Farr y R. Randall. 1951. Protein measurement with the Folinphenol reagent. Journal Biological Chemistry 193: 265-275.
Lüttge, U. 2004. Ecophysiology of Crassulacean Acid Metabolism (CAM). Annals of Botany 93: 629-652.
Lüttge, U., M. Kluge y G. Bauer. 1993. Botánica. McGraw-Hill Interamericana. España. pp 523
Meloni, D. 2012. Respuestas fisiológicas a la suplementación con calcio de plántulas de vinal (Prosopisrus cifolia G.) estresadas con NaCl. Revista de la Facultad de Ciencias Agrarias UNcuyo 44 (2): 79-88.
Nedjimi, B. y Y. Daoud. 2009. Effects of calcium chloride on growth, membrane permeability and root hydraulic conductivity in two Atriplex species grown at higt (sodium chloride) salinity. Journal of Plant Nutrition 32: 1818-1830.
Nobel, P. 2006. Parenchyma-chlorenchyma water movement during drought for the hemiepiphytic cactus Hylocereus undatus. Annals of Botany 97: 469-474.
Pimienta, E., M. González y P. Nobel. 2002. Ecophysiology of a wild platyopuntia exposed to prolonged drougth. Enviromental and experimental Botany 47: 77-86.
Poljakoff-Mayber, A., G. Somers, E. Waker y J. Gallagher. 1994. Seeds of Kosteletz kyavirginica (Malvaceae): their structure, germination, and salt tolerance. II. Germination and salt tolerance. American Journal of Botany 81: 54-59.
Prat, D. y R. Fathi. 1990. Variation in organic and minerals components in young Eucaliptus seedlings under saline stress. Physiology Plantarum 79: 479-486.
Rains, D. y E. Epstein. 1967. Sodium absorption by barley roots: role of the dual mechanisms of alkali cation transport. Plan Physiology 42: 314-318.
Rayder, L. y I. Ting. 1981. Carbon metabolism in two species of Pereskia (Cactaceae). Plant Physiology 68: 139-142.
Ross, C. 1974. Plant Physiology laboratory manual. Wadsworth Publishing Company, Inc. Belmont, California. U.S.A. 200 pp.
Serrano, R., J. Mulet, G. Ríos, J. Márquez, I. de Larrinoa, M. Leube, I. Mendizabal, P. Ahuir, M. Proft, R. Ros y C. Montesinos. 1999. A glimpse of the mechanisms of ion homeostasis during salt stress. Journal of Experimental Botany 50: 1023-1036.
Schomburg, M. 1994. Untersu chugenuber das thermotrope Phasenver halten das tonoplastenbei der CAM Pflanze Kalanchoe daigremontiana. Dr. rer. nat. Thesis. Darmstadt: fachbereich Biologie, Thechnical University. 106 pp.
Shah, S., S. Wainwright y M. Merrett. 1990. The interaction of sodium and calcium chlorides and light on growth, potassium nutrition, and proline titulation in callus cultures of Medicago sativa L. New Phytologist 116: 37-45.
Sokal, R. y F. Rohlf. 1979. Principios y métodos estadísticos en la investigación biológica. H. Blume Ediciones. Madrid. España. Pp: 832.
Takemoto, B., A. Bytnerowicz y D. Olszyk. 1988. Depression of photosynthesis, growth, and yield in field-grown green pepper (Capsicum annum L.) exposed to acidic fog and ambient ozone. Plant Physiology 88: 477-482.
White, P. y M. Broadley. 2003. Calcium in plant. Annals of Botany 92: 487-511.
Información adicional
Citación del artículo: Pérez-Nasser, S. 2017. Efecto del CaCl2 sobre el contenido de proteínas, prolina, acidez titulable, clorofila y contenido relativo de agua de Aloe vera expuesta a salinidad por NaCl. Biota Colombiana 18 (1): 29–40. DOI: 10.21068/c2017.v18n01a2