Charophyta, Chlorophyta y Cryptophyta del embalse Riogrande II (Antioquia), Colombia
Charophyta, Chlorophyta and Cryptophyta in Riogrande II reservoir (Antioquia) Colombia
Charophyta, Chlorophyta y Cryptophyta del embalse Riogrande II (Antioquia), Colombia
Biota Colombiana, vol. 18, núm. 1, pp. 50-67, 2017
Instituto de Investigación de Recursos Biológicos "Alexander von Humboldt"
Recepción: 14 Marzo 2016
Aprobación: 22 Mayo 2017
Resumen: En muestras recolectadas mensualmente, entre agosto de 2011 y agosto de 2012, en el embalse Riogrande II (cuenca del río Grande, Antioquia, Colombia), se identificaron en total 29 géneros, 48 especies y una variedad taxonómica, pertenecientes a Charophyta, Chlorophyta y Cryptophyta. De las 48 especies, 18 especies y una variedad, son nuevos reportes para la ficoflórula colombiana. La división con mayor número de géneros fue Chlorophyta, sin embargo, Staurastrum (Charophyta) fue el género más diverso y de mayor contribución a la biomasa. Las diferencias entre las características descritas en la literatura y las observadas en los ejemplares, dificultaron la determinación taxonómica, lo cual plantea la necesidad de realizar estudios morfológicos detallados.
Palabras clave: Cuenca del río Grande, Embalse tropical, Ficoflora, Fitoplancton, Taxonomía.
Abstract: In monthly samples collected from August 2011 to August 2012 in the Riogrande II reservoir (Grande River drainage, Antioquia, Colombia). 29 genera, 48 species and one taxonomic variety belonging to Charophyta, Chlorophyta and Cryptophyta were identified. 18 species and one variety are new reports to the algal flora of Colombia. Chlorophyta was the Division with the largest number of genera and Staurastrum (Charophyta) the most diverse genus and also the largest contributer to biomass. Differences from the characteristics described in the literature and those observed in the specimens studied, made some taxonomic identification rather difficult, pointing out the need for careful and meticulous morphological studies before reaching taxonomical identifications.
Keywords: Grande River, Phycoflora, Phytoplankton South America, Taxonomy, Tropical reservoir.
Introducción
El estudio del fitoplancton de los embalses de Colombia se inició en la década de los 70 y desde entonces se han realizado aportes importantes a su conocimiento, especialmente en los embalses El Peñol-Guatapé (Uribe y Roldán 1975, Ramírez 1986, Ramírez et al. 2000 y Aguirre et al. 2007), La Fé (Ramírez y Machado 1982, Ramírez et al. 2005 y Ramírez et al. 2012), Betania (Duque y Donato 1988 y Ramírez y Guillot 2001), La Salvajina (Naundorf 1990 y Zamora-González et al., datos no publicados), Chisacá y La Regadera (Gaviria 1991 y León-López et al. 2012), San Lorenzo y Las Playas (Ramírez et al. 2000), El Guavio (Roldán et al. 2000), Neusa (Canosa y Pinilla 2007), Prado (Canosa y Pinilla 2007 y Reinoso-Florez y Villa, datos no publicados), Riogrande II (Loaiza-Restano et al. 2011, Meneses et al. 2011, Bustamante et al. 2012 y Ospina-Calle y Ramírez, datos no publicados), Chuza y San Rafael (León-López et al. 2012), Amaní (Roldán y López-Muñoz, datos no publicados) y Urrá (Duque y Rueda-Linares, datos no publicados).
La mayor parte de estos estudios enfatiza la dinámica del fitoplancton, su relación con las variables físicas, químicas y/o biológicas del agua y los aspectos ecológicos y sanitarios de las comunidades fitoplanctónicas. En algunas investigaciones, se realizaron ensayos sobre su ecología y sólo Duque y Donato (1988) se ocuparon de aspectos taxonómicos y registraron 110 taxones en el embalse Betania, de los cuales 16 fueron nuevos registros para la ficoflórula de Colombia. En Riogrande II, a partir de datos obtenidos entre julio de 2002 y julio de 2003, se ha estudiado la autoecología de Schroederia setigera (Meneses et al. 2011) y la de Ceratium furcoides (Bustamante et al. 2012), además de la ecología de cuatro especies de Staurastrum (Loaiza-Restano et al. 2011) y la sucesión del fitoplancton dominante (Ospina-Calle, datos no publicados).
Con este trabajo se participa en el incremento del conocimiento de la riqueza taxonómica fitoplanctónica colombiana y, en particular, la de los embalses, ambientes cada vez más abundantes en el territorio nacional.
Material y métodos
Descripción del área de estudio
El embalse Riogrande II está ubicado a 2150 m s.n.m., al noroccidente de Medellín (Antioquia, Colombia), en jurisdicción de los municipios de Don Matías, San Pedro, Belmira, Santa Rosa de Osos y Entrerrios, entre las coordenadas 75º32’-75º26’ W y 6º33’-6º28’ N. Tiene un volumen, hasta la cota de vertedero (2270 m s.n.m.) de 240 millones m3, una profundidad máxima de 50 m y un caudal aproximado de 35 m3 seg-1, en la captación. Capta las aguas de un área media de drenaje de 1214 ha, recibiendo, principalmente las aguas de los ríos Grande y Chico y de la quebrada Las Ánimas, cuenca del río Grande. El embalse fue construido para generación hidroeléctrica, abastecimiento de agua potable y para contribuir al saneamiento del río Medellín y en su área de influencia se desarrollan actividades agrícolas y ganaderas, con uso de agroquímicos.
Para recabar la información se seleccionaron cinco estaciones de muestreo (Figura 1) localizadas al ingreso (1) y al final (2) del brazo del río Chico, en la torre de captación (3), al final del brazo de la quebrada Las Ánimas (4) y al final del brazo del río Grande (5).
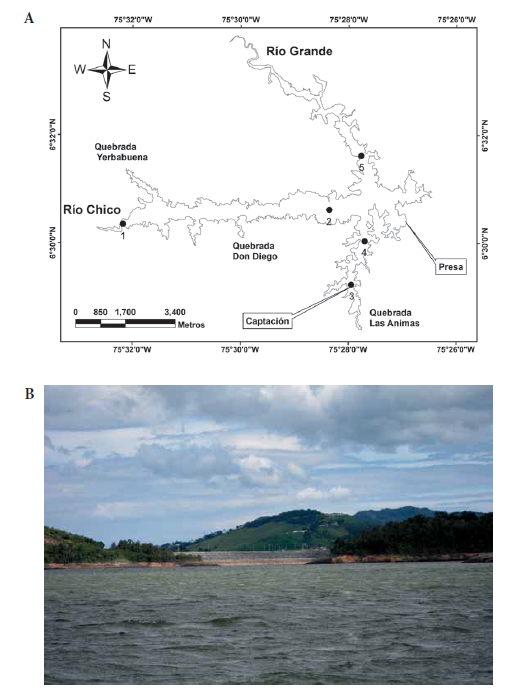
Figura 1.
A) Ubicación geográfica del embalse Riogrande II y localización de las estaciones de muestreo. B) Foto del embalse Riogrande II.
Muestreo
La recolección de muestras de fitoplancton para el análisis cualitativo se realizó mensualmente entre agosto de 2011 y agosto de 2012. La colecta se efectuó mediante arrastres horizontales superficiales de cinco minutos con red de plancton (malla de 30 μm de poro). Las muestras obtenidas fueron fijadas con una solución acuosa de formalina al 4 %. Para la cosecha cuantitativa (con la que se complementó el análisis cualitativo) se retiraron muestras de tres profundidades de la zona fótica las cuales se definieron a partir de los resultados de transparencia (Dsd): subsuperficie, 10 % (Dsd x 1,35) y 1 % (Dsd x 2,70) de irradiancia incidente, utilizando una botella van Dorn de cinco litros. El material colectado fue fijado con una solución de lugol acidificada con ácido acético.
Análisis de las muestras
Las muestras se observaron en un microscopio fotónico. La información de las características métricas se obtuvo mediante el uso de fotomicrografías y el programa de morfometría geométrica TPSdig2. La identificación y descripción taxonómica se realizó siguiendo el concepto de morfoespecie y utilizando, principalmente, las claves dicotómicas presentes en West et al. (1923), Uherkovich (1966), Teiling (1967), Fott (1969), Prescott et al. (1972, 1975, 1982), Hindák (1977, 1984, 1988), Ettl (1983), Komárek y Fott (1983), Sant’Anna (1984), Hegewald y Silva (1988), Comas (1996), Castro y Bicudo (2007) y Loaiza-Restano (2013). La clasificación taxonómica se basó en el sistema de Cavalier-Smith (1981) y la nomenclatura fue actualizada de acuerdo a la base de datos del listado mundial de algas Algaebase (www.algaebase.org).
El material se encuentra depositado en la colección del Laboratorio de Limnología Básica y Experimental y Biología y Taxonomía Marina de la Universidad de Antioquia, Colombia (CLUA).
Resultados
En total se identificaron 48 especies, de las cuales 13 correspondieron a variedades taxonómicas típicas de sus respectivas especies y cinco a variedades no típicas. La división Charophyta estuvo representada por 15 especies, Chlorophyta por 29 y una variedad y Cryptophyta por 4 especies.
Charophyta
Closterium acutum (Lyngb.) Brébisson ex Ralfs 1848 var. acutum (Figura 2a).
Célula 27,9-36,4 veces más larga que ancha, curvatura 40°-60°, ápice gradualmente atenuado. Dimensiones: 47,7-73,8 x 1,7-2,0 µm.
Comentarios: el largo celular de algunos de los ejemplares estuvo por debajo del límite inferior reportado por Prescott et al. (1975) para la especie (70 µm) y en general, el ancho celular fue menor al límite inferior de lo indicado en la descripción original (3 µm).
Closterium striolatum Ehrenberg var. subtruncatum (West et West) Krieger 1937 (Figura 2b).
Célula 20 veces más larga que ancha, curvatura 70°, ápice ligeramente engrosado; pared celular con delicadas estrías, bandas de cintura ausentes. Dimensiones: 465,1 x 23,5 µm.
Comentarios: el único ejemplar encontrado mostró una longitud levemente mayor al límite superior referenciado por Prescott et al. (1975) para la especie (453 µm).
Actinotaenium aff. cucurbita (Brébisson ex Ralfs) Teiling 1954dos (Figura 2c).
Célula 1,8 veces más larga que ancha; constricción media poco profunda; semicélulas ligeramente convexas, estrechándose hacia el ápice truncado; pared celular con puntos en líneas horizontales. Dimensiones: 28,98 x 16,31 µm.
Comentarios: no se observaron los cloroplastos.
Cosmarium contractum Delponte var. minutum (Delponte) West et West 1905 (Figura 2d).
Célula 1,6 veces más larga que ancha; constricción media muy profunda, seno medio ampliamente abierto; semicélulas circulares en vista frontal; cloroplasto axial con un pirenoide central y placas amplias radiadas. Dimensiones: 15,3 x 9,4 µm.
Cosmarium quadratulum (Gay) De Toni 1889 var. quadratulum f. quadratulum (Figura 2e).
Célula 1,8 veces más larga que ancha; constricción media bastante profunda, linear; cloroplastos axiales, con un pirenoide central cada uno; margen superior de la semicélula con una constricción mediana rasa. Dimensiones: 17,1 x 9,7 µm, istmo 5,4 µm.
Staurastrum americanum West et West 1905 var americanum f. americanum (Figura 2f).
Célula 1,1-1,5 veces más larga que ancha excluyendo procesos; constricción media moderada, seno medio formando una “U” ó “V”; semicélulas obsemicirculares, con el ápice algo convexo, liso; procesos con márgenes crenadas, 3-4-espinados en los extremos. Vista apical elíptica, 2-angular. Dimensiones: 21,1-28,6 x 15,0-20,3(24,0) µm (sin procesos); (45,2)49,0-71,1(75,7) x 35,1-56,3 µm (con procesos); istmo: 10,7-14,1(15,1) µm.
Comentarios: en general, las dimensiones sin procesos y el ancho celular con procesos son menores a las descritas en la literatura. Así mismo, el largo con procesos es menor en algunos ejemplares (29-31 x 26 µm sin procesos; 61-75 x 90 µm con procesos) (Prescott et al. 1982). Aunque según la descripción, los procesos son 3-espinados en los extremos, se observaron algunos ejemplares con cuatro espinas.
Staurastrum chaetoceras (Schröder) G.M. Smith 1924 var chaetoceras (Figura 2g).
Célula 1,2-1,8 veces más larga que ancha excluyendo procesos; constricción media superficial, seno medio formando una “U” ó “V”; semicélulas claramente 3-angulares, márgenes laterales divergentes, ápice recto en el sector medio; procesos divergentes, márgenes crenadas, series anulares de pequeñas espinas alrededor, 3-espinados en los extremos. Vista apical 3-angular. Dimensiones: 21,0-26,0(30,9) x (13,7)14,7-20,9 µm (sin procesos); (45,0)49,7-65,2 x (32,2)41,0-50,0(61,4) µm (con procesos); istmo: 7,8-11,0 µm.
Comentarios: aunque esta especie es 2-radiada, Brook (1958) ilustró una forma (facies) de tres radios (triradiata) que concuerda con el material analizado. En algunos ejemplares, el largo celular sin procesos está por encima del límite superior (22 µm) y/o el ancho sin procesos por debajo del límite inferior (19 µm). En general, la amplitud del istmo es superior (5,5-7,0 µm), al rango descrito (Prescott et al., 1982).
Staurastrum gracile Ralfs ex Ralfs 1848 var gracile (Figura 2h).
Célula 1,0-2,0 veces más larga que ancha excluyendo procesos; constricción media superficial, seno medio formando una “U” ó “V”; semicélulas ciatiformes, márgenes basales primero ligeramente convexas, después divergentes entre sí, ápice convexo a casi recto; procesos horizontalmente dirigidos a levemente divergentes, márgenes crenados, 4-7 series de gránulos alrededor, extremos 4-dentados; vista apical 3-angular. Dimensiones: (18,0)20,2-29,3 x (12,9)14,1-26,5 µm (sin procesos); (45,8)50,4-83,4(95,3) x 33,1-69,9(78,2) µm (con procesos); istmo: 7,8-14,9(15,2) µm.
Comentarios: las dimensiones de los ejemplares no coinciden con las registradas por Prescott et al. (1982), siendo menores el largo y el ancho celular sin procesos (32,0-36,0 x 25,0 µm) y en algunos individuos, mayor el istmo (8,0-10,0 µm).
Staurastrum muticum (Brébisson) Ralfs 1848 var. muticum f. muticum (Figura 2i).
Célula 1,1-1,5 veces más larga que ancha; constricción media profunda, seno medio abierto, ápice redondeado; semicélulas transversalmente elípticas a reniformes, margen ampliamente convexa. Vista apical 3-4-angular, márgenes cóncavas, ángulos ampliamente redondeados; pared celular lisa. Dimensiones: (19,2)21,5-28,7 x 16,9-23,0(24,3) µm.
Comentarios: los ejemplares presentaron un notable polimorfismo, especialmente en relación a la profundidad de la constricción media de las células, del seno medio y de los ángulos de las semicélulas.
Staurastrum paradoxum Meyen ex Ralfs 1848. (Figura 2j).
Célula 0,5-0,8 veces más larga que ancha excluyendo procesos; constricción media moderada, seno medio formando una “U” ó “V”; semicélulas ciatiformes, márgenes laterales poco convexas, lisas a moderadamente onduladas, ápice convexo a casi recto; procesos hacia arriba, márgenes crenadas, 5-7 series de gránulos alrededor, 3-4-dentados en los extremos. Vista apical 3-4-angular. Dimensiones: (20,4)22,3-29,0(30,9) x (31,4)34,1-46,5(54,6) µm (sin procesos); (49,0)61,7-81,4(93,9) x (37,2)44,1-70,6(78,2) µm (con procesos); istmo: (9,1)10,0-13,8(15,5) µm.
Staurastrum trifidum Nordstedt (1869) 1870 var. glabrum Lagerheim 1885 (Figura 2k).
Célula casi tan larga como ancha; constricción media moderada a profunda, seno medio formando una “U” ó “V”; semicélulas subcuneadas, márgenes laterales convexas, lisas, ápice convexo a casi recto, ángulos apicales truncados, con tres espinas dirigidas hacia la semicélula opuesta. Vista apical 3-angular. Dimensiones: 35,1-39,7 x 30,6-31,5 µm (sin espinas), 35,0-36,0 µm (con espinas); istmo: 15,3-15,5 µm.
Comentarios: en general, las dimensiones sin espinas son superiores a las descriptas por otros autores: 29 x 20,5-25 µm. (Prescott et al. 1982).
Staurastrum sp. (Figura 2l).
Célula 0,6-1,0 veces más larga que ancha excluyendo procesos; constricción media profunda, seno medio formando una “U” ó “V”; semicélula obtrapezoidal, con el ápice algo saliente, truncado, márgenes laterales suavemente convexas. Vista apical elíptica 2-angular, procesos con anillos paralelos de gránulos, ápice 4-espinado. Dimensiones: (19,2)22,5-28,6 x (12,6)15,0-22,0 µm sin procesos; 45,6-71,6(76,8) x 30,8-55,3(61,0) µm con procesos; istmo: (7,5)9,5-13,5(15,0) µm.
Comentarios: probablemente se trate de una especie nueva para la ciencia. Esta afirmación se debe a que son relativamente pocas las especies de Staurastrum con vista apical 2-angular y esta especie difiere de todas las descritas en la literatura en que las semicélulas son obtrapezoidales. Puede, hasta cierto punto, ser comparada con S. natator var. crassum West et West 1896; más es suficientemente diferente, ya que la pared de las semicélulas es lisa, sin ningún tipo de decoración. S. natator var. crassum tiene la pared de las semicélulas extremadamente prominente y decorada con un círculo de gránulos diminutos que envuelven otros tres en el centro.
La confirmación dependerá de la ratificación de las características diagnósticas en un número mayor de individuos.
Staurodesmus cuspidatus (Brébisson) Teiling 1967 (Figura 2m).
Célula 0,6-1,2 veces más larga que ancha; semicélulas 3-angulares, base más o menos alargada, formando un istmo cilíndrico, margen apical angular, ligeramente cóncava y superficie apical inflada a ligeramente convexa; espinas paralelas, convergentes o divergentes. Dimensiones: (12,9)15,3-23,7 x 16,9-21,4(23,1) µm; istmo: (5,3)7,0-9,4 µm.
Comentarios: la mayoría de los ejemplares presentaron una longitud menor al límite inferior (22 µm) descrito (Teiling 1967).
Gonatozygon pilosum Wolle 1882 (Figura 2n).
Célula cilíndrica, 13 veces más larga que ancha, ápice truncado y levemente dilatado; pared densamente cubierta por pequeñas espinas rectas, como pelos; varios pirenoides (5 a 6) por cloroplasto. Dimensiones: 100,9 x 7,9 µm.
Elakatothrix gelatinosa Wille 1898 (Figura 2o).
Colonia mucilaginosa elipsoidal; células fusiformes; multiplicación por división transversal de las células en diagonal una frente a otra; cloroplasto único parietal con un pirenoide. Dimensiones: (8,3)10,6-22,1 x (1,9)2,5-4,9 µm.
Comentarios: en algunos ejemplares observados tanto el largo como el ancho celular estuvieron por debajo de los límites inferiores (9 µm y 4 µm, respectivamente) mencionados por otros autores (Ferragut et al. 2005, Fernandes y Bicudo 2009).

Figura 2.
Charophyta: a) Closterium acutum; b) C. striolatum; c) Actinotaenium aff. cucurbita; d) Cosmarium contractum; e) C quadratulum var. quadratulum f. quadratulum; f) Staurastrum americanum var americanum f. americanum; g) S. chaetoceras var chaetoceras; h) S. gracile var gracile; i) S. muticum var. muticum f. muticum; j) S. paradoxum; k) S. trifidum var. glabrum; l) Staurastrum sp.; m) Staurodesmus cuspidatus; n) Gonatozygum pilosum; o) Elakatothrix gelatinosa.
Chlorophyta
Chlamydomonas microsphaera Pascher et Jahoda 1928 (Figura 3a).
Células ampliamente ovadas a esféricas; polo anterior con papila, a veces poco diferenciada; pared celular gruesa; cloroplasto poculiforme con un pirenoide basal; flagelos cerca del doble de la longitud de la célula. Dimensiones: 7,1-9,7(10,4) µm diámetro.
Comentarios: aunque se trata de una especie de hábito solitario, se encontraron algunas agrupaciones de cuatro células, que posiblemente correspondan a la formación de células-hijas que permanecen temporalmente en el interior de la pared de la célula.
Chlamydomonas microsphaerella Pascher et Jahoda 1928 (Figura 3b).
Células esféricas, sin papila; pared celular de espesura variada; cloroplasto poculiforme con un pirenoide basal, dos vacuolas pulsátiles apicales; flagelos cerca del doble de la longitud de la célula. Dimensiones: 5,0-11,3(13,6) µm diámetro.
Comentarios: según Ettl (1983), la pared celular es delgada; sin embargo, en algunos ejemplares se observó una pared gruesa. Para algunos individuos se ampliaron los límites del diámetro citados en la literatura (6,0-8,0 µm). Pese a ser una especie de hábito solitario, se encontraron algunas agrupaciones de 2, 4, 8 células, que posiblemente corresponden a la formación de células-hijas que permanecen temporalmente en el interior de la pared de la célula madre.
Chlamydomonas praecox Pascher 1943 (Figura 3c).
Células esféricas; polo anterior con una papila, a los lados de la cual emergen los flagelos; pared celular gruesa; cloroplasto poculiforme hasta casi en forma de “U”, un pirenoide basal. Dimensiones: 17,0 µm diámetro.
Comentarios: se amplía el límite inferior (18 µm) del diámetro reportado por Ettl (1983).
Gonium cf. octonarium Pocock 1955 (Figura 3d).
Cenobio hexagonal; ocho células de diferentes dimensiones, 2 pequeñas centrales y 6 más grandes periféricas, muy juntas, aplanadas; cloroplasto poculiforme con un pirenoide. Dimensiones: diámetro celular de las células periféricas 3,3-7,2 µm.
Comentarios: en general, el ancho celular fue menor (9,0 µm) al reportado por Ettl (1983)
Gonium pectorale O. F. Müller 1773 (Figura 3e).
Cenobio elipsoidal a esférico; de 8, a 32 células, dispuestas casi ⅓ parte centralmente y las demás periféricamente, separadas a juntas, casi esféricas; flagelos 2 a más veces el diámetro celular; estigma fuerte; cloroplasto poculiforme con un pirenoide basal. Dimensiones: diámetro celular (4,6)5,0-12,6 µm.
Comentarios: se encontraron algunos ejemplares con impregnaciones de sales de hierro en la pared.
Phythelios viridis Frenzel 1891 (Figura 3f).
Células aisladas, esféricas; pared celular con setas, uniformemente distribuidas y de tamaño similar en cada célula; cloroplasto poculiforme. Dimensiones: 12,1-14,6(17,3) µm diámetro; setas 2,0-32,1 µm longitud.
Comentarios: en algunos ejemplares se observaron dimensiones mayores a las referidas en la literatura (Sant’Anna 1984): diámetro celular: 14 µm y setas largo: hasta 25 µm. Numerosos autores refieren esta especie como Golenkinia viridis (Frenzel) Printz; sin embargo, este epíteto específico está actualmente aceptado para P. viridis. Además, entre los géneros Golenkinia y Phythelios, la única diferencia morfológica es la presencia de pirenoide en el primero de ellos, y debido a que no observaron estas estructuras en los ejemplares colectados, se optó por el género Phythelios.
Monoraphidium tortile (West y West) Komárková-Legnerová 1969 (Figura 3g).
Células elongado-fusiformes, 5,2-12,0 veces más largas que anchas, rectas a levemente sigmoides; polos puntiagudos; cloroplasto parietal sin pirenoide. Dimensiones: (8,6)11,0-28,2(35,9) x 1,2-3,9(5,0) µm.
Comentarios: algunos ejemplares con dimensiones superiores (30 µm-3,6 µm), a las registradas por otros autores (Komárková-Legnerová 1969, Komárek y Fott 1983 y Comas 1996).
Ankyra judayi (G.M. Smith) Fott 1957 (Figura 3h).
Células elongado-fusiformes, 5,0-11,0 veces más largas que anchas, rectas a levemente curvadas; extremo basal bifurcado; cloroplasto parietal con pirenoide. Dimensiones: (16,9)21,0-33,4(37,8) x 3,0-3,7(5,3) µm.
Comentarios: algunos ejemplares mostraron una longitud inferior al límite menor referido en la literatura (Komárek y Fott 1983, Hindák 1988, Comas 1996).
Monactinus simplex (Meyen) Corda var. sturmii (Reinsch) Pérez, Maidana et Comas 2009 (Figura 3i).
Cenobio circular de 16 células, ordenadas concéntricamente, las marginales con la base truncada, márgenes convexas y un proceso apical fino que se proyecta hacia el exterior, las internas con las márgenes levemente convexas a casi rectas. Dimensiones: células: 9,9-12,9 x 8,1-10,2 µm.
Pseudopediastrum boryanum (Turpin) E. Hegewald 2005 (Figura 3j).
Cenobio aplanado, redondeado, de ocho células, no perforado o con diminutos espacios intercelulares; células poligonales, bilobadas, con dos proyecciones cortas, truncadas en los extremos, con un pirenoide; pared celular granulosa. Dimensiones: células 6,2-8,3 x 5,1-6,2 µm.
Comentarios: la fuerte impregnación de sales de hierro en la pared celular, impidió la observación de características diagnósticas para reconocer variedades. El largo celular algo menor que el citado para las diferentes variedades (6,5 µm) y en general, el ancho celular (mínimo 6,8 µm) fue menor al descrito (Comas 1996, Loaiza-Restano 2013).
Eutetramorus globosus Walton 1918 (Figura 3k).
Colonias generalmente esféricas, eventualmente irregulares, compuestas por (2-)4-8(-16) células y a veces por algunas subcolonias, envoltura mucilaginosa incolora, bien diferenciada; células esféricas, reunidas o principalmente dispuestas en anillo en la periferia del mucílago; cloroplasto poculiforme con un pirenoide. Dimensiones: diámetro celular: (3,7)4,2-11,9 µm.
Comentarios: algunos ejemplares presentaron un diámetro menor al descrito (5 µm) en Komárek y Fott (1983). En varias colonias se observaron impregnaciones de sales de hierro en la pared celular.
Coelastrum microporum Hantzsch in Rabenhorst 1866 var. microporum (Figura 3l).
Cenobio esférico; ocho células esféricas, unidas lateralmente por la pared. Dimensiones: diámetro celular: 4,9-8,5 µm.
Comentarios: se encontraron ejemplares con impregnaciones de sales de hierro en la pared.
Coelastrum microporum Hantzsch in Rabenhorst 1866 var. octaedricum (Skuja) Sodomkova 1972 (Figura 3m).
Se diferencia de la variedad tipo de la especie porque el cenobio es octaédrico y por el mayor tamaño de las células. Dimensiones: diámetro celular: 9,3-11,1 µm diámetro.
Comentarios: impregnaciones de sales de hierro en la pared.
Desmodesmus opoliensis (P.G. Richter) E. Hegewald var. mononensis (Chodat) E. Hegewald 2000 (Figura 3n).
Cenobios de cuatro células alineadas; células más o menos elipsoidales, unidas por casi toda la longitud celular, las interiores con ambas caras casi rectas y las marginales arqueadas a convexas en sus caras externas; cuatro espinas en los polos de las células marginales; cloroplasto parietal con un pirenoide. Dimensiones: (11,5)12,5-17,3(19,2) x (3,3)4,4-6,6(7,3) µm; espinas: 6,0-14,2 µm longitud.
Desmodesmus perforatus (Lemmermann) E. Hegewald 2000 var. perforatus (Figura 3o).
Cenobios de cuatro células alineadas; células más o menos cilíndricas, las interiores con ambas caras levemente cóncavas y las marginales levemente convexas en sus caras externas; polos celulares poco engrosados, tocándose uno con otro, formando espacios intercelulares; espinas en los polos de las células marginales; cloroplasto parietal con un pirenoide. Dimensiones: 9,9-12,9 x 2,2-3,2 µm; espinas hasta 12,9 µm longitud; espacios intercelulares: 0,6-1,2 µm ancho.
Comentarios: ejemplares con ancho celular e intercelular menor a los referidos en la literatura: 3 µm y 2,5 µm, respectivamente (Uherkovich 1966, Komárek y Fott 1983, Sant’Anna 1984, Hegewald y Silva 1988, Comas 1996).
Scenedesmus ellipticus Corda 1835 (Figura 3p).
Cenobios de cuatro células alineadas; células más o menos cilíndricas, con la cara interna levemente cóncava, las interiores de mayor longitud y las marginales levemente convexas en sus caras externas; polos celulares redondeados, tocándose uno con otro, formando espacios intercelulares; cloroplasto parietal con un pirenoide. Dimensiones: 5,2-11,7 x 1,3-3,6 µm; espacios intercelulares 1,1-1,2 µm ancho.
Comentarios: algunos de los ejemplares mostraron dimensiones menores a los límites inferiores referidos en Godinho et al. (2010) y Ramos et al. (2015): largo 7,5 µm, ancho 2,5 µm.
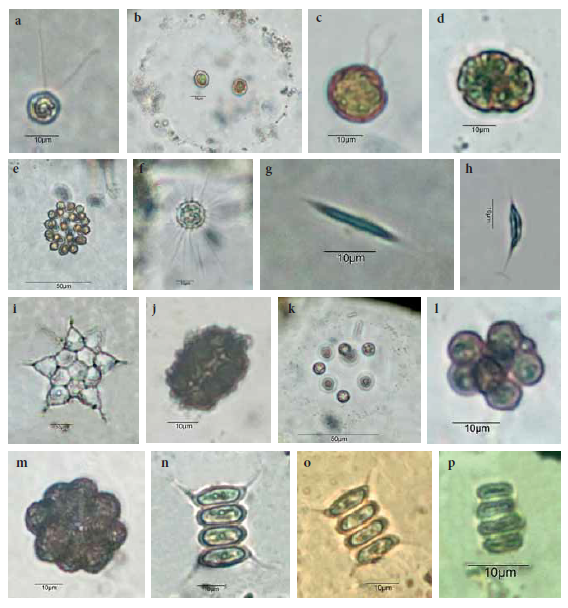
Figura 3.
Chlorophyta: a) Chlamydomonas microsphaera; b) C. microsphaerella; c) C. praecox; d) Gonium cf. octonarium; e) G. pectorale; f) Phythelios viridis; g) Monoraphidium tortile; h) Ankyra judayi; i) Monactinus simplex var. sturmii; j) Pseudopediastrum boryanum; k) Eutetramorus globosus; l) Coelastrummicroporum var. microporum; m) C. microporum var. octaedricum; n) Desmodesmus opoliensis var. mononensis;o) D. perforatus var. perforatus; p) Scenedesmus ellipticus.
Scenedesmus ecornis (Ehrenberg) Chodat 1926 (Figura 4a).
Cenobio de cuatro células alineadas; células oblongas, las marginales arqueadas, marcadamente convexas en sus caras externas; polos celulares redondeados; cloroplasto parietal con un pirenoide. Dimensiones: 8,5-9,0 x 2,5-3,2 µm.
Tetrastrum komarekii Hindák 1977 (Figura 4b).
Cenobio aplanado, más o menos cuadrado; cuatro células 3-angulares a trapezoides, caras externas convexas; pared celular lisa; cloroplasto parietal, sin pirenoide. Dimensiones: célula 7,7-13,6 x 4,7-11,5 µm.
Comentarios: todos los individuos se observaron con impregnación de sales de hierro en la pared.
Chlorolobion braunii (Nägeli) Komárek 1979 (Figura 4c).
Células fusiformes, 3,4-5,8 veces más largas que anchas, rectas a levemente curvadas; polos puntiagudos a redondeados; cloroplasto parietal con un pirenoide. Dimensiones: (9,9)12,4-28,0(30,1) x (2,1)2,6-5,8 µm.
Comentarios: según Heynig y Krienitz (1982) y Krienitz et al. (2011) la mayoría de las especies de este género, y en particular esta especie, pertenecen al género Monoraphidium, por lo que frecuentemente se encuentra en la literatura como Monoraphidium braunii (Nägeli) Komárková-Legnerová 1969. Sin embargo, en la base de datos mundial Algaebase aparece como nombre aceptado C. braunii y M. braunii como sinónimo holotípico.
Eudorina elegans Ehrenberg 1831 (Figura 4d).
Cenobio elipsoidal a casi esférico; (8)32(64) células en coronas regulares, ubicadas a intervalos aproximadamente iguales, perpendicularmente al eje longitudinal del cenobio; células esféricas, más o menos iguales; pared celular sin papilas; cloroplasto poculiforme con uno a varios pirenoides; un estigma, dos vacuolas pulsátiles apicales.Dimensiones: diámetro celular: 5,4-15,7(19,1) µm.
Comentarios: aunque según la descripción de Ettl (1983), el número mínimo de células en el cenobio es de 16, entre los ejemplares observados se encontraron cenobios de ocho células. La mayoría de los cenobios con células de un diámetro menor al descripto (12 µm). Algunos de los individuos encontrados con impregnaciones de sales de hierro en la pared.
Eudorina unicocca G. M. Smith 1931 (Figura 4e).
Cenobio elipsoidal, ovoide-elipsoidal a casi esférico, mínimo 64 células en coronas regulares; células esféricas a ligeramente ampuliformes, las de la corona anterior levemente menores; cloroplasto poculiforme, un pirenoide basal; estigma claramente diferenciado en las células más superficiales. Dimensiones: diámetro celular: (4,1)6,1-10,0 µm.
Comentarios: según Ettl (1983), el máximo de células en el cenobio es de 32, pero todos los ejemplares observados tenían entre 64 y alrededor de 128 células, lo que podría deberse a estados reproductivos en los que los autocenobios no se han separado del cenobio madre. Algunos de los cenobios mostraron células de un diámetro menor al descrito (5,5 µm). Algunos ejemplares se encontraron con impregnaciones de sales de hierro en la pared.
Parachlorella kessleri (Fott et Nováková) Krienitz, E.H. Hegewald, Hepperle, V. Huss, T. Rohr et M. Wolf 2004 (Figura 4f).
Células esféricas, aisladas o eventualmente en pequeños agregados; pared celular delgada; cloroplasto ocupa casi totalmente la célula dejando pequeña abertura, un pirenoide. Dimensiones: 7,5-9,3 µm diámetro.
Chlorella vulgaris Beijerinck 1890 var. vulgaris (Figura 4g).
Células esféricas, aisladas; pared celular delgada; cloroplasto acopado que ocupa ¾ de la célula, con un pirenoide. Dimensiones: 7,6-9,7 µm diámetro.
Mucidosphaerium pulchellum (Wood) C. Bock, Proschold et Krienitz 2011 (Figura 4h).
Colonias esféricas a ovoides, formadas por hasta 35 grupos de cuatro células ovales a elípticas, unidas por hilos de mucílago; cloroplasto poculiforme con un pirenoide. Dimensiones: diámetro celular: 2,1-5,6 µm diámetro.
Comentarios: se amplían los límites de las dimensiones referidas en la literatura (Komárek y Fott 1983, Sant’Anna 1984, Comas 1996), diámetro celular: desde 2,5 µm.
Nephrocytium allantoideum Bohlin 1897 (Figura 4i).
Colonias hialinas de 2-8 células; células 2-4 veces más largas que anchas, más o menos cilíndricas, marcadamente arqueadas; extremos con polos redondeados; cloroplasto parietal con un pirenoide. Dimensiones: (9,6)10,3-19,1 x (2,8)3,3-6,0(7,1) µm.
Comentarios: numerosos ejemplares presentaron una menor longitud que la reportada por Komárek y Fott (1983) y por Comas (1996) y en algunos, las células fueron más anchas que el límite superior establecido para la especie (5 µm).
Nephrocytium perseverans Printz 1914 (Figura 4j).
Colonias de 2-8 células; células 1-3 veces más largas que anchas, ovales a reniformes; extremos con polos ampliamente redondeados; cloroplasto parietal con un pirenoide. Dimensiones: (5,9)8,1-13,7(15,0) x (4,4)5,2-8,4(9,5) µm.
Comentarios: para algunos ejemplares se ampliaron los límites de las dimensiones celulares referidas en Komárek y Fott (1983) para la especie (8,4-14 x 2-8,3 µm).
Oocystis lacustris Chodat 1897 (Figura 4k).
Células aisladas o formando colonias de 2-16 células, a veces diferentes generaciones con envolturas individuales bien delimitadas; células irregularmente distribuidas en un mucílago que puede o no tener engrosamientos polares, células elípticas a ovales, polos aguzados a redondeados, con o sin nódulos polares; 1-4 cloroplastos parietales, con o sin pirenoide. Dimensiones: células (5,3)6,1-13,7(14,7) x (3,0)4,0-8,0(10,6) µm.
Comentarios: debido a que la única diferencia descrita entre esta especie y O. parva West et West es la forma de liberación de las autosporas (Fott 1969,Komárek y Fott 1983, Comas 1996), a que no fue posible observar esta característica, y que según Stoyneva et al. (2007)O. parva es sinónimo de O. lacustris, se decidió incluir a todos los ejemplares encontrados dentro de esta especie.
Oocystis solitaria Wittrock in Wittrock y Nordstedt 1879 (Figura 4l).
Células aisladas, elípticas a ovales, polos redondeados con engrosamientos polares; numerosos cloroplastos poligonales con un pirenoide. Dimensiones: 12,3-13,2 x 7,6-8,6 µm.
Selenoderma malmeana K. Bohlin 1897 (Figura 4m).
Colonias de hasta 200 células; células anchas, semilunares, arciformes, lados cóncavo y convexo formando arcos de lados regulares, contorno irregular; cloroplasto parietal con un pirenoide. Dimensiones: diámetro celular (4,0)5,0-9,0(10,9) µm.
Botryococcus braunii Kützing 1849 (Figura 4n).
Colonias globosas, compuestas por densas agregaciones de grupos de cuatro células elípticas, unidas por hilos de mucílago; envoltura mucilaginosa de coloración oscura, envolviendo casi completamente las células, dejando libre el extremo redondeado. Dimensiones: células 3,5-7,2 x 2,3-5,3 µm.
Comentarios: en algunos ejemplares las dimensiones celulares fueron algo menores a las descritas en la literatura: largo: 5,7µm y ancho: 2,5 µm. (Komárek y Fott 1983, Sant’Anna 1984).
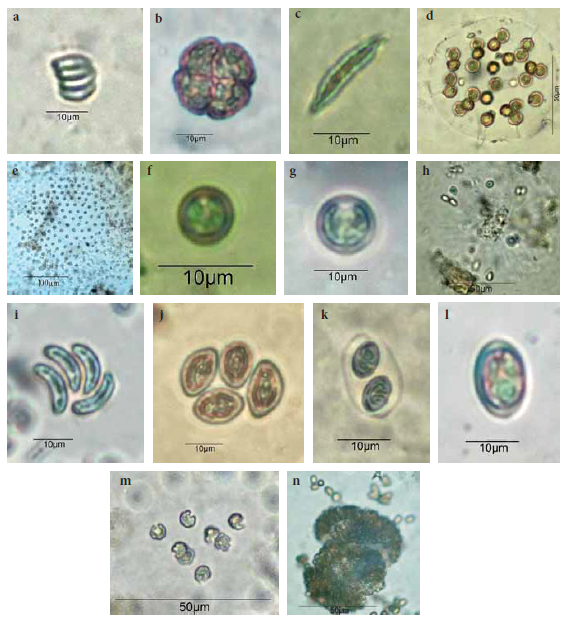
Figura 4.
Chlorophyta: a) Scenedesmus ecornis; b) Tetrastrum komarekii; c) Chlorolobion braunii (o Monoraphidium braunii); d) Eudorina elegans; e) E. unicocca; f) Parachlorella kessleri; g) Chlorella vulgaris; h) Mucidosphaerium pulchellum var. pulchellum; i) Nephrocytium allantoideum; j) N. perseverans; k) Oocystis lacustris; l) O. solitaria; m) Selenoderma malmeana; n) Botryococcus braunii.
Cryptophyta
Cryptomonas erosa Ehrenberg 1838 var. erosa (Figura 5a).
Célula elíptica, 1,2-2,1 veces más larga que ancha, obovada a ovada; polo anterior oblicuamente truncado, porción dorsal formando o no rostro evidente; polo posterior redondeado-afilado; dos cromoplastos dorsiventrales, pirenoides ausentes; citofaringe casi siempre evidente; corpúsculos de Maupa, normalmente presentes; dos flagelos subapicales, diferente tamaño. Dimensiones: (12,4)14,1-23,7 x (7,4)8,5-15,9(17,8) µm.
Comentarios: se amplió el límite inferior del largo celular (13 µm) reportado en la literatura (Castro y Bicudo 2007).
Cryptomonas marssonii Skuja 1948 (Figura 5b).
Célula de contorno subsigmoide, 1,2-2,2 veces más larga que ancha; polo anterior oblicuamente truncado, porción dorsal formando o no rostro evidente; polo posterior afilado, agudo, volteado hacia la face dorsal; dos cromoplastos laterales, pirenoides ausentes; citofaringe poco a muy evidente; corpúsculos de Maupa, a veces presentes; dos flagelos subapicales, tamaño similar. Dimensiones: (9,1)12,2-22,1(25,1) x 7,7-12,5(14,6) µm.
Comentarios: se amplió el límite inferior del largo (15 µm) y/o el límite superior del ancho celular (12 µm), según las dimensiones referidas en la literatura (Castro y Bicudo 2007).
Cryptomonas phaseolus Skuja 1948 (Figura 5c).
Célula oblonga a obovada, 1,3-1,8 veces más larga que ancha; polo anterior oblicuamente truncado, sin rostro; polo posterior redondeado; dos cromoplastos laterales, sin pirenoides; citofaringe evidente; corpúsculos de Maupa, a veces presentes; dos flagelos subapicales, tamaño similar. Dimensiones: 13,0-25,3 x 10,0-17,5 µm.
Comentarios: se ampliaron los límites superiores del largo (23 µm) y del ancho (13 µm) reportados por Castro y Bicudo (2007).
Goniomonas truncata (Fresenius) Stein 1878 var. truncata (Figura 5d).
Célula ovada, 1,4-2,5 veces más larga que ancha; polo anterior oblicuamente truncado, porción dorsal formando rostro evidente; polo posterior redondeado; dos flagelos subapicales, poco distintos entre sí. Dimensiones: 7,3-20,3 x (3,8)4,3-9,0(10,2) µm.
Comentarios: la mayoría de los ejemplares presentó un largo celular por debajo del límite inferior referido para la especie (12,2)15 µm (Castro y Bicudo 2007).
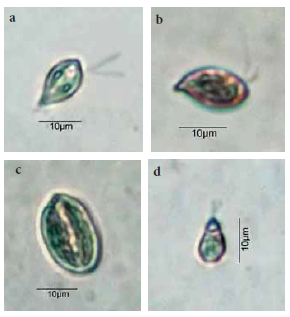
Figura 5.
Cryptophyta: a) Cryptomonas erosa var. erosa; b) C. marssonii; c) C. phaseolus; d) Goniomonas truncata var. truncata.
Discusión y conclusiones
Un alto porcentaje (51 %) de las especies encontradas presentó diferencias leves con las dimensiones reportadas en la literatura. Así mismo, en algunas especies (4 %) se evidenciaron pequeñas variaciones con las características morfológicas referenciadas y un 6 % de las especies mostró claras diferencias en las dimensiones y en las características morfológicas. A pesar de ello, la evidencia reunida se consideró insuficiente para proponer otras categorías taxonómicas.
La causa más plausible de las diferencias registradas es el hecho de que todas ellas fueron identificadas sobre el material fijado, bien fuera con formalina o lugol acidificado. No obstante, es necesario aclarar que según Daufresne et al. (2009), una de las respuestas del fitoplancton al calentamiento global en los ecosistemas acuáticos, además de los cambios en la distribución de las especies y la fenología, es la disminución en el tamaño.
En algunas de las especies más abundantes como Stauratrum paradoxum, S. muticum var. muticum f. muticum, Cryptomonas erosa, Oocystis lacustris y Selenoderma malmeana, las diferencias morfológicas observadas, complicaron la determinación taxonó-mica. En el caso de S. paradoxum, S. chaetoceras var chaetoceras, S. gracile var gracile, Elakatothrix gelatinosa, O. lacustris y S. malmeana, la falta de uniformidad en la presentación de las descripciones y en las ilustraciones de las características diacríticas entre los autores, dificulta aún más la determinación.
Entre las especies encontradas, las de mayor frecuencia (>0,80) fueron Staurastrum paradoxum, S. gracile var. gracile, S. muticum var. muticum f. muticum, Oocystis lacustris, Monoraphidium tortile, Parachlorella kessleri, Chlorolobion braunii (o Monoraphidium braunii), Cryptomonas erosa var. erosa, C. marsonii,Selenoderma malmeana y Staurodesmus cuspidatus, siendo entre ellas S. paradoxum la de mayor aporte a la biomasa fitoplanctónica.
Cosmarium quadratulum var. quadratulum f. quadratulum, Staurastrum americanum var. americanum f. americanum y S. trifidum var. glabrum de las Charophyta, Chlamydomonasmicrosphaera, C. microsphaerella, C. praecox, Parachlorella kessleri, Chlorolobion braunii (o Monoraphidium braunii), Desmodesmus perforatus var. perforatus, Eutetramorusglobosus, Gonium pectorale, Nephrocytium perseverans, Phythelios viridis, Scenedesmus ellipticus, Selenoderma malmeana y Monactinus simplex var. sturmii de las Chlorophyta y Cryptomonas erosa var. erosa, C. phaseolus y Goniomonas truncata var. truncata de las Cryptophyta, constituyen nuevos reportes para la ficoflórula colombiana.
Agradecimientos
Los autores agradecen a las Empresas Públicas de Medellín, por el financiamiento del programa de investigación “Estudio de las condiciones ambientales de tres embalses de Empresas Públicas de Medellín para la gestión integral y adecuada del recurso hídrico”, del cual hace parte el presente estudio, a Liliana Marcela Ospina Calle por la valiosa ayuda en la estimación de las características métricas de los ejemplares y a los evaluadores anónimos por las correcciones y observaciones al texto, las cuales mejoraron sustancialmente el artículo.
Referencias
Aguirre, N., J. Palacio y J. Ramírez. 2007. Características limnológicas del embalse El Peñol-Guatapé, Colombia. Revista de Ingenierías Universidad de Medellín 6 (10): 53-66.
Brook, A. J. 1958. Desmids from the plankton of some Irish loughs. Proceeding of the Royal Irish Academy 59B (6): 71-91.
Bustamante-Gil, C., J. J. Ramírez-Restrepo, A. Boltovskoy y A. Vallejo. 2012. Spatial and temporal change characterization of Ceratium furcoides in the equatorial reservoir Riogrande II, Colombia. Acta Limnologica Brasiliensia 24 (2): 207-219.
Canosa, A. y G. Pinilla. 2007. Relaciones entre las abundancias del bacterioplancton y del fitoplancton en tres ecosistemas lénticos de los Andes Colombianos. Revista de Biología Tropical 55 (1): 135-146.
Castro, A. A. J. y C. E. M. Bicudo. 2007. Flora ficológica do Estado de São Paulo. Cryptophyceae. Rima, FAPESP. São Paulo. 121 pp.
Comas, A. 1996. Las Chlorococcales duliacuícolas de Cuba. Bibliotheca Phycologia Band 99. Cramer, Stuttgart. 192 pp.
Daufresne, M., K. Lengfellner y U. Sommer. 2009. Global warming benefits the small in aquatic ecosystems. Proceding of the National Academy of Sciences 106: 12788-12793.
Duque, S. y J. Ch. Donato. 1988. Estudio del fitoplancton durante las primeras etapas de llenado del embalse de la Central Hidroeléctrica de Betania, Huila, Colombia. Revista Facultad de Ciencias, Universidad Javeriana 1 (2): 29-52. Disponible en: http://revistas.javeriana.edu.co/index.php/scientarium/article/view/5090/3930
Ettl, H. 1983. Chlorophyta I. Phyomonadina. Pp. 14 – 807. En: Ettl, H., J. Gerloff, H. Heynig, D. Mollenhauer (Eds.) SüBwasserflora von Mitteleuropa. Gustav Fischer Verlag. Stuttgart. New York.
Fernandes S, C. E. M. Bicudo. 2009. Criptógamos do Parque Estadual das Fontes do Ipiranga, São Paulo, SP. Algas, 26: Chlorophyceae (famílias Chlorococcaceae e Coccomyxaceae). Hoehnea 36 (1): 173-191.
Fott, B. 1969. Studies in Phycology. E. Schweizerbart’sche Verlagsbuchhandlung, Stuttgart. 304 pp.
Gaviria, S. 1991. Monitoreo de embalses del sistema de acueducto de Bogotá. Revista Acodal 147: 29-47.
Godinho, L. R., A. A. Comas y C. E. M. Bicudo. 2010. Criptógamos do Parque Estadual das Fontes do Ipiranga, São Paulo, SP. Algas, 30: Chlorophyceae (família Scenedesmaceae). Hoehnea 37 (3): 513-553.
Hegewald, E. y P. C. Silva. 1988. Annotated catalogue of Scenedesmus and nomenclaturally related genera, including original descriptions and figures. Bibliotheca Phycologica Band 80. Cramer, Stuttgart. 587 pp.
Heynig, H. y L. Krienitz. 1982. Monoraphidium negledum n. sp. sowie einige Bemerkungen zu den Gattungen Monoraphidium, Chlorolobion und Keratococcus (Chlorococcales). Archiv für Protistenkunde 125 (1): 335-344.
Hindák, F. 1977. Studies on the chlorococcal algae (Chlorophycea). I. Biologické Práce. Bratislava. 190 pp.
Hindák, F. 1984. Studies on the chlorococcal algae (Chlorophycea). III. Biologické Práce. Bratislava. 308 pp.
Hindák, F. 1988. Studies on the chlorococcal algae (Chlorophycea). V. Biologické Práce. Bratislava. 225 pp.
Komárek, J. y B. Fott. 1983. Das Phytoplankton des SüBwassers. E. Schweizerbart’sche Verlagsbuchhandlung. Stuttgart. 1044 pp.
Komárková-Legnerová, J. 1969. The systematics and ontogenesis of the genera Ankistrodesmus Corda and Monoraphidium gen. nov. Pp. 75-144. En: Fott, B. (Ed.) Studies in Phycology. Stuttgart: Schweizerbart’sche.
Krienitz, L., C. Bock, H. Nozaki y M. Wolf. 2011. SSU rRNA gene phylogeny of morphospecies affiliated to the bioassay alga “Selenastrum capricornutum” recovered the polyphyletic origin of crescent-shaped Chlorophyta. Journal of Phycology 47: 880–893.
León-López, N., C. A. Rivera-Rondón, A. Zapata, J. Jiménez, W. Villamil, G. Arenas, C. Rincón y T. Sánchez. 2012. Factors controlling phytoplankton in tropical high-mountain drinking-water reservoirs. Limnetica 31 (2): 305-322.
Loaiza-Restano, A. M. 2013. Família Hydrodictyaceae (Sphaeropleales, Chlorophyceae) no Estado de São Paulo: levantamento florístico. Dissertação de Mestrado. Instituto de Botânica da Secretaria de Estado do Meio Ambiente. São Paulo. 164 pp.
Loaiza-Restano, A. M., J. J. Ramírez, R. O. Echenique, A. Vallejo y L. Y. Ortiz. 2011. Dinámica espacio-temporal de cuatro especies de Staurastrum (Meyen 1829, emend. Ralfs 1848) en un embalse eutrófico colombiano. Oecologia Australis 15 (3): 726-746.
Mazo-B., D., J. J. Ramírez, A. Díaz-C. 2015. Caracterización física y química del embalse Riogrande II (Antioquia), Colombia. Actualidades Biológicas 37 (103): 155-168.
Meneses, V., A. Vergara, J. J. Ramírez, H. Palacio. 2011. Estudio autoecológico de Schroederia setigera en un embalse ecuatorial. Boletín de la Sociedad Argentina de Botánica 46 (2): 96.
Naundorf, G. 1990. Caracterización de la comunidad fitoplanctónica y determinación de la productividad primaria del embalse “La Salvajina” y su área de influencia. Revista Asociación Colombiana de Ciencias Biológicas 4: 154-163.
Prescott, G. W., H. T. Croasdale y W. C. Vinyard. 1972. North American Flora. The New York Botanical Garden. 84 pp.
Prescott, G. W., H. T. Croasdale y W. C. Vinyard. 1975. A Synopsis of North American Desmids. Part II. Desmidiaceae: Placodermae. Section 1. University of Nebraska Press.USA. 275 pp.
Prescott, G. W., H. T. Croasdale, W. C. Vinyard y C. E. M. Bicudo. 1982. A Synopsis of North American Desmids. Part II. Desmidiaceae: Placodermae. Section 4. University of Nebraska Press.USA. 700 pp.
Ramírez, J. J. 1986. Fitoplancton de red en el embalse de El Peñol. Actualidades Biológicas 15 (56): 2-13.
Ramírez, J. J., C. E. M, Bicudo, G. Roldán y L. C. García. 2000. Temporal and vertical variations in phytoplankton community structure and its relation to some morphometric parameters of four Colombian reservoirs. Caldasia 22 (1): 108-126.
Ramírez, J. J., R. González-Ballesteros y F. L. Gutiérrez. 2012. Establecimiento del nutriente limitante con base en los cambios de la estructura del ensamblaje fitoplanctónico en un embalse tropical colombiano. Caldasia 34 (2): 421-441.
Ramírez, M. y G. Guillot. 2001. Variaciones espaciales y temporales de la abundancia y diversidad del fitoplancton del embalse tropical de Betania, Huila-Colombia: 237-251. En: Alveal y Antezana (Eds). Sustentabilidad de la biodiversidad, un problema actual. Bases Científico-Técnicas. Teorizaciones y Proyecciones. Universidad de Concepción, Chile.
Ramírez, J. J., F. Gutierrez y A. Vargas. 2005. Respuesta de la comunidad fitoplanctónica a experimentos de eutrofización artificial realizados en la represa La Fe, El Retiro, Antioquia, Colombia. Caldasia 27 (1):103-115.
Ramírez, J. J. y T. Machado. 1982. Influencia de la precipitación y los ortofosfatos en el fitoplancton de la represa La Fe. Actualidades Biológicas 11 (39): 3-21.
Ramos, G. J. P, C. E. M. Bicudo y C. W. do N. Moura. 2015. Scenedesmaceae (Chlorophyta, Chlorophyceae) de duas áreas do Pantanal dos Marimbus (Baiano e Remanso), Chapada Diamantina, Estado da Bahia, Brasil. Hoehnea 42 (3): 549-566.
Roldán, G., A. Bohórquez, R. Cataño y J. Ardila. 2000. Estudio limnológico del embalse del Guavio (Colombia). Revista de la Academia Colombiana de Ciencias 24 (90): 73-84.
Sant’Anna, C. L. 1984. Chlorococcales (Chlorophyceae) do Estado de Sao Paulo, Brasil. Bibliotheca Phycologica Band 67. Cramer, Vaduz. 348 pp.
Stoyneva, M. P., C. Cocquit, G. Gärtner y W. Vyverman. 2007. Oocystis lacustris Chod. (Chlorophyta, Trebouxiophyceae) in Lake Tanganyika (Africa). Linzer Biologische Beiträge 39 (1): 571-632.
Teiling, E. 1967. The desmid genus Staurodesmus. A taxonomic study. Arkiv För Botanik, Serie 2, Band 6, nr 11. Almqvist y Wiksell. Stockholm. 629 pp.
Uherkovich, G. 1966. Die Scenedesmus-Arten Ungarns. Akadémia Kiadó, Budapest. 173 pp.
Uribe, A. y G. Roldán. 1975. Estudio comparativo de algunas características físicoquimicas y biológicas del embalse El Peñol. Actualidades Biológicas 4: 2-12.
West, W., G. S. West y N. Carter. 1923. A Monograph of the British Desmidiaceae. Vol. 5. The Ray Society. London. 299 pp.
Información adicional
Citación del artículo: López-Muñoz, M, T., C. E. De Mattos-Bicudo, R. O. Echenique, J. J. Ramírez-Restrepo y J. A. Palacio. 2017. Charophyta, Chlorophyta y Cryptophyta del embalse Riogrande II (Antioquia) Colombia. Biota Colombiana 18 (1): 50–67. DOI: 10.21068/c2017.v18n01a4