Chinches patinadoras marinas (Hemiptera: Heteroptera: Gerromorpha): diversidad de los hábitats oceánicos del Neotrópico
Marine water striders (Hemiptera: Heteroptera: Gerromorpha): diversity of ocean habitats in the Neotropics
Chinches patinadoras marinas (Hemiptera: Heteroptera: Gerromorpha): diversidad de los hábitats oceánicos del Neotrópico
Biota Colombiana, vol. 18, núm. 1, pp. 172-191, 2017
Instituto de Investigación de Recursos Biológicos "Alexander von Humboldt"
Recepción: 22 Junio 2016
Aprobación: 16 Marzo 2017
Resumen: Las chinches acuáticas del infraorden Gerromorpha son especies adaptadas a caminar o patinar sobre la película superficial del agua principalmente en ambientes de agua dulce, sin embargo, algunas especies se han adaptado a vivir en ambiente marinos y actualmente no se cuenta con un inventario de la riqueza y composición de la fauna de chinches patinadoras marinas para el Neotrópico. A partir de la revisión bibliográfica, de los especímenes depositados en colecciones entomológicas y expediciones en campo, se obtuvieron los registros de chinches asociadas a ambientes marinos. A cada registro se les asignó una categoría de hábitat (estuarios/manglares, lagunas formadas por arrecifes de coral, guarida de cangrejo en manglar, charcas formadas por las mareas, mar cerca de la costa, ambientes pelágicos) y su distribución geográfica actualizada. Se registran 203 especies a nivel mundial de Gerromorpha en ambientes asociados a ecosistemas marinos. Para el Neotrópico se registraron cinco familias, 13 géneros y 48 especies que representan el 23 % de las especies a nivel mundial. En orden de riqueza de especies la familia Gerridae tuvo la mayor con 22 especies distribuidas en tres géneros, seguida de Veliidae con 17 especies de cinco géneros, Mesoveliidae con seis especies y tres géneros, Hermatobatidae con dos especies y un género, y por último Hebridae con un género y una especie.
Palabras clave: Gerridae, Hermatobatidae, Mesoveliidae, Veliidae, Hebridae.
Abstract: The water strider of infraorder Gerromorpha are species adapted to walk or skate on the water surface film in freshwater environments. However some have adapted to live in marine environments and currently there is no census of the species richness or faunal composition of sea skaters for the Neotropics. Records were obtained from the bibliographical review, specimens deposited in entomological collections and expeditions. A habitat category (estuaries / manglars, coral reef lagoons, mangrove crab holes, ponds formed by the tides, sea near the coast, pelagic environments), and current geographic distribution was assigned to each species. There are 203 species of Gerrormorpha worldwide in environments associated with marine ecosystems. In the Neotropical region, a total of five families, 13 genera and 48 species were recorded, representing 23% of species worldwide. The family Gerridae had the greatest species richness with 22 species distributed in three genera, followed by Veliidae with 17 species in five genera, Mesoveliidae with six species and three genera, Hermatobatidae with two species and one genus and finally Hebridae with one genus and one species.
Keywords: Gerridae, Hermatobatidae, Mesoveliidae, Veliidae, Hebridae.
Introducción
Actualmente, cerca de las tres cuartas partes de las especies descritas de animales vivientes, son insectos (Clapham et al. 2016). De esta alta riqueza de especies, se estima que solo el 1 %, aproximadamente 1,400 especies, utilizan las zonas marinas como hábitat preferencial en alguna parte o todas sus etapas de desarrollo (Cheng 1976, Ruxton y Humphries 2008). Según Camus y Barahona (2002), cerca de 20 órdenes tienen especies que viven expuestos al mar o en condiciones oceánicas; entre ellos están los órdenes Coleoptera, Diptera, Hemiptera y Trichoptera como los mejores representados. A pesar de estas cifras, varios autores coinciden en que los insectos son comunes en muchos hábitats cercanos a la costa y pueden ser bastante abundantes en los manglares y los arrecifes de coral (Andersen 1982, Cheng y Mathis 2003, Andersen y Cheng 2004).
Las chinches acuáticas del infraorden Gerromorpha (Hemiptera: Heteroptera), repre-sentadas por 2,100 especies, distribuidas en todos los continentes, exceptuando la Antártica (Moreira 2015), son insectos adaptados a caminar sobre la película superficial del agua, donde pasan casi todo el período activo de su vida. La mayoría de las especies de gerromorfos, viven en ambientes lénticos y lóticos de agua dulce, pero algunas especies habitan el océano abierto (Andersen 1998) como por ejemplo especies representantes de Halobates Eschscholtz, 1822 (Andersen y Cheng 2004, Ferrú y Sielfeld 2010, Ikawa et al. 2012) y otras en las aguas salobres estuarinas (Cheng 1976), por ejemplo especies del Rheumatobates Bergroth, 1892 (Polhemus y Manzano 1992).
Desde los trabajos pioneros de Hadden (1931), Henry (1932) y Herring (1958, 1961), así como los de Polhemus (1975, 1991), Andersen y Weir (1999), Andersen (1999) y Cheng (1976, 2006) con chinches marinas, se han descrito más de 180 especies, distribuidas principalmente en cinco familias: Hebridae, Hermatobatidae, Mesoveliidae, Gerridae y Veliidae. De estas especies solo cinco (Halobates micans, H. germanus, H. sericeus, H. splendens, H. sobrinus) son estrictamente oceánicas y se distribuyen ampliamente en los océanos Pacifico, Atlántico e Índico (Andersen y Cheng 2004, Sekimoto et al. 2013). La familia con mayor número de especies de hábitos marinos es Gerridae, con aproximadamente 80 especies (Cheng 2006), las cuales según su distribución espacial en el hábitat se pueden dividir en dos grupos: especies de hábitats costeros y especies de los océanos, cada uno con sus propias necesidades alimentarias, de comportamientos y con particulares adaptaciones ambientales (Andersen y Cheng 2004); como presencia de bosques de manglar, estuarios, entrada de agua dulce al mar, temporalidad de mareas, disponibilidad de refugios.
Actualmente, la atención de las investigaciones que en el campo taxonómico, biológico, comportamental, evolutivo, genético y como indicadores de calidad de agua (Moreira 2015), se han hecho sobre las chinches patinadoras, se han centrado hacia los taxones que ocupan los ambientes dulciacuícolas, lo que ha dejado de lado a una fracción importante de especies que se especializaron en los ambientes marinos. Para la región Neotropical en este grupo de especies se cuenta con las contribuciones de Polhemus y Manzano (1992), quienes realizaron una lista de Heterópteros marinos del Pacífico tropical oriental, que incluyó especies de las familias Gelastocoridae, Gerridae, Mesoveliidae, Saldidae y Veliidae, además, presentaron una clave de indentificación, mapas de distribución y la descripción de siete nuevas especies. Aunque se encuentra un gran número de publicaciones que han abordado aspectos taxonómicos y de diversidad de las chinches marinas, actualmente no se cuenta con un censo de la riqueza y composición de estas chinches en el Neotrópico.
Dada esta falta de información, el objetivo de esta investigación es recopilar datos de diversas fuentes y presentar la lista actualizada de los géneros y especies de Heteroptera (Gerromorpha) que tienen relación directa con ambientes marinos, con especial énfasis en el Neotrópico, dando los datos sobre su distribución geográfica y su preferencia de hábitat.
Material y métodos
La investigación se hizo a partir de tres fuentes de información: 1. Revisión bibliográfica, principalmente las contribuciones de Andersen (1989, 1998, 1999); Andersen y Cheng (2004); Andersen y Polhemus (1980); Andersen y Weir (1999); Cheng (1976); Polhemus (1975); Polhemus y Cheng (1982); Polhemus y Manzano (1992); Polhemus y Polhemus (2012). 2. Revisión de especímenes de colecciones. Se revisaron los ejemplares depositados en las siguientes colecciones entomológicas: Colección Entomológica de la Universidad del Magdalena, Santa Marta-Colombia (CEUM); Colección Nacional de Insectos, Instituto de Biología, Universidad Nacional Autónoma de México, México. D.F. (CNIN); Instituto de Ciencias Naturales, Museo de Historia Natural, Colección de Entomología, Universidad Nacional de Colombia, Bogotá-Colombia (ICN); Laboratorio de Entomología, Universidad del Quindío, Armenia-Colombia (CIBUQ); Colección de Entomología Acuática, Museo de Zoología, Escuela de Biología, Universidad de Costa Rica, San José-Costa Rica (MZUCR) y el Laboratorio de Entomología, Museo de Historia Natural “Luis Gonzalo Andrade” Tunja-Colombia (UPTC). 3. Por último, se realizaron salidas de campo en las siguientes localidades: Golfo de Urabá (Antioquia), Islas de San Bernardo (Bolivar), San Andrés y Providencia, Santa Marta (Magdalena), Nuquí (Chocó), Bahía Solano (Chocó). Los métodos de recolecta utilizados en ambientes marinos fueron: redes entomológicas acuáticas y red de plancton, donde se hicieron barridos en la película superficial del agua, y se utilizaron aspiradores bucales. En cada uno de los ambientes se buscó que todos los microhabitats propuestos por Andersen (1999) quedaran representados.
A cada especie se le asignó una categoría de hábitat de acuerdo con la clasificación propuesta por Andersen (1999): estuarios/manglares, lagunas formadas por arrecifes de coral, guarida de cangrejo en manglar, charcas formadas por las mareas, mar cerca de la costa, ambientes pelágicos y también su distribución geográfica detallada. De acuerdo a las observaciones y recolecciones en los diferentes muestreos, se adicionan a las categorías de hábitat propuestas por Andersen (op. cit.), las charcas formadas por mareas cercanas a la costa y guaridas de cangrejo en manglar.
Resultados y discusión
A nivel mundial se obtuvieron registros de 203 especies, 25 géneros y cinco familias de Gerromorpha estrechamente relacionadas con los hábitats marinos (Anexo 1). Para la familia Gerridae se registran tres subfamilias, diez géneros y 89 especies; Veliidae cuatro subfamilias, nueve géneros y 91 especies; Mesoveliidae cuatro géneros y 11 especies; Hebridae un género y tres especies y Hermatobatidae con un género y nueve especies. Los resultados encontrados complementan los expuestos por Andersen (1999) quien registró 182 especies, distribuidas en 25 géneros y cinco familias, dado que en los últimos 16 años se han descrito cerca de 21 especies principalmente de los géneros Rheumatobates y Halobates (Andersen y Cheng 2004, Castro-Vargas y Morales-Castaño 2011).
Para la región Neotropical se registraron cinco familias, 13 géneros y 48 especies asociadas a ecosistemas marinos, que representan el 23 % de las especies de los gerromorpha marinos a nivel mundial. De las especies registradas para la región se encontraron 46 endémicas, lo cual incrementa en un 30 % lo registrado por Andersen (1999). Para la familia Gerridae se registraron tres subfamilias, tres géneros y 22 especies; Veliidae cuatro subfamilias, cinco géneros y 17 especies; Mesoveliidae tres géneros y cinco especies, Hermatobatidae: un género, dos especies y Hebridae un género y una especie (Anexo 2). El género Rheumatobates (Figura 1a) presentó el mayor número de especies, de acuerdo con Westlake et al. (2000); este género tiene cerca de la mitad de las especies descritas en cuerpos de agua dulce en hábitats lenticos o de remanso (Molano-Rendón et al. 2008), es así como las especies asociadas a ecosistemas marinos como manglares y estuarios ofrecen un hábitat similar a las lagunas continentales, bordeadas de vegetación y en muchas ocasiones con poco movimiento de agua. Le sigue Rhagovelia Mayr, 1865 (Veliidae) (Figura 1c) que estuvo representado por ocho especies (Anexo 2), como cabe esperar ya que este género comprende un grupo de insectos común y diverso en las regiones tropicales (Floriano y Moreira 2015).

Figura 1.
Representantes de chinches patinadoras marinas de la región Neotropical. A. Halobates micans (Gerridae). B. Rheumatobates bergrothi (Gerridae). C. Husseyella turmalis (Veliidae). D. Rhagovelia colombianus (Veliidae).
Distribución de las especies por tipo de hábitats
Estuarios / manglares
Según Rico (1993), los manglares se distribuyen en Baja California, Florida, hasta el sur este de Brasil en el Atlántico y hasta Ecuador en el Pacífico. Los bosques de manglar ofrecen refugios y sombra a las chinches patinadoras y la preferencia de este hábitat ha sido registrada para varias especies de la familia Gerridae en Colombia (Molano-Rendón et al. 2008). Estos insectos han sido recolectados entre las raíces de los manglares (observaciones personales), lo que indica el importante papel que juegan estos ambientes en la dinámica ecológica para el mantenimiento de la fauna semiacuática. A nivel mundial cerca de 70 especies de las chinches patinadoras se asocian la mayor parte de su ciclo de vida a estos ecosistemas (Andersen 1998, Zettel 2003). En el Neotrópico, de las 47 especies registradas, 39 tienen preferencia por este tipo de hábitats usándolos como zona de refugio, buscando las zonas sombreadas para su protección, siendo la distribución de las especies de Gerromorpha marinos similar a la de los manglares en América (Figura 2).
Las especies del género Rheumatobates son exclusivamente Neotropicales, con 38 especies descritas (Castro-Vargas y Morales-Castaño 2011), las cuales habitan diferentes cuerpos de agua dulce como lagunas, lagos y ríos (Molano-Rendón et al. 2008), sin embargo 16 especies se encuentran de manera exclusiva en manglares y estuarios (Anexo 2), distribuyéndose en los océanos Pacífico y Atlántico, estando la especie R. bergrothi Meinert 1895 registrada en ambos océanos (Figura 1b). De las especies reportadas en este tipo de hábitats (estuarios y manglares), R. bergrothi Meinert, 1895 (Figura 1b), R. mexicanus Drake & Hottes, 1951 y R. peculiaris Polhemus & Spangler, 1989 se han reportado también en cuerpos de agua dulce (Polhemus y Spangler 1989). Rheumatobates minutus Hungerford, 1936 está ampliamente distribuida en el Caribe, sin embargo, es una especie difícil de observar, encontrándose algunas veces ejemplares alados en cuerpos de agua temporales formados por pequeños charcos hechos por la lluvia los cuales son alimentados por agua del mar que se filtra a través de la arena. Algunas especies son abundantes entre las raíces de las diferentes especies de manglares del Pacífico y han sido recolectadas en la desembocadura de ríos que llegan al mar, hallando siempre pocos individuos en esos hábitats, como la especie R. carvalhoi Drake & Harris, 1944 reportada en Ecuador (río Atacames, Polhemus y Manzano 1992) y Colombia (río Joví, Nuquí), y la especie R. prostatus Polhemus, 1975 en Panamá (Bahía Honda), Polhemus y Manzano (op. cit.). Aunque la especie R. carvalhoi es muy común dentro de hábitats salobres, se ha recolectado en cuerpos de agua dulce y estanques que se conectan a los estuarios durante la marea alta (Molano-Rendón et al 2008). Las especies distribuidas en hábitats marinos del Pacífico, suelen recolectarse entre las raíces de los manglares en marea baja, las cuales quedan restringidas en pequeños charcos que se forman sobre los pantanos de mangle y las especies que habitan estuarios buscan las zonas de sombra que hacen los árboles de mangle (observaciones personales).
Rhagovelia es uno de los géneros más diversos de la familia Veliidae con cerca de 184 especies registradas para América (Padilla-Gill y Moreira 2013a), de las cuales hasta el momento ocho especies del grupo salina tienen preferencia de hábitats marinos; especialmente la especie R. plumbea Uhler, 1894, que es de amplia distribución en el Caribe y se encuentra asociada a las raíces de manglares expuestos al mar en amplias flotillas o a varios metros de la costa y en algunas ocasiones ha sido recolectada en la sombra generada por lanchas estacionadas en la orilla. Padilla-Gil y Arcos (2011) registraron R. aguaclara Padilla-Gil, 2010 en esteros rodeados por manglar, la cual prefiere condiciones de aguas umbrosas rodeadas por vegetación y R. colombianus (Polhemus y Manzano, 1992) (Figura 1d) fue reportada por Polhemus y Manzano (1992) habitando esteros del pacífico colombiano.
Algunas especies ocupan hábitats crípticos, como cuevas donde llega el agua de mar, así como guaridas de cangrejos o madera en descomposición en los pantanos de manglar. Todas las especies del género Hebrus Curtis, 1831 (Polhemus y Polhemus 1989) y dos especies de Nereivelia Polhemus y Polhemus, 1989 han sido recolectadas en agujeros de madera de mangle hechos por organismos barrenadores en Singapur, sureste de Tailandia y Filipinas (Zettel 2004) (Figura 2).
Se han recolectado algunas especies dominantemente de agua dulce en cuerpos de agua salobres como lo son: Limnogonus franciscanus (Stål, 1859) y Trepobates taylori (Kirkaldy, 1899) que fueron recolectadas por Manzano et al. (1995) en manglares de la Isla Gorgona (Cauca - Colombia). Padilla-Gil y Arcos (2011) recolectaron las mismas especies para los manglares del departamento de Nariño - Colombia, e incluyen a Mesovelia mulsanti White, 1879 describiéndola como visitante marina. La especie M. mulsanti es de amplia distribución en el Neotrópico y frecuentemente recolectada en cuerpos de agua continentales, se encuentran comúnmente en las hojas flotantes de plantas acuáticas en estanques (Moreira 2015), sin embargo, ha sido reportada como asociada a ambientes de manglar o estuarios, siendo una de las especies eurihalinas verdaderas (Anexo 2). Telmatometra ujhelyi Esaki, 1937 ha sido recolectada en lagunas intermareales en el Pacífico colombiano, así como en quebradas de agua dulce que tienen contacto con el mar durante la marea alta (Nuquí - Chocó, Molano et al. En prep.).
Los ríos que tienen flujo de agua constante durante todo el año hacia el mar pueden desembocar en áreas con bosques de mangle, formando grandes extensiones de estuarios que albergan especies permanentes en estos microhábitats como las pertenecientes al género Rheumatobates (Figura 2). Pero a medida que se asciende en el río, las especies de éste género desaparecen y son remplazadas por otras, que aunque cerca de la desembocadura, nunca se han colectado en aguas salobres como Potamobates Champion, 1898, Platygerris Buchanan-White, 1883, Tachygerris Drake, 1957 y Brachymetra albinervis (Amyot y Seville, 1843), las cuales son frecuentes en la costa pacífica colombiana.
El género Hydrometra (Hydrometridae) se encuentra en los márgenes de los ríos y arroyos donde la corriente es moderada y en los bordes de los lagos, estanques y piscinas (Moreira 2015), sin embargo existe un único registro asociado con estuarios en Cuba por Muñoz et al. (2012). De igual manera el género Merragata (Hebridae) se asocia típicamente con los estanques completamente cubiertos por algas o con las hojas flotantes (Moreira 2015) y fue reportado por Muñoz et al. (2012) en estuarios de Cuba.
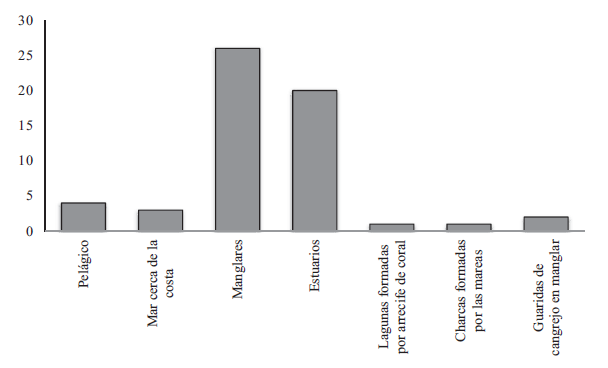
Figura 2.
Riqueza de especies de chinches patinadoras marinas por hábitat, en la región Neotropical.
Guarida de cangrejo en manglar y charcas formadas por las mareas
En este tipo de hábitat se han reportado dos géneros y tres especies (Figura 2). Las especies Microvelia chanita Polhemus y Hogue, 1972 y M. inquilina Polhemus y Hogue, 1972, fueron recolectadas en guaridas realizados por cangrejos en Costa Rica (Polhemus y Hogue 1972), al parecer estas especies ocupan este tipo de microhábitats de manera accidental y hasta el momento no se tienen otros registros del hábitat de estas especies. La única especie reportada en charcas formadas por las mareas es Speovelia mexicana Polhemus, 1975, la cual fue recolectada debajo de rocas encima de una zona costera similar a un arrecife, corriendo sobre el agua de mar atrapada por el arrecife después de que la marea retrocediera en el Pacífico (Polhemus 1975, Polhemus y Manzano 1992, Damgaard et al. 2012, Moreira 2015).
Lagunas de arrecifes de coral y mar cerca de la costa
Tres géneros, y cuatro especies se han reportado en este tipo de hábitat: Hermatobatidae es una familia con 12 especies halófilas exclusivas, que siempre se han recolectado en el mar cerca de la costa, sin embargo, en el Caribe se han reportado la especie Hermatobates bredini Herring, 1965 en lagunas de arrecife de coral, así como la especie Speovelia mexicana Polhemus, 1975 (Mesoveliidae) en Baja California (Polhemus 1975) (Figura 2). Hermatobates hawaiiensis China, 1977 es una especie difícil de recolectar, en las oportunidades en que se ha hecho ha sido con muchas horas de esfuerzo de redes de Neuston y con luces durante la noche (Cheng y Leis 1980, Polhemus y Polhemus 2012). Tanto los adultos como las ninfas que se distribuyen en este tipo de hábitats durante la marea alta se ocultan en huecos de los corales muertos como método de protección a depredadores y al embate de las olas (Andersen 1989). Otra especie asociada a las costas, en este caso alrededor de islas es Halobates robustus una especie endémica de las costas de las islas Galapagos (Ecuador) (Figura 2).
Ambientes pelágicos
Las especies exclusivamente oceánicas o de ambientes pelágicos reportadas para la región Neotropical fueron: Halobates micans Eschscholtz, 1822 (cosmopolita) (Figura 1a), Halobates sericeus Eschscholtz, 1822, Halobates sobrinus White, 1883 y Halobates splendens Witlaczil, 1886 (Océano Pacífico) (Anexo 2, Figura 2). La baja diversidad de especies registradas hasta el momento en ambientes pelágicos puede deberse a que estas especies se encuentran adaptadas a soportar condiciones extremas propias de este tipo de hábitat, como por ejemplo la falta de sustratos sólidos para ovipositar (Ruxton y Humphries 2008). De las cerca de 41 especies de Halobates descritas hasta el momento y que no se han vuelto totalmente oceánicas se asocian principalmente con manglares, otras con plantas y rocas emergentes para proporcionar un sustrato para la puesta de huevos (Andersen y Cheng 2004).
Distribución geográfica de las especies en el Neotrópico
De 48 especies registradas para la región Neotropical, 34 se encuentran restringidas a las costas del Pacífico y son pertenecientes a los géneros Darwinivelia Andersen y Polhemus, 1980, Halobates, Limnogonus Stål, 1868, Mesovelia Mulsant y Ray, 1852, Microvelia Westwood, 1834, Platyvelia, Rhagovelia, Rheumatobates, Speovelia Esaki, 1929, Trepobates (Uhler, 1894) y Telmatometroides Polhemus, 1991, seguida de la región Caribe (14 especies) con los géneros: Halobates, Halovelia Bergroth, 1893, Husseyella Herring, 1955 (Figura 1c), Hermatobates Carpenter, 1892, Merragata White 1877, Rhagovelia y Rheumatobates (Figura 3). Cinco especies de los géneros Darwinivelia, Halobates, Husseyella y Rhagovelia se distribuyen en el sureste de Brasil y dos especies, Rheumatobates aestuarius Polhemus, 1969 y Speovelia mexicana en las costas del Pacífico de Baja California y la especie Hermatobates hawaiiensis China, 1977 en las islas de Hawaii (Anexo 2, Figura 3).
En la familia Gerridae la especie que se encuentra más ampliamente distribuida en la región Neotropical es H. micans, especie oceánica que tiene una amplia distribución en el planeta, ocupando todos los mares (Sekimoto et al. 2013), en el Neotrópico se ha recolectado a pocos kilómetros de la isla de Malpelo en el Pacífico y en el Caribe (Molano-Rendón et al. 2008) y recientemente se registró muy cerca de las islas de Providencia y San Andrés en el Caribe colombiano por Barrera (2014). Mesovelia mulsanti, otra especie de amplia distribución en el Neotrópico y recolectada con frecuencia en ecosistemas marinos costeros, sin embargo, es también muy abundante en cuerpos de agua dulce en el continente (Moreira et al. 2008).
Veliidae es una de las familias más diversas, con 600 especies descritas (Moreira 2015), ampliamente distribuidas en la región Neotropical, siendo Sur América el área geográfica con mayor diversidad de especies (Anexo 2). Halovelia es el género con mayor número de especies (32), distribuidas desde la costa del Mar Rojo hasta el Pacífico sur cerca de las Costa de Samoa, norte de Australia, Islas Fiji y Tonga (Andersen 1998). De las especies actuales del género Halovelia, ninguna se ha recolectado en el Caribe, sin embargo, Andersen y Poinar (1998) describieron H. electrodominica de ámbar Dominicano, hace 20 a 30 millones de años; siendo esta descripción el primer registro de insecto marino en ámbar y probablemente la extinción de esta especie sucedió durante finales del Terciario.
Hermatobatidae es una familia de insectos obligatoriamente marinos, y el género Hermatobates actualmente cuenta con 12 especies descritas, distribuidas principalmente entre el Trópico de Capricornio y el Trópico de Cáncer (Polhemus y Polhemus 2012), de estas especies solo dos se distribuyen en el Neotrópico: H. breddini Herring, 1965 en el mar Caribe (Polhemus y Herring 1979) y H. hawaiiensis endémica de Hawaii (Anexo 2).
En la región Neotropical, Mesoveliidae está representada principalmente por el género Darwinivelia con tres especies distribuidas en las costas de Colombia, el norte de Brasil, y las Islas Galápagos (Anexo 2); el género Mesovelia, con M. mulsanti, distribuida en Estados Unidos y Canadá, además de ser introducida en las islas de Hawaii (Damgaard et al. 2012, Moreira 2015) y M. halirrhyta Polhemus, 1975 que solo se ha registrado hasta el momento para Costa Rica y Colombia (Anexo 2) y Speovelia con un solo representante neotropical reportado para México (Anexo 2).
La región Pacífica fue la que presentó mayor riqueza de especies (Figura 3), esta riqueza es debida a que existe una mayor franja de manglares, donde la mayoría de las especies costeras tiene preferencia, adicionalmente algunos lugares de las zonas litorales Neotropicales son altamente lluviosos, y en esta región discurren de manera permanente cuerpos de agua dulce hacia el mar de diferente manera, haciendo que se presenten microhábitats que pueden dar lugar a que algunas especies de agua dulce puedan encontrarse a pocos metros del mar y en algunas ocasiones estas especies pueden soportar cierta salinidad fruto de los cambios de marea que inundan estas zonas de agua dulce.
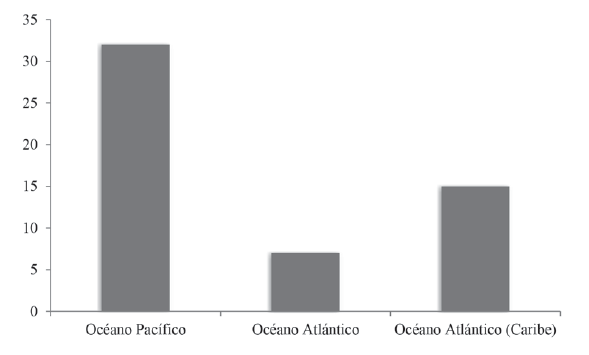
Figura 3.
Riqueza de especies de chinches patinadoras marinas por área biogeográfica en la región Neotropical.
Conclusión
Con esta nueva aproximación se cuenta con un conocimiento detallado de la diversidad y de algunos aspectos ecológicos de las especies de chinches marinas en la región del Neotrópico. El hecho que la región Pacífica presente la mayor riqueza de especies y que se encontraran dos nuevas especies para el Caribe y Pacífico colombiano (Molano et al. en prep.), da la certeza que la lista aumentará con nuevos inventarios, principalmente sobre las zonas identificadas con bajos registros y cuando se avance en detalle en los aspectos taxonómicos de los géneros y familias identificadas en el Neotrópico.
Agradecimientos
A los curadores de las colecciones visitadas: Cesar Tamaris (CEUM), Harry Brailovsky (CNIN), Fernando Fernández (ICN), Ana Lucia López (CIBUQ) y Monika Springer (MZUCR). A Felipe Moreira (Instituto Oswaldo Cruz-Brasil) y Carla Floriano (Universidad de Sao Paulo), por toda la disposición y colaboración. A Patricia Mondragón su cooperación, a la Escuela de Ciencias Biológicas y al Museo de Historia Natural Luis Gonzalo Andrade de la Universidad Pedagógica y Tecnológica de Colombia (UPTC), por el apoyo para la realización de las salidas de campo. A los estudiantes de las asignaturas Invertebrados marinos y Ecología marina (semestres VII – VIII) del programa de Biología de la UPTC, quienes aportaron datos con su componente práctico en esta región durante el mencionado período y a los pescadores de las regiones visitadas por su entusiasta ayuda en la fase de campo. A la Dirección de Investigaciones de la Universidad Pedagógica y Tecnológica de Colombia por la financiación de este trabajo, con el proyecto: Chinches Patinadoras (Hemiptera: Heteroptera: Gerridae) de Colombia: Taxonomía, Distribución y Datos Biológicos: SGI 1952.
Referencias
Andersen, N. M. 1982. The semiaquatic Bugs (Hemiptera, Gerromorpha). Phylogeny, adaptations biography, and classification. Entomograph 3: 1–455.
Andersen, N. M. 1989. The coral bugs, genus Halovelia Bergroth (Hemiptera, Veliidae). I. History, Classification, and taxonomy of species except the H. malaya-group. Entomological Scandinavia 20: 75–120.
Andersen, N. M. 1998. Marine water striders (Heteroptera, Gerromorpha) of the Indo-Pacific: cladistic biography and cenozoic paleogeography. Biogeography and Geological Evolution of the SE Asia 341–354.
Andersen, N. M. 1999. The evolution of marine insects: phylogenetic, ecological and geographical aspects of species diversity in marine water striders. Ecography 22: 98–111.
Andersen, N. M. y L. Cheng. 2004. The marine insect Halobates (Heteroptera: Gerridae) biology, adaptations, distribution and phylogeny. Oceanography and Marine Biology An Annual Review 42: 119–180.
Andersen, N. M. y G. O. Poinar. 1998. A marine water strider (Hemiptera: Veliidae) from Dominican amber. Entomologica Scandinavica 29: 1–9.
Andersen, N. y J. Polhemus. 1980. Four new genera of Mesoveliidae (Hemiptera, Gerromorpha) and the phylogeny and classification of the family. Entomologica scandinavica 11: 369–392.
Andersen, N. y T. Weir. 1999. The marine Haloveliinae (Hemiptera:Veliidae) of Australia, New Caledonia and southern New Guinea. Invertebrate Taxonomy 13: 309–350.
Barrera, J. V. 2014. Las chinches patinadoras (Hemiptera: Gerromorpha) en ecosistemas marinos del Caribe Colombiano. Trabajo de grado. Universidad Pedagógica y Tecnológica de Colombia, Facultad de Ciencias, Escuela de Biología. Tunja, 45 pp.
Camus, P. A. y R. M. Barahona. 2002. Insectos del intermareal de Concepción, Chile: perspectivas para la investigación ecológica. Revista Chilena de Historia Natural 75 (4): 793–803.
Carvalho, J. C. M. 1984. On a new species of intertidal water strider from Brazil (Hemiptera, Gerromorpha, Mesoveliidae). Amazoniana 8 (4): 519–523.
Castro-Vargas, M. y I. Morales-Castaño. 2011. The Rheumatobates Bergroth, 1892 (Hemiptera: Heteroptera: Gerridae) of Colombia, including the description of R. plumpes n. sp. and a key to represented species. Zootaxa 3040: 1–18.
Cheng, L. 2006. A bug on the ocean waves (Heteroptera, Gerridae, Halobates Eschscholtz). Denisia 19: 1033–1040.
Cheng, L. 1976. Marine Insects. North-Holland Publishing Company. Amsterdam The Netherlands, 581pp.
Cheng, L. y E. W. Leis. 1980. Notes on the seabed Hermatobates hawaiiensis China (Heteroptera: Hermatobatidae). Proceeding Hawaiian Entomological Society 23 (2): 193–197.
Cheng, L. y R. Lewin. 1971. An interesting marine insect, Rheumatobates aestuarius (Heteroptera: Gerridae), from Baja California, Mexico. Pacific Insects 13 (2): 333–341.
Cheng, L. y W. Mathis. 2003. Marine insects of Guam: Heteroptera and Diptera. Micronesica 35–36: 514–522.
Clapham, M. E, J. A. Karr y D. B. Nicholson, A. J Ross y P. J. Mayhew. 2016. Ancient origin of high taxonomic richness among insects. Proceeding of the Royal Society B 283: 2015–2476.
Damgaard, J., F. F. Moreira, M. Hayashi, T. Weir y A. Zettel. 2012. Molecular phylogeny of the pond treaders (Insecta: Hemiptera: Heteroptera: Mesoveliidae), discussion of the fossil record and a checklist of species assigned to the family. Insect Systematics & Evolution 43: 175–212.
Drake, C. J. 1958. New Neotropical Veliidae (Hemiptera). Proceedings of the Biological Society of Washington 71: 133–142.
Drake, C. J. y H. M. Harris.1933 New American Veliidae (Hemiptera). Proceedings of the Biological Society of Washington 46: 45–54.
Drake, C. J y P. H. Van Doesburg. 1966. Water–Striders of the American Genus Trochopus (Hemiptera: Veliidae). Studies on the Fauna of Suriname and Other Guyanas 31: 65–76
Epler, J. H. 2006. Identification manual for the aquatic and semi–aquatic Heteroptera of Florida (Belostomatidae, Corixidae, Gelastocoridae, Gerridae, Hebridae, Hydrometridae, Mesoveliidae, Naucoridae, Nepidae, Notonectidae, Ochteridae, Pleidae, Saldidae, Veliidae). Florida Department of Environmental Protection, Tallahassee, 195 pp.
Floriano, C. F. B. y F. F. F. Moreira. 2015. A new species of Rhagovelia Mayr, 1865 (Hemiptera: Heteroptera: Veliidae) from Brazil. Zootaxa 4018: 437–443.
Ferrú, M. y W. Sielfeld. 2010. Nuevos registros de Halobates splendens (Hemiptera: Gerridae) en el Norte de Chile y comentarios sobre la distribución en el Pacífico suroriental. Revista Chilena de Entomología 35: 83–87.
Hadden, F. C. 1931. The Pelagic Halobates. Proceedings Hawaiian Entomological Society 7: 457–459.
Henry, G. M. 1932. Note on the diving powers of Halobates. Spolia Zeylanica 16: 353–354.
Herring, J. L. 1958. The marine water-striders of the ‘Dana’ Expeditions (Insecta: Hemiptera). Dana Report 44: 1–14.
Herring, J. L. 1961. The genus Halobates (Hemiptera: Gerridae). Pacific Insects 3: 223–305.
Hungerford, H.B. 1954. The Genus Rheumatobates Bergoth (Hemiptera-Gerridae). The University of Kansas Science Bulletin 36 (7): 529–588.
Ikawa, T., H. Okabe y L. Cheng. 2012. Skaters of the seas comparative ecology of nearshore and pelagic Halobates species (Hemiptera: Gerridae), with special reference to Japanese species. Marine Biology Research 8: 915–936.
Manzano, M. R., N. Nieser y G. Caicedo. 1995. Lista preliminar de heterópteros acuáticos en la Isla Gorgona y Llanura del Pacífico. Biblioteca José Jerónimo Triana 11: 47–72.
Molano, F., F.F.F. Moreira y I. Morales. 2016. New species and records of Microveliinae and Veliinae (Hemiptera: Heteroptera: Veliidae) from Colombia. Zootaxa 4171 (3): 575–585.
Molano-Rendón, F., I. T. Morales-Castaño y C. Serrato-Hurtado. 2008. Clasificación y Hábitats de Gerridae (Heteroptera-Gerromorpha) en Colombia. Acta Biológica Colombiana 13 (2): 41–60.
Moreira, F. F. F. 2015. The Semiaquatic Gerromorphans. Pp. 113–156. En: Panizzi A. y J. Grazia. (Eds.). True Bugs (Heteroptera) of the Neotropics. 1 ed. Dordrecht: Springer Science+Business Media, Brazil.
Moreira, F. F., J. R. I. Ribeiro y J. L. Nessimian. 2008. A synopsis of the species of Mesovelia (Insecta: Heteroptera: Mesoveliidae) occurring in the floodplain of the amazon river, Brazil, with redescriptions of Mesovelia mulsanti White and M. zeteki Harris & Drake. Acta Amazonica 38 (3): 539–550.
Moreira, F. F. F., J. L. Nessimian, J. A. Rúdio y F.F. Salles. 2010. New species and new records of Veliidae from Espírito Santo State and adjacent Minas Gerais State, Brazil, with notes on nomenclature (Insecta: Heteroptera: Gerromorpha). Journal of Natural History 44: 2761–2801.
Muñoz S., C. Naranjo y F. F. F. Moreira. 2012. New distributional records of Gerromorpha Popov, 1971 (Insecta: Hemiptera: Heteroptera) from Cuba. Check List 8 (2): 307–309.
Nieser, N. y M. Alkins-Koo. 1991. The water bugs of Trinidad & Tobago. Occasional Papers of the Zoology Department, University of the West Indies 9: 1–127.
Padilla-Gil, D. N. y O. Arcos. 2011. Hemiptera acuáticos asociados a los estuarios de la costa pacífica colombiana. Revista Colombiana de Entomología 37 (1): 350–353.
Padilla-Gil, D. N. y B. Pacheco-Chávez. 2012. New records of Rheumatobates Bergroth (Hemiptera: Heteroptera: Gerridae) from the Pacific coast of Colombia and Costa Rica, with a key to males of Rheumatobates in the Eastern Tropical Pacific. Zootaxa 3427: 33–46.
Padilla-Gil, D. N. y F. F. F. Moreira. 2013a. Checklist, taxonomy and distribution of the Rhagovelia Mayr, 1865 (Hemiptera: Heteroptera: Veliidae) of the Americas. Zootaxa 3640 (3): 409-424.
Padilla-Gil, D. N. y F. F. F. Moreira. 2013b. Two new species of Microvelia Westwood, 1834 (Hemiptera: Heteroptera: Veliidae) from Colombia, with a key to Colombian species. Zootaxa 3745 (5): 587–595.
Polhemus, J. T. 1975. New estuarine and intertidal water from Mexico and Costa. The Pan–Pacific Entomologist 51 (3): 243–247.
Polhemus, J. T. 1991. Two new Neotropical genera of Trepobatinae (Gerridae: Heteroptera). Journal New York Entomologist Society 99 (1): 78–86.
Polhemus, J. T. y L. Cheng. 1976. A new Rheumatobates from Costa Rica (Hemiptera: Gerridae). The Pan–Pacific Entomologist 52 (4): 321–323.
Polhemus, J. T. y J. L. Herring. 1979. A Further description of Hermatobates bredini Herring and a new record for Cuba (Hemiptera: Hermatobatidae). Proceedings of the Entomological Society of Washington 81 (2): 253–254.
Polhemus, J. T. y C. L. Hogue. 1972. Two new Microvelia from crabholes in Costa Rica. Contributions in Science Natural History Museum Los Angeles 224: 1–6.
Polhemus, J.T. y L. Cheng. 1982. Notes on marine water-strider with descriptions new species. Pacific Insects 24 (3–4): 219–227.
Polhemus, J. T. y M. R. Manzano. 1992. Marine Heteroptera of the eastern tropical Pacific (Gelastocoridae, Gerridae, Mesoveliidae, Saldidae, Veliidae). Pp. 302–320, 650, 660. En: Quintero, D. y A. Aiello. (Eds.). Insects of Panama and Mesoamerica: selected studies. Oxford University Press, Oxford, New York & Tokyo.
Polhemus, J. T. y D. A. Polhemus. 1989. A New Mesoveliid genus and two new species of Hebrus (Heteroptera: Mesoveliidae, Hebridae) from Intertidal habitats in Southeast Asian mangrove swamps. Raffles Bulletin of Zoology 37 (1–2): 73–82.
Polhemus J. T y D. A. Polhemus 1993. Two New Genera for New World Veliinae (Heteroptera: Veliidae). Journal of the New York Entomological Society 101 (3): 391– 398.
Polhemus J. T. y D. A. Polhemus. 2012. A Review of the Genus Hermatobates (Heteroptera: Hermatobatidae), with Descriptions of Two New Species. Entomologica Americana 118 (1): 202–241.
Polhemus, J. T. y P. J. Spangler. 1989. A new species of Rheumatobates Bergroth from Ecuador and distribution of the genus (Heteroptera: Gerridae). Proceedings of the Entomological Society of Washington 91 (3): 421–428.
Prado, E. 2008. Conocimiento actual de Hemiptera – Heteroptera de Chile con lista de especies. Boletin del Museo Nacional de Historia Natural, Chile 57:31–75.
Rico, V. 1993. Origen y rutas de dispersión de los mangles: una revisión con énfasis en las especies de América. Acta Botánica Mexicana 25: 1–13.
Ruxton, G. y S. Humphries. 2008. Can ecological and evolutionary arguments solve the riddle of the missing marine insects?. Marine Ecology 29: 72–75.
Sekimoto, T., K. Iyota, Y. Osumi, T. Shiraki y T. Harada. 2013. Lowered Salinity Tolerance in Sea Skaters Halobates micans, Halobates sericeus, and Halobates sp. (Heteroptera: Gerridae). Environmental Entomology 42 (3): 572–577.
Westlake, K. P., L. Rowe y D. Currie. 2000. Phylogeny of the water strider genus Rheumatobates (Heteroptera: Gerridae). Systematic Entomology 25: 125–145.
Zettel, H. 2003. Notes on the marine Haloveliinae (Insecta: Heteroptera: Veliidae) of the Philippines, with descriptions of four new species, identification key, and classification of all species of Haloveloides Andersen, 1992. Naturhistorisches Museum Wien 104B: 163–181.
Zettel, H. 2004. Hebrus murphyi, new species (Heteroptera: Hebridae) from an intertidal mangrove habitat in Burias Island, Philippines. The Raffles Bulletin of Zoology 52 (1): 75–77.
Anexos
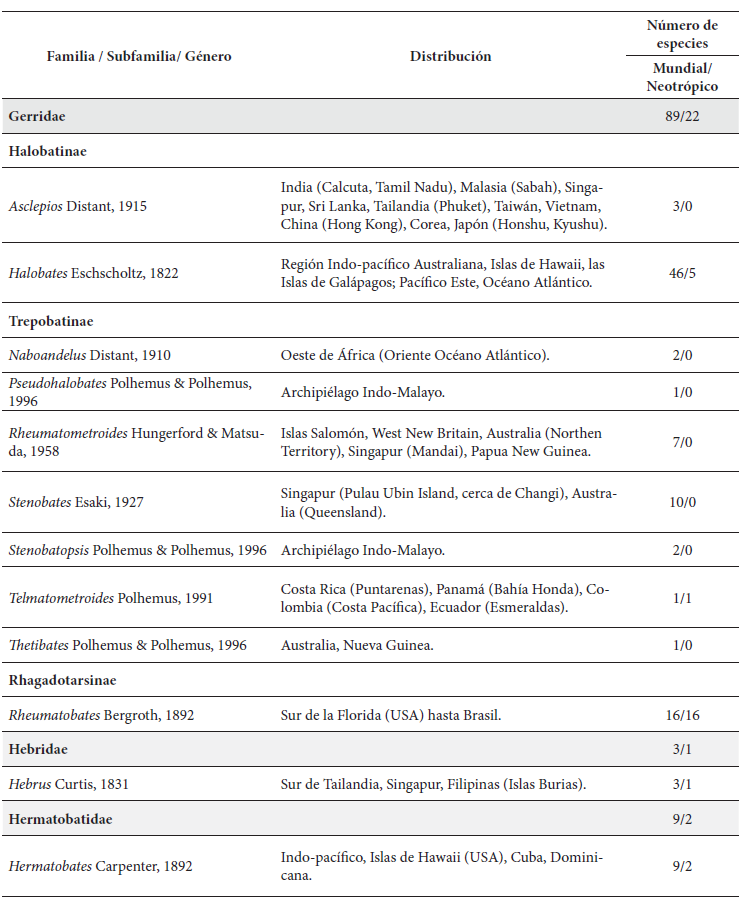
Lista de familias, subfamilias y géneros de Gerromorpha (Hemiptera: Heteroptera) de ambientes marinos. Se presenta la distribución de especies asociadas a ecosistemas marinos y el número de especies a nivel mundial / Neotropical.
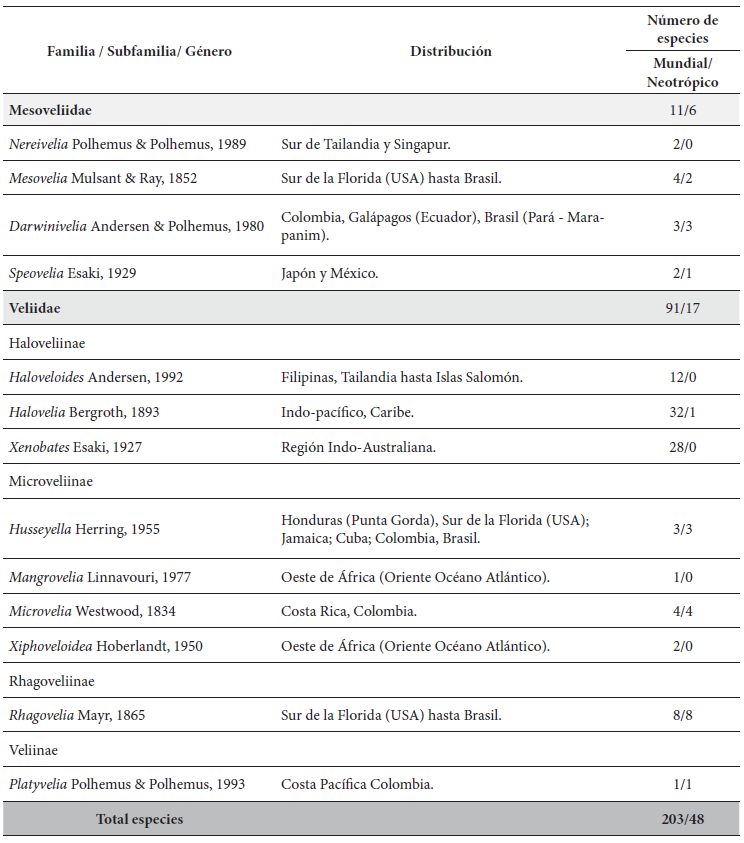
Lista de familias, subfamilias y géneros de Gerromorpha (Hemiptera: Heteroptera) de ambientes marinos. Se presenta la distribución de especies asociadas a ecosistemas marinos y el número de especies a nivel mundial / Neotropical.
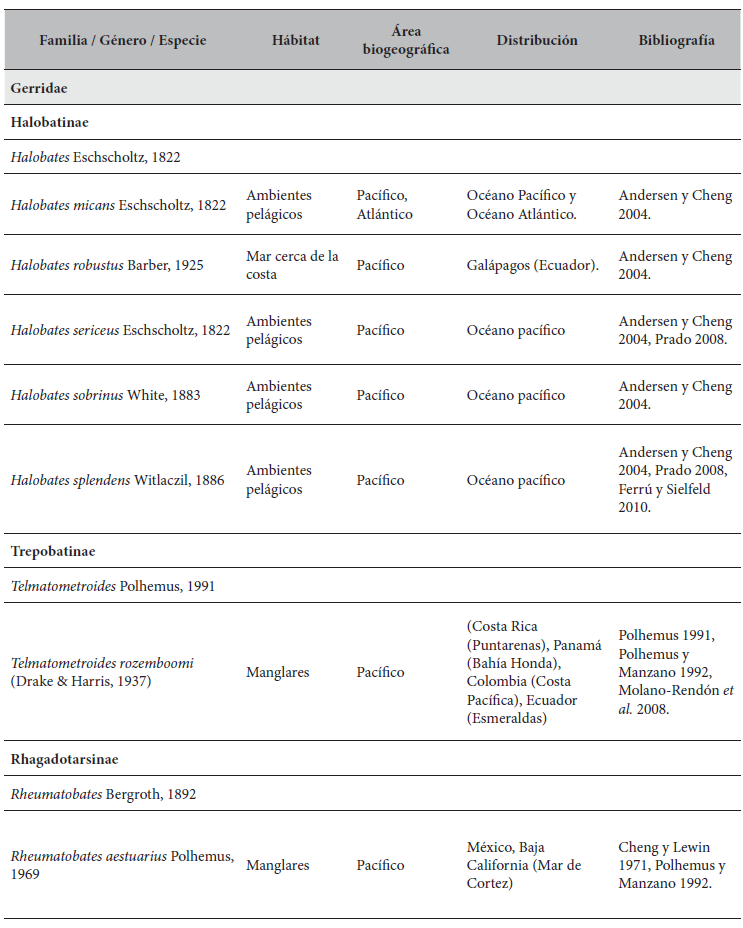
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
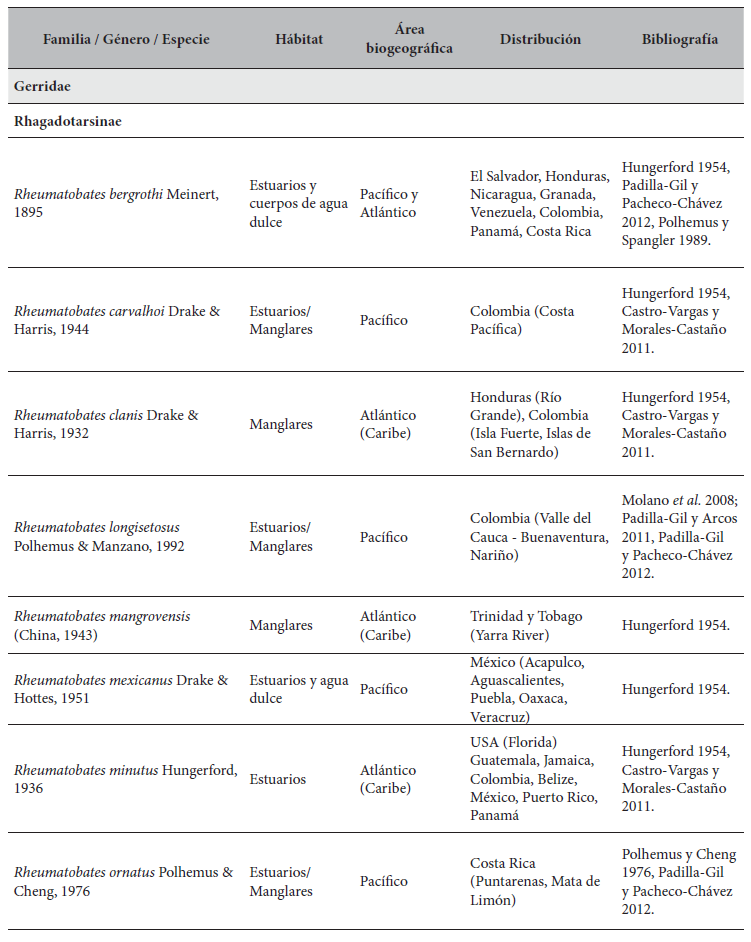
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
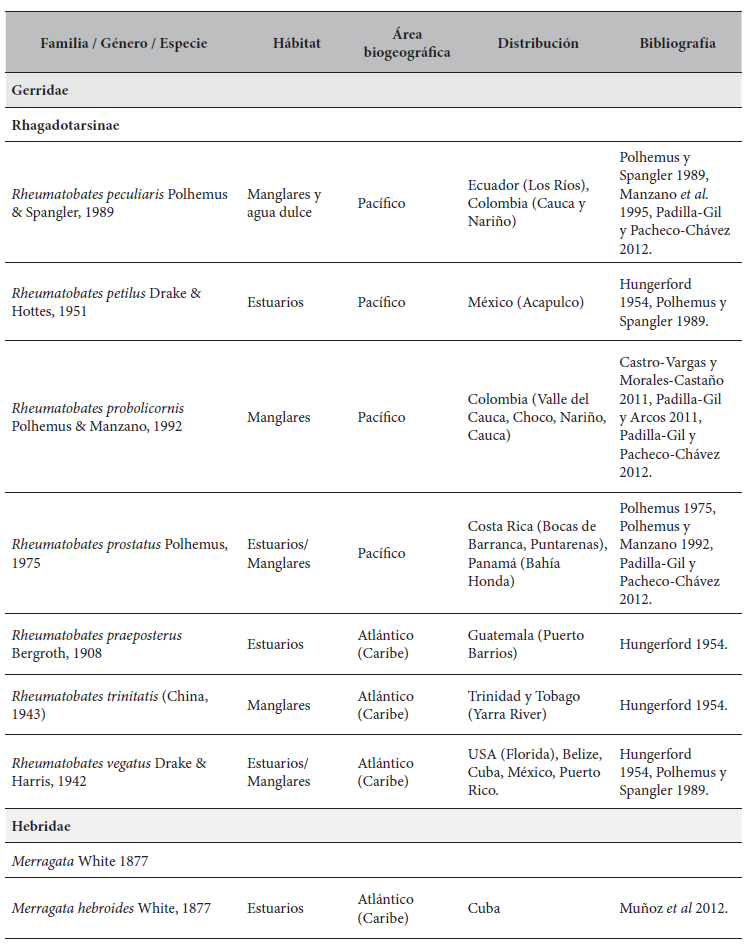
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
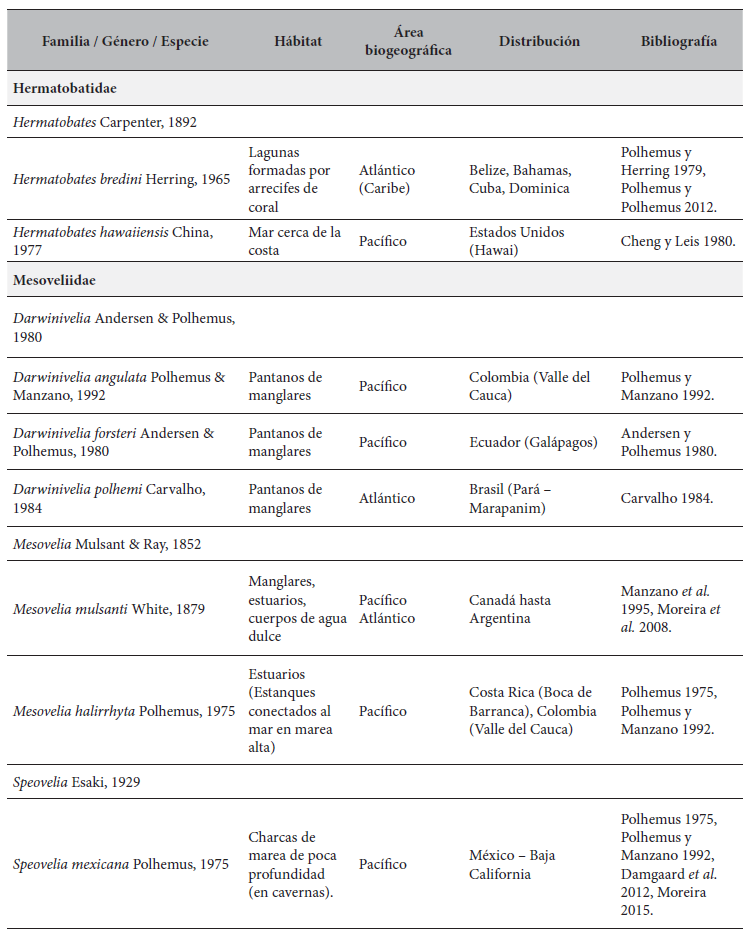
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
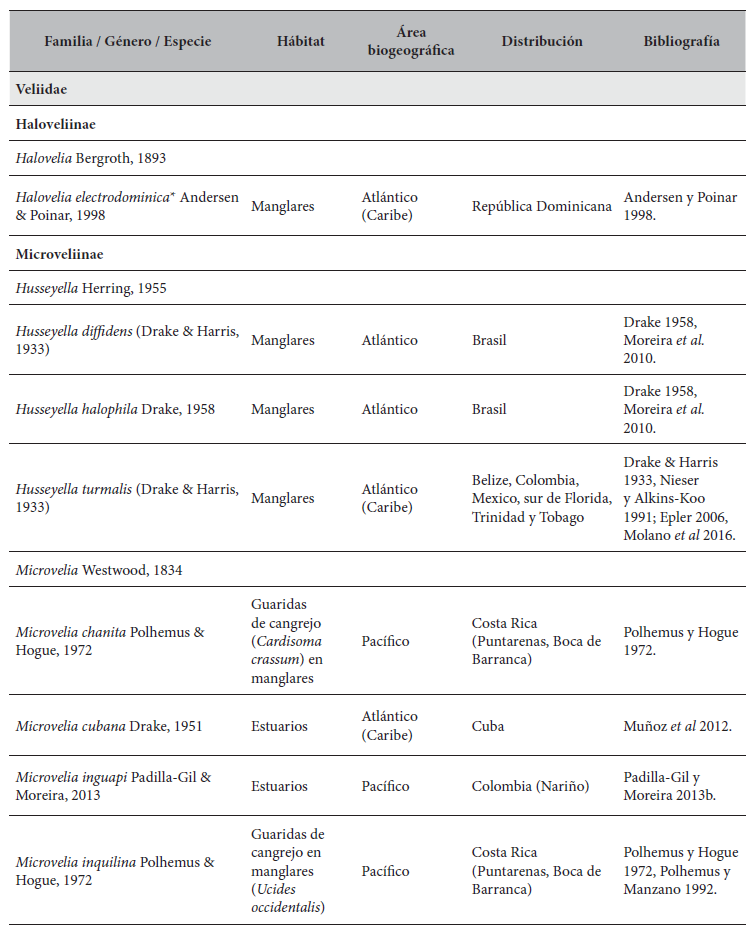
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
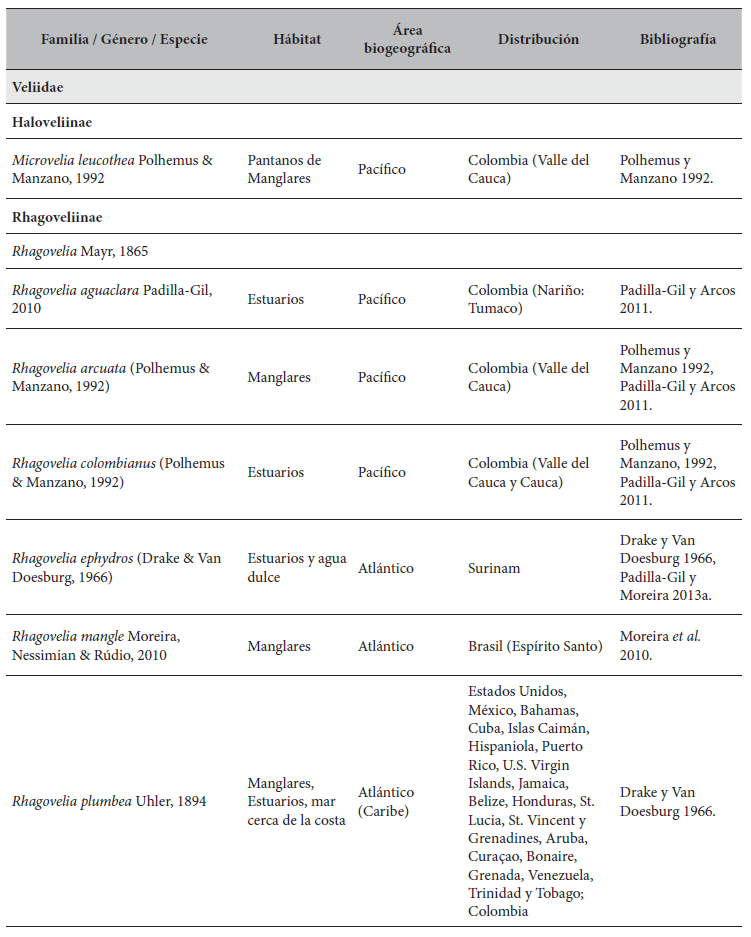
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
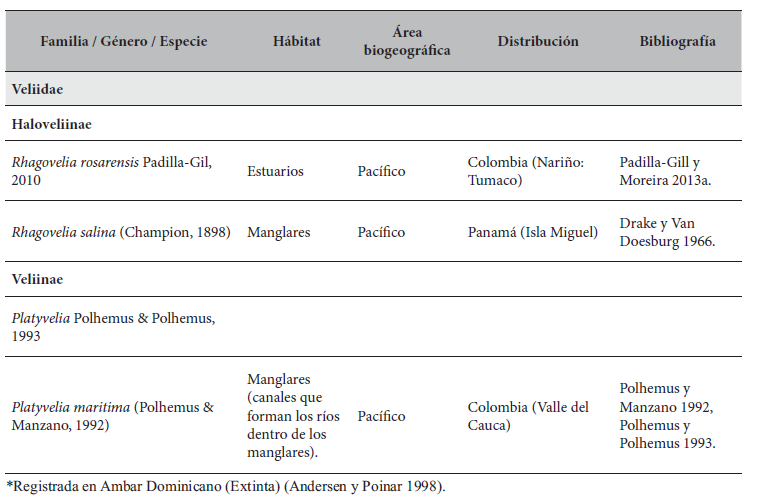
Especies de Gerromorpha (Hemiptera: Heteroptera) con distribución Neotropical de ambientes marinos.
Información adicional
Citación del artículo:: Molano-Rendón, F. e I. Morales 2017. Chinches patinadoras marinas (Hemiptera: Heteroptera: Gerromorpha): diversidad de los hábitats oceánicos del Neotrópico. Biota Colombiana 18 (1): 172-191. DOI: 10.21068/c2017.v18n01a10