Artículos
Evaluación del desempeño reproductivo de una cepa domesticada de Penaeus vannamei en una maduración comercial
Reproductive performance evaluation of a domesticated strain of Penaeus vannamei in a commercial maturation
Evaluación del desempeño reproductivo de una cepa domesticada de Penaeus vannamei en una maduración comercial
AquaTIC, núm. 53, pp. 18-31, 2019
Universidad de Zaragoza

Esta obra está bajo una Licencia Creative Commons Atribución 3.0 Internacional.
Resumen: La sostenibilidad de la camaronicultura depende del desarrollo de técnicas reproductivas de especies objetivo en cautiverio. Debido a lo escasa de la información sobre el desempeño de Penaeus vannamei en instalaciones de maduración, especialmente acerca de una especie domesticada, se consideró valioso ofrecer parámetros de benchmarking. Se presenta un análisis detallado de los registros de un año de una empresa dedicada a la producción de nauplios de camarón blanco. La facilidad operaba con fotoperiodo natural y estaba provista con 22 tanques circulares de maduración, provistos con especímenes fenotípicamente seleccionados, de 10 a 12 meses de edad, de una cepa con 14 generaciones en cautividad. Los reproductores fueron alimentados con productos frescos (calamar, mejillón, gusanos y biomasa de Artemia enriquecida), suplementada con un alimento seco balanceado. El recambio de agua diario promedió 108,7%. Los padrotes fueron abastecidos a 8 ind/m2, a una proporción sexual macho: hembra de 1,2:1. Las hembras fueron ablacionadas manualmente. En promedio, 51,5 hembras maduras copularon diariamente (tasa de apareo de 6,5%). Las hembras copuladas desovaron masivamente hasta 1,5 ind/m2 en tanques circulares. La tasa de fertilidad promedió 91,8%. Los nauplios fueron cosechados con luz y flujo de agua. Como media, se produjeron 7,76 millones de nauplios/día, con un rendimiento de 158,3 millares de nauplios/hembra y una fecundidad de 173,3 millares de huevos/hembra. El desempeño reproductivo de las hembras estudiadas fue satisfactorio, a pesar del bajo recambio de agua, permitiendo afirmar que la domesticación no ha perjudicado la capacidad reproductiva de esta cepa de Penaeus vannamei.
Palabras clave: camarón blanco, padrotes, apareo, desove, eclosión, nauplios.
Abstract: Shrimp culture sustainability depends of reproductive techniques of target species in captivity. Because information about performance of Penaeus vannamei in commercial maturation facilities is really scarce, specially of a domesticated strain, it was thought useful to offer benchmarking parameters. A detailed analysis of one year records of an enterprise dedicated to production of white shrimp nauplii is presented. Facility operated with natural photoperiod and was provided with 22 circular maturation tanks, sourced with phenotypically selected, 10-12 months old specimens, from a 14 generations in captivity stock. Broodstock were fed with fresh products (squid, mussels, worms and enriched Artemia biomass), complimented with a dry formulated feed. Daily water exchange averaged 108.7%. Shrimps were stocked at 8 ind/m2 and at sex proportion male:female of 1,2:1. Females were ablated manually. As a mean, 51.5 mature female were mated daily (mating rate of 6.5%). Mated females spawned massively until 1.5 ind/m2 in circular tanks. Fertility rate averaged 91.8%. Nauplii were harvested with light and water flow. As a mean, 7.76 million of nauplii/day were produced, with a yield of 158.3 thousand of nauplii by female and a fecundity of 173.3 thousands of eggs by female. Reproductive performance of studied females was satisfactory, in spite of low water exchange, allowing to affirm that domestication have not perjudicated the reproductive output of this strain of Penaeus vannamei.
Keywords: white shrimp, broodstock, mating, spawning, hatching, nauplii.
Introducción
En América, las experiencias comerciales de cultivo de camarón comenzaron tempranamente en la década de 1970, basadas en especies autóctonas: Penaeus vannamei y P. stylirostris en la costa del Pacífico, y P. setiferus, P. duorarum y P. aztecus en el lado Atlántico (Lawrence y Huner, 1987). Los resultados poco satisfactorios obtenidos en esta última región (Scelzo, 1983), condujeron a un cambio de estrategia: la introducción de especies pacíficas hacia las costas atlánticas (Jory et al., 1999). Paralelamente a su movilización en el continente americano, Penaeus vannamei y P. stylirostris fueron introducidas sucesivamente en Fiji, China continental, Taiwán, Filipinas, Tailandia, Indonesia, Vietnam, Malasia e India (Briggs et al., 2005). Recientemente, Penaeus vannamei se ha convertido en la especie más popular entre los cultivadores de camarón a nivel mundial (Wyban, 2007).
Debido a la imposibilidad de suministro silvestre de semilla, así como por la poca disposición de las autoridades pesqueras de los países receptores a permitir importaciones frecuentes debido a razones ecológicas y sanitarias, los proyectos camaroneros debieron aplicar esfuerzos tempranos en el ámbito reproductivo. Es así como, tras años de persistencia, se lograron importantes adelantos en este aspecto, hasta el punto de soportar el crecimiento de sus propios sectores productivos, particularmente en Venezuela y Brasil, avanzando en términos de domesticación (Jory et al., 1999). Los satisfactorios resultados obtenidos estimularon programas de desarrollo de cepas libres de patógenos específicos (SPF) (Kuljis y Brown, 1992) o resistentes a patógenos específicos (SPR) e incluso de mejoramiento genético (Benzie, 1998). Cuzon et al. (2004) refirieron la existencia de cepas domesticadas de camarones desde la década de 1990 en contadas regiones del mundo: Tahiti, Hawaii y Venezuela. Posteriormente, tras varios episodios de carácter epizoótico, y la creciente amenaza de sobreexplotación de algunas poblaciones silvestres por sobrepesca y contaminación, las instalaciones de maduración de camarones peneidos se han vuelto populares en otros países (Chimsung, 2014). De acuerdo a Wyban (2007), para el 2006 casi el 80% de camarón cultivado provenía de programas de domesticación, proporción con una clara tendencia al alza.
Aunque es un hecho claramente visible el apuntalamiento de técnicas reproductivas en facilidades comerciales de maduración de camarones de télico abierto, especialmente de Penaeus vannamei (Kawahigashi, 2010), poco se conoce sobre las particularidades de este tipo de operaciones. Por esta razón, generar un registro detallado de la productividad de una empresa de esta naturaleza constituyó uno de los objetivos de este trabajo.
Por otra parte, el carácter domesticado de una especie puede generar dudas sobre su potencial reproductivo. Los programas de reproducción de camarones, a largo plazo, suelen conducir a un incremento en la endogamia del núcleo poblacional, lo cual puede conducir a bajos desempeños en crecimiento, supervivencia y reproducción (Campos-Montes et al., 2011; de Donato et al., 2005). En este sentido, el otro objetivo de este trabajo se orienta a ofrecer luces sobre la posible pérdida de la potencialidad reproductiva de una cepa de camarón blanco asociable a la domesticación.
Material y Métodos
El trabajo se centró en la compilación y análisis meticuloso de los registros operativos de un año entero de una empresa dedicada a la producción comercial de nauplios de camarones marinos y su comparación con los estándares productivos de la especie. Los reproductores correspondían a una cepa domesticada de camarón blanco, Penaeus vannamei Boone, 1931, con al menos 14 generaciones en cautiverio.
Las instalaciones productivas de la empresa estaban situadas al SE del Mar Caribe, específicamente al sur de la Isla de Coche, Nueva Esparta, Venezuela (10° 45′ 57″ N, 63° 57′ 10″ W). Estaba sometida a un fotoperiodo natural y dotada de una sala de maduración y dos salas de desove y eclosión como principales áreas operativas. Adicionalmente, contaba con dos estaciones de bombeo, y áreas independientes de filtrado, reservorios, chequeo de calidad, lavado, despacho y preparación de alimentos. La sala de maduración tenía 22 tanques circulares de 4,5 m de diámetro x 1 m de altura, de fibra de vidrio y polivinilo, recubiertos con liner de PVC o EDPM, con descarga central. El número de tanques dedicados a la maduración de Penaeus vannamei varió entre cinco y 22 unidades durante el período estudiado, en respuesta a la demanda del mercado, con un promedio de 14,83 y una moda de 16 tanques. Las salas de desove reunían 12 tanques, del mismo material que los precedentes, pero de menores dimensiones (3,6 m de diámetro x 0,75 m de altura), con descarga lateral.

Imagen 1
Vista parcial de la sala de maduración de una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
Los padrotes fueron seleccionados siguiendo criterios fenotípicos como buen crecimiento y ausencia de signos clínicos de patologías (Aguirre, 2000; de Donato et al., 2005). Como tallas mínimas de selección, se establecieron 40 g para las hembras y 35 g para los machos, con una edad oscilante entre 10 y 12 meses. Al incorporarse a producción, las densidades se ajustaron a 8 ind/m2, y a una proporción sexual macho: hembra de 1: 0,86 (70 machos y 60 hembras). Al mismo tiempo, se practicó ablación unilateral del pedúnculo ocular a las hembras, para promover el desarrollo gonadal (Aquacop, 1979; Treece, 2000a), ejerciendo presión manual. Los reproductores se mantuvieron por cuatro meses en maduración para evitar deterioro en la calidad de los nauplios.
La alimentación de los reproductores se basó en tasas de alimentación aplicadas sobre la biomasa total ajustada diariamente. Consistió principalmente en productos marinos frescos: mejillones, calamar, biomasa de Artemia enriquecida y gusanos (20%, 40%, 20% y 10%, respectivamente), así como un balanceado preparado in situ, suplementado con vitaminas y minerales (10%). Se consideró el apetito de los camarones, haciendo ajustes cuando fue necesario.
El recambio de agua en los tanques de maduración siguió el esquema de flujo casi constante (22 h/día), interrumpiéndose sólo para retrolavado de filtros y aplicación de Artemia. La aireación, provista por dispositivos “air lift”, combinada con la pendiente de los tanques, generaba patrones de circulación que favorecían la expulsión del agua de menor calidad por la descarga. Los residuos alimenticios, heces y exuvias se extrajeron diariamente por sifón. De la misma manera, se removieron los especímenes muertos empleando un salabardo. Algunos parámetros de calidad de agua fueron determinados diariamente: temperatura, salinidad y pH.
El cortejo se observó desde las 10:00 am, notándose apareos desde ese momento hasta las 6:00 pm. La pesca de hembras apareadas y su paso a desove se realizó entre 5:00 y 6:30 pm, aunque sólo se concretó en ocasión de requerimientos de nauplios. Las hembras con máximo desarrollo gonadal fueron identificadas por su coloración característica (Aquacop, 1979; Brown y Patlan, 1974), pescadas y examinadas por una apropiada fijación del espermatóforo masculino. Las hembras maduras copuladas se transfirieron a la sala de desove, retornándose a sus tanques originales alrededor de las 10 pm, una vez desovadas.

Imagen 2
Reproductores de Penaeus vannamei (izq.) cortejando, y ejemplar adulto (dcha.) en una facilidad comercial de reproducción en Venezuela
En los tanques de desove se acopiaban hasta 12 hembras por tanque (técnica de desove masivo). El agua de estos tanques se ajustaba a una salinidad de 32, quelaba con EDTA (10 ppm), filtraba a 1 micra y recirculaba a través de lámparas ultravioleta.
A partir del segundo clivaje de los huevos, el agua de los tanques de desove se agitaba regular, pero sutilmente, para favorecer su distribución homogénea e intercambio gaseoso. El desarrollo embrionario duró entre 12 y 14 horas, dependiendo de la temperatura. La eclosión ocurrió entre 9:00 y 11:00 am. Los nauplios fueron seleccionados por luz, desplazando una lámpara sobre el tanque, y cosechados entre las 2:00 y 3:00 pm. Al cosecharse, los nauplios fueron cuantificados por medio de una estimación volumétrica y desinfectados con yodo, manteniéndose en flujo continuo hasta su despacho.
Para evaluar el desempeño reproductivo de las hembras de Penaeus vannamei se calcularon los siguientes parámetros:
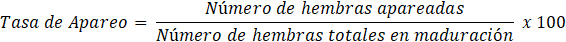 [Tasa de Apareo]
[Tasa de Apareo]
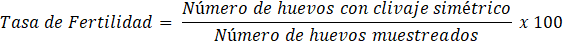 [Tasa de Fertilidad]
[Tasa de Fertilidad]
 [Rendimiento]
[Rendimiento]
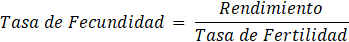 [Tasa de Fecundidad]
[Tasa de Fecundidad]
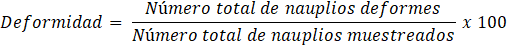 [Deformidad]
[Deformidad]En cuanto a análisis estadísticos, se practicaron correlaciones entre los parámetros ambientales determinados y los índices reproductivos calculados, para establecer la existencia de alguna vinculación entre dichas variables.
Resultados
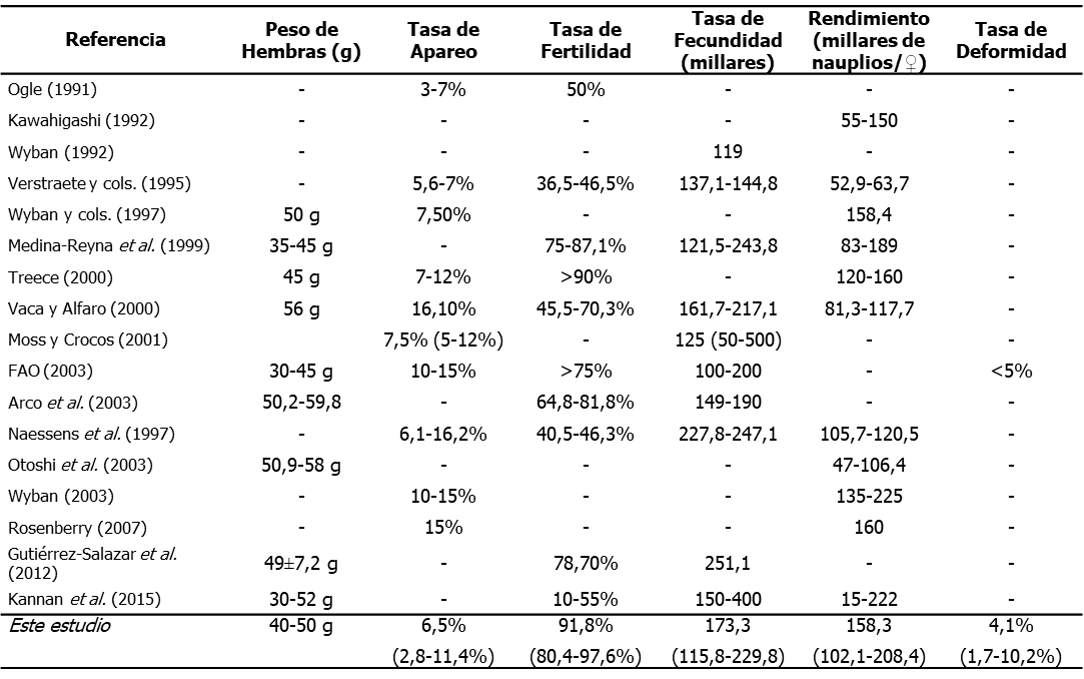
La temperatura del agua osciló entre 24,8 y 30,5 °C, promediando 27,1 °C, con máximos valores entre septiembre y noviembre y mínimos entre enero y marzo (Figura 1). El pH se mantuvo estable en 8,2 durante el tiempo de evaluación. La salinidad tampoco varió mucho durante la evaluación, registrándose mayormente en 38, subiendo levemente a 39 durante los meses fríos.
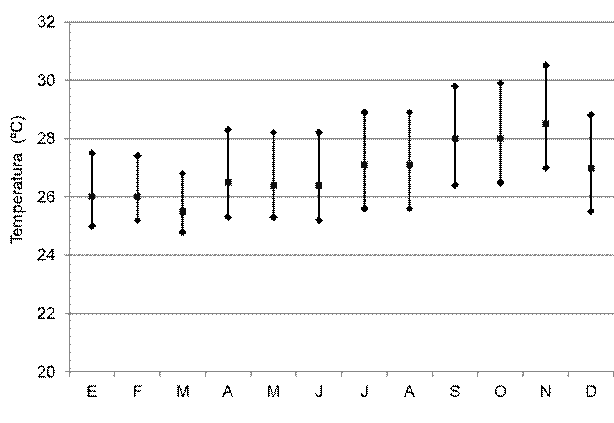
Figura 1
Temperaturas del agua registradas en tanques de maduración durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
El flujo de agua hacia los tanques de maduración promedió 6,6 l/min (1,5 y 15,3 l/min), correspondiendo a una tasa de recambio diario de 108% (24,2 – 247,5%).
Los parámetros reproductivos más importantes se muestran en la Tabla 1, comparados con valores análogos obtenidos de la literatura.
Entre 21 y 84 hembras de Penaeus vannamei copularon por noche en el período estudiado, promediando 51,5 hembras (Figura 2). Todas estas hembras aparearon naturalmente, sin necesidad de practicar inseminación. La tasa de apareo osciló entre 2,76 y 11,40%, con 6,49% como media (Figura 3). Los desoves parciales y abortos fueron muy escasos. La fecundidad de estas hembras varió entre 116 y 230 millares de huevos, promediando 173,3 millares de huevos (Figura 4). La tasa de fertilidad osciló entre 80,40 y 97,59%, con promedio de 91,84 (Figura 5). La producción diaria de nauplios varió entre 2,35 y 14,58 millones, con una media de 7,76 millones de nauplios (Figura 6). El rendimiento fluctuó entre 102 y 208 millares de nauplios por hembra, promediando 158,3 millares de nauplios por hembra (Figura 7). La tasa de deformidad se movió entre 1,7 y 10,2%, con promedio de 4,1% (Figura 8).
Todas las correlaciones planteadas dieron resultados poco significativos, demostrando la falta de vinculación entre las variables examinadas.
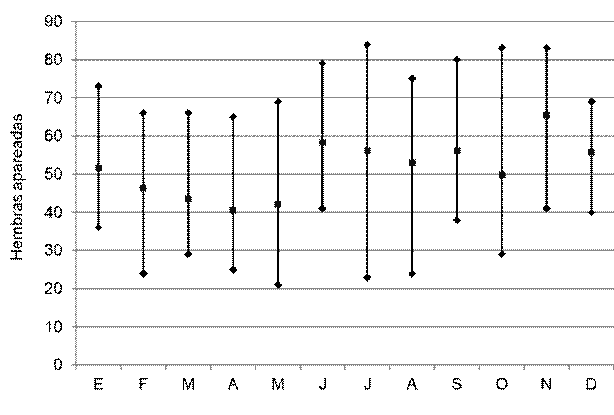
Figura 2
Cópulas diarias registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
Figura 3
Tasas de apareo registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
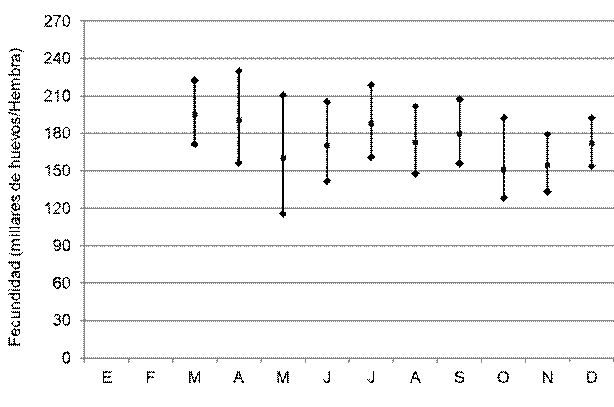
Figura 4
Fecundidades registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
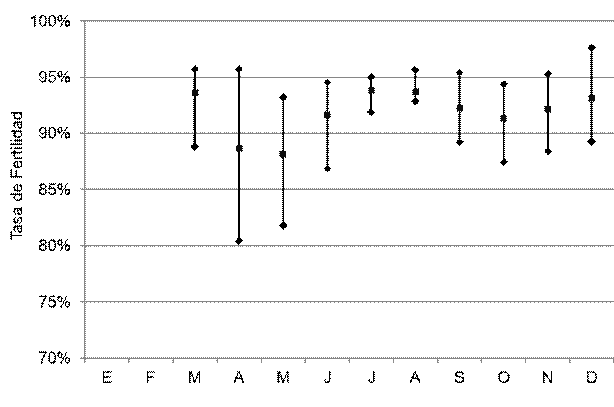
Figura 5
Tasas de fertilidad registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
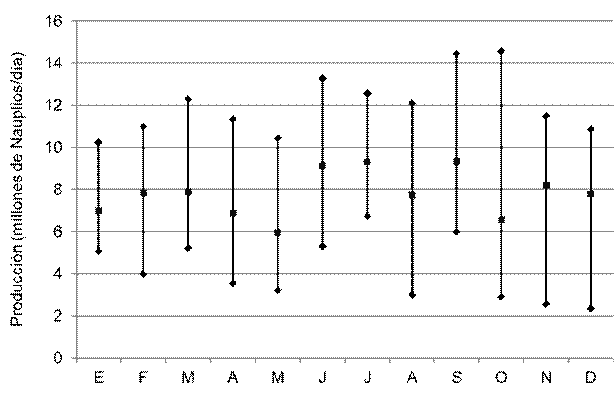
Figura 6
Producciones diarias de nauplios registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
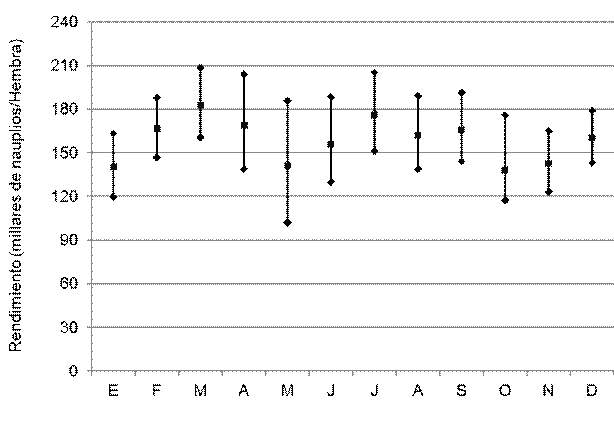
Figura 7
Rendimientos registrados durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
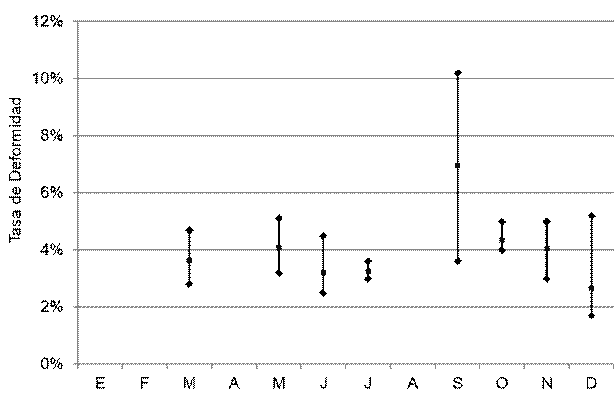
Figura 8
Tasas de deformidad registradas durante un año en una facilidad comercial de reproducción de Penaeus vannamei en Venezuela
Discusión
Las condiciones operativas generales referidas para instalaciones de maduración (forma, materiales, dimensiones, profundidad y aditamentos de los tanques, tipo de recambio) concuerdan con lo establecido como idóneo en la literatura (Treece y Fox, 1993), así como con lo comúnmente aplicado en instalaciones comerciales (Moss y Crocos, 2001). La mayoría de las facilidades de maduración del continente americano trabajan con 20 tanques (Moss y Crocos, 2001), coincidiendo con lo observado en este caso, en clara vinculación a la capacidad requerida para satisfacer los requerimientos de mercado.
Siguiendo a Treece (2000a; 2000b), quien definió los rangos apropiados para la maduración de camarones peneidos, las condiciones fueron satisfactorias para la operación reproductiva. La mayoría de los parámetros medidos coincidieron con los rangos recomendados. Este fue el caso de la temperatura (27 - 29 ºC) y pH (8,0 a 8,2). Sin embargo, la salinidad fue más alta que los niveles recomendados (28 – 36‰). Este incremento a la tolerancia a la salinidad podría estar asociado a la sucesiva selección a este ambiente, lo cual ha conducido a la domesticación.
La tasa de recambio de agua fue bajo en comparación con los estándares recomendados, alrededor de 200% (Browdy et al., 1996; Naessens et al., 1997; Wyban et al., 1997). Ello pudo conducir a niveles elevados de residuos metabólicos en los tanques de maduración, lo cual pudo afectar todas las funciones vitales de los reproductores. En este caso, se debió a problemas eventuales en el sistema de bombeo de la facilidad.
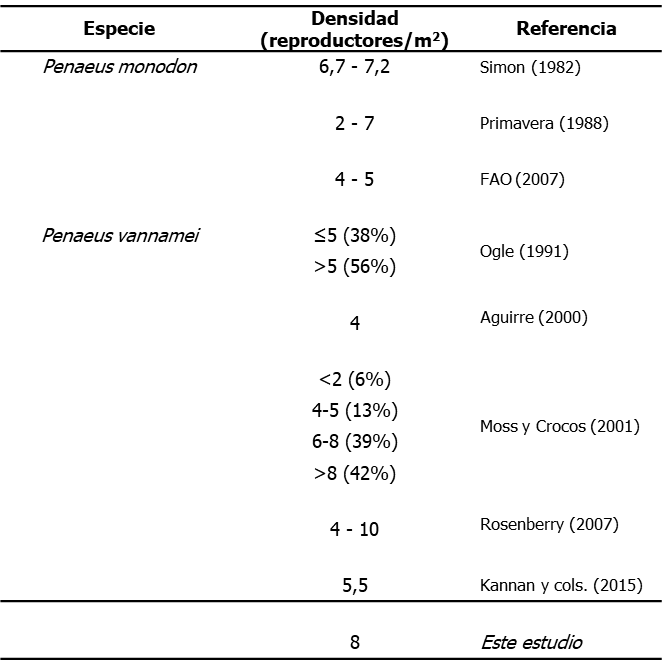
Moss y Crocos (2001) afirmaron que el 95% de las facilidades comerciales de maduración lograban menos de 12 hembras copuladas por noche, según lo cual estos resultados son destacables. No obstante, las tasas de apareo observadas en la cepa domesticada de Penaeus vannamei se encontraron dentro de los límites referidos en la literatura, aunque en el rango inferior (Tabla 1). Esta disminución a lo esperado podría estar asociada a parámetros no determinados de calidad de agua, como el amonio, vinculables al eventual bajo recambio registrado. Es sabido el efecto inhibitorio de sobre la maduración gonádica en camarones peneidos (Treece, 2000b). Por otro lado, aunque es una práctica muy común el uso de altas densidades en facilidades comerciales (Tabla 2), se acepta que los mejores resultados de apareo se consiguen con las densidades más bajas (Rosenberry, 2007), lo cual pudiera explicar los valores relativamente bajos.
Con relación a la fecundidad, se observó un buen solapamiento de la cantidad de huevos producidos por las hembras objeto de estudio con lo referido en la literatura. Este parámetro suele relacionarse con una nutrición bien balanceada, abundante en productos frescos (Nguyen et al., 2009; Sangpradub et al., 1994), como la que se administró. De la misma manera, la fertilidad se corresponde muy bien con lo registrado en trabajos previos. El rendimiento de las hembras se encontró dentro de los rangos señalados en los trabajos anteriores, aunque en su margen superior. La deformidad es uno de los criterios más importantes para hacer inferencias acerca de la calidad de los nauplios y, lógicamente, de los padrotes de los cuales deriva. Este indicador se mantuvo bajo, dentro de los rangos aceptables, salvo en el mes de septiembre cuando se produjo una incorporación masiva de padrotes.
Aunque los programas de mejoramiento genético se han multiplicado globalmente para dar soporte a la masificación del cultivo de camarones peneidos, existen algunas inquietudes sobre el desempeño de las líneas resultantes de los mismos. En este orden de ideas, Campos-Montes et al. (2011) refirieron bajas tasas de fertilización y rendimiento de nauplios en reproductores de camarón blanco provenientes de programas de mejoramiento con elevada endogamia. Arnold et al. (2013) señalaron menores tasas de fecundidad en hembras de Penaeus monodon con 8 generaciones en cautividad, así como una baja eclosión de sus huevos. Doyle (2016) indicó que la pérdida de heterocigosidad asociada a los programas de mejoramiento pueden incrementar la incidencia, prevalencia y letalidad de algunas enfermedades.
Sin embargo, esto se opone a los hallazgos de este trabajo en una cepa de Penaeus vannamei con 14 generaciones en cautividad, buen desempeño reproductivo de los camarones, evidenciado por altas tasas de fecundidad, fertilidad y rendimiento, aunque moderado apareo.
Coherentemente, De Donato et al. (2005) refirieron varios parámetros productivos (sobrevivencia, tasa de crecimiento y conversión alimenticia) que se vieron favorecidos con el paso del tiempo en ejemplares de Penaeus vannamei provenientes de programas genéticos, a pesar de la pérdida de variabilidad. Pareciera ser que la domesticación no implica necesariamente una limitación directa a los estándares productivos de la cepa. Resultados antagónicos pudieran vincularse a la base de selección de los padrotes o problemas de manejo.
Conclusiones
El desempeño reproductivo de la cepa evaluada de Penaeus vannamei fue compatible con parámetros obtenidos en otros estudios, en algunos casos con los valores más altos, a pesar de los eventuales problemas de calidad de agua referidos.
El valor moderado de las tasas de apareos puede estar asociado a las elevadas densidades de acopio utilizadas en los tanques de maduración o al bajo recambio de agua logrado, más que a limitaciones estrictas de la cepa.
En el caso de esta cepa venezolana de Penaeus vannamei, la domesticación no ha conducido a una reducción de su desempeño reproductivo.
Agradecimientos
Los autores expresan su gratitud a Luigi Botazzi por la lectura crítica del manuscrito.
Bibliografía
1. Aguirre, M. E. (2000). Manejo de reproductores para camarones peneidos de telicum abierto. AquaTIC, 10: 1-11.
2. Aquacop. (1979). Penaeid reared brood stock: closing the cycle of P. monodon, P. stylirostris and P. vannamei. Proc. World Maricul. Soc., 10: 445-452.
3. Arcos, F. G., Ibarra, A. M., Palacios, E., Vazquez-Boucard, C., Racotta, I. S. (2003). Feasible predictive criteria for reproductive performance of white shrimp Litopenaeus vannamei: egg quality and female physiological condition. Aquaculture, 228: 335-349.
4. Arnold, S. J., Coman, G. J., Emerenciano, M. (2013). Constraints on seedstock production in eighth generation domesticated Penaeus monodon broodstock. Aquaculture, 410-411: 95-100.
5. Benzie, J. A. H. (1998). Penaeid genetics and biotechnology. Aquaculture, 164: 23-47.
6. Briggs, M., Funge-Smith, S., Subasinghe, R. P., Phillips, M. (2005). Introductions and movement of two penaeid shrimp species in Asia and the Pacific / FAO-FTP-47. Rome, Italy. Food and Agriculture Organization of the United Nations.
7. Browdy, C., McGovem-Hopkins, K., Stokes, A., Hopkins, J., Sandifer, P. (1996). Factors affecting reproductive performance of the atlantic white shrimp, Penaeus setiferus, in conventional and unisex tank systems. J. Appl. Aquacult., 6: 11-25.
8. Brown, A., Patlan, D. (1974). Color changes in the ovaries of penaeid shrimp as a determinant of their maturity. Mar. Fish. Rev., 36: 23-26.
9. Campos-Montes, G. R., Castillo-Juárez, H., Montaldo, H. H. (2011). Inbreeding affects growth, survival, reproduction of white shrimp. Glob. Aquacult. Adv., 14(1): 42-43.
10. Chimsung, N. (2014). Maturation diets for black tiger shrimp (Penaeus monodon) broodstock: a review. Songklanakarin J. Sci. Technol., 36: 265-273.
11. Cuzon, G., Arena, L., Goguenheim, J., Goyard, E., Aquacop. (2004). Is it possible to raise, offspring of the 25th generation of Litopenaeus vannamei (Boone) and 18th generation Litopenaeus stylirostris (Stimpson) in clear water to 40 g? Aquac. Res., 35: 1244-1252.
12. De Donato, M., Manrique, R., Ramírez, R., Mayer, L., Howell, C. (2005). Mass selection and inbreeding effects on a cultivated strain of Penaeus (Litopenaeus) vannamei in Venezuela. Aquaculture, 247: 159-167.
13. Doyle, R. W. (2016). Inbreeding and disease in tropical shrimp aquaculture: a reappraisal and caution. Aquac. Res., 47: 1-15.
14. FAO (2003). Health management and biosecurity maintenance in white shrimp (Penaeus vannamei) hatcheries in Latin America. FAO Fisheries Technical Paper 450. Rome, Italy. Food and Agriculture Organization of the United Nations.
15. FAO (2007). Improving Penaeus monodon hatchery practices: Manual based on experience in India / FAO-FTP 446 (FAO-FTP 44). Roma, Italia: Food and Agriculture Organization of the United Nations.
16. Gutiérrez-Salazar, G. J., González-González, A., Hernández-Acosta, M., Loredo-Osti, J., Guzmán-Sáenz, F. M. (2012). Evaluación de la maduración y la reproducción de camarones Litopenaeus vannamei en sistema de recirculación de agua. Cienc. Pesq., 20: 29-37.
17. Jory, D. E., Cabrera B., T., Polanco, B., Sánchez, R., Millán Q., J., Rosas C., J., Alceste, C., García, E., Useche, M., Agudo, R. (1999). Aquaculture in Venezuela: Perspectives. Aquac. Mag., 25(5): 51-55.
18. Kannan, D., Thirunavukkarasu, P., Jagadeesan, K., Shettu, N., Kumar, A. (2015). Procedure for maturation and spawning of imported shrimp Litopenaeus vannamei in commercial hatchery, south east coast of India. Fish. Aquac. J., 6(4): 1-5.
19. Kawahigashi, D. (1992). A survey of commercial maturation technology in the western hemisphere. In J. A. Wyban (Ed.), Proccedings of the Special Session on Shrimp Farming (pp. 52–54). Baton Rouge, Louisiana, U.S.A.: World Aquaculture Society.
20. Kawahigashi, D. (2010). Overview of P. vannamei culture and broodstock domestication in Asia. Proc. World Acuacul. Aquaculture 2010. Tahiti, French Polinesia.
21. Kuljis, A. M., Brown, C. L. (1992). A market study of specific pathogen-free shrimp. Cent. Trop. Subtrop. Aquacul. Pub., 112: 1-23.
22. Lawrence, A. L., Huner, J. V. (1987). Penaeid shrimp culture in the United States: A brief overview stressing species, seed production, and growout. In C. J. Sindermann (Ed.), Reproduction, maturation, and seed production of cultured species. NOAA Technical Report NMFS 47 (pp. 31-41). Seattle, Washington: U.S. Dept. of Commerce, National Marine Fisheries Service.
23. Medina-Reyna, C. E., Beltrán-González, M. H., Salinas-Orta, H. T. (1999). Nauplii production of white shrimp, Litopenaeus vannamei (Decapoda: Penaeidae), on-board of commercial trawlers. Rev Biol. Trop., 47: 913-916.
24. Moss, S. M., Crocos, P. J. (2001). Global Shrimp OP: 2001 - Maturation. Glob. Aquacult. Adv., 4(4): 28-29.
25. Naessens, E., Lavens, P., Gomez, L., Browdy, C. L., Mcgovem-Hopkins, K., Spencer, A. W., Kawahigashi, D., Sorgeloos, P. (1997). Maturation performance of Penaeus vannamei co-fed Artemia biomass preparations. Aquaculture, 155: 87-101.
26. Nguyen, D. H., Wouters, R., Wille, M., Thanh, V., Kim Dong, T., Hao, N. Van Sorgeloos, P. (2009). A fresh-food maturation diet with an adequate HUFA composition for broodstock nutrition studies in black tiger shrimp Penaeus monodon (Fabricius, 1798). Aquaculture, 297: 116-121.
27. Ogle, J. T. (1991). Maturation of Penaeus vannamei based upon a survey. Gulf Res. Rep., 8: 295-297.
28. Otoshi, C. A., Arce, S. M., Moss, S. M. (2003). Growth and reproductive performance of broodstock shrimp reared in a biosecure recirculating aquaculture system versus a flow-through pond. Aquac. Eng., 29: 93-107.
29. Primavera, J. H. (1988). Maturation, reproduction, and broodstock technology. In Biology and culture of Penaeus monodon (pp. 37–57). Tigbauan, Iloilo, Philippines. Aquaculture Department of the Southeast Asian Fisheries Development Center.
30. Sangpradub, S., Fast, A. W., Piyatiratitivorakul, S., Menasveta, P., 1994. Effects of different feeding regimes on ovarian maturation and spawning of pond-reared giant tiger prawn in Thailand. Aquac. Int., 2: 49-58.
31. Scelzo, M. (1983). Crustáceos. In F. Cervigón (Ed.), La acuicultura en Venezuela; estado actual y perspectivas (pp. 57-63). Caracas, Venezuela. Editorial Arte.
32. Simon, C. M. (1982). Large-scale, commercial application of penaeid shrimp maturation technology. J. World Maricul. Soc., 13: 301-312.
33. Rosenberry, B. (2007). Shrimp maturation tanks - Size matters. Recuperado de www.shrimpnews.com.
34. Treece, G. D. (2000a). Shrimp maturation and spawning. In C. C. Tamaru, C. S., Tamaru, J. P. McVey, K. Ikuta (Eds.). Spawning and maturation of aquaculture species. Proceedings of the 28th US-Japan Natural Resources Aquacultue Panel / UJNR Technical Report No 28 (pp. 121-134). Kihei, Hawai, USA. University of Hawaii/Sea Grant College Program.
35. Treece, G. D. (2000b). Shrimp Culture. In R. R. Stickney (Ed.). Encyclopedia of Aquaculture (pp. 798-868). New York, USA. John Wiley and Sons, Inc.
36. Treece, G. D., Fox, J. M. (1993). Design, operation and training manual for an intensive culture shrimp hatchery, with emphasis on P. monodon and P. vannamei. TAMU-SG-93-505. Galveston, Texas, USA. Texas AM University, Sea Grant College Program.
37. Vaca, A. A., Alfaro, J. (2000). Ovarian maturation and spawning in the white shrimp, Penaeus vannamei, by serotonin injection. Aquaculture, 182: 373-385.
38. Verstraete, P., De La Mora, B., Lavens, P. (1995). Maturation of Penaeus vannamei by using dry pellets as a partial substitute of the natural diet. In P. Lavens, E. Jaspers, I. Roelants (Eds.), Larvi´95 - Fish and Shellfish Larviculture Symposium (pp. 397–399). Gent, Belgium: European Aquaculture Society.
39. Wyban, J. (1992). Development of high health shrimp using specific pathogen free SPF broodstock Penaeus vannamei. In J. A. Wyban (Ed.), Proccedings of the Special Session on Shrimp Farming (pp. 254–260). Baton Rouge, Louisiana, U.S.A. World Aquaculture Society.
40. Wyban, J. (2003). Penaeus vannamei seedstock production: Recent developments in Asia. Glob. Aquacult. Adv., 6: 78-79.
41. Wyban, J. (2007). Domestication of Pacific white shrimp revolutionizes aquaculture. Glob. Aquacult. Adv., 10(4): 42-44.
42. Wyban, J. A., Martínez, G., Sweeney, J. N. (1997). Adding paprika to Penaeus vannamei maturation diet improves nauplii quality. World Aquacult., 28: 59-62.
Notas de autor
arnaldo.figueredo@ne.udo.edu.ve