Desarrollo y validación de un método para la cuantificación de fructooligosacáridos en un helado prebiótico
Development and validation of a method for the quantification of fructooligosaccharides in a prebiotic ice cream
Desarrollo y validación de un método para la cuantificación de fructooligosacáridos en un helado prebiótico
Journal of Pharmacy & Pharmacognosy Research, vol. 6, núm. 2, pp. 108-116, 2018
Asociación de Académicos de Ciencias Farmacéuticas de Antofagasta
Recepción: 16 Agosto 2017
Recibido del documento revisado: 27 Noviembre 2017
Aprobación: 03 Enero 2018
Publicación: 20 Enero 2018
Resumen: Contexto: Los fructooligosacáridos (FOS) se conocen como oligofructanos u oligofructosa, clasificados como prebióticos. Uno de los métodos más empleados en la industria para la cuantificación y control de calidad de sustancias nutracéuticas es el método de cromatografía líquida de alta resolución (CLAR). Objetivos: Desarrollar un procedimiento eficaz para la determinación de FOS por CLAR en materias primas y un helado prebiótico. Métodos: Para la separación cromatográfica se empleó un CLAR con detector de índice de refracción (IR). La separación se realizó empleando dos columnas acopladas Sugar-pak I™ usando un procedimiento isocrático con agua tipo 1 a 0,35 mL/min. Como estándares se emplearon kestosa (GF2), nistosa (GF3) y fructofuranosilnistosa (GF4). La robustez se evaluó aplicando el test de Youden y Steiner. Resultados: Se lograron buenas correlaciones lineales (y = 14191,4470 x + 285684,2, r2 = 0,9904) dentro del rango de concentración de 8,0-12,0 mg/mL. Las recuperaciones de FOS fueron del 99.5% con desviación estándar relativa intradía e interdía (RSD) menor al 0,8%. El test de robustez demostró que los parámetros de temperatura de la columna y velocidad de flujo son factores críticos en el método. Conclusiones: Este método confiable, simple y rentable podría aplicarse al monitoreo rutinario de FOS (GF2, GF3 y GF4) en materias primas y helados prebióticos.
Palabras clave: fructofuranosilnistosa, helado, índice de refracción, kestosa, nistosa, prebiótico.
Abstract: Context: Fructooligosaccharides (FOS) are known as oligofructanes, oligosaccharides or oligofructose, which fall within the concept of prebiotics. One of the methods most commonly used in the industry for quantification and quality control nutraceutical substances classification is the method of high performance liquid chromatography (HPLC). Aims: To develop a procedure for the determination of FOS by HPLC in raw materials and a prebiotic ice cream. Methods: For the chromatographic separation, an HPLC was used with a refractive index detector (IR). The separation was performed using two columns coupled Sugar-pak I™ using an isocratic procedure with water type 1 at 0.35 mL/min. Kestose (GF2), nistose (GF3) and fructofuranosylnystose (GF4) were used as standards. Robustness was assessed by applying the Youden and Steiner test. Results: Good linear correlations were obtained (y = 14191.4470 x + 285684.2, r2 = 0.9904) within the concentration range of 8.0-12.0 mg/mL. The FOS recoveries were 99.5% with the intra-day and inter-day relative standard deviation (RSD) less than 0.8%. The robustness test showed that the temperature parameters of the column and flow velocity are critical factors in the method. Conclusions: This reliable, simple and cost-effective method could be applied to the routine monitoring of FOS (GF2, GF3, and GF4) in raw materials and prebiotic ice creams.
Keywords: fructofuranosylnystose, ice cream, kestose, nystose, prebiotic, refractive index.
INTRODUCCIÓN
La evolución de la industria alimenticia ha introducido un nuevo concepto de "alimento funcional" el cual abarca todo alimento capaz de aportar un nutriente o componente con una actividad selectiva relacionada con una o varias funciones del organismo, con un efecto fisiológico benéfico y a la vez saludable (Bersaneti et al., 2016). Esta definición ha generado la búsqueda de componentes capaces de enriquecer las propiedades nutricionales en alimentos de consumo masivo, entre estos componentes se agrupan los prebióticos; los cuales son oligosacáridos no digeribles por el tracto digestivo pero elementales para favorecer el crecimiento de la flora bacteriana benéfica del tracto intestinal (Roberfroid, 2002).
Los fructooligosacáridos (FOS) son compuestos que poseen como principal característica en su estructura química una molécula de glucosa ligada a un número variable de moléculas de fructosa que oscila entre 2 a 10 unidades. Los enlaces que unen las moléculas de fructosa en el oligosacárido resisten la hidrólisis de las enzimas digestivas humanas llegando hasta la última porción del intestino grueso, sirviendo como sustrato para la microflora benéfica del colon (Hermann et al., 2005). El consumo de FOS favorece el crecimiento de bifidobacterias y lactobacilos, beneficiando el organismo, regula el tránsito intestinal, la absorción de minerales y mejoran la inmunidad del organismo El efecto bifidogénico se da gracias a la fermentación de los FOS de forma anaerobia, el aumento de la población de bacterias benéficas reprime el crecimiento de los organismos patógenos generadores de sustancias toxicas y cancerígenas en el colon (Roberfroid, 1996). La acción positiva de las bifidobacterias en el organismo extiende beneficios como la reducción de niveles de azúcar y grasas en la sangre, inhibiendo la lipogénesis hepática, disminuyendo el riesgo de arterioesclerosis, normalizando la presión sanguínea y mejorando el metabolismo de las personas diabéticas, o con problemas de colesterol alto o cardiovasculares (Larico Perez et al., 2016).
Con el emergente mercado de alimentos funcionales se hace necesario, desarrollar métodos capaces de evaluar este tipo de componentes declarados y establecer la actividad y vida útil de los mismos. En cromatografía líquida se cuenta con una variada gama de opciones, por parte de las fases estacionarias, a necesidad de las diferentes moléculas que cada día surgen en el mercado farmacéutico, alimenticio y biotecnológico. Existen diversos métodos para la cuantificación de sacáridos, oligosacáridos y fibra soluble, sin embargo, una de las técnicas más confiables es la cromatografía liquida de alta resolución. Esta técnica es específica y minimiza las interferencias de matriz y el tiempo de tratamiento de la muestra en métodos tradicionales. Esta es ampliamente utilizada gracias a que reúne características de un método idóneo para el análisis, alta sensibilidad, fácil adaptación, exactitud en la cuantificación, separación de sustancias químicas de alto interés en la industria, además de su gran variedad en la adaptación de detectores, columnas y demás aditamentos que permiten desarrollar métodos altamente confiables (Foitzich Molina, 2013).
El objetivo de esta investigación fue validar un método para cuantificar FOS en materia prima FOS comercial mediante CLAR con detector de índice de refracción (IR) e implementar el método a una muestra de helado prebiótico. Las columnas con micropartículas de gel de intercambio catiónico, capaces de excluir por tamaño moléculas en matrices complejas, fue la mejor opción para realizar los ensayos y establecer un método cromatográfico eficiente capaz de separar los analitos de interés para la matriz estudiada en esta investigación.
MATERIALES Y MÉTODOS
Los ensayos para el desarrollo y validación del método para la cuantificación de FOS en un helado prebiótico mediante CLAR–IR se realizaron en el Laboratorio Fisicoquímico de Carval de Colombia, Cali durante los meses de enero, febrero, agosto y septiembre de 2016.
Estándares y reactivos
Se emplearon estándares de FOS (1-kestosa (GF2) pureza: 99,8%; nistosa (GF3) pureza: 99,1% y 1F-fructofuranosilnistosa (GF4) pureza: 97,6%), marca Wako® Chemicals, USA, lote AWL2713. Como materia prima certificada se empleó el estándar secundario de FOS (Yunehing, lote 1501080112 y lote 1501010101); edetato cálcico disódico (Merck, ref.1.08407.0250, lote VP526507319); ácido acético (Merck, ref. 1.00063.2500, lote K47121363540); agua desionizada tipo 1, preparada usando un equipo de purificación de agua Wasserlab® Autwomatic. Como muestra de análisis para evaluar el método se empleó helado prebiótico formula de ensayo Lote 1605F4 (formulado de FOS 15,0%).
Certificación estándar de trabajo de FOS
Se realizó la certificación de un estándar de trabajo empleando los estándares de referencia. Se evaluaron seis muestras preparadas por dos analistas. El resultado se comparó con la potencia individual de GF2, GF3 y GF4 dando así una pureza grupal de FOS de 90,0% en base húmeda.
Soluciones estándares y curva de calibración
Para evaluar la linealidad del sistema se prepararon soluciones a cinco niveles de la concentración del activo. Para tal fin, del estándar secundario de FOS se realizaron cinco pesajes cubriendo el rango de concentración de la muestra desde 80 a 120%, es decir, 8,0 a 12,0 mg/mL, representando la concentración de FOS en la solución de 10 mg/mL el punto 100% de la curva. Usando agua tipo 1 como solvente. La materia prima FOS se empleó para realizar la evaluación y comparación de linealidad del método. Después de haber definido las condiciones cromatográficas finales para descartar la interferencia de alguna señal se analizó previamente un blanco del solvente.
Preparación de la muestra de helado
Se pesaron aproximadamente 3,0 g de la fórmula de ensayo de helado prebiótico (15% de FOS) y se transfirieron a un balón volumétrico de 50 mL. Se adicionaron 30 mL de agua tipo 1, 1 mL de ácido acético. Se agitó manualmente durante 1 min. Posteriormente, la muestra se dejó en reposo por 5 min. Se observó la precipitación de la proteína y se llevó al aforo con agua tipo 1, luego se agitó y se transfirió una porción de la solución a un tubo de centrífuga y se centrifugó durante 10 min (centrífuga Thermo IEC, Medilite, USA). La porción sobrenadante se filtró por membrana 0,22 µm (Millex® Syringe filters PVDF, Merck Millipore, USA). La concentración final de la muestra estuvo entre 9 a 10 mg/mL de FOS.
Instrumentación y condiciones analíticas
El cromatógrafo líquido de alta resolución (CLAR) utilizado fue el modelo Alliance 2695e (Waters, Milford, MA, USA). Las columnas analíticas del CLAR fueron dos columnas acopladas Sugar-pak I™ 10 µm, 6,5 mm × 300 mm (Waters®) la temperatura de las columnas se mantuvo a 90°C empleando un horno externo para análisis con detector de índice de refracción 2414 Waters, sistema operativo y de procesamiento Empower 3®, balanza analítica Mettler Toledo AB204-S/FACT, centrifuga Thermo IEC, Medilite. La fase móvil fue agua tipo 1. El acondicionamiento de las columnas se realizó siguiendo las instrucciones recomendadas por el fabricante, usando un gradiente para la velocidad de flujo aumentando cada hora 0,1 mL/min el flujo y 30°C la temperatura del horno para columna hasta llegar a la condición final. Las condiciones finales fueron flujo 0,35 mL/min, temperatura del horno de columnas 90°C, el volumen de inyección 10 µL, tiempo total de corrida cromatográfica 37 minutos. Para el detector de índice de refracción se programó una temperatura de 40°C y sensibilidad de 16. Se estableció un conjunto de parámetros de eficiencia para el método los cuales están resumidos en la Tabla 1. La curva de calibración se evaluó por el método de mínimos cuadrados.
Evaluación de la recuperación de FOS en la muestra de helado prebiótico
Como límite de control se estableció que el porcentaje de recuperación promedio para tres muestras de helado prebiótico preparadas debía encontrarse entre 98,0 al 102,0%. El análisis de los resultados de la validación se realizó con el programa de procesamiento de datos Excel.
| Parámetros | Especificaciones | ||
| Kestosa (GF2) | Nistosa (GF3) | Fructofuranosilnistosa (GF4) | |
| Tiempo de retención (min) | Entre 17,2 y 21,0 | Entre 15,6 y 19,0 | Entre 14,5 y 17,7 |
| Factor de asimetría | < 2,0 | < 2,0 | < 2,0 |
| Platos teóricos | > 1000 | > 1000 | > 1000 |
| Resolución | > 1,0 | > 1,0 | > 1,0 |
Análisis estadístico
Especificidad: Evaluación de las interferencias cromatográficas
Se preparó una muestra de cada estándar (GF2, GF3 y GF4) al 100% de la concentración de trabajo. Se inyectaron los estándares en el cromatógrafo y se identificaron las respectivas señales cromatográficas. Se evaluó simultáneamente la existencia de alguna interferencia del diluente con las señales de los activos. Se inyectaron 10 µL de diluente bajo las condiciones cromatográficas establecidas.
Linealidad del sistema
Se evaluó la linealidad del sistema empleando soluciones a cinco niveles de la concentración del activo. Construyendo una curva de concentración entre 8,0 mg/mL y 12,0 mg/mL empleando el estándar secundario de FOS. Para aceptar la validación se establecieron los siguientes criterios de aceptación: 1) coeficiente de regresión mayor a 0,990; 2) test de hipótesis para la pendiente: ts > ttabla, pendiente significativamente diferente de cero; 3) test de hipótesis para el intercepto: ts < ttabla, intercepto no es significativamente diferente de cero; 4) análisis de varianza para la regresión lineal: Fs > Ftabla, la regresión es estadísticamente representativa; y por último 5) el criterio de aceptación para la linealidad: Fs < Ftabla, la falta de ajuste no es estadísticamente representativa.
Linealidad del método
Se prepararon muestras a cinco niveles de concentración que cubrieran el rango de 80% a 120% de la concentración de análisis. Para ello se realizaron pesajes de FOS materia prima (lote 1501010101), que fue previamente analizado arrojando un resultado de valoración de 89,9% B.H. Se establecieron los mismos criterios de aceptación que se consideraron para la linealidad del sistema.
Repetibilidad
Se prepararon seis muestras al 100% de la concentración de análisis empleando la materia prima FOS (lote 1501010101), posteriormente se realizó una inyección de cada muestra en el equipo cromatográfico. Se ejecutó dicho procedimiento durante tres días en que se evaluó la precisión y se expresó los resultados en términos de porcentaje del analito recuperado, calculado mediante la ecuación de la recta obtenida para el sistema; a fin de facilitar la comparación entre los resultados obtenidos por el mismo analista en el mismo equipo y en un periodo corto de tiempo. Para verificar la validez de la repetibilidad se estableció que la desviación estándar relativa por día de análisis entre los datos obtenidos por cada día de análisis debía ser menor al 2,0%.
Precisión intermedia
La precisión intermedia se evaluó a partir de los 18 resultados obtenidos durante los tres días en los que se realizó la prueba de repetibilidad. Se estableció como parámetro de validez que la desviación estándar relativa entre los datos obtenidos en los tres días de análisis debía ser menor al 2,0%. Adicionalmente al realizar el test Fisher (nivel de significación del 95%) Fs < Ftabla, lo cual indica que no existe diferencia significativa entre las varianzas obtenidas por los dos analistas.
Exactitud
La exactitud se evaluó a partir de las curvas de calibración de FOS obtenidas para el sistema y para el método en todo el intervalo analizado, que comprendió de 80% hasta 120% de la concentración de análisis. Se evaluó en términos de porcentaje de analito recuperado, calculado mediante la ecuación de la recta obtenida para el sistema. La evaluación de la influencia de la concentración en la exactitud se realizó mediante el test de G de Cochram (nivel de confianza del 95%), el criterio de aceptación establecido fue: Gexp < Gtabla, lo cual indica que el factor concentración no tiene influencia en la variabilidad de los resultados. Como límite de control se estableció que el porcentaje de recuperación promedio por nivel de concentración debe encontrarse entre 98,0% al 102,0%.
Robustez
La robustez se evaluó aplicando el test de Youden y Steiner. Para cada uno de los ocho ensayos se preparó una muestra al 100% de la concentración de trabajo, empleando materia prima de FOS (lote 1501010101), y se determinó el porcentaje de recuperación de cada una, por comparación contra una solución estándar secundario, analizada por triplicado bajo las condiciones nominales del método. Los factores que se evaluaron durante la prueba de robustez fueron: velocidad de flujo, temperatura de la columna, temperatura del detector y tiempo de espera para inyección (estabilidad en solución). Con lo cual se determinaron los parámetros críticos del método.
RESULTADOS Y DISCUSIÓN
En la Tabla 2 se presenta un resumen de los resultados de la validación del método. En la Tabla 3 se presentan los resultados de la evaluación estadística para la repetibilidad, precisión intermedia y exactitud. En la Tabla 4 los resultados de la evaluación estadística para la robustez.
Las condiciones cromatográficas se optimizaron para favorecer los resultados de resolución y se cumplió con todos los parámetros establecidos para la evolución de la eficiencia del método descritos en la Tabla 1. Las condiciones cromatográficas mostraron un perfil como el que se observa en la Fig. 1. El método cumplió todos los criterios de aceptación indicados para cada prueba de desempeño de la validación.
El creciente auge de los alimentos funcionales desafía los métodos fisicoquímicos de control establecidos para el análisis de alimentos. La adición de sustancias prebióticas como los FOS implica el uso de tecnologías más específicas que garanticen un análisis de control de calidad confiable para el alimento. Si bien es cierto que existen métodos para la cuantificación de FOS como fibra dietaria, estos métodos no discriminan la cantidad de oligosacárido específico dentro del alimento, generando falsos positivos por sustancias de propiedades fisicoquímicas similares. En la revisión bibliográfica realizada para el desarrollo de un método eficiente para la cuantificación de FOS en un helado prebiótico, se encontraron métodos cromatográficos trabajados con detectores de índice de refracción o evaporación detección de dispersión (Li et al., 2014), ideales y populares para el análisis de sacáridos y oligosacáridos (Valliyodan et al., 2015), el medio de separación consistía en una fase de acetonitrilo: agua (Rodríguez-Gómez et al., 2015) y una fase estacionaria de sílice aminada (columnas amino) (Krol y Grzelak, 2006); sin embargo, este tipo de columnas con relleno amino pierde su eficiencia rápidamente debido al desgaste de su grupo funcional, a medida que se retienen azucares reductores y otras sustancias capaces de interactuar con el grupo amino.
Evaluando una serie de columnas comerciales para el análisis de oligosacáridos se llegó a la columna Sugar-pak I™ 10 µm 6,5 mm × 300 mm (Waters®), esta columna posee un relleno de gel de intercambio catiónico de micropartículas de calcio. Esta es recomendada principalmente para separar monosacáridos, polioles, y alcoholes. Los disacáridos y azúcares más grandes son también separados según el peso molecular. Así, esta columna acopla dos funciones importantes para la separación de los tres analitos de interés: intercambio catiónico (Walton, 1995) y exclusión por tamaño.
La alta solubilidad de la materia prima FOS en agua permitió el uso de la misma como solvente y fase móvil del método. El uso de una sola columna no fue suficiente para realizar la separación de los picos obteniendo resultados de resolución inadecuados, por lo tanto, se emplearon dos columnas acopladas para aumentar la cantidad de relleno y mejorar la interacción de los analitos con la fase estacionaria. Los parámetros de temperatura y velocidad de flujo fueron indispensables para obtener resultados óptimos, se evaluaron temperaturas desde los 70°C hasta los 90°C evidenciando un aumento en la resolución de los picos a mayor temperatura, así mismo se trabajó en un rango de flujo de 0,8 mL/min a 0,25 mL/min donde ocurrió que al disminuir el flujo la resolución entre los picos de interés también mejoraba. Para el uso de las columnas se siguió las recomendaciones de uso y cuidado suministradas por el fabricante, realizando regeneración continua de la columna después de cada ensayo con una solución de edetato cálcico disódico 50 mg/L (acuoso).
Luego de obtener las condiciones ideales se validó el método para la cuantificación de FOS en materia prima comercial de alta pureza. Esta materia prima fue valorada y empleada en la formulación de un helado prebiótico endulzado totalmente con FOS, (15,0% p/p). Se realizó el tratamiento de la muestra extrayendo la fase acuosa y analizando bajo las mismas condiciones cromatográficas de la materia prima se obtuvo una recuperación de 98,0% de FOS en el helado, es decir 14,7% p/p.
| Evaluación de parámetros | Linealidad del sistema | Linealidad del método |
| Parámetro estadístico | Valor obtenido | Valor obtenido |
| b (Pendiente) | 285684,2 | 281328,38 |
| a (Intercepto) | 14191,447 | 55197,1804 |
| R (Coeficiente de correlación) | 0,9904 | 0,994 |
| Test de hipótesis para la pendiente | ||
| t exp b | 25,81 | 33,67 |
| t tabla (p=0,05; 13 gl) | 2,16 | 2,16 |
| Conclusión | t exp b >> t tabla | t exp b >> t tabla |
| Test de hipótesis para el intercepto | ||
| t exp a | 0,13 | 0,65 |
| t tabla (p=0,05; 13 gl) | 2,16 | 2,16 |
| Conclusión | t exp a < t tabla | t exp a < t tabla |
| Límites de confianza para la pendiente | ||
| Límite superior | 309593,6 | 299377,2 |
| Límite inferior | 261774,7 | 263279,5 |
| Límites de confianza para el intercepto | ||
| Límite superior | 256127,63 | 237318,5 |
| Límite inferior | -227744,73 | -126924,14 |
| Test de Fisher para la regresión | ||
| F exp | 666,33 | 1133,9 |
| F tabla | 4,67 | 4,67 |
| Conclusión | F exp >> F tabla | F exp >> F tabla |
| Test de Fisher para la linealidad | ||
| F exp | 0,15 | 0,27 |
| F tabla | 3,71 | 3,71 |
| Conclusión | F exp < F tabla | F exp < F tabla |
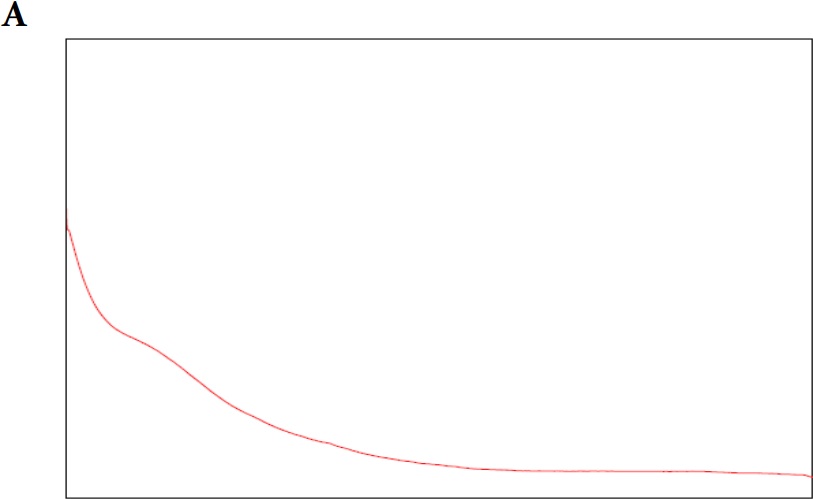
Figura 1
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
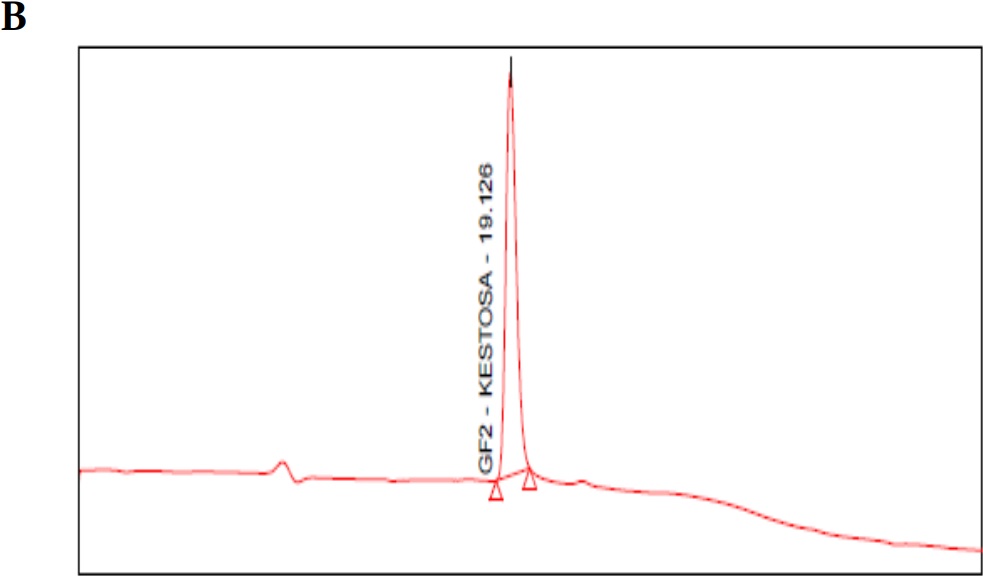
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
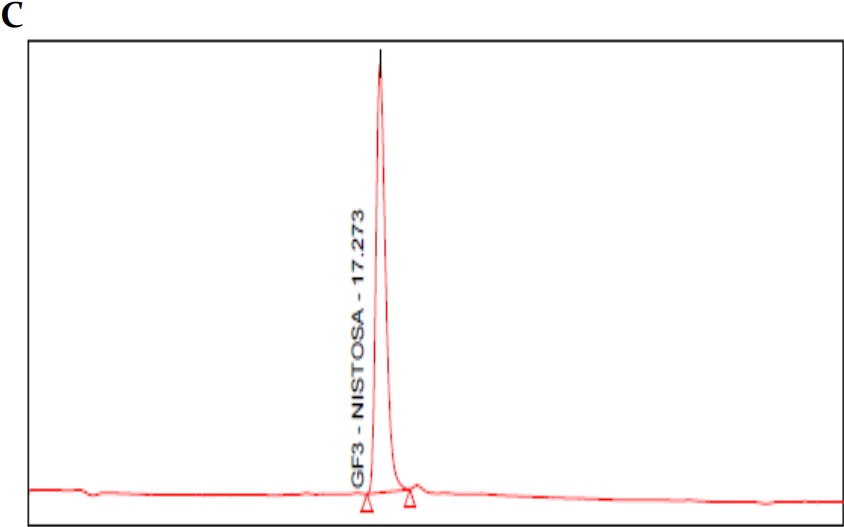
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
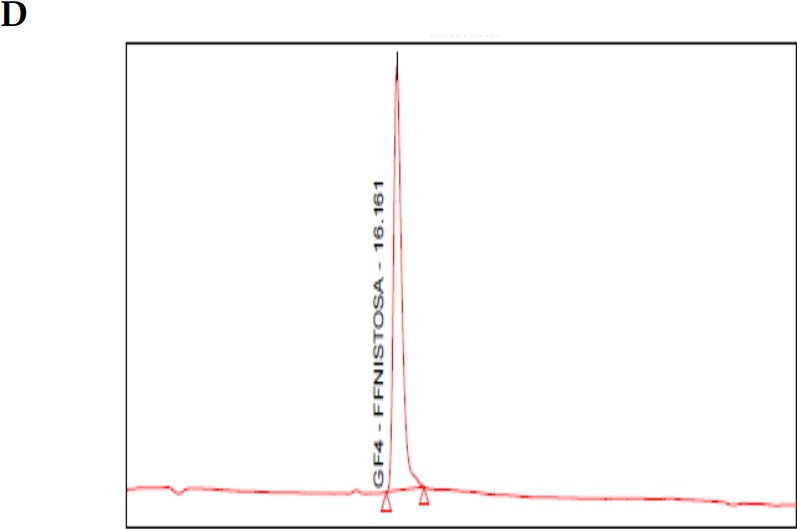
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
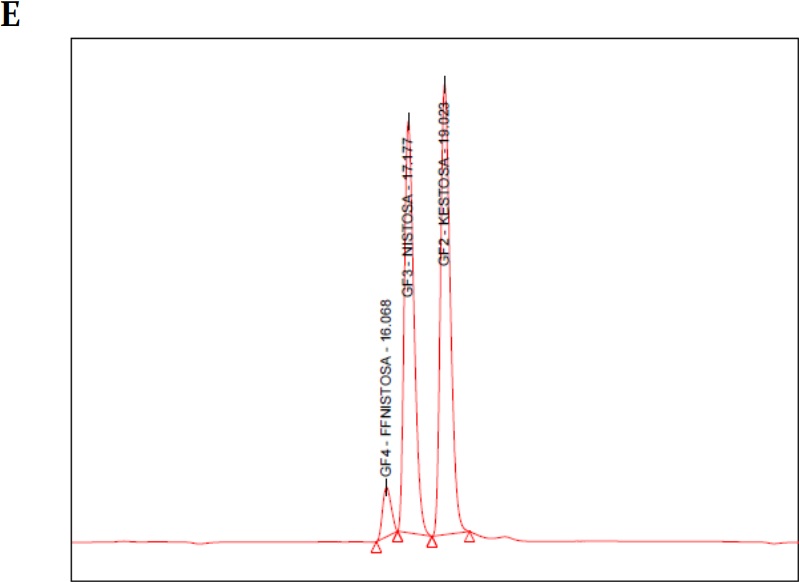
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
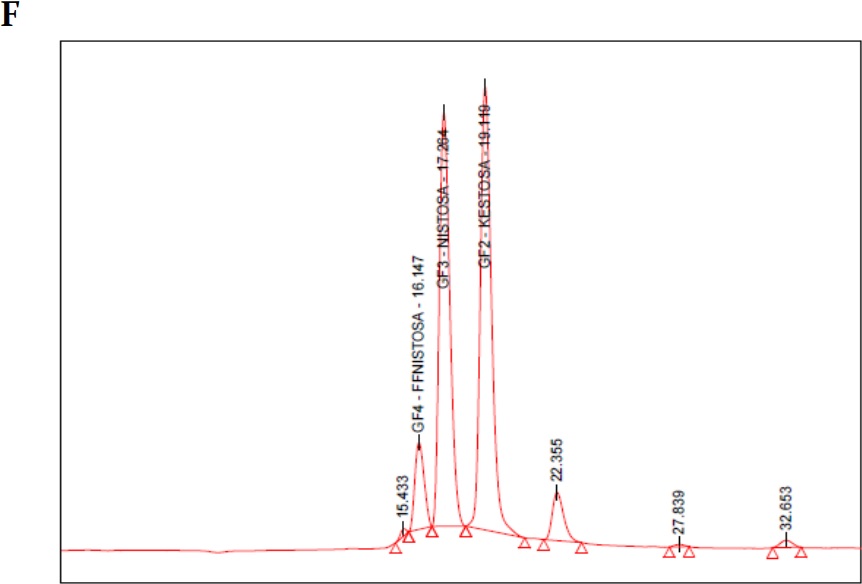
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
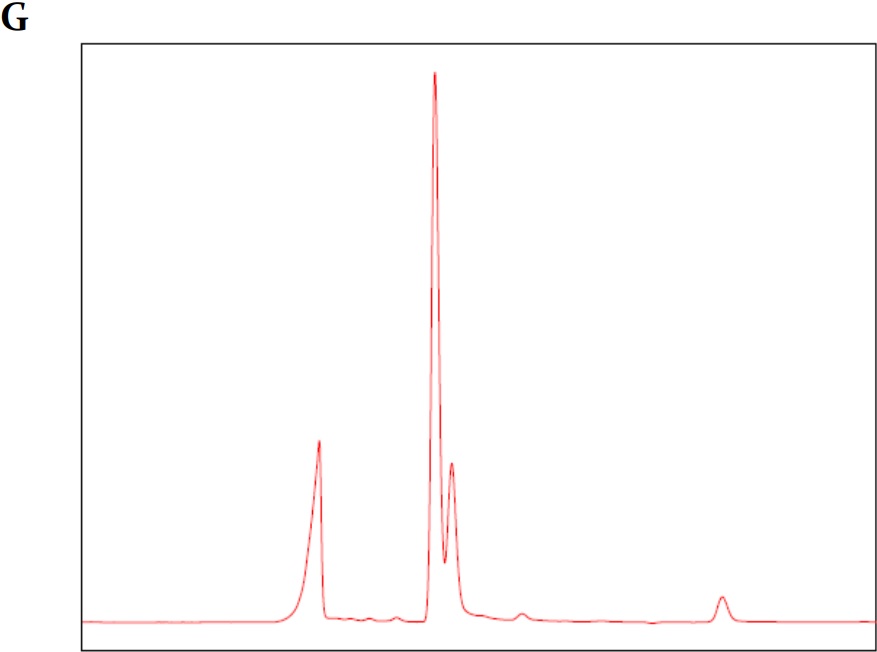
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
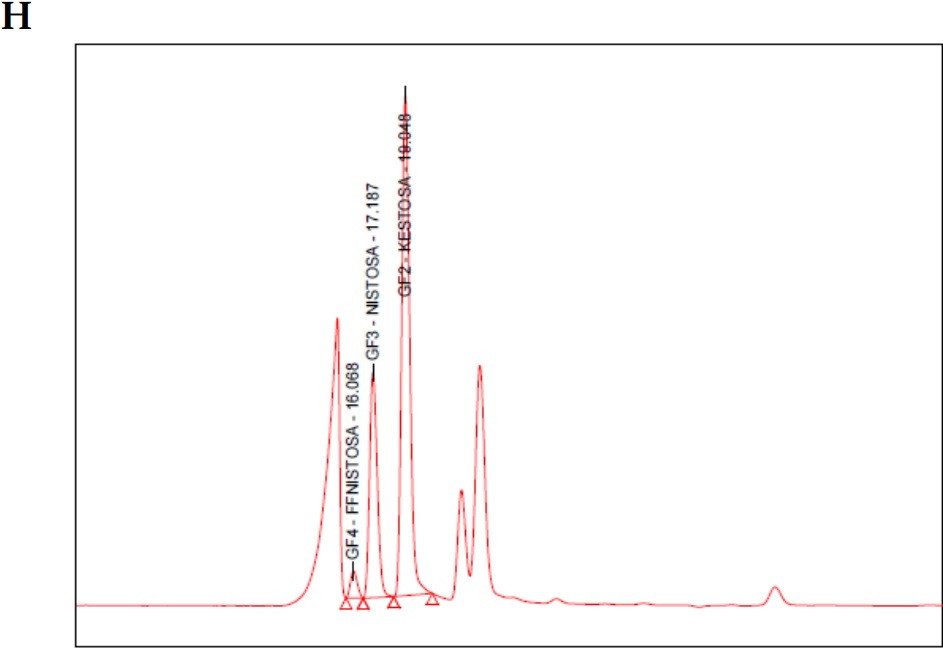
Figura 1 (Cont.)
(A) Cromatograma blanco fase móvil (agua tipo 1); (B) cromatograma estándar 1-kestosa; (C) cromatograma estándar de nistosa; (D) cromatograma estándar de 1-fructofuranosilnistosa; (E) cromatograma mezcla de estándares primarios de FOS; (F) cromatograma estándar secundario FOS (MP FOS LOTE 1501010101); (G) cromatograma blanco de helado prebiótico; (H) cromatograma helado prebiótico con FOS 15%.
| Comparación de pendientes | Pendientes | Interceptos |
| t exp b | 0,31 | 0,29 |
| t tabla | 2,06 | 2,06 |
| Conclusión | t exp b < t tabla | t exp a < t tabla |
| Parámetro estadístico | Valor obtenido | |
| Resultados de precisión intermedia | % de recuperación promedio (n=18) | 99,5 |
| Σ n-1 (N=18) | 0,8 | |
| D.r.s (%) | 0,80% | |
| Concepto = d.r.s. (%) < 2,0 % | Cumple | |
| Análisis de varianza de un solo factor | F calc | 3,29 |
| F tab | 3,68 | |
| Concepto: F calc < F tab | Cumple | |
| Test G de Cochram para evaluar la influencia de la concentración en la exactitud | Parámetro estadístico | Valor obtenido |
| Valor máximo de varianza | 1,3 | |
| Sumatoria de la varianza | 4,1 | |
| G exp | 0,32 | |
| G tabla (p=0,05 ; K=5; n=3) | 0,683 | |
| Concepto | G exp < G tab | |
| El factor concentración no influye en la variabilidad de los resultados |
| Factor * | Variabilidad │X – x│ | S√2 | Concepto V < S√2 | ||
| A,a | Tiempo de espera para inyección | 0,98 | 1,11 | El factor NO es crítico | |
| B,b | Velocidad de flujo | 29,60 | El factor ES crítico | ||
| C,c | Temperatura de la columna | 6,69 | El factor ES crítico | ||
| D,d | Temperatura del detector | 0,59 | El factor NO es crítico | ||
*Variabilidad para cada factor evaluada según la matriz de Youden y Steiner (1975).
CONCLUSIONES
Este método desarrollado posee una adecuada sensibilidad y reproducibilidad para la cuantificación de fructooligosacaridos (GF2, GF3 y GF4) en materia prima FOS. Se obtiene una recuperación del 98,0% en un helado prebiótico formulado al 15% p/p.
Agradecimientos
Los autores expresan sus sinceros agradecimientos a la empresa Carval de Colombia por facilitar los equipos instrumentales, instalaciones y reactivos para llevar a cabo dicha investigación. También a los Sres. Martha Viveros y Scott Pettit por su desinteresada ayuda con la revisión y corrección del texto en inglés.
REFERENCIAS
Bersaneti G, Mantovan J, Magri A, Mali S, Celligoi M (2016) Edible films based on cassava starch and fructooligosaccharides produced by Bacillus subtilis natto CCT 7712. Carbohydr Polym 151: 1132–1138.
Foitzich Molina AC (2013) Desarrollo y validación de una metodología para determinar azúcares simples en matrices orgánicas mediante HPLC-IR. Tesis de Ingeniería en Alimentos, Universidad Austral de Chile, Valdivia, Chile.
Hermann M, Manrique I, Parraga A (2005) Jarabe de yacón: Principios y procesamiento. Lima: Centro Internacional de la Papa (CIP).
Krol B, Grzelak K (2006) Qualitative and quantitative composition of fructooligosaccharides in bread. Eur Food Res Technol 223(6): 755–758.
Larico Perez RP, Yanqui Gilari JJ, Escobar Copa KU (2016) Elaboración de helado dietético a partir de jarabe de yacón (Smallanthus sonchifolius) con características prebióticas. J High Andean Res 18(1): 77–82.
Li J, Hu D, Zong W, Lv G, Zhao J, Li S (2014) Determination of inulin-type fructooligosaccharides in edible plants by high-performance liquid chromatography with charged aerosol detector. J Agric Food Chem 62(31): 7707–7713.
Roberfroid MB (1996) Functional effects of food components and the gastrointestinal system: chicory fructooligosaccharides. Nutr Rev 54(11 Pt 2): S38–S42.
Roberfroid MB (2002) Functional food concept and its application to prebiotics. Dig Liver Dis 34(2): S105–S110.
Rodríguez-Gómez R, Jiménez-Díaz I, Zafra-Gómez A, Morales J (2015) Improved sample treatment for the determination of fructooligosaccharides in milk related products by liquid chromatography with electrochemical and refractive index detection. Talanta 144: 883–889.
Valliyodan B, Shi H, Nguyen HT (2015) A simple analytical method for high-throughput. Chromatogr Res Int 2015: 1-8.
Walton H (1995) Ligand-exchange chromatography: a brief. Ind Eng Chem Res 34(8): 2553–2554.
Youden WJ, Steiner EH (1975) Statistical manual of AOAC. Washington, USA: Association of Official Analytical Chemistry.
Información adicional
CONFLICTOS DE INTERÉS: Los autores declaran no poseer
conflictos de interés.
Citation Format: González-Aguirre
CL, Ramírez-Navas JS (2018) Desarrollo y validación de un
método para la cuantificación de fructooligosacáridos en un helado prebiótico [Development and validation of a method for the quantification of fructooligosaccharides in a prebiotic ice cream]. J Pharm Pharmacogn Res 6(2): 108–116.
Enlace alternativo
http://jppres.com/jppres/pdf/vol6/jppres17.302_6.2.108.pdf (pdf)
http://jppres.com/jppres/cuantificacion-de-fructooligosacaridos-en-helado-prebiotico/ (html)