TRATAMIENTOS PREGERMINATIVOS EN Geoffroea decorticans (Gillies ex Hook. & Arn.) Burkart var. decorticans
TRATAMIENTOS PREGERMINATIVOS EN Geoffroea decorticans (Gillies ex Hook. & Arn.) Burkart var. decorticans
Foresta Veracruzana, vol. 16, núm. 2, pp. 31-36, 2014
Recursos Genéticos Forestales
Resumen: El objetivo de este trabajo fue evaluar el efecto de la escarificación sobre la germinación de los frutos de G. decorticans (chañar), especie nativa del parque chaqueño. Los mismos fueron recolectados de árboles ubicados en el departamento Pellegrini (Santiago del Estero, Argentina). Previa separación del mesocarpio del resto del fruto, después de 24 hs de maceración en agua, se aplicaron los siguientes tratamientos de escarificación: frutos (testigo); semillas (T1); frutos despuntados y con incisiones longitudinales (T2); fruto despuntados y sumergidos en agua durante 4 hs (T3) y 6 hs (T4). El ensayo se condujo en germinadores que fueron colocados en cámaras de crecimiento a 30 ºC con un fotoperiodo de 14 hs de luz. Se sembraron 10 frutos por tratamiento, en un diseño completamente aleatorizado con 5 repeticiones. Se calculó porcentaje de germinación y velocidad de germinación (VG). Los resultados se analizaron con modelos lineales generalizados y la diferencias entre medias de tratamientos con la prueba LSD de Fisher (α=0.05). Los mejores tratamientos de escarificación fueron T3 (68%) y T4 (82%) y que además presentan los menores valores de velocidad de germinación (5 y 4,6 días respectivamente), por lo que se recomiendan como los más adecuados para la producción de plantines de la especie.
Palabras clave: escarificación, poder germinativo, velocidad de germinación, chañar.
Abstract: The purpose of this work was to evaluate the effect of scarification on the germination of the G. decorticans (or chañar) fruits, native species from the Chaco park. Said fruits were collected from trees located in the Pellegrini Department (Santiago del Estero, Argentina). Previously separating the mesocarp from the rest of the fruit, after 24 hours of maceration in water, the following scarification treatments were applied: fruits (witness); seeds (T1); fruits blunted and incised lengthwise (T2); fruits blunted and submerged in water during 4 hours (T3) and 6 hours (T4). The test was conducted in germinators placed on growth chambers at 86ºF (30ºC) with a photoperiod of 14 hours with light. Ten fruits were sawed per treatment, on a completely randomized pattern with 5 repetitions. The germination percent and the germination speed (VG) were calculated. Results were analyzed with general linear models and the differences between treatment averages and the Fisher’s LSD test (α=0.05). The best scarification treatments were T3 (68%) and T4 (82%) and they also present the lower germination speed values (5 and 4.6 days, respectively), so they are recommended as the most adequate treatments for the production of the species seedling.
Keywords: scarification, germination power, germination speed, chañar.
Introducción
Geoffroea decorticans (Gillies ex Hook. & Arn.) Burkart var. decorticans (Fabaceae) denominada comúnmente chañar, es una especie nativa, utilizada por los pueblos rurales de zonas áridas y semiáridas por ser una valiosa fuente de recursos. Es importante por su función ambiental en la fijación de nitrógeno, estructura y fertilidad del suelo, movilización de nutrientes, microclima propicio para el establecimiento de plantas y bienestar animal entre otros. Además el hombre la utiliza para diferentes finalidades como fuente maderable, melífera, forrajera, alimenticia, medicinal, tintórea y artesanal (Pensiero et al., 2005). Posee una amplia distribución en el país, desde Salta y Jujuy hasta Río Negro y sudoeste de Buenos Aires, adaptándose a distintos tipos de suelos, desde los arenosos a salitrosos, integra tanto bosques xerófilos como hidrófilos. Es una especie heliófila, pionera, tolerante a la sequía y al frío. En zonas áridas, es indicadora de salinidad y de napa freática poco profunda.
Frecuentemente crece asociado con otras especies como Algarrobo (Prosopis alba), Quebracho blanco (Aspidosmerma quebracho blanco Shlech), Quebracho colorado (Schinopsis quebracho colorado), etc., pero también se presenta en bosquecillos puros (Marzocca, 1994 y Marzocca y del Puerto, 1976).
La dormición en especies nativas es un tipo de mecanismo de supervivencia, que responde a causas físicas, fisiológica, o a ambas (Pérez et al., 2009;Heather et al. 2010 e ISTA 2012). Una de las principales causas de dormición es la presencia de cubiertas duras, impermeables a la entrada de agua y gases. Si bien estos tegumentos duros contribuyen a la supervivencia de la semilla en su ambiente natural protegiendo al embrión de daños fisiológicos o mecánicos, impide o retrasa la germinación, por lo que es necesario algún tratamiento para obtenerla, cuando se trata de implantar una especie con estas características (Schutz et al., 2002; Thompson et al., 2003).
El fruto del chañar es una drupa con endocarpio leñoso, cuya dureza representa un obstáculo a la entrada de agua y al intercambio gaseoso, dificultando la germinación de la/s semilla/s. Dicha restricción, denominada “dormición física” (Schmidt, 2000) es muy común en especies de ambientes tropicales, particularmente en zonas áridas (Villagra, 1995). Para mejorar este proceso y acelerar la obtención de plántulas, existen diversos tratamientos pregerminativos como la escarificación mecánica, química o física entre otras (Atencio et al., 2003).
La escarificación tiene por finalidad ablandar, perforar, rasgar o abrir la cubierta responsable de la dormición. Se ha comprobado que la remoción completa del endocarpio leñoso, favorece la germinación en especies de la familia de las Rhamnaceae tales como Ziziphus lotus, Z. jujuba, Z. mauritiana y Z. mistol (Araoz y del Longo, 2006).
Según Ortega et al. (2001), las Fabaceae presentan latencia física de las semillas, por lo que necesitan ser escarificadas para germinar (Janzen, 1981; Catalán y Balzarini, 1992; Izhaki y Ne’eman, 1997). En la literatura se registra información sobre métodos de escarificación de semillas de las siguientes Fabaceae: Prosopis spp. (D’Aubeterre et al., 2002) Caesalpina paraguariensis (Ortega et al., 2001), Enterolobium contortisiliqum, Leucaena glauca, Parkinsonia aculeata, Tipuana tipu (Rossini et al., 2006) Leucaena leucocephala (Faría et al., 1996), Mimosa aculeaticarpa (Martínez et al., 2006); sin embargo, no existen referencias sobre métodos de escarificación para los frutos de G. decorticans, por lo que el objetivo de este trabajo fue evaluar diferentes tratamientos pregerminativos que permitan superar la dormición física impuesta por el endocarpio y que sean de fácil aplicación.
Material y métodos
Los frutos maduros de G. decorticans fueron recolectados en Diciembre de 2011, de árboles ubicados en el departamento Pellegrini (Santiago del Estero). En laboratorio, se separó el mesocarpio del resto del fruto después de 24 hs de maceración en agua. Estos se colocaron en bolsas de papel y se almacenaron en heladera hasta el inicio de los experimentos.
Los tratamientos ensayados fueron: frutos (testigo T); semillas (T1) las que fueron separadas del pericarpio mediante procedimiento mecánico (con uso de alicate); frutos despuntados con alicate y con incisiones longitudinales mediante sierra (T2); frutos despuntados y sumergidos en agua durante cuatro horas (T3) y 6 horas (T4).
El ensayo se condujo en germinadores preparados en botellas de plástico, cubiertas internamente de papel secante y rellenas con arena esterilizada (figura 1).

Figura 1.
Vista general del ensayo.
Se sembraron 10 frutos y/o semillas por cada tratamiento, en un diseño completamente aleatorizado con 5 repeticiones. Los germinadores se colocaron en cámaras de crecimiento a 30 ºC y un fotoperiodo de 14 hs de luz. La germinación se registró diariamente. Se consideró fruto y/o semilla germinada cuando la radícula alcanzó 1 ½ vez el tamaño del fruto y/o semilla. Se calculó porcentaje de germinación y la velocidad de germinación (VG) mediante la siguiente expresión (Krzyzanowski et al., 1999):
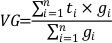
Donde:
ti= número de días desde 1 a n;
gi= número de semillas germinadas en el tiempo ti
El análisis de datos se realizó con modelos lineales generalizados. La componente aleatoria fue modelada con la distribución binomial y función de enlace logit (Crawley, 2007). Los modelos generalizados permiten relajar los supuestos tradicionales del modelo lineal general y modelar de manera flexible las distribuciones no normales de datos. La comparación de medias de tratamiento se realizó mediante la prueba de comparaciones múltiples LSD Fisher (Balzarini et al., 2013). La variable velocidad de germinación se evaluó también con modelos lineales generalizados pero con distribución normal y función de enlace identidad (Crawley, 2007). El procesamiento de estos modelos se efectuó mediante el paquete estadístico INFOSTAT (Di Rienzo et al., 2013).
Resultados y discusión
Los métodos de escarificación influyeron en forma positiva sobre la proporción de semillas germinadas de G. decorticans, obteniéndose los mayores valores, 0.68 y 0.82, en aquellos tratamientos en los que se combinó el despuntado y el remojo en agua durante 4 (T3) y 6 horas (T4), no existiendo diferencias significativas entre ellas y, obteniéndose con el tratamiento 4 el máximo porcentaje de germinación que se diferencia significativamente del resto de los tratamientos. Esto evidencia que el agua que penetró a través del corte apical del fruto, favoreció la imbibición de la semilla contenida en él. Este efecto fue mayor cuando se utilizó 6 horas de imbibición, diferenciándose del tratamiento 1 (P<0.05) (figura 2). Según Baskin y Baskin (1998) una perforación pequeña en el fruto debería ser suficiente para iniciar el proceso de germinación. Sin embargo Martínez Pérez et al. (2006) recomienda realizar una apertura grande y de tamaño uniforme, cuidando de no dañar el embrión.
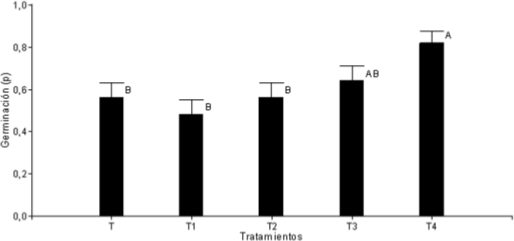
Figura 2
Proporción de semillas germinadas para los diferentes tratamientos de escarificación. Medias con letras iguales no son significativamente diferentes (p > 0.05).
A diferencia de lo obtenido en este trabajo, el remojo en agua durante 24 h de endocarpios de Zizuphus mistol, no influyeron en su germinación siendo similares al testigo; resultados semejantes se obtuvieron en Peltophorumn pterocarpum (Fabaceae) lo que posiblemente se debió a la condición anaeróbica que no permitió el intercambio gaseoso, imprescindible para el proceso de respiración de las semillas durante la germinación (Atencio et al., 2003).
Sin embargo en otras especies del género Zizuphus tales como Z. lotus; Z. Jujuba; Z. mauritana (Aráoz y Del Longo, 2006) al igual que en Tabebuia rosea e Inga inicuil (Chan Quijano et al., 2012), 24 hs de remojo en agua favoreció la germinación.
Los porcentajes de germinación acumulado para los diferentes tratamientos se presentan en la figura 3, siendo el número de días necesarios para alcanzar el 50% de germinación los siguientes: 4 días para los frutos despuntados y sumergidos en agua durante 6 horas (T4); 5 días para los frutos despuntados y sumergidos en agua durante 3 horas (T3); 9 días para los frutos despuntados con alicate y con incisiones longitudinales mediante sierra (T2); correspondiendo 14 días para el testigo (T), las semillas (T1) no alcanzaron el 50% de germinación.
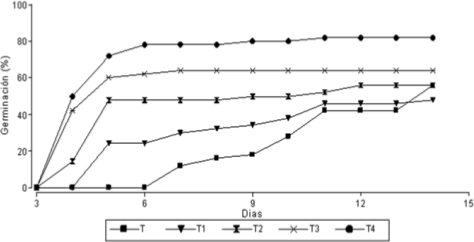
Figura 3.
Porcentajes de germinación acumulada de los diferentes tratamientos de escarificación en G. decorticans.
El análisis de la velocidad de germinación, muestra que los tratamientos T3 y T4 presentan los menores valores (5 y 4, 6 días, figura 4), no diferenciándose entre ellos (P<0.05). Este resultado asociado con el porcentaje de germinación indicaría que estos son los tratamientos más adecuados para la producción de plantines de la especie.
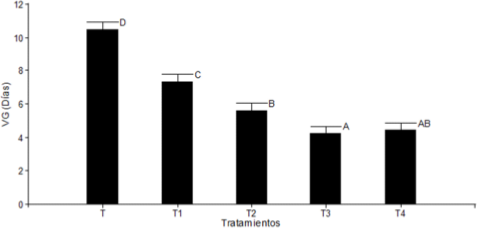
Figura 4.
Tiempo medio de germinación de frutos/semillas de G. decorticans sometidos a diferentes tratamientos de escarificación. Medias con letras iguales no son significativamente diferentes (p > 0.05).
En este trabajo se evaluaron tratamientos sencillos de aplicar, no significa que sean los mejores métodos de escarificación posibles, pues no se probó el sin número de tratamientos pregerminativos que existen. Sin embargo se trata de técnicas de fácil aplicación y en general de alta efectividad, los que pueden ser adoptados por pequeños productores forestales que no cuenten con equipos sofisticados.
Conclusiones
El empleo de la escarificación incrementó el número de semillas germinadas. Los tratamientos más efectivos fueron: despuntado del fruto e inmersión en agua durante 3 y 6 horas, por corresponderle mayor porcentaje de germinación y menor cantidad de días para germinar.
Los tratamientos seleccionados son sencillos de aplicar, por lo que se recomienda su uso por pequeños productores forestales.
Literatura citada
ARÁOZ, S.D. y DEL LONGO, O.T. 2006. Tratamientos pregerminativos para romper la dormición física impuesta por el endocarpio en Ziziphus mistol Grisebach. Quebracho 13: 56-65.
ATENCIO, L.; COLMENARES, R.; RAMÍREZ-VILLALOBOS, M. y MARCANO, D. 2003. Tratamientos pregerminativos en Acacia sanfrancisco (Peltophorum pterocarpum) Fabaceae. Revista de la Facultad de Agronomía No. 20. 9 p.
BALZARINI, M.G.; GONZÁLEZ, L.; TABLADA, M.; CASANOVES, F.; DI RIENZO, J.A. y ROBLEDO, C.W. 2013. Manual del Usuario. Editorial Brujas, Córdoba, Argentina.
BASKIN, J.M. y BASKIN, C.C. 1998. Seed ecology, bioegeography and evolution of dormancy and germination. Academic Press, San Diego.
CATALÁN, L. y BALZARINI, M. 1992. Improved laboratory germination conditions for several arboreal Prosopis species: P. chilensis, P. flexuosa, P. nigra, P. alba, P. caldenia and P. affinis. Seed Sci. Technol. 20:293-298.
CHAN-QUIJANO, J.G.; OCHOA-GAONA, S.; GUTIÉRREZ-AGUIRRE, M.A. y PÉREZ-HERNÁNDEZ, I. 2012. Aplicación de técnicas de germinación a semillas promisorias para la fitorremediación de suelos contaminados por hidrocarburos en Tabasco, México. RIACRE, Boletín 6(1):12-14.
CRAWLEY, M.J. 2007. The R book. Chichester: John Wiley & Sons. 942 p.
D’ AUBETERRE, R.; PRINCIPAL, J. y GARCÍA, J. 2002. Efecto de diferentes métodos de escarificación sobre la germinación de tres especies del género Prosopis. Revista científica. Vol. XII suplemento 2: 557-577.
DI RIENZO, J.A.; CASANOVES, F.; BALZARINI, M.G.; GONZÁLEZ, L.; TABLADA, M. y ROBLEDO, C.W. 2013. InfoStat, versión 2013, Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina.
FARIA, M.J.; GARCÍA, A.L. y GONZÁLEZ, B. 1996. Nota técnica: métodos de escarificación en semillas de cuatro leguminosas forrajeras tropicales. Rev. Fac. Agro. (LUZ) 13: 573-579.
HEATHER, A.E.; PÉREZ, H.E. y WILSON, S.B. 2010. Non-deep physiological dormancy in seeds of two Polygonella species with horticultural potential. Hortscience, 45 (12):1854-1858.
ISTA. 2012. International rules for seed testing. International Seed Testing Association (Eds.). Bassersdorf. Switzerland.
IZHAKI, I. and NE’EMAN, G. 1997. Hares (Lepus spp. As seed disperses of Retama raetan (Fabaceae) in a sandy landscape. J. Arid Environ. 37:343-354.
JANZEN, D.H. 1981. Enterolobium cyclocarpum seed passage rate and survival in horses, Costa Rican Pleistocene seed dispersal agents. Ecology 62:593-601.
KRZYZANOWSKI, F.C.; VIERIA, R.D. y FRANÇA NETO, J. DE B. 1999. Vigor de sementes: conceitos e testes. Associaçăo Brasileira de Tecnologia de Sementes. Comitê de Vigor de Sementes. Londrina. Brasil: ABRATES. pp. 218.
MARTÍNEZ, P.G.; OROZCO, S. A. y MARTORELL, C. 2006. Efectividad de algunos tratamientos pre-germinativos para ocho especies leñosas de la Mixteca Alta Oaxaqueña con características relevantes para la restauración. Boletín de la Sociedad Botánica de México 79:9-20.
MARZOCCA, A. 1994. Guía descriptiva de malezas del cono sur. INTA. Buenos Aires. 295 p.
MARZOCCA, A. y DEL PUERTO, O. 1976. Manual de malezas. Hemisferio Sur. Buenos Aires. 564 p.
ORTEGA, B.P.; DE VIANA, M.L.; LARENAS, G. y SARAVIA, M. 2001. Germinación de semillas de Caesalpinia paraguariensis (Fabaceae): agentes escarificadores y efecto del ganado. Rev. Biol. Trop. 49(1): 301-304.
PENSIERO, J.; MUÑOZ, J. DE D. y MARTÍNEZ, V. 2005. Alternativas de sustentabilidad del bosque nativo del Espinal. Proyectos de Investigación Aplicada a los Recursos Forestales Nativos (PIARFON). Proyecto Bosques Nativos y Áreas Protegidas Argentina Banco Mundial - N° 4085-AR.
PÉREZ, H.E.; ALMIRA, F. y BRENNAN, M. 2009. Germination timing and dormancy break in seeds of summer farewell (Dalea pinnata, Fabaceae). Ecological Restoration 27 (2): 160-168.
ROSSINI, O.S.; VALDÉS, B.; ANDRÉS, M.C.; MÁRQUEZ, C.F. y BUESO, L.M. 2006. Germinación de las semillas en algunas especies americanas de Fabaceae y Bignoniaceae cultivadas en Sevilla (SO España). Lagascalia 26:119-129.
SCHMIDT, L. 2000. Dormancy and pretreatment. Guide to handling of tropical and subtropical forest seed. Sanina Forest Seed Centre. Editor Olesen K., pp. 263-303.
SCHUTZ, W.; MILBERT, P. and LAMONT, B.B. 2002. Seed dormancy, afterripening and light requirements of four annual Asteraceae in southwestern Australia. Annals of Botany, 90(6): 707.
THOMPSON, K.; CERIANI, R.M.; BAKKER, J.P. and BEKKER, R.M. 2003. Are seed dormancy and persistence in soil related? Seed Science Research, 13 (2): 97.
VILLAGRA, P.E. 1995. Temperature effects on germination of Prosopis argentina and P. alpataco (Fabaceae, Mimosoideae). Seed Science & Technology. 23: 639-646.