Artigos Originais
Efeito fotossenssibilizador in vitro da violeta de genciana na terapia fotodinâmica sobre Candida albicans
Photosensitizing effects of In vitro crystal violet on photodynamic therapy for Candida albicans
Efecto fotosensibilizador in vitro de la violeta de genciana en la terapia fotodinámica sobre Candida albicans
Efeito fotossenssibilizador in vitro da violeta de genciana na terapia fotodinâmica sobre Candida albicans
Revista Família, Ciclos de Vida e Saúde no Contexto Social, vol. 6, núm. 2, pp. 158-165, 2018
Universidade Federal do Triângulo Mineiro
Resumo: Este estudo tem como objetivo avaliar a ação do corante violeta de genciana, in vitro, sobre Candida albicans, isolado ou como fotossensibilizante, em comparação ao azul de metileno na Terapia Fotodinâmica. Foi uma pesquisa experimental com abordagem quantitativa. A linhagem de Candida albicans ATCC 1106 foi inoculada obtendo-se um overnight de 1,37x104 UFC/ml. Foram adicionados 50µl da suspensão fúngica (overnight) em 18,0ml de caldo Saboraud. A esse conjunto foi adicionado o 0,2ml do corante da violeta genciana a 1%, foi plaqueado, esperou-se o tempo de pré-irradiação de 5 minutos e aplicou-se o laser vermelho. A dose aplicada foi de 100J/cm², com energia total de 3J, depois foram subcultivadas a 37°C em caldo Saboraud por 1 hora. Após este período, uma alíquota de 1,0 ml foi diluída em 9,0ml de solução salina 0,85% esterilizada. 0,1 ml dessa diluição foi plaqueada e semeada em ágar saboraud. As placas, em triplicata, foram incubadas em estufa para microrganismos a 37°C, e após 48h foi feita a contagem das UFCs/ml. Além da violeta genciana a 1% combinada ao laser, foram analisados os grupos: azul de metileno a 1% associado ao laser, azul de metileno a 1%, violeta genciana a 1%, e o laser sem adição de corantes. As análises foram realizadas no software IBM SPSS (21.0), utilizou-se o teste de Kruskal-Wallis (Mann-Whitney) e o teste de Friedman (Wilcoxon), adotando-se um nível de significância de α=5%. Como resultado observou-se que a violeta genciana a 1% associada ao laser tem efeito importante contra Candida albicans na terapia fotodinâmica.
Palavras-chave: Fotoquimioterapia, Candida albicans, Terapia a laser, Violeta de genciana, Azul de metileno.
Abstract: This study aimed at evaluating the action of the in vitro dye crystal violet on Candida albicans, isolated or as a photosensitizing tool, when compared to methylene blue in photodynamic therapy. It was an experimental and quantitative research. The ATCC 1106 Candida albicans strain was inoculated with an overnight103 UFC/ml. 50µl of the fungal suspension (overnight) were added to 18,0ml of Saboraud agar. To this, 0.2ml of the crystal violet dye was added at 1% and plated. A five-minute period of pre-irradiation was conceded to the sample, after which the red laser was applied. The dosage applied was that of 100J/cm², with a total energy of 3J. After that, the samples were subcultured in Saboraud agar at 37ºC, for 1 hour. After this period, an aliquot of 1.0 ml was diluted in 9.0 ml of 0.85% sterilized saline solution. 0.1 ml of the diluted result was plated and cultured in saboraud agar. Three plates were incubated in a growth chamber for micro-organisms at 37ºC, and after 48h, the UFCs/ml were counted. In addition to the 1% crystal violet with the laser, the following groups were analyzed: 1% methylene blue with laser, 1% methylene blue, 1% crystal violet, and the use of the laser with no dying. The analyses were conducted in the IBM SPSS (21.0) software. The Kruskal-Wallis (Mann-Whitney U test) was used as well as the Friedman (Wilcoxon) text, with a significance level α=5%. As a result, the 1% crystal violet in conjunction with the laser has an important effect against Candida albicans in the photodynamic therapy.
Keywords: Photochemotherapy, Candida albicans, Laser therapy, Gentian violet, Methylene blue .
Resumen: Este estudio tiene como objetivo evaluar la acción del colorante violeta de genciana, in vitro, sobre Candida albicans, aislado o como fotosensibilizante, en comparación al azul de metileno en la Terapia Fotodinámica. Fue una investigación experimental con abordaje cuantitativo. El linaje de Candida albicans ATCC 1106 fue inoculado obteniéndose un overnight de 1,37x104 UFC/ml. Fueron agregados 50µl de la suspensión fúngica (overnight) en 18,0ml de caldo Saboraud. A este conjunto fue agregado el 0,2ml del colorante de la violeta genciana a 1%, fue plaqueado, se esperó el tiempo de pre-irradiación de 5 minutos y se aplicó el láser rojo. La dosis aplicada fue de 100J/cm², con energía total de 3J, después fueron subcultivadas a 37°C en caldo Saboraud por 1 hora. Después de este período, una alícuota de 1,0ml fue diluida en 9,0ml de solución salina 0,85% esterilizada. 0,1ml de esta dilución fue plaqueada y plantada en agar saboraud. Las placas, en triplicata, fueron incubadas en estufa para microorganismos a 37ºC, y después de 48h fue hecho el conteo de las UFCs/ml. Además de la violeta genciana a 1% combinada a láser, fueron analizados los grupos: azul de metileno a 1% asociado al láser, azul de metileno a 1%, violeta genciana a 1%, y el láser sin adición de colorantes. Los análisis fueron realizados en el software IBM SPSS (21.0), se utilizó el test de Kruskal-Wallis (Mann-Whitney) y el test de Friedman (Wilcoxon), adoptándose un nivel de significancia de α=5%. Como resultado se observó que la violeta genciana a 1% asociada al láser tiene efecto importante contra Candida albicans en la terapia fotodinámica.
Palabras clave: Fotoquimioterapia, Photochemotherapy, Candida albicans, Terapia a láser, Violeta de genciana, Azul de metileno.
INTRODUÇÃO
A incidência de infecções fúngicas superficiais e profundas tem crescido significativamente ao longo dos últimos 20 anos.
Várias razões são propostas para explicar este aumento, incluindo o uso de medicamentos antineoplásicos e imunossupressores, antibióticos de amplo espectro, próteses, enxertos e cirurgias mais agressivas1. Com o desenvolvimento da medicina, no campo da cirurgia e transplantologia, o número de indivíduos imunocomprometidos e, consequentemente, mais suscetíveis a essas infecções, vem crescendo2.
Micoses invasivas representam uma ameaça crescente para a saúde humana devido a uma combinação de diagnósticos lentos e da existência de poucas drogas antifúngicas disponíveis e eficazes3, essa combinação pode desencandear infecções sistêmicas e/ou locais mais graves, extensas e difíceis de serem tratadas na presença desse fungo4,5.
Candida albicans (CA), um dos mais frequentes microrganismos oportunistas da microbiota oral, caracteriza-se como a espécie mais prevalente responsável por infecções das mucosas e pele de pacientes com imunidade comprometida com especial importância para a saúde humana6-8, por provocar micoses superficiais e doença sistêmica disseminada9.
Em decorrência da alta taxa de mortalidade pelas infecções invasivas por Candida, da disponibilidade limitada de agentes antifúngicos eficazes e do aumento da resistência a estas drogas disponíveis comercialmente, pesquisas são realizadas no intuito de se obter alternativas de tratamento10,11. Por isso, estudos estão sendo realizado na área de Terapia Fotodinâmica (TFD), que têm mostrado efeito bactericida e fungicida em microrganismos orais, a partir da terapia com laser de baixa intensidade (TLBI)11-13.
A TFD foi desenvolvida para combater lesões malignas, porém tem sido utilizada com sucesso para o tratamento de infecções fúngicas, sendo empregada com êxito contra a Candida albicans e outras espécies de Candida7, reduzindo a possibilidade de a CA causar uma infecção sistêmica14 e surgindo como uma opção eficaz, a qual desde a pesquisa de Raab em 1900, que provou a ação do corante acridina com a luz de relâmpagos sobre paramécios, encontra-se bem fundamentada cientificamente.
Essa terapia baseia-se no conceito de que um corante não tóxico, conhecido como fotossensibilizador (FS), costuma localizar-se, preferencialmente, em certos tecidos ou células, e subsequentemente, é ativado pela luz visível, produzindo espécies reativas de oxigênio (EROS), as quais podem matar as células que se ligam ao FS15-17.
A multiplicidade de alvos nas células (mitocôndrias, lisossomos e núcleos) dos fungos reduz o risco de cepas resistentes fotomutantes e este risco é minimizado pela ausência de efeitos mutagênicos da TFD18, a qual pode ser repetida várias vezes, sem indução aparente de resistência, já que o DNA não é o alvo principal das EROS19.
O perigo de danos no DNA em fungos é reduzido pela presença de uma membrana que envolve o núcleo, atuando como uma barreira para a penetração de corantes ou seus fotoprodutos de alta energia20.
Diferentes tipos de FSs são propostos na TFD. A interação entre o FS, a membrana celular e estruturas intracelulares são de grande relevância na resposta à TFD. Devido à grande diversidade de microrganismos, um FS com propriedades físico-químicas distintas pode ser requerido21.
A violeta genciana (VG) é uma mistura de corantes triarilmetanos, usada para tingir o cabelo, colorir papel ou tecidos, sendo usada em laboratórios de microbiologia. Derivada do alcatrão de carvão, tem sido amplamente utilizada como um produto antisséptico. Sua atividade antimicrobiana é reconhecida e recomendada para tratamento de candidíase22. O mecanismo de ação da VG não está relacionado com uma lesão primária da membrana citoplasmática sendo provavelmente relacionada com a inibição de uma via metabólica23.
A Organização Mundial da Saúde recomenda a aplicação tópica de VG em uma concentração de 1% para o tratamento inicial de candidíase oral em pacientes infectados pelo HIV em contextos de recursos limitados, uma vez que o custo do tratamento é baixo e bem tolerado24.
No entanto, devido a suas propriedades de coloração da mucosa bucal, a VG não é usada atualmente para o tratamento da CA. Um estudo para avaliar a segurança e eficácia de VG em concentrações diferentes de VG mostrou que esse FS na concentração de 0,00165% não mancha a cavidade oral, é estável, bem tolerado, e possui uma potente atividade anti-Candida25. Em outra pesquisa23 realizada, verificou-se que VG apresenta uma atividade fungicida para a maioria das espécies de Candida, sendo as C. albicans e C. tropicalis as espécies mais suscetíveis.
A VG apresenta potencial de ação para tratamento da candidíase oral devido à sua atividade antibiofilme e antigerminação. O mecanismo de ação do VG não está associado à lesão primária na membrana citoplasmática, e provavelmente se relaciona à inibição do metabolismo celular23.
É possível que a produção de radicais hidroxil/peróxido facilite a penetração de VG através da matriz, levando à inibição da síntese da parede celular dos fungos. Os estudos clínicos para determinar a eficácia da VG no tratamento desta doença são garantidos26.
Uma dificuldade, na TFD, é a administração dos FSs, os quais provocam uma coloração indesejável nos dentes e na mucosa bucal10. Porém, estudos in vivo demonstraram que a cavidade oral é especialmente adequada para a TFD, pois é relativamente acessível à aplicação da luz27,28. Além disso, o FS é de fácil manuseio7
Sabendo dos resultados positivos da ação da VG como antifúngico sobre CA, este trabalho tem como objetivo avaliar a ação do corante violeta de genciana, in vitro, sobre Candida albicans, isolado ou como fotossensibilizante em comparação ao azul de metileno na Terapia Fotodinâmica.
MÉTODO
Realizou-se um estudo experimental, in vitro, no Laboratório de Genética de Microrganismos do Departamento de Biologia do Centro de Ciências Exatas e da Natureza da Universidade Federal da Paraíba (UFPB), na cidade de João Pessoa-Pb, no período compreendido entre dezembro de 2014 a janeiro de 2015.
Foi utilizada a linhagem de CA ATCC 1106 (padrão internacional, referência), pertencente à coleção de microrganismos do Laboratório de Micologia do Departamento de Ciências Farmacêuticas, Centro de Ciências da Saúde, UFPB.
Este estudo baseou-se no método proposto por Craig; Gudmundson (1991), modificado por Pereira et. al, (2014) 15. Para a determinação fúngica, a linhagem de Candida albicans ATCC 1106 foi inoculada em caldo Saboraud e incubada a 37°C por 18-20 horas, obtendo-se um overnight de 1,37x104 UFC/ml.
Foram adicionados 50µl da suspensão fúngica (overnight) em 18,0ml de caldo Saboraud; a esse conjunto foi adicionado 0,2 ml do corante AM a 1% ou a VG a 1%. Em seguida este conjunto foi levado ao vórtex, e depois, plaqueado. Esperou-se o tempo de pré-irradiação (TPI) de cinco minutos e aplicou-se o laser. A dose aplicada foi de 100J/cm², com energia total de 3J, potência de 100mW, numa distância de 1,0 cm por ponto em toda extensão da placa de petri, com a ponta a 1,0 cm de altura da placa. Depois foram subcultivadas a 37°C em caldo Saboraud por 1 hora.
Após esse período, uma alíquota de 1ml foi diluída, convenientemente, em 9ml de solução salina 0,85%, esterilizada e levada para o vórtex. Em seguida, 0,1 ml desse subcultivo foi plaqueado e semeado em ágar saboraud.
As placas foram incubadas em estufa de crescimento de microrganismos a 37°C. A contagem de células viáveis, neste tubo, foi determinada e designada como o tempo 0 para a determinação do efeito pós-antimicrobiano. O recrescimento da cultura foi monitorado por um período de 0, 24 e 48 horas, pelo método padrão de contagem em placas. A leitura das placas foi efetuada após incubação por 48 horas, a 37° C.
Os experimentos foram realizados em triplicata. Os resultados da contagem de células viáveis (UFC/ ml) da cultura tratada foram descritos na Tabela 1.
A sequência foi respeitada na manipulação e determinação do efeito fungicida e na contagem das UFCs — com exceção do TPI, que não foi necessário, para os grupos dos corantes AM a 1% e VG a 1% sem uso do laser, para o grupo controle e para o grupo do laser sem FS.
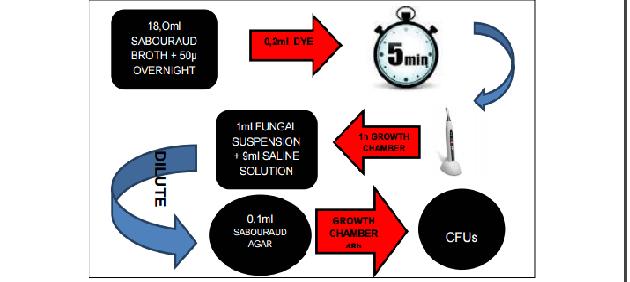
Figura 1
Esquema do passo a passo da metodologia. Segundo Pereira15, 2014.
Foi empregado o Laser vermelho semicondutor (GaA1As e InGaAlP), aparelho laser DUO MMOPTICS São Carlos, SP, Brasil, com comprimento de onda (λ) de 660 nm, a potência do aparelho foi de 100 mW, a dose aplicada foi de 100J/cm², com energia total de 3J, numa distância de 1 cm por ponto em toda extensão da placa de petri, com a ponta do spot a 1cm de altura da placa, a emissão do laser foi contínua, com o modo de operação pontual.
Essas especificações foram indicadas pelo fabricante do aparelho no caso de terapia fotodinâmica sem fibra óptica. As placas de petri selecionadas para o uso do FS + laser esperaram o tempo de pré-irradiação de 5 minutos.
Realizou-se o teste de normalidade (Shapiro-Wilk) para verificar a distribuição dos dados, onde se observou que, para todos os grupos, a distribuição da contagem de UFCs foi não-normal (p<0,05). Na comparação das médias de UFCs entre os grupos, nos mesmos períodos de tempo, realizou-se o teste de Kruskal-Wallis, e na comparação entre os grupos, dois a dois, realizou-se o teste de Mann-Whitney.
Já para a comparação da contagem de UFCs dentro dos grupos, nos diferentes períodos de tempo, utilizou-se o teste de Friedman, sendo as diferenças identificadas mediante o teste de Wilcoxon. Para todas as análises adotou-se um nível de significância =5%. As análises foram realizadas no software estatístico IBM SPSS (21.0).
RESULTADOS
Na referida pesquisa, quando se utilizou a VG a 1% associado ao laser, foi realizada a TFD, e observou-se que na 0h houve uma diminuição nas UFCs, porém nas 24h e 48h não houve formação de colônias, o que pode ser observado na Tabela 1.
Ao se pesquisar apenas a VG a 1%, foi observado que, na 0h, houve uma redução nas UFCs, e nas 24h e 48h não houve formação de colônias (Tabela 1).
Quando se pesquisou o AM a 1% combinado com o laser, ou seja, foi efetivada a TFD, constatou-se que na 0h houve uma redução das UFCs, e nas 24h e 48h não houve o desenvolvimento de UFCs (Tabela 1).
No grupo do AM a 1% isolado foi registrado que a 0h, 24h e 48h houve um aumento gradativo na formação das UFCs (Tabela 1).
No grupo em que apenas o laser foi utilizado, houve uma diminuição das UFCs na 0h, e nas 24h e 48h não houve produção dessas colônias (Tabela 1).

Tabela 1
Valores médios para as Unidades Formadoras de Colônia (UFCs) obtidas para o grupo controle e para os grupos tratados com Laser, Violeta, Laser + Violeta, Azul de metileno e Laser + Azul de metileno, nos tempos “0h”, “24h” e “48h”. João Pessoa, PB. 2015.
Valores expressos em UFC/ml. Letras maiúsculas iguais em colunas e minúsculas iguais em linhas indicam não haver diferenças estatisticamente significantes (p> 0,05) entre os grupos. Teste de Kruskal-Wallis. Teste de Friedman.
DISCUSSÃO
A resistência de microrganismos aos medicamentos utilizados para tratar infecções10,11,18,21 causa sérios danos em pacientes imunocomprometidos e debilitados3,6,29,30, podendo aumentar as infecções sanguineas31 e elevar a morbidade e a mortalidade. Estudos em busca de uma terapia que proporcione a cura sem causar resistência vêm crescendo na atualidade, surgindo, desta forma, a TFD.
Por reduzir a habilidade de a Candida albicans causar uma infecção sistêmica14,24 a TFD tem sido considerada um tratamento alternativo promissor para infecções localizadas7,11,28.
É comum usuários de prótese apresentarem candidíase, uma infecção oportunista multifatorial, decorrente da ação patogênica do fungo CA, sendo considerada a doença de maior prevalência na mucosa oral 3,29,32,33. Apesar das orientações quanto à higiene e a recomendação do uso de antifúngicos, observa-se frequente recorrência dessa infecção34.
A VG é um tradicional fungicida agente utilizado para o tratamento de candidíase 22,35, é muito comum o seu uso em crianças e idosos, além de pacientes portadores de vírus HIV.
Ao se associar, nesta pesquisa, a VG a 1% com o laser vermelho (660nm), foi constatado que houve uma redução, nas primeiras horas, de colônias formadas, e, no decorrer das horas, não foi verificada a presença de UFCs. Um estudo36 em célula de adenosarcoma, in vitro, utilizou a VG a 1% associada ao laser Nd:YAG, com resultado satisfatório. Nesta mesma pesquisa36, o pesquisador também utilizou o AM a 1% com o laser Nd:YAG, com resultados satisfatórios.
No estudo aqui apresentado, ao se utilizar a VG a 1%, sem a TFD, foi observado que na 0h houve uma diminuição das UFCs, e nas 24h e 48h não houve formação de colônias.
Uma pesquisa testou concentrações menores do FS. A VG a 4µg/ml (0,0004%), reduziu a massa de biofilmes em pacientes com o vírus HIV, porém ele verificou que quanto maior a concentração da VG, melhores são os resultados obtidos26.
Outro estudo25 que também testou em pacientes com HIV a concentração da VG que fazia diferença no tratamento da CA, com uso de concentrações variadas, mostrou que a concentração de 0,00165%, a mais baixa testada por ele, revelou-se estável, bem tolerada, não manchou a mucosa oral e possuiu potente ação contra a CA. Apesar de esses dois últimos estudos terem um resultado bom com concentrações mais baixas da VG, visto que buscavam tratar pacientes sem trazer o desconforto de corar a boca, ainda houve formação de UFCs.
Ao ser testado o corante AM a 1% com o laser, foi analisado que ele, gradativamente, com o tempo, diminuiu as UFCs, ou seja, tem ação antifúngica. Outra investigação36 utilizou concentrações mais baixas do corante AM, e quase todas reduziram as UFCs, mas as concentrações do AM a 0,045% e 0,05% foram as únicas que obtiveram resultados semelhantes a este estudo, não havendo crescimento de colônias.
Corroborando esta pesquisa, há um consenso de que o AM pode ser utilizado com excelentes resultados6,13,38,39. Deve-se ter precaução ao se determinar as concentrações dos FSs, pois uma concentração mais alta faz-se necessária para uma eficácia maior da TFD, porém, concentrações muito altas tendem a não ser absorvidas pelos fungos, dificultando a ação da TFD3,14.
Ao se utilizar o AM a 1% sem o laser, foi possível observar um aumento do número de CAs. Ainda que tenha ocorrido redução, ela não foi significativa, e não é viável o uso do AM sem a TFD40.
No presente estudo, constatou-se que o laser sem FS é fatal para o microrganismo. Corroborando esses resultados está outra pesquisa12 in vivo, que comparou o uso do laser de comprimento de onda de 685nm e 830nm, com o uso de gel oral antifúngico (myconazolum), associado a uma solução antisséptica para a prótese.
Tal pesquisa12 mostrou que não há condiçoes de concluir se o efeito fungicida foi alcançado devido ao efeito da bioestimulçaõ a do LBI, ou devido a efeitos fototérmico ou fotodinâmico relacionados com cromóforos endógenos presentes nos fungos. Indo de encontro a esses achados outro estudo40 não apresentou redução para a CA e sim para a Candida tropicalis ao usar apenas o laser sobre esses fungos.
CONCLUSÃO
Os resultados in vitro indicam que a TFD associada à VG a 1% pode ser utilizada no tratamento de infecções causadas pela CA, mas existe a necessidade de se realizar pesquisas em humanos, visto que pode haver alteração desses resultados in vivo, para comprovar a eficácia desse corante na TFD.
REFERÊNCIAS
1. Donnelly RF, McCarron PA, Tunney MM. Antifungal photodynamic therapy. Microbiol Res. 2008; 163(1):1-12.
2. Karkowska-Kuleta J, Rapala-Kozik M, Kozik A. Fungi pathogenic to humans: molecular bases of virulence of Candida albicans, Cryptococcus neoformans and Aspergillus fumigatus. Acta Biochim Pol. 2009; 56(2):211-24.
3. Dai T, Fuchs BB, Coleman JJ, Prates RA, Astrakas C, Denis TGS, et al. Concepts and principles of photodynamic therapy as an alternative antinfungal discovery platform. Front Microbiol. 2012; 3:1-16.
4. Eggimann P, Garbino J, Pittet D. Epidemiology of Candida species infections in critically ill non-immunocompromised patients. Lancet Infect Dis. 2003; 3(11):685-702.
5. Pupo YM, Gomes GM, Santos EB, Chaves L, Michel MD, Koslowski Jr. VA et al. Susceptibility of Candida albicans to photodynamic therapy using methylene blue and toluidine blue as photosensitizing dyes. Acta Odontol Latinoam. 2011; 24(2):188-92.
6. Mitra S, Haidaris PHD, Snell SB, Giesselman BR, Hupsher SM, Foster TH. Susceptibility of Candida albicans to photodynamic therapy using methylene blue and toluidine blue as photosensitizing dyes. Lasers Surg Med. 2011; 43(4):324-32.
7. Lyon JP, Moreira LM, de Moraes PC, dos Santos FV, Resende MA. Photodynamic therapy for pathogenic fungi. Mycoses. 2011; 54(5):e265-71.
8. Grice EA, Segre JA. The human microbiome: our second genome. Annu Rev. Genomics Hum Genet. 2012; 13:151-70.
9. Pfaller MA, Diekema DJ. Epidemiology of invasive candidiasis: a persistent public health problem. Clin Microbiol Rev. 2007; 20(1):133-63.
10. Calzavara-Pinton PG, Rossi MT, Sala R. A retrospective analysis of real-life practice of off-label photodynamic therapy using methyl aminolevulinate (MAL-PDT) in 20 Italian dermatology departments. Part 2: oncologic and infectious indications. Photochem Photobiol Sci. [Internet]. 2013 [citado em 12 jan 2017]; 12(1): 158-65. DOI: 10.1039/c2pp25125f
11. Li DD, Xu Y, Zhang D-G, Quan H, Mylonakis E, Hu DD, et al. Fluconazole assists berberine to kill fluconazole-resistant Candida albicans. Antimicrob Agents Chemother. 2013; 57(12):6016-27.
12. Maver-Biscanin M, Mravak-Stipetic M, Jerolimov V, Biscanin A. Fungicidal effect of diode laser irradiation in patients with denture stomatitis. Lasers Surg Med. 2004; 35(4):259-62.
13. Queiroga AS, Trajano VN, Lima EO, Ferreira AF, Queiroga AS, Limeira FA Jr. In vitro photodynamic inactivation of Candida spp by different doses of low power laser light. Photodiagnosis Photodyn Ther. 2011; 8(4):332-6.
14. Kato IT, Prates RA, Sabino CP, Fuchs BB, Tegos GP, Mylonakis E et al. Antimicrobial photodynamic inactivation inhibits Candida albicans virulence factors and reduces In vivo pathogenicity. Antimicrob Agents Chemother. 2013; 57(1):445-51.
15. Pereira MSV, Siqueira-Júnior JP, Rodrigues E, Cavalcanti ML, Nascimento AE, Campos-Takaki GM. Evaluation of ultrastrutural changes induced by ofloxacin associated with cephalexin against human and bovine strains of staphylococcus aureus during post antibiotic effect (PAE). Int J Pharmacol Res. 2014; 1(1):15-21.
16. Dai T, Bil de Arce VJ, Tegos GP, Hamblin MR. Blue dye and red light, a dynamic combination for prophylaxis and treatment of cutaneous Candida albicans infections in mice. Antimicrob Agents Chemother. 2011; 55(12):5710-7.
17. Machado-de-Sena RM, Corrêa L, Kato IT, Prates RA, Senna AM, Santos CC et al. Photodynamic therapy has antifungal effect and reduces inflammatory signals in Candida albicans-induced murine vaginitis. Photodiagnosis Photodyn Ther. 2014; 11(3):275-82.
18. Calzavara-Pinton P, Rossi MT, Sala R, Venturini M. Photodynamic antifungal chemotherapy. Photochem Photobiol. 2012; 88(3):512-22.
19. Maisch T. A new strategy to destroy antibiotic resistant microorganisms: antimicrobial photodynamic treatment. Mini Rev Med Chem. 2009; 9(8):974-83.
20. Zeina B, Greenman J, Purcell WM, Das B. Killing of cutaneous microbial species by photodynamic therapy. Br J Dermatol. 2001; 144(2):274-8.
21. Dovigo LN, Pavarina AC, Ribeiro AP, Brunetti IL, Costa CA, Jacomassi DP et al. Investigation of the photodynamic effects of curcumin against Candida albicans. Photochem Photobiol. 2011; 87(4):895-903.
22. Mardh PA, Rodrigues AG, Genç M, Novikova N, Martinez-de-Oliveira J, Guaschino S. Facts and myths on recurrent vulvovaginal candidosis – a review on epidemiology, clinical manifestations, diagnosis, pathogenesis and therapy. Int J STD AIDS. 2002; 13(8):522-39.
23. Gomes-de-Elvas AR, Palmeira-de-Oliveira A, Gaspar C, Gouveia P, Palmeira-de-Oliveira R, Pina-Vaz C. et al. In vitro assessment of gentian violet anti-candida activity. Gynecologic Obstet Invest. 2012; 74(2):120-4.
24. Maley AM, Arbiser JL. Gentian violet: a 19th century drug re-emerges in the 21st century. Exp Dermatol. 2013; 22(12):775-80.
25. Jurevic RJ, Trabolsi RS, Mukherjee PK, Salata RA, Ghanoum MA. Identification of gentian violet concentration that does not stain oral mucosa, possesses anti-candidal activity and is well tolerated. Eur J Clin Microbiol Infect Dis. 2011; 30(5):629-33.
26. Traboulsi RS, Mukherjee PK, Chandra J, Salata RA, Jurevic R, Ghannoum MA. Gentian violet exhibits activity against biofilms formed by oral candida isolates obtained from HIV-infected patients. Antimicrob Agents Chemother. 2011; 55(6):3043-45.
27. Dörtbudak O, Haas R, Bernhart T, Mailath-Pokorny G. Lethal photosensitization for decontamination of implant surfaces in the treatment of peri-implantitis. Clin Oral Implants Res. 2001; 12(2):104-8.
28. Perni S, Prokopovich P, Pratten J, Parkin IP, Wilson M. Nanoparticles: heir potential use in antibacterial photodynamic therapy. Photochem Photobiol Sci. 2011; 10(5):712-720.
29. Sharon V, Fazel N. Oral Candidiasis and Angular Cheilits. Dermatol Ther. 2010; 23(3):230-42.
30. Carvalho GG, Felipe MP, Costa MS. The photodynamic effect of methylene blue and toluidine blue on Candida albicans is dependent on medium conditions. J Microbiol. 2009; 47(5):619-23.
31 Atalay MA, Koc AN, Demir G, Sav H. Investigation of possible virulence factors in Candida strains isolated from blood cultures. Niger J Clin Pract. 2015; 18(1):52-5.
32. Morales DK, Grahl N, Okegbe C, Dietrich LEP, Jacobs NJ, Hogan DA. Control of Candida albicans metabolism and biofilm formation by pseudomonas aeruginosa phenazines. MBio. 2013; 4(1):e00526-12.
33. Ford CB, Funt JM, Abbey D, Issi L, Guiducci C, Martinez DA et al. The evolution of drug resistance in clinical isolates of Candida albicans. Elife. 2015; 4:e00662.
34. Neppelenbroek KH, Machado AL, Pavarina AC, Massucato EM, Colombo AL, Vergani CE. Effectiveness of microwave disinfection of complete dentures on the treatment of Candida-related denture stomatitis. J Rehabil Oral. 2008; 25(3):232-44.
35. Vazquez JA, Sobel JD. Mucosalcandidiasis. Infect Dis Clin North Am. 2001; 16(4):793-820.
36. Teichert MC, Jones JW, Usacheva MN, Biel MA. Treatment of oral candidiasis with methylene blue-mediated photodynamic therapy in an immunodeficient murine model. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2002; 93(2):155-60.
37. Oliveira CS, Turchiello R, Kowaltowski AJ, Indig GL, Baptista MS. Major determinants of photoinduced cell death: subcellular localization versus photosensitization efficiency. Free Radic Biol Med. 2011; 51(4): 824-33.
38. Mima EG, Pavarina AC, Ribeiro DG, Dovigo LN, Vergani CE, Bagnato VS. Effectiveness of photodynamic therapy for the inactivacion of candida SSP. on dentures: in vitro study. Photomed Laser Surg. 2011; 29(12):827-33.
39. Khademi H, Torabinia N, Allameh M, Jebreilamtigh HR. Comparative evaluation of photodynamic therapy induced by two different photosensitizers in rat experimental candidiasis. Dent Res J. 2014; 11(4):452-9.
40. Souza SC, Junqueira JC, Balducci I, Koga-Ito CY, Munin E, Jorge AO. Photosensitization of different Candida species by low power laser light. J Photochem Photobiol B. 2006; 83(1):34-8.
Autor notes