Artigos Originais

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 19 Abril 2021
Aprobación: 31 Agosto 2021
Resumo: Este é um estudo de corte transversal com delineamento descritivo, com dois grupos populacionais, tipo antes e depois, com abordagem quantitativa do tipo analítica com correlação entre variáveis, realizado entre 2018 e 2019, com objetivo de analisar fatores de risco cardiometabólicos, clínicos e laboratoriais associados à síndrome metabólica em mulheres com tireoidite crônica autoimune eutireoideas, na pré e pós-menopausa, acompanhadas em serviço terciário. Participaram 109 mulheres, sendo 56 com Tireoidite Crônica Autoimune em status eutireoideo e 53 sem disfunção tireoidiana. Das 56 mulheres, 25 foram incluídas no grupo com Tireoidite Crônica Autoimune na pré-menopausa e 31 foram incluídas na pós-menopausa e, das 53 mulheres com função tireoidiana normal, 25 foram incluídas no grupo comparativo na pré-menopausa e 28 no grupo comparativo na pós-menopausa. O perfil metabólico sugeriu resistência insulínica, com taxas mais elevadas no grupo com tireoidite pré e pós-menopausa e grupo controle pós, bem como perfil lipídico desfavorável. Apresentaram síndrome metabólica 36% do grupo afetado pré-menopausa e 51,6% do grupo afetado pós, contra nenhuma e 14,3% dos grupos comparativos, respectivamente. Se resistência insulínica ou obesidade decorreram da tireoidite, o estudo não permitiu concluir. Pacientes com tireoidite devem receber atenção com relação ao perfil lipídico.
Palavras-chave: Tireoidite autoimune, Síndrome metabólica, Resistência à insulina, Fatores de risco.
Abstract: This is a cross-sectional study with a descriptive design, with two population groups before and after, type, with a quantitative approach of the analytical type with correlation between variables, carried out between 2018 and 2019. It aimed to analyze cardiometabolic, clinical and laboratory risk factors associated with metabolic syndrome in women with chronic autoimmune euthyroid thyroiditis, in pre and post-menopause, followed up in a tertiary service. 109 women participated, 56 with Chronic Autoimmune Thyroiditis in euthyroid status and 53 with no thyroid dysfunction. Of the 56 women, 25 were included in the premenopausal Chronic Autoimmune Thyroiditis group and 31 were included in the postmenopausal group, and of the 53 women with normal thyroid function, 25 were included in the premenopausal comparative group and 28 in the postmenopausal comparative group. The metabolic profile suggested insulin resistance, with higher rates in the pre and post-menopausal thyroiditis group and post-menopausal control group, as well as an unfavorable lipid profile. 36% of the premenopausal affected group and 51.6% of the postmenopausal affected group had metabolic syndrome, against none and 14.3% of the comparative groups, respectively. Whether insulin resistance or obesity resulted from thyroiditis, the study did not allow us to conclude. Patients with thyroiditis should be given attention to their lipid profile.
Keywords: Tiroiditis autoinmune, Metabolic syndrome, Insulin resistance, Risk factors.
Resumen: Este es un estudio transversal con diseño descriptivo, con dos grupos poblacionales, tipo antes y después, con enfoque cuantitativo de tipo analítico con correlación entre variables, realizado entre 2018 y 2019, con el objetivo de analizar los factores de riesgo cardiometabólicos, clínicos y de laboratorio asociados al síndrome metabólico en mujeres con tiroiditis crónica autoinmune eutiroidea, pre y postmenopáusicas, monitoreadas en un servicio terciario. Participaron 109 mujeres, 56 con Tiroiditis Crónica Autoinmune en estado eutiroideo y 53 sin disfunción tiroidea. De las 56 mujeres, 25 se incluyeron en el grupo con Tiroiditis Crónica Autoinmune en la premenopausia y 31 en la posmenopausia, y de las 53 mujeres con función tiroidea normal, 25 se incluyeron en el grupo de comparación en la premenopausia y 28 en el grupo de comparación en la posmenopausia. El perfil metabólico sugirió resistencia a la insulina, con tasas más elevadas en el grupo con tiroiditis pre y posmenopáusica y en el grupo de control posmenopáusico, así como un perfil lipídico desfavorable. El 36% del grupo afectado premenopausia y el 51,6% del grupo de afectado posmenopausia tenían síndrome metabólico, frente a ninguna y el 14,3% de los grupos de comparación, respectivamente. El estudio no pudo concluir si la resistencia a la insulina o la obesidad eran consecuencia de la tiroiditis. Los pacientes con tiroiditis deben recibir atención respecto a su perfil lipídico.
Palabras clave: Tiroiditis autoinmune, Síndrome metabólico, Resistencia a la insulina, Factores de riesgo.
INTRODUÇÃO
A Tireoidite Crônica Autoimune (TCA), também denominada Tireoidite de Hashimoto (TH) ou Tireoidite Linfocítica Crônica, representa a causa mais comum de hipotireoidismo em áreas suficientes em iodo1-2. Tem prevalência estimada em 5% da população adulta, com uma prevalência cinco vezes superior em mulheres do que em homens; e sua incidência tem aumentado nos últimos 50 anos, sobretudo entre 45 e 65 anos3-4.
A autoimunidade tireoidiana se desenvolve em decorrência de perda da tolerância imunológica e reatividade a auto-antígenos. O ataque ao sistema imunológico se manifesta pela infiltração da tireoide por linfócitos T, produção de anticorpos antitireoglobulina (anti-TG) e antitireoperoxidase (anti-TPO), podendo se apresentar sob duas formas clínicas: atrófica e bociosa1-3. Vários são os fatores associados à quebra de tolerância imunológica, como infecções, predisposição genética, medicamentos e fatores ambientais como concentrações de iodo, selênio e outros1,5.
A Síndrome Metabólica (SM) é um transtorno complexo, constituído por um conjunto de fatores de risco cardiometabólicos. Caracteriza-se pelo acúmulo de gordura abdominal, dislipidemia (HDL baixo e hipertrigliceridemia), resistência insulínica e hipertensão arterial sistêmica (HAS)6-7. Confere predisposição 2,5 vezes maior a doenças cardiovasculares, aumentando a mortalidade geral em cerca de 1,5 vezes7-8.
Nos últimos anos, alguns estudos têm demonstrado associação entre disfunções tireoidianas, desenvolvimento de distúrbios metabólicos e doenças cardiovasculares6,9, enquanto outros trabalhos reportaram associação entre concentrações de T4 livre (T4L), ocorrência de resistência insulínica e dislipidemia mesmo em indivíduos eutireoideos10. Os hormônios tireoidianos atuam em várias vias metabólicas referentes aos carboidratos e lipídeos, influenciando na regulação da gliconeogênese hepática, lipogênese e lipólise10. Sendo assim, é de se esperar que disfunções tireoidianas que interferem em vias metabólicas específicas predisponham a SM e aumentem fatores de risco cardiovascular11.
As alterações metabólicas que ocorrem no hipotireoidismo são similares aos presentes na SM, além de compartilharem fatores de risco como idade e climatério, elevando a probabilidade de ocorrência simultânea das duas condições11. Assim, este estudo tem como objetivo analisar fatores de risco cardiometabólicos, clínicos e laboratoriais associados à síndrome metabólica em mulheres com tireoidite crônica autoimune eutireoideas, na pré e pós-menopausa, acompanhadas em serviço terciário.
MÉTODO
Trata-se de estudo observacional de corte transversal com delineamento descritivo, com dois grupos populacionais, tipo antes e depois, com abordagem quantitativa do tipo analítica com correlação entre variáveis, desenvolvido no Ambulatório de Tireoide da Disciplina de Endocrinologia e Metabologia da Universidade Federal do Triângulo Mineiro (UFTM).
A amostra do estudo foi de conveniência através do livro de arquivo de atendimentos, selecionando-se todas as mulheres que se enquadraram nos critérios de inclusão: mulheres com idade entre 21 e 66 anos, dividida em quatro grupos, sendo dois grupos com TCA na pré (G1) e na pós-menopausa (G2) e seus respectivos grupos comparativos, sendo o grupo comparativo na pré (GC1) e o grupo comparativo na pós-menopausa (GC2), pareados por idade e status de pré ou pós-menopausa e com função tireoidiana normal.
Os critérios de inclusão para o G1 foram: ser do sexo feminino, apresentar idade igual ou superior a 18 anos, ciclos menstruais regulares, portanto estar em status de pré-menopausa, ter diagnóstico prévio de TCA (o diagnóstico prévio deve ter levado em consideração a presença das seguintes alterações: TSH elevado, T4L normal ou diminuído, anticorpos anti-tireoidianos positivos ou alterações ultrassonográficas e/ou citológicas sugestivas de TCA), estar em tratamento com hormônio tireoidiano e apresentar dosagens hormonais compatíveis com o controle adequado da doença.
Os critérios de inclusão para o G2 foram: ser do sexo feminino, apresentar idade igual ou superior a 40 anos, não apresentar mais ciclos menstruais e estar no status pós-menopausa, ter diagnóstico prévio de TCA e estar em tratamento com hormônio tireoidiano e apresentar dosagens hormonais compatíveis com o controle da doença.
Os critérios de inclusão para o GC1 foram: ser do sexo feminino, apresentar idade igual ou superior a 18 anos, não apresentar diagnóstico de doenças relacionadas à tireoide, apresentar ciclos menstruais regulares e estar no status pré-menopausa.
Os critérios de inclusão para o GC2 foram: ser do sexo feminino, apresentar idade igual ou superior a 40 anos, não apresentar diagnóstico de doenças relacionadas à tireoide, não apresentar mais ciclos menstruais e estar no status de pós-menopausa. Excluíram-se mulheres em período gestacional, com irregularidades menstruais e outras doenças crônicas capazes de interferir na função tireoidiana.
Os dados foram coletados de fevereiro de 2018 a junho de 2019. Foi utilizado um questionário semiestruturado, dois sistemas ambulatoriais utilizados para visualizar os exames laboratoriais, os prontuários das pacientes e os registros de atendimentos. As pacientes com TCA e as voluntárias dos grupos comparativos passaram por avaliação clínica, avaliação dos parâmetros antropométricos e laboratoriais. Foram realizadas duas consultas para cada grupo: na primeira consulta, aplicou-se o questionário semiestruturado, submeteu-se o pedido de exames e agendou-se a consulta de retorno. Na consulta de retorno dos quatro grupos, eram analisados os resultados dos exames e entregue um plano alimentar individualizado para cada participante.
Na avaliação clínica, foram mensurados peso, altura, pregas cutâneas (tricipital, bicipital, supra ilíaca e subescapular), medida a circunferência abdominal determinada no ponto médio entre o rebordo costal inferior e a crista ilíaca, aferição da pressão arterial e classificada de acordo com a 7ª Diretriz Brasileira de Hipertensão Arterial (2016)12 e calculado o Índice de Massa Corporal (IMC) e o percentual de gordura corporal.
A avaliação laboratorial foi composta pelas determinações plasmáticas das concentrações de glicemia de jejum, colesterol total, frações e triglicerídeos, ácido úrico, hemoglobina glicada, TSH, T4L, anticorpos Anti-TPO e Anti-TG e insulina basal. Além disso foi calculado o índice Homeostasis model assessment insulin resistance (HOMA-IR)13 segundo a fórmula:
HOMA-IR = glicemia de jejum ( mmol/L*) x insulina jejum (µUI/mL) / 22,5
Para conversão da glicose de mg/dL para mmol/L, multiplica-se o valor em mg/dl por 0,0555 (Diretrizes da Sociedade Brasileira de Diabetes, 2019-2020)13.
O presente estudo adotou os critérios estabelecidos pela International Diabetes Federation (IDF) (2006)14 para diagnóstico da Síndrome Metabólica e o Escore de Risco Global (ERG) para estimativa da probabilidade de ocorrência de infarto do miocárdio ou morte por doença coronariana no período de 10 anos, calculado segundo a Sociedade Brasileira de Cardiologia (2017)15.
Para testar os dados foram verificados pressupostos de normalidade pelo teste de Kolmogorov-Smirnov e homogeneidade de variâncias pelo teste de Levene. As variáveis foram transformadas por:
√𝑥, ou √𝑥+0,5 , ou 𝑙𝑜𝑔𝑥 , ou 𝑙𝑜𝑔𝑥+1,
ou por boxcox, quando não atendidos pressupostos de normalidade ou apresentavam heterogeneidade de variâncias.
A comparação das frequências das ocorrências dos fatores de risco cardiometabólicos entre os grupos foi por meio do teste qui-quadrado. O teste ANOVA ou Kruskal Wallis foram aplicados para comparações entre 3 ou mais grupos, seguido do teste de Tukey ou teste de Dun para comparações múltiplas, respectivamente. Para verificar a correlação entre as variáveis, foram utilizados os coeficientes de Pearson ou Spearman. Adotou-se um nível de significância de 5%.
Os aspectos éticos foram baseados na Resolução CNS 466/12 sobre pesquisa envolvendo seres humanos e foi aprovada pelo Comitê de Ética em Pesquisa da Universidade Federal do Triângulo Mineiro sob o CAE: 51789915.5.0000.5154. As participantes assinaram o Termo de Consentimento Livre e Esclarecido (TCLE), garantindo seu anonimato e o direito de desistir da pesquisa a qualquer instante.
RESULTADOS
Participaram 109 mulheres, sendo 56 com TCA em status eutireoideo e 53 sem disfunção tireoidiana. Das 56 mulheres, 25 foram incluídas no grupo com TCA na pré-menopausa (G1) e 31 foram incluídas no grupo com TCA na pós-menopausa (G2) e, das 53 mulheres com função tireoidiana normal, 25 foram incluídas no grupo comparativo na pré-menopausa (GC1) e 28 no grupo comparativo na pós-menopausa (GC2).
Nas Tabelas 1 e 2, foram representados dados clínicos e bioquímicos. Não se evidenciou diferenças quanto ao IMC (p=0,372), bem como em relação às frequências segundo estado nutricional (p=0,215). A idade foi significantemente maior nos grupos G2 e GC2.
A C.A no G2 foi significativamente maior que GC1 (p=0,004), e as frequências de participantes com CA alterada também foi maior no G2 (p=0,002). Da mesma forma, em relação ao %GC, detectou-se diferença significativa entre os grupos (p=0,016), sendo o GC2 maior que GC1(p=0,04), e, em relação às frequências, o GC1 apresentou maior frequência de participantes com %GC na média em relação ao GC2 (p=0,044) (Tabelas 1 e 2). Não foram observadas diferenças significativas ao se comparar as médias de PAS entre os grupos, e, com relação a PAD, o teste de Kruskal Wallis indicou diferença entre os grupos (p=0,027), mas o teste de comparações múltiplas de DUN não revelou entre quais grupos havia diferença (Tabela 1). As frequências de PAS normais e alteradas não diferiram entre os grupos (p= 0,105) e, em relação à PAD, não foi feita esta comparação, pois todas as participantes estavam com a PAD normal (Tabela 2).
Ao se comparar a glicemia de jejum (mg/dL) entre os grupos de mulheres com TCA e comparativos, foram verificadas diferenças significativas entre os grupos, sendo o G2 significativamente maior que G1 (p<0,0001), GC1 (p<0,0001) e GC2 (p<0,0001), e GC2 significativamente maior que G1 (p<0,0001), e GC1 (p<0,0001) (Tabela 1). As frequências de GJ alterada entre as participantes foram significativamente maiores no grupo G2 em relação a todos os grupos, enquanto a frequência de mulheres com GJ normal foi significativamente maior no GC1 (Tabela 2).
Observou-se diferença significativa ao se comparar a HbA1c entre os grupos (p<0,0001), sendo o G1 maior que o GC1 (p<0,0001); G2 maior que GC1 (p<0,0001) e GC2 maior que GC1 (p<0,02) (Tabela 1). A frequência de mulheres com HbA1c normal no GC1 foi significativamente maior do que a frequência de mulheres do GC1 com HbA1c alterada (p=0,047) (Tabela 2).
Da mesma forma, observou-se diferença significativa ao se comparar as concentrações de insulina (µUI/mL) entre os grupos (p=0,008), sendo GC2 significativamente maior que GC1 (p=0,003) e G2 (p=0,01) (Tabela 1). As frequências de insulina normais e alteradas entre os grupos não demonstrou significância estatística (p=0,115) (Tabela 2).
Em relação ao índice Homa-IR, foi observado que GC2 foi significativamente maior que GC1 (p=0,04), e não foi observada diferença entre G1 e G2 (Tabela 1). As frequências de HOMA-IR normais e alteradas entre os grupos não demonstrou significância estatística (p= 0,281) (Tabela 2).
Não foram observadas diferenças significativas ao se comparar as médias das variáveis TSH, T4L e ácido úrico entre os grupos (Tabela 1). As frequências de ácido úrico normais e alteradas entre os grupos não demonstrou significância estatística (p=0,107) e, em relação ao TSH e T4L, não foram calculadas, pois todas as participantes estavam com as concentrações dentro dos valores considerados normais (Tabela 2).
A comparação das variáveis do perfil lipídico entre os grupos demonstrou que as concentrações médias do HDL-c (mg/dL) foram significativamente maiores no GC1 (p=0,04) e GC2 (p=0,012) em relação a G1, não havendo diferenças entre os demais grupos (Tabela 1). As frequências de HDL-c normais e alteradas entre os grupos não demonstrou significância estatística (p= 0,251) (Tabela 2).
As médias de LDL-c (mg/dL) nos grupos GC1 e GC2 foram significativamente menores do que no do G2 p=0,008, p=0,039, respectivamente. E quanto às frequências normais e alteradas, não houve diferença entre os grupos (p=0,357).
As médias de ñ-HDL-c não foram diferentes entre G1 e G2 (Tabela 1), porém as concentrações médias no G2 foram significativamente maiores do que no GC2 (p=0,025), e o percentual de mulheres com ñ-HDL-c alterado foi maior do que o percentual normal no grupo G2 (p=0,005).
Não foi observada significância estatística ao se comparar as médias de CT e TG entre os grupos (Tabela 1), bem como em relação as frequências de normais e alteradas também não apresentaram diferenças (Tabela 2).
De acordo com orientações reportadas na atualização da V Diretriz Brasileira de Dislipidemia e Aterosclerose (2017), o escore de risco global (ER) foi calculado em pacientes acima de 30 anos. No G1, o ER foi calculado em 16 pacientes, sendo alto em duas, intermediário em duas e baixo nas demais. No GC1, o ER calculado em 15 pacientes foi baixo em todas. No G2, foi alto em uma, intermediário em 16 e baixo nas demais. No GC2, foi intermediário em quatro, baixo nas demais e a comparação de ER entre os grupos não demonstrou diferença estatística (p= 0,107) (Tabela 1).
Características clínicas e bioquímicas entre os grupos, Uberaba, 2020.
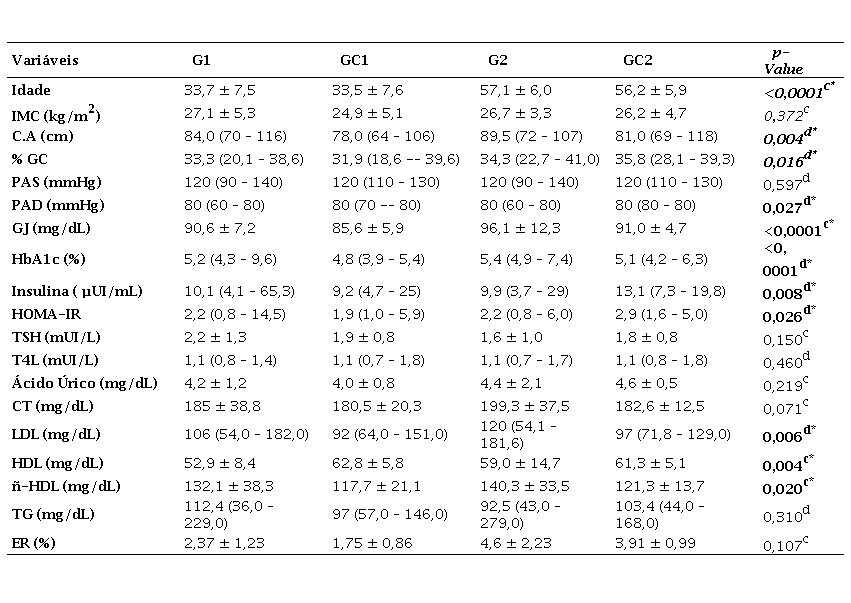
%GC – Gordura Corporal; CA – Circunferência abdominal; PAS – Pressão Arterial Sistólica; IMC – Índice de Massa Corporal; PAD – Pressão Arterial Diastólica; GJ – Glicemia de Jejum; HbA1c – Hemoglobina Glicada; TSH – Thyroid-stimulating hormone; T4L –Tiroxina; Anti TPO - Antiperoxidase; Anti TG – Antitireoglobulina; CT – Colesterol Total; LDL– c– Low Density Lipoproteic Cholesterol; HDL–c – High Density Lipoproteic Cholesterol; Ñ HDL–c – Não - High Density Lipoproteic Cholesterol; VLDL– c – Very low density lipoprotein; TG – Triglicerídeos; ER – Escore de risco. cANOVA: Idade – G2>G1 p<0,0001; GC2>G1 p<0,0001; G2>GC1 p<0,0001; GC2>GC1 p<0,0001/ GJ – G2>G1 p<0,0001; G1>GC1 p<0,0001; GC2>G1 p<0,0001; G2>GC1 p<0,0001; G2>GC2 p<0,0001; GC2>GC1 P<0,0001. dKruskal Wallis: C.A – G2>GC1 p=0,002 / %GC – GC2>GC1 p=0,04; HbA1c – G1>GC1 p<0,0001; G2>GC1 p<0,0001; GC2>GC1 p<0,02 / Insulina - G4>G2 p=0,03; GC2>GC1 p=0,01 / HOMA-IR – GC2>GC1 p= 0,04. *p<0.05.
Variáveis clínicas e bioquímicas entre os grupos, Uberaba, 2020.

CA – Circunferência abdominal; IMC – Índice de Massa Corporal; %GC – Gordura Corporal; PAS – Pressão Arterial Sistólica; GJ – Glicemia de Jejum; HbA1c – Hemoglobina Glicada; TSH – Thyroid-stimulating hormone; T4L –Tiroxina; Anti TPO - Antiperoxidase; Anti TG – Antitireoglobulina; CT – Colesterol Total; LDL– c– Low Density Lipoproteic Cholesterol; HDL–c – High Density Lipoproteic Cholesterol; Não HDL–c – Não - High Density Lipoproteic Cholesterol; VLDL– c – Very low density lipoprotein; TG – Triglicerídeos. aTeste qui quadrado. *p<0.05.
Na Tabela 3, as pacientes foram analisadas segundo a presença dos critérios para diagnóstico da SM. Os percentuais se apresentaram maiores no G1 em relação ao grupo comparativo e, ao se comparar as frequências entre os dois grupos, foi demonstrada diferença estatística, sendo frequência de mulheres do GC1 sem fatores de risco significativamente maior do que do G1. O mesmo ocorreu no G2 em relação ao GC2 e, ao se comparar as frequências entre os dois grupos, foi demonstrada diferença, sendo a frequência de mulheres do GC2 sem fatores de risco significativamente maior do que do G2, enquanto a frequência de mulheres do G2 com síndrome metabólica foi significativamente maior que no GC2.
Comparação das frequências de fatores de risco em mulheres com tireoidite crônica autoimune (TCA) e mulheres dos grupos comparativos, Uberaba, 2020.
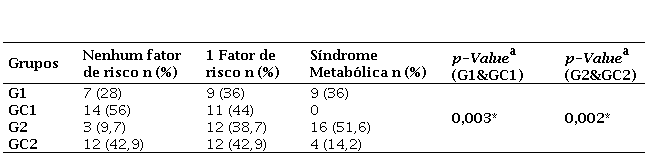
a Teste Qui-Quadrado; *p<0.05
A Tabela 4 apresenta os valores do coeficiente de correlação para as relações entre variáveis clínicas, laboratoriais e perfil lipídico das participantes na pré-menopausa. Nota-se que, no G1, a GJ, concentrações de Insulina e índice HOMA-IR se correlacionaram significativamente com IMC e %GC. HOMA-IR ainda se correlacionou com CA e HDL-c. Correlações inversas ocorreram entre HbA1c e HDL-c, e diretas entre AU e T4L com TG. Não foram demonstradas correlações entre dados clínicos e perfil lipídico. Já no GC1, GJ, HbA1c, insulina, índice HOMA-IR, AU e perfil lipídico (excetuando-se HDL-c) se correlacionaram diretamente com índices de adiposidade (IMC, CA e %GC). GJ ainda se correlacionou significativamente com ñ-HDL-c e TG, insulina com TG e HOMA-IR positivamente com CT e inversamente com HDL-c. AU se correlacionou positivamente com CT e ñ-HDL-c e TSH com CA, HbA1c apresentou correlação inversa com HDL-c e direta com ñ-HDL-c e TG.
E na Tabela 5 são apresentados os valores do coeficiente de correlação para as relações entre variáveis clínica, laboratoriais e perfil lipídico das participantes na pós-menopausa. Nota-se que, no G2, menos correlações foram significativas entre variáveis bioquímicas e dados antropométricas. As concentrações de insulina apresentaram correlações fracas, mas significantes, com IMC, CA, moderadas com TG e inversas com HDL-c. HbA1c se correlacionou significativamente com CA, %GC e correlação inversa com CT. TSH apresentou correlação inversa com ñ-HDL-c. O perfil lipídico apresentou correlação inversa com variáveis antropométricas. E no GC2, GJ se correlacionou positiva e significativamente com CA e TG e negativamente com HDL-c. HOMA-IR se correlacionou positiva e significativamente com ñ-HDL-c e TG e negativamente com HDL-c.
Correlações entre as variáveis clínicas e metabólicas de participantes com TCA na pré-menopausa (G1) e grupo comparativo (GC1). Uberaba-MG, 2020.
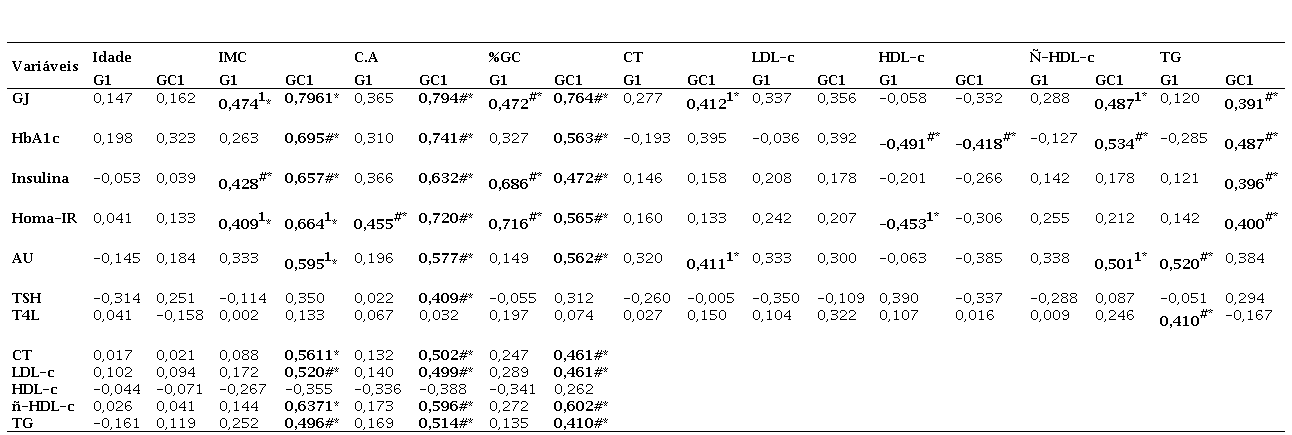
1 Teste de Pearson; #Teste de Spearman; *p<0.05.
Correlações entre as variáveis clínicas e metabólicas de participantes com TCA tratadas na pós-menopausa (G2) e grupo comparativo (GC2). Uberaba-MG, 2020.
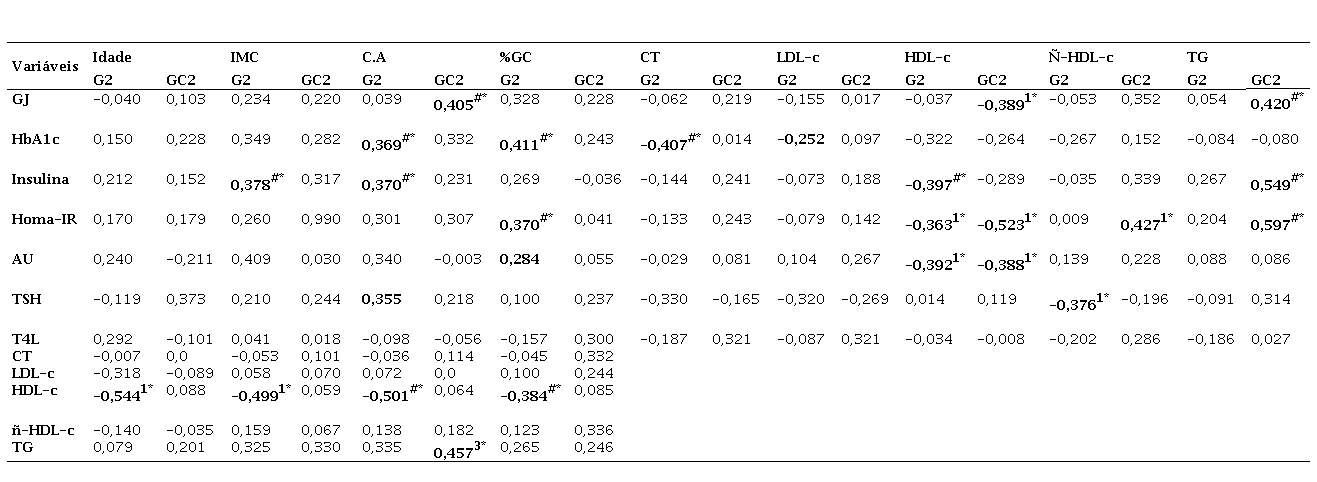
1 Teste de Pearson; #Teste de Spearman; *p<0.05.
DISCUSSÃO
A presente pesquisa analisou fatores de risco cardiometabólicos, clínicos e laboratoriais em mulheres com TCA tratadas na pré e pós-menopausa, com vistas a responder ao principal questionamento, qual seja, se as mulheres com TCA que tiveram hipotireoidismo ao diagnóstico, mas que atualmente estão em tratamento regular com L-tiroxina, se comportam, em relação ao perfil clínico e metabólico, de maneira similar as mulheres sem patologias relacionadas à tireoide.
Como era de se esperar, na seleção, as idades do G1 e GC1 foram significantemente menores que G2 e GC2 pois obedeceu ao critério idade e status hormonal, ou seja, grupos com ciclos menstruais regulares e grupos com climatério já iniciado.
A maioria das mulheres do G1 apresentaram percentuais de IMC de sobrepeso/obesidade (56%), e de C.A (64%) acima de 80 cm, embora sem diferença em relação ao grupo comparativo GC1, sugerindo que estes dados não se devem somente a presença da TCA, mas também estão associados a maior prevalência de sobrepeso e obesidade na população geral. Como em outros países, a obesidade no Brasil vem sendo considerada uma epidemia em crescimento16, sendo a sua etiologia complexa e multifatorial, resultante da interação de genes, fatores emocionais, ambientais, culturais e estilos de vida17.
Da mesma forma, no G2, participantes também apresentaram percentuais mais elevados de IMC de sobrepeso/obesidade (63,6%), mas de modo geral não houve diferença estatística entre os grupos. Entretanto, a C.A. esteve acima de 80 cm em 90,2% das participantes do G2, apresentando diferença em relação ao GC2, ainda que mesmo neste grupo, 53,6% das mulheres apresentassem CA acima de 80 cm, sugerindo somatória de fatores como a presença de TCA, o aumento de sobrepeso/obesidade na população geral e climatério, no G2 e no seu grupo comparativo os dois últimos fatores poderiam ser responsabilizados9,11.
A comparação entre os grupos dos índices de adiposidade não demonstrou diferença significante em IMC, mas a CA no G2 foi maior quando comparada a mulheres jovens (GC1), bem como a frequência já referida, maior no G2, no qual se associaram três condições: idade, climatério e TCA. O %GC foi maior no GC2 do que no GC1, sugerindo também a relevância do fator idade e climatério no acúmulo de gordura subcutânea. Com o avançar da idade e chegada do climatério, a prevalência de sobrepeso/obesidade aumenta, ocorre diminuição da massa magra, redistribuição da gordura corporal para o tipo central, resistência à insulina e síndrome metabólica9,11.
A TCA atinge a tireoide, porém as alterações imunológicas dos indivíduos afetados apresentam repercussões sistêmicas com produção e secreção de citocinas pró-inflamatórias, sobretudo a interleucina 6 (IL-6), também produzida por adipócitos e macrófagos do tecido adiposo. Elevações das concentrações de IL-6 têm sido relacionadas a maior risco aterosclerótico, e concentrações séricas de citocinas inflamatórias têm sido encontradas em pacientes com TCA, o que sugere que mesmo em status eutireoidiano, seriam caracterizados por um estado pró-inflamatório11 capaz de interferir na distribuição de gordura corporal, justificando assim percentuais encontrados e valores de C.A mais elevados nos grupos G1 e G2, ainda que a significância estatística tenha sido demonstrada apenas no G2.
Uma investigação que avaliou mulheres com hipotireoidismo subclínico na pós-menopausa encontrou resultados similares a esta pesquisa em relação à CA, associando seus achados a alterações de autoimunidade, pois pacientes que apresentaram auto-anticorpos anti-tireoide reagentes foram os mais afetados11. Já em pesquisa que se propôs a avaliar mulheres com TCA em status eutireoideo, assim como nesta pesquisa, e o achado encontrado com relação a CA foi o mesmo, mulheres com TCA tratadas apresentaram CA mais elevada em relação ao grupo controle18.
Estudo realizado com homens e mulheres na pós-menopausa observou que o acúmulo de gordura no tronco em mulheres eutireoideas na pós-menopausa está relacionado ao aumento na concentração de T3 livre (T3L)19. Na presente pesquisa, todas as participantes estavam tratadas e em eutireoidismo, mas não é rotina da avaliação do tratamento realizar dosagem de T3L. Na prática clínica, considera-se como bem tratada a paciente que apresenta TSH e T4L nos valores de referência, mas o T4L é considerado um pró-hormônio do T3L, e suas concentrações sanguíneas podem não expressar o que de fato ocorre em nível tecidual e molecular20.
Os hormônios tireoidianos, sobretudo o T3L, são de extrema importância para manutenção do metabolismo basal, modulação do apetite e ingestão alimentar, facilitam a termogênese adaptativa e regulam o peso corporal. Juntamente com a leptina, regulam a sinalização no núcleo arqueado do hipotálamo e refletem as alterações nos estoques de energia. Em pacientes com hipotireoidismo, seguidos antes e após o tratamento, foram observados níveis elevados de leptina, o qual se correlacionaram com IMC e concentrações de TSH20. Na presente pesquisa, a condição de eutireoidismo pressupõe que não haja anormalidades nestes níveis de regulação. Entretanto, a avaliação foi transversal e não investigamos se, ao longo do tempo ou na duração do tratamento, as pacientes apresentaram regularidade absoluta do tratamento.
A análise do perfil glicêmico demonstrou que no G2 a GJ, mesmo dentro dos valores de referência, foi maior que em todos os grupos. Por outro lado, no GC2 foi maior do que no G1 e GC1. É esperado que, com o envelhecimento, as funções e massa das células beta fiquem comprometidas, diminuindo a liberação de insulina e aumentando glicose plasmática21 desviando o metabolismo intermediário para neoglicogênese, glicogenólise, acúmulo de gordura abdominal e aumento de C.A. Além disso existem os outros fatores a serem considerados no contexto da TCA e do climatério no grupo G2, da TCA no G1 e da obesidade populacional aumentada em todos. Pela mesma forma a HbA1c também esteve mais elevada nos grupos afetados do que nos grupos comparativos (G1>GC1; G2>GC1) e mesmo entre os grupos comparativos, no GC2 foi significativamente maior que no GC1, reforçando a justificativa.
Em relação às concentrações de insulina, neste estudo o GC2 foi maior que GC1 e G2, refletindo-se no índice HOMA-IR, que também foi maior no GC2 em relação ao GC1, enquanto não houve diferença entre os outros grupos. Era esperado que estas variáveis fossem menores nos grupos comparativos; entretanto, as pacientes foram pareadas pela idade e status hormonal e não por variáveis antropométricas, logo tais alterações expressam os índices de adiposidade alterados na população geral22-23. Há escassez de trabalhos na análise de pacientes com TCA em status eutireoideano e variáveis metabólicas, mas alguns estudos1,11não observaram diferença na concentração de GJ, enquanto outro18 apontou diferenças significativas em relação a concentração de GJ. Com relação ao índice HOMA-IR, foi observada diferença entre pacientes com TCA01, e observada associação entre obesidade central, HBA1c mais elevada, índice HOMA-IR alterado, concentrações lipídicas anormais e presença da síndrome metabólica24.
Como em outras pesquisas25-26, no GC1 encontrou-se correlações positivas entre as variáveis antropométricas (IMC, CA e %GC) com as variáveis do perfil metabólico, além de correlação positiva entre TSH e CA. Já no GC2, as correlações entre dados antropométricos e perfil metabólico não foram tão claras, sendo significantes apenas em relação a GJ e CA, mostrando relação direta entre CA e resistência insulínica, sendo ambos fatores de risco para a SM22-23.
Considerando o perfil lipídico, observou-se correlação entre CA e TG. O consumo excessivo de alimentos ricos em lipídeos, eleva a densidade calórica da dieta e aumenta a obesidade na região abdominal e, consequentemente, a CA27, principalmente em mulheres na pós-menopausa, que já possuem tendência a acumular gordura nesta região9,11.
No G1, houve correlações significantes entre algumas variáveis do perfil glicêmico com variáveis antropométricas, o que sugere associação direta entre índices de adiposidade e distribuição de gordura corporal com as variáveis metabólicas. Diferentemente do GC1, no G1 não se observou correlação entre TSH ou T4L com os índices de adiposidade. E, no G2, correlações positivas entre HbA1c, CA e %GC, das concentrações de insulina com IMC, CA, do índice HOMA-IR e %GC, indicam conexões entre concentrações médias de glicose, resistência insulínica, estado nutricional e distribuição de gordura, sendo consenso em outra pesquisa, na qual há presença da resistência insulínica na obesidade e em indivíduos com maior acúmulo de gordura abdominal25. Ainda neste grupo, observou-se correlações significantes entre ácido úrico e IMC e entre TSH e CA, como já demonstrado em outros estudos11. Considerando-se o perfil lipídico, observou-se correlações inversas do HDL-c com variáveis antropométricas, o que está dentro do contexto da resistência à insulina e síndrome metabólica mais encontrada nestas pacientes.
De modo geral, houve predomínio de valores limítrofes e altos nos grupos afetados (G1 e G2) em relação ao perfil lipídico como um todo. Avaliando parâmetros lipídicos e o excesso de lipoproteína (a) em um subgrupo de mulheres com TCA em eutireoidismo foi verificado aumento das concentrações de CT, LDL-c e TG em relação aos controles28. Os dados corroboram os deste estudo28, embora ele não tenha avaliado HDL-c. Por sua vez, outro estudo não encontrou diferença estatística em relação ao perfil lipídico (CT, TG, HDL-c e LDL-c) entre os participantes com TCA em eutireoidismo e grupo controle, mas demonstraram que concentrações de hormônios tireoidianos correlacionaram positivamente com CT, TG, LDL-c e HOMA-IR, concluindo que pacientes com TCA apresentam risco aumentado de desenvolver desordens no metabolismo de lipídeos01.
Além disso, no GC1 houve correlação positiva entre as variáveis antropométricas com o perfil lipídico, à exceção da variável HDL-c. E correlações positivas e significantes, além de esperadas, entre algumas variáveis do perfil lipídico e do perfil glicêmico, sugerindo que a RI está fortemente relacionada a um perfil lipídico desfavorável. Com produção excessiva de ácidos graxos pelo fígado, há redução da sensibilidade à insulina no tecido muscular, produção de interleucinas, fatores de crescimento e outras citosinas pelo tecido adiposo, podendo haver também hiperinsulinemia que aumenta a reabsorção de sódio e a atividade do sistema simpático. As concentrações de TG e HDL-C apresentam uma boa capacidade em identificar a RI na prática clínica, visto que se correlacionaram fortemente29. Na análise entre perfil glicêmico e perfil lipídico no GC2, também foram observadas algumas correlações significativas, portanto mesmo a análise dos grupos comparativos sugere um espectro de correlações ao longo do tempo, pois os dois grupos diferem basicamente na idade e no status hormonal.
No G1, encontrou-se correlação significante e negativa entre HbA1c e HDL-c, e entre HOMA-IR e HDL-c, e correlações positivas entre ácido úrico e TG e entre T4L e TG. É esperada a associação entre resistência insulínica expressa por HOMA-IR alterado e anormalidades da HbA1c e também com concentrações mais baixas de HDL-c. Além disso, tem sido descrita a interferência dos hormônios tireoidianos na metabolização dos lipídeos, mas a correlação positiva encontrada entre T4L e TG não faz nenhum sentido. E, ao se correlacionar perfil metabólico com perfil lipídico no G2, observou-se correlação inversa entre HbA1c e CT e entre insulina, HOMA-IR, ácido úrico com HDL-c, indicando que alterações metabólicas e lipídicas apresentam associações no contexto anteriormente referido.
As concentrações elevadas de CT e de LDL-c e baixas taxas de HDL-c exercem papel relevante na gênese da aterosclerose e doença cardiovascular30. Estudo sugere que a dislipidemia secundária ao hipotireoidismo é reversível com o tratamento, mas o hipotireoidismo subclínico é um fator de risco a ser considerado20, e a presente pesquisa sugere que inúmeros outros fatores persistem mesmo na TCA compensada.
Ao se analisar fatores de risco cardiometabólicos, 72% das pacientes do G1 apresentam 1 ou mais fatores de risco, e 36% apresentaram critérios para síndrome metabólica. No grupo comparativo (GC1), a maioria das participantes estiveram normais ou apresentaram apenas 1 fator de risco (44%). Com relação ao G2, 90,3% das pacientes apresentam 1 ou mais fatores de risco, e 51,6% têm síndrome metabólica. No GC2, a maioria das participantes não apresentaram nenhum fator de risco (42,9%) ou apresentaram apenas 1 (42,9%), enquanto apenas 14,3% preencheram critérios para síndrome metabólica. Portanto, entre pacientes com TCA os fatores de risco se somam com idade e climatério, somando-se em critérios para diagnóstico de SM. Em estudo feito em mulheres na pós-menopausa a prevalência de SM também foi mais elevada em pacientes com autoimunidade tireoidiana11. Na pesquisa aqui apresentada, o grupo G2 superou o GC2, indicando a interferência da TCA, além da idade e climatério.
Estudo demonstrou que níveis mais elevados de TSH podem predizer a SM06, entretanto outros trabalhos observaram SM tanto em mulheres com TCA eutireoideanas (47%) quanto em mulheres com hipotireoidismo subclínico (49%), ou seja, independente das concentrações de TSH11. Por outro lado, encontrou associação entre obesidade, CA, relação cintura-quadril, pressão arterial sistólica e índice HOMA-IR em pacientes com concentrações de anticorpos anti-tireoide, sugerindo envolvimento de fatores autoimunes tireoidianos que apresentam algumas características comuns com a condição de inflamação de baixo grau encontrada no sobrepeso/obesidade e que resultam em RI e pré-diabetes, fases evolutivas que podem ou não progredir para DM ou doença cardiovascular.
CONCLUSÃO
Os resultados do perfil metabólico sugerem a presença da resistência insulínica em ambos os grupos, sendo o G1, G2 e GC2 com taxas mais elevadas, porém se a mesma se deve à TCA ou à obesidade, o desenho do estudo não permitiu concluir. Para tal, um estudo futuro deverá selecionar pacientes com TCA e comparativos com IMC normal.
No perfil lipídico, em ambos os grupos afetados os resultados foram mais desfavoráveis em relação aos seus grupos comparativos. A TCA é um fator de risco independente para aterosclerose, deve-se ter atenção especial com as concentrações de colesterol, frações lipídicas e triglicerídeos ao acompanhar essas pacientes.
Os critérios de inclusão e a regularidade de tratamento limitaram o número de pessoas selecionadas, porém acredita-se que as informações coletadas serão fundamentais para direcionar as condutas de atendimentos ambulatoriais de pacientes que apresentam o diagnóstico de TCA, com atenção dirigida não somente ao aspecto da reposição hormonal com hormônios tireoidianos, mas também na abordagem terapêutica de cada um desses fatores de risco cardiovascular, que podem ser quantificados em nível ambulatorial.
REFERÊNCIAS
1. Lei Y, Yang J, Li H, Zhong H, Wan Q. Changes in glucose‐lipid metabolism, insulin resistance, and inflammatory factors in patients with autoimmune thyroid disease. J Clin Lab Anal. [Internet]. 2019 [citado em 13 jan 2020]; 33(7):e22929. DOI: https://doi.org/10.1002/jcla.22929
2. Moreira JN. Estudo dos fatores de risco cardiometabólicos em mulheres com tireoidite crônica autoimune. [dissertação]. Uberaba, MG: Universidade Federal do Triângulo Mineiro/UFTM; 2017. 94p.
3. Antonelli A, Ferrari SMF, Corrado A, Di-DomenicantoniO A, Fallahi P. Autoimmune thyroid disorders. Autoimmun Rev. [Internet]. 2015 [citado em 13 jan 2020]; 14(2):174-80. Disponível em: https://core.ac.uk/download/pdf/80258257.pdf
4. Jabrocka-Hybel A, Skalniak A, Piatkowski J, Turek-JabrockA R, Vyhouskaya P, Ludwig-SlomczyskA A, et al. How much of the predisposition to Hashimoto's thyroiditis can be explained based on previously reported associations? J Endocrinol Invest. [Internet]. 2018 [citado em 13 jan 2020]; 41(12):1409-16. Disponível em: https://link.springer.com/article/10.1007/s40618-018-0910-4
5. Merril SJ, Minucci SB. Chapter six- Thyroid autoimmunity: an interplay of factors. Vitam Horm [Internet]. 2018 [citado em 02 fev 2020]; 106:129-45. DOI: https://doi.org/10.1016/bs.vh.2017.07.001
6. Delitala AP, Scuteri A, Fiorillo E, Lakatta EG, Schlessinger D, Cucca F. Role of adipokines in the association between thyroid hormone and components of the metabolic syndrome. J Clin Med. [Internet]. 2019 [citado em 15 mar 2020]; 8(6):764-74. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6617115/
7. Vieira EC, Peixoto MRG, Silveira EA. Prevalência e fatores associados à síndrome metabólica em idosos usuários do Sistema Único de Saúde. Rev Bras Epidemiol. [Internet]. 2014 [citado em 10 jun 2020]; 17(4):805-17. DOI: http://dx.doi.org/10.1590/1809-4503201400040001
8. Phing CH, Saad HA, Yusof BNM, Taib N. Effectiveness of physical activity intervention among government employees with metabolic syndrome. J Exerc Sci Fit. [Internet]. 2017 [citado em 15 mar 2020]; 15(2):55-62. Disponível em: https://www.sciencedirect.com/science/article/pii/S1728869X17300886?via%3Dihub
9. Pereira DCL, Lima SMRR. Prevalência e sobrepeso e obesidade em mulheres após a menopausa. Arq Med Hosp Fac Ciênc Med Santa Casa São Paulo [Internet]. 2015 [citado em 05 fev 2020]; 60:1-6. Disponível em http://arquivosmedicos.fcmsantacasasp.edu.br/index.php/AMSCSP/article/view/158/168
10. Karakose M, KarbeK B, Sahin M, Arslan MS, TopaloglU O, Erden G, et al. The association of autoimmune thyroiditis and non-functional adrenal incidentalomas with insulin resistance. Arch Endocrinol Metab. [Internet]. 2015 [citado em 15 jan 2020]; 59(1):42-6. Disponível em: https://www.scielo.br/scielo.php?pid=S2359-39972015000100042&script=sci_arttext
11. Sieminska L, Woojciechowska C, Walczak K, Borowski A, Marek B, Nowak M, et al. Associations between metabolic syndrome, serum thyrotropin, and thyroid antibodies status in postmenopausal women, and the role of interleukin-6. Endokrynol Pol. [Internet]. 2015 [citado em 16 jun 2020]; 66(5):394-403. Disponível em: https://journals.viamedica.pl/endokrynologia_polska/article/view/EP.2015.0049/29962
12. Sociedade Brasileira de Cardiologia. 7ª Diretriz Brasileira de Hipertensão Arterial. Arq Bras Cardiol. [Internet]. 2016 [citado em 01 out 2021]; 107(Supl3):1-83. Disponível em: http://publicacoes.cardiol.br/2014/diretrizes/2016/05_HIPERTENSAO_ARTERIAL.pdf
13. Sociedade Brasileira de Diabetes. Diretrizes da Sociedade Brasileira de Diabetes. São Paulo: Clannad; 2019-2020. 491p.
14. International DiabeteS Federation. The IDF consensus worldwide definition of metabolic syndrome [Internet]. Brussels, Belgium: IDF; 2006 [citado em 01 out 2021]. 24p. Disponível em: https://www.idf.org/e-library/consensus-statements/60-idfconsensus-worldwide-definitionof-the-metabolic-syndrome.html
15. Sociedade Brasileira de Cardiologia. Atualização da V Diretriz Brasileira de Dislipidemias e Prevenção da Aterosclerose. Arq Bras Cardiol. [Internet]. 2017 [citado em 01 out 2021]; 109(2 Supl1):1-76. Disponível em: http://publicacoes.cardiol.br/2014/diretrizes/2017/02_DIRETRIZ_DE_DISLIPIDEMIAS.pdf
16. Martins-Silva T, Vaz JS, Mola CL, Assunção MCF, Tovo-Rodrigues L. Prevalência de obesidade em zonas rurais e urbanas no Brasil: Pesquisa Nacional de Saúde, 2013. Rev Bras Epidemiol. [Internet]. 2019 [citado em 13 jan 2020]; 22:E190049. DOI: https://doi.org/10.1590/1980-549720190049
17. Marques DSM, Siqueira HGR, Cruz MA, Vieira MSV, Apolônio RSPT, Esteves AVS. A relação entre pré-eclâmpsia e obesidade: uma revisão integrativa. Rev Cad Med UNIFESO [Internet]. 2019 [citado em 13 jun 2020]; 2(2):56-61. Disponível em: http://www.revista.unifeso.edu.br/index.php/cadernosdemedicinaunifeso/article/view/1394/608
18. Biyikli HH, Arduc A, Isik S, Azuguz U, Caner S, Dogru F, et al. Assessing the relationship between serum ghrelin levels and metabolic parameters and autoimmunity in patients with euthyroid Hashimoto’s thyroiditis. Endocr Pract. [Internet]. 2014 [citado em 29 jan 2020]; 20(8):818-24. DOI: https://doi.org/10.4158/EP13469.OR
19. Nie X, Xu Y, Ma X, Shen Y, Wang Y, Bao Y. Trunk fat and leg fat in relation to free triiodothyronine in euthyroid postmenopausal women. Endoc Conect.[Internet]. 2019 [citado em 29 jan 2020]; 8(10):1425-32. Disponível em: https://ec.bioscientifica.com/view/journals/ec/8/10/EC-19-0394.xml
20. Mullur R, Liu YY, Brent GA. Thyroid hormone regulation of metabolism. Physiol Rev. [Internet]. 2014 [citado em 15 jan 2020]; 94(2):355-82. Disponível em: https://journals.physiology.org/doi/full/10.1152/physrev.00030.2013?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org
21. Wan XM, Zhang M, Zhang P, Xie ZS, Xu FG, Zhou P, et. al. Jiawei Erzhiwan improves menopausal metabolic syndrome by enhancing insulin secretion in pancreatic β cells. Chin. J Nat Med. [Internet]. 2016 [citado em 02 mar 2020]; 14(11):823-34. DOI: https://doi.org/10.1016/S1875-5364(16)30099-1
22. Santos ML, Martiniano SREG, Tavares RE. Avaliação de circunferência abdominal, razão cintura/quadril e IMC em adultos saudáveis. Rev Campo Saber [Internet]. 2017 [citado em 05 jan 2020]; 3(3):14. Disponível em: https://periodicos.iesp.edu.br/index.php/campodosaber/article/view/100/81
23. Fonseca EJNC. Síndrome metabólica e resistência insulínica pelo HOMA-IR no climatério. Int J Cardiovasc. [Internet]. 2018 [citado em 15 jan 2020]; 31(3):201-8. Disponível em: https://www.scielo.br/pdf/ijcs/v31n3/pt_2359-4802-ijcs-31-03-0201.pdf
24. Chen Y, Chunfang Z, Yingchao C, Ningjian W, Quin L, Bing H, et al. Are thyroid autoimmune diseases associated with cardiometabolic risks in a population with normal thyroid-stimulating hormone? Mediat Inflamm. [Internet]. 2018 [citado em 13 nov 2020]; 2018:1856137. DOI: https://doi.org/10.1155/2018/1856137
25. Asghar A, Sheikh N. Role of immune cells in obesity induced low grade inflammation and insulin resistance. Cell Immunol. [Internet]. 2017 [citado em 03 mar 2020]; 315:18-26. DOI: https://doi.org/10.1016/j.cellimm.2017.03.001
26. Park YM, ZhanG J, Steck SE, Fung TT, Hazlett LJ, Han K, et al. Obesity mediates the association between mediterranean diet consumption and insulin resistance and inflammation in US adults. J Nutr. [Internet]. 2017 [citado em 15 jan 2020]; 147(4):563-71. Disponível em: https://academic.oup.com/jn/article/147/4/563/4584819
27. Deon RG, Rosa RD, Zanardo VPS, Closs VE, Schwanke CHA. Consumo de alimentos dos grupos que compõem a pirâmide alimentar americana por idosos brasileiros: uma revisão. Ciênc Saúde [Internet]. 2015 [citado em 15 jun 2020]; 8(1):26-34. DOI: https://doi.org/10.15448/1983-652X.2015.1.18065
28. Yetkin DO, Dogantekin, B. The lipid parameters and lipoprotein(a) excess in Hashimoto Thyroiditis. Int J Endocrinol. [Internet]. 2015 [citado em 02 fev 2020]; 2015:952729. DOI: https://doi.org/10.1155/2015/952729
29. Pereira, R. A relação entre dislipidemia e diabetes mellitus tipo 2. Cad UniFOA [Internet]. 2011 [citado em 15 jan 2020]; 6(17):89-94. Disponível em: http://revistas.unifoa.edu.br/index.php/cadernos/article/view/1087/938
30. Schiavo M, Lunardelli A, Oliveira JR. Influência da dieta na concentração sérica de triglicerídeos. J Bras Patol Med Lab. [Internet]. 2003 [citado em 06 fev 2020]; 39(4):283-8. DOI: https://doi.org/10.1590/S1676-24442003000400004
Notas de autor
