Artículos
Espectro Alimentario de la lagartija Sceloporus internasalis (Reptilia: Phrynosomatidae) del Bastonal, Sierra de Santa Martha, Los Tuxtlas, Veracruz
Espectro Alimentario de la lagartija Sceloporus internasalis (Reptilia: Phrynosomatidae) del Bastonal, Sierra de Santa Martha, Los Tuxtlas, Veracruz
Revista de Zoología, núm. 27, pp. 17-37, 2016
Universidad Nacional Autónoma de México
Resumen: Se determinó el espectro alimentario de la lagartija Sceloporus internasalis; (Reptilia: Sauria; Phrynosomatidae), en el poblado del Bastonal, Sierra de Santa Martha, Los Tuxtlas, Veracruz. De 56 organismos hallados 26 son Machos, divididos en (14 Adultos, 7 Juveniles y 5 Crías), y 30 Hembras con (13 Adultos, 11 Juveniles y 6 Crías). De cada ejemplar se determinaron presas consumidas, a nivel de Clase, Orden y Familia. Con los datos obtenidos se calculó Valor de importancia Alimentaría, Diversidad y Similitud. Los organismos revisados presentaron tres Clases–Presa: Insecta, con 95.1%; Aranae 3.8%, y la Clase: Isopoda, con 1.1%. De 11 Ordenes–Presa 55.3% corresponden a Hymenóptera (adultos), 20.89% a Coleóptera (Adultos), y 11.37% son Orthoptera (Adultos). Se registraron 20 Familias–Presa, destacando Formicidae con 50.9%; Coccinelidae con 10.8% y Blattidae con 8.1%. Los resultados nos permiten ubicar a Sceloporus internasalis como generalista y oportunista, con semejanzas en las presas consumidas por adultos, juveniles y crías, tanto en machos como en hembras.
Palabras clave: Alimento, Sceloporus internasalis.
Abstract: The food spectrum of the lizard Sceloporus interansalis was determined; (Reptilia: Sauria; Phrynosomatidae), in the village of Bastonal, Sierra de Santa Martha, Los Tuxtlas, Veracruz. Of the 56 organisms found, 26 are males, divided into (14 adults, 7 juveniles and 5 young), and 30 females with (13 adults, 11 juveniles and 6 offspring). From each specimen were determined dams consumed, at Class, Order and Family level. With the data obtained, it was calculated Food Import Value, Diversity and Similarity. The reviewed organisms presented three Classes-Presa: Insecta, with 95.1%; Aranae 3.8%, and Class: Isopoda, with 1.1%. Of 11 Order-Presa 55.3% correspond to Hymenoptera (adults), 20.89% to Coleoptera (Adults), and 11.37% are Orthoptera (Adults). There were 20 Families-Presa, with Formicidae standing out with 50.9%; Coccinelidae with 10.8% and Blattidae with 8.1%. The results allow us to locate S. internasalis as generalist and opportunist, with similarities in the prey consumed by adults, juveniles and offspring, in both males and females.
Keywords: Food, Sceloporus internasalis.
INTRODUCCIÓN
Dada la riqueza biológica que presenta nuestro país, el estudio de la fauna silvestre mexicana ha resultado de gran interés, como se demuestra con infinidad de trabajos enfocados hacia diferentes puntos de la zoología. Sin embargo, es claro que estos estudios han determinado áreas de interés hacia ciertos grupos. De esta manera, el entendimiento de cada uno de ellos es cada vez mas especifico y profundo; Así podemos observar que el conocimiento que se tiene de la herpetofauna se ha incrementado considerablemente, México, como se sabe posee flora y fauna muy variada con respecto al mundo, la cual es consecuencia del efecto combinado de variaciones en topografía y clima encontrados en su superficie (Flores y Gerez, 1994).
Con la biodiversidad existente en nuestro país, es necesario entender las relaciones entre los organismos y el medio, pues son la base principal de la ecología y un paso primordial para el manejo de los ecosistemas. Por lo que la realización de estudios enfocados a conocer los recursos bióticos que existen dentro de un ecosistema y sus interacciones es esencial para una mejor protección y aprovechamiento de los recursos naturales. En la actualidad la evaluación de los recursos y sus estudios ecológicos son de suma importancia, y estos han sido abordados principalmente mediante el estudio de tópicos como diversidad y biogeografía, por mencionar algunos, pero realmente se conoce muy poco sobre alimentación de nuestras especies faunísticas, tal es el caso de los saurios, tales como Sceloporus internasalis, y al igual que muchas otras especies es necesaria la realización de trabajos más profundos y completos con respecto al tema mencionado. Entre de los trabajos que contemplan dicho temas relacionados se encuentran Barbault, et al. (1978); García, (1989); Greene (1982); Gutiérrez y Sánchez (1986); Ramos (1982); De la Cruz et al. (1988); Whitfort y Bryant (1979); Gadsden y Palacios (2000); Altamirano y Soriano (2003); entre otros.
Ubicación y características del área de estudio.
El área de estudio se encuentra en la región de “Los Tuxtlas”, específicamente en las estribaciones de las montañas de Santa Martha, a 11 Km Aproximadamente, el área esta enclavada en la vertiente del Golfo de México; al Sureste del estado de Veracruz. Su situación geográfica se localiza entre los 10º 24´ Latitud Norte y a los 94º 56´ Longitud Oeste.
Figura (1)
Localización del área de estudio, Sierra de Santa Martha, Los Tuxtlas, Veracruz.
METODOLOGIA
Los muestreos mensuales con duración de 5 días, se realizaron a lo largo de un ciclo anual de abril de 2015 a mayo de 2016. Los ejemplares se capturaron con la mano (Gaviño, 1977 y Knudsen, 1966). Todos los organismos se enumeraron, con una etiqueta, y se tomaron los siguientes datos: hora de colecta a la que se observó la lagartija, temperatura corporal, temperatura ambiental, temperatura del microhábitat donde se encontró, humedad ambiental, sexo y edad. Cada organismo se designó de la siguiente manera; macho adulto (M.A.); macho juvenil (M.J.); cría de macho (M.C.); hembra adulta (H.A.); hembra juvenil (H.J.); cría de hembra (H.C.).
El tipo de substrato utilizado por cada ejemplar también se considero de la siguiente forma:

Tipo se sustrato donde se encuentra posada la lagartija
Una vez tomados los datos anteriores, se determinaron las siguientes medidas;
Longitud hocico- cloaca; Longitud de la cola; Longitud total y Ancho de la cabeza, los ejemplares se fijaron con formol amortiguado al 10%, y se transportaron en frascos de plástico totalmente herméticos, al Museo de Las Ciencias Biológicas “Enrique Beltrán” de la FES Iztacala UNAM. Para efectuar el análisis del contenido estomacal de los organismos, se procedió a la disección de las lagartijas, con el fin de extraerles el estomago, el cual se peso con todo el contenido estomacal, en una balanza analítica y posteriormente se pasó el estómago a una probeta de 10 ml. (0.1 ml.) (Pianka, 1975), con un volumen conocido de agua. Para obtener el volumen del contenido estomacal se extrajo el contenido estomacal y se colocó en un frasco vial debidamente etiquetado, con los datos de colecta, para su posterior análisis. El estómago vació se colocó en la probeta con un volumen conocido de agua y con la diferencia de las dos medidas de volumen desplazado, se obtuvo el volumen del contenido estomacal. A continuación, se secó el estómago vacío, con papel absorbente y se pesó en la balanza analítica. Las muestras de los contenidos estomacales, se colocaron en una caja petri y se analizaron con el auxilio de un microscopio estereoscopio Karl Zeiss para la separación y conteo de las presas ingeridas por las lagartijas, para establecer la proporción de cada tipo de alimento en porcentaje y fueron identificadas mediante claves específicas de insectos (Ross, 1982 y Ross et al., 1982), Leahy, C. (1998) hasta la categoría taxonómica de género.
Una vez identificadas las presas consumidas, se determino dureza, utilizando cuatro categorías, que se establecieron arbitrariamente, dependiendo de la consistencia de la presa, como se muestra a continuación: MB = Muy blando; B = blando; Med = medio duro y D = duro.
También se determinó el estado de desarrollo de las presas como sigue: H = huevo; L = larva; P = pupa; N = ninfa y A = adulto.
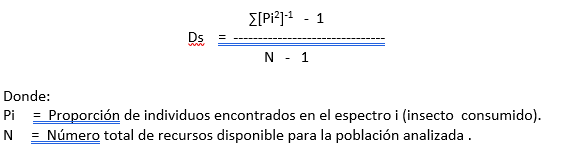
Con la información registrada se obtuvieron tres parámetros básicos para el estudio alimentario, para cuantificar la importancia de cada familia–presa en la dieta del organismo, para ello se utilizó el índice de Valor de Importancia, el cual suma tres valores (volumen, peso y frecuencia) para cada presa y define la importancia de un elemento alimenticio en la dieta de un organismo (Acosta, 1982) y se obtiene con la siguiente formula:

Los valores obtenidos de este índice varían de 0 a 3, y fueron utilizados para determinar y graficar los elementos fundamentales. Considerando como importantes en la dieta aquellos que presentaron valores arriba de 0.1 (Acosta idem).
Amplitud del recurso alimento.
Sobreposicion trófica: para determinar si existe un grado de sobreposicion trofica entre las categorías machos y hembras, machos y juveniles, hembras y juveniles.
Para estimar la magnitud de aprovechamiento de los recursos en la localidad, se calculó Amplitud de Nicho de cada una de las dimensiones consideradas de acuerdo al Índice de Diversidad de Simpson en forma estandarizada (Levins; 1968), teniendo a 0 como especialización extrema y a 1 para las generalistas.
Para el solapamiento de nichos entre sexos y clase de edad se utilizó el índice propuesto por Pianka (1973), teniendo a 0 para las poblaciones que no se solapan y a 1 para las poblaciones con un 100% de solapamiento.
Sobreposicion trófica: para determinar si existe un grado de sobreposicion trofica entre las categorías machos y hembras, machos y juveniles, hembras y juveniles.

Para la comparación de las fluctuaciones de la diversidad específica en la relación con las temperaturas y humedad, se utilizó el índice de Diversidad de Shannon y Weaver (Brower y Zar, 1981), para evaluar la diversidad de las especies que constituyen la dieta.

RESULTADOS
Se revisaron un total de 56 organismos, de los cuales se separaron en Machos y Hembras, con sus categorías de edad como se muestra en la tabla 1.
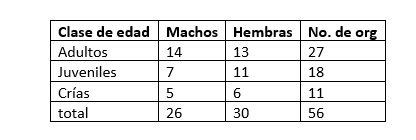
Tabla 1:
Organismos revisados de Sceloporus internasalis por edad y sexo.
A cada organismo se le tomó como medida morfométrica longitud hocico cloaca (LHC) para cada sexo y edad (tabla, 2).
También se obtuvieron las medidas del ancho del hocico y peso, determinando promedio por sexo y edad (tabla 3).
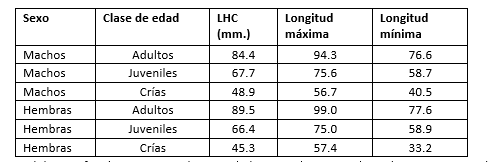
Tabla 2
Medidas morfométricas, promedio por edad para ambos sexos de Sceloporus internasalis.
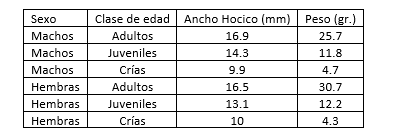
Tabla 3
Promedios de medidas del hocico y peso, por sexo y edad.
Los datos obtenidos de los organismos colectados, total, por sexo y edad se muestran en la tabla 4 (fig. 2, 3 y 4), mostrando el comportamiento de la captura de S. internasalis.
Los microhabitats que exploran los organismos de S. internasalis, se observan en la tabla 5, mostrando el número de organismos que explotan cada tipo de nicrohabitats, así como el total de organismos. De acuerdo a estos datos el aprovechamiento que la especie tiene, se refleja en los valores de de amplitud de nicho espacial, el cual fue bajo de 0.54, utilizando 4 microhabitats con un total de 227 individuos.
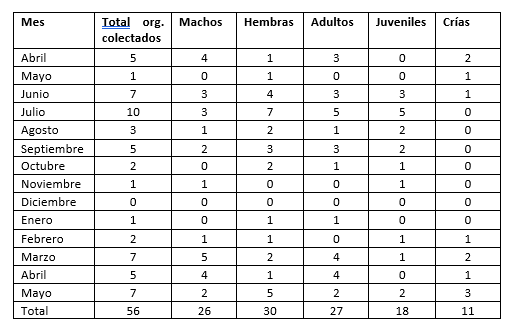
Tabla 4
Total de organismos revisados, por sexo y edad durante el periodo de estudio.
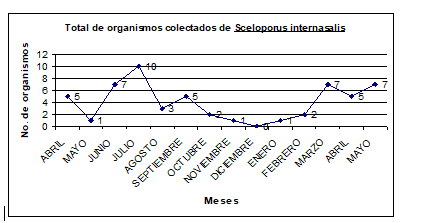
Figura 2
Total de organismos revisados
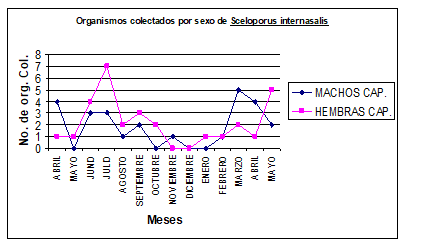
Figura 3
Total de organismos capturados por sexo
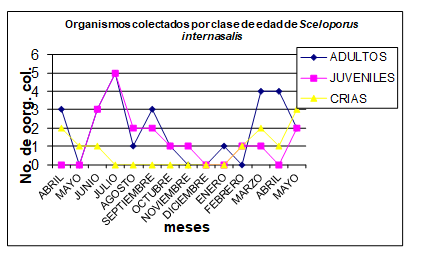
Figura 4.
Organismos encontrados por clase de edad.
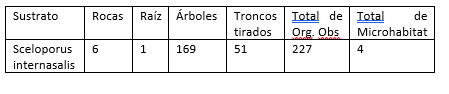
Tabla 5.
Sustratos utilizados por S. internasalis.
En cuanto a la alimentación, se registraron 11 tipos de orden–presa, consumidos por machos y hembras, como se muestra en la tabla 6.
Con base al alimento que utiliza S. internasalis, se pudo establecer cuantitativamente las preferencias que esta especie tiene, en Machos y Hembras. Observando que los valores más altos son del orden Hymenóptera, en Machos con 0.5529 y en Hembras con 0.3195. En lo que se refiere a los valores de amplitud del recurso temporal relacionado con las horas del dia, en su frecuencia de aparición se registro un valor de Ds = 0.60, teniendo 12 periodos a lo largo del dia, y un total de 227 organismos observados, comenzando las frecuencias temporales desde las 07:00 hrs hasta las 19:00 hrs. El tipo de alimento que consume S. internasalis, esta compuesta principalmente por tres clases de Artrópodos los cuales son: Clase Insecta; Clase Aranae y Clase Isopoda.
Para estas clases de alimento, se obtuvo la frecuencia de aparición en los contenidos estomacales del tipo de alimento, en la que los machos muestran a la clase Insecta con el porcentaje mas alto con 94.7%; siguiendo la clase Aranae con 3.4% y finalmente la clase Isopoda con 1.9%, mientras que para las hembras se obtuvo en primer lugar a la clase Insecta con 95.3%, seguido de Aranae con 4.2% y finalmente para la clase Isopoda con 0.5%. Los resultados muestran un total de 651 presas consumidas, en 56 contenidos estomacales, entre las tres Clases-Presas (tabla 7; fig. 5).
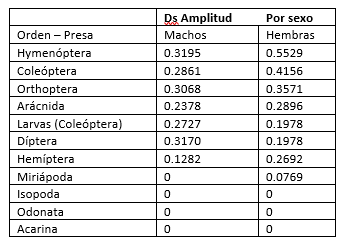
Tabla 6.
Ordenes-presa utilizados por machos y hembras de S. internasalis.
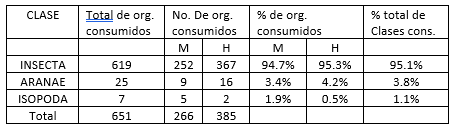
Tabla 7.
Porcentajes de las Clases – Presa consumidas por S. internasalis.
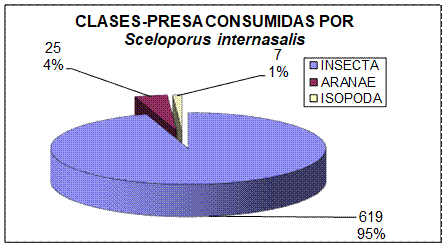
Figura 5.
Porcentaje Total de Clases – Presa consumidas por Sceloporus internasalis, con su respectivo porcentaje de importancia encontrados en los contenidos estomacales.
Para cada clase de alimento se obtuvieron los principales ordenes taxonómicos de organismos consumidos, por sexo de S. internasalis. Teniendo para la clase Insecta a seis Ordenes de importancia; a) Himenóptera, b) Coleoptera, c) Orthoptera, d) Díptera, e) Hemiptera y f) Odonata. Mientras que para la clase Aranae, solo se presentan dos Órdenes, Arácnida y Acarina, y para Isopodos con dos órdenes, Isopoda y Miriapoda. Se obtuvieron un total de diez ordenes–presa, consumidos por esta especie de lacertilio, considerándose a las larvas (coleópteros) como un orden.
Al igual que en las clases, a los ordenes–presa se obtuvo, la frecuencia de aparición de organismos encontrados en los contenidos estomacales, así como el porcentaje, tanto para las hembras como para los machos. Encontrando que el porcentaje más elevado corresponde a Hymenoptera con 51.8% para machos y 57.6% en hembras; siguiendo los Coleoptera con 22.5% en machos y 19.7% en hembras; Orthoptera con 12.4% en machos y 10.6% en hembras y con valores mas bajos tenemos a Miriapoda, Isopoda, Odonata y Acarina con 0.3% en hembras y 1.5%, 0.4%, 0 y 0 para machos respectivamente, (tabla 8; fig. 6).
Para cada orden se obtuvieron las familias–presa más importantes en la dieta de la especie estudiada, las cuales son: del orden Hymenoptera tres familias: Formicidae, Vespidae y Bombidae, en donde Formicidae, es la de mayor frecuencia de aparición en los contenidos estomacales, con 315 organismos consumidos, siguiendo Vespidae, con 33 y Bombidae con 12. Para Coleoptera se encontraron a seis familias–presa de importancia; Coccinelidae, Langurridae, Scarabeidae, Curculionidae, Chrysomelidae y Passalidae, en cuanto a frecuencia de aparición de los coleopteros, se registraron 20 larvas. Para el orden Orthoptera se encontraron tres familias–presa: Blattidae, Grillidae y Acrididae. Finalmente del orden Díptera se halló una sola familia, Pentatomidae y para Odonata la familia Coenagrionidae.
En la tabla 9 se muestran las diferentes familias–presa de importancia, en la dieta de S. internasalis pertenecientes a la clase Insecta, teniendo un total 16 familias–presa, considerando a las larvas de coleópteros como una familia–presa, teniendo un total de 619 presas consumidas, en 56 estómagos analizados.
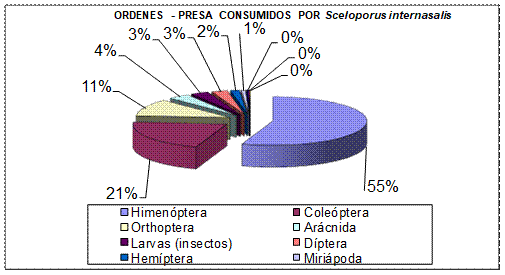
Figura 6.
Porcentaje Total de los Ordenes – Presas consumidas por Sceloporus internasalis.
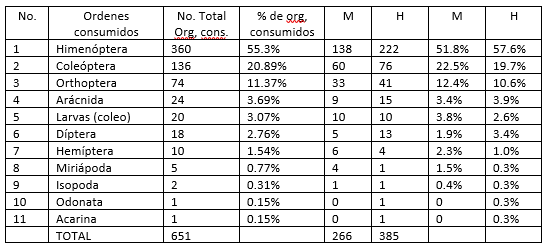
Tabla 8.
Frecuencia de aparición de Ordenes – Presa en los contenidos, así como su porcentaje, en ambos sexos.
En la figura 7 se observan los porcentajes de las familias-presa consumidas por S. internasalis y en la figura 11 se muestra el no. de organismos totales, por familia–presa pertenecientes a la clase Insecta.
Los hábitos alimentarios que presenta esta especie de lagartija en general, se puede determinar como insectívora, predominando, la Clase Insecta, con el orden Hymenóptera, con la familia Formicidae, siguiéndole las categorías con un valor alimentario menor.
Se determino el alimento de la especie por sexo, obteniéndose los siguientes resultados, para las familias–presas (Tabla 10).
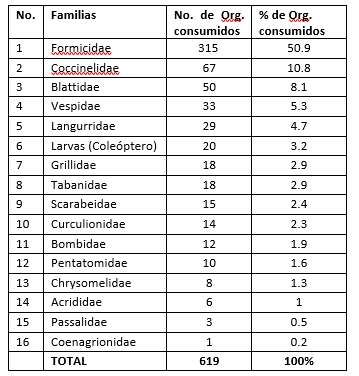
Tabla 9.
Familias–presa consumidas, por Sceloporus internasalis, con su frecuencia de aparición en los contenidos estomacales, así como su porcentaje, en importancia progresiva de la dieta. Pertenecientes a la clase Insecta.
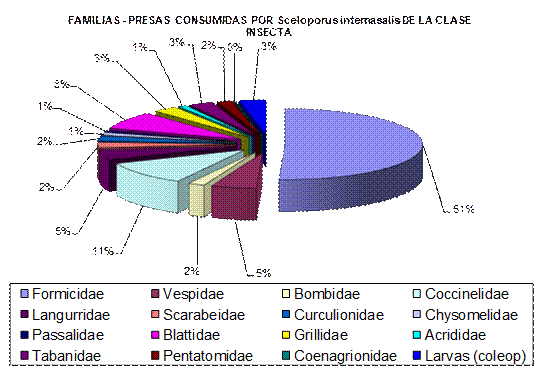
Figura 7.
Porcentaje Total de las familias–presas consumidas por S. internasalis, pertenecientes a la clase Insecta.
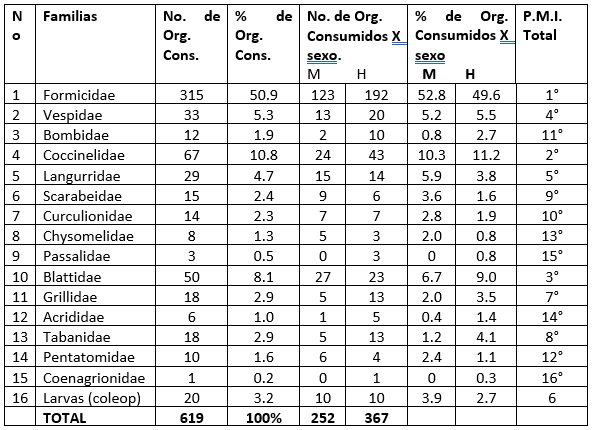
Tabla 10.
Familias–presas consumidas por sexo y su % de importancia en la dieta de Sceloporus internasalis.
Se obtuvo el número total de organismos consumidos, por cada familia–Presa, por sexo (machos y hembras, tabla 10). Además de su porcentaje. También podemos observar el comportamiento de la frecuencia de aparición de las familias consumidas (la figura 8). Para comprobar si existe alguna variación en el tipo de alimento entre sexos, se obtuvieron los datos por edad (tabla 11).
De igual forma se obtuvieron los datos de organismos consumidos correspondientes a las familias–presas (tabla 12). Las familias–presas consumidas por esta lagartija, que se obtuvieron en los contenidos estomacales, se clasificaron dependiendo de la edad, para comprobar si existe alguna preferencia alimentaría, entre adultos, juveniles crías (tablas 13 y 14).
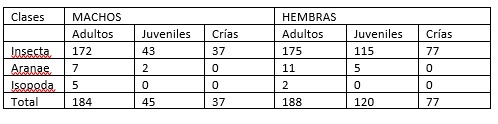
Tabla 11.
Frecuencia de presas consumidos por S. internasalis por sexo y edad.
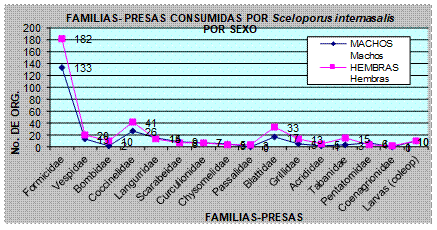
Figura 8.
Frecuencia de aparición de las familias – presa, en los contenidos estomacales de Sceloporus internasalis por sexo.
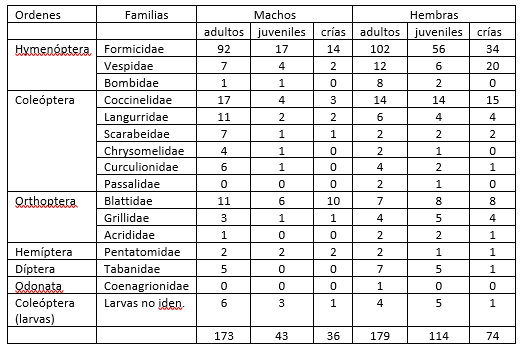
Tabla 12.
Frecuencia de organismos de las Familias–Presas, encontrados en los contenidos estomacales por edad de cada sexo, de la clase Insecta.
Se puede observar que esta especie alcanza su mayor frecuencia de aparición (fig. 10) durante las horas entre las 09:00 y 11:00 alcanzando una temperatura ambiental de 23 a 24° C. y con una humedad ambiental de 78 a 80% . A lo largo del día se presenta un comportamiento bimodal de máxima frecuencia de aparición, un pico de actividad se observa por la mañana y otro por la tarde de las 15:00 a las 16:00 horas. Cuando las condiciones ambientales son adecuadas y no cambian drásticamente. A medida que aumenta o disminuye la temperatura a lo largo del dia, esta especie baja su frecuencia de aparición y solo se le puede observar nuevamente cuando las condiciones climáticas sean las adecuadas para su actividad (fig. 9).
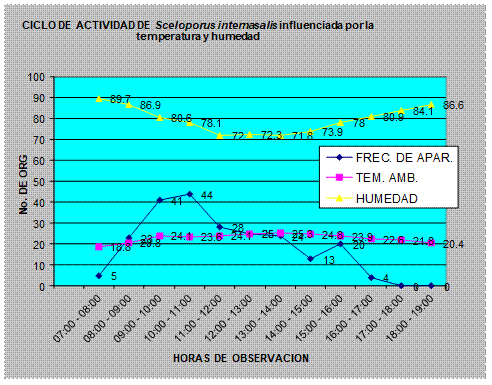
Figura 9.
Ciclo de actividad a lo largo del día por S. internasalis relacionando la temperatura y humedad
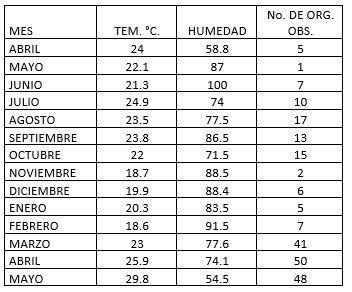
Tabla 13.
Frecuencia de aparición de S. internasalis por mes en relación a la temperatura y humedad.
DISCUSION y CONCLUSONES
Los resultados arrojados, nos indican que utiliza los estratos arbóreos para obtener su alimento, además muestra una especialización muy marcada, en el tipo de sustrato que aprovecha para obtener a sus presas, así como para desarrollar sus actividades diarias. Ya que solo se les puede observar en árboles grandes y en árboles tirados, en los cuales, estas lagartijas realizan recorridos periódicos a lo ancho y largo de los troncos, en busca del recurso trófico, que consta principalmente de invertebrados, entre los cuales destacan los insectos. El tipo de estrategia o técnica que utiliza en la obtención del recurso utiliza principalmente el acecho combinado con forrajeo intensivo, aunque muestra el uso de presas en tiempos y espacios de máxima productividad. Para la detección de presas realiza recorridos verticales u horizontales, cuando localiza alguna se aproxima lentamente y hasta una distancia reducida se abalanza sobre ella, con movimientos rápidos, atrapándola mediante una mordida para sujetarla, y tragarla completamente, como ocurre, con la mayoría de los saurios, que no tienen capacidad de masticación. Esta especie utiliza las primeras horas del día para alimentarse, de las 09:00-11:00 hrs., con una temperatura ambiental que fluctúa de los 23° - 24.5°, dicha actividad dependerá de las condiciones ambientales, ya que en esta zona, las variaciones climáticas son muy frecuentes, imposibilitando a los organismos desempeñar sus actividades diarias, ocasionando que la especie permanezca resguardada en sus madrigueras u oquedades de los arboles, dificultando la observación y captura de las mismas y solo se pueden observar nuevamente, hasta que las condiciones ambientales son favorables.
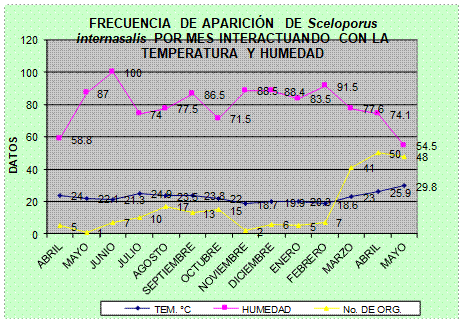
Figura 10.
Frecuencia de aparición de S. internasalis relacionada con la temperatura y humedad.
S. internasalis presento una dieta principalmente insectívora, debido a que la clase Insecta presento el 94.7% en la dieta total consumida por la especie, de estos organismos, y el porcentaje restante lo complementa con otros dos grupos de artrópodos (Aranae 3.4% e Isopoda 1.9%). Los resultados de la abundancia muestran que los Hymenópteros (adultos, determinados hasta el nivel de Familia) predominaron en la dieta de machos y hembras, al igual que en las edades (adultos, juveniles y crías)..
Ballinger (1995), encontró que Xenosaurus grandis, en su alimentación se basa principalmente de larvas de Lepidópteros Gadsden y Palacios–Orona (2000) obtuvieron, que la dieta de Cnemidophorus tigris se conforma principalmente por larvas de Lepidópteros. Barbault y Maury (1981) reportan que C. tigris es un consumidor generalista, pero presenta preferencia por las termitas. De acuerdo a los índices de diversidad de S. internasalis, esta muestra ciertas semejanzas con las especies antes mencionadas, pues también existe una tendencia a ser generalista en el consumo de presas, ya que presenta una gama amplia de presas consumidas pero con preferencia por la familia Formicidae. En relación entre los sexos (machos y hembras), estos consumen el mismo tipo de presas en su alimentación, al igual que en las edades (adultos, juveniles y crías). Esto nos indica que S. internasalis aparentemente tiene preferencia por una presa en particular, a los Formícidos, sin destacar que aprovecha a otras de menor importancia. Esta selección por las hormigas desfoliadoras son el recurso que abundan en todo el año, por lo que esta especie la encuentra directamente en el sustrato (árboles) donde ella desarrolla sus actividades de hábitos alimentarios, por lo que aprovecha oportunamente un recurso disponible.
La temperatura y la humedad afectan directamente a la actividad diaria de esta especie, estos cambios del medio influyen en la dieta, debido a la forma en que afectan la abundancia y disponibilidad del recurso alimentario, Ortega y Hernández (1983), analizaron la influencia de estos cambios ambientales, en la abundancia de los recursos en la dieta de Sceloporus dugesi intermedius, observando que la disminución de la disponibilidad de Coleópteros, en ciertas partes del año, lleva a esta especie a tener que alimentarse de otras presas (artrópodos) para cubrir sus requerimientos energéticos, este comportamiento alimentario también se observa en S. internasalis, y por la amplia gama de presas detectadas en este trabajo es por lo que a esta especie de lagartija la catalogamos como generalista y oportunista en elaprovechamiento de los recursos alimentarios, de acuerdo al criterio de Barbault et.al., (1978); Ping y Barbault, (1986).
Espectro Alimentario de la lagartija Sceloporus internasalis (Reptilia: Phrynosomatidae) del Bastonal, Sierra de Santa Martha, Los Tuxtlas, Veracruz.
Altamirano, A. T., y M. Soriano. 2003. “Espectro alimenticio y desempeño ecológico de los anfibios y reptiles de Alvarado, Veracruz”. Rev. Zool. 14: 23-35.
Altamirano Alvarez, T. A., & Soriano Sarabia, M. (2007). Espectro alimentario de Aspidoscelis guttata (Reptilia: Teiidae). Revista de Zoología, (18).
Altamirano Álvarez, T. A., Pérez Sánchez, E., Soriano, M., García Bernal, A. D. J., & Miranda González, N. P. (2014). Determinación del espectro alimentario de la lagartija Sceloporus torquatus (Reptilia: Phrynosomatidae) a través de excretas. Revista de Zoología, (25).
Arnet, H. R. and L. R. Jacques. 1981. « Guide to Insect ». Pub. Simon and Shuster. New York. 512 p.
Arnet, R. H. Jr. 2000. “American Insects. A handbook of insects of American borth of Mexico.” CRC. Press LLC. Florida. 850 p.
Flores Villela, O., & Gerez, P. (1994). Biodiversidad y conservación en México: vertebrados, vegetación y uso del suelo (No. 575.2 F5 1994).
Avery, R. A. 1971. “Estimates of food consumption by the lizard Lacerta vivipara” Ecology. 40: 351-365.
Ballinger, R. E., Lemos-Espinal, J., Sanoja-Sarabia, S., & Coady, N. R. (1995). Ecological observations of the lizard, Xenosaurus grandis in Cuautlapán, Veracruz, México. Biotropica, 128-132.
Barbault, R. (1978). Principios y métodos de estudio de la organización de las comunidades (No. AS 50136; 333.950972 R433). Instituto de Ecología, México DF (México)..
Barbault, R. , A. Ortega y Maury M. E. 1985. “Food partitioning and community organitazion in a mountain lizard guiad of Northern Mexico”. Oecologia (Berlin) Springer- Verlag 65: 550-554.
Borror, J. D. and E. R. White. 1970. “A field guide to the insects of American North of Mexico”. Hougthon Wifflin Company Boston. 404 p.
Brower J. E. and J. H. Zar. 1981. “Field and laboratory methods for general ecology”. Wm. C. Brown Company Publishers. 827 p.
De la Cruz, F. R. M., Guillette Jr, L. J., Santa Cruz, M. V., & Casas-Andreu, G. (1988). Reproductive and fat body cycles of the viviparous lizard, Sceloporus mucronatus (Sauria: Iguanidae). Journal of Herpetology, 1-12.
Gadsden, H., & Palacios-Orona, L. (2000). Composición de dieta de Cnemidophorus tigirs marimoratus (Sauria: Teiidae) en dunas del centro del Desierto Chihuauhense. Acta zoológica mexicana, (79), 61-76.
Gaviño de la Torre, G. (1977). Técnicas biológicas selectas de laboratorios y de campo (No. 574.072 G38).
García, E. 1981. Modificaciones al sistema de clasificación cilmática de Copen. 3ª ed. Instituto de Geografía. U.N.A.M. 252 p.
García, C. R. 1989. Ciclo reproductivo y hábitos alimenticios de Sceloporus variabilis variabilis (Reptilia:Sauria:Iguanidae) en Alvarado, Veracruz. Tesis. Licenciatura. ENEP Iztacala. UNAM. 95 p.
Greene, H. W. 1982. Dietary and phenotypic diversity in lizards: why are some organisms specialized. En: Environmental adaptations and evolutions. D. Massakowski y G. Roth (eds). Gustav Fisher Stuttgart. N. Y.
Gutiérrez-Mayén, M. G. y Sánchez-Trejo, R. 1986. “Repartición de recursos alimenticios de la comunidad de lacertilios de Cahuacán, Estado de México”. Tesis Licenciatura. E.N.E.P. Iztacala. U.N.A.M. México. 177 p.
Knudsen,, JW 1966. Biological Techniques. Harper and Row. New York. 185 pp
Huey, R. B., & Pianka, E. R. (1981). Ecological consequences of foraging mode. Ecology, 62(4), 991-999.
Leahy, C. (1998). Peterson first guide to insects of North America. Houghton Mifflin Harcourt.
Levins, R. (1968). Evolution in changing environments: some theoretical explorations (No. 2). Princeton University Press.
Méndez, F. C. y S. M. Villagran.1983. “Contribución al conocimiento de la ecología y ciclo reproductor de la lagartija vivípara Sceloporus mucronatus mucronatus. Tesis Licenciatura. E.N.E.P. Iztacala. U.N.A.M. México. 78 p.
Méndez-de la Cruz, F. R., Casas-Andreu, G., & Cruz, M. V. S. (1992). Variación anual en la alimentación y condición física de Sceloporus mucronatus (Sauria: Iguanidae) en la sierra del Ajusco, Distrito Federal, México. The Southwestern Naturalist, 349-355.
Ortega, A. L. F. R. E. D. O., & Hernandez, L. (1983). Abundancia relativa de insectos en un medio estacional; su influencia en la historia de vida de dos iguanidos simpatricos. Folia Entomologica Mexicana, 55, 129-144.
Pianka, E. R. (1973). The structure of lizard communities. Annual review of ecology and systematics, 4(1), 53-74.
Ramos, A. R. 1982. “Aspects of the food resources of Coleodactylus amazonicus (Sauria:Gekkonidae)”. Acta Amazonica. 11(3): 511-526.
Ross, H. H., Ross, C. A. R., June, R. P., Charles, A. R., & June, R. P. (1982). A textbook of entomology (No. QL 463. R67 1982).
Ross, H. H.1982. “Introducción a la entomología eneral y aplicada”. Omega. Barcelona 536 p.
Whitford, W.E. y M. Bryant. 1979. “Behavior of a predator and its prey the horned lizard (Phrynosoma cornutum) and harvester ants (Pogonomyrmex sp.)”. Ecology. 60 (4): 686-694.