Aspectos de la reproducción, dieta y edad de la especie microendémica Sceloporus macdougalli Smith y Bumzahem, 1953 (Squamata: Phrynosomatidae), de Tehuantepec, Oaxaca.
Aspectos de la reproducción, dieta y edad de la especie microendémica Sceloporus macdougalli Smith y Bumzahem, 1953 (Squamata: Phrynosomatidae), de Tehuantepec, Oaxaca.
Revista de Zoología, núm. 30, pp. 1-22, 2019
Universidad Nacional Autónoma de México
Resumen: Se describen aspectos de la reproducción, dieta y la edad del lacertilio microendémico Sceloporus macdougalli utilizando datos de individuos recapturados y observados entre septiembre del 2002 y septiembre del 2003. La especie presenta un patrón reproductivo de tipo otoñal y sincrónico entre sexos, la preñez se desarrolla durante el invierno y primavera con duración de cuatro meses. El tamaño de la camada va de dos a cuatro crías, es el más pequeño registrado en el grupo Poinsettii, al que pertenece. No existe relación entre tamaño de camada, la talla y edad de la hembra. El lacertilio es carnívoro y oportunista, existe diferencia en la composición de la dieta entre sexos seguramente por el uso diferencial del microhábitat. Los individuos de la especie son longevos por alcanzar edades de hasta ocho años.
Palabras clave: Sceloporus macdougalli, reproducción, dieta, edad.
Abstract: It describes aspects of reproduction, food and age, of the restricted endemic lizard Sceloporus macdougalli using data from individuals captured and observed between 2002 and 2003. This specie shows fall reproductive activity, synchronous between sexes, pregnancy develops during the winter and spring with a duration of four months. Litter size of two to four young, it is the smallest registered in the Poinsettii group, to which it belongs. There is no relationship between litter, body size and age of the female. The lizard is carnivorous and opportunistic, there is a difference in the diet between sexes, probably due to the differential use of the microhabitat. The individuals of the species are long-lived to reach ages of up to eight years.
Keywords: Sceloporus macdougalli, reproduction, food, age.
INTRODUCCIÓN
El saurio Phrynosomatidae Sceloporus macdougalli Smith y Bumzahem, 1953 también llamada lagartija escamosa de MacDougall, pertenece al grupo Poinsettii (Wiens, et al., 2010), especie microendémica del Istmo de Tehuantepec en el Estado de Oaxaca (Smith y Bumzahem, 1953), habita la selva baja caducifolia, es vivípara y ocupa rocas megalíticas de difícil acceso. Desde el descubrimiento y descripción de la especie, no es hasta muy recientemente que se ha aportado información en algunos aspectos de su Biología, como la presencia de un marcado dicromatismo sexual (Mendoza-Quijano et al., 2002), la descripción de su cariotipo (Mendoza-Quijano y Goyenechea, 2004), aspectos de la Biología térmica y locomoción en hembras grávidas (López, 2005) y sobre su filogenia (Martínez-Méndez y Méndez-de la Cruz, 2007; Wiens, et al., 2010). En lo referente a su estado de conservación, S. macdougalli está catalogada como una especie bajo protección especial (Diario Oficial de la Federación, 2010). Ante la escaza información sobre la Biología de la especie, el objetivo del presente trabajo fue contribuir en el conocimiento de aspectos reproductivos, dieta y de la edad de Sceloporus macdougalli.
MATERIAL Y MÉTODOS
Área de estudio
La población del lacertilio se encuentra en las inmediaciones del poblado de Santa Cruz Bamba, Municipio de Tehuantepec, Oaxaca y a 12.8 km de la costa de la Bahía Bamba a 16° 0.25’ latitud norte y 95° 25’ longitud oeste, en una altitud de entre 100 y 300 m s.n.m. (INEGI, 1987). El clima corresponde al Aw0 (w) cálido subhúmedo con lluvias en verano (García, 1973), con precipitación del mes más seco menor de 60 mm y la primera con lluvia invernal menor a 5 mm y una temperatura promedio de 28.8°C, en cuanto a la humedad, presenta dos temporadas bien marcadas: la lluviosa y la seca con seis meses de estiaje (SPP, 1981; SMN, 2003). La vegetación predominante es el Bosque Tropical Bajo Caducifolio, entre las especies representativas se encuentran Acacia coulteri, Beaucarnea inermes, Bursera spp, Casimiroa pringlei, Cedrela mexicana, Chiococca alba, Leucaena pulverulenta, Guazuma ulmifolia, Lysiloma acapulcensis, L. divaricata, Phoebe tampicensis, Pithecellobium flexicaule, Sapindus saponaria, Thouinia villosa y Wimmeria concolor (Rzedowski, 1981; Puig, 1991).
a, que contenía cinco embriones en el estadio 34.5, así mismo, una hembra preñada del mes de mayo que fue encontrada muerta, contenía cinco embriones en el estadio 40 que corresponde al total desarrollo del embrión (Cuadro 2). Los cuerpos grasos están presentes durante la vitelogénesis, no siendo así durante la previtelogénesis y tampoco durante la preñez (Cuadro 2).
Con base en la condición de la
MÉTODOS
Debido a que es una especie endémica de distribución restringida, se decidió no sacrificar muchos animales para evitar daños a la población, ante la falta de información sobre su tamaño poblacional. Los datos se obtuvieron en muestreos bimensuales realizados de septiembre del 2002 a septiembre del 2003. La recaptura de los organismos se efectuó con una caña de pescar con un nudo corredizo. Se registro el sexo y se anotaron para cada uno de los organismos, la Longitud Hocico Cloaca (LHC), Ancho de Hocico (AH) y Largo Cola (LC) con un calibrador vernier, todas las medidas (± 0.1mm), y el peso total del organismo (PTO) con una pesola (± 0.2 gr) (Casas-Andreu et al., 1991).
Para los aspectos reproductivos se utilizaron ocho hembras, dos de ellas encontradas muertas y siete machos, los organismos fueron capturados, sacrificados y fijados con formaldehído al 10% en campo (Casas–Andreu et al., 1991). En el laboratorio, se extrajeron las gónadas y cuerpos grasos de ambos sexos y fueron pesados en una balanza analítica (± 0.0001 gr.); además, se midió el largo y ancho del testículo izquierdo para establecer el volumen testicular. El volumen testicular se determinó con la formula para el volumen de un elipsoide: V = 4/3 π a2 x b Donde: V = Volumen, π= 3.1416, a2 = ½ diámetro menor y b = ½ diámetro mayor (García, 1989; Ramírez, 2002). A los testículos se le aplico el procedimiento de histología convencional y tinción con Hematoxilina y Eosina (Humason, 1979) para identificar los componentes espermatogénicos y establecer dos condiciones reproductivas: a) actividad reproductiva espermatogénica, por la presencia de esperma maduro en túbulos seminíferos; b) inactividad reproductiva espermatogénica, ausencia de esperma. En hembras se determino la actividad reproductiva por la presencia de folículos vitelogénicos y/o preovulatorios o embriones. La inactividad reproductiva se determinó por la presencia de folículos previtelogénicos, de acuerdo con Ramírez-Bautista et al., (1995). En los embriones se identifico el estadio de desarrollo de acuerdo con las descripciones e ilustraciones de Defaure y Hubert (1961).
La talla mínima de madurez sexual en machos se estableció con la LHC del organismo más pequeño que evidenciaba espermatogénesis y un epidídimo largo y enroscado y externamente con los caracteres sexuales secundarios, en este caso los parches de color vivo del vientre (Ramírez-Bautista et al., 1995; Ramírez-Bautista y Vitt, 1997; Ramírez-Bautista et al., 1998). Mientras que en hembras se estableció con la mínima LHC del organismo, que presento vitelogénesis o embriones en desarrollo usando las hembras sacrificadas y otras 21 hembras que fueron capturadas, inspeccionadas visual y táctilmente, y posteriormente liberadas: esto también ayudo a establecer la temporalidad de la gestación.
El tamaño de la camada se estableció con el número de crías nacidas provenientes de nueve hembras preñadas, capturadas en marzo y mantenidas vivas en el laboratorio y con el conteo de embriones en desarrollo de dos hembras encontradas muertas, una en marzo y otra en mayo. Los valores medios de la LHC, LC, AH y peso (± 0.1) de las crías al momento del nacimiento, se obtuvo de las medidas de 40 crías nacidas en cautiverio y de seis crías capturadas y liberadas en el mes de mayo. Las hembras con sus crías fueron liberadas en su sitio de origen.
Para describir la dieta se analizaron los estómagos de ocho hembras y siete machos. Los artrópodos encontrados en los estómagos se identificaron al nivel taxonómico de familia, con claves especializadas (Daly et al., 1978; Triplehorn y Jonson, 2005) a cada categoría presa se le estimó el volumen por desplazamiento volumétrico. Para establecer la importancia de los componentes alimentarios, se utilizó el Valor de Importancia Alimentaría (VIA), para cada tipo de presa con la formula VIA = V’ij + F’ij + N’ij donde (V’ij) es el Volumen de cada tipo de presa con respecto al total de las presas; (F’ij ) es la Frecuencia Relativa o sea el numero de estómagos en los que se encontró cada tipo de presa y (N’ij) es la Abundancia Relativa o proporción del número de representantes del mismo tipo de presa con respecto al total (Acosta, 1982). Los valores del VIA cercanos al número uno representa dietas especializadas y cercanos a tres dietas generalistas. Para conocer la diferencia en la composición de la dieta entre sexos, se aplico un análisis de similitud (Sigma Stat Ver. 2.0)
Se estableció la edad de 31 organismos, siete machos y ocho hembras utilizados para el análisis de dieta y 16 organismos capturados y liberados. A cada individuo se le ectomizó una falange para aplicar la técnica modificada de Esqueletocronología, que consistió en preservar las falanges en alcohol al 70%, después descarnarlas y posteriormente desmineralización por 10 horas con ácido nítrico al 3%. Y deshidratadas en alcohol etílico al 70% hasta alcohol al 100%. Aclaradas en xilol e inclusión en parafina y fueron cortadas en secciones transversales de 15 mm de espesor con un micrótomo de rotación y teñidas durante cinco minutos con Hematoxylina de Harris. Las secciones cortadas fueron montadas en Entellan para su inspección al microscopio y contar los anillos hematoxylinofilicos, que sirvieron para determinar la edad de cada individuo (Castanet y Roche, 1981; Castanet et al., 1988; Castanet y De Buffrénil, 2000). Se utilizó la correlación de Pearson (Brunning y Kintz, 1977) para determinar la relación existente entre la LHC de cada individuo y su respectivo número de anillos hamatoxylinofílicos.
RESULTADOS
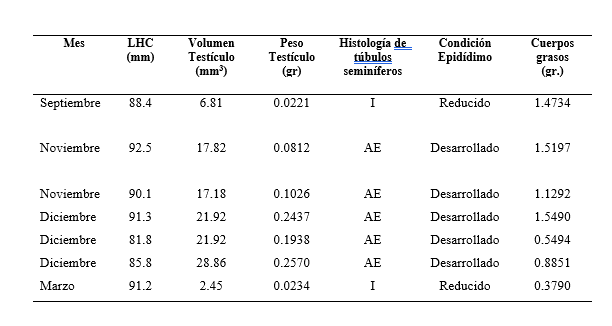
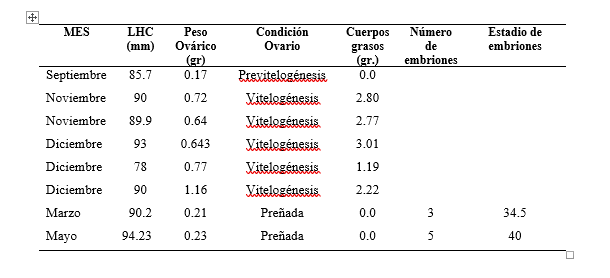
De acuerdo con la condición espermatogénica y la hipertrofia del epidídimo de siete machos, se presenta actividad reproductiva, en noviembre y diciembre, que corresponde al otoño (Cuadro 1). En el caso de las hembras igualmente se observó actividad reproductiva otoñal, evidenciado por el tamaño agrandado de la gónada y la actividad vitelogénica. En campo fue posible observar el apareamiento de tres parejas en el mes de diciembre; la gestación se desarrolla durante cinco meses, de diciembre a abril, porque los nacimientos se dan a finales de abril y principios de mayo. En el mes de marzo se encontró una hembra preñada, que contenía cinco embriones en el estadio 34.5, así mismo, una hembra preñada del mes de mayo que fue encontrada muerta, contenía cinco embriones en el estadio 40 que corresponde al total desarrollo del embrión (Cuadro 2). Los cuerpos grasos están presentes durante la vitelogénesis, no siendo así durante la previtelogénesis y tampoco durante la preñez (Cuadro 2).
Con base en la condición de la gónada, los machos tienen madurez sexual a la talla de 81.80 mm en intervalo de 81.80 a 92.5 mm de LHC (X= 88.82 ± 3.85; n= 7). Los caracteres sexuales secundarios de coloración se observan s a partir de los 72.0 mm en un intervalo de 72.0 a 100.9 mm en la LHC (X= 84.34 ± 8.63; n= 18). Las hembras maduran a partir de los 72.5 mm en el intervalo de 72.5 a 95.4 mm de LHC (X= 83.84 ± 6.92; n= 29).
El tamaño medio de la camada fue de 4 ± 1.33 crías, (intervalo 2 a 5 n= 11). No existe relación entre la LHC y PTO de la hembra y el número de crías (r= 0.03; n=11; p= 0.05; r= 0.25; p= 0.05; n= 11, respectivamente). Las crías nacen con una LHC promedio de 36.9 ± 2.0 mm (intervalo 30.6 a 39.6, n= 46), LC promedio de 44.8 ± 3.5 mm (intervalo 33 a 50, n= 46), AH de 8.7 ± 0.36 mm (intervalo 7.89 a 9.2, n= 46), PTO promedio de 1.8 ± 0.3 (intervalo 1.05 a 2.2, n= 46). Y la proporción de sexos en crías fue del 1:1.
La dieta de la especie estuvo constituida por 15 tipos de presas animales y un elemento vegetal de la familia Magnoliopsiae. La clase Insecta tuvo mayor importancia en la dieta, sobresalieron por el VIA los himenopteros de la familia Vespidae, Formicidae, Apoide y escarabajos Carabidae (Figura 1). Los machos consumieron 11 tipos de presa y las hembras 11. Entre sexos, se presentó un 52.2% de similitud en la composición de la dieta.
El análisis esqueletocronológico muestra que en la población se presentan de cero hasta ocho anillos hematoxylinofilicos, cada anillo corresponde a un año de edad, por la marcada estacionalidad climática anual que impera en el área de estudio (Fig. 2). Se observó una relación positiva y significativa entre la LHC y el número de anillos en ambos sexos (r= 0.82; p= 0.05; n= 31), igualmente en las hembras (r= 0.91; p= 0.05; n= 18) y machos (r= 0.86; p= 0.05; n= 14). No se encontró relación significativa entre el número de crías y el número de anillos en hembras (r= 0.44; p= 0.05; n= 17).
DISCUSIÓN
La especie Sceloporus macdougalli exhibe un patrón reproductivo de tipo otoñal y sincrónico entre sexos, la preñez se desarrolla durante cuatro meses, de diciembre a abril. Este patrón es similar al presentado por S. serrifer (Rivera, 2001) del mismo grupo Poinsettii, en un similar tipo de clima. El patrón reproductivo es similar al de las especies del grupo hermano Torquatus de zonas montañosas templadas (Ballinger, 1973; Guillette y Méndez del Cruz, 1993; Feria et al., 2001; Ramírez Bautista et al., 2002; Gadsden et al., 2005).
El tiempo de gestación de cuatro meses es relativamente corto, consecuencia de la temperatura alta que prevalece en su hábitat, que acelera el desarrollo embrionario (Shine, 1980), de similar manera sucede en S. serrifer (Rivera, 2001) con tres meses de duración, en clima calido, y en contraste con cinco meses de gestación en S. mucronatus (Méndez de la Cruz et al., 1994) en un ambiente templado, todas ellas del grupo Poinsettii. El nacimiento de las crías en primavera, antes de la temporada de lluvias asegura que tendrán una mayor disponibilidad de alimento (Méndez de la Cruz et al., 1988; Méndez de la Cruz et al., 1992; Guillette et al., 1993; Méndez de la Cruz et al., 1994; Rivera, 2001). La no presencia de cuerpos grasos en las hembras durante la gestación evidencia su utilización en la vitelogénesis.
El patrón reproductor otoñal tiene un gran éxito en especies vivíparas de clima templado, ya que les da una ventaja, porque sus embriones se encuentran protegidos, dentro de la madre, de las condiciones ambientales extremas y de los depredadores (Qualls, 1997). El patrón otoñal de S. macdougalli en un ambiente cálido seco, tiene como ventaja que durante este periodo las temperaturas no llegan a ser tan altas que puedan ser perjudiciales a su descendencia (López, 2005). Por otro lado, en el caso de los machos también la actividad otoñal evade las temperaturas elevadas que se presentan en primavera y verano y que pueden ser un factor adverso, porque afectan negativamente a la espermatogénesis (Scott, 1994).
Mendoza-Quijano et al., (2002) reportaron la presencia de dos crías en una hembra de 85.7 de LHC con el presente trabajo se muestra que S. macdougalli presenta el tamaño de camada más pequeño reportado en el grupo Poinsettii y en el grupo Torquatus, su grupo hermano. El tamaño pequeño de camada en la especie se debe a que su microhábitat corresponde a enormes rocas graníticas. La camada pequeña contribuye en tener buen desplazamiento, evadir depredadores, en la obtención de alimento y alcanzar la temperatura adecuada para el desarrollo de los embriones (Shine, 1985).
En hembras es menor la talla en la que maduran sexualmente, con respecto a los machos, esto coincide con otras especies del grupo Poinsettii: S. serrifer (Rivera, 2001), S. mucronatus (Méndez de la Cruz et al., 1988; Salazar, 2003) y con otras especies vivíparas, saxícolas o trepadoras del género tales como: S. torquatus (Gillette y Méndez de la Cruz, 1993), S. grammicus (Gillette y Casas Andreu, 1980) y S. megalepidurus (González, 1991). Aunque, los datos del presente trabajo no son numerosos hay evidencia de la inexistente relación entre la talla de la hembra y el tamaño de camada, lo cual muestra que las hembras jóvenes invierten la misma energía en la reproducción que las hembras de mayor edad.
S. macdougalli es un depredador carnívoro, porque su dieta se compone fundamentalmente de artrópodos y el consumo de material vegetal, se atribuye a un consumo accidental, al alimentarse de algún animal. Al mismo tiempo, es oportunista por que consumió presas ocasionales o en masa según su disponibilidad (Barbault et al., 1978). Por otro lado, la baja similitud en la dieta entre sexos puede deberse a un uso diferente del microhábitat o a que las hembras se alimentan menos durante la preñez, debido a la compactación del tubo digestivo, por la presencia de los embriones en desarrollo.
La edad máxima que puede alcanzar la especie es de ocho años, mientras que S. serrifer alcanza la edad máxima de tres años (Méndez, 2002). Lo que muestra que S. macdougalli es más longeva o tiene menor presión depredatoria o competencia por los recursos, debido al microhábitat que utiliza. El estudio esqueletocronológico también permitió establecer que, a partir de un año de edad, las hembras pueden reproducirse y tener crías. Existieron diferencias en el desarrollo entre sexos, ya que cuatro de las hembras con uno y dos años de edad tenían una talla similar a la de dos machos juveniles que no alcanzaban un año de edad, así mismo, dos hembras que presentaban cuatro años de edad al compararse con un macho de un año de edad poseían una talla similar lo que muestra las diferencias en el crecimiento entre sexos (Wake y Castanet, 1995; Harvey, 2001). La especie presento una relación directa y significativa entre la LHC y el número de anillos hematoxylinofilicos, por lo que la talla puede ser usada como un indicador de la edad de los organismos.
El tiempo de gestación de cuatro meses es relativamente corto, consecuencia de la temperatura alta que prevalece en su hábitat, que acelera el desarrollo embrionario (Shine, 1980), de similar manera sucede en S. serrifer (Rivera, 2001) con tres meses de duración, en clima calido, y en contraste con cinco meses de gestación en S. mucronatus (Méndez de la Cruz et al., 1994) en un ambiente templado, todas ellas del grupo Poinsettii. El nacimiento de las crías en primavera, antes de la temporada de lluvias asegura que tendrán una mayor disponibilidad de alimento (Méndez de la Cruz et al., 1988; Méndez de la Cruz et al., 1992; Guillette et al., 1993; Méndez de la Cruz et al., 1994; Rivera, 2001). La no presencia de cuerpos grasos en las hembras durante la gestación evidencia su utilización en la vitelogénesis.
CONCLUSIONES
Sceloporus macdougalli presenta un patrón reproductivo de tipo otoñal y sincrónico entre sexos. La preñez tiene una duración de cuatro meses, durante el invierno y primavera. El tamaño de la camada va de dos a cuatro crías, es el más pequeño registrado en el grupo Poinsettii. No existe relación entre el tamaño de camada, la talla y edad de la hembra. Este saurio tiene una dieta carnívora y oportunista. Presenta diferencia en la composición de la dieta entre sexos seguramente por el uso diferencial del microhábitat. Los individuos de la especie alcanzan edades de hasta ocho años.
AGRADECIMIENTOS
Damos las gracias a Saúl López por su ayuda en el trabajo de campo; a la Mtra. Pilar Villeda por su asesoría en la determinación de artrópodos, a Felipe Correa S., Atahualpa de Sucre M. y Alberto Rodríguez por sus comentarios a la primera versión del trabajo. A la FES Iztacala UNAM por el apoyo financiero otorgado a R.G.C. y C.CH. T. y por facilitar un vehículo.
Figura 1
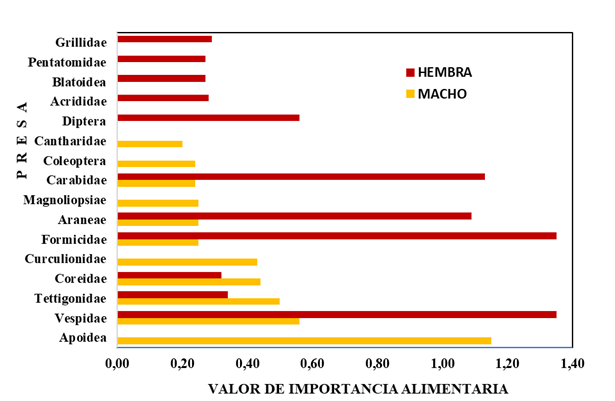
Figura 1.
Figura 1.
Valor de importancia alimentaría de cada presa en la dieta de S. macdougalli.
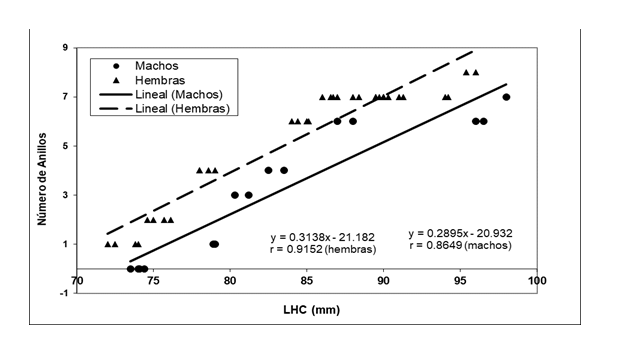
Figura 2
Figura 2.
Correlación del número de anillos hematoxilínicos y la longitud hocico-cloaca de ambos sexos de S. macdougalli.
Cuadro 1.
Cuadro 1.
Valores de la condición reproductiva de machos. I= Inactividad espermatogénica. AE = Actividad espermatogénica.
Cuadro 2.
Cuadro 2.
Datos de la condición reproductiva de las hembras. Estadio embrionario de acuerdo a Defaure y Hubert (1961).
Referencias
Acosta, M. 1982. Índice para el Estudio del Nicho Trófico. Ciencias Biológicas. Academia de Ciencias de Cuba. 70: 125 – 127.
Ballinger, R. E. 1973. Comparative Demography of two viviparous Iguanid lizards (Sceloporus jarrovi and S. poinsetti). Ecology 54: 269-283.
Barbault, R. ; G. Grenot et Z. Uribe. 1978. Le Partege des Lézards du Désert de Mapimí (Mexique). La Terre el la vie. 32:135-150.
Brunning, J. L. y B. Kintz. 1977. Computational Handbook Statistcs, 2nd Ed. Scott Foresman and Co. Glensview Illinois.
Casas-Andreu, G.; G. Valenzuela-López y A. Ramírez Bautista. 1991. Como Hacer una Colección de Anfibios y Reptiles. Departamento de Zoología. Instituto de Biología. UNAM. 68 p.
Castanet, J. y V. De Buffrénil. 2000. Age Estimation by Skeletochronology in the Nile Monitor (Varanus niloticus), a Highly exploited Species. Journal of Herpetology. 34(3): 414-424.
Castanet, J.; D.G. Newman y H. Saint Girons. 1988. Skeletochronological Data on the Growth, Age, and Population Structure of the Tuatara, Sphenodon punctatus, on Stephens and Lady Alice Islands. New Zealand. Herpetologica, 44 (1): 25-37.
Castanet, J. et E. Roche. 1981. Détermination de l’âge chez le lézard des murailles, Lacerta muralis (Laurenti, 1768) au moyen de la squelettochronologie. Revue suisse Zool., 88 (1):215 – 226.
Daly, H. V.; J. T. Doyen y P.R. Ehrlich. 1978. Introduction to Insect Biology and Diversity. Ed. Mc Graw Hill. Tokio, Japan. 564 p.
Defaure, J. P. y J. Hubert. 1961. Table de Développement du Lézard Vivipare: Lacerta (Zootoca) Vivipara Jacquin. Arch. Anat. Microscop. Morphol. Exp. 50: 309-328.
Diario Oficial de la Federación (DOF). 2010. Norma Oficial Mexicana. NOM–059-SEMARNAT–2010, Protección ambiental-Especies Nativas de México de flora y fauna silvestres-categorías en riesgo y especificaciones para su inclusión, exclusión o cambio-Lista de especies en riesgo. Jueves 30 diciembre de 2010.
Feria-Ortiz M.; A. Nieto-Montes de Oca y I. H. Salgado-Ugarte. 2001. Diet and reproductive biology of the viviparous lizard Sceloporus t. torquatus (Squamata: Prhynosomatidae). Journal of Herpetology. 35: 104-112.
Gadsden H.; F. J. Rodríguez-Romero; F. R. Méndez-de la Cruz y R. Gil-Martínez. 2005. Ciclo reproductor de Sceloporus poinsettii Baird y Girard 1852 (Squamata: Phrynosomatidae) en el centro del desierto Chihuahuense, México. Acta Zoológica Mexicana (n.s.) 21(3): 93-107.
García, E. 1973. Modificaciones al sistema de clasificación climática de Köppen (para adaptarlo a las condiciones de la Republica Mexicana). Instituto de Geografía. UNAM, México. 256 p.
García, C. R. 1989. Ciclo Reproductivo y Hábitos Alimenticios de Sceloporus variabilis variabilis (Reptilia: Sauria: Iguanidae) en Alvarado, Veracruz. Tesis de Licenciatura. ENEP Iztacala UNAM.
González, R. G. 1991. Aspectos de la Ecología Poblacional de Sceloporus magalepidurus megalepidurus Smith (Reptilia: Suaria: Igunidae), al oriente de Tlaxcala, México. paginas (Tesis Profesional, ENEP Iztacala. Universidad Nacional Autónoma de México, México).
Guillette, L. J. y G. Casas-Andreu. 1980. Fall Reproductive Activity in the Altitude Mexican Lizard Sceloporus grammicus microlepidotus. Journal of Herpetology. 14 (2): 143–147.
Guillette, L. J. Jr. y F. R. Méndez de la Cruz. 1993. The Reproductive Cycle of the Viviparous Mexican Lizard Sceloporus torquatus. Herpetology. 27 (2): 168–174.
Harvey, P. F. 2001. Herpetology. Editorial Prentice Hall. Segunda Edición. USA. 612 p
Humason, G. L. 1979. Animal tissue techniques 4th ed. San Francisco. Wolt Freeman and Company. 661 p. INEGI. 1987 y 1996. Cartas geográficas, vegetación y topográficas E 15-10, C 82. Escala 1:50,000.
López A. S. 2005. Biología térmica y desempeño locomotor en tres especies de lacertilios vivíparos del grupo Sceloporus torquatus. (Tesis Profesional, Maestría en Ciencias. Universidad Nacional Autónoma de México, México).
Martínez-Méndez, N. y F. R. Méndez-de la Cruz. 2007. Molecular phylogeny of the Sceloporus torquatus species-group (Squamata: Phrynosomatidae). Zootaxa 1609: 53-68.
Méndez, J. B. 2002. Aspectos de la Estrategia Reproductora en la Especie Vivípara Sceloporus serrifer. (Tesis Profesional, FES Iztacala. Universidad Nacional Autónoma de México, México).
Méndez de la Cruz, F. R.; L. J. Guillette Jr.; M. Villagrán-Santa Cruz y G. Casas-Andreu. 1988. Reproductive and Fat Body Cycle of the Viviparous Lizard Sceloporus mucronatus. Journal of Herpetology. 22: 1-12.
Méndez de la Cruz, F. R.; G. Casas-Andreu y M. Villagran-Santa Cruz. 1992. Variación en la Alimentación y Condición Física de Sceloporus mucronatus (Lacertilia: Iguanidae). The Southwestern Naturalist. 37 (4): 349-355.
Méndez de la Cruz, F. R.; M. Feria-Ortiz y O. Cuellar. 1992. Geographic Variation of Reproductive Trains in a Mexican Viviparous Lizard, Sceloporus torquatus. C.R. Soc. Biogeogr. 68(4): 149–156.
Méndez de la Cruz, F. R.; M. Villagrán-Santa Cruz y O. Cuellar. 1994. Geographic Variation of espermatogenesis in the Mexican Viviparous Lizard Sceloporus mucronatus. Biogeographica. 70(2): 59–67.
Mendoza-Quijano, F. e I. Goyenechea. 2004. The karyotype of Sceloporus macdougalli (Squamata: Phrynosomatidae). Revista Española de Herpetología. 18: 75-78.
Mendoza-Quijano, F.; G. Kohler y H. M. Smith. 2002. Extraordinary Sexual Dichromatism in Sceloporus macdougalli (Reptilia: Phrynosomatidae) in Oaxaca, Mexico. Salamandra. Rheinbach. 38(3): 185-190.
Puig, H. 1991. Bosque Tropical Bajo Caducifolio. En: Vegetación de la Huasteca, México. Editorial Collection Études Mesoaméricaines. México.
Qualls, C. 1997. The Effects of Reproductive Mode and Climate on Reproductive Success in the Australian Lizard, Lerista bougainvilli. Australian Journal of Herpetology. 31: 60-65.
Ramírez-Bautista, A.; J. Barba-Torres y J. Vitt. 1998. Reproductive Cycle and Brood Size of Eumeces lynye From Pinal de Amoles, Queretaro, Mexico. Journal of Herpetology. 32: 18-24.
Ramírez-Bautista, A.; O. Ramos-Flores y J. W. Sites Jr. 2002. Reproductive Cycle of the Spiny Lizard Sceloporus jarrovii (Sauria: Phrynosomatidae) from North-Central México. J. Herpetol. 36: 225-233.
Ramírez-Bautista, A.; Z. Uribe-Peña y L. J. Guillette Jr. 1995. Reproductive Biology of the Lizard Urosaurus bicarinatus bicarinatus (Reptilia: Phrynosomatidae) From Rio Balsas Basin, Mexico. Herpetologica. 51: 103-110.
Ramírez-Bautista, A. y J. Vitt. 1997. Reproduction in the Lizard Anolis nebulosus (Polichrotidae) From the Pacific Coast of Mexico. Herpetologica. 53 (4): 423-431.
Rivera, M. J. 2001. Estrategia Reproductora de la Lagartija Tropical Sceloporus serrifer en el Estado de Yucatán. (Tesis Profesional, FES Iztacala. Universidad Nacional Autónoma de México).
Rzedowski, J. 1981. Vegetación de México. Editorial Limusa, México. 215-235.
Salazar, H. D. 2003. Estudio de la Reproducción y Alimentación de Sceloporus mucronatus (Sauria: Phrynosomatidae) en el Sistema modificado de San José Deguedo, Estado de México. (Tesis Profesional FES Iztacala. Universidad Nacional Autónoma de México).
Scott. S. G. 1994. Development Biology. Edit. Sunderland. 4th. Edition. USA. 798–803.
Secretaría de Programación y Presupuesto (SPP). 1981. Carta Geográfica. E 15 – 10. Escala 1:250,000. Servicio Meteorológico Nacional (SMN). 2003. Comisión Nacional del Agua.
Shine, R. 1980. Cost of Reproduction in Reptiles. Oecologia. 46: 92-100
Shine, R. 1985. A new Hypothesis. for the Evolution of Viviparity in Reptiles. Am. Nat. 145:809-823.
Smith, H. M. y C. B. Bumzahem. 1953. A New Lizard of the Genus Sceloporus From the Isthmus of Tehuantepec. Herpetologica. 9:185–188.
Triplehorn, H. A. y N. F. Johnson. 2005. Borror and DeLong´s Introducction to the Study of Insects. Thomson. Brooks/Cole. Seventh Edition. 864 p.
Wake, D. B. y J. Castanet. 1995. A Skeletochronological Study of Growth and Age in Relation to Adult Size in Batrachoseps attenuatus. Journal of Herpetology, 29(1): 60-65.
Wiens, J. J.; C. A. Kuczynski; S. Arif y T.W. Reeder. 2010. Phylogenetic relationships of phrynosomatidae lizards based on nuclear and mitocondrial data, and a revised phylogeny for Sceloporus. Molecular Phylogenetics and Evolution. 54: 150-161.
Notas de autor
collazo@unam.mx