VIROLOGÍA
Estudio del desempeño de dos métodos de detección de antígenos rápidos en hisopados combinados y en hisopados nasofaríngeos para la detección de SARS-CoV-2
Performance study of two rapid antigen detection methods in combined swabs and nasopharyngeal swabs for detection of SARS-CoV-2
Estudo de desempenho de dois métodos de detecção de antígeno rápidos em amostras de esfregaços combinados e esfregaços nasofaríngeos para a detecção de SARS-CoV-2
Estudio del desempeño de dos métodos de detección de antígenos rápidos en hisopados combinados y en hisopados nasofaríngeos para la detección de SARS-CoV-2
Acta Bioquímica Clínica Latinoamericana, vol. 55, núm. 4, pp. 485-489, 2021
Federación Bioquímica de la Provincia de Buenos Aires
Recepción: 17 Noviembre 2020
Aprobación: 24 Septiembre 2021
Resumen: Se realizó una comparación del desempeño de los métodos rápidos de detección de antígenos para el diagnóstico de SARS-CoV-2 Veritor System de Becton Dickinson y Panbio de Abbott versus una reacción en cadena de la polimerasa con retrotranscripción en tiempo real (RT-PCR) de Roche en un triage de demanda espontánea de pacientes febriles de un hospital público, para la detección de COVID-19. Se procesaron 36 hisopados de pacientes sospechosos por los tres métodos. La concordancia entre ambos métodos con la RT-PCR fue del 97%. La sensibilidad de los métodos de detección de antígenos versus la RT-PCR fue del 83% y la especificidad fue del 100%. El valor predictivo positivo (VPP) fue del 100% y el valor predictivo negativo (VPN) fue del 97%. La muestra que resultó discordante presentó un ciclo umbral (Ct) de 29,8. El método para detección de antígenos tuvo un desempeño aceptable, incluso con resultados de sensibilidad mayores que los declarados por los fabricantes (84% para el Veritor System y 93,3% para el Panbio).
Palabras clave: SARS-CoV-2, COVID-19, Antígenos, RT-PCR en tiempo real, Sensibilidad.
Abstract: A comparison of the performance of the rapid antigen detection methods for the diagnosis of SARS-CoV-2 Veritor System from Becton Dickinson and Panbio from Abbott versus a real-time polymerase chain reaction with reverse transcription (RT-PCR) Roche in a spontaneous demand triage of febrile patients of a public hospital was made, for the detection of COVID-19. Thirty six swabs from suspected patients were processed by the three methods. The concordance between both methods with RT-PCR real time was 97%. The sensitivity of the antigen detection methods versus RT-PCR real time was 83% and specificity was 100%. The positive predictive value (PPV) was 100% and the negative predictive value (NPV) was 97%. The sample that was discordant presented a threshold point (Ct) of 29.8. The method for antigen detection resulted in an acceptable performance, even with S results higher than those declared by the manufacturers (84% for the Veritor System and 93.3% for the Panbio).
Keywords: SARS-CoV-2, COVID-19, Antigens, RT-PCR real time, Sensitivity.
Resumo: Uma comparação do desempenho dos métodos rápidos de detecção de antígenos para o diagnóstico deSARS-CoV-2 Veritor System de Becton Dickinson e Panbio de Abbott versus uma reação em cadeia da polimerasecom transcrição reversa em tempo real (RT-PCR) da Roche em uma triagem de demanda espontâneade pacientes febris de um hospital público, para a detecção de COVID-19. Foram processadas 36 amostrasde esfregaços de pacientes suspeitos pelos três métodos e a concordância entre os dois métodos com aRT-PCR foi de 97%. A sensibilidade dos métodos de detecção de antigenos versus a RT-PCR foi de 83% ea especificidade de 100%. O valor preditivo positivo (VPP) foi de 100% e o valor preditivo negativo (VPN)foi de 97%. A amostra que resultou discordante apresentou um ciclo limiar (Ct) de 29,8. O método paradetecção de antígenos teve um desempenho aceitável, mesmo com resultados de sensibilidade superioresaos declarados pelos fabricantes (84% para o Veritor System e 93,3% para o Panbio).
Palavras-chave: SARS-CoV-2, COVID-19, Antígenos, RT-PCR em tempo real, Sensibilidade.
Introducción
Debido a la necesidad de una respuesta oportuna en el diagnóstico de la infección por SARS-CoV-2 han surgido diferentes tests con diferentes sensibilidades y desempeño. Todos son útiles en tanto se tenga en cuenta el contexto en donde se utilicen, es decir, con qué frecuencia se usan, para quiénes se aplican, en qué etapa del curso de la infección, cuál es el porcentaje de positividad de la población en estudio y cuál es el tiempo de respuesta adecuado para evitar la propagación.
Es relevante en este punto diferenciar entre la sensibilidad analítica de una prueba (el límite inferior de su capacidad para detectar correctamente pequeñas concentraciones de moléculas) y la sensibilidad para detectar infecciones (la probabilidad de saber a tiempo si las personas están infectadas, de forma de ser aisladas de la población y prevenir la propagación de la enfermedad) (1) (2). Una prueba del tipo point of care es lo suficientemente económica, sencilla, rápida y exime de la necesidad de utilizar personal altamente capacitado así como también equipamiento específico como lo requieren las técnicas que utilizan la reacción en cadena de la polimerasa con retrotranscripción en tiempo real (RT-PCR) (3). Son tests que, como pueden usarse frecuentemente y presentan una buena sensibilidad, son apropiados para ser utilizados en estudios de vigilancia epidemiológica y detectar infecciones a tiempo para poder actuar, sin llegar al límite analítico de sensibilidad de una prueba de RT-PCR (4) (5) (6) (7).
El objetivo del presente trabajo fue comparar dos métodos rápidos de detección de antígenos (Ag) para el diagnóstico de SARS-CoV-2 con una RT-PCR en un triage de demanda espontánea de pacientes febriles de un hospital público, para la detección de COVID-19.
Materiales y Métodos
Se analizaron 36 muestras de pacientes considerados casos sospechosos, según definición de caso del Ministerio de Salud de la Nación del día 21 de octubre de 2020, que concurrieron al triage de pacientes febriles del Hospital de Alta Complejidad El Cruce “Dr. Néstor Carlos Kirchner”.
De cada paciente se obtuvo un hisopado combinado (orofaríngeo más nasofaríngeo) para la detección de ARN viral de SARS-CoV-2 por el método de RT-PCR de Roche Diagnostics y un hisopado nasofaríngeo de la restante narina para ser analizados por ambos métodos rápidos de detección de antígenos cualitativos para SARS-CoV-2, Veritor System de Becton Dickinson y Panbio de Abbott. Se utilizó el mismo hisopo para ambos tests rápidos. Las muestras se procesaron en cuatro días consecutivos, con variación del personal de toma de muestras entre los días.
Para el Veritor System, la lectura del cassette se realizó mediante el dispositivo de lectura automatizada que provee el fabricante, a los 15 minutos en el modo Analyze Now Mode.
Para el Panbio de Abbott, la lectura del cassette se realizó visualmente a los 15 minutos.
Todas las muestras para los tests de antígenos se procesaron antes de los 10 minutos.
Para la RT-PCR se utilizaron las sondas específicas para los genes E y N. Las muestras fueron procesadas dentro de las 24 h y se determinaron los ciclos umbral (Ct) de los positivos. Para la extracción del ARN viral se utilizaron las columnas Zymo Research RNA Isolation kit.
Se determinó la sensibilidad (S) S=VP/(VP+FN), la especificidad (E) E=VN/(VN+FP), el valor predictivo positivo VPP=VP/(VP+FP) y el valor predictivo negativo VPN=VN/(VN+FN), donde VP eran los verdaderos positivos, VN los verdaderos negativos, FP los falsos positivos y FN los falsos negativos.
Resultados
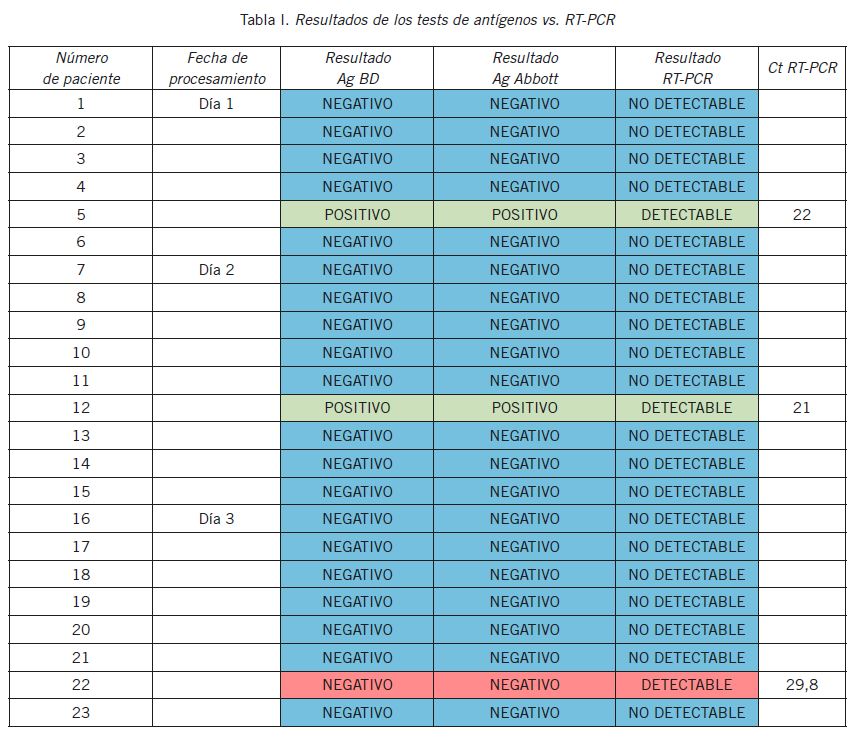
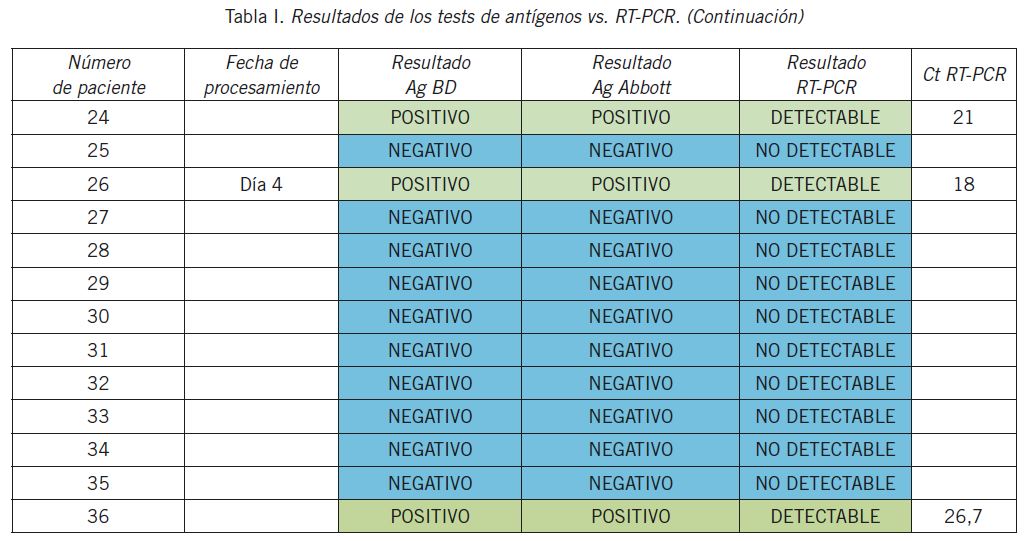
En la Tabla I se muestran los resultados de los tests de antígenos y de la RT-PCR para cada uno de los pacientes y en la Tabla II los resultados de los tests de Ag vs. PCR positivas y PCR negativas.
La concordancia entre ambos métodos de detección de antígeno con la PCR fue del 97% (35/36). Su sensibilidad fue del 83% (5/6) y su especificidad fue del 100% (30/30). El VPP fue del 100% (5/5) y el VPN fue del 97% (30/31). No se registraron cassettes inválidos ni repeticiones.
La muestra que resultó discordante presentó un Ct de 29,8.
Discusión y Conclusiones
Ambos métodos para detección de antígenos tuvieron un desempeño aceptable, con resultados de S menores que los declarados por los fabricantes (84% para el Veritor System de Becton Dickinson y 93,3% para el Panbio de Abbott), pero se requiere de un mayor número de muestras para su mejor evaluación y para poder extraer resultados concluyentes.

Los métodos de detección de antígenos permiten obtener resultados rápidos (20 minutos) en comparación con los obtenidos por RT-PCR (4-5 h), lo que agiliza considerablemente el flujo de trabajo en el triage de un hospital de demanda espontánea de pacientes considerados “casos sospechosos” para COVID- 19.
Después de la recolección, las muestras de hisopados destinadas al test de PCR generalmente requieren ser transportadas a un laboratorio centralizado con personal experto, lo que aumenta los costos y puede retrasar los resultados en uno o más días. Esto resulta en que personas infectadas, todavía pueden propagar la infección durante días antes de la notificación, lo que limita el impacto del aislamiento y el rastreo de contactos. Otro beneficio es que no se necesita una cabina de bioseguridad tipo IIA ni un termociclador. Tampoco se requiere contar con personal altamente calificado para su procesamiento. Por todo esto, es que se concluye que los métodos de detección de antígenos son óptimos para los estudios de vigilancia epidemiológica, a pesar de que no poseen un sensibilidad clínica tan elevada como los métodos moleculares.
Fuentes de financiación
Los kits de Panbio y Veritor Plus fueron provistos por los laboratorios Abbott y Becton Dickinson respectivamente. No hubo incentivo económico para la realización del trabajo, ni para los autores ni para la institución.
Conflictos de intereses
Los autores declaran no tener conflictos de intereses respecto del presente trabajo.
Correspondencia
Bioq. MARTÍN ZUBIETA
Centro de diagnóstico COVID-Centro de Excelencia en Medicina Traslacional (CEMET), Hospital de Alta Complejidad en Red El Cruce Dr. Néstor C. Kirchner –SAMIC.
Av. Calchaquí 5401, FLORENCIO VARELA Provincia de Buenos Aires, Argentina
Correo electrónico:mzubieta74@gmail.com
Referencias bibliográficas
1. Saah AJ, Hoover DR. “Sensitivity” and “specificity” reconsidered: the meaning of these terms in analytical and diagnostic settings. Ann Intern Med 1997; 126: 91-4.
2. Larremore DB, Wilder B, Lester E, Shehata S, Burke JM, Hay JA, et al. Test sensitivity is secondary to frequency and turnaround time for COVID-19 surveillance. Sci Adv 2021 Jan 1; 7(1): eabd5393.
3.Paltiel AD, Zheng A, Walensky RP. Assessment of SARSCoV- 2 screening strategies to permit the safe reopening of college campuses in the United States. JAMA Netw Open 2020; 3(7): e2016818.
4. Chin ET, Huynh BQ, Chapman LAC, Murrill M, Basu S, Lo NC. Frequency of routine testing for COVID-19 in highrisk healthcare environments to reduce outbreaks. Clin Infect Dis 2020 Oct 26: ciaa1383.
5. He X, Lau EHY, Wu P, Xilong D, Jian W, XinXin H, et al. Temporal dynamics in viral shedding and transmissibility of COVID-19. Nat Med 2020; 26: 672-5.
6. Centers for Disease Control and Prevention. Transcript for the CDC telebriefing update on COVID-19. June 25, 2020. Disponible en: https://www.cdc.gov/media/releases/ 2020/t0625-COVID-19-update.html. (Fecha de acceso: 5 de julio de 2020).
7. Mina MJ, Parker R, Larremore DB. Rethinking Covid-19 test sensitivity - A strategy for containment. N Engl J Med 2020 Nov 26; 383 (22): e120.
Notas de autor
Bioq. MARTÍN ZUBIETA Centro de diagnóstico COVID-Centro de Excelencia en Medicina Traslacional (CEMET), Hospital de Alta Complejidad en Red El Cruce Dr. Néstor C. Kirchner –SAMIC. Av. Calchaquí 5401, FLORENCIO VARELA Provincia de Buenos Aires, Argentina Correo electrónico:mzubieta74@gmail.com