VIROLOGÍA
Recepción: 28 Abril 2021
Aprobación: 04 Octubre 2021
Resumen: La detección de SARS-CoV-2 y su implicancia en el diagnóstico de COVID-19 han sido muy debatidas en la pandemia. El objetivo de este estudio fue evaluar el costo/beneficio de la detección de SARS-CoV-2 en contactos estrechos asintomáticos (CE) mediante el uso de distintas pruebas de diagnóstico molecular. Se estudiaron 51 CE de personas con diagnóstico de SARS-CoV-2 confirmado por RTqPCR, clasificadas por el umbral de ciclos (Ct) (<20, entre 20 y 30 y >30) en hospitales públicos de la provincia de Buenos Aires. Del total de contactos estudiados el 15,7% resultó confirmado para SARS-CoV-2; no hubo contactos positivos de casos con Ct>30. La cantidad de contactos positivos de casos con Ct<20 fue significativamente mayor que la de casos con Ct>20. Las muestras con Ct<20 se asociaron a una carga viral estimada de entre uno a cuatro órdenes de magnitud de diferencia con los rangos de Ct>20. Un 13,7% de contactos positivos fueron casos con Ct<20. De las muestras positivas confirmadas por PCR, correspondientes a la semana epidemiológica 1 de 2021 (SE1), sólo un 19,35% correspondían a muestras con Ct<20 y un 50,7% con Ct entre 20 y 30. Estos datos muestran un incremento de sólo un 3,7% de casos detectados. El esfuerzo por parte del sistema de salud pública para esta estrategia, con bajo poder predictivo, puede tener un efecto negativo para el cumplimiento del aislamiento de los contactos y podría generar una demora en los resultados de los casos sospechosos, sin aportar significativamente en el control de la pandemia.
Palabras clave: SARS-CoV-2, Contactos estrechos, Carga viral, Medidas sanitarias, Contención de COVID-19.
Abstract: The detection of SARS-CoV-2 and its implication in the diagnosis of COVID-19 have been highly debated in the pandemic. The objective of this study was to evaluate the cost/benefit of detecting SARS-CoV-2 in asymptomatic close contacts (CC) using different molecular diagnostic tests. A total of 51 CC of people with a diagnosis of SARS-CoV-2 confirmed by RTqPCR, classified by the cycle threshold (Ct) (<20, between 20 and 30 and >30), were studied in public hospitals in the Province of Buenos Aires. Of the total contacts studied, 15.7% were confirmed for SARS-CoV-2; there were no positive contacts of cases with Ct>30 positive. The number of positive contacts of cases with Ct<20 was significantly higher than that of cases with Ct>20. Samples with Ct<20 were associated with an estimated viral load of one to four orders of magnitude difference with Ct ranges >20. A total of 13.7% of positive close contacts were from cases with Ct<20. When studying positive samples with confirmed diagnosis by PCR, corresponding to 1 epidemiological week of 2021 (EW1), only 19.35% corresponded to samples with Ct<20 and 50.7% with Ct between 20 and 30. From these data it is shown that with the CC test only 3.7% of the cases were detected. The effort by the public health system for this strategy, with low predictive power, may have a negative effect on the fulfillment of the isolation of contacts and could generate a delay in the results of suspected cases, without contributing significantly to controlling the pandemic.
Keywords: SARS-CoV-2, Close contacts, Viral load, Public health measures, COVID-19 containment.
Resumo: A detecção do SARS-CoV-2 e seu envolvimento no diagnóstico da COVID-19 têm sido muito discutidos durante a pandemia. O objetivo desse estudo foi avaliar a relação custo/benefício na detecção de SARSCoV- 2 em casos de contatos próximos assintomático (CP), por meio do uso de diferentes testes de diagnóstico molecular. Foram estudados 51 casos de CP de pessoas com diagnóstico de SARS-CoV-2 confirmado pelo RTqPCR, sendo classificados pelo limiar de ciclos (Ct) (<20, entre 20 e 30 e >30), em hospitais públicos da província de Buenos Aires. Do total de contatos estudados, 15,7% foram confirmados para SARS-CoV-2, não houve contatos positivos de casos com Ct>30. O número de contatos positivos de casos com Ct<20, foi significativamente maior que os casos com Ct>20. As amostras com Ct<20 foram associadas a uma carga viral estimada de uma a quatro ordens de magnitude de diferença com os intervalos de Ct>20. Dos casos positivos, 13,7% foram com Ct<20. Das amostras positivas confirmadas por PCR, correspondentes à semana epidemiológica 1 de 2021 (SE1), apenas 19,35% correspondiam a amostras com Ct>20 e 50,7% com Ct entre 20 e 30. Esses dados mostram incremento de apenas 3,7% de casos detectados. O esforço por parte do sistema de saúde pública para essa estratégia, com baixo poder preditivo, pode ter um efeito negativo no cumprimento do isolamento dos contatos e poderia gerar uma demora nos resultados dos casos suspeitos, sem contribuir significativamente para o controle da pandemia.
Palavras-chave: SARS-CoV-2, Contatos próximos, Carga viral, Medidas sanitárias, Contenção da COVID-19.
Introducción
La detección de SARS-CoV-2 y su implicancia en el diagnóstico de la enfermedad COVID-19 ha sido una de las preocupaciones más grandes de esta pandemia. El diagnóstico molecular es una de las herramientas necesarias para contener la propagación del virus y para el manejo de casos. Por esta razón, el acceso al diagnóstico molecular ha cobrado gran interés y constituye una parte esencial de las políticas públicas.
El método indicado para la confirmación estándar de la infección aguda por el SARS-CoV-2 se basa en la detección de secuencias específicas del genoma viral mediante pruebas de amplificación de ácidos nucleicos (ARN de simple cadena en el caso de SARS-CoV-2), como la transcripción reversa seguida de la reacción en cadena de la polimerasa en tiempo real (RTqPCR). Este método consiste en la amplificación del material genético viral luego de su extracción a partir de una muestra de vías respiratorias y es considerado el método gold standard para el diagnóstico de personas sintomáticas con sospecha de COVID-19 (1).
El diagnóstico de la COVID-19 y la detección de SARS-CoV-2 han sido objeto de interés y debate desde los inicios de la pandemia, pero, sobre todo, se puso énfasis en la identificación de la población destinataria de estudios de diagnóstico molecular. Mucho se ha discutido acerca de la utilidad de testear personas asintomáticas y, entre ellas, contactos estrechos de casos confirmados (2). Tanto desde el ámbito científico como desde el no científico han emanado posiciones encontradas. Desde el campo de la investigación, numerosas publicaciones mostraron los beneficios del testeo de contactos (3) (4) (5), fundamentalmente a partir de modelos matemáticos, pero no se informaron evaluaciones del impacto cuantitativo en experiencias concretas de gestión de la pandemia, que incorporen las dimensiones técnicas y logísticas en la obtención de las muestras y la interpretación de sus resultados. Sin embargo, sí se ha probado ampliamente que el aislamiento de los contactos estrechos y el distanciamiento son las medidas más efectivas (5). Tampoco hay dudas acerca de la sensibilidad de las técnicas de diagnóstico molecular utilizadas. La sensibilidad analítica de este método es de aproximadamente un 85-95%, dependiendo del gen blanco utilizado y de otros factores (6) (7). El virus puede ser detectado en las vías respiratorias superiores de 1 a 3 días antes de aparecer los síntomas. La concentración de SARS-CoV-2 en las vías respiratorias superiores alcanza su valor más alto en torno al momento de la aparición de los síntomas y luego va disminuyendo paulatinamente (8) (9) (10) (11) (12) (13) (14). Es por esta razón que para minimizar la probabilidad de un resultado falsamente negativo, la muestra para diagnóstico debe ser tomada en casos sospechosos, es decir, en personas que presenten síntomas. Estas son directrices internacionales, a las cuales adhiere el Ministerio de Salud de la Nación en su protocolo, que se adecua jurisdiccionalmente en el caso de este estudio a la Provincia de Buenos Aires (PBA). Esta evidencia es consistente con la información de la OMS, el CDC de los EE.UU. y otras publicaciones nacionales (15).
También se ha estudiado la transmisibilidad de SARS-CoV-2 en relación con la carga viral de la persona portadora. Existe respaldo en la literatura que asocia cuadros clínicos con mayor expresión sintomática, con cargas virales y, por ende, con menores valores de umbral de ciclos (Ct, del inglés: cycle threshold) (16). No obstante, existen casos confirmados asintomáticos cuya carga viral es alta, lo cual complejiza aún más el cuadro epidemiológico (17).
A pesar de la evidencia publicada, el debate acerca del testeo masivo de personas asintomáticas continúa cobrando importancia sobre todo en los medios de comunicación, redes sociales y en los espacios no especializados en el tema que, en ocasiones, generan lo que se ha denominado infodemia en la cual predomina la desinformación que impacta sobre la toma de decisiones, especialmente a nivel individual (18). Por esta razón, se consideró necesario estudiar localmente cuán efectiva podría ser la medida de testear a contactos estrechos de casos confirmados que se encuentren asintomáticos teniendo en cuenta aspectos técnicos, operativos y epidemiológicos.
En la República Argentina, bajo un marco normativo general y disposiciones del Ministerio de Salud de la Nación, las jurisdicciones trazan sus estrategias y adecuan la normativa para abordar la pandemia de COVID-19 de acuerdo a las particularidades de su demografía y la capacidad y estructura del sistema de salud y sus subsistemas en su territorio. El gobierno de la PBA, a través de su Ministerio de Salud (MinSal PBA), garantiza de forma pública y no arancelada el acceso al diagnóstico molecular por el laboratorio, al constituir y coordinar una red de laboratorios asistenciales públicos de gestión nacional, provincial y municipal y laboratorios de investigación de universidades y otros organismos públicos, a los que abastece total o parcialmente en materia de reactivos e insumos. La articulación entre el MinSal PBA y aquellos efectores que no son de administración provincial se encuentra mediada por la Dirección Provincial de Regiones Sanitarias, que establece un circuito de derivación para las muestras obtenidas para diagnóstico.
El objetivo de este estudio fue evaluar el costo/beneficio de la detección viral de SARS-CoV-2 en contactos estrechos asintomáticos mediante el uso de tres herramientas diagnósticas disponibles y utilizadas en la PBA (19). Estos tres tipos de pruebas fueron la detección de antígeno viral por inmunocromatografía [test de antígeno (Ag)], que se utiliza para mejorar la oportunidad del diagnóstico solo en aquellos lugares donde el acceso a métodos de biología molecular es dificultoso, la RTqPCR y las técnicas de amplificación isotérmica de ácidos nucleicos. A fin de poder llevar adelante un estudio más profundo, se buscó encontrar si existía una relación entre los Ct de las muestras de los casos confirmados y la transmisibilidad a sus contactos estrechos.
Se consideraron también, como aspectos a estudiar en este trabajo, la adherencia de los contactos estrechos para ser testeados y la factibilidad logística del testeo de contactos estrechos a fin de hacer un análisis completo de la utilización del testeo de contactos estrechos como herramienta epidemiológica y su efecto concreto en la salud pública.
Materiales y Métodos
El estudio de contactos estrechos se inició a partir de personas con diagnóstico de SARS-CoV-2 confirmado por laboratorio mediante RTqPCR (DisCoVery SARS-CoV-2RT-PCR Detection Kit, AP Biotech) (20) en cinco laboratorios de hospitales públicos de la PBA: Hospital Interzonal Especializado de Agudos y Crónicos (HIEAyC) San Juan de Dios de La Plata, Hospital Interzonal General de Agudos (HIGA) Dr. Alende de Mar del Plata, HIGA Dr. José Penna de Bahía Blanca, Hospital Zonal Especializado Materno Infantil (HZEMI) Argentina Diego de Azul y el HIGA Eva Perón de San Martín.
El cálculo del tamaño de la muestra de contactos estrechos se realizó en base a los datos publicados en la bibliografía sobre la proporción de resultados positivos encontrados en muestras de contactos estrechos (21). Para el cálculo se tomó como valor conocido una proporción del 20% encontrada, un 95% de confianza (riesgo alfa), un 90% de precisión (riesgo beta) y un 10% de pérdida, y se determinó que el número adecuado de la muestra debía ser de 70.
De los resultados de diagnóstico de COVID-19 por RTqPCR, los equipos de laboratorio eligieron personas confirmadas clasificadas por rango de Ct.
Los criterios de inclusión para la elección de las personas confirmadas por cada laboratorio fueron los siguientes:
Ct: se seleccionaron pacientes confirmados con Ct menores de 20, Ct entre 20 y 30, y Ct mayores de 30.
Lugar de residencia: aquellos con residencia dentro del área programática del laboratorio de procesamiento de muestras.
Una vez elegidos los casos, se realizó el relevamiento de los contactos estrechos de los casos confirmados (dos por caso confirmado) bajo la definición del protocolo de la provincia de Buenos Aires (22). Ninguno de los contactos estrechos elegidos presentaba síntomas a la hora de realizar el estudio y todos residían en el área programática del Hospital/Municipio.
Los contactos estrechos fueron mayores de 18 años, en lo posible, no convivientes y sin COVID-19 diagnosticado previamente.
En los casos en que los contactos estrechos no estaban registrados en el Sistema Nacional de Vigilancia de la Salud (SNVS), el Municipio se encargó de comunicarse con la persona confirmada para relevar dicha información.
El Comité de Ética central del MinSal PBA aprobó el estudio a fin de poder utilizar los datos del SNVS para el mismo.
Los contactos estrechos fueron contactados telefónicamente por el Centro de Telemedicina COVID-19 (Ce- Tec-19, MinSal PBA) para su participación, informados sobre el estudio y, de aceptar, firmaron conformidad mediante consentimiento informado. Los procedimientos de toma de muestra fueron realizados luego de la firma del consentimiento informado. Los contactos estrechos seleccionados que no aceptaron ser parte del estudio no fueron reemplazados, ya que el cálculo del tamaño de la muestra contempló una posibilidad de pérdida o no adherencia del 10% y la adherencia constituyó una variable para el análisis.
Una vez confeccionada la lista de contactos estrechos, se envió al equipo de muestreo designado (equipo de hospital, municipio o regiones, según organización local), quien realizó los hisopados en domicilio al día siguiente de la obtención del resultado detectable para el caso confirmado (Fig. 1). Para ello, se contó con transporte a disposición e hisopadores con equipos de protección personal.
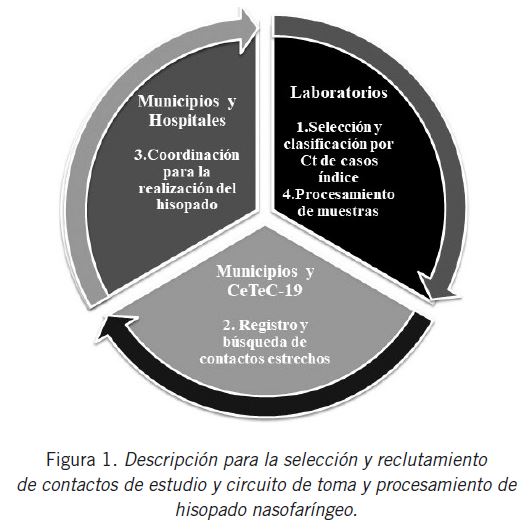
El equipo de muestreo ofreció, mediante consentimiento informado, la posibilidad de participación en este estudio. Se registró cada caso como “contacto de caso confirmado o probable de SARS-CoV-2” en papel y en el SNVS.
De cada contacto estrecho se obtuvo un hisopado nasofaríngeo para ser analizado por el método rápido de detección de antígenos cualitativo para SARS-CoV-2, PANBIO COVID-19 Ag Rapid Test Device, Abbott (test de Ag). En aquellos casos en que la muestra no pudo ser enviada en menos de una hora al laboratorio, se realizó la prueba de Ag en el momento.
Cuando el resultado del test de Ag fue positivo, el municipio o la Región Sanitaria, según correspondiera, completó la información necesaria para la notificación del caso en el SNVS y se tomaron todas las conductas establecidas en el protocolo del MinSal PBA. Cuando el resultado fue negativo, se registró también como “contacto de caso confirmado o probable de SARS-CoV-2” en papel y en el SNVS y se realizó un segundo hisopado para enviar al laboratorio para la detección de ARN viral de SARS-CoV-2 por RTqPCR y por el método de amplificación isotérmica (Neokit). Todos los resultados del test de Ag se registraron en una planilla, para comparar los negativos con los resultados de la RTqPCR y la amplificación isotérmica.
Las muestras para PCR y amplificación isotérmica (un hisopado por contacto estrecho) fueron enviadas, bajo condiciones de bioseguridad, al laboratorio del hospital para ser procesadas ese día o el día siguiente.
Para los contactos positivos de casos por estas técnicas se registró el evento como un nuevo caso confirmado en el SNVS.
A los contactos de casos que tuvieron resultado negativo para este primer screening (toma 1: T1) se les efectuó otro hisopado a domicilio, para realizar nuevamente las pruebas de RTqPCR, amplificación isotérmica y Ag, luego de 7 días desde el último contacto con el caso confirmado tal como fue descripto para la T1 (Fig. 2).
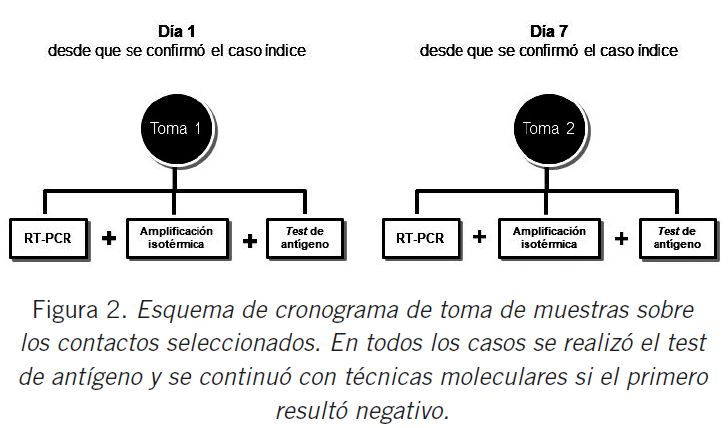
Con esta información se determinó la prevalencia encontrada en función de la clasificación de Ct y se comparó la sensibilidad y especificidad de los métodos empleados contra RTqPCR.
Relevamiento de casos confirmados en la primera semana epidemiológica de 2021
Se realizó un relevamiento del número de muestras con resultado detectable durante la semana epidemiológica 1 de 2021 (SE1) que abarcaba desde el 4 hasta el 11 de enero de 2021. El mismo involucró a 5 laboratorios correspondientes a las regiones sanitarias número 1, Laboratorio del Hospital Provincial General de Agudos Dr. José Penna (con la mayor parte de las muestras recibidas del Partido de Bahía Blanca); número 6, Laboratorio de la Plataforma de Servicios Biotecnológicos (PSB) de la Universidad Nacional de Quilmes (con la mayor parte de las muestras recibidas del Partido de Quilmes); número 7, Laboratorio de la Universidad Nacional de Hurlingham (UNAHUR) (con la mayor parte de las muestras recibidas de Ituzaingó y Hurlingham); Instituto de Investigaciones Biomédicas de Retrovirus y SIDA de la Universidad de Buenos Aires emplazado en la Ciudad Autónoma de Buenos Aires (con la mayor parte de las muestras provenientes de los partidos de La Matanza, Quilmes, Morón, Moreno, Vicente Lopez, San Isidro, Cañuelas, Pilar, Campana) y número 11, Laboratorio de Virología del Hospital Provincial Interzonal Especializado de Agudos San Juan de Dios (con la mayor parte de las muestras recibidas del Partido de La Plata).
Las muestras que recibieron los laboratorios fueron procesadas por RTqPCR y en cada caso detectable se registró el valor de Ct obtenido.
Adicionalmente, en el Laboratorio de la UNAHUR, se cuantificó la carga viral (copias génicas/µL) en las muestras que resultaron detectables mediante un ensayo de RTqPCR desarrollado para tal fin: cuantificación absoluta mediante una curva de calibración generada con un estándar de concentración conocido (en este caso un plásmido que contiene el fragmento de amplificación de la PCR correspondiente al gen E de SARS-CoV-2). Para ello, se adaptó la RT-qPCR desarrollada por Corman et al. (23). Brevemente, se obtuvo la secuencia de un fragmento del gen E empleando el set de primers descriptos por dicho autor y una muestra de ARN que había resultado detectable como templado. El amplificado obtenido se insertó en el plásmido pGEM-Teasy (PROMEGA). La construcción obtenida se cuantificó y se empleó para generar la curva de calibración (diluciones seriadas en base 10 desde 108 copias/µL hasta 101 copias/µL). Esta curva se ensayó por triplicado en el momento de cuantificar las muestras seleccionadas y presentó una eficiencia del 98,4% y un R2=0,996. La carga viral se expresó como copias genómicas/µL.
Análisis estadístico
Para la preparación de los datos y los análisis se utilizó el software GraphPad Prism 7.0. Las asociaciones entre variables cualitativas se analizaron en tablas de contingencia mediante test de Chi cuadrado. Se consideraron estadísticamente significativas las pruebas que presentaron un valor de p<0,05. Los datos se muestran como frecuencias, porcentajes o medias ponderadas.
Resultados
Se estudiaron 51 contactos estrechos de personas con diagnóstico de SARS-CoV-2 confirmados por laboratorio mediante RTqPCR en cuatro hospitales públicos de la provincia de Buenos Aires establecidos originalmente.
– HIGA Dr. José Penna: n=27 (7<20, 14 entre 20 y 30, 6>30)
– HIGA Dr. Alende: n=14 (8<20, 2 entre 20 y 30, 4>30)
– HZEMI Argentina Diego: n=8 (1<20, 4 entre 20 y 30, 3>30)
– HIEAyC San Juan de Dios: n=2 (<20)
No se alcanzó el número establecido debido a falta de adhesión y problemas logísticos por la complejidad de articulación entre laboratorio, región sanitaria y municipio; esto imposibilitó continuar con el estudio en esos casos donde solo se llegó a la elección de los casos confirmados por el laboratorio, pero no pudo identificarse a los contactos ni realizar la toma de muestra.
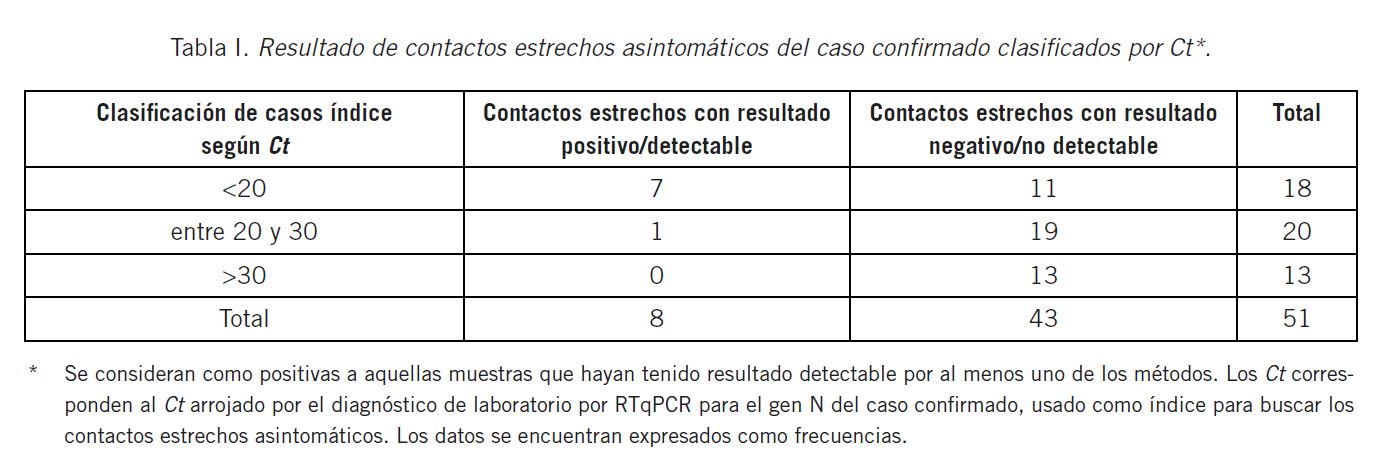
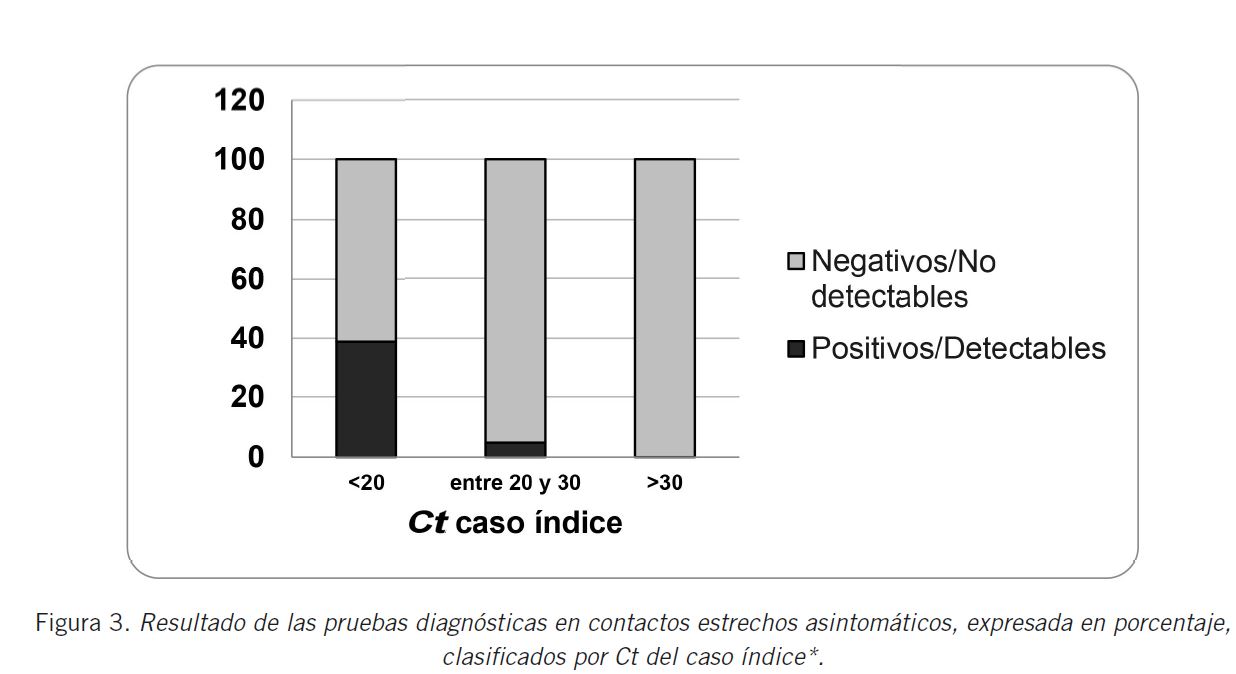
Para evaluar la asociación entre el resultado arrojado y el Ct del caso confirmado, se realizó una prueba de Chi cuadrado. Existió una asociación entre estas variables (p=0,0032); los contactos de casos con Ct bajos (medida indirecta e inversamente proporcional de la carga viral) presentaron más resultados positivos (Tabla I). En la Figura 3 se pueden observar los porcentajes de contactos con resultado positivo relativos al total de cada categoría.
De los 8 positivos, 6 (75%) eran de T1 (tiempo variable del último contacto con el caso confirmado) ya que correspondían al día siguiente a la confirmación por laboratorio del caso índice. La mediana de T1 fue de 3 días. Dos de los casos (25%) correspondían a T2 (7 días después del último contacto con el caso índice).
En T1 el test de Ag no presentó diferencias con la RTqPCR ni con la amplificación isotérmica. La concordancia para los resultados obtenidos para la RTqPCR y para la técnica isotérmica fue del 100%.
En T2 dos personas arrojaron resultados positivos por RTqPCR y por amplificación isotérmica y registraron resultados negativos por el test de Ag.
Se considera como positivas a aquellas muestras que hayan tenido resultado detectable por al menos uno de los métodos. Los Ct corresponden al Ct arrojado para alguno de los genes por el diagnóstico de laboratorio por RTqPCR del caso confirmado, usado como índice para buscar los contactos estrechos asintomáticos. El eje Y está expresado como porcentaje de casos calculado sobre el total de cada categoría.
Clasificación de muestras confirmadas por Ct de la RTqPCR de la primera semana epidemiológica de 2021
Para poder analizar e interpretar los resultados arrojados en este estudio se consideró necesario conocer el porcentaje de personas confirmadas en la SE1 a fin de poder evaluar el impacto de los resultados obtenidos.
Para ello se relevó este dato de cinco laboratorios de la Red Pública Provincial de vigilancia y diagnóstico de COVID-19 mediante detección de SARS-CoV-2 por RTqPCR.
La cantidad de muestras con resultado detectable analizadas fueron 2781, correspondientes a la semana epidemiológica 1 de 2021 (4 al 11 de enero).
El rango porcentual de muestras con Ct menores de 20 fue de 11 a 49% con un promedio ponderado de 19,35%.
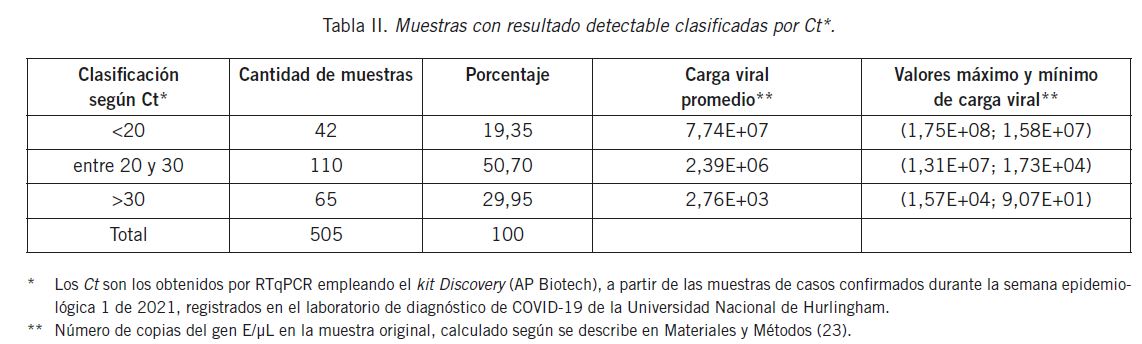
A 505 muestras, de las 2781, procesadas en el laboratorio de la Universidad Nacional de Hurlingham se les estudió la carga viral mediante una RTqPCR que cuantifica el número de copias del gen E. Estas muestras se encuentran clasificadas por Ct en la Tabla II.
Discusión y Conclusiones
El estudio de contactos estrechos asintomáticos mostró que la cantidad de contactos de casos con resultado positivo con Ct más bajos (<20) era significativamente mayor que la de confirmados con Ct mayores de 20. El número de contactos estrechos positivos de casos con Ct<20 positivos representó un 13,7% de los contactos evaluados. Sin embargo, es importante considerar que el porcentaje de muestras con Ct menores de 20 osciló entre un 11 y un 49% entre establecimientos, con un promedio de 19,35% al evaluar las muestras tomadas durante la SE1 en 5 laboratorios de la red provincial de diagnóstico de COVID-19, pertenecientes a 5 regiones sanitarias distintas. La cantidad de muestras positivas de estos 5 laboratorios fue de 2781 personas con diagnóstico confirmado por PCR. Si se extrapola ese 13,7% al 19,35% el porcentaje final de contactos estrechos positivos sería de un 2,7%. Al analizar los contactos estrechos positivos de casos con Ct entre 20 y 30 se puede observar que éstos representaron un 2% del total de contactos evaluados. El porcentaje de casos con Ct entre 20 y 30 de la SE1 de 2021 representó el 50,7%. Al analizar estos datos se puede decir que el porcentaje de contactos positivos de casos para este rango sería de un 1%. De este modo, el impacto final de detección de casos con esta estrategia sería de 3,7%.
Cabe mencionar que, para las muestras positivas analizadas en el laboratorio de la UNAHUR, la carga viral promedio en aquellas con Ct<20 fue de 7,74 E+07, para las muestras con Ct entre 20-30 fue de 2,39 E+06 y para las muestras con Ct>30 fue de 2,76 E+03 cg/µL. En este sentido, un estudio realizado por Kawasuji et al., demostró que la transmisión de SARS-CoV-2 estaba favorecida por las personas que presentaban una alta carga viral, evaluada en hisopados nasofaríngeos, lo que contribuía a un mayor contagio entre contactos estrechos (24).Teniendo en cuenta que la infectividad de una muestra se comprueba mediante el aislamiento viral, en una serie publicada por Wendtner et al. se obtuvieron cultivos positivos en aquellas que tenían una carga viral mayor de 10 E+06 cg/mL; esta carga viral se corresponde en nuestros datos con aquellas que presentaban un Ct<20. Los mismos autores señalaban que en ningún caso hubo aislamiento en muestras tomadas después del día 8 del curso de la enfermedad (25).
En otro trabajo, se determinó que un número significativo de pacientes con altos niveles de virus (>8 log10 copias/ mL) en muestras respiratorias eran responsables de una mayor transmisión tanto a contactos estrechos como al ambiente. En cambio, las personas con baja carga viral (<1000 copias/mL) presentaban un bajo riesgo de transmisión. Por lo tanto, la detección cuantitativa de SARS-CoV-2 constituye una metodología que aporta información de gran utilidad para controlar la transmisión de la enfermedad (26).
Las pruebas de Ag no mostraron diferencias con las otras técnicas evaluadas dentro de los primeros días luego del contacto con el caso índice. En las muestras tomadas en el día 7 después del contacto con el caso confirmado se presentaron diferencias entre técnicas. El tamaño muestral fue pequeño como para poder sacar conclusiones sobre esta diferencia observada. Por otra parte, la adherencia de los contactos estrechos al estudio fue baja, de manera que no se alcanzó el número establecido. A esta dificultad se adicionó la complejidad que implica que los municipios y su coordinación con la estructura provincial contacten e hisopen a los contactos estrechos, lo que implicó que dos municipios no pudieran llevar a cabo el estudio. Debido a estas razones, el estudio se realizó con 51 personas ya que no se logró alcanzar las 70 personas establecidas originalmente como número mínimo de individuos a evaluar.
Uno de los objetivos de este estudio fue el relevamiento de información necesaria para el diseño de estrategias a implementar en la gestión de políticas sanitarias para el control y mitigación de brotes y este resultado aportó una valiosa información en este sentido. Un contexto de pandemia presenta numerosas y complejas exigencias para los sistemas de salud en todos sus niveles. A escala de la provincia de Buenos Aires, los agentes municipales, junto con los provinciales, tuvieron incumbencia compartida en el desarrollo de búsquedas activas de casos, en la vigilancia de instituciones de estancia prolongada y en la respuesta en cuanto a recursos humanos y materiales de sus efectores de salud y de los laboratorios de diagnóstico de la Red Provincial disponibles en sus regiones sanitarias. La implementación de estrategias adicionales que insumen el trabajo de los mismos actores a cargo del abordaje de las tareas antes mencionadas deben poder acreditar beneficios demostrables en políticas públicas que garanticen el derecho a la salud de la población, la captación de casos y el control de brotes y la evidencia acumulada no sugiere que deba recomendarse en ese contexto epidemiológico y del estado del arte para el diagnóstico de COVID-19. Estas acciones resultan indispensables y han demostrado ser efectivas en el control de la enfermedad a nivel poblacional, por lo que resulta necesario que sean privilegiadas en comparación con aquellas que no tengan efectos significativos en la comunidad sobre la contención de la pandemia. Cabe aclarar que se trata, mayormente de una población de trabajadores cuyo desgaste se ha visto en todo el mundo como común denominador dentro del sector sanitario (27) (28) (29).
Otra característica de los resultados obtenidos es que aquellos municipios que pudieron participar del estudio cuentan con una población urbana que corresponde a ciudades pequeñas a medianas, características de la demografía de la provincia que no corresponde al Área Metropolitana de Buenos Aires (AMBA). Esta configuración urbana en la que la amplitud y la saturación de redes de transporte público, entre otros espacios de aglomeración, no son un factor que contribuye fuertemente a la transmisión viral, brinda las condiciones para que la identificación y seguimiento de los contactos estrechos de casos confirmados sea eficaz. Esto está en contraposición con la frecuente circulación de personas en las redes de transporte público terrestre (trenes, colectivos) en forma intermunicipal e interjurisdiccional, fundamentalmente vinculada a la actividad laboral que se da en el AMBA.
Esto permitió también, en la dinámica de la pandemia, que la detección de brotes y la realización de acciones concretas que detienen o circunscriben las cadenas de contagios hayan tenido efectos en morigerar el crecimiento exponencial de casos en forma rápida.
La utilización de metodologías costosas en cuanto a tiempo, recurso humano y disponibilidad, en personas que deban igualmente continuar el aislamiento, disminuye la posibilidad de utilizarlas en quienes presenten síntomas y deban ser estudiados; además, se corre el riesgo de saturar la capacidad de los laboratorios en pos de brindar resultados que no son informativos. Esta situación, además de generar una demora en los resultados de los casos sospechosos que sí permiten tomar medidas que contribuyen a frenar la diseminación, contribuiría al agotamiento del personal de salud. Este aspecto no es menor, ya que el agotamiento emocional y físico del personal de salud informado en todo el mundo (30) (31) (32) no solo es una alarma a nivel de los individuos y su bienestar sino también en términos colectivos y de contención de la pandemia. La saturación del sistema con estrategias que no contribuyen de manera significativa a reducir el riesgo de propagación de la infección en la comunidad pueden aumentar este estado e incluso son contraproducentes en este contexto.
Resultaría en este caso una alta relación costo/beneficio en términos de fuerza de trabajo, independientemente de la baja eficiencia en la captación de nuevos casos y, especialmente, teniendo en cuenta que si la adherencia a las medidas de aislamiento por el período establecido en los protocolos vigentes es buena, el riesgo de contagios se ve disminuido (33) (34) (35) (36). En relación con esto último, de poder destinarse mayor cantidad de recursos a las tareas de seguimiento, su uso más racional comprendería el que apunte al cumplimiento y sensibilización sobre la importancia del aislamiento como medida más efectiva para cortar cadenas de contagio en la comunidad. No se evaluó en este estudio la contribución de esta estrategia para la detección temprana de casos en establecimientos de estancia prolongada o en poblaciones con mayor riesgo de desarrollar formas graves de la enfermedad y que podría tener implicancias en su abordaje terapéutico.
Según este estudio no resultaría efectivo por el costo, tiempo y logística requerida estudiar a contactos estrechos de casos confirmados con Ct mayores de 20 ciclos. En caso de ser estudiados luego del séptimo día del último contacto con el caso confirmado se recomienda usar RTqPCR o amplificación isotérmica.
El esfuerzo por parte de todo el sistema de salud pública para el testeo de contactos estrechos en la comunidad no contribuye significativamente a la contención de la pandemia. La obtención de resultados negativos en las pruebas de laboratorio, con un bajo poder predictivo, generan una preocupación adicional ya que los mismos tienen un efecto contraproducente en lograr el cumplimiento del plazo de dos semanas para el aislamiento de los contactos. Esto representa la posible multiplicación de conductas de riesgo en términos epidemiológicos y la ocurrencia de mayores daños que si no se interviniera, dada la dificultad que implica en el plano de la comunicación y la divulgación el dar cuenta de las limitaciones en la interpretación de las pruebas de laboratorio a la población general. Sobre esto último, se identifica un punto en el que se justifican los esfuerzos dentro del conjunto de medidas de sensibilización que sí pueden tener impacto en la población para promover el autocuidado y los hábitos de higiene y distanciamiento.
Agradecimientos Los autores agradecen a los trabajadores de laboratorios de hospitales públicos y universidades que llevaron a cabo el estudio, realizaron la toma, el procesamiento de la muestra y la carga del resultado, así como también a los trabajadores de los Ce- Tec-19 que realizaron el seguimiento de casos y contactos.
Este trabajo no hubiera sido posible sin la participación activa de los municipios que trabajan de manera mancomunada con los hospitales públicos, las regiones sanitarias y los laboratorios. Un profundo agradecimiento a la UNAHUR, la Universidad de Buenos Aires, la Universidad Nacional de Quilmes e INTA por ser parte de la red pública de diagnóstico de COVID-19 de PBA y por haber aportado información y experimentos para este estudio.
La solidaridad, el compromiso y el deseo de generar conocimiento para mejorar la toma de decisiones en el contexto de emergencia del personal de salud y los trabajadores de la ciencia ha sido uno de los pilares fundamentales para la contención de la pandemia en la PBA. Desde hace meses los hospitales públicos y las universidades nacionales responden a cada necesidad de generación de conocimiento sumándose una tarea más por el bienestar del pueblo a pesar del cansancio acumulado.
Fuentes de financiación
El presente trabajo fue realizado sin haberse recibido una financiación específica.
Conflictos de intereses
Los autores declaran no tener conflictos de intereses respecto del presente trabajo.
Correspondencia
Lic. MARINA PIFANO
Ministerio de Salud de la Provincia de Buenos Aires
Correo electrónico:marinapifano@gmail.com
Referencias bibliográficas
1. Kim J, Chen X, Bidokhti SS, Sarkar S. Tracing and testing the COVID-19 contact chain: cost-benefit tradeoffs. medRxiv. 2020 Oct. doi: https://doi.org/10.1101/2020 .10.01.20205047.
2. Schuetz AN, Hemarajata P, Mehta N, Campbell S, Mitchell S, Palavecino E, et al. When should asymptomatic persons be tested for COVID-19? J Clin Microbiol 2020 Dec 17; 59 (1): e02563-20.
3. Tan JK, Leong D, Munusamy H, Ariffin NH Z, Kori N, Hod R, et al. The prevalence and clinical significance of presymptomatic COVID-19 patients: how we can be one step ahead in mitigating a deadly pandemic. BMC Infect Dis 2021 Mar 9; 21 (1): 249.
4. Johansson MA, Quandelacy TM, Kada S, Prasad PV, Steele M, Brooks J, et al. SARS-CoV-2 transmission from people without COVID-19 symptoms. JAMA Netw Open 2021 Jan; 4 (1): e2035057.
5. Corman VM, Landt O, Kaiser M, Molenkamp R, Meijer A, Chu DK, et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveill 2020 Jan; 25 (3): 2000045.
6. Long C, Xu H, Shen Q, Zhang X, Fan B, Wang C, et al. Diagnosis of the coronavirus disease (COVID-19): rRTPCR or CT? Eur J Radiol 2020 May; 126: 108961.
7. Kucirka L, Lauer S, Laeyendecker O, Boon D, Lessler J. Variation in false negative rate of reverse transcriptase polymerase chain reaction-based SARS-CoV-2 tests by time since exposure. Ann Intern Med 2020 Aug 18; 173 (4): 262-7.
8. Vashist SK. In vitro diagnostic assays for COVID-19: recent advances and emerging trends. Diagnostics (Basel) 2020 Apr 5; 10 (4): 202.
9. He X, Lau EH, Wu P, Deng X, Wang J, Hao X, et al. Temporal dynamics in viral shedding and transmissibility of COVID-19. Nat Med 2020; 26 (5): 672-5.
10. Wölfel R, Corman VM, Guggemos W, Seilmaier M, Zange S, Müller MA, et al. Virological assessment of hospitalized patients with COVID-2019. Nature 2020; 581 (7809): 465-9.
11. Weiss AM, Jellingso M, Sommer MOA. Spatial and temporal dynamics of SARS-CoV-2 in COVID-19 patients: a systematic review and meta-analysis. EBioMedicine 2020; 58: 102916.
12. Sethuraman N, Jeremiah SS, Ryo A. Interpreting diagnostic tests for SARS-CoV-2. JAMA 2020 Jun 9; 323 (22): 2249-51.
13. Zou L, Ruan F, Huang M, Liang L, Huang H, Hong Z, et al. SARS-CoV-2 viral load in upper respiratory specimens of infected patients. N Engl J Med 2020; 382 (12): 1177-9.
14. Wang Y, Zhang L, Sang L, Ye F, Ruan S, Zhong B, et al., Kinetics of viral load and antibody response in relation to COVID-19 severity. J Clin Invest 2020 Oct 1; 130 (10): 5235-44.
15. Ministerio de Salud de la Nación. Consenso sobre el uso de pruebas diagnósticas para SARS-CoV-2, Ministerio de Salud de la Nación, Argentina, 23 de septiembre 2020. Disponible en: https://bancos.salud.gob.ar/recurso/ consenso-sobre-el-uso-de-pruebas-diagnosticas-para- sars-cov-2. (Fecha de acceso: 27 de abril de 2021).
16. Cevik M, Tate M, Lloyd O, Maraolo AE, Schafers J, Ho A. SARS-CoV-2, SARS-CoV-1 and MERS-CoV viral load dynamics, duration of viral shedding and infectiousness: a living systematic review and meta-analysis. Lancet Microbe 2021 Jan; 2 (1): e13-22.
17. Hasanoglu I, Korukluoglu G, Asilturk D, Cosgun Y, Kalem AK, Altas AB, et al. Higher viral loads in asymptomatic COVID-19 patients might be the invisible part of the iceberg. Infection 2021 Feb; 49 (1): 117-26.
18. Datta R, Yadav AK, Singh A, Datta K, Bansal A. The infodemics of COVID-19 amongst healthcare professionals in India. Med J Armed Forces India 2020 Jul; 76 (3): 276-83.
19. Coronavirus COVID-19. Información y recomendaciones del Ministerio de Salud. Disponible en: https://www.argentina. gob.ar/noticias/reactivos-covid-19 y https://www. argentina.gob.ar/anmat/covid-19-acciones-regulatoriasde- anmat. (Fecha de acceso: 27 de abril de 2021).
20. Biotech. DisCoVery SARS-CoV-2 RT-PCR Detection Kit Rox. Disponible en: https://apbiotech.com.ar/pub/ media/Content/Datasheet/APB-COV19R2ROX.pdf? v=20210111142935. (Fecha de acceso: 27 de abril de 2021).
21. Bi Q, Wu Y, Mei S, Ye C, Zou X, Zhang Z, et al. Epidemiology and transmission of COVID-19 in 391 cases and 1286 of their close contacts in Shenzhen, China: a retrospective cohort study. Lancet Infect Dis 2020; 20 (8): 911-9.
22. Protocolo de preparación para la respuesta ante la contingencia de Enfermedad por coronavirus 2019 (COVID- 19), Ministerio de Salud de la Provincia de Buenos Aires, Septiembre 2020, Argentina. Disponible en: https://portal-coronavirus.gba.gob.ar/docs/protocolo/ Protocolo%20COVID-19.pdf. (Fecha de acceso: 2 de julio de 2021).
23. Corman VM, Landt O, Kaiser M, Molenkamp R, Meijer A, Chu DK, et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Eurosurveillance 2020; 25 (3): 2000045.
24. Kawasuji H, Takegoshi Y, Kaneda M, Ueno A, Miyajima Y, Kawago K, et al. Transmissibility of COVID-19 depends on the viral load around onset in adult and symptomatic patients. PLoS ONE 2020; 15 (12): e0243597.
25. Wölfel R, Corman VM, Guggemos W, Seilmaier M, Zange S, Müller MA, et al. Virological assessment of hospitalized patients with COVID-2019. Nature 2020; 581 (7809): 465-9.
26. Kleiboeker S, Cowden S, Grantham J, Nutt J, Tyler A, Berg A, et al. SARS-CoV-2 viral load assessment in respiratory samples. J Clin Virol 2020 Aug; 129: 104439.
27. Johnson SU, Ebrahimi OV, Hoffart A. PTSD symptoms among health workers and public service providers during the COVID-19 outbreak. PLoS One 2020; 15 (10): e0241032.
28. Luceño-Moreno L, Talavera-Velasco B, García-Albuerne Y, Martín-García J. Symptoms of posttraumatic stress, anxiety, depression, levels of resilience and burnout in Spanish health personnel during the COVID-19 pandemic. Int J Environ Res Public Health 2020 Jul 30; 17 (15): 5514.
29. Khasne R, Dhakulkar BS, Mahajan HC, Kulkarni AP. Burnout among healthcare workers during COVID-19 pandemic in India: results of a questionnaire-based survey. Indian J Crit Care Med 2020 Aug; 24 (8): 664-71.
30. Silva-Gomes RN, Silva-Gomes VT. Pandemia de la COVID- 19: síndrome de burnout en profesionales sanitarios que trabajan en hospitales de campaña en Brasil. Enferm Clin Mar-Apr 2021; 31 (2): 128-9.
31. Salazar de Pablo G, Vaquerizo-Serrano J, Catalan A, Arango C, Moreno C, Ferre F, et al. Impact of coronavirus syndromes on physical and mental health of health care workers: systematic review and meta-analysis. J Affect Disord 2020 Oct 1; 275: 48-57.
32. Que J, Shi L, Deng J, Liu J, Zhang L, Wu S, et al. Psychological impact of the COVID-19 pandemic on healthcare workers: a cross-sectional study in China. Gen Psychiatr 2020 Jun; 33 (3): 1-12.
33. Hellewell J, Abbott S, Gimma A, Bosse NI, Jarvis CI, Russell TW, et al. Feasibility of controlling COVID-19 outbreaks by isolation of cases and contacts. Lancet Glob Health 2020 Apr; 8, e488-96.
34. MacIntyre CR. Case isolation, contact tracing, and physical distancing are pillars of COVID-19 pandemic control, not optional choices. Lancet Infect Dis 2020; 20 (10): 1105-6.
35. Salathé M, Althaus CL, Neher R, Stringhini S, Hodcroft E, Fellay J, et al. COVID-19 epidemic in Switzerland: on the importance of testing, contact tracing and isolation. Swiss Med Wkly 2020 Mar 19; 150: w20225.
36. Kretzschmar ME, Rozhnova G, Bootsma MC, van Boven M, van de Wijgert JH, Bonten MJ. Impact of delays on effectiveness of contact tracing strategies for COVID-19: a modelling study. Lancet Pub Health 2020; 5 (8): e452-9.
Notas de autor
Lic. MARINA PIFANO Ministerio de Salud de la Provincia de Buenos Aires Correo electrónico:marinapifano@gmail.com
