Resumen: El síndrome de quilomicronemia familiar (SQF) es un trastorno caracterizado por hipertrigliceridemias severas (HTGs) originado por mutaciones en cinco genes canónicos, principalmente el de la lipoproteína lipasa (LPL). Los scores para identificar SQF presentan inconsistencias con resultados genéticos y la medición de actividad de LPL sería una herramienta diagnóstica complementaria que necesitaría estandarización de metodologías y valores de referencia (VR). El objetivo fue revisar la literatura sobre la actividad de LPL en SQF integrando hallazgos propios; en pacientes con HTGs, identificar SQF y distinguirlo de formas multifactoriales (SQM), mediante la actividad de LPL, utilizando un método de referencia y VR establecidos en este laboratorio. Se evaluaron 10 pacientes con HTGs, se los clasificó como muy probable (≥10), improbable (≤9) y muy improbable (≤8) SQF, según el score de Molin. En 22 controles normotrigliceridémicos se determinó el VR de actividad de LPL. Se midió actividad enzimática en plasma posinyección de heparina, con y sin activadores enzimáticos, y se realizaron análisis genéticos en saliva. El VR para actividad de LPL fue 33,3 (18,7-70,3) mUI utilizando el valor de 6,6 mUI (20% del VR) como criterio diferencial entre SQF y SQM. De siete pacientes con score de Moulin ≥10, cuatro presentaron genética incompatible con SQF, de los cuales dos presentaron actividad de LPL <20% y dos actividad >30%. En pacientes con score de Moulin <10 y diagnóstico genético no concluyente, la actividad de LPL fue >20%. La actividad de LPL podría diferenciar SQF y SQM, especialmente en casos sin confirmación genética; esto resalta la importancia de un laboratorio especializado.
Palabras clave: Lipoproteína lipasa, Hiperquilomicronemia, Pancreatitis.
Abstract: Familial chylomicronemia syndrome (FCS) is a disorder characterised by severe hypertriglyceridemia (HTG), caused by mutations in five canonical genes, primarily the lipoprotein lipase (LPL) gene. Scores used to identify FCS show inconsistencies with genetic results, and measuring LPL activity could be a complementary diagnostic tool, requiring standardised methodologies and reference values (RV). The objective of this work was to review the literature on LPL activity in FCS, integrating our findings. In patients with HTG, it was to identify FCS and distinguish it from multifactorial forms (MCS) by measuring LPL activity using a reference method and RV established in our laboratory. Ten patients with HTG were evaluated and classified as very likely (≥10), unlikely (≤9), and very unlikely (≤8) for FCS according to the Moulin score. In 22 normotriglyceridemic controls, the RV for LPL activity was determined. Enzymatic activity in plasma post-heparin injection, with and without enzymatic activators, was measured, and genetic analyses were performed using saliva samples.The RV for LPL activity was 33.3 (18.7–70.3) mUI, with 6.6 mUI (20% of RV) used as a differential criterion between FCS and MCS. Of seven patients with Moulin scores ≥10, four had genetic findings incompatible with FCS. Among these, two showed LPL activity >20%, and two had activity >30%. In patients with Moulin scores <10 and inconclusive genetic diagnoses, LPL activity was >20%. LPL activity could differentiate FCS from MCS, particularly in cases without genetic confirmation, highlighting the importance of specialised laboratory analysis.
Keywords: Lipoprotein lipase, Hyperchylomicronemia, Pancreatitis.
Resumo: A síndrome de quilomicronemia familiar (SQF) é um distúrbio caracterizado por hipertrigliceridemias graves (HTGs), originado por mutações em cinco genes canônicos, principalmente o da lipoproteína lipase (LPL). Os escores para identificar SQF apresentam inconsistências com resultados genéticos, e a medição da atividade de LPL seria uma ferramenta diagnóstica complementar, necessitando padronização de metodologias e valores de referência (VR). O objetivo foi revisar a literatura sobre a atividade de LPL em SQF, integrando achados próprios. Em pacientes com HTGs, identificar SQF e distingui-la de formas multifatoriais (SQM) por meio da atividade de LPL, utilizando um método de referência e VR estabelecidos em nosso laboratório. Foram avaliados 10 pacientes com HTGs, classificando-os como muito provável (≥10), improvável (≤9) e muito improvável (≤8) SQF, segundo o escore de Moulin. Em 22 controles normotrigliceridêmicos, determinou-se o VR da atividade de LPL. Foram avaliados a atividade enzimática no plasma após injeção de heparina, com e sem ativadores enzimáticos, e se realizaram análises genéticas em saliva. O VR para atividade de LPL foi 33,3 (18,7-70,3) mUI, utilizando o valor de 6,6 mUI (20% do VR) como critério diferencial entre SQF e SQM. De sete pacientes com escore Moulin ≥10, quatro apresentaram genética incompatível com SQF; dos quai dos deles tinham atividade de LPL <20% e dois atividade, >30%. Em pacientes com escore Moulin <10 e diagnóstico genético inconclusivo, a atividade de LPL foi >20%. A atividade de LPL pode diferenciar SQF e SQM, especialmente em casos sem confirmação genética, ressaltando a importância de um laboratório especializado.
Palavras-chave: Lipoproteína lipase, Hiperquilomicronemia, Pancreatite.
BIOQUÍMICA CLÍNICA
Síndrome de quilomicronemia familiar: informe de casos e importancia del laboratorio de bioquímica clínica para su diagnóstico
Familial chylomicronaemia syndrome: case reports and the importance of the clinical biochemistry laboratory for diagnosis
Síndrome de quilomicronemia familiar: relatos de casos e importância do laboratório de bioquímica clínica para o seu diagnóstico
Federación Bioquímica de la Provincia de Buenos Aires
Recepción: 20 Diciembre 2024
Aprobación: 28 Enero 2025
El síndrome de quilomicronemia familiar (SQF) es un desorden hereditario autosómico recesivo muy poco frecuente (1-3 pacientes en 1 000 000 de habitantes) que se caracteriza por hipertrigliceridemia severa (HTGs), consecuencia de un déficit del catabolismo de las lipoproteínas de síntesis intestinal, los quilomicrones (Qm) y su consiguiente acumulación en plasma (1).
La principal responsable del catabolismo de los Qm es la enzima lipoproteína lipasa (LPL), que hidroliza los triglicéridos (TG) contenidos en el Qm y genera ácidos grasos libres. Si bien la LPL también degrada los TG provenientes de la síntesis endógena transportados por la lipoproteína de muy baja densidad (VLDL), el déficit de actividad de LPL afecta en primer lugar el catabolismo de los Qm (2). La acumulación de estas partículas grandes y cargadas de TG en la circulación origina, además de la presencia de suero lechoso en los pacientes portadores de esta enfermedad, manifestaciones clínicas características como xantomas eruptivos en tronco y extremidades, lipemia retinalis, dolor abdominal recurrente, hepatoesplenomegalia y pancreatitis aguda o recurrente, y esta última es la mayor causa de morbimortalidad en los pacientes (3).
La actividad de la LPL depende no solo de la correcta expresión del gen que la codifica, sino también de diversos activadores e inhibidores de su actividad. Entre los factores que regulan positivamente la expresión génica se encuentra la insulina y los receptores activados por proliferadores peroxisomales (PPAR), especialmente el gamma (PPARg). Sin embargo, la regulación postranscripcional, mediada por distintos activadores e inhibidores, es la más significativa. Hasta el momento se reconocen cuatro principales activadores, la apoproteína (apo) AV, la apoCII, el glicosilfosfatidilinositol anclado a la lipoproteína de alta densidad-proteína de unión 1 (GPIHBP1) y el factor 1 de maduración de lipasas (LMF1) (4). A su vez, dentro de los inhibidores se destacan la apoCIII y las proteínas similares a la angiopoyetina tipo 3 y 4 (ANGPTL 3 y 4) (5). Dada esta importante regulación postraduccional, la medición de las concentraciones de LPL no refleja completamente su actividad final (2) (6).
En la bibliografía publicada hasta el momento se informa que las alteraciones genéticas más frecuentes en el SQF son mutaciones con pérdida de función (LOF) en los genes LPL (60-80%), APOC2 (5%), APOA5 (10%), LMF-1 (1%) y GPIHBP1 (5%) (4). Sin embargo, estos datos proceden de estudios realizados sobre otras poblaciones, con escasa evaluación de la prevalencia de SQF o de las mutaciones más frecuentes en Latinoamérica (7) (8).
Es importante destacar que, aun realizando un estudio genético dirigido, en aproximadamente el 30% de los pacientes no se encuentra la variante causal, lo que dificulta el diagnóstico de SQF y su diferenciación de la otra causa genética de HTGs, el síndrome de quilomicronemia multifactorial (SQM) (9). Este último incluye pacientes con polimorfismos que afectan a genes involucrados en la síntesis o catabolismo de lipoproteínas ricas en TG (LRT), o pacientes que presentan heterocigosidad para alguno de los cinco genes canónicos del SQF (3). La evaluación de la actividad de LPL para confirmar la patogenicidad de nuevas variantes o genes aún no descriptos es crucial. Dada la dificultad que presenta el diagnóstico de esta patología, se han propuesto diferentes sistemas de puntuación que intentan identificar casos “probables, improbables o muy improbables”, entre los que se destacan los puntajes de Moulin (10), Brisson (11) y Campos (12). Si bien estos puntajes son indicativos, no son concluyentes y en algunos casos presentan resultados contradictorios con la genética. En este sentido, la medición de la actividad de LPL es una herramienta diagnóstica complementaria a un abordaje clínico-bioquímico-genético integral.
Los ensayos in vitro para la evaluación de la actividad de LPL en plasma posheparina (PPH) fueron desarrollados hace ya muchos años. Se trata de procedimientos manuales complejos, que emplean diferentes sustratos y métodos de detección, inhibidores de otras lipasas y dependen de la experiencia del laboratorio de diagnóstico (13). A pesar de estas limitaciones, estos métodos aún se consideran el estándar de oro para la evaluación de la actividad enzimática (14). Por lo tanto, dado que los valores de referencia dependen de la complejidad del método y de la diversidad de condiciones utilizadas, cada laboratorio debe establecer los propios, teniendo en cuenta que los intervalos de actividad normal de LPL no son necesariamente intercambiables. En este sentido, es importante destacar que, si se utiliza la actividad de LPL para el diagnóstico de SQF, es necesaria la estandarización de las metodologías y los valores de corte (15) (16). Además, es necesario resaltar que, dada la naturaleza, tanto de la muestra utilizada para medir la actividad de LPL como del ensayo manual utilizado, el número de individuos incluidos en el trabajo para la obtención del intervalo de referencia (IR) es relativamente pequeño, aunque ha sido contrastado y transferido con el IR obtenido hace varios años en este laboratorio.
El objetivo principal de este trabajo fue realizar una revisión de la literatura publicada en torno a la actividad de LPL en el SQF, enmarcada en los resultados obtenidos a través de la investigación propia. Se buscó analizar de manera crítica los estudios previos para contextualizar y contrastar hallazgos propios, identificando coincidencias, diferencias y posibles contribuciones al conocimiento existente. De esta manera, el trabajo no solo pretende resumir lo que ya se ha investigado, sino también aportar nuevas perspectivas y reflexiones a partir de resultados propios. Se pretende destacar también la capacidad de lograr el diagnóstico de la patología desde un laboratorio de referencia en Lípidos y Aterosclerosis en Bioquímica Clínica, incluyendo la medida de la actividad de LPL a partir de un método de referencia, y utilizando intervalos de referencia establecidos en este laboratorio, para poder así discriminar entre pacientes con SQF o SQM.
En este marco, se incluye como parte de investigaciones propias aún no publicadas el resultado de la evaluación de 10 sujetos con HTGs, la obtención del intervalo de referencia de actividad de LPL y la capacidad diagnóstica de la actividad enzimática del SQF en comparación con el resultado genético.
Se evaluaron 10 sujetos con HTGs (TG >880 mg/dL) y sospecha de SQF, previa verificación de la ausencia de causas secundarias de HTGs (p.ej. diabetes mellitus previa a la HTG, alcoholismo, enfermedad renal crónica, lipodistrofia, medicación hipertrigliceridemiante, etc.), que fueron derivados a este laboratorio por profesionales médicos de distintas regiones de la Argentina. Todos los pacientes presentaron estudio genético dirigido a mutaciones en los cinco genes canónicos (LPL, APOC2, APOA5, GPIHBP1 y LMF-1). Se calculó el score de Moulin, como se ha publicado (10), a partir del cual se clasificaron los pacientes como muy probable SQF (score de Moulin ≥10), improbable (score de Moulin ≤9) y muy improbable SQF (score de Moulin ≤8).
Un grupo de 22 sujetos adultos sanos y normotrigliceridémicos (NTG) (33±5 años, 68% hombres) fueron reclutados como grupo control para determinar el intervalo de referencia de actividad de LPL posheparina. Todos los participantes asistieron al Laboratorio de Lípidos y Aterosclerosis del Hospital de Clínicas José de San Martín entre diciembre de 2021 y diciembre de 2022 y se evaluaron los factores de riesgo personales y familiares mediante cuestionarios de autorreporte.
A los controles NTG se les aplicaron los siguientes criterios de exclusión: consumo de alcohol >20 g/día, antecedentes personales o familiares de diabetes, sobrepeso u obesidad, enfermedades cardiovasculares (ECV), hipotiroidismo, antecedentes recientes de enfermedades agudas, trastornos renales, hepatitis B o C seropositivas u otros trastornos endocrinos como ovarios poliquísticos. Ninguno de los sujetos control recibió corticosteroides, terapias hormonales, agentes inmunosupresores o fármacos que influyeran en el metabolismo lipídico, como estatinas o fibratos.
Se obtuvo el consentimiento escrito de todos los participantes incluidos en el estudio, que fue aprobado por Comités de Ética de la Facultad de Farmacia y Bioquímica de la Universidad de Buenos Aires.
Después de un ayuno 12 h se extrajeron muestras de sangre previas a la inyección de heparina. En suero se evaluó colesterol total, TG y ApoB. Para medir la actividad de LPL se administró heparina (60 UI/kg de peso corporal) por vía intravenosa. Después de 10 minutos se recogió sangre del brazo contralateral en tubos sobre hielo. El plasma posheparínico (PPH) se obtuvo mediante centrifugación a 1500 g a 4 °C durante 10 minutos y se mantuvo a -70 °C hasta el análisis de actividad de LPL.
El colesterol total (C-total) y los TG se midieron utilizando kits enzimáticos comerciales (Mindray, China) en un autoanalizador Mindray BS360E [coeficiente de variación (CV) intraensayo 0,9 y 0,8% respectivamente, CV entre ensayos 1,4 y 1,6% respectivamente]. La ApoB sérica se determinó mediante inmunoturbidimetría (Mindray, China) (CV intraensayo 1,5% y CV interensayo 2,4%).
La actividad de LPL se determinó en PPH midiendo el ácido oleico producido por la hidrólisis catalizada por enzimas de una emulsión que contenía trioleína [9,10-3H(N)] (ARC ART-199, 1 mCi/mL) y trioleína sin marcar (Sigma T-7140) (concentración final 1,3 mmol/mL de trioleato de glicerol, actividad específica 10 x 106cpm/mmol), mezclada con 0,11 mmol/mL de L-lisofosfatidilcolina (Sigma L- 4129) y albúmina sérica bovina al 4% (Sigma A-6003), según un método modificado de Nilsson-Ehle (17) (18). Esta mezcla se sonicó (6 ciclos de 30 segundos) en un sonicador Vibra-cell en buffer Tris-HCl 0,2 M pH 8,0 con NaCl 0,3 M y ésta se constituyó en el sustrato para la determinación de la actividad de LPL. En paralelo se prepararon dos sustratos, uno con solución fisiológica y otro con el agregado de 10% v/v de suero humano normolipémico (suero activador, SA) inactivado a 56 °C durante 30 minutos, como fuente exógena de cofactores enzimáticos como apoCII y apoAV. Este último se estableció como un ensayo funcional in vitro para descartar ausencia de cofactores. Ambos sustratos se incubaron en paralelo con el PPH en solución salina 1:10 para determinar la actividad lipolítica total y simultáneamente con PPH en solución salina 1:5 y NaCl 1M (como inhibidor de LPL) durante 45 minutos a 37 °C. Después de la incubación, la reacción se detuvo en hielo y los ácidos grasos liberados se aislaron mediante extracción con una mezcla de metanol/cloroformo/heptano (1,45:1,25:1 en volumen) y buffer carbonato-borato, pH 10,5. Los ácidos grasos tritiados liberados se cuantificaron en un analizador de centelleo líquido (HIDEX 300 SL). La actividad LPL de cada individuo se calculó a partir de la diferencia entre la actividad total y la actividad medida en presencia de NaCl 1 M. La actividad enzimática se expresó en miliunidades internacionales (mUI, como 1 UI = 1 μmol de ácido graso liberado por minuto) por mL de PPH.
En los casos de pacientes con sospecha de SQF se realizó la toma de muestra de saliva y su derivación a Laboratorios Bitgenia para el posterior análisis de los cinco genes canónicos (LPL, APOC2, APOA5, GPIHBP1, LMF-1, APOE) cumpliendo con los requisitos de calidad preanalítica para la conservación de la muestra. Luego de superar satisfactoriamente los controles de calidad, se procedió a realizar la preparación de la biblioteca siguiendo el protocolo basado en enriquecimiento por captura (library construction, kit SureSelect XT V6-Agilent). Posteriormente se procedió a realizar la secuenciación por síntesis paired-end utilizando la plataforma NovaSeq Sequencing System (Illumina). El procedimiento de mapeo, alineamiento y llamado de variantes fue realizado utilizando el genoma humano de referencia GRCh38, mediante un protocolo desarrollado en Bitgenia, basado en las buenas prácticas establecidas por el Broad Institute (Eli and Edythe L. Broad Institute of Harvard and MIT). El análisis del archivo de variantes (VCF) se realizó mediante el software B-platform. Las variantes se identificaron siguiendo las recomendaciones de nomenclatura de la HGVS (19). La interpretación del impacto de las mismas se realizó en el contexto del transcripto clínicamente relevante (MANE SELECT).
El análisis se enfocó en la secuencia codificante de dichos transcriptos, 20pb flanqueantes a los extremos de los exones (sobre los intrones) y otras regiones genómicas específicas que se hayan demostrado que son causantes de enfermedad al momento del diseño del ensayo. Promotores, regiones no traducidas (UTR) y demás regiones no codificantes no fueron analizadas. Teniendo en cuenta el diagnóstico clínico y el modelo de enfermedad propuesto se priorizaron variantes utilizando la información disponible en bases de datos (como GnomAD, ClinVar, OMIM, PubMed, LOVD, dbSNP, NCBI Genome, RefSeqGene, entre otros). Las variantes priorizadas fueron clasificadas según la guía internacional de ACMG/AMP.
Se utilizaron pruebas estadísticas de Shapiro-Wilk para definir la distribución paramétrica o no paramétrica de los datos. Se informaron medidas de resumen de los datos según la distribución de los mismos. Las pruebas de comparación de medias se aplicaron de acuerdo con dicha distribución y se utilizaron tests paramétricos (test t de Student) o no paramétricos (test de Mann-Whitney) según correspondiera en cada caso. Se realizó la comparación de rangos de actividad de LPL utilizando la prueba de Mann-Whitney, dada la distribución no paramétrica de los datos. Se consideró como de significación estadística a un valor de p<0,05. Se utilizaron los programas SPSS.19 y GraphPad Prism 8.01.
Los intervalos de referencia de la actividad de LPL en este laboratorio se obtuvieron a partir del grupo NTG. En la Figura 1 se observa que la actividad de la enzima no varía con el agregado de suero humano normal, por lo que se estableció un valor de referencia único independiente del agregado de cofactores.
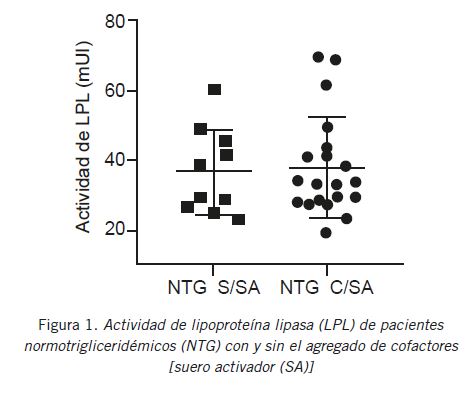
Figura 1
En la Tabla I se describen los estadísticos del valor de referencia; el CV intraensayo fue 5,1%, en tanto que el CV interensayo, calculado a partir de la repetición de una misma muestra en 20 ensayos sucesivos fue 13,2%. El valor de actividad correspondiente al 20% de la mediana de los NTG fue de 6,6 mUI, valor que permite la diferenciación entre SQF y SQM (4).
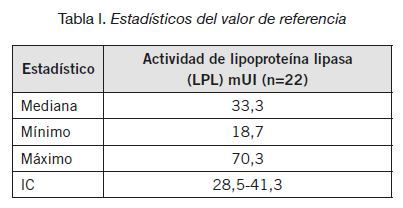
Tabla I
En la Tabla II A se describen las características clínicas y el perfil lipídico lipoproteico de los 10 pacientes; a partir de estos datos se estimaron los índices ApoB/TG y TG/colesterol total. En la Tabla II B se muestra el score de Moulin, el máximo valor de TG, la actividad de LPL y el estudio genético. Todos los pacientes presentaron antecedentes de TG >880 mg/dL en una o varias oportunidades. Como puede verse, de los 10 pacientes, 7 presentaron un score de Moulin ≥10 y se consideró muy probable la presencia de SQF. Un paciente presentó score de Moulin ≤9 (SQF: improbable) y dos ≤8 (SQF: muy improbable). De los 7 pacientes con score ≥10, dos fueron doble heterocigotas para mutaciones sin sentido en APOA5 y LPL (# 7 y 8), y uno homocigota para una mutación sin sentido en APOA5 (# 9), en tanto que cuatro presentaron resultados del estudio genético incompatibles con SQF. En tres de estos últimos pacientes el gen afectado fue APOE (# 1, 5 y 10). El restante fue un aparente heterocigota para una mutación sin sentido en APOC2 (# 6).
Respecto de la actividad de LPL, en los tres casos confirmados de mutaciones compatibles con SQF (# 7, 8 y 9), la actividad de la enzima sin el agregado de SA se encontró por debajo del 25% del valor de la mediana del intervalo de referencia para NTG (Tabla II B). Por su parte, entre los 7 pacientes sin estudio genético concluyente se verificó que dos de ellos presentaron actividad <25% (# 5 con mutación en APOE, score Moulin 11 y # 6 heterocigota APOC2, score de Moulin 12), en tanto que otros 3 presentaron actividad superior al 30% en todos los casos (# 1, 2 y 3). A su vez, uno de los pacientes con score de Moulin <10 (# 4, con heterocigosis en APOA5) presentó actividad de LPL por debajo del 25% de la mediana del intervalo de referencia para NTG. En estos casos, el ensayo funcional con el agregado de suero activador confirmó un incremento de la actividad in vitro de LPL, lo que destaca cómo el agregado exógeno del cofactor afectado incrementa la actividad de la enzima (Fig. 2). En aquellos pacientes con score de Moulin <10 y diagnóstico genético no concluyente la actividad de LPL fue >25% de la mediana del intervalo de referencia para NTG, lo que confirmó la presencia de SQM. En los pacientes con resultado genético dudoso, la presencia de actividad de LPL <25% de dicha mediana se utilizó como confirmación de SQF.
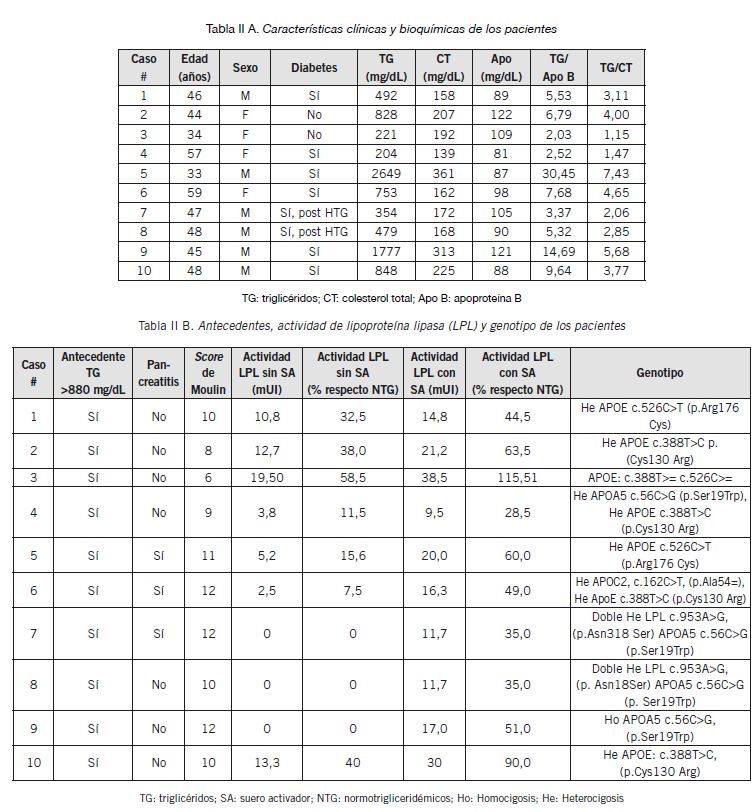
Tabla II A y II B
El SQF es una enfermedad rara descripta hace muchos años, que permaneció huérfana de tratamiento hasta 2014 (20). Esta característica, junto con la complejidad metodológica para la medida de la actividad de LPL y el poco conocimiento de sus reguladores, condicionó durante mucho tiempo el diagnóstico de la enfermedad y su diferenciación del SQM. Los pacientes portadores suelen sufrir un deterioro en su calidad de vida, con posibilidad de desarrollar pancreatitis a repetición y consultas sucesivas con distintos profesionales médicos (21).
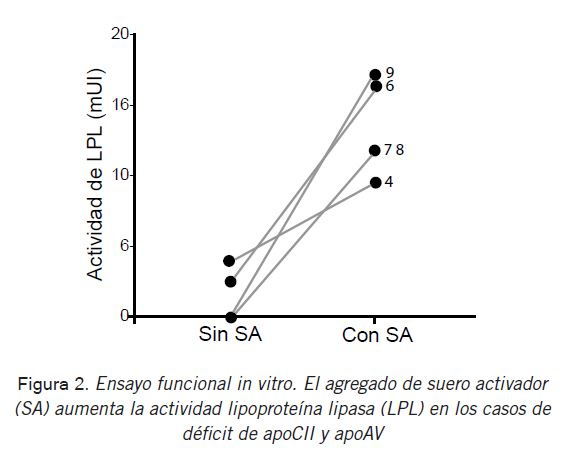
Figura 2
A partir de la sospecha clínica, el diagnóstico de certeza lo brinda un análisis genético confirmatorio de mutaciones homocigotas o dobles heterocigotas para los cinco genes canónicos, si bien el uso de la genética como única herramienta diagnóstica nos impone una visión parcial del SQF (22). En este sentido, en muchos pacientes el resultado genético no es concluyente aún con un score de Moulin que indique SQF muy probable. Además, en el estudio APPROACH, el 21% de los pacientes no tenía variantes genéticas definidas, pero fueron reclutados por su fenotipo clínico y una actividad de LPL por debajo del 20% de su población normal (23). En esos casos, la medición de la actividad de LPL surge como una herramienta diagnóstica certera y con mayor precisión (22), si bien los métodos para su medida suelen ser difíciles de estandarizar dada la alta heterogeneidad que existe entre técnicas y laboratorios. Esto destaca la necesidad de validar el ensayo y establecer valores de referencia propios para individuos NTG a partir de los cuales es posible establecer un porcentaje de actividad que ayuda a completar el diagnóstico de SQF. Son pocos los laboratorios a nivel mundial que realizan esta determinación, y el Laboratorio de Lípidos y Aterosclerosis de la Facultad de Farmacia y Bioquímica (Universidad de Buenos Aires) representa el único en América Latina. En este laboratorio, el valor de corte para diferenciar SQF de SQM con mayor sensibilidad y especificidad, corresponde al 25% de la mediana de actividad de LPL en sujetos NTG (8,42 mU/mL). El valor de corte sugerido previamente correspondiente al 20% de la mediana de la actividad LPL de NTG (23), en nuestro caso 6,26 mUI, presenta la misma sensibilidad, pero menor especificidad y, por tanto, menor valor predictivo negativo, por lo que su uso dejaría pacientes sin diagnosticar en esta población. Por ello, dada la heterogeneidad del ensayo de LPL, el valor de corte para diferenciar SQF de SQM también debería establecerse en cada laboratorio.
Cabe destacar que se ha evaluado la actividad de LPL y establecido su intervalo de referencia en un grupo de sujetos sanos, lo cual es más representativo de la práctica bioquímica, a diferencia de otros autores que utilizaron pacientes con SQM como grupo control (10). Además, utilizar el 25% de la actividad de LPL de la mediana del intervalo de referencia para NTG como punto de corte para diferenciar SQF de SQM, permite incluir a pacientes con HTGs en el tratamiento específico sin excluir a pacientes potenciales de SQF con actividad de LPL entre el 20 y el 25% de la mediana de actividad de los sujetos NTG.
El agregado de cofactores (apoCII y apoAV) en el ensayo funcional in vitro permite desenmascarar la falta de éstos. En el presente trabajo, en los controles NTG no hubo diferencias con y sin el agregado de cofactores, lo que permitió establecer un valor de actividad de LPL de referencia único. Sin embargo, en los casos de dos pacientes con mutaciones en APOC2 y APOA5, se verificó un aumento de actividad ante el agregado de cofactores y se observó que estos resultados coincidieron con el estudio genético, lo que indica que la deficiencia de activadores se traduce en un déficit de actividad de LPL y que este ensayo representa una validación in vitro de las mutaciones. Más aún, en uno de los pacientes el ensayo funcional demostró un aumento de actividad de LPL, sin identificación de mutación en ninguno de los genes relacionados a SQF, lo que permite sospechar mutaciones en genes aún no descriptos como involucrados en la regulación de la enzima.
En comparación con otros métodos utilizados para la medida de actividad de LPL, el que se utiliza en este laboratorio cuenta con vasto reconocimiento internacional y aún hoy demuestra fortalezas. En el método propuesto por Di Filippo et al. (16) se utiliza VLDL humana como sustrato. En este laboratorio se utiliza un sustrato preparado a partir de un triglicérido comercial (trioleína) con lo cual se reduce la variabilidad entre ensayos, dado que el uso de VLDL exige para cada ensayo el aislamiento de la lipoproteína a partir de plasma humano normal por ultracentrifugación. Por su parte, el método de Rioja et al. (15) utiliza una emulsión comercial (intralipid) que, si bien reduce la variabilidad introducida por la sonicación, también requiere el uso de tritio. Además, estos autores establecieron el valor de referencia a partir de pacientes con SQM, lo cual no es lo ideal desde el punto de vista clínico y no realizaron el ensayo funcional con el agregado de cofactores. Recientemente se ha descripto un método fluorométrico (14) que presenta la ventaja de no requerir el uso de material radioactivo. Este método ha sido validado frente a un método equivalente al utilizado en este laboratorio y su implementación requiere el agregado de un péptido sintético análogo a apoCII y otro análogo a ANGPTL4, por lo que el costo del ensayo se incrementa. De cualquier manera, el ensayo de Oldham et al. (14) es una alternativa interesante que amerita ser considerada en el futuro. En todos estos ensayos, ante un resultado de actividad nula no puede descartarse que la misma sea producto de la presencia de inhibidores o anticuerpos anti-LPL o anti-cofactores. La experiencia de estos autores en trabajos en tejido adiposo epicárdico humano demostró que la presencia incrementada de ANGPTL4 disminuye significativamente la actividad enzimática de LPL, mientras que el aumento en la concentración de activadores como el GPIHBP1 se asocia directamente a la actividad de LPL (6) (24). Por su parte, estados proinflamatorios también afectan la actividad de LPL, muchas veces a través del efecto de lípidos bioactivos como ceramidas (25); sin embargo, estos resultados ex vivo en tejidos no han demostrado ser causantes de HTGs como es el caso de los pacientes con SQF.
En esta revisión se presentan diez casos de pacientes con HTGs cuyo diagnóstico pudo complementarse con la medida de la actividad de la LPL. Cabe destacar que los casos estudiados confirman y amplían observaciones anteriores en otras cohortes, que generalmente informan que los pacientes con SQF presentan una edad más joven en el momento del diagnóstico, un IMC más bajo, un HDL-C plasmático más bajo y una prevalencia más alta de pancreatitis, en comparación con los pacientes con SQM (26).
En conjunto, los datos disponibles y la experiencia de los autores del presente trabajo demuestran que la medición de la actividad plasmática de LPL en pacientes con HTGs podría ser una herramienta de diagnóstico adicional para diferenciar SQF de SQM, especialmente en aquellos pacientes donde no se detectan mutaciones en los genes buscados. Esto también destaca el rol del laboratorio especializado de bioquímica clínica en el diagnóstico de esta patología rara, lo que así asegura el acceso al tratamiento (23) y mejora la calidad de vida de estos pacientes.
Fuentes de financiación
Los autores agradecen el apoyo de la Universidad de Buenos Aires, Argentina (UBACYT 20020190100033BA y 20020220200173BA) y de PTC Pharmaceutical Argentina. Las fuentes de financiación no participaron en el diseño del estudio, ni en la recopilación, análisis e interpretación de los datos, ni en la redacción del informe, ni en la decisión de enviar el artículo para su publicación.
Conflictos de intereses
Los autores declaran no tener conflictos de intereses respecto del presente trabajo.
Correspondencia
Dra. GABRIELA BERG
Correo electrónico: gaberg@ffyb.uba.ar
redalyc-journal-id: 535
gaberg@ffyb.uba.ar

Figura 1

Tabla I

Tabla II A y II B

Figura 2
