Dossiê
A Campanha Mundial de Erradicação da Febre Amarela da Fundação Rockefeller: um experimento de saúde global no período entre guerras (1918-1939)
The Rockefeller Foundation's World Yellow Fever Eradication Campaign: a global health experiment in the interwar period (1918-1939)
La Campaña Mundial de Erradicación de la Fiebre Amarilla de la Fundación Rockefeller: un experimento de salud global en el período de entreguerras (1918-1939)
A Campanha Mundial de Erradicação da Febre Amarela da Fundação Rockefeller: um experimento de saúde global no período entre guerras (1918-1939)
HISTÓRIA DEBATES E TENDÊNCIAS, vol. 21, núm. 3, pp. 99-117, 2021
Programa de Pós-Graduação em História da Universidade de Passo Fundo
Recepção: 30 Junho 2021
Aprovação: 30 Julho 2021
Publicado: 01 Setembro 2021
Resumo: A Campanha Mundial de Erradicação da Febre Amarela foi lançada pela Comissão de Saúde Internacional (CSI) da Fundação Rockefeller (FR) em 1918. Primeiro programa internacional de saúde destinado a eliminar uma doença em escala planetária, ela se constituiu em um experimento decisivo para testar os limites e possibilidades da saúde global. O objetivo deste trabalho é analisar a implementação da Campanha nas Américas e na África, destacando os principais pressupostos práticos e epidemiológicos que orientaram as suas atividades. O foco da análise também recairá sobre os intercâmbios médico-científicos mantidos entre os especialistas da FR, a produção de novos conhecimentos sobre a doença, bem como o impacto de alguns acontecimentos e descobertas que abalaram os pilares de sustentação da campanha e colocaram em xeque a sua continuidade.
Palavras-chave: Febre amarela, Fundação Rockefeller, Saúde global..
Abstract: The World Campaign to Eradicate Yellow Fever was launched by the International Health Commission (IHC) of the Rockefeller Foundation (RF) in 1918. The first international health program designed to eliminate a disease on a planetary scale, it constituted a decisive experiment to test the limits and possibilities of global health. The objective of this paper is to analyze the implementation of the Campaign in the Americas and Africa, highlighting the main practical and epidemiological assumptions that guided its activities. The focus of the analysis will also be on the medical-scientific exchanges maintained between RF specialists, the production of new knowledge about the disease, as well as the impact of some events and discoveries which shook the pillars of support of the campaign and put its continuity in check.
Keywords: Yellow fever, Rockefeller Foundation, Global health..
Resumen: La Campaña Mundial de Erradicación de la Fiebre Amarilla fue lanzada por la Comisión de Salud Internacional (CSI) de la Fundación Rockefeller (FR) en 1918. Primer programa de salud internacional diseñado para eliminar una enfermedad a escala planetaria, ella constituyó un experimento decisivo para probar la límites y posibilidades de la salud global. El objetivo de este trabajo es analizar la implementación de la Campaña en las Américas y África, destacando los principales supuestos prácticos y epidemiológicos que guiaron sus actividades. El foco del análisis también estará en los intercambios médico-científicos mantenidos entre especialistas en RF, la producción de nuevos conocimientos sobre la enfermedad, así como el impacto de algunos eventos y descubrimientos que sacudieron los pilares de apoyo de la campaña y puso en jaque su continuidad.
Palabras clave: Fiebre amarilla, Fundación Rockefeller, Salud global..
Introdução
A luta contra a febre amarela foi impulsionada em 1918, quando a Comissão de Saúde Internacional (CSI)i da Fundação Rockefeller (FR) lançou a Campanha Mundial de Erradicação da Febre Amarela, primeiro programa internacional de saúde destinado a eliminar uma doença em escala planetária. Durante as mais de duas décadas de seu desenvolvimento, ela se constituiu em um experimento decisivo para testar os limites e possibilidades da saúde global, evidenciando as suas origens periféricas nas primeiras décadas do século XX.ii
O objetivo do presente trabalho é analisar a implementação da Campanha Mundial de Erradicação da Febre Amarela, nas Américas e na África, destacando os principais pressupostos práticos e epidemiológicos que orientaram as suas atividades, os intercâmbios médico-científicos mantidos entre os especialistas da FR, que levaram à produção de novos conhecimentos sobre a doença, bem como o impacto de alguns acontecimentos e descobertas que abalaram os pilares de sustentação da campanha e colocaram em xeque a sua continuidade.
O lançamento da Campanha Mundial de Erradicação da Febre Amarela da FR
Na década de 1910, a presença endêmica da febre amarela nas Américas do Sul e Central representava um obstáculo para o comércio e um perigo permanente para o sul dos Estados Unidos. Em julho de 1914, então, o diretor da CSI, Wickliffe Rose, e o general William Gorgas, Cirurgião-Geral dos Estados Unidos, começaram a elaborar um programa mundial de erradicação da doença. Gorgas havia se notabilizado pela organização das campanhas contra a febre amarela em Havana, em 1901, na Zona do Canal do Panamá, entre 1912 e 1914, e defendia que a enfermidade podia ser eliminada do Hemisfério Ocidental (GORGAS, 1909). Rose, por sua vez, temia a disseminação do flagelo amarílico pelo extremo oriente após a abertura do Canal do Panamá, que seria inaugurado em agosto de 1914.iii Livres da doença até então, as regiões tropicais da Ásia reuniam todas as condições para uma epidemia, caso fossem ligadas às áreas infectadas do Caribe (CUETO, 1992).
Ainda em 1914, Gorgas e Rose se reuniram com notórios especialistas em febre amarela, como Henry Carter, cujas pesquisas epidemiológicas haviam contribuído para determinar o papel do mosquito na transmissão da doença, e Joseph White, responsável pela bem-sucedida campanha contra a enfermidade em Nova Orleans em 1905. Como resultado, em 1915 foi criada a Comissão de Febre Amarela, composta por Gorgas, Carter, White e por Juan Guiteras, diretor do Departamento de Saúde Pública de Cuba.iv
Lançada em 1918, a Campanha Mundial de Erradicação da Febre Amarela da FR estava embasada na teoria dos “focos-chave” (key focus theory), elaborada por Carter. De acordo com esta teoria, entre duas epidemias da doença, o seu agente etiológico continuava existindo em um número limitado de áreas endêmicas - os “focos-chave” - em geral cidades costeiras, nas quais o número de pessoas não imunes à febre amarela seria suficiente para garantir a sua transmissão de um indivíduo a outro através dos mosquitos. Acreditava-se, então, que a redução da população de mosquitos nos “focos-chave” a um índice inferior a 5% quebraria a cadeia de transmissão do vírus da febre amarela e levaria à erradicação da doença.v
A teoria dos “focos-chave” gerou um entendimento que a febre amarela era uma doença humana dos grandes centros urbanos, transmitida pelo Aedes aegypti, uma espécie doméstica que se reproduz em reservatórios artificiais de água. Tais ideias não eram compartilhadas pelos médicos latino-americanos, que defendiam que a febre amarela era endêmica nas áreas rurais do continente (FRANCO, 1969, p. 152-156).
Quando a Campanha teve início em Guaiaquil, no Equador, em novembro de 1918, contudo, todos os aspectos biomédicos da febre amarela “pareciam estar cientificamente equacionados” (CUETO, 1992, p. 2-3). As atividades consistiram em um ataque aos locais de reprodução do Aedes aegypti, com a colocação de peixes larvicidas nos reservatórios d’água, e na realização de inspeções regulares nas residências com objetivo de eliminar as larvas do mosquito em cisternas e em outros recipientes.vi O resultado foi considerado espetacular pelos dirigentes da FR (SAWYER, 1937, p. 40-41). Seis meses após o início da Campanha foi registrado o último caso da doença no país, o que parecia consagrar os princípios estabelecidos pela Comissão de Febre Amarela (CONNOR, 1920). Com a eliminação das larvas do vetor no foco-chave, o mosquito se extinguiu e a febre amarela desapareceu de maneira espontânea das cidades e localidades ao redor (BENCHIMOL, 2001, p. 7).
Com o sucesso alcançado em Guaiaquil, os norte-americanos começaram a atacar os outros focos-chave da doença no continente.vii Assim, as atividades da Campanha Mundial de Erradicação da Febre Amarela se expandiram para a Guatemala (1919), Peru (1920-1922) (CARTER, 1922; CUETO, 1992), América Central (1921-1922), México (1921-1923) (SOLORZANO, 1994; BIRN, 2006) e Colômbia (1923) (QUEVEDO et al., 2004, 2008).
Em 1923, a Campanha Mundial de Erradicação da Febre Amarela aportou no Brasil. Àquela altura, o país já tinha uma importante tradição de estudos e campanhas direcionados à doença que era, inclusive, a base do prestígio da medicina e da saúde pública brasileiras no continente. A ideia da FR era reproduzir no país as mesmas medidas de enfrentamento à febre amarela implementadas anteriormente em outros países das Américas, visando a obtenção de resultados semelhantes. Apesar dos atritos constantes com os médicos brasileiros, a campanha produziu resultados rápidos. Já em 1925, o número de casos da doença havia diminuído consideravelmente, desencadeando uma onda de otimismo acerca da iminência de sua erradicação. Para os dirigentes da FR, em breve a febre amarela já poderia ser declarada extinta do país e do continente e os esforços direcionados para a sua erradicação da África.
Descobertas na África, epidemia no Brasil e o fim das certezas sobre a febre amarela
Em paralelo às atividades desenvolvidas nas Américas, em junho de 1920 a FR organizou a primeira Comissão de Febre Amarela da África Ocidental. Os seus objetivos eram determinar se os casos notificados no continente eram de fato febre amarela, se a doença era a mesma encontrada no Hemisfério Ocidental e, em caso afirmativo, verificar se a adoção de medidas de controle já empregadas nas Américas era viável no continente africano.viii
Os integrantes da Comissão desembarcaram em Lagos, na Nigéria, em 17 de julho de 1920. A escolha recaiu sobre a cidade por ela ser a região com mais fácil comunicação com outros pontos do litoral e do interior do continente, o mais importante núcleo de população branca - considerada, então, mais suscetível à febre amarela - da África Ocidental Britânica, um centro de grande atividade comercial e, do ponto de vista epidemiológico, a localidade que mais importava a doença de outras regiões e a que melhor revelava o seu status no continente.ix
Os membros da Comissão não identificaram nenhum caso autêntico de febre amarela nos países que visitaram, embora tenham encontrado indícios de sua ocorrência nos três anos anteriores. Os resultados iniciais corroboravam a crença, bastante difundida na época, segundo a qual a febre amarela era originária do continente americano, de onde teria se propagado para outras partes do mundo. Dessa forma, o desaparecimento dos “focos-chave” nas Américas não apenas teria contido a disseminação da febre amarela no continente, como também sido o responsável por eliminá-la da costa ocidental da África (BENCHIMOL et al., 2009, p. 328).
Em 1925, foi formada uma segunda Comissão de Febre Amarela da África Ocidental. O seu objetivo era realizar uma investigação mais profunda sobre as características e a epidemiologia da doença na região, de modo a determinar a sua relação com a febre amarela encontrada nas Américas, isolar o seu agente etiológico, descobrir o mecanismo de transmissão e identificar as regiões do continente africano onde ela era endêmica (BENCHIMOL et al., 2009, p. 330-331). Para alcançar estas metas, nesse mesmo ano foi fundado um Laboratório de Febre Amarela em Lagos, na Nigéria, o primeiro do gênero criado pela FR (Figura 1).x

Figura 1
Laboratório de Febre Amarela de Lagos, na Nigéria (janeiro de 1933).
Fonte: Wilbur A. Sawyer Papers, NLM.
Em 1927, ocorreram duas epidemias de febre amarela na Costa do Ouro (atual Gana), o que possibilitou aos pesquisadores da FR obter amostras de sangue de vítimas da doença nos primeiros dias de contaminação. Um laboratório auxiliar, inclusive, foi criado na região, na cidade de Acra.xi Pouco tempo antes, Adrian Stokes, Johannes Bauer e Paul Hudson conseguiram infectar experimentalmente o macaco rhesus com o sangue de um africano de 28 anos, chamado Asibi, que sobrevivera à doença, (STRODE, 1951, p. 19). Com a domesticação do agente etiológico da febre amarela, em poucos meses os pesquisadores confirmaram que a doença era causada por um vírusxii ultramicroscópico e filtrável, capaz de ser transmitido entre os macacos e que podia ser transportado pelo Aedes aegypti (STOKES, BAUER, HUDSON, 1928a, 1928b). Faltava, no entanto, uma confirmação que o vírus que eles haviam conseguido transmitir de macaco para macaco e destes para os mosquitos era de fato o agente etiológico da febre amarela (BENCHIMOL et al., 2009, p. 339-340). Uma fatalidade confirmaria a transmissão da enfermidade do macaco rhesus para o homem através do mosquito. Em 19 de setembro de 1927, Stokes faleceu após contaminação acidental no laboratório pelo vírus da febre amarela.xiii A sua morte comprovou que a doença humana e aquela desenvolvida pelo macaco eram idênticas.xiv
No ano seguinte, Bauer descobriu que outras espécies do mosquito Aedes existentes no continente africano também podiam transmitir a doença, o que sugeria que a sua epidemiologia era bem mais complexa do que se acreditava (BAUER, 1928). Até então, a febre amarela era definida como uma doença urbana, transmitida pelo Aedes aegypti, que tinha o homem como o seu único hospedeiro vertebrado e que dependia de uma densa população de pessoas não imunes para a sua propagação. Tais conhecimentos sobre a doença, assentados nas Américas na passagem do século XIX para o XX, começaram a desabar na África, nos anos 1920, representando um duro golpe na Campanha Mundial de Erradicação da Febre Amarela da FR.
As descobertas realizadas no continente africano também contribuíram para que a FR iniciasse, a partir de 1927, um processo de reorganização interna, que conferiu à pesquisa científica um lugar de destaque e relegou a saúde pública ao segundo plano de suas atividades filantrópicas. No plano administrativo, a organização passou a contar com cinco divisões: Artes, Ciências Sociais, Ciências da Natureza, Ciências Médicas e a Divisão de Saúde Internacional (DSI). A nova orientação da FR se refletiu na criação, em 1928, de um Laboratório de Febre Amarela na Bahia, Brasil, que centralizaria as investigações sobre a doença na América do Sulxv e realizaria um intenso intercâmbio de pesquisas, amostras e dados com o Laboratório de Lagos, na Nigéria, contribuindo para um melhor entendimento acerca da epidemiologia da doença nos continentes africano e americano (Figura 2).xvi

Figura 2
Laboratório de Febre Amarela da FR na Bahia (junho de 1934).
Fonte: Wilbur A. Sawyer Papers, NLM.
Frederick F. Russell, que assumiu a direção da DSI no lugar de Rose, acreditava, no entanto, que os vírus da febre amarela da África e da América do Sul deveriam ser reunidos em um laboratório central - longe dos laboratórios de campo da Nigéria e do Brasil - e testados para imunidade cruzada. Em 1928 foi criado, então, nas dependências do Instituto Rockefeller, em Nova Iorque, o Laboratório Central de Febre Amarela da DSIxvii, sob a direção do médico norte-americano Wilbur Sawyer (Figura 3).xviii Em junho do mesmo ano, Sawyer, Wray Lloyd, Stuart Kitchen e Martin Frobisher Jr. iniciaram o perigoso trabalho de pesquisa sobre a doença.xix
Os pesquisadores do Laboratório Central de Febre Amarela da DSI coletaram três cepas do vírus da doença, duas africanas - o “Asibi” (enviado pela Comissão de Febre Amarela da África Ocidental) e o “francês” (obtido de um paciente no Instituto Pasteur de Dacar) - e uma da América do Sul, o “brasileiro”, enviado pelo Instituto Oswaldo Cruz (IOC). Já no primeiro ano de atividades do Laboratório, eles comprovaram, por meio de testes de imunidade cruzada, que as três cepas produziam anticorpos protetores no macaco rhesus, o que significava que os vírus eram idênticos ou, na pior das hipóteses, muito semelhantes (SAWYER et al., 1930).

Figura 3
Wilbur Sawyer no Laboratório de Febre Amarela da DSI, em Nova Iorque (maio de 1935).
Fonte: Wilbur A. Sawyer Papers, NLM.
Enquanto isso, no Brasil, país escolhido pela FR como palco final para a sua Campanha Mundial contra a doença, cada vez mais denúncias eram feitas sobre a existência de casos de febre amarela nas áreas rurais da Bahia e de Pernambuco. Acreditando, no entanto, que a FR tinha a situação sob controle, o Departamento Nacional de Saúde Pública (DNSP) vinha reduzindo as ações de combate ao Aedes aegypti no Rio de Janeiro, extinguindo-as por completo em janeiro de 1928 (WILLIAMS, 1994). As consequências não tardariam. Em maio desse ano, uma violenta epidemia de febre amarela se abateu sobre a cidade, onde o Aedes aegypti não era encontrado há vinte anos e sem que houvesse uma região endêmica próxima. Além da capital federal, a epidemia atingiu outras quarenta e três localidades do estado, deixando um rastro de mais de 800 casos e 436 mortes (FRAGA, 1928, 1930).
Controlada em 1929, a epidemia do Rio de Janeiro foi o ápice de um processo de desabamento das certezas sobre a febre amarela, iniciado com as descobertas realizadas no continente africano. Os eventos dramáticos do final da década de 1920, na África e no Brasil, puseram em xeque os principais conhecimentos epidemiológicos sobre a doença, bem como as teorias e práticas sobre a melhor forma de combatê-la, que sustentavam a Campanha Mundial de Erradicação da Febre Amarela da FR. Os anos 1930 assistiriam, então, a uma reorganização da Campanha, com base em novas descobertas e em renovados estudos sobre a doença. Esse processo ocorreu em grande medida no Brasil, país que desde 1923 concentrava as atividades da Campanha nas Américas e onde o combate à febre amarela entraria em um novo patamar.
Fred Soper e a reorganização da Campanha Mundial de Erradicação da Febre Amarela nos anos 1930
Em 1927, pouco antes da eclosão da epidemia, o médico norte-americano Fred Soperxx assumiu a chefia do Escritório Regional da FR, no Rio de Janeiro. Em junho de 1930, ele foi nomeado também inspetor-geral do recém-criado Serviço Cooperativo de Febre Amarela (SCFA)xxi, passando a comandar a campanha contra a doença no Brasil. Empossado no cargo, Soper expandiu as atividades antiamarílicas para as áreas rurais do país, estreitou os contatos com os médicos brasileiros e implementou uma completa reorganização administrativa do SCFA.xxii Entre 1930 e 1934, ele reestruturou por completo a campanha contra a febre amarela, estabelecendo uma coleta de dados mais detalhada das atividades de campo, um rígido controle dos supervisores sobre as atividades dos seus subordinados, uma rotina de aplicação de óleo em recipientes d’água e uma busca meticulosa por mosquitos adultos e larvas no interior das residências. O objetivo destas medidas era identificar com maior precisão os principais focos de febre amarela e combatê-los.xxiii
Duas novas técnicas laboratoriais favoreceram as medidas adotadas por Soper. Rapidamente incorporadas aos métodos de diagnóstico da febre amarela, elas aumentaram a visibilidade da doença e a precisão na identificação dos seus sintomas. A primeira delas foi a viscerotomia, que consistia na introdução de uma lâmina pontiaguda no fígado dos cadáveres para a retirada de uma amostra do órgão. A técnica permitia a confirmação laboratorial de que a morte ocorrera em decorrência da febre amarela, cujos sintomas eram semelhantes aos de outras enfermidades.xxiv As análises histopatológicas do fígado de vítimas fatais de febre amarela conferiam uma maior confiabilidade aos inquéritos sanitários e permitia a realização de um mapeamento da extensão da doença. Desse modo, a organização de serviços de viscerotomia, primeiro no Brasil e posteriormente em todo o continente, ajudou a preencher o mapa da febre amarela na América do Sul nos anos 1930.xxv
A segunda técnica laboratorial adotada com sucesso nos anos 1930 foi o desenvolvimento de um novo modelo animal da febre amarela. O responsável por esta realização foi Max Theiler, da Universidade de Harvard. Em suas pesquisas, ele observou que os camundongos desenvolviam encefalite quando o vírus da febre amarela era inoculado no seu cérebro e que a gravidade da doença aumentava a cada transferência de tecido cerebral infectado de um animal a outro. Para comprovar que a encefalite nos camundongos era causada pelo vírus, Theiler demonstrou que, ao misturá-lo com o soro de uma pessoa que havia sobrevivido à febre amarela e que, portanto, se tornou imune à doença, e injetá-lo no cérebro do animal, o vírus era neutralizado, imunizando camundongo contra a encefalite. Por outro lado, se fosse utilizado o soro de uma pessoa não imune à febre amarela, o animal desenvolvia a doença.xxvi
O novo modelo animal da febre amarela tornava mais fácil e econômica a sobrevivência do vírus em laboratório, possibilitando a realização de novas pesquisas sobre a doença. A descoberta viabilizou a elaboração de um teste de imunidade padronizado, capaz de revelar a presença de anticorpos neutralizantes contra a febre amarela nas pessoas. O teste de proteção em camundongos, como ficou conhecido, era realizado mediante a mistura do soro de pessoas que habitavam regiões onde casos de febre amarela tinham sido reportados com o vírus da doença e a sua inoculação no cérebro do animal. O não desenvolvimento de encefalite no camundongo significava que o doador do soro tinha contraído a febre amarela em algum momento e sobrevivido, adquirindo imunidade para a doença, pois o seu sangue apresentava anticorpos que haviam neutralizado o vírus transmitido ao animal. Sabia-se, então, que a febre amarela existia na região naquele momento ou tinha existido por lá em um passado recente. Esta importante ferramenta conferia, assim, uma maior visibilidade à doença, ao possibilitar que a sua presença fosse detectada em uma determinada localidade e que se mapeasse as regiões de maior incidência.xxvii
O novo contexto político-institucional do Brasil também favoreceu as atividades da FR e as novas estratégias implementadas por Soper no combate à febre amarela. A chegada de Getúlio Vargas ao poder, em 1930, assinalou o início de um processo de modernização e de aprofundamento da colaboração com os Estados Unidos, assim como a implementação de uma abordagem mais centralizadora da saúde pública (HOCHMAN, 2001; FONSECA, 2007). Tais elementos estavam em sintonia com a atuação dos norte-americanos (LOWY, 1999, p. 659). Assim, durante toda a década de 1930, o apoio irrestrito de Vargas possibilitou à FR intervir nos problemas sanitários do país em condições extremamente favoráveis (Figura 4). A aliança expressava tanto uma necessidade que a FR tinha de obter um rápido respaldo legal para o seu trabalho sanitário, quanto um esforço local para ampliar as políticas intervencionistas estatais que, em parte, embasavam a sua legitimidade no acesso a serviços de saúde pública (CUETO, 1996, p. 194-195). Nesse sentido, não havia exagero algum na afirmação de Soper de que “o Dr. Getúlio Vargas é o pai e a mãe do Serviço de Febre Amarela” (SOPER; DUFFY, 1977).

Figura 4
Fred Soper caminhando com Getúlio Vargas (16 de outubro de 1940).
Fonte: Fred L. Soper Papers, NLM.
Em 1932, contudo, eclodiu uma epidemia de febre amarela no Vale do Canaã, uma localidade do Espírito Santo onde o Aedes aegypti não havia sido encontrado anteriormente. Soper e os seus colaboradores viajaram até lá e observaram que praticamente todos os casos de “febre amarela sem Aedes aegypti” da região ocorreram em indivíduos que habitavam regiões próximas a florestas ou lá realizavam suas atividades (Figura 5). As pesquisas atestaram que o vírus da febre amarela tinha um reservatório natural em animais selvagens, que o Aedes aegypti não era o único vetor da doença no continente americano e que os seres humanos não eram os seus únicos hospedeiros vertebrados (SOPER et al., 1933).xxviii

Figura 5
Fred Soper e Alexander Burke investigando a febre amarela silvestre (Espírito Santo, 1934).
Fonte: Fred L. Soper Papers, NLM.
A descoberta da febre amarela silvestre modificou a percepção que se tinha da febre amarela que, de doença que vitimava exclusivamente o ser humano, passou a ser considerada uma enfermidade típica dos animais selvagens, que contaminava o homem de maneira acidental e cujas epidemias ocorriam porque o vírus podia ser facilmente transmitido por um mosquito que vivia nas proximidades das habitações humanas (LOWY, 2006, p. 173-174). Embora idênticas do ponto de vista clínico, a febre amarela silvestre e a urbana tinham uma diferença importante. Enquanto a modalidade urbana da doença era contraída no interior ou nas cercanias das casas e assentava-se no ciclo homem/Aedes aegypti /homem, a febre amarela silvestre era transmitida, geralmente, longe das residências e dependia de um ciclo de infecção no qual nem o ser humano nem o Aedes aegypti eram os elos mais importantes (BENCHIMOL, 2001, p. 148).
No plano da Campanha Mundial de Erradicação da Febre Amarela, a convicção de que o vírus da doença possuía um reservatório natural nos animais selvagens diminuiu o entusiasmo dos dirigentes da FR sobre a possibilidade de erradicá-la. As atividades foram então reorientadas, dividindo-se em duas frentes: o combate ao Aedes aegypti nas cidades e o controle do vírus nas regiões rurais onde a doença era endêmica, o que só poderia ser feito mediante a vacinação da população que habitava essas áreas. Neste contexto, ganharam impulso as pesquisas relacionadas à produção de uma vacina contra a febre amarela.xxix
Como resultado, em 1937, Max Theiler, Hugh Smith e outros pesquisadores do Laboratório Central de Febre Amarela da DSI, em Nova Iorque, desenvolveram um vírus atenuado e seguro da febre amarela, por meio da cepa 17D. Eles também criaram métodos para a produção da vacina em larga escala, tornando possível a organização de programas de vacinação em massa contra a doença.xxx Os primeiros testes de campo com a nova vacina ocorreram no Brasil em 1937.xxxi No ano seguinte, oitocentos mil brasileiros foram imunizados contra a febre amarela (Figura 6).xxxii Em meados de 1940, esse número havia subido para cerca de dois milhões (FRANCO, 1965). A vacina 17D foi rapidamente incorporada aos programas de combate à doença na América do Sul, passando a ser produzida nos Laboratórios de Febre Amarela do Rio de Janeiro e de Bogotá e distribuída para os demais países do continente (SOPER, 1939; BENCHIMOL, 2001, 2017).xxxiii
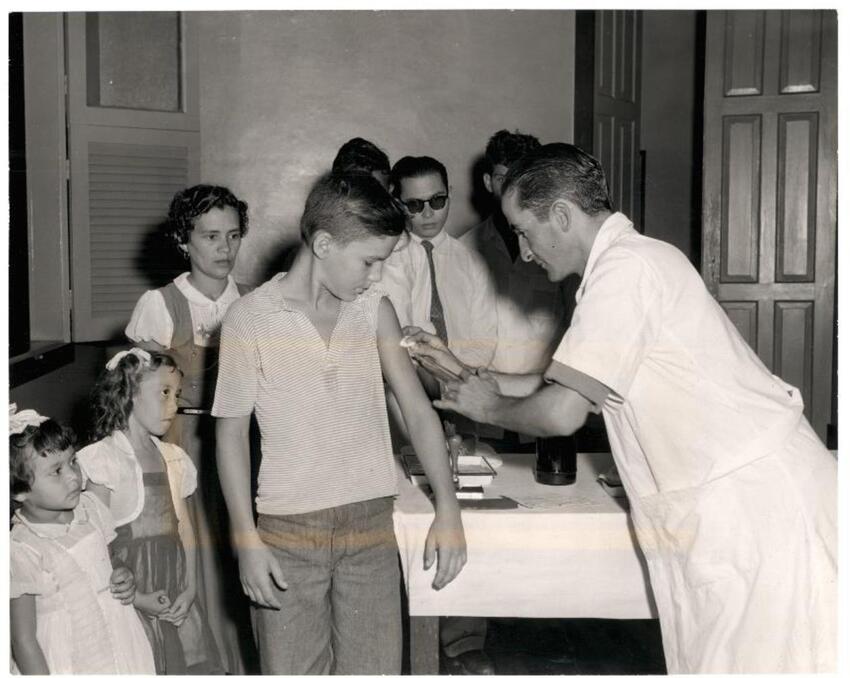
Figura 6
Vacinação contra a febre amarela em Belém, Pará, nos anos 1930.
Fonte: Fred L. Soper Papers, NLM.
Considerações finais
Com a descoberta da febre amarela silvestre e o advento da vacina 17D, o objetivo da Campanha Mundial de Erradicação da Febre Amarela da FR passou a ser a erradicação do Aedes aegypti, considerado o meio mais eficaz de evitar a eclosão de epidemias urbanas da doença. Nos anos da Segunda Guerra Mundial, Fred Soper comandaria campanhas de erradicação de vetores no Egito e na Itália, baseadas em sua experiência no Brasil e contando, inclusive, com o apoio de muitos especialistas brasileiros que recrutou para trabalhar com ele nesses países. Tais campanhas consolidaram a doutrina de erradicação dos vetores, que marcaria o campo da saúde global no pós-Segunda Guerra Mundial e da qual Soper se tornaria o principal defensor e expoente (FARLEY, 2004; STEPAN, 2011; MAGALHÃES, 2016).
Referências
BAUER, J. Transmission of Yellow Fever by mosquitoes other than Aedes aegypti. American Journal of Tropical Medicine, v. 8, n. 4, p. 261-282, jul. 1928.
BENCHIMOL, J. Febre Amarela: a doença e a vacina, uma história inacabada. Rio de Janeiro: Editora Fiocruz, 2001.
BENCHIMOL, J. et al. Cerejeiras e cafezais: relações médico-científicas entre Brasil e Japão e a saga de Hideyo Noguchi. Rio de Janeiro: Bom Texto, 2009.
BENCHIMOL, J. Yellow fever vaccine in Brazil: fighting a tropical scourge, modernizing the nation. In: HOLMBERG, C.; BLUME, S.; GREENOUGH, P. (Orgs.). The Politics of Vaccination: a Global History. Manchester: Manchester University Press, 2017. p. 174-208.
BIRN, A. Marriage of Convenience: Rockefeller International Health and Revolutionary Mexico. Rochester: University of Rochester Press, 2006.
BROWN, T.; CUETO, M.; FEE, E. A transição de saúde pública ‘internacional’ para ‘global’ e a Organização Mundial da Saúde. História, Ciência, Saúde - Manguinhos, Rio de Janeiro, v. 13, n. 3, p. 623-647, set. 2006.
CARTER, H. Yellow fever in Peru: epidemic of 1919 and 1920. American Journal of Tropical Medicine, v. 2, n. 2, p. 87-106, mar. 1922.
CONNOR, M. Yellow fever control in Ecuador: preliminary report. The Journal of the American Medical Association, v. 74, n. 10, p. 650-651, mar. 1920.
CUETO, M. Sanitation from above: yellow fever and foreign intervention in Peru, 1919-1922. Hispanic American Historical Review, v. 72, n. 1, p. 1-22, fev. 1992.
CUETO, M. Los ciclos de la erradicación: la Fundación Rockefeller y la salud pública latinoamericana (1918-1914). In: CUETO, M. (Org.). Salud, cultura y sociedad en America Latina: nuevas perspectivas historicas. Lima: IEP/OPS, 1996. p. 179-202.
CUETO, M. O valor da saúde: história da Organização Pan-Americana da Saúde. Rio de Janeiro: Editora Fiocruz, 2007.
CUETO, M. Saúde global: uma breve história. Rio de Janeiro: Editora Fiocruz, 2015.
CUETO, M. La Salud Global, la Salud Planetaria y los historiadores. Quinto Sol, v. 24, n. 3, p. 1-21, set.-dez. 2020.
FARLEY, J. To cast out disease: a history of the International Health Division of the Rockefeller Foundation (1913-1951). New York: Oxford University Press, 2004.
FONSECA, C. Saúde no governo Vargas (1930-1945): dualidade institucional de um bem público. Rio de Janeiro: Editora Fiocruz, 2007.
FRAGA, C. Sobre o surto epidêmico de febre amarela no Rio de Janeiro. Boletín de la Oficina Sanitaria Panamericana, v. 7, n. 12, p. 1535-1546, dez. 1928.
FRAGA, C. A febre amarella no Brasil: notas e documentos de uma grande campanha sanitária. Rio de Janeiro: Officina Graphica da Inspetoria de Demographia Sanitária, 1930.
FRANCO, O. Vacinação antiamarílica. Revista Brasileira de Malariologia e Doenças Tropicais, v. 17, n. 1, p. 75-81, 1965.
FRANCO, O. História da febre amarela no Brasil. Rio de Janeiro: Ministério da Saúde, Departamento Nacional de Endemias Rurais, 1969.
GORGAS, W. Sanitation of the tropics with specific reference to malaria and yellow fever. The Journal of American Medical Association, v. 52, n. 14, p. 1075-1077, abr. 1909.
HERNANDEZ TASCO, A. A construção de um modelo internacional de Saúde Pública: o programa dos laboratórios de febre amarela da Fundação Rockefeller nos Estados Unidos, América do Sul e África (1935-1950). 2016. Programa de Pós-Graduação em Política Científica e Tecnológica, Universidade Estadual de Campinas, Campinas, 2016. Disponível em: <http://www.repositorio.unicamp.br/handle/REPOSIP/321799>. Acesso em: 25 jun. 2021.
HOCHMAN, G. A Saúde Pública em tempos de Capanema: continuidades e inovações. In: BOMENY, H. Constelação Capanema: intelectuais e política. Rio de Janeiro: Editora FGV, 2001. p. 127-151.
LARA, J. A Virologia no Instituto Oswaldo Cruz e a emergência da dengue como problema científico. Programa de Pós-Graduação em História das Ciências e da Saúde, Casa de Oswaldo Cruz, Fundação Oswaldo Cruz, Rio de Janeiro, 2020. Disponível em: <https://www.arca.fiocruz.br/bitstream/icict/44088/2/Jorge_Lara_COC_Dissertação_2020>. Acesso em: 30 jun. 2021.
LOWY, I. Representação e intervenção em saúde pública: vírus, mosquitos e especialistas da Fundação Rockefeller no Brasil. História, Ciências, Saúde - Manguinhos, Rio de Janeiro, v. 5, n. 3, p. 647-677, fev. 1999.
LOWY, I. Vírus, mosquitos e modernidade: a febre amarela no Brasil entre ciência e política. Rio de Janeiro: Editora Fiocruz, 2006.
MAGALHÃES, R. A Erradicação do Aedes aegypti: febre amarela, Fred Soper e saúde pública nas Américas (1918-1968). Rio de Janeiro: Editora Fiocruz, 2016.
PALMER, S. Gênese da Saúde Global: a Fundação Rockefeller no Caribe e na América Latina. Rio de Janeiro: Editora Fiocruz, 2015.
QUEVEDO, E. et al. Café y gusanos, mosquitos y petróleo: el transito desde la higiene hacia la medicina tropical y la salud publica en Colombia, 1873-1953. Bogotá: Universidad Nacional de Colombia, 2004.
QUEVEDO, E. et al. Knowledge and power: the asymmetry of interests of colombian and Rockefeller doctors in the construction of the concept of ‘jungle yellow fever’, 1907-1938. Canadian Bulletin of Medical History, v. 25, n. 1, p. 71-109, 2008.
SAWYER, W. et al. The relationship of yellow fever of the Western Hemisphere to that of Africa and to leptospiral jaundice. The Journal of Experimental Medicine, v. 51, n. 3, p. 493-517, fev. 1930.
SAWYER, W. A history of the activity of the Rockefeller Foundation in the investigation and control of yellow fever. American Journal of Tropical Medicine, v. 17, n. 1, p. 35-50, jan. 1937.
SOLORZANO, A. The Rockefeller Foundation in revolutionary Mexico: yellow fever in Yucatan and Veracruz. In: CUETO, M. (Org.). Missionaries of Science: The Rockefeller Foundation and Latin America. Indianapolis: Indiana University Press, 1994. p. 52-71.
SOPER, F. Progressos realizados nos estudos e combate da febre amarela entre a IX e a X Conferências Sanitárias Panamericanas 1934-1938. Separata dos Archivos de Hygiene, v. 9, n. 1, p. 3-25, 1939.
SOPER, F. et al. Yellow fever without Aedes aegypti: study of a rural epidemic in the Valle do Chanaan, Espírito Santo, Brazil, 1932. American Journal of Epidemiology, v. 18, n. 3, p. 555-587, nov. 1933.
SOPER, F.; DUFFY, J. Ventures in world health: the memories of Fred Lowe Soper. Washington. D.C.: PAHO, 1977.
STEPAN, N. Eradication: ridding the world of diseases forever? Ithaca, New York: Cornell University Press, 2011.
STOKES, A.; BAUER, J.; HUDSON, P. Transmission of yellow fever to Macacus rhesus, preliminary note. The Journal of the American Medical Association, v. 90, n. 4, p. 253-254, jan. 1928a.
STOKES, A.; BAUER, J.; HUDSON, P. Experimental transmission of yellow fever to laboratory animals. The American Journal of Tropical Medicine, v. 8, n. 2, p. 103-164, jan. 1928b.
STRODE, G. Yellow fever. New York, Toronto, London: McGraw-Hill, 1951.
WILLIAMS, G. The plague killers. New York: Scribner, 1969.
WILLIAMS, S. Nationalism and public health: the convergence of the Rockefeller Foundation techniques and the Brazilian federal authority during the time of yellow fever. In: CUETO, M. (Org.). Missionaries of Science: The Rockefeller Foundation and Latin America. Bloomington, Indianapolis: Indiana University Press, 1994. p. 23-51.
Notas
