Artículos
Aplicación de ultrasonido para el control de cianobacterias y la degradación de cianotoxinas
Application of ultrasound for the control of cyanobacteria and the degradation of cyanotoxins
Aplicación de ultrasonido para el control de cianobacterias y la degradación de cianotoxinas
Revista UIS ingenierías, vol. 22, no. 4, pp. 51-60, 2023
Universidad Industrial de Santander
Received: 23 February 2023
Accepted: 10 August 2023
Published: 01 November 2023
Resumen: Las floraciones cianobacterianas en cuerpos de agua son un problema de gran interés entre la comunidad científica, debido a la producción de metabolitos tóxicos, denominados cianotoxinas. Las cianobacterias están formadas por un amplio número de géneros y especies, con diversos mecanismos de intoxicación; por lo que constituyen un grave problema ambiental con serias repercusiones en la salud de los seres vivos y del hombre. Adicionalmente, la alta producción de cianotoxinas asociada a la presencia de cianobacterias ha crecido enormemente en frecuencia y extensión en todo el mundo, lo cual aumenta la preocupación por parte de las autoridades y los prestadores de servicios públicos. Por otro lado, es importante señalar que los procesos convencionales con los que operan las instalaciones de tratamiento de agua son ineficientes para su eliminación y/o degradación dado que las cianotoxinas son solubles en agua y persistentes. En este sentido, se hace necesaria la aplicación de tecnologías alternativas a los sistemas de tratamiento tradicionales de potabilización con el fin de obtener un agua de calidad apta para el consumo humano. En el presente trabajo, se describe el uso de ultrasonido en el tratamiento de aguas contaminadas con cianobacterias y cianotoxinas, haciendo especial hincapié en la influencia de la variación de parámetros significativos que intervienen en la eficiencia de eliminación e inactivación de las cianobacterias, y la degradación de sus toxinas a través del proceso de sonicación. Con ello, se pretender posicionar el ultrasonido de baja frecuencia como tecnología de oxidación avanzada que permita controlar la proliferación de las cianobacterias y sus toxinas, y evitar la reducción de la calidad de los cuerpos de agua que abastecen las plantas de producción de agua potable.
Palabras clave: Afloramiento, cianobacteria, contaminación del agua, eutrofización, microcistina-LR, nutrientes, potabilización del agua, procesos avanzados de oxidación, sistemas lóticos, tratamientos alternativos.
Abstract: Cyanobacterial blooms in water bodies are a problem of a great concern among the community, because of the production of toxic metabolites, called cyanotoxins. Cyanobacteria are made up of many genera and species, with various mechanisms of intoxication; therefore, they constitute a serious environmental problem with detrimental repercussions on the health of living beings and humankind. Additionally, the high production of cyanotoxins associated with the presence of cyanobacteria has increased in extent and frequency throughout the world, which increases the concern of authorities and public service providers. On the other hand, it is important to point out that the conventional processes water treatment facilities are operating with are inefficient for their elimination and/or degradation, since cyanotoxins are soluble in water and persistent. In this regard, applying alternative technologies to traditional purification treatment systems is required to obtain water of quality that is suitable for human consumption. In this work, the use of ultrasound in the treatment of water contaminated with cyanobacteria and cyanotoxins is described, with special emphasis on the influence of the variation of significant parameters that intervene in the efficiency of elimination and inactivation of cyanobacteria, and the degradation of its toxins through the sonication process. With this, it is intended to position low-frequency ultrasound as an advanced technology that allows controlling the alteration of cyanobacteria and their toxins and avoiding the reduction of the quality of the water bodies that will supply the drinking water treatment plants.
Keywords: Advanced oxidation processes, alternative treatments, bloom, cyanobacteria, eutrophication, lotic systems, microcystin-LR, nutrients, water pollution, water purification.
1. Introducción
Las algas verde-azuladas, más conocidas como cianobacterias, son organismos procariotas, unicelulares y fotosintéticos presentes en diversos ecosistemas acuáticos [1], [2], [3]. En sistemas lénticos, tales como lagos y lagunas naturales y artificiales, particularmente cuando se encuentran ubicados en el Trópico, es muy frecuente encontrar cianobacterias, cuyo desarrollo se ve favorecido debido a la gran cantidad de nutrientes y a las altas temperaturas. Estas circunstancias dan lugar a la eutrofización de los cuerpos de agua, lo que produce un aumento excesivo de la cantidad de fitoplancton, generando así un evento llamado afloramiento [3], [4], [5].
Dado que ciertas cianobacterias producen toxinas, denominadas cianotoxinas, esta explosión demográfica implica que existe un riesgo para el hombre y el resto de seres vivos, provocando incluso hasta su muerte. Esto es de crucial interés particularmente cuando estas aguas o reservorios se utilizan para recreación, riego o suministro de agua a la población sin un tratamiento previo adecuado para eliminar el riesgo asociado [6], [7], [8]. En humanos, ha habido algunos casos documentados de envenenamiento letal o grave después de una exposición a corto plazo a niveles altos o aguda. No obstante, el principal problema subyace en la exposición crónica o prolongada a niveles bajos de estas toxinas [9]. Además de su alta toxicidad, es importante destacar su capacidad para acumularse en los organismos [10] y aumentar su toxicidad a medida que avanza en la cadena alimentaria [10], [11]. La variante más tóxica y ampliamente distribuida es la microcistina-LR (MC-LR) [12].
Cabe destacar que se ha establecido un valor límite máximo permisible de 1 μg/L para la MC-LR en agua potable. Este valor ha sido definido por la WHO (Organización Mundial de la Salud, por sus siglas en inglés). Sin embargo, preocupa el hecho de que en cuerpos de agua donde hay cepas de microorganismos potencialmente tóxicos, las concentraciones de MC-LR suelen ser mayores que este valor guía [13]. Este problema se está presentando con gran frecuencia en todo el mundo [14], lo que se debe particularmente a la falta de medidas preventivas encaminadas a reducir las descargas de contaminantes a los cuerpos de agua y al impacto del cambio climático, lo que favorece el crecimiento de estos microorganismos [15]. En contraste, los procesos convencionales de potabilización generalmente implican la retención de las células cianobacterianas, más no la degradación efectiva de las toxinas [16]. De hecho, la desinfección con cloro, compromete la integridad de las células sin garantizar su eliminación, provocando la lisis celular y, por consiguiente, la liberación de toxinas intracelulares al medio [1]. Adicionalmente, se ha reportado que el uso de haluros en la desinfección del agua puede estar asociada a la generación de subproductos de desinfección [17]. Es por esto que en los últimos años se han propuesto nuevas técnicas como los procesos de oxidación avanzada (POA); entre ellos el ultrasonido, el cual sirve para degradar las cianotoxinas, al tiempo que permite controlar la proliferación de cianobacterias [18], [19].
En este sentido, con este trabajo se pretende posicionar al ultrasonido como una tecnología de oxidación avanzada alternativa a los procesos de tratamiento convencional. Con el fin de discernir el principio de funcionamiento de esta tecnología, así como su aplicación, se describe con detalle la influencia de cada uno de los parámetros que influyen el proceso de sonicación en el funcionamiento y la estructura de las células cianobacterianas y en la eficiencia de degradación de las cianotoxinas.
2. Características de las floraciones bacterianas
Las algas verde-azuladas son bacterias que realizan la fotosíntesis, de modo que son capaces de generar su propio alimento. Estos microorganismos son ubicuos, dado que se pueden encontrar en cuerpos de agua a nivel mundial. Su capacidad para sobrevivir en condiciones extremas y adaptarse a una variedad de hábitats se debe en gran parte a su historia evolutiva, ya que son uno de los organismos que primero aparecieron en el planeta Tierra [20]. De allí, parte el hecho de que existan similitudes en la función ecológica de algas y las cianobacterias planctónicas, al conjugar una estructura celular típicamente bacteriana, con el proceso de la fotosíntesis oxigénica, confiriendo una alta resistencia.
Las cianobacterias pueden ser bentónicas o pelágicas, y representan uno de los filos procariotas más diversos, en términos fisiológicos y morfológicos. Adicionalmente, estos organismos realizan la fotosíntesis a través del pigmento verde, clorofila-a. No obstante, a menudo producen otro tipo de pigmentos que según sus niveles les confiere colores que varían entre diferentes tonos de azul y verde, y con menos frecuencia, de marrón a rojo [21], [22]. Estos organismos tienen la capacidad de formar colonias grandes y densas que pueden observarse a simple vista. Cuando estas colonias son abundantes, pueden cambiar el color del agua o formar biofilms en la superficie del agua. Es de resaltar que aquellas floraciones con capacidad de causar efectos adversos se denominan cianoHABs, cuyo tiempo de vida va desde unos pocos días hasta meses [23].
Una floración algal o afloramiento es un fenómeno en el cual se produce biomasa de manera significativa durante un corto periodo de tiempo, lo cual se encuentra relacionado simultáneamente con una disminución de la diversidad del fitoplancton [1]. Anabaena spp., Aphanizomenon spp., Planktothrix spp., Lyngbya spp. Cylindrospermopsis spp., Nodularia spp., Microcystis spp., y Oscillatoria spp. conforman el grupo de los géneros más comunes de cianobacterias que forman afloramientos; aunque en menor proporción se encuentran también Gloeotrichia spp., Gomphosphaeria spp., Nostoc spp. y Coelosphaerium spp [24].
Son muchos los tipos de toxinas que pueden producir las especies de cianobacterias. A estas toxinas se las conoce como cianotoxinas. El aumento de la eutrofización, entre otros factores ambientales, tales como las altas temperaturas, los valores de pH del agua elevados, el estancamiento de las aguas y los valores bajos de turbidez puede contribuir a la formación de floraciones de cianobacterias [25]. No obstante, la presencia de una floración no significa necesariamente que haya producción de toxinas, ya que distintos genotipos de cianobacterias pueden o no producir cianotoxinas, y su producción puede estar condicionada por factores ambientales específicos. Puede haber diversos tipos de genotipos de cianobacterias; es por ello que no todas las cianobacterias van a generar cianotoxinas por igual. Adicionalmente, es importante señalar que la producción de cianotoxinas puede estar influenciada por ciertas condiciones ambientales. Incluso en una sola especie de cianobacteria, puede haber una combinación de cepas tóxicas y no tóxicas, de manera que la toxicidad asociada a las cepas es variable [6]. Son varios los factores que afectan el crecimiento de las algas verde-azuladas y la producción de cianotoxinas. Entre estos factores, debe mencionarse el pH del agua, la intensidad y el tipo de radiación ultravioleta y visible, la temperatura, los nutrientes, el viento, la salinidad, los metales traza y otros contaminantes que puedan estar en las aguas. A pesar de que todavía se está investigando activamente en esta área de conocimiento, se sabe que las condiciones que pueden desencadenar o inhibir la producción de cianotoxinas son un tema de estudio gran interés [26].
3. Efectos adversos de las cianobacterias
Las cianotoxinas afectan las poblaciones de los ecosistemas a través de fenómenos como la bioacumulación y biomagnificación a lo largo de la cadena trófica de ecosistemas acuáticos. Adicionalmente, se incluye el fenómeno biológico de la alelopatía, el cual consiste en la producción por parte de los organismos de uno o más productos bioquímicos, afectando el metabolismo de otros organismos en la misma comunidad. Aquellos productos que tienen efectos alelopáticos negativos son importantes en la defensa de las cianobacterias contra la herbivoría, y determinan la abundancia y distribución de las poblaciones en las comunidades [27]. Por otro lado, desde el punto de vista químico, cabe destacar que los lipopolisacáridos, péptidos, aminoácidos y alcaloides contenidos en las moléculas de cianotoxinas son los responsables de su efecto patógeno debido a que actúan como endotoxinas.
Si bien la apariencia y sabor desagradables del agua contaminada por floraciones de cianobacterias probablemente han impedido su ingesta hasta niveles tóxicos, evitando muertes consecuentes, hay cada vez más evidencias de que la exposición crónica puede causar efectos adversos en la salud [28]. Entre los diferentes mecanismos de intoxicación se incluyen las reacciones neurotóxicas, citotóxicas, dermatotóxicas y hepatotóxicas, asociados a la exposición directa a cianotoxinas mediante el contacto cutáneo o la ingesta [26].
Las hepatotoxinas son, probablemente, las cianotoxinas más comunes y conforman un grupo de compuestos estructuralmente diferentes que incluye más de 100 variantes de microcistina (MC), además de nodularina (NOD) y cilindrospermopsina (CYN). Las hepatotoxinas son moléculas solubles en agua que representan una seria amenaza, y cuya estructura cíclica les proporciona gran estabilidad. Las MC comparten una estructura general de heptapéptidos monocíclicos (Figura 1) que tiene la capacidad de resistir factores físicos y químicos [26] ; son producidas comúnmente por los géneros de cianobacterias Microcystis spp., Anabaena spp., Planktothrix spp., Nostoc spp., Oscillatoria spp., Anabaenopsis spp. y Hapalosiphon spp., mientras las NOD son producidas, principalmente, por Nodularia spumigena en aguas salobres, y las CYN por Cylindrospermopsis raciborskii en aguas dulces [22].
![Estructura química de las microcistinas. Adaptado de Malik et al. [26].](../2145-8456-uisi-22-04-51-gf1.png)
Figura 1
Estructura química de las microcistinas. Adaptado de Malik et al. [26].
Como se ha indicado anteriormente, las condiciones ambientales no solamente influyen en la generación de cianotoxinas, sino también el tipo de cepa cianobacteriana. Esto significa que el grado de toxicidad de una mezcla de estas toxinas es variable [29]. Mundialmente, las cianotoxinas más comunes que se encuentran en los blooms de cianobacterias son las MC y NOD [30].
La presencia de cianotoxinas es diferente a otras sustancias tóxicas, ya que generalmente se encuentran en el interior de las células de las cianobacterias o unidas a ellas, siendo solamente una pequeña fracción la que está disuelta en el agua, a menos que haya lisis celular. Las cianotoxinas son altamente estables y resistentes a la degradación tanto física como química. Entre todas las cianotoxinas, las MC y NOD son las más resistentes y estables, además de ser las más peligrosos para la salud humana [6]. La variante más ampliamente distribuida y tóxica es la microcistina-LR (MC-LR). Esta toxina es considerada un promotor tumoral y potencial carcinógeno para humanos y animales, clasificada incluso como un potencial carcinógeno de clase 2B por la IARC (Agencia Internacional de Investigación sobre el Cáncer, por sus siglas en inglés) [26]. Por otro lado, las MC tienen la capacidad de afectar órganos como los riñones, el hígado, el cerebro, los intestinos, el corazón y los pulmones, así como los sistemas inmunitario y reproductivo [31]. Así mismo, los efectos nocivos de otras variantes de MC parecen ser similares a los de la MC-LR, pero difieren en potencia; además de otros factores a tener en cuenta, como la dosis, la ruta de exposición y la duración e intensidad de la exposición a las toxinas cianobacterianas [32].
4. Aplicación del ultrasonido
El ultrasonido consiste en una serie de ondas producidas generalmente por transductores de materiales piezoeléctricos a una frecuencia superior a los 20 kHz, el cual se define como el valor límite audible por parte del ser humano [33]. La cavitación acústica se da por medio de la propagación de dichas ondas de presión con frecuencia de 20 kHz o superior en un fluido como es el agua, dando lugar a la generación de núcleos de cavitación (o microburburjas) en el seno acuático. Así, sucede la formación, crecimiento y colapso de microburbujas, que liberan gran cantidad de energía, generando ciclos de rarefacción y compresión; es decir, cambios locales de presión y temperatura elevadas tras la implosión [34]. A este fenómeno se le conoce como sonicación y se produce a intervalos de tiempo extremadamente pequeños (milisegundos), transmitiendo la energía suficiente a los compuestos presentes en el agua como para efectuar daños significativos en su estructura, así como desencadenar múltiples reacciones [33].
Cuando se aplica radiación ultrasónica al agua contaminada, se pueden producir los siguientes efectos físicos y químicos en las sustancias contaminantes presentes en el agua: pirólisis o descomposición a alta temperatura, oxidación por la producción de radicales libres, resonancia de burbujas de cavitación y efecto de cizallamiento mecánico por micro-chorro. Cualquiera de estos mecanismos puede llegar a destruir la pared celular o la estructura de la membrana celular cianobacteriana, así como degradar las toxinas liberadas en el medio [34].
El ultrasonido tiene tres funciones: 1) destruir directamente la pared celular y matar las algas, 2) inhibir la actividad de crecimiento de las algas no muertas y 3) degradar las toxinas [34]. Como se ha mencionado, la efectividad del proceso estará dada por tres parámetros operativos importantes para el uso de la sonicación como estrategia de control algal: frecuencia, intensidad (o potencia) y duración de la exposición. Así, la configuración del proceso de ultrasonido juega un papel muy importante [33].
De la frecuencia empleada depende la predominancia de los efectos químicos o mecánicos [35], ya que a pesar de ser un proceso físico que no involucra la adición de químicos, también se desencadena una serie de reacciones por medio de la descomposición de la molécula de agua en una variedad de especies altamente oxidantes. A bajas frecuencias, la cavitación conduce principalmente a fuerzas cortantes. Las burbujas tienen tiempo suficiente para crecer, y esto da como resultado una onda de choque más fuerte cuando implosionan. A altas frecuencias, aunque hay menor tiempo disponible para la creación de burbujas, se produce mayor cantidad de radicales libres y, por lo tanto, aumenta el estrés oxidativo [36], [37]. Chen et al. refuerzan esta teoría, ya que plantean que cuando la frecuencia ultrasónica está entre 300 y 600 kHz, el mecanismo de inactivación puede encontrarse dominado por la oxidación de radicales libres. Por su parte, en el rango de baja frecuencia (20-100 kHz), el daño causado puede depender principalmente de la acción de cizallamiento mecánico y la pirólisis térmica del micro-chorro [34].
En este sentido, a medida que aumenta la frecuencia, se debe emplear también mayor potencia para lograr la cavitación, lo cual deriva en un mayor consumo de energía. Zhang et al. encontró que una mayor potencia y frecuencia ultrasónica aceleran la tasa de eliminación de las células de las algas, pero cuando la potencia es superior a 48 W, la liberación de toxinas aumenta significativamente. Por lo tanto, es necesario establecer la potencia por debajo de 48 W [38], ya que, a bajas frecuencias y altas potencias, la cavitación puede provocar la ruptura celular. Así, tanto la frecuencia como la potencia son factores clave que afectan la efectividad del proceso de ultrasonido.
Por otro lado, una mayor duración de la sonicación significa más ciclos de rarefacción y compresión que conducen a mayores efectos sonoquímicos. Además, Chen et al. muestran que la tasa de eliminación de MC puede alcanzar el máximo en poco tiempo tras la aplicación del tratamiento ultrasónico, para estabilizarse posteriormente [34].
Por su parte, Purcell et al. encontraron que diferentes estructuras celulares tenían diferente sensibilidad al ultrasonido. La sensibilidad de las algas filamentosas al ultrasonido es más fuerte que la de las algas unicelulares, de modo que la destrucción de la estructura celular se rompe más fácil y rápidamente [36]. Múltiples estudios han demostrado también, que la irradiación con ultrasonido puede conducir al aumento de ROS (especies reactivas de oxígeno, por sus siglas en inglés). Cuando el sistema de defensa antioxidante en las células de las algas no elimina estas especies reactivas, causará daño celular y la muerte [34]. Por otro lado, Tang et al. observaron que el ultrasonido puede inhibir eficazmente la fotosíntesis de las algas al destruir el pigmento fotosintético de las células. Este efecto da como resultado la disminución de la tasa de producción de oxígeno, obteniendo que el daño de la ficobiliproteína por ultrasonido es mucho mayor que el de la clorofila a. [39], [40]. Sin embargo, vale la pena estudiar la posibilidad de destruir el sistema fotosintético de las algas y mantener la integridad de las células en la medida de lo posible, optimizando los parámetros de sonicación. No obstante, es oportuno destacar que son escasos los estudios reportados en la literatura hasta el momento a pesar de que se han realizado investigaciones previas en cuanto a la capacidad del ultrasonido para colapsar las vacuolas de gas de las cianobacterias y lograr su control por medio de su sedimentación [34].
4.1. Capacidad de flotabilidad de las cianobacterias
Múltiples estudios confirman los riesgos que implica la presencia en los cuerpos de agua de cianobacterias [1]. Así mismo, se ha evidenciado que estos afloramientos pueden regular su capacidad de flotación y, por lo tanto, su posición en la columna de agua por medio del uso de unos orgánulos celulares denominados vacuolas de gas. Esta capacidad de flotación supone una ventaja competitiva frente a otras especies del fitoplancton [41], permitiendo su proliferación. En muchos procariotas acuáticos, como las cianobacterias, bacterias fotosintéticas anoxigénicas y halobacterias, se pueden encontrar cavidades huecas conocidas como vacuolas de gas. Estas vacuolas están compuestas por filas de vesículas gaseosas individuales que son cilindros intracelulares huecos recubiertos de proteínas. La función principal de las vacuolas de gas consiste en mantener la flotabilidad de las células, permitiéndoles permanecer a la profundidad adecuada para obtener suficiente oxígeno, luz y nutrientes en el agua [41]. La aplicación de ultrasonido rompe estas vacuolas de gas y facilita la sedimentación de las células cianobacterianas, permitiendo que éstas permanezcan en las zonas más profundas de la columna de agua en los embalses donde las condiciones de luz y oxígeno son limitadas, interrumpiendo así sus funciones vitales como la fotosíntesis y la absorción de nutrientes, por lo que eventualmente morirán [42].
4.2. Efectos de la cavitación sobre las vacuolas de gas
Durante el proceso de sonicación se destruye la vacuola de gas por rompimiento de la capa de proteína que la conforma, debido al colapso de las burbujas de cavitación, más no por las reacciones químicas que se desencadenan en el agua al generarse radicales libres [35]. De esta manera, se ve favorecido el rompimiento por la frecuencia empleada en el proceso de sonicación [42]. A bajas frecuencias, pero alta potencia, la cavitación acústica conduce principalmente a efectos mecánicos o fuerzas de cizallamiento elevadas que pueden provocar la ruptura celular. A altas frecuencias, por su parte, se produce mayor cantidad de radicales libres, destacando el radical hidroxilo (HO.) y, por lo tanto, el daño químico a las células es significativo [43]. La frecuencia del ultrasonido debe ser tal que destruya la estructura celular interna de la cianobacteria más no la externa, ya que podría producir la lisis celular y aumentar la cantidad de cianotoxinas extracelulares en el ambiente [44], como se ilustra en la Figura 2. De este modo, la efectividad estará dada por tres parámetros operativos importantes para el uso de la sonicación como estrategia de control de estas algas verde-azuladas: frecuencia, intensidad (o potencia) y duración de la exposición [42]. Estudios recientes sugieren que diferentes especies de algas verde-azuladas pueden requerir diferentes frecuencias de operación para maximizar la inhibición de su crecimiento [36], [45]. Se sabe que el ultrasonido es efectivo para la eliminación de toxinas de algas como las microcistinas producidas por Microcystis aeruginosa [18], la cual resulta ser la variante más estudiada.
4.3. Regeneración de la vacuola de gas
A pesar de que la aplicación de ultrasonido induce el colapso de las vacuolas de gas y consigo la precipitación de las cianobacterias, inhibiendo su crecimiento [46], las vacuolas pueden nuevamente ser regeneradas en un tiempo relativamente corto después de que cesa la aplicación del ultrasonido [42]. Según los resultados obtenidos por Rodríguez-Molares et al., el proceso de sedimentación es significativo en los dos primeros días después de la irradiación, un lapso que podría ser suficiente para que las células desciendan a un nivel en el que la intensidad de la luz no sea suficiente para reformar las vesículas de gas y el proceso de sedimentación sea irreversible. Sin embargo, cada especie posee cierta inercia; es decir, mayor o menor tasa de hundimiento o fuerza de sedimentación [47]. Adicionalmente, la sonicación no es el único método para eliminar las cianobacterias por cavitación. Recientemente, la cavitación de chorro hidráulico ha sido reportada como una alternativa al ultrasonido para la eliminación de algas. De igual manera, se ha evidenciado que esta técnica permite destruir también las vesículas de gas [48], [49].
5. Perspectivas futuras
A pesar de que en la literatura se reporta la alta eficiencia del proceso de ultrasonido a escala de laboratorio para el control de algas [36], [50], sus condiciones de ensayo pueden no representar las condiciones de campo. En este sentido, hay varios factores adicionales que deben ser considerados en el diseño experimental para la aplicación de estos tipos de tratamientos y discusión certera de resultados obtenidos [18], como son las condiciones ambientales y los valores de los parámetros fisicoquímicos de calidad del agua (pH, nutrientes, intensidad y duración de la radiación solar, turbidez y temperatura, entre otros). Estas variables pueden llegar a afectar las concentraciones de biomasa de algas, la capacidad fotosintética, además de la distribución de algas en los reservorios, la cual está sujeta a los flujos de agua, turbulencia o viento, resultando en concentraciones muy variables de algas que dificulta su control.
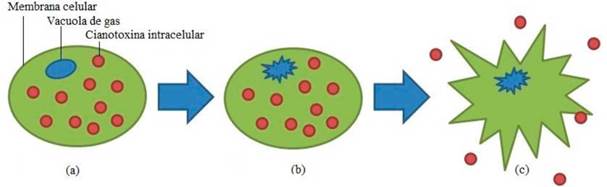
Figura 2
Escenarios tras la aplicación de ultrasonido: (a) estructura celular intacta; (b) ruptura de la vacuola de gas; (c) lisis celular.
Fuente: elaboración propia.
Bajo este escenario, resulta de gran importancia para aplicaciones futuras a gran escala, evaluar si dicha tecnología pudiera considerarse como una alternativa óptima a las unidades de operación con las que operan tradicionalmente las plantas de tratamiento de aguas y si, realmente, proporcionaría una mejora significativa de la calidad de las aguas, ejerciendo un control del crecimiento de las cianobacterias a largo plazo y eliminando los efectos nocivos causados por estos microorganismos. Lo anterior, teniendo en cuenta que el radio de cobertura de los instrumentos ultrasónicos de eliminación de algas, generalmente, es de 50 a 300 m. Por ello, se tiene un buen efecto inhibidor sobre los brotes de algas en estanques y pequeños lagos; si bien para grandes masas de agua es necesario instalar múltiples dispositivos ultrasónicos de eliminación de algas, asegurando una cobertura total del cuerpo de agua.
Se ha observado que la aplicación de ultrasonido sobre masas grandes de agua ha logrado evidenciar su eficacia, más aún, cuando en la actualidad contamos con aplicaciones regionales de ultrasonido de baja frecuencia que se han venido implementando como medidas de control en sistemas de abastecimiento de agua potable tan importantes para ciudades ampliamente habitadas, como es el caso de los reservorios de agua que abastecen la ciudad de Medellín, Antioquia (Colombia). Es primordial, por tanto, ampliar el conocimiento en este campo de estudio, y profundizar acerca de la efectividad de este tratamiento y su optimización.
6. Conclusiones
El uso del ultrasonido, como técnica de oxidación avanzada, presenta un futuro prometedor, ya que ha experimentado un rápido desarrollo durante la última década. La efectividad del proceso viene dada por los tres parámetros operativos que juegan un papel crucial: la frecuencia, la potencia o intensidad, y la duración o tiempo de exposición a las burbujas de cavitación. Esta técnica de tratamiento de agua ha demostrado controlar eficazmente el crecimiento de algas, por medio de la destrucción estructural y funcional de las células, así como la degradación de cianotoxinas, tales como las microcistinas (MC). Además, resulta inocua para otras especies, ya que las ondas ultrasónicas tienen un mayor efecto de inhibición sobre las cianobacterias que otras algas, mejora la transparencia y la calidad fisicoquímica del agua, y reduce los riesgos de seguridad causados por la liberación de sustancias químicas en el agua. Es entonces, una tecnología segura, respetuosa con el medio ambiente y económicamente viable, en comparación con los métodos tradicionales de eliminación de algas. En este sentido, la implementación de ultrasonido a baja frecuencia tiene altas perspectivas de aplicación, especialmente para la prevención y control de cianotoxinas y cianobacterias en fuentes de agua potable.
Referencias
S. Merel, D. Walker, R. Chicana, S. Snyder, E. Baurès, O. Thomas, "State of knowledge and concerns on cyanobacterial blooms and cyanotoxins," Environ. Int., vol. 59, pp. 303-327, 2013, doi: https://doi.org/10.1016/j.envint.2013.06.013
K. Zhao, L. Wang, Q. You, J. Zhang, W. Pang, Q. Wang, "Impact of cyanobacterial bloom intensity on plankton ecosystem functioning measured by eukaryotic phytoplankton and zooplankton indicators," Ecol. Indic., vol. 140, no. 100, p. 109028, 2022, doi: https://doi.org/10.1016/j.ecolind.2022.109028
L. You et al., "Multi-class secondary metabolites in cyanobacterial blooms from a tropical water body: Distribution patterns and real-time prediction," Water Res., vol. 212, p. 118129, 2022, doi: https://doi.org/10.1016/j.watres.2022.118129
P. Nowicka-Krawczyk et al., "Persistent Cyanobacteria Blooms in Artificial Water Bodies-An Effect of Environmental Conditions or the Result of Anthropogenic Change," Int. J. Environ. Res. Public Health, vol. 19, no. 12, p. 6990, 2022, doi: https://doi.org/10.3390/ijerph19126990
M. L. Wells et al., "Harmful algal blooms and climate change: Learning from the past and present to forecast the future," Harmful Algae, vol. 49, pp. 68-93, 2015, doi: https://doi.org/10.1016/j.hal.2015.07.009
I. Chorus, J. Bartram, Toxic Cyanobacteria in Water: A guide to their public health consequences, monitoring and management. London, 1999.
H. W. Paerl, T. G. Otten, R. Kudela, "Mitigating the Expansion of Harmful Algal Blooms Across the Freshwater-to-Marine Continuum," Environ. Sci. Technol., vol. 52, no. 10, pp. 5519-5529, 2018, doi: https://doi.org/10.1021/acs.est.7b05950
P. Labohá et al., "Cyanobacteria, cyanotoxins and lipopolysaccharides in aerosols from inland freshwater bodies and their effects on human bronchial cells," Environ. Toxicol. Pharmacol., vol. 98, p. 104073, 2023, doi: https://doi.org/10.1016/j.etap.2023.104073
H. Falfushynska, N. Kasianchuk, E. Siemens, E. Henao, P. Rzymski, "A Review of Common Cyanotoxins and Their Effects on Fish," Toxics, vol. 11, no. 2, p. 118, 2023, doi: https://doi.org/10.3390/toxics11020118
A. C. Mehinto et al., "Synthesis of ecotoxicological studies on cyanotoxins in freshwater habitats - Evaluating the basis for developing thresholds protective of aquatic life in the United States," Sci. Total Environ., vol. 795, p. 148864, 2021, doi: https://doi.org/10.1016/j.scitotenv.2021.148864
M. Crettaz-Minaglia, D. Sedan, L. Giannuzzi, "Bioacumulacion y biomagnificacion de cianotoxinas en organismos acuaticos de agua dulce," Cianobacterias como determinantes ambientales de la salud. Argentina: Ministerio de Salud de la Nación, departamento de Salud Ambiental, 2017.
D. M. M. Caramés, "Tecnologías de control de floraciones de cianobacterias y algas nocivas en cuerpos de agua, con énfasis en el uso de irradiación por ultrasonido," Innotec, vol. 12, no. 12, pp. 54-61, 2016.
OMS, Guías para la calidad del agua potable, Tercera. Organización Mundial de la Salud, 2006.
A. Serrà, L. Philippe, F. Perreault, S. Garcia-Segura, "Photocatalytic treatment of natural waters. Reality or hype? The case of cyanotoxins remediation," Water Res., vol. 188, p. 116543, 2021, doi: https://doi.org/10.1016/j.watres.2020.116543
H. W. Paerl et al., "Mitigating cyanobacterial harmful algal blooms in aquatic ecosystems impacted by climate change and anthropogenic nutrients," Harmful Algae, vol. 54, pp. 213-222, 2016, doi: https://doi.org/10.1016/j.hal.2015.09.009
X. He et al., "Toxic cyanobacteria and drinking water: Impacts, detection, and treatment," Harmful Algae, vol. 54, pp. 174-193, 2016, doi: https://doi.org/10.1016/j.hal.2016.01.001
M. A. Mazhar et al., "Chlorination disinfection byproducts in municipal drinking water - A review," J. Clean. Prod., vol. 273, p. 123159, 2020, doi: https://doi.org/10.1016/j.jclepro.2020.123159
J. Park, J. Church, Y. Son, K. T. Kim, W. H. Lee, "Recent advances in ultrasonic treatment: Challenges and field applications for controlling harmful algal blooms (HABs)," Ultrason. Sonochem., vol. 38, pp. 326334, 2017, doi: https://doi.org/10.1016/j.ultsonch.2017.03.003
D. Ghernaout, N. Elboughdiri, "Dealing with Cyanobacteria and Cyanotoxins: Engineering Viewpoints," Open Access Libr. J., vol. 7, no. 5, p. e6363, 2020, doi: https://doi.org/10.4236/oalib.1106363
L. A. Gaysina, A. Saraf, P. Singh, "Cyanobacteria in diverse habitats," Cyanobacteria: From Basic Science to Applications, 2019, pp. 1 -28. doi: https://doi.org/10.1016/B978-0-12-814667-5.00001-5
F. M. Buratti et al., "Cyanotoxins: producing organisms, occurrence, toxicity, mechanism of action and human health toxicological risk evaluation," Arch. Toxicol., vol. 91, no. 3, pp. 1049-1130, 2017, doi: https://doi.org/10.1007/s00204-016-1913-6
G. Kaur, "Freshwater Cyanotoxins," in Biomarkers in Toxicology, Elsevier Inc., 2019, pp. 601613, doi: https://doi.org/10.1016/b978-0-12-814655-2.00035-9
A. K. D. D. S. Sá et al., "Algal blooms and trophic state in a tropical estuary blocked by a dam (Northeastern Brazil)," Ocean Coast. Res., vol. 69, p. e21009, 2021.
J. Huisman, G. A. Codd, H. W. Paerl, B. W. Ibelings, J. M. H. Verspagen, P. M. Visser, "Cyanobacterial blooms," Nat. Rev. Microbiol., vol. 16, no. 8, pp. 471-483, 2018, doi: https://doi.org/10.1038/s41579-018-0040-1
F. S. Alvarez Dalinger, V. L. Lozano, C. N. Borja, L. B. Moraña, S. María Mónica, "Short-Term Meteorological Conditions Explain Cyanobacterial Blooms in a Tropical Reservoir," Water, vol. 15, no. 2, p. 302, 2023, doi: https://doi.org/10.3390/w15020302
J. K. Malik, V. K. Bharti, A. Rahal, D. Kumar, R. C. Gupta, "Cyanobacterial (blue-green algae) toxins," in Handbook of Toxicology of Chemical Warfare Agents, 2020, pp. 467-478. doi: https://doi.org/10.1016/b978-0-12-819090-6.00031-3
J. S. Yunes, "Cyanobacterial Toxins," in Cyanobacteria: From Basic Science to Applications. Rio Grande, Brazil: Elsevier Inc., 2019, pp. 443-458. doi: https://doi.org/10.1016/B978-0-12-814667-5.00022-2
L. M. Grattan, S. Holobaugh, J. G. Morris, "Harmful algal blooms and public health," Harmful Algae, vol. 57, pp. 2-8, 2016, doi: https://doi.org/10.1016/j.hal.2016.05.003
S. Merel, M. Clément, O. Thomas, "State of the art on cyanotoxins in water and their behaviour towards chlorine," Toxicon, vol. 55, no. 4, pp. 677-691, 2010, doi: https://doi.org/10.1016/j.toxicon.2009.10.028
S. Merel, M. C. Villarín, K. Chung, S. Snyder, "Spatial and thematic distribution of research on cyanotoxins," Toxicon, vol. 76, pp. 118-131, 2013, doi: https://doi.org/10.1016/j.toxicon.2013.09.008
I. Y. Massey et al., "Exposure routes and health effects of microcystins on animals and humans: A minireview," Toxicon, vol. 151, pp. 156-162, 2018, doi: https://doi.org/10.1016/j.toxicon.2018.07.010
L. Chen, J. P. Giesy, P. Xie, "The dose makes the poison," Sci. Total Environ., vol. 621, pp. 649-653, 2018, doi: https://doi.org/10.1016/j.scitotenv.2017.11.218
Y. Yao, Y. Pan, S. Liu, "Power ultrasound and its applications: A state-of-the-art review," Ultrason. Sonochem., vol. 62, p. 104722, 2020, doi: https://doi.org/10.1016/j.ultsonch.2019.104722
G. Chen, X. Ding, W. Zhou, "Study on ultrasonic treatment for degradation of Microcystins (MCs)," Ultrason. Sonochem., vol. 63, p. 104900, 2020, doi: https://doi.org/10.1016/j.ultsonch.2019.104900
M. Kurokawa, P. M. King, X. Wu, E. M. Joyce, T. J. Mason, K. Yamamoto, "Effect of sonication frequency on the disruption of algae," Ultrason. Sonochem., vol. 31, pp. 157-162, 2016, doi: https://doi.org/10.1016/j.ultsonch.2015.12.011
D. Purcell, S. A. Parsons, B. Jefferson, "The influence of ultrasound frequency and power, on the algal species Microcystis aeruginosa, Aphanizomenon flos-aquae, Scenedesmus subspicatus and Melosira sp.," Environ. Technol., vol. 34, no. 17, pp. 2477-2490, 2013, doi: https://doi.org/10.1080/09593330.2013.773355
X. Tan, X. Shu, J. Guo, K. Parajuli, X. Zhang, Z. Duan, "Effects of low-frequency ultrasound on Microcystis aeruginosa from cell inactivation to disruption," Bull. Environ. Contam. Toxicol., vol. 101, no. 1, pp. 117-123, 2018, doi: https://doi.org/10.1007/s00128-018-2348-y
G. Zhang, P. Zhang, B. Wang, H. Liu, "Ultrasonic frequency effects on the removal of Microcystis aeruginosa," Ultrason. Sonochem., vol. 13, no. 5, pp. 446-450, 2006, doi: https://doi.org/10.1016/j.ultsonch.2005.09.012
H. Hao, M. Wu, Y. Chen, J. Tang, Q. Wu, "Cavitation mechanism in cyanobacterial growth inhibition by ultrasonic irradiation," Colloids Surfaces B Biointerfaces, vol. 33, no. 3-4, pp. 151-156, 2004, doi: https://doi.org/10.1016/j.colsurfb.2003.09.003
J. W. Tang, Q. Y. Wu, H. W. Hao, Y. Chen, M. Wu , "Effect of 1.7 MHz ultrasound on a gas-vacuolate cyanobacterium and a gas-vacuole negative cyanobacterium," Colloids Surfaces B Biointerfaces, vol. 36, no. 2, pp. 115-121, 2004, doi: https://doi.org/10.1016/j.colsurfb.2004.06.003
F. Cobo, "Métodos de control de las floraciones de cianobacterias en agues continentales," Limnetica, vol. 34, no. 1, pp. 247-268, 2015.
P. Rajasekhar, L. Fan, T. Nguyen, F. A. Roddick, "A review of the use of sonication to control cyanobacterial blooms," Water Res., vol. 46, no. 14, pp. 4319-4329, 2012, doi: https://doi.org/10.1016/j.watres.2012.05.054
C. Huu Nguyen, R. V. Tikekar, N. Nitin, "Combination of high-frequency ultrasound with propyl gallate for enhancing inactivation of bacteria in water and apple juice," Innov. Food Sci. Emerg. Technol., vol. 82, p. 103149, 2022, doi: https://doi.org/10.1016/j.ifset.2022.103149
Y. Kong, Y. Peng, Z. Zhang, M. Zhang, Y. Zhou, Z. Duan, "Removal of Microcystis aeruginosa by ultrasound: Inactivation mechanism and release of algal organic matter," Ultrason. Sonochem., vol. 56, pp. 447457, 2019, doi: https://doi.org/10.1016/j.ultsonch.2019.04.017
O. D. Schneider, L. A. Weinrich, S. Brezinski, "Ultrasonic treatment of Algae in a New Jersey Reservoir," J. Am. Water Works Assoc., vol. 107, no. 10, pp. E533-E542, 2015, doi: https://doi.org/10.5942/jawwa.2015.107.0149
L. Zhang et al., "Simultaneous removal of colonial Microcystis and microcystins by protozoa grazing coupled with ultrasound treatment," J. Hazard. Mater., vol. 420, p. 126616, 2021, doi: https://doi.org/10.1016/j.jhazmat.2021.126616
A. Rodriguez-Molares, S. Dickson, P. Hobson, C. Howard, A. Zander, M. Burch, "Quantification of the ultrasound induced sedimentation of Microcystis aeruginosa," Ultrason. Sonochem., vol. 21, no. 4, pp. 1299-1304, 2014, doi: https://doi.org/10.1016/j.ultsonch.2014.01.027
D. Jancula, P. Mikula, B. Marsálek, P. Rudolf, F. Pochyly, "Selective method for cyanobacterial bloom removal: Hydraulic jet cavitation experience," Aquac. Int., vol. 22, no. 2, pp. 509-521, 2014, doi: https://doi.org/10.1007/s10499-013-9660-7
P. Li, Y. Song, S. Yu, H. D. Park, "The effect of hydrodynamic cavitation on Microcystis aeruginosa: Physical and chemical factors," Chemosphere, vol. 136, pp. 245-251, 2015, doi: https://doi.org/10.1016/j.chemosphere.2015.05.017
M. V. Villanueva, M. C. Luna, M. I. Gil, A. Allende, "Ultrasound treatments improve the microbiological quality of water reservoirs used for the irrigation of fresh produce," Food Res. Int., vol. 75, pp. 140-147, 2015, doi: https://doi.org/10.1016/j.foodres.2015.05.040
Notes
Author notes
ajinna.loaiza@udea.edu.cobainhoa.rubioc@udea.edu.cocgustavo.penuela@udea.edu.co
Conflict of interest declaration
