Resumen: Las enfermedades anorrectales benignas abarcan un amplio espectro de patologías comunes, que pueden causar una morbilidad significativa, la incidencia de estas afecciones es común y puede presentarse con una enfermedad avanzada y la extensión de la patología puede no reflejar con precisión la sintomatología. La diferenciación de estas afecciones benignas identifica a aquellas susceptibles de terapias conservadoras, de estilo de vida y basadas en tratamiento médico o quirúrgico. En este artículo se exponen las principales características de las mismas, fisiopatología, epidemiología, criterios diagnósticos y principales recomendaciones de tratamiento.
Palabras clave:trastornos anorrectalestrastornos anorrectales,hemorroideshemorroides,dolordolor,sangradosangrado,manometríamanometría.
Abstract: The anorectal benign diseases cover a wide spectrum of common pathologies, which can cause significant morbidity. The incidence of these conditions is common and may present with advanced disease and the extent of the pathology may not accurately reflect the symptoms. The differentiation of these benign conditions identifies those susceptible to conservative therapies, lifestyle changes and medical surgical treatment. In this article the main characteristics of these aliments, physiopathology, epidemiology, diagnostic criteria and main treatment recommendations are exposed.
Keywords: anorectal disorders, hemorrhoids, pain, bleeding, manometry.
Artículos
Fisiopatología, diagnóstico y manejo de las principales enfermedades anorrectales
Pathophysiology, diagnosis and management of the main anorectal diseases

Las enfermedades anorrectales benignas se encuentran definidas por síntomas específicos y cuyo diagnóstico en muchas oportunidades es por exclusión, en la actualidad se continúan estudiando estos trastornos, evaluándose diversas técnicas diagnósticas que permitan identificar las características y funcionalidad anal1. Por lo cual es común diferenciar las patologías como orgánicas o funcionales, dependiendo de la afectación1-3.
Los trastornos anorrectales son comunes y afectan aproximadamente al 25% de la població4., se han demostrado anormalidades estructurales o funcionales, ya sea anorrectales o en el piso pélvico en pacientes con síntomas como: dificultad para defecar, incontinencia fecal (IF), hemorragia rectal, dolor anorrectal y prolapso rectal. Diversos avances recientes en técnicas de diagnóstico, principalmente la manometría anorrectal, ultrasonografía y la defecografía de alta resolución y definición han expuesto de mejor manera los cambios anatómicos y funcionales con respecto a la fisiopatología de estos trastornos, que por lo general conllevan a un mejor tratamiento5.
Generalmente los síntomas son subreportados, en un estudio el 2% de las consultas de práctica general fueron reservadas por síntomas anales y del total, solo 10% de pacientes informaron síntomas después del interrogatorio en la consulta. El sangrado rectal fue la queja más común, seguido por el dolor anal6. El riesgo de hemorragia rectal causado por malignidad subyacente es bajo, alrededor de 3,4%, pero aumenta a 9,2% si se combina con un cambio en el hábito evacuatorio intestinal7.
Trastornos como la IF se encuentran definidos por síntomas específicos, sin embargo, aquellas patologías funcionales de la defecación requieren a su vez tener síntomas y pruebas diagnósticas anorrectales normales8. En la actualidad este tipo de enfermedades se interroga mediante la ayuda de cuestionarios que reportan síntomas intestinales, no obstante, es prudente que se le interrogue al paciente con respecto a los hábitos diarios y síntomas que incluso pueden pasar desapercibidos, por lo cual es indispensable realizar una investigación completa de los mismos9.
En la presente investigación se evaluarán las características clínicas, fisiopatología, métodos de diagnóstico y estrategias terapéuticas, de los principales diagnósticos de la patología anorrectal.
ANATOMÍA Y FISIOLOGÍA DEL PISO PÉLVICO
Se debe poseer el conocimiento de los mecanismos normales de defecación y continencia, ya que estos procesos son claves y dependen de la integridad funcional y anatómica de los músculos del piso pélvico y el sistema nervioso10. El elevador del ano es una unidad bastante compleja que consiste en varios grupos musculares: pubococcígeo, ileococcígeo y puborectal, este grupo muscular forma parte fundamental del sostén de los órganos pélvicos, en estado basal el elevador del ano atrae las partes distales de la uretra, vagina y recto hacia los huesos del pubis11.
La función antes descrita mantiene la angulación anorrectal y de esta manera se crea una barrera mecánica para el flujo de las heces y el mantenimiento de la función de continencia12. En las capas superficiales del piso pélvico se encuentran el esfínter anal interno (EAI) y el esfínter anal externo (EAE) adaptados mediante el tejido conectivo. Estas capas superficiales forman parte del control del proceso de evacuación de las heces de la ampolla rectal13, durante el proceso de defecación el individuo genera un esfuerzo voluntario aumentando la presión intraabdominal, asimismo se genera la contracción del recto y los músculos perineales, de manera simultánea se relajan los esfínteres anales y el puborectal, ensanchando el ángulo anorrectal y descendiendo el perineo, todos estos movimientos generan la evacuación de las heces14.
El piso pélvico recibe inervación de las ramas de las raíces nerviosas sacras de S2, S3 y S4, el nervio pudendo, los nervios perineales y los nervios simpático y parasimpático14. La descoordinación de los músculos del piso pélvico puede conducir a trastornos de la defecación, y el daño a estos músculos y nervios conduce a la IF. Del mismo modo, la disfunción de los nervios del piso pélvico puede causar hiposensibilidad rectal y control motor anormal que conduce a IF, estreñimiento o dolor rectal15. En los siguientes apartados se exponen los principales trastornos anorrectales:
INCONTINENCIA FECAL
Definición y Epidemiología
La IF se define como el paso no controlado de tipo recurrente de materia fecal a través del recto y su salida al exterior al menos por 3 meses, se encuentra en controversia el uso de la ropa interior sucia como criterio de diagnóstico, ya que esto puede deberse a higiene deficiente, prolapso rectal o hemorroides, sin embargo en la actualidad se continua utilizando para definir un probable caso de IF. Es importante excluir la secreción clara de mucosidad mediante un interrogatorio cauteloso, el no control de los flatos, no entra dentro de la clasificación de la IF, ha sido incluido en la incontinencia anal (IA) que es un trastorno multifactorial que puede ocurrir debido a condiciones que causen episodios de diarrea, disminución de la capacidad de almacenamiento colorrectal y debilitamiento del piso pélvico. La IF se considera anormal después de que se ha logrado el entrenamiento para ir al baño, generalmente alrededor de los 4 años de edad16.
Se han realizado grandes estudios poblacionales, los cuales han sugerido que la IF es común, y se ha reportado una prevalencia que oscila entre los 7 a 15% en las mujeres de la comunidad17-23, del 50 al 70% en centros de cuidado para ancianos24,25, en algunos casos la prevalencia es comparable entre sexo18,26, y en otros se expone una prevalencia menor en hombres con respecto a las mujeres27,28. Asimismo, se ha descrito una mayor prevalencia en mujeres blancas con respecto a las afroamericanas23,24, de igual manera hay reportes en los que no se llega a esta conclusión19,29, es importante destacar que la mayor proporción de individuos con este tipo de patologías son mujeres, no evidenciándose diferencias entre razas en los estudios de hombres30.
Las diferencias que se observan en la prevalencia de la IF pueden deberse a diferentes factores dentro de los que se encuentran diferentes encuestas utilizadas, diferencias en el tiempo de estudio o diversas preguntas al momento del contacto con el médico tratante16,18,31, así como en lo referente a los criterios diagnóstico utilizados. En un estudio comunitario de seguimiento (50 años en adelante), la incidencia de IF fue 7,0%32.
Etiología y factores de riesgo para la incontinencia fecal
Como se ha comentado previamente la IF tiene un origen multifactorial por lo cual es fundamental evaluar estos factores asociados, en estudios realizados a individuos en comunidades destacan como factores de riesgo las alteraciones del patrón evacuatorio, en especial la diarrea, urgencia rectal y enfermedades intestinales crónicas, estos factores fueron independientes de la lesión del piso pélvico relacionado con el acto obstétrico32,33. Por su parte, en un estudio realizado a 176 mujeres seleccionadas de manera aleatoria con IF y sin IF, se evidenció que en aquellas con IF la presencia de diarrea representó casi 7 veces más riesgo de presentar esta patología, 4 veces más con colecistectomía, casi 5 veces más aquellos que eran fumadores actuales, similar a lo referido al rectocele, 3 veces más cuando la mujer tenía incontinencia urinaria de esfuerzo y finalmente el índice de masa corporal elevado34.
La atrofia del esfínter externo también ha sido referido como factor de riesgo para la IF3,34, otras afecciones asociadas con IF incluyen edad avanzada, carga de enfermedad (recuento de comorbilidades, diabetes), traumatismo del esfínter anal (lesión obstétrica, cirugía previa) e inactividad física. De acuerdo con los hallazgos de estudios basados en la comunidad, la gran mayoría de las mujeres con IF que consultan a un médico pueden no tener un trastorno neurológico o inflamatorio, sino trastornos intestinales, generalmente diarrea, a menudo asociados con un historial de factores de riesgo obstétricos. Sin embargo, el déficit neurológico solo se puede identificar con pruebas neurofisiológicas, y éstas no están ampliamente disponibles35.
En una serie de casos reciente se identificó que el 8% de las mujeres que fueron sometidas a parto vaginal presentaron IF36, esto puede estar determinado por diferentes cambios que se han realizado en la práctica clínica actual, como lo son una disminución del uso de fórceps, ventosas y otros instrumentos, uso moderado de la episiotomía reservándola solo para los casos en los cuales realmente es necesario y una mayor incidencia de partos por cesárea, sin embargo, no obstante existen estudios en los cuales no existe diferencia entre los casos de IF de las mujeres sometidas a parto vaginal o cesárea37.
Las laceraciones de tercer grado (que involucran el EAE) y de cuarto grado (que se extienden a través de los esfínteres anales externos e internos) son fuertes factores de riesgo para la IA y la IF38. Un estudio prospectivo del National Institute of Health identificó un OR para IF casi 2 veces mayor para las mujeres con lesión del esfínter durante el parto en comparación con un grupo control39.
Fisiopatología
La continencia es mantenida por varios mecanismos, incluyendo factores anatómicos (cojines endovasculares, integridad del esfínter anal y músculo puborectal), sensación rectoanal, distensibilidad rectal, inervación, consistencia de las heces, movilidad y factores psicológicos que ya han sido expuestos previamente40.
La debilidad del esfínter anal se ha reportado como la anomalía más frecuente en la IF, entre las mujeres mayores aproximadamente el 40% tenía una presión anal de reposo disminuida y una presión de compresión reducida del 80%. La disfunción del EAI se describe por una relajación espontánea exagerada del mismo o una disminución de la presión de reposo41, se asocia con alteraciones estructurales como defectos tras una lesión obstétrica y/o adelgazamiento por esclerodermia, edad avanzada), esto se visualiza mejor con ultrasonografía. Entre las mujeres posparto, la gravedad de la IF fue mayor en mujeres con defectos del EAI42.
La debilidad del EAE se puede deber a uno de estos factores o a la combinación de los mismos: lesión del esfínter, miopatía o disminución del impulso nervioso cortico espinal, de igual manera el complejo de los músculos elevadores del ano juegan un papel fundamental, es decir que cualquier lesión a este nivel también contribuirá a la IF42. Los pacientes con descenso perineal excesivo tienen un ángulo anorrectal más obtuso, lo que sugiere que la válvula que normalmente mantiene la continencia cuando aumenta la presión intraabdominal está deteriorada43.
En los hombres la IF puede estar determinada por factores diferentes a los evidenciados en la mujer, dentro de los principales se encuentran la lesión anal iatrogénica, que ocurre posterior a procedimientos perianales44-48 o defecación disinérgica49, en donde la alta presión anal en reposo atrapa las heces durante la defecación y posteriormente las expulsa50, radioterapia o debilidad aislada del EAI51.
Evaluación clínica
Historia clínica
Es esencial desarrollar una buena relación con los pacientes con IF y con habilidad evaluar su gravedad, conocimiento de las evacuaciones, incluido el tipo (sólido, líquido y/o gas), la cantidad, la frecuencia y las condiciones predisponentes. Las manchas, suciedad y filtraciones reflejan la naturaleza y severidad de la IF52, la suciedad indica una fuga más extensa que la mancha de la ropa interior y puede ser mejor especificada (es decir, ensuciar la ropa interior o el mobiliario / ropa de cama). La caracterización del hábito intestinal es útil e importante debido a que puede dar indicios de la causa de estos signos53, se ha descrito de igual manera que el estreñimiento con impactación fecal es un factor de riesgo significativo en asilos de ancianos54.
Los antecedentes patológicos del individuo también deben tomarse en cuenta, debido a que la IF puede ser secundaria a algunas enfermedades como: esclerosis múltiple, neuropatía diabética o la esclerodermia55. Los pacientes que tienen incontinencia de urgencia refieren presentar la sensación del deseo de defecar, sin embargo, no llegan a tiempo al inodoro, mientras que los pacientes con incontinencia pasiva han disminuido o no tienen conciencia del deseo de defecar antes del episodio de incontinencia. Los pacientes con incontinencia de urgencia a menudo tienen presiones reducidas de compresión56y/o duración de compresión57, reducción de la capacidad rectal y aumento de la percepción de distensión rectal de la ampolla58, mientras que los pacientes con incontinencia pasiva a menudo tienen presiones de reposo más bajas56,57.
Pruebas de diagnóstico
Examen físico
Se debe realizar un examen físico que incluya evaluación rectal digital, asimismo se necesita un examen multisistémico, abdominal y un examen neurológico enfocado en los síntomas como la IF. El examen digital se realiza en una posición lateral izquierda y antes de administrar enemas o laxantes. Durante esta inspección es importante identificar cicatrices por una cirugía previa, lesión obstétrica, esfínter lesionado, dermatitis o residuos fecales a nivel rectal o perianal, un reflejo anocutáneo ausente en respuesta al acariciamiento suave de la región perianal sugiere deterioro del nervio. Después de la inspección, se debe realizar la palpación anorrectal digital, esto puede revelar debilidad o defectos del EAI y/o del puborectal, la impactación de las heces y la presencia de disinergia durante la defecación simulada. Una evaluación rectal meticulosa realizada por un examinador experimentado tiene un valor predictivo positivo de 67% y 81% para identificar bajas presiones de reposo y compresión, respectivamente59.
Las pruebas deben adaptarse al problema clínico del paciente, gravedad, posible etiología, impacto en la calidad de vida y la respuesta al tratamiento médico.
Endoscopia de vías digestivas inferiores
En los pacientes con diarrea o cambios en el patrón evacuatorio se debe considerar la realización de endoscopia de la mucosa rectosigmoidea o la colonoscopia completa con biopsias60.
Manometría
La manometría anorrectal (MAR) evalúa la continencia y los mecanismos de defecación mediante la determinación de la presión anal en reposo, que es predominantemente atribuible a la función del EAI (70%); presión de compresión: la fuerza y duración de la contracción voluntaria del EAE y contracción puborectal; presencia de un reflejo inhibidor del EAI; volumen umbral de distensión rectal requerida para provocar la primera sensación de distensión, una sensación sostenida de urgencia para defecar, y el volumen máximo tolerable, si el intento de defecación se acompaña de una mayor presión intraabdominal y relajación de los músculos del piso pélvico (normal) o por la contracción paradójica de los músculos del piso pélvico, que puede ser relevante a los síntomas. La compatibilidad anorrectal se puede evaluar mediante la determinación de la relación presión-volumen durante la distensión gradual de un globo de látex, pero es preferible hacerlo con un globo de polietileno compatible y un baróstato61.
Endosonografía de ano
La endosonografía de ano identifica el adelgazamiento del esfínter anal y/o defectos que a menudo no se reconocen clínicamente y pueden repararse quirúrgicamente60, o el adelgazamiento del EAI, mientras que la interpretación de las imágenes del EAE pueden plantear problemas técnicos. Por el contrario, la endosonografía tridimensional puede medir la longitud y el volumen del esfínter anal y su atrofia62,63, la ecografía vaginal puede proporcionar información adicional62.
Resonancia magnética
La imagen pélvica por resonancia magnética es la única modalidad de imagenología que puede visualizar tanto la anatomía del esfínter anal como el movimiento global del piso pélvico (es decir, compartimientos anterior, medio y posterior) en tiempo real sin exposición a la radiación64.
De esta manera, la endosonografía es la primera opción para la obtención de imágenes del esfínter anal en IF por su disponibilidad y el EAI se visualiza más claramente. La resonancia magnética es más útil para identificar la atrofia del EAE y un canal anal anormal, que es un marcador no solo de lesión del esfínter anal, sino de trastornos más allá de la lesión del esfínter, como daño a los cojines anales o denervación anal65.
Pruebas neurofisiológicas
Las pruebas neurofisiológicas pueden caracterizar trastornos en la inervación motora y sensorial de los músculos anorrectales y del piso pélvico, estas pruebas incluyen latencias del motor terminal del nervio pudendo, electromiografía (EMG), pruebas sensoriales rectoanales y potenciales motores evocados. Existen varias limitaciones metodológicas para las latencias motoras terminales del nervio pudendo, y se ha cuestionado la utilidad de esta medición. La aguja de EMG puede identificar lesiones neurogénicas o musculares. Recientemente, se han observado potenciales motores evocados rectales y anales prolongados en la mayoría de los pacientes con IF, lo que sugiere que la disfunción neurofisiológica juega un papel importante66.
Tratamiento
El tratamiento del paciente con IF debe enfocarse en la corrección de las manifestaciones clínicas, modificación del hábito evacuatorio con intervenciones dietéticas o farmacológicas ya que las heces blandas son un factor de riesgo importante para IF (la corrección de factores reversibles como laxantes u otros medicamentos puede ayudar). Los ensayos dietéticos (p. Ej., baja lactosa o baja fructosa) en pacientes seleccionados pueden normalizar la forma de las heces, entre los suplementos de fibra, solo psyllium pero no goma arábica o carboximetilcelulosa, mejoró la IF en comparación con el placebo67.
Por su parte, la loperamida administrada a una dosis adecuada (es decir, 2-4 mg, 30 minutos antes de las comidas) puede mejorar la consistencia de las heces y aumentar el tono interno del esfínter, reduciendo la incontinencia43. El difenoxilato, combinado con atropina, es una alternativa a la loperamida, pero puede haber efectos secundarios anticolinérgicos68. En un estudio abierto de 18 pacientes, la amitriptilina (20 mg diarios), que tiene efectos anticolinérgicos, mejoró la IF en la mayoría de los pacientes69.
Los pacientes con estreñimiento, impactación fecal e incontinencia por rebosamiento a menudo se benefician de un programa para aumentar el vaciamiento del colon por diferentes medios. Por ejemplo, un régimen basado en un laxante osmótico diario (lactulosa 10 ml dos veces al día) más un enema semanal fue útil en la mayoría de los pacientes ancianos con IF, incluidos aquellos con demencia70, sin embargo, ablandar las heces puede agravar la IF. Otras medidas destinadas a mejorar el vaciado rectal, como el uso de supositorios o enemas, suplementos de fibra, laxantes orales, y corrección de cualquier comportamiento anormal al defecar, o posicionamiento pueden ser útiles71. Con respecto al abordaje quirúrgico de la reparación del esfínter anal, aunque bien establecido, no parece ser efectiva a largo plazo.
DOLOR FUNCIONAL ANORRECTAL
Se han descrito tres tipos de trastornos de dolor funcional anorrectal: síndrome del elevador del ano, proctalgia fugax y síndromes no especificados, se distinguen principalmente por la duración del dolor y la presencia o ausencia de sensibilidad anorrectal. A pesar de algunas diferencias entre las series, existe una superposición significativa entre estas condiciones72.
SÍNDROME DEL ELEVADOR DEL ANO
Definición y Epidemiología
El síndrome del elevador del ano también se llama espasmo del elevador, síndrome del puborectal, proctalgia crónica, síndrome piriforme y mialgia de la tensión pélvica. El síndrome del elevador del ano se caracteriza por dolor anorrectal relativamente constante y/o frecuente, a menudo asociado con sensibilidad a la palpación del elevador del ano, pero no con síntomas urinarios o una enfermedad orgánica que pueda explicar el dolor72. En una encuesta, la prevalencia del dolor anorrectal debido a todas las causas y síntomas del síndrome del elevador del ano fue del 11,6% y 6,6%, respectivamente73.
Fisiopatología
En la actualidad se cree que el síndrome del elevador del ano es el resultado de un espasmo de los músculos del piso pélvico y a elevadas presiones en la región anal durante el reposo74. Sin embargo, un estudio aleatorizado controlado encontró características de defecación disinérgica y la mayoría (85%) tenían sensibilidad del músculo elevador. La disinergia se revirtió después de una bioretroalimentación exitosa, lo que sugiere que la incoordinación rectoanal puede ser una explicación fisiopatológica para este síndrome75.
Pruebas de diagnóstico
Evaluación clínica
El diagnóstico se basa principalmente en la presencia de síntomas característicos y hallazgos en el examen físico (ver definición). La evaluación a menudo incluye sigmoidoscopia, ultrasonografía e imágenes pélvicas para excluir enfermedades anorrectales alternativas.
Tratamiento
Los tratamientos incluyen estimulación electro galvánica; entrenamiento de bioretroalimentación; relajantes musculares como: metocarbamol, diazepam y ciclobenzaprina; masaje digital de los músculos elevadores del ano; y baños de asiento. Sin embargo, solo se informaron 2 ensayos controlados aleatorios, el primero se realizó en 157 pacientes con proctalgia crónica que recibieron estimulación eléctrica o masaje digital del elevador del ano y baños de asiento tibios o bioretroalimentación del piso pélvico más asesoramiento psicológico76. Entre los pacientes que informaron dolor a la palpación, el análisis mostró que el 87% informó un alivio adecuado del dolor rectal después de la bioretroalimentación, en comparación con el 45% para la estimulación eléctrica y el 22% para el masaje, esta mejora se mantuvo 12 meses después. En otro ensayo controlado aleatorizado, 12 pacientes fueron asignados al azar a inyecciones de esfínter anal con toxina botulínica A o placebo administrados en un intervalo de 3 meses; las inyecciones de toxina botulínica no mostraron diferencias a las inyecciones de placebo77.
PROCTALGIA FUGAZ
Definición y Epidemiología
La proctalgia fugaz se define como un dolor repentino y severo en el área rectal, que dura de unos segundos a varios minutos (raramente más de 30 minutos), y luego desaparece por completo78. El dolor se encuentra localizado en el recto en el 90% de los casos, con crisis infrecuentes que pueden ocurrir menos de 5 veces al año en el 51% de los pacientes75. Las características del dolor referidas por el paciente suelen ser, cólicos o dolor punzante, que puede llegar a ser incómodo incluso hasta insoportable78. Casi el 50% de los pacientes tuvieron que interrumpir su actividades normales durante una crisis, incluso pueden llegar a despertar al paciente durante el sueño78. La prevalencia de proctalgia fugax varió del 8% al 18% sin diferencias entre sexos, los síntomas rara vez comienzan antes de la pubertad pero se han reportado casos en niños de 7 años77-79.
Fisiopatología
La corta duración y la naturaleza esporádica e infrecuente de este trastorno han dificultado la identificación de mecanismos fisiopatológicos, pero las contracciones anormales del músculo liso pueden ser responsables del dolor80. Dos estudios citaron familias en las que se encontró una forma hereditaria de proctalgia fugaz, está asociada con la hipertrofia del EAI y el estreñimiento81. Las crisis de proctalgia fugax a menudo son precipitadas por eventos estresantes de la vida o ansiedad75, en un estudio no controlado a doble ciego la mayoría de los pacientes eran perfeccionistas, ansiosos y/o hipocondríacos78.
Pruebas de diagnóstico
Evaluación clínica
El diagnóstico se basa en la presencia de síntomas característicos como se describe en la definición y la exclusión de patologías anorrectales y pélvicas.
Tratamiento
Para la mayoría de los pacientes, los episodios son tan breves que el tratamiento remediador no es práctico y la prevención no es factible, el tratamiento normalmente consistirá en explicarle al paciente el problema. Sin embargo, los pacientes con síntomas frecuentes requerirán terapia; un ensayo aleatorizado controlado mostró que la inhalación de salbutamol fue más efectiva que el placebo para acortar la duración de los episodios de proctalgia en pacientes en quienes los episodios duraron 20 minutos o más82.
TRASTORNOS FUNCIONALES DE DEFECACIÓN
Definición y Epidemiología
El estreñimiento crónico se clasifica de manera general como el tránsito lento en el colon o disfunción de salida de las heces, aunque algunos pacientes pueden tener criterios para ambos. La disfunción de salida de las heces es considerada un desorden de defecación funcional, este se encuentra caracterizado por una contracción paradójica o relajación inadecuada de los músculos del piso pélvico durante el intento de la defecación; estos trastornos funcionales se encuentran relacionados de manera habitual con síntomas como esfuerzo excesivo, sensación de evaluación incompleta y la facilitación digital de las evacuaciones83. Sin embargo, los síntomas (por ejemplo, desimpactación digital, dolor anal) no distinguen consistentemente entre los pacientes con un trastorno funcional de defecación y los que no lo tienen83,84. Por lo tanto, los criterios para este deben basarse tanto en los síntomas como en las pruebas fisiológicas.
La prevalencia de los trastornos funcionales de la defecación en la población general es desconocida, debido a que su diagnóstico no solo se basa en las características clínicas, sino que se necesitan una serie de pruebas para poder determinarla, en los centros de atención a pacientes de tercera edad la prevalencia de defecación disinérgica entre los pacientes con estreñimiento crónico ha variado ampliamente del 20% al 81%85. Sin embargo, la prevalencia de disinergia puede haber sido sobreestimada debido a las altas tasas de falsos positivos observadas en algunos estudios86, en un centro de atención terciaria la prevalencia de disinergia fue 3 veces mayor en las mujeres que en los hombres, pero fue similar en los individuos más jóvenes y mayores87.
Pruebas de diagnóstico
Evaluación clínica
Una evaluación detallada de los síntomas intestinales (por ejemplo: esfuerzo prolongado o excesivo, sensación de evacuación incompleta después de la defecación, facilitación digital de la defecación) y un examen digital rectal meticuloso a menudo hacen pensar en un trastorno funcional de la defecación. Al momento de la entrevista se debe tomar en cuenta el interrogatorio de los hábitos evacuatorios diarios del individuo, debido a que no es suficiente solo con los cuestionarios generalmente utilizados, lo que por lo general puede generar sesgos en el estudio.
En un estudio el examen digital rectal tuvo una sensibilidad del 75% y una especificidad del 87% para detectar la disinergia, que se encuentra asociada con la contracción o falta de relajación del musculo puborectal y/o del esfínter anal, de igual manera la disminución del descenso perineal cuando el paciente intenta expulsar el dedo del examinador88.
Prueba de expulsión de globos
La expulsión rectal se puede evaluar pidiendo a los pacientes que expulsen globos llenos de agua o aire del recto89, el tiempo requerido para expulsar el globo depende del método utilizado y oscila entre 1 minuto para expulsar un globo de 50 ml lleno de agua a 2 minutos, se recomienda que el paciente se siente en una silla con inodoro detrás de una pantalla de privacidad90. La prueba de expulsión de globos es una prueba de detección útil para este tipo de trastornos, pero no define el mecanismo del desorden en la defecación. Debido a que el globo puede no simular las heces de los pacientes, un estudio de expulsión normal con globo no siempre excluye un trastorno de la defecación91.
Evaluación manométrica
Tradicionalmente, la MAR se ha considerado esencial para el diagnóstico del trastorno funcional de la defecación, esta prueba consiste en la medición de las presiones intrarrectales, la medición de las presiones anales y/o la actividad EMG durante el intento de defecación. Sin embargo, dada la superposición de los hallazgos en personas asintomáticas y pacientes con trastorno funcional de la defecación, los criterios precisos y la utilidad de la manometría para el diagnóstico de trastornos defecatorios se encuentran en evaluación constante. Además, la posición del cuerpo y los sistemas de manometría pueden influir en los hallazgos91.
Prueba de marcador radiopaco del tiempo de tránsito intestinal completo
Por sí mismo, el tránsito lento del colon no es diagnóstico de un trastorno primario de la motilidad colónica debido a que el estreñimiento por tránsito lento existe de forma aislada, o coexiste con un trastorno funcional de la defecación, y hasta dos tercios de los pacientes con un trastorno de defecación también presentan retraso del tránsito colónico92,93. En un estudio, el tránsito colónico mejoró después de la bioretroalimentación para disfunción de evacuación, que sugiere que la disfunción de evacuación fue responsable del tránsito colónico diferido93. El tiempo de tránsito colónico puede medirse obteniendo radiografías abdominales después de que los pacientes ingieren marcadores radiopacos94, una cápsula de motilidad inalámbrica, o mediante gammagrafía95-97.
Tratamiento
Históricamente, se han recomendado 2 tipos de entrenamiento del suelo pélvico que implican modificación del comportamiento: entrenamiento de bioretroalimentación en el que sensores de presión o EMG colocados dentro del ano y el recto proporcionan bioretroalimentación al paciente sobre la actividad muscular98 y defecación simulada en la que el paciente practica la evacuación98.99. La defecación simulada se ha combinado con el entrenamiento del músculo diafragmático pélvico por parte de algunos investigadores98,100.
FISURA ANAL
Definiciones y epidemiología
La fisura anal es una ruptura longitudinal similar a una úlcera en la línea media del canal anal, distal a la línea dentada; en casi el 90% de los casos una fisura idiopática se localiza en la línea media posterior, pero también puede ocurrir en la línea media anterior. Las fisuras en las posiciones laterales deberían despertar la sospecha de procesos patológicos como enfermedad de Crohn, tuberculosis, sífilis, VIH/SIDA, afecciones dermatológicas como psoriasis) y el carcinoma anal.
Una fisura aguda se ve como una simple rotura en el anodermo, mientras que una fisura crónica, definida con una duración de más de 8 a 12 semanas, se caracteriza además por edema y fibrosis. Las fibras del EAI pueden ser visibles en la base de la fisura, las características acompañantes típicas de las fisuras crónicas incluyen una "pila centinela" (etiqueta cutánea) en el margen distal de la fisura, y una papila anal hipertrofiada en el canal anal proximal a la fisura. El sello distintivo clínico de la fisura anal es el dolor durante la defecación y, a menudo, persiste después de la defecación. Con frecuencia existe la historia de una sensación de desgarro durante el paso de heces. El sangrado rectal, generalmente limitado a un mínimo de sangre roja brillante en el papel higiénico, también es frecuente101.
La fisura anal crónica se presenta como una úlcera no cicatrizante por el espasmo del esfínter y la consiguiente isquemia. El tratamiento para la fisura anal crónica generalmente se dirige a aliviar el espasmo y, como tal, es una afección predominantemente médica, con cirugía reservada para casos médicamente refractarios10.
Tratamiento de la fisura anal aguda
En esta patología se deben usar tratamientos no quirúrgicos como baños de asiento, fibra de psyllium y agentes de carga como primer paso en el tratamiento de la fisura aguda. Casi la mitad de todos los pacientes con fisura anal aguda sanará con medidas de soporte, es decir, baños de asiento, fibra de psyllium y agentes de volumen, con o sin la adición de anestésicos tópicos o ungüentos antiinflamatorios103. Además de la cicatrización de las fisuras, se puede lograr un alivio sintomático del dolor y la hemorragia prácticamente sin efectos secundarios.
Tratamiento de la fisura anal crónica
Por su parte, la fisura anal crónica se debe tratar con agentes farmacológicos tópicos, como bloqueadores de los canales de calcio o nitratos, se debe remitir a los pacientes que no responden al tratamiento conservador o farmacológico para las inyecciones locales de toxina botulínica o esfinterotomía anal interna quirúrgica95. La fisura anal crónica se puede tratar con nitratos tópicos, aunque los nitratos son marginalmente superiores al placebo con respecto a la cicatrización. Los medicamentos tópicos con nitrato como el 0,2% de pomada de nitroglicerina dos veces al día durante 6-8 semanas se han asociado con la curación en al menos el 50% de las fisuras crónicas tratadas, y el uso de nitroglicerina tópica disminuye significativamente el dolor durante el período de terapia.
La fisura anal crónica también se puede tratar con bloqueadores de los canales de calcio tópicos, con una incidencia más baja de efectos adversos que los nitratos tópicos. No hay datos suficientes para concluir si son superiores al placebo en la cicatrización de las fisuras anales. Los bloqueadores tópicos de los canales de calcio como el diltiazem al 2% aplicado dos veces al día durante 6-8 semanas se han asociado con la curación de la fisura anal crónica en el 65 al 95% de los pacientes104.
Debido a que el diltiazem tópico tiene una incidencia menor de cefalea y recurrencia de fisuras que la nitroglicerina tópica, puede ser el tratamiento tópico preferido por el paciente105. Los bloqueadores de los canales de calcio por vía oral pueden ser tan buenos como los bloqueadores de los canales de calcio tópicos, lo que sugiere que es más influyente el fármaco que la vía de administración106.
HEMORROIDES
Definiciones y epidemiología
Las hemorroides se encuentran entre los problemas anorrectales más comunes en el mundo industrializado, las estructuras normales del canal anal proximal llamadas almohadillas anales se renombran como hemorroides internas cuando sangran y/o sobresalen. Los signos cardinales de las hemorroides internas son el sangrado característico, definido como hemorragia indolora con deposiciones y protrusión intermitente y reducible. A menudo, el médico tratante tiene la función de proporcionar el diagnóstico de exclusión de hemorroides internas sintomáticas al descartar otras fuentes de sangrado y protrusión. La condición vagamente relacionada llamada hemorroides externa trombosada implica un coágulo en una vena debajo del anodermo que es la piel del borde anal107.
Diagnóstico
El diagnostico se realiza por historia clínica y examen físico, si hay sangrado la fuente a menudo requiere confirmación mediante estudios endoscópicos. El examen físico debe incluir una inspección visual del ano, tanto en reposo como durante el esfuerzo y un examen digital para descartar otra patología anal. Las hemorroides internas se pueden asignar con una calificación funcional basada en su historia: las hemorroides de primer grado (no prolapso), de segundo grado (prolapsadas), pero sí reducen, las hemorroides de tercer grado sobresalen y requieren reducción manual, y las hemorroides de cuarto grado sobresalen y no pueden ser reducidas. Las pruebas de laboratorio casi nunca son útiles, el diagnóstico clínico de las hemorroides generalmente incluye un sangrado de patrón hemorroidal que exige al menos una sigmoidoscopia para descartar otras fuentes de sangrado. En pacientes mayores de 50 años o con una historia familiar sugestiva, esta puede ser la ocasión para la evaluación del colon completo, generalmente mediante colonoscopia108,109.
Tratamiento de las hemorroides internas
Se deben tratar a los pacientes con hemorroides sintomáticas primero con un mayor consumo de fibra y líquidos adecuados, una revisión Cochrane demostró el beneficio del aumento de la ingesta de fibra en la reducción tanto del prolapso como del sangrado111, mientras que los laxantes tienen un papel limitado en el tratamiento inicial de las hemorroides112. Se debe aconsejar a los pacientes que eviten tensiones y limiten el tiempo que pasan en el inodoro, porque ambos están asociados con tasas más altas de hemorroides sintomáticas113.
Se debe considerar a los pacientes con hemorroides de primer a tercer grado que permanecen sintomáticos, después de modificaciones en la dieta, para procedimientos de consultorio como anillamiento, escleroterapia, coagulación por infrarrojos y la ligadura, siendo esta última probablemente la opción más efectiva.
Existen muchas técnicas invasivas para reducir el tamaño, desvascularizar y cicatrizar los cojines anales para disminuir el sangrado y la protrusión, estos procedimientos ambulatorios son relativamente bien tolerados, todos muestran tasas de recurrencia variables, y todos pueden requerir una aplicación repetida114. Debido al riesgo de hemorragia importante, los procedimientos ambulatorios generalmente deben evitarse en pacientes con trombocitopenia o uso de warfarina, productos de heparina y agentes antiplaquetarios como el clopidogrel. La ligadura con banda de caucho (banda) es el tratamiento más popular y eficaz para las hemorroides internas, esta puede lograrse a través de un anoscopio rígido o usando un endoscopio flexible retroflexionado con un accesorio de ligadura114.
La ligadura es probablemente el tratamiento de elección para las hemorroides de segundo grado y es un tratamiento de primera línea razonable para las hemorroides de tercer grado. El uso de la succión para colocar la hemorroide para la ligadura es algo menos doloroso y causa menos sangrado que las pinzas, aunque ambos métodos son aceptables115.
Se deben referir para intervenciones quirúrgicas (hemorroidectomía, hemorroidopexia con grapas y ligadura de la arteria hemorroidal asistida por Doppler) a aquellos pacientes que son refractarios o no toleran los procedimientos ambulatorios, que tienen fisuras externas grandes y sintomáticas junto con sus hemorroides, que tienen hemorroides grandes de tercer grado o que tienen hemorroides de cuarto grado. La hemorroidectomía tradicional sigue siendo muy efectiva, cuando se comparó con los procedimientos ambulatorios, la hemorroidectomía fue más efectiva para las hemorroides grado III, pero más dolorosa y tuvo una mayor tasa de complicaciones116. La hemorroidectomía estándar deja heridas abiertas o cerradas117, y se puede realizar con una variedad de dispositivos quirúrgicos, ninguno de los cuales muestra una clara ventaja sobre los otros118.
La hemorroidopexia con grapas es una alternativa establecida a la hemorroidectomía en la mayoría de los casos, la ligadura de la arteria hemorroidal asistida por Doppler usa un anoscopio equipado con Doppler para identificar y ligar las arterias que suministran las hemorroides internas. Un posible beneficio comparativo es que se extirpa menos tejido, aunque esto puede no abordar el problema de la redundancia, así como otras operaciones. Las tasas de éxito son comparables a las informadas tanto para la hemorroidectomía como para la hemorroidopexia con grapas119, aunque todavía no se han realizado estudios comparativos.
Tratamiento de hemorroides externas trombosadas
La mayoría de los pacientes que presentan una urgencia (dentro de ~ 3 días de inicio) con una hemorroide externa trombosada se benefician de la escisión, aunque las hemorroides externas trombosadas tratadas sin escisión eventualmente resolverán sus síntomas, la extirpación de hemorroides externas trombosadas proporciona una resolución más rápida, una menor incidencia de recurrencia y mayores intervalos de remisión110. La mayoría de las extirpaciones se pueden realizar con seguridad en el consultorio o en la sala de emergencias, con una inyección de un anestésico local. La trombosis se debe extirpar junto con la piel suprayacente para dejar una herida abierta, en lugar de simplemente incidir y drenar.
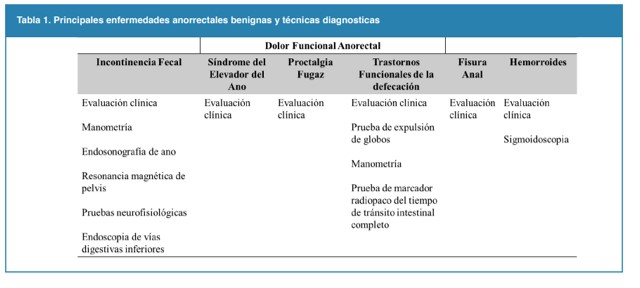
La prevalencia de afecciones anorrectales en el entorno de atención primaria es alta, aunque en la actualidad existen métodos diagnósticos para los mismos, estos no se encuentran disponibles en todos los centros de atención, por lo cual es fundamental realizar un adecuado interrogatorio y examen físico con la finalidad de llegar a un diagnóstico apropiado y oportuno, para establecer un tratamiento adecuado Tabla 1. Asimismo, además de reconocer trastornos anorrectales benignos comunes, los médicos deben mantener un alto índice de sospecha de trastornos inflamatorios y malignos.
Tabla 1. Principales enfermedades anorrectales benignas y técnicas diagnosticas
jonathan_35_@hotmail.com
