Artículos

Esta obra está bajo una Licencia Creative Commons Atribución-SinDerivar 4.0 Internacional.
Recepción: Febrero , 28, 2021
Aprobación: Marzo , 15, 2021
Publicación: Agosto , 10, 2021
DOI: https://doi.org/10.5281/zenodo.5451093
Resumen: La caries dental es una enfermedad infecciosa, crónica y multifactorial. Se estima que afecta del 60-90% de niños escolares, así como también a un considerable número de adultos. La presencia de caries dental se encuentra determinada por factores ambientales, genéticos y microbianos incluyendo la flora bacteriana habitual, malos hábitos alimenticios, infrecuencia en el cepillado dental e ineficiente higiene oral, exposición al flúor, fluido y composición salival, iones, proteínas y anatomía, y estructural dental. Según diversos estudios el padecimiento de caries se debe a factores genéticos, con un 60% de riesgo y a elementos del genoma del huésped. En la actualidad, se han reportado investigaciones de un modelo genético que podría estar relacionado con la etiología de la caries basándose según su susceptibilidad en: genes según el desarrollo morfológico del esmalte dental, genes según la preferencia de ciertos sabores, genes según la vía de señalización y genes según el Antígeno Leucocitario Humano (HLA).
Palabras clave: genoma, polimorfismo, caries dental, genética.
Abstract: Dental caries is an infectious, chronic, and multifactorial disease. It is estimated that it affects 60-90% of school children, as well as a considerable number of adults. The presence of dental caries is determined by environmental, genetic, and microbial factors including the usual bacterial flora, poor eating habits, infrequent tooth brushing and inefficient oral hygiene, exposure to fluoride, fluid and salivary composition, ions, proteins and anatomy, and dental structure. According to various studies, caries disease is due to genetic factors, with a 60% risk, and to elements of the host's genome. Currently, investigations of a genetic model that could be related to the etiology of caries have been reported based on its susceptibility according to: genes according to the morphological development of tooth enamel, genes according to the preference of certain flavors, genes according to the pathway of signaling, and genes according to the Human Leukocyte Antigen (HLA).
Keywords: genome, polymorphism, dental caries, genetics.
INTRODUCCIÓN
Desde 1930 se inició la investigación de la relación entre factores genéticos y la presencia de caries dental, los estudios fueron realizados inicialmente en animales y en la actualidad los polimorfismos genéticos en humanos siguen siendo motivo de análisis. La producción de ácidos por parte de microrganismos Gram positivos, como es el caso del Streptococo Mutans, provoca la desmineralización de la estructural dental. Debido a la ingesta frecuente de sacarosa, se ha planteado que el uso prolongado de chicles que contienen “Xilitol”, considerado no cariogénico al no fermentar microorganismos, reduce los recuentos de esta bacteria en la placa dental y en la saliva1-3.
El papel de los factores genéticos en la aparición y desarrollo de la caries dental, así como su interacción con factores medioambientales aún es motivo de intensa investigación. La siguiente revisión incluye varios reportes de los últimos 2 años (2018-2020), obtenidos a partir de la búsqueda organizada en distintas fuentes de información bibliográfica (secundaria y primaria) como lo son PubMed y Genes Cards.
ASPECTOS GENERALES
En la actualidad se han reportado estudios de un modelo genético que podría estar relacionado con la etiología de la caries, producto de un efecto pleiotrópico en el cual varios genes son susceptibles para incentivar el desarrollo de caries, principalmente por genes dominantes.
La etiología de la caries depende de 4 grupos de genes según la susceptibilidad individual4:
1. Genes según el desarrollo morfológico del esmalte dental: causa colonización inmediata de microrganismos, por no cumplir la función protectora.
2. Genes según la preferencia de ciertos sabores: causa en el humano el consumo excesivo de carbohidratos y azúcares.
3. Genes según la vía de señalización: causa enfermedades genéticas, las cuales se manifiestan en la saliva y en la función protectora.
4. Genes según el HLA: causa la ausencia de respuesta inmunitaria por parte de HLA (principal sistema presentador de antígenos).
Asimismo, diversos estudios realizados confirman múltiples análisis de polimorfismo de un solo nucleótido (SNP) para cada gen, analizados mediante una prueba de desequilibrio de transmisión (TDT)5. El cuerpo humano posee células madre, que son líneas celulares indiferenciadas capaces de formar ciertos tipos de células en el organismo, las que pueden ser genéticamente manipuladas y potencialmente usadas como fuentes de renovación celular para reparar la función de los tejidos dentales5.
GENES QUE CODIFICAN LAS PROTEÍNAS DEL ESMALTE DENTAL
La dentina y el esmalte sirven como bóvedas para el desarrollo, crecimiento y proliferación de microrganismos causantes de caries dental. Los defectos en el esmalte dental, el cual forma parte de la morfología del diente, crean una biopelícula que se adhiere a la pieza dental, facilitando un entorno favorable para la propagación de los desechos bacterianos, de tal manera que se han detectado tres niveles de susceptibilidad (bajo, medio y alto), lo cual se relaciona íntimamente con la composición arquitectónica y dureza del esmalte, la porosidad y fase cristalina6.
En la Amelogénesis Imperfecta (AI), que se caracteriza por trastornos hereditarios, clínicos y genéticamente heterogéneos, se ha encontrado alteraciones en los genes que codifican las proteínas del esmalte dental como la Amelogenina (AMELX), Enamelina (ENAM), Tuftelina (TUFT1), Enamelisina (MMP-20), Ameloblastina (AMBN) y Calicrenina (KLK-4); estos genes determinan fenotipos de acuerdo con la alteración en cada estadio de la formación del esmalte dental. Adicionalmente, se sabe que más o menos alrededor del 5% de los casos con AI genera cambios en el gen AMELX y heredan un patrón ligado al cromosoma X6.
Estos genes permiten clasificar la enfermedad según:
1. Fenotipos:
1.1. AI. Hipoplasia
1.2. AI. Hipocalcificada
1.3. AI. Hipomadurativa
1.4. AI. Hipomadurativa con taurodontismo
2. Modo de herencia en:
2.1. Autosómica dominante
2.2. Autosómica recesiva
2.3. Ligadura a cromosoma X
Según investigaciones realizadas en niños escolares turcos con caries tempranas, se cree que el gen Tuftelina (TUFT1) parece tener ciertos genotipos que interactúan con elevadas concentraciones de Streptococo Mutans, al igual que los genotipos del gen Ameloblastina (AMBN) con respecto a la microdureza del esmalte6.
La variación del gen Amelogenina (AMELX) demostró codificar para el gen metaloproteinasa 20 (MMP-20) y controlar la formación de cristales dentales además de promover la mineralización, la misma que participa en el desarrollo inicial del esmalte dental y en la formación de caries. Su mínima incidencia en la producción de caries se relaciona con la presencia de un alelo T, que se observó en estudios realizados en Rio de Janeiro (Brasil) a personas descendientes de africanos entre los cinco y catorce años así como en adultos. En este reporte se observó una variante en el cromosoma X (Xp22.31) que parece afectar la transcripción de esta proteína, originando la disminución en la producción de caries. Además, se demostró un incremento de la sensibilidad para sufrir caries cuando los prismas del esmalte crecen de manera desorganizada6.
Por su parte, el gen ENAM demostró tener un patrón de herencia autosómico dominante y un recesivo cuando se trata de una mutación en el gen MMP-207. Actualmente, se están realizando estudios con una nueva expresión entre un gen y células madre postnatales de la pulpa dental “POST-NATAL DENTAL PULP STEM CELLS” (DPSCs) y células madre de estroma médula ósea “BONE MARROW STROMAL STEM CELLS” (BMSSCs). Para la obtención de estas expresiones génicas se necesitan secuencias de ADN que se clasifican en8:
a) Promotores simples: resultado de una gran variedad de genes diferentes.
b) Intensificadores: identificadores de genomas virales que pueden considerarse también como una superposición de secuencias de ADN que aumentan de forma independiente9.
c) Regiones reguladoras: corresponde a una secuencia de ADN que interacciona con proteínas para asegurar la correcta especificidad tisular o expresión temporal específica, en este caso usando tecnología como los sistemas de análisis de secuenciación de ADN tales como el GF211. Esta es una red muy precisa de alta densidad de muestras de ácido nucleico de una sola cadena; dicha tecnología permite comparar dos o tres hibridaciones9.
Genes que codifican proteínas del esmalte
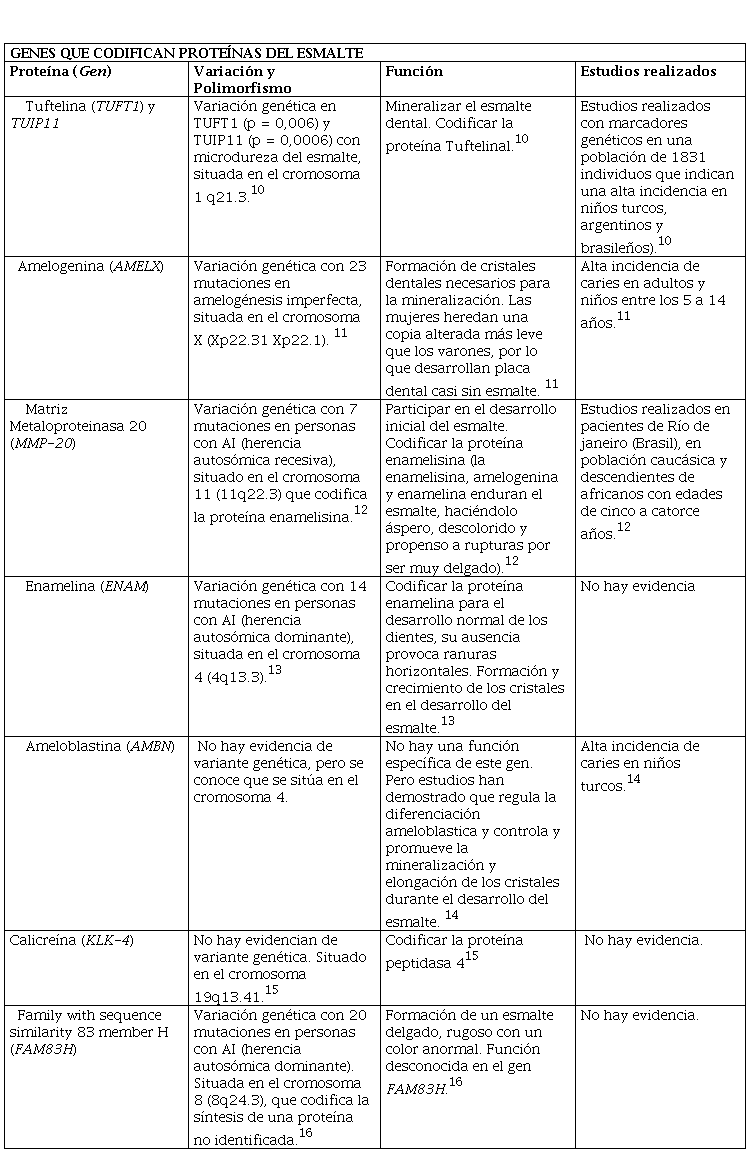
GENES RELACIONADOS AL SENTIDO DEL GUSTO
En estudios realizados recientemente se demuestra que la percepción del sabor amargo del vinotinto se encuentra influenciada por al menos 25 genes funcionales de TAS2R, que se caracterizan por ser genes altamente polimórficos de amplia gama a respuestas fenotípicas de estímulos amargos, los mismos que se relacionan con moléculas como: taninos, flavan-3-oles, fracciones de polimerasa de ácidos tánico, atocianinas, procianidinas y catequinas. Estas variantes polimórficas se encuentran determinadas por genes asociados al sabor y receptores gustativos afectados principalmente por el alcohol17.
Mediante un enfoque de aleatorización mendeliana se han identificado varios genes TAS (TAS2R4, TAS2R5, TAS2R39 y TAS2R7) encargados de activar compuestos polifenólicos propios del vinotinto18. El gen TAS2R38 se caracteriza por participar en los procesos biológicos dentales en niños, los cuales cambian notablemente al llegar a la adultez, encargándose de codificar la proteína de sensación del gusto (6-n-propiltiouracilo “PROP”), la que determina la sensación de amargura y astringencia generadas por una bebida alcohólica. El receptor TAS ha identificado un heterodímero que participa como receptor de preferencia para el dulce y estos son: TAS1R2 – TAS1R3, hoy en día se desconoce su mecanismo.
Es importante tener en cuenta que, debido a trastornos genéticos, existen personas que no tienen papilas gustativas o las poseen en escasa cantidad, imposibilitando la capacidad de percibir sabores, por lo que pequeños cambios en la secuencia de aminoácidos en los genes TASR2 y R3, generan diferencias en la señalización intercelular con respecto a los edulcolorantes mediante la modificación de la secuencia de ADN19.
Genes relacionados el sentido del Gusto
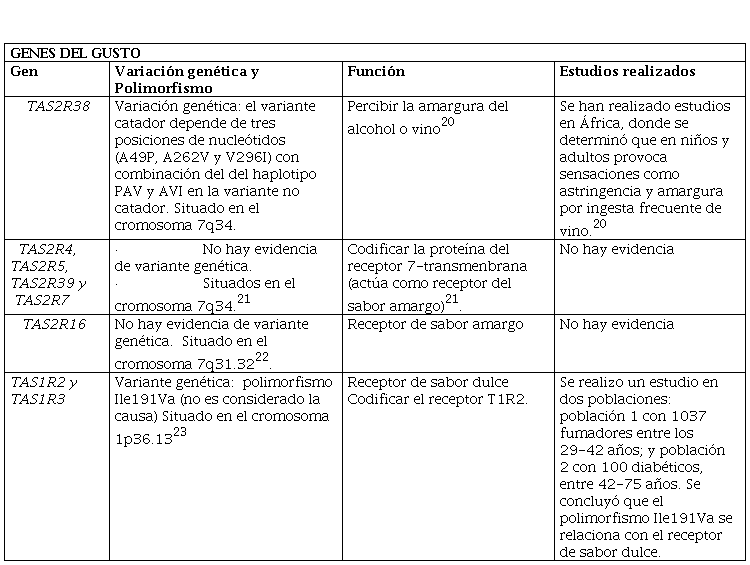
GENES DE VÍAS DE SEÑALIZACIÓN
En las caries dentales se ha distinguido diversos genes que se encuentran relacionados a la vía de señalización de MAPK tales como RPS6KA2 y PTK2B, los mismos que varían según la dentición permanente, que es aquella que se forma después de la dentición temporal y no existen cambios en la placa dental durante toda la vida24.
Los genes RHOU, FZD1 y TLR2 son los encargados de participar en la respuesta inmune ante la presencia de caries dental, y por último los genes ADMTS e ISLI presentan una baja susceptibilidad a las caries, ubicados en la región 5q12.1-5q1324.
Estudios realizados en la población de Rio de Janeiro, Brasil demuestran que el gen Factor de Transcripción Básico 3 (BTF3) estudia la saliva y la sensibilidad a la caries dental; dicho gen es necesario para la transcripción de un complejo al unirse a la RNA polimerasa IIB, el cual puede modificar diferentes isoformas y estudia también la activación del factor nuclear kB1, el mismo que puede asociarse a la aparición de células tumorales24.
Genes de Vía de Señalización
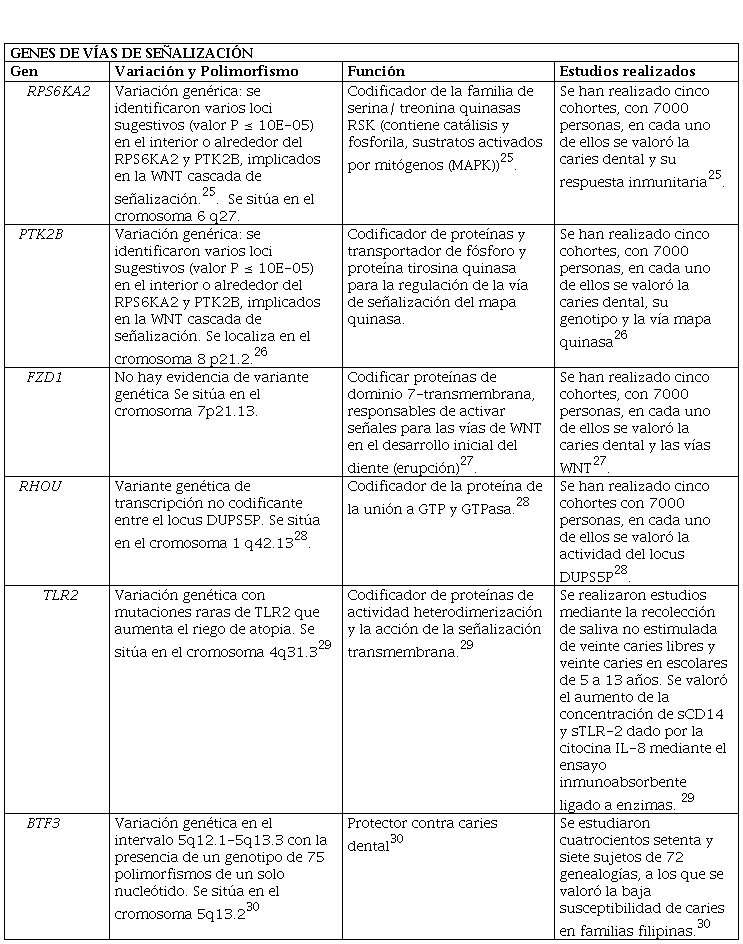
GENES DEL ANTÍGENO LEUCOCITARIO HUMANO
El antígeno leucocitario humano o HLA, es una familia de genes que se relaciona íntimamente con el complejo mayor de histocompatibilidad o MHC, tales como:
a. MHC clase I, depende de tres genes, como son: HLA-A, HLA-B y HLA-C.
b. MHC clase II, depende de seis genes, como son: HLA-DPA1, HLA-DPB1, HLA-DQA1, HLA-DQB1, HLA-DRA y HLA-DRB1.31
Los alelos que participan en la lucha contra bacteria codifican la molécula de HLA clase II, puesto que presenta antígenos con alta eficacia en relación a la clase I. Se sabe que el Streptococcus Mutans representa ser un importante factor con respecto a las alteraciones a nivel del esmalte dental y la predisposición de presentar infecciones cariogénicas, según estudios realizados en Japón32.
Asimismo, estudios realizados en EE.UU, en mujeres afrodescendientes, demostraron que el HLA de clase II y sus alelos correspondientes activan el crecimiento de microorganismos cariogénicos como el Streptococcus Mutans, Lactobacilos Acidophilus y Lactobacilos Casei33. Aunque algunos reportes señalan que si no existe la presencia de microorganismos en la cavidad oral, no tiene por qué existir caries dental en la misma, aunque no es dato confirmado se plantea como dato curioso.
Otras investigaciones realizadas denotan una hipótesis de alta importancia, donde el HLA-II y los antígenos de clase I y II inmunodominantes son los encargados de dar una respuesta netamente sensible al encontrarse en la superficie del Streptococcus Mutans y otros microorganismos cariogénicos letales, también se demostró la existencia del gen HLA-DR4, que aumentaría la susceptibilidad a presentar caries debido a que se altera la presentación de antígenos I y II, expresando los siguientes genes: HLA-DRA1, DRA2, DR3 y DRW634.
Genes del antígeno leucocitario humano
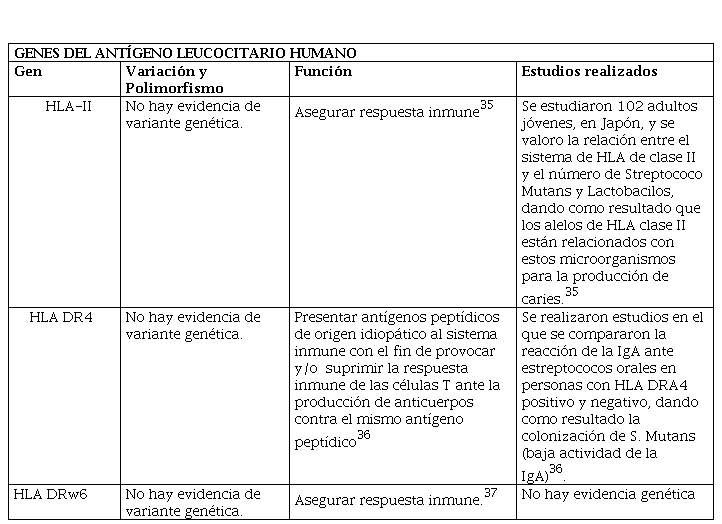
CONCLUSIÓN
La caries dental es una enfermedad crónica, infecciosa y multifactorial que afecta a un importante porcentaje de la población general, incluyendo a niños y adultos. El padecer caries está determinado por varios factores, entre ellos: ambientales, microbianos y por supuesto genéticos; los mismos que dependen según el desarrollo morfológico del esmalte dental, según la percepción de ciertos sabores, según la vía de señalización y según el HLA.
BIBLIOGRAFÍA
1. Weber M, Søvik JB, Mulic A, Deeley K, et al. Redefining the Phenotype of Dental Caries. MEDLINE. 2018 Enero 25; 52(4): p. 263-271.
2. Wendell S, Wang X, Brown M, Cooper ME, DeSensi RS, Weyant RJ, et al. Taste Genes Associated with Dental Caries. Journal of Dental Research. 2010 Septiembre 21; 89(11): 1198-202.
3. Gutierrez S, García D, Santacoloma S, Mejía J. Caries dental: ¿Influyen la genética y la epigenética en su etiología? Universitas Odontologica 2017;32(69), 83-92..
4. Trevilatto RWMMP. A critical review: an overview of genetic influence on dental caries. PUBMED - US National Library of Medicine National Institutes of Health. 2010 Septiembre 15; 16(7): p. 613-623.
5. . Toors F,. Chewing gum and dental health. Literature review. Rev Belge Med Dent. 1992; 47(3): 67-92.
6. Russell R. How Has Genomics Altered Our View of Caries Microbiology? Kanger. 2008 Septiembre; 42(5): 319–327.
7. Piekoszewska-Ziętek P, Turska-Szybka Anna, Olczak-Kowalczyk D. Single Nucleotide Polymorphism in the Aetiology of Caries: Systematic Literature Review. Karger. 2017 Agosto; 51(4): p. 425-435.
8. Shimizu T, Ho B, Deeley K, Briseño-Ruiz J, Faraco Jr I, Schupack BI, Brancher JA, et al. Enamel formation genes influence enamel microhardness before and after cariogenic challenge. PLoS One. 2012 Septiembre 24; 7(9): p. 2- 4.
9. IVAMI. [Online]. España; 2017 [cited 2019 Enero 29. Available from: HYPERLINK "https://www.ivami.com/es/pruebasgeneticas-mutaciones-de-genes-humanos-enfermedades-neoplasias-yfarmacogenetica/2378-pruebas-geneticas-amelogenesis-imperfecta-amelogenesis-imperfecta-genes-i-amelx-enam-mmp20-i-y-i-fam83h-i" https://www.ivami.com/es/pruebasgeneticas-mutaciones-de-genes-humanos-enfermedades-neoplasias-yfarmacogenetica/2378-pruebas-geneticas-amelogenesis-imperfecta-amelogenesis-imperfecta-genes-i-amelx-enam-mmp20-i-y-i-fam83h-i .
10. Rocha-Buelvas A. La incursion de la genetica en la regeneracion de los tejidos dentales. Revista centro de estudios en salud. 2015 Julio; 2(9): 48-58.
11. Haznedaroğlu E, Koldemir-Gündüz M, Bakır-Coşkun N, Bozkuş HM, Çağatay P, Süsleyici-Duman B, Menteş A. T Association of sweet taste receptor gene polymorphisms with dental caries experience in school children. Caries Res. 2015;49(3):275-81..
12. Carrai M, Campa D, Vodicka P, Flamini R, Martelli I, Slyskova J. Association between taste receptor (TAS) genes and the perception of wine characteristics. Sci rep. 2017 Agosto 23; 7 (1): 9239.
13. Lips A, Santos Antunes L, Azeredo Antunes L, Vaz Braga Pintor A, et al. Salivary protein polymorphisms and risk of dental caries: a systematic review. Braz Oral Res 2017 Jun 5;31:e41.
14. Triantafillou V, Workman AD, Kohanski MA, Cohen N. Taste Receptor Polymorphisms and Immune Response: A Review of Receptor Genotypic-Phenotypic Variations and Their Relevance to Chronic Rhinosinusitis. Front Cell Infect Microbiol. 2018 Mar 7;8:64.
15. Yildiz G, Ermis RB, S Calapoglu NS, Celik EU, Türel GY. Gene-environment Interactions in the Etiology of Dental Caries. J Dent Res. 2016;95(1):74-9.
16. Tobar Suárez CX. Detección de las mutaciones g.14917delT y g.12573C> ubicadas en el exón 10 del gen enamelina (ENAM) en pacientes de familias afectadas con amelogénesis imperfecta de tipo hipoplásica. 2012; Disponible en http://repositorio.uchile.cl/handle/2250/111776
17. Hidalgo Gato- Fuentes Iliana, Duque de Estrada Riverón Johany, Pérez Quiñones José Alberto. La caries dental: Algunos de los factores relacionados con su formación en niños. Rev Cubana Estomatol . 2008; 45( 1 ): 2-14
18. Upadhyaya J, Singh N, P Bhullar R, Chelikani P. The structure-function role of C-terminus in human bitter taste receptor T2R4 signaling. Biochim Biophys Acta . 2015;1848(7):1502-8.
19. GeneCards. GeneCards The Human Genes database. [Online].; 2017 [cited 2018 Abril 29. Available from: HYPERLINK "https://www.genecards.org/cgi-bin/carddisp.pl?gene=TAS2R4" https://www.genecards.org/cgi-bin/carddisp.pl?gene=TAS2R4 .
20. Pereira DDV. Clinica PropDental.; 2018 (consultado:8/4/21) 2020 Disponible: HYPERLINK "https://www.propdental.es/blog/odontologia/diferencias-entre-los-dientes-temporales-y-los-dientes-permanentes/" https://www.propdental.es/blog/odontologia/diferencias-entre-los-dientes-temporales-y-los-dientes-permanentes/ .
21. Shimizu T, Deeley K, Briseño J. Fine-Mapping of 5q12.1–13.3 Unveils New Genetic Contributors to Caries. Kanger. 2013; 47: p. 273-283.
22. Rioboo Crespo M, Bascones A, Rioboo García R. El HLA y su implicación en Odontología. Av Odontoestomatol. 2005; 21( 2 ): 95-107.
23. Shuler, CF. Inherited risks for susceptibility to dental caries. J Dent Educ. 2001; 65: 1038-45.
24. Wang X, Shaffer JR, Zeng Z, Begum F, Vieira AR, et al. Genome-wide association Scan of dental caries in the permanent dentition. BMC Oral Health. 2012;12:57.
25. Roux P, Stephanie A R, John B. Phosphorylation of p90 ribosomal S6 kinase (RSK) regulates extracellular signal-regulated kinase docking and RSK activity». Mol. Cell. Biol. 2003;23 (14): 4796-804..
26. González Sanz Ángel Miguel, González Nieto Blanca Aurora, González Nieto Esther. Salud dental: relación entre la caries dental y el consumo de alimentos. Nutr. Hosp. 2013; 28( Suppl 4 ): 64-71.
27. Mobley C, Marshall TA, Milgrom P, Coldwell SE. The contribution of dietary factors to dental caries and disparities in caries. Acad Pediatr 2009; 9 (6): 410-4.
28. Cards G. FDZ1 Gene (Protein Coding). Gene Card The Human Genes. 2018;: p. 3-6.
29. Cards G. RHOU Gene. Gene Cards The Human genes. 2017;: p. 1-3.
30. Cards G. TLR2 Gene. Gene Cards The Human Genes. 2018;: p. 3-5.
31. Zhao A, Blackburn C, Chin J, Srinivasan M. Soluble toll like receptor 2 (TLR-2) is increased in saliva of children with dental caries. BMC Oral Health. 2014;14:108.
32. Costa SM, Martins CC, Bonfim Mde L, Zina LG, Paiva SM, Pordeus IA, Abreu MH. A systematic review of socioeconomic indicators and dental caries in adults. Int J Environ Res Public Health. 2012;9(10):3540–3574..
33. Cards G. BTF3 Gene. Gene Cards The Human genes. 2017;: p. 2-6.
34. Yarzabek B, Zaitouna AJ, Olson E, et al. Variations in HLA-B cell surface expression, half-life and extracellular antigen receptivity. Elife. 2018;7:e34961
35. Opal S, Garg S, Jain J, Walia I. Genetic factors affecting dental caries risk. Aust Dent J. 2015;60(1):2-11.
36. Wieczorek M, Abualrous ET, Sticht J, et al. Major Histocompatibility Complex (MHC) Class I and MHC Class II Proteins: Conformational Plasticity in Antigen Presentation. Front Immunol. 2017;8:292.
37. Werneck RI, Mira MT, Trevilatto PC. A critical review: an overview of genetic influence on dental caries. Oral Dis. 2010 Oct;16(7):613-23.
Notas de autor
javiteri@uce.edu.ec
