Artículos
Técnicas de Craneoplastía, luego de craniectomía descompresiva. Revisión de tres casos
Cranioplasty techniques, after decompressive craniectomy. Review of three cases
Técnicas de Craneoplastía, luego de craniectomía descompresiva. Revisión de tres casos
Archivos Venezolanos de Farmacología y Terapéutica, vol. 39, núm. 8, pp. 960-966, 2020
Sociedad Venezolana de Farmacología Clínica y Terapéutica

Esta obra está bajo una Licencia Creative Commons Atribución-SinDerivar 4.0 Internacional.
Recepción: 28 Septiembre 2020
Aprobación: 15 Octubre 2020
Publicación: 09 Diciembre 2020
Resumen: Se presentan tres casos clínicos en diferentes escenarios luego de una hemorragia intraparenquimatosa espontanea en el primer caso y de trauma craneoencefálico grave en el segundo y tercer caso en los que se realizó craniectomía descompresiva y en los cuales posteriormente se efectuó la reconstrucción craneal utilizando malla de titanio, cemento a base de metacrilato; y en el último caso malla de PEEK confeccionado en impresora 3D. Realizamos un repaso de las indicaciones y beneficios de la craneoplastia, así como sus complicaciones, además revisaremos las diferentes técnicas que se han venido realizando con el paso del tiempo y de los diferentes materiales empleados, haciendo una revisión comparativa en lo que concierne a biocompatilidad e índice de complicaciones.
Palabras clave: craneoplastía, craniectomía descompresiva, accidente cerebrovascular, trauma craneoencefálico.
Abstract: Three clinical cases are presented in different settings after spontaneous intraparenchymal hemorrhage in the first case and severe head trauma in the second and third cases in which decompressive craniectomy was performed and in which cranial reconstruction was subsequently performed using titanium mesh, cement based on methacrylate; and in the last case PEEK mesh made on a 3D printer. We review the indications and benefits of cranioplasty, as well as its complications, in addition we will review the different techniques that have been carried out over time and the different materials used, making a comparative review regarding biocompatibility and complication rate.
Keywords: cranioplasty, decompressive craniectomy, cerebrovascular accident, head trauma..
Introducción
Diversos padecimientos neuroquirúrgicos que producen hipertensión endocraneana requerirán en su tratamiento la realización de una craniectomía descompresiva como medida terapéutica de salvataje; entre estas entidades tenemos: trauma craneoencefálico, enfermedad cerebrovascular hemorrágica o isquémica, neuroinfección, tumores cerebrales, citando la más frecuentes. Con la finalidad de dar lugar a la reconstrucción del defecto craneal se planeará en un plazo mediato la reconstrucción de la misma, no sólo con la finalidad estética y para brindar protección, sino también para aliviar el síndrome del trepanado que pueden presentar estos pacientes y de ésta manera inclusive obtener una mejoría neurológica tras la reposición del colgajo óseo, como lo indican diferentes estudios. Diferentes estudios indican otros beneficios como mejoría en el flujo sanguíneo cerebral y en la dinámica del líquido cefalorraquídeo (LCR) y metabolismo cerebral.1
Existen diversos modelos y materiales que se utilizan para realizar craneoplastia, desde el hueso autologo guardado en un bolsillo subaponeurotico en el abdomen, hasta prótesis preformadas o e inclusive diseñadas en impresora 3D u otros materiales que se usan dando forma manualmente durante la cirugía. Los materiales sintéticos que se usan principalmente son titanio, metilmetacrilato y PEEK (polieter éter cetona)1,2.
A pesar de ser la craneoplastia un procedimiento electivo y relativamente simple se puede presentar diversas complicaciones como infección, que inclusive puede presentarse a largo plazo y en algunos casos el único tratamiento es retirar el material autologo o sintético utilizado. Otras complicaciones son hematomas, tromboembolismo pulmonar, higromas subdurales, fistulas, convulsiones, reabsorción del colgajo óseo, hidrocefalia1-6.
Caso Clínico 1, reconstrucción craneal con malla de titanio preformada: Paciente masculino de 40 años de edad, llevado al servicio de emergencia por presentar cefalea holocraneana de gran intensidad seguido de pérdida súbita de la conciencia, es llevado al Hospital Homero Castanier Crespo, hallándose parálisis del hemicuerpo del lado izquierdo y desviación de la comisura labial del mismo lado. Al examen neurológico; paciente estuporoso, con escala de coma de Glasgow: Apertura Ocular: 2, respuesta motora: 5 y respuesta verbal: 3, con un total de 10/15, hemiplejia fascio-braquio-crural izquierda, babinsky izquierdo. Se realiza Tomografía axial computarizada simple de cráneo evidenciándose imagen hiperdensa en región parietooccipital derecha en relación a hemorragia intraparenquimatosa, volumen: A x B x C/2 = 40ml (diámetros A: anteroposterior, B: transversal, C: altura) que ejerce efecto de masa y desplaza estructuras (Figura 1).
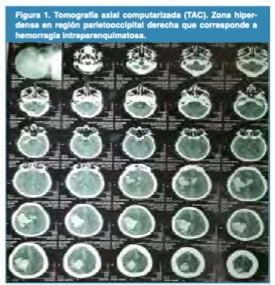
Figura 1.
Tomografía axial computarizada (TAC). Zona hiperdensa en región parietooccipital derecha que corresponde a hemorragia intraparenquimatosa .
Tratamiento y evolución: Se realizó craniectomía descompresiva (figura 2) y manejo neurointensivo, luego de 12 días de hospitalización se decide alta.
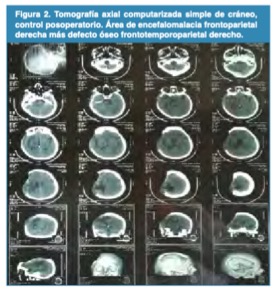
Figura 2.
Tomografía axial computarizada simple de cráneo, control posoperatorio. Área de encefalomalacia frontoparietal derecha más defecto óseo frontotemporoparietal derecho.
A los tres meses de posoperatorio paciente con índice de Karnofsky de 80, con hemiparesia braquiocrural izquierdo daniels 3/5, se programó electivamente craneoplastía con malla de titanio preformada a los 8 meses post- craniectomía descompresiva (figura 3), hasta los 12 meses operatorios paciente con evolución favorable.
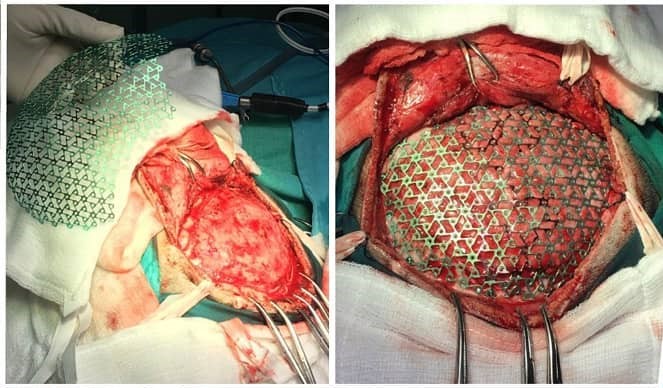
Figura 3.
Colocación malla de craneoplastía de titanio luego de craniectomía descompresiva.
Caso Clínico 2, reconstrucción craneal con cemento/ metilmetacrilato. Paciente masculino de 26 años de edad, sufre accidente de tránsito en moto, llevado por paramédicos al Hospital IESS- Babahoyo. paciente somnoliento, con escala de coma de Glasgow: Apertura Ocular: 3, respuesta motora: 4 y respuesta verbal: 3, con un total de 10/15, anisocoria pupilar, pupila izquierda 4mm, derecha 2mm hiporreactivas.
Tratamiento y evolución: Se realizó craniectomía descompresiva mas evacuación de hematoma subdural agudo. A los tres meses de posoperatorio paciente con índice de Karnofsky de 70, con hemiparesia braquial izquierda daniels 4/5. En la figura 4, se puede evidenciar el control tomografía antes y después de la craneoplastia. Se empleó para la reconstrucción craneal, cemento de metilmetacrilato (figura 5) a los seis meses post- craniectomia descompresiva; hasta los 12 meses posoperatorios paciente con evolución favorable.
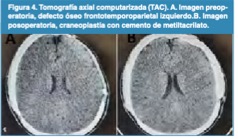
Figura 4.
Tomografía axial computarizada (TAC). A. Imagen preoperatoria, defecto óseo frontotemporoparietal izquierdo.B. Imagen posoperatoria, craneoplastia con cemento de metiltacrilato.
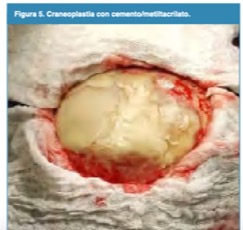
Figura 5.
Craneoplastia con cemento/metiltacrilato.
Caso Clínico 3, reconstrucción con prótesis preformada de PEEK confeccionada con impresión 3D. Paciente masculino de 34 años de edad, sufre accidente de tránsito en vehículo. A la valoración paciente somnoliento; con escala de coma de Glasgow: Apertura Ocular: 2, respuesta motora: 4 y respuesta verbal: 2, con un total de 8/15.
Tratamiento y evolución: Se realiza TAC simple de cráneo evidenciándose hematoma subdural agudo frontotemporoparietooccipital y múltiples contusiones cerebrales, que ejerce efecto de masa. Se realizó craniectomía descompresiva, con cuidado neurocrítico indicando el alta luego de 18 días de hospitalización. A los nueve meses de posoperatorio paciente con índice de Karnofsky de 90, se programó electivamente craneoplastía con prótesis preformada de PEEK (figura 5 y 6); hasta los 12 meses operatorios paciente con evolución favorable
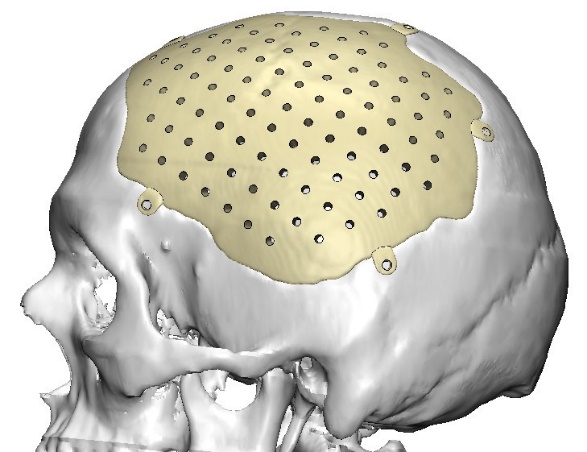
Figura 6.
Proyecto anatómico pre quirúrgica con prótesis de PEEK.
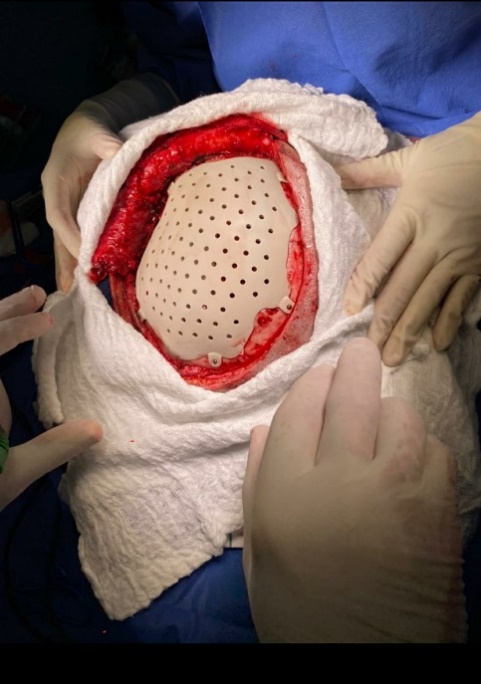
Figura 7.
Craneoplastia con prótesis preformada de PEEK confeccionada con impresión 3D.
Discusión
El término “Síndrome del trepanado o trefinado” fue acuñado por Grant y Norcross en el año de 1939, Ann Surg. para nominar una entidad infrecuente que causaba complicaciones a los pacientes sometidos a craniectomías amplias, definiéndolo como un conjunto de síntomas como cefalea, mareos, fatiga, sensaciones inespecíficas de la zona operada, dificultad en la concentración, trastornos amnésicos, cambios en el humor e intolerancia a las vibraciones, los cuales desaparecieron ose revertían con la craneoplastía. El primer caso de este síndrome fue descrito por Yamaura y Makino en 1977., en las cuales estas manifestaciones cedieron tras la reposición ósea. Este cuadro fue definido también como "Síndrome del colgajo hundido". En la actualidad se emplean en forma indistinta, los términos “síndrome del craniectomizado, trefinado, postcraniectomía7.
Hasta la fecha la fisiopatología se cree que es multifactorial, las cuales incluyen alteraciones hemodinámicas del líquido cefalorraquídeo, cambios en el metabolismo y flujo sanguíneo cerebral, presión ejercida por el gradiente atmosférico y movimientos del parénquima. En condiciones basales un individuo en decúbito dorsal presenta una presión del LCR de 15 cm H2O y en posición erecta una presión de 0 a nivel de la cisterna magna y -8 cm de H2O en los ventrículos. Esta presión negativa en un paciente craniectomizado genera un efecto vacuum o suctor que se adiciona a la presión atmosférica positiva en sentido opuesto, favoreciendo la depresión de flap cutáneo y el tejido cerebral subyacente. Además, este hundimiento provoca colapso del espacio subaracnoideo, contribuyendo a la alteración de la dinámica normal del LCR7,8.
En pacientes craniectomizados se presenta disminución del flujo arterial como decremento del retorno venoso. La disminución del flujo arterial ocurre como consecuencia del aumento de la resistencia vascular secundaria a la transmisión de la presión atmosférica a los vasos sanguíneos cerebrales, así como también debido a la distorsión de los vasos sanguíneos por desviación de las estructuras de la línea media. El retorno venoso, por su parte se ve afectado por la compresión cerebral focal en el sitio del hundimiento. En conjunto estos fenómenos contribuyen a la disminución de la pulsatilidad del cerebro hundido y al efecto vaccum sobre el colgajo7,8.
La craneoplastía es el medio quirúrgico más antiguo, fueron practicados por muchas civilizaciones en la antigüedad. Hay una amplia gama de evidencia en Perú de "cirujanos" preincaicos que realizaron dicho procedimiento 3.000 años A.C. Se has descubierto cráneos trepanados incaicos junto a conchas y placas de plata y oro. Además, hay evidencia de cráneos con estos materiales colocados en el sitio cubriendo el defecto craneal.
El caso más representativo es un cráneo que data de 2000 antes de Cristo hallado en el cerro Colorado (Paracas-Perú). Este presentaba un defecto frontal izquierdo cubierto con una placa de oro de 1 mm de espesor. Se dice que la reconstrucción con metales preciosos quedaba limitada para las clases sociales más altas, mientras que el empleo de elementos más débiles y comunes se aplicaba a las clases sociales bajas9.
Diversos autores de la antigua Asia, Egipto, Grecia y Roma aportan pocas innovaciones respecto a las culturas previas. La primera craneoplastía exitosa con injerto óseo fue descrita por Job Janszoon van Meekeren, cirujano holandés que trato a un noble ruso que había sufrido una pérdida de una porción craneal tras el impacto de una espada. La reconstrucción se procedió con un fragmento craneal de un perro muerto adaptándolo al defecto9.
A comienzos del siglo XIX, los nativos de los mares del Sur utilizaban la cascara de coco como material para craneoplastía y en el reciente siglo XX se empleó cuerno de búfalo como material reconstructivo9.
Por muchos años, se han desarrollado y estudiado varios tipos de materiales en un intento de satisfacer las necesidades de cada paciente al momento de realizar una craneoplastia. Dentro de estos materiales se incluyen: metales como el titanio (ti), acrílicos como el polimetilmetacrilato (PMMA), plásticos como la poliéter éter cetona (PEEK) y otros tipos de materiales que incluyen huesos de cemento o biocerámicas como la hidroxiapatita.
La comparación directa entre todos los materiales disponibles hoy por hoy, sumada a los escasos estudios disponibles hasta la fecha nos coloca en una verdadera encrucijada al momento de decidir que material debemos utilizar.
Sin embargo, y a pesar de la limitada investigación, en este trabajo se ha recabado información relevante de estudios que han puesto a prueba y comparado de alguna manera estos materiales.
Naturalmente al momento de elegir que material usar en el acto quirúrgico, elegiremos aquel que menos complicaciones nos traiga a corto y largo plazo tomando siempre en cuenta la disponibilidad del mismo en nuestro medio, al igual que su costo.
En cuanto a los diferentes materiales utilizados actualmente, nos referiremos a los utilizados en los casos presentados: titanio, metacrilato y PEEK.
Las placas de titanio ofrecen una excelente opción para la craneoplastía en términos de resistencia, baja tasa de infección, alta biocompatibilidad, inercia biológica y características de manejo favorables. A menudo la utilización de este material se evita debido a la capacidad del titanio para conducir el frio y el calor, y los altos costos asociados. A pesar de todo esto, la craneoplastía con placas de titanio hechas a medida se ha utilizado en colgajos óseos infectados, contaminación del colgajo óseo en la lesión inicial y resorción o espiración del colgajo óseo, respectivamente 54%, 14% y el 10% de los 113 pacientes cuyos resultados a largo plazo fueron analizados retrospectivamente (con un seguimiento mínimo de 6 meses) por Posada, Meneses y Moreno22. En esta serie, las complicaciones fueron comunes (n=33; 29%), particularmente la infección que requirió la eliminación de la placa (n¼18; 16%). Los defectos de cráneo grandes se asociaron con una mayor tasa de complicaciones (P¼0,009), en particular infección (P¼0,04), que se observó en el 32% de las hemicráneoplastias y el 19% de las craneoplastias bifrontales, mientras que solo el 9,2% de las pequeñas se infectaron10,11.
El polimetilmetacrilato es una resina acrílica moldeable que ofrece fuerza y protección similar al tejido óseo nativo, y su utilidad en la craneoplastía se ha establecido desde hace mucho tiempo. Las resinas acrílicas son estables, químicamente inertes, no se ven afectados por la temperatura, no conductivos, económicos, bien tolerados por los tejidos y se colocan y modifican fácilmente, y el PMMA es uno de los aloplásticos más biocompatibles materiales actualmente disponibles10,11.
La utilización de metilmetacrilato se ha convertido en una opción de tratamiento seguro y practico, ya que evita la toma de injertos óseos, preservando el hueso con menor morbilidad. Empero se necesita el uso de tecnología, es de mayor costo y su fijación e integración pueden ser complejas ya que conlleva mayor prevalencia de infección, mayor reacción tisular y rechazo. En contraste con todo esto, asimismo tiene múltiples ventajas, entre las que destacan la resistencia, estabilidad y biocompatibilidad que el material presenta, así como ser radiotransparente, lo que provoca mínimos artefactos en la resonancia magnética y con una rigidez y resistencia similares al hueso, pero con bajo peso en comparación con este. De todos los materiales disponibles, este es el de menor costo11,12. Este material tiene ya varias décadas de uso, desde que fue descrito por primera vez en un artículo en 194917. En el mismo estudio realizado por Souza et al18 donde compararon el PMMA con otros materiales (hueso autólogo, titanio, cerámica e hidroxiapatita) se demostró que el PMMA es el tercer material con mayores complicaciones, siendo superado por el hueso autólogo y la hidroxiapatita, mientras que la cerámica fue el que menor porcentaje de complicaciones tuvo18.
PEEK (polieter éter cetona) es un polímero semicristalino aromático que es resistente a altas temperaturas y radiaciones, con una rigidez y resistencia similar a la de un hueso cortical y cuya naturaleza inerte impide la degeneración mecánica o química y la liberación de sustancias citotóxicas. Gracias a su estabilidad a temperaturas de hasta 300 °C, las prótesis fabricadas con este material se pueden esterilizar en calor húmedo o seco sin alteraciones dimensionales. Su baja densidad parece también proporcionar a los pacientes una mayor comodidad, especialmente en quienes se necesitan implantes grandes12,13. Según metaanálisis, los implantes de este material desarrollaron complicaciones postoperatorias en un 15.3% de los casos, con una tasa de reintervención necesaria del 8.7%17.
El titanio ha sido usado con mayor frecuencia respecto al PEEK con la excepción de que este último es el favorito en cuanto a reparación de defectos amplios se refiere, gracias a que otorga mayor facilidad al momento de la cirugía, se puede moldear artesanalmente a diferencia del titanio que es un material definitivo12.
En 2011 Camarin et al.i23 describió un paciente de reconstrucción de defecto óseo frontal vía PEEK- PSI (Synthes, Jacksonville, FL) después de una lesión cerebral traumática con fractura conminuta. El equipo de neurocirugía había realizado inicialmente una cranealización del seno frontal, pero a los 2 años de la primera intervención la paciente fue remitida a los equipos de cirugía y traumatología oral y maxilofacial, quejándose de un problema estético en el tercio superior de la cara. Se utilizó un implante de PEEK-PSI para recontornear esta zona, y el seguimiento postoperatorio no reveló signos de infección posterior y que los contornos anatómicos y los resultados estéticos se mantuvieron 18 meses después de la intervención quirúrgica. La tomografía computarizada mostró una buena adaptación del implante a las estructuras óseas, y los autores concluyeron que PEEK-PSI es una opción segura, estética y funcionalmente exitosa en la reconstrucción de defectos óseos craneofaciales10,13.
A pesar de la craneoplastia ser un procedimiento quirúrgico electivo, no está exento de complicaciones. Las principales complicaciones referidas en revisiones sistémicas fueron: reabsorción del colgajo óseo, hematoma epidural, seromas, fractura de la prótesis, desplazamiento protésico, hidrocefalia e infecciones (superficiales y profundas), siendo las últimas las más frecuentes17.
La reabsorción del colgajo óseo, también denominado osteonecrosis aséptica, es una complicación muy conocida luego de la craneoplastía en especial en pacientes pediátricos. Su incidencia oscila entre el 7,2 y 50% Los factores que se ha demostrado que aumentan el riesgo de reabsorción ósea son fracturas múltiples, fragmentación ósea, mayor tamaño del defecto, edad más joven y la presencia de derivaciones ventriculoperitoneales. Además, la reabsorción del colgajo óseo puede dar como resultado un defecto grande, lo que aumenta el riesgo de daño cerebral o propiedades cosméticas inaceptables para el paciente. Se debe utilizar craneoplastía y materiales sintéticos cuando se prevé una osteonecrosis tardía14,15.
Bowers y col. evaluaron retrospectivamente 54 pacientes pediátricos que se sometieron a craneoplastía después de CD (craniectomía descompresiva). Aproximadamente el 50% de los pacientes desarrollaron reabsorción del colgajo óseo14,15.
En un estudio llevado a cabo en el Instituto de Ciencias Médicas Sher I Kashmir de la donde se compararon los resultados de craneoplastía artificial utilizando malla de titanio y metilmetacrilano vs pacientes sometidos a craneoplastia con materiales autólogos se encontraron complicaciones en el 15,26% de todos los pacientes –las más comunes- infección y dehiscencia de la herida. La infección de la herida se observó en el 10% de los pacientes sometidos a craneoplastia artificial versus el 6.12% de los pacientes que recibieron un procedimiento autólogo, en resumen, el grupo autólogo tuvo un total de 14.79% de complicaciones en comparación con el 17.5% del grupo artificial4.
A pesar de que el material aloplástico ofrece mayor resistencia, bajo o nulo porcentaje de reabsorción y menor dificultad para su remodelación, tiene mayor prevalencia de infección, reacción tisular y rechazo, así como un elevado costo3. En varios centros médicos se prefiere la reconstrucción craneal con prótesis de metilmetacrilato que siempre se cubre con fascia lata después de fijarla en su sitio definitivo. El uso de metilmetacrilato es una opción segura y práctica que evita injertos óseos y menor morbilidad, sin embargo, su uso requiere tecnología, altos costos y su fijación e integración pueden ser complejas, pues están acompañadas de prevalencia de infección, reacción tisular y rechazo. Sus ventajas son varias entre las que destacan la resistencia, estabilidad y biocompatibilidad, es radiotransparente lo que provoca mínimo efecto en la RMN12,20.
Por último, el material más utilizado en craneoplastía es la malla de titanio, las historias clínicas de diversos pacientes que han recibido esta prótesis, evidenciaron mínimas reacciones adversas a este material mientras que el metilmetacrilato presentó complicaciones tempranas que fueron resueltas en la estadía hospitalaria.. Otra pequeña parte de pacientes presentó complicaciones tardías, incluso causando rechazo en algunos21.
El titanio ofrece baja tasa de infecciones y buena integración ósea pero su costo es elevado y tiene pobre maleabilidad sumado a que ejerce un efecto artefacto durante resonancia magnética o tomografía computarizada, del otro lado el metilmetacrilato es un polímero resistente durable de bajo costo, con mejor efecto estético pero la infección y reacciones inflamatorias son algunas de sus desventajas18,21.
Resaltando una vez más el hecho de que cualquiera que sea el material elegido, puede presentar la misma prevalencia de exposición si no se le otorga una adecuada cobertura y se desarrolla de la manera correcta.
Actualmente no hay estudios que soporten diferencias significativas en las tasas de infección entre colgajos autólogos o sintéticos, ni diferencias en otro tipo de complicaciones.
Dentro de los injertos metálicos, el titanio es actualmente el único material utilizado para reparar los defectos craneales, fue introducido en la década de los sesenta y en la actualidad es usado como una alternativa a la craneoplastía –con hueso autólogo- post craniectomía de gran tamaño gracias a su fuerza, biocompatibilidad, y su escaso riesgo de reacciones alérgicas17.
En una revisión sistemática de la literatura realizada por de Souza et al18 se observó que las tasas de complicaciones entre el PMMA y el titanio eran prácticamente similares.
En otra revisión sistemática llevada a cabo por Andrabi, Sarmast, Kirmani y Bhat19, se concluyó que la complicación más común después de una craneoplastia con malla de titanio era la infección con un rango de frecuencia entre el 4-15%.
La tasa de infección del sitio quirúrgico después de CD (Craniectomia Descompresivs) / craneoplastía osciló entre el 2,3% y el 20%. En una revisión sistemática de Becking et al. Al comparar las craneoplastías autólogas con las craneoplastías aloplásticas, se encontró que el riesgo global de infección era del 5,6%. Sin embargo, dependiendo de los materiales utilizados en la craneoplastía, el riesgo de infección varía; Se encontró que la craneoplastía autóloga tenía el mayor riesgo (6,9%) y la craneoplastía con hidroxiapatita (3,3%) tenía el menor riesgo de infección. En otro estudio, se encontró que la infección era la complicación más común, con un riesgo del 8,7%, y se observó un riesgo adicional de infección en pacientes sometidos a craneoplastía bifrontal versus craneoplastía hemisférica o bihemisférica unilateral. Los predictores de infección del sitio quirúrgico después de una craneoplastía autóloga eran el tamaño del defecto del cráneo y los niveles de glucosa en sangre14,16.
Así mismo se describe Hidrocefalia, como complicación. Existen múltiples causas que pueden contribuir a la hidrocefalia en pacientes sometidos a craneoplastía después de CD (Craniectomia Descompresivs), incluida la hemorragia intraventricular, la hemorragia subaracnoidea o la propia CD. La hidrocefalia post-DC fue evidente en el 2% y el 29% de los pacientes. Dos revisiones sistemáticas mostraron un mayor riesgo de hidrocefalia después de una craneoplastía temprana, lo que podría atribuirse a la hidrocefalia pre-craneoplastia y al hecho de que la craneoplastía tardía puede proporcionar más tiempo para la resolución espontánea de la hidrocefalia14,16.
Conclusiones
La craneoplastia, como técnica de reconstrucción quirúrgica debe ser adaptada individualmente a cada paciente. Sin embargo, en nuestro servicio hemos podido realizar la reconstrucción de los defectos craneales con diferentes materiales, obteniéndose resultados favorables con el uso de prótesis preformada de PEEK confeccionada con impresión 3D y mallas de titanio preformadas en defectos que sobrepasen los 10 cm. Haciendo uso de cemento/ metilmetacrilato para defectos menores de 10 cm. Retomando la idea previa no existe hasta hoy material 100% efectivo, la elección del mismo dependerá de las condiciones del paciente y la disponibilidad del material, así como la economía del paciente. En nuestro servicio, sugerimos la reconstrucción a los 6 meses posterior la craniectomía descompresiva. Sería interesante realizar estudios empíricos sobre sobre las afectaciones a zonas cerebrales derivadas del coronavirus (24,25,26) relacionados con aspectos emocionales (27) y educativos (28,29,30).
CONFLICTOS DE INTERESES
Los autores declaran que no existen conflicto de Intereses.
AGRADECIMIENTOS
Laboratorio de Psicometría del Centro de Investigación, Innovación y Transferencia de Tecnología de la Universidad Católica de Cuenca (CIITT) y a la Carrera de Medicina y Enfermería de la Universidad Católica de Cuenca sede Azogues.
DERECHO A LA PRIVACIDAD Y CONSENTIMIENTO INFORMADO. Se solicitó el consentimiento informado por escrito a los pacientes que participaron en este estudio, para la publicación de éste artículo.
FUENTE DE FINANCIACIÓN
Los autores declaran que no existió ningún tipo de financiamiento.
BIBLIOGRAFIA
1. Paredes I, Castaño-León AM, Munarriz PM, et al. Cranioplasty after decompressive craniectomy. A prospective series analyzing complications and clinical improvement. Neurocirugia (Astur). 2015;26(3):115-125. doi:10.1016/j.neucir.2014.10.001
2. Jitender Chaturvedi, Ragasudha Botta, A. R. Prabhuraj, Dhaval Shukla, Dahnanjay I. Bhat, B. Indira Devi. (2016) Complications of cranioplasty after decompressive craniectomy for traumatic brain injury. British Journal of Neurosurgery 30:2, pages 264-268.
3. Ee Shern Liang, Geoffrey Tipper, Lyn Hunt, Peter Yee Chiung Gan. (2016) Cranioplasty outcomes and associated complications: A single-centre observational study. British Journal of Neurosurgery 30:1, pages 122-127.
4. Goedemans T, Verbaan D, van der Veer O, et al. Complications in cranioplasty after decompressive craniectomy: timing of the intervention. J Neurol. 2020;267(5):1312-1320. doi:10.1007/s00415-020-09695-6
5. Salunke P, Garg R, Kapoor A, Chhabra R, Mukherjee KK. Symptomatic contralateral subdural hygromas after decompressive craniectomy: plausible causes and management protocols. J Neurosurg. 2015;122(3):602-609. doi:10.3171/2014.10.JNS14780
6. Wan Y, Shi L, Wang Z, et al. Effective treatment via early cranioplasty for intractable contralateral subdural effusion after standard decompressive craniectomy in patients with severe traumatic brain injury. Clin Neurol Neurosurg. 2016;149:87-93. doi:10.1016/j.clineuro.2016.08.004
7. Aguirre Emilio A, Cuello Javier F, Purves Cynthia P. Coma secundario a síndrome del trefinado. MEDICINA (Buenos Aires). 2018;78(4):282-5.
8. Halani SH, Chu JK, Malcolm JG, et al. Effects of cranioplasty on cerebral blood flow following decompressive craniectomy: a systematic review of the literature. Neurosurgery 2017; 81: 204-16.
9. Zubilaga Rodríguez I SAG, Montalvo Moreno J. Reconstrucción craneal con biomateriales revision historica y estado actual. Rev Esp Cir Oral y Maxilofac. 2007;29(2):79-89.
10. Zanotti B, Zingaretti N, Verlicchi A, Robiony M, Alfieri A, Parodi PC. Cranioplasty: Review of Materials. The Journal of craniofacial surgery. 2016;27(8):2061-72
11. Zhong S, Huang GJ, Susarla SM, et al. Quantitative analysis of dualpurpose, patient-specific craniofacial implants for correction of temporal deformity. Neurosurgery 2015; 11:220–229.
12. Ugalde-Vitelly J, Palacios-Juárez J, Carpinteyro-Espín U, Ríos-Lara R, Del Vecchyo-Calcáneo C. Craneoplastía en deformidad postraumática y postquirúrgica, 18 años de experiencia en el Hospital General de México: una opción reconstructiva segura. Cir plást iberolatinoam. 2017;43(2):157-62.
13. Feroze AH, Walmsley GG, Choudhri O, et al. Evolution of Cranioplasty techniques in neurosurgery: historical review, pediatric considerations, and current trends. J Neurosurg 2015; 123:1098–1107.
14. Alkhaibary A, Alharbi A, Alnefaie N, Oqalaa Almubarak A, Aloraidi A, Khairy S. Cranioplasty: A Comprehensive Review of the History, Materials, Surgical Aspects, and Complications. World neurosurgery. 2020; 139:445-52.
15. Morton RP, Abecassis IJ, Hanson JF, et al.Timing of cranioplasty: a 10.75-year single-center analysis of 754 patients. J Neurosurg. 2018;128: 1648-1652.
16. Park SP, Kim JH, Kang HI, Kim DR, Moon BG, Kim JS. Bone flap resorption following Cranioplasty with autologous bone: quantitative measurement of bone flap resorption and predictive factors. J Korean Neurosurg Soc. 2017; 60:749-754.
17. Morselli C, Zaed I, Tropeano MP, Cataletti G, Iaccarino C, Rossini Z, et al. Comparison between the different types of heterologous materials used in cranioplasty: A systematic review of the literature. J Neurosurg Sci. 2019;63(6):723–36.
18. De Souza R, Souto Maior J, Araújo C, Cavalcanti B, Japiassú Resende M, Dantas de Moraes S. Complications with PMMA compared with other materials used in cranioplasty: a systematic review and meta-analysis. Braz Oral Res. 2018;32:e31.
19. Andrabi S, Sarmast A, Kirmani A, Bhat A. Cranioplasty: Indications, procedures, and aoutcome - An institutional experience. Surg Neurol Int. 2018;9(1):0–5.
20. Montoya A, Ortiz C. Cirugía de craneoplastia; materiales y complicaciones. Experiencia de 34 casos en Hospital Universitario del Valle y revisión de la literatura. Rev of Asoc Colomb Neurocir. 2016;23.
21. Suárez A, Pinela C. Factores de riesgo de presentar complicaciones post quirúrgicas en pacientes sometidos a craneoplastía en el hospital Abel Gilbert Pontón en periodo 2016-2018 [Doctor]. Universidad de Guayaquil; 2019.
22. Posada AC, Meneses TR, Moreno DV. Evaluación posquirúrgica de pacientes pediátricos con craneoplastia a la medida en Titanio y Peek. ICRAN 2016, 204.
23. Camarini ET, Tomeh JK, Dias R, Da Silva EJ. Reconstruction of frontal bone using specific implant polyether-ether-ketone. Journal of Craniofacial Surgery. 2011;22(6):2205-2207.
24. Ramírez-Coronel A, Martínez-Suárez P, Pogyo-Morocho G, Estrella-González M, Mesa-Cano I, Minchala-Urgilés R, et al. Evaluación psicométrica e intervención de Enfermería frente al Miedo a COVID-19. Arch Venez Farmacol y Ter. 2020;39(5):660–6.
25. Torres-Criollo LM, Ramírez-Coronel AA, Martínez-Suárez PC, Romero-Sacoto LA, Mesa-Cano IC, González-León FM, et al. Clinical and para clinical variables predicting prognosis in patients with covid-19: Systematic review. Arch Venez Farmacol Ter 2020;39(5):667-671.
26. Ramírez-Coronel AA, Martínez-Suárez PC, Pogyo-Morocho GL, Estrella-González MÁ, Mesa-Cano IC, Minchala-Urgilés RE, et al. Psychometric assessment and nursing intervention in fear of covid-19. Project crimea. Arch Venez Farmacol Ter 2020;39(5):660-666.
27. Ramírez-Coronel AA., Martínez-Suárez PC, Cabrera-Mejía JB, Buestán-Andrade PA, Torracchi-Carrasco E, Carpio MG. Social skills and aggressiveness in childhood and adolescence. Arch Venez Farmacol Ter 2020;39(2):209-214.
28. Ramírez AA. Laterality and reader process: correlational study. Espirales. 2019;3(27), 105-117.
29. Cabrera-Mejía JB, Martínez-Suárez PC, Ramírez-Coronel AA, Montánchez-Torres ML, Torracchi-Carrasco E, Castro-Ochoa FL. Analysis of problem-based learning impact on academic performance according to the forgotten(Fuzzy) effects theory. Arch Venez Farmacol Ter 2020;39(5):651-659.
30. Andrade MC, Urgilés PT, Estrella MA. Information and communication technologies in the development of stochastic models applied to the health sector. Medicina 2020;80(1):31-38.
Notas de autor
larry.torres@ucacue.edu.ec
