Artículos
Actividad antioxidante del extracto etanólico de Capsicum baccatum L
Antioxidant activity of the ethanolic extract of Capsicum baccatum L.
Actividad antioxidante del extracto etanólico de Capsicum baccatum L
Archivos Venezolanos de Farmacología y Terapéutica, vol. 40, núm. 1, pp. 54-57, 2021
Sociedad Venezolana de Farmacología Clínica y Terapéutica

Esta obra está bajo una Licencia Creative Commons Atribución-SinDerivar 4.0 Internacional.
Recepción: 28 Diciembre 2020
Aprobación: 15 Enero 2021
Publicación: 10 Febrero 2021
Resumen: Se determinó la actividad antioxidante y el contenido fenólico del fruto de ají chivato (Capsicum baccatum L.) proveniente del municipio de Ovejas (Sucre) – Colombia. Los frutos de ají chivato (Capsicum baccatum L.) fueron recolectados en el municipio de Ovejas – Sucre (9°31′33″N 75°13′38″O). El extracto etanólico se obtuvo por la técnica de maceración. La actividad antioxidante fue determinada por los métodos DPPH• y ABTS., asimismo el contenido de fenoles totales se realizó por el método colorimétrico Folin-Ciocalteu. Los resultados de la prueba de actividad antioxidante mostraron que el extracto etanólico de ají chivato (Capsicum baccatum L.) obtenido mediante maceración, tuvo valores de CI50 de 315,0±1,0 μg/mL y 160,11±0,20 μg/mL mediante la técnica de DPPH• y ABTS.+ respectivamente y un alto contenido fenólico. El extracto etanólico de ají chivato (Capsicum baccatum L.) podría ser considerado como promisorio para diseñar productos farmacéuticos y cosméticos con actividad antioxidante.
Palabras clave: Actividad antioxidante, Capsicum baccatum, extracto etanólico.
Abstract: It was determined the antioxidant activity and phenolic content of the fruit of pepper chivato (Capsicum baccatum L.) from the municipality of Ovejas (Sucre) - Colombia. The fruits of the plants of pepper chivato (Capsicum baccatum L.) were collected in the municipality of Ovejas – Sucre (9°31′33″N 75°13′38″O). The ethanolic extract was obtained by the maceration technique. The antioxidant activity was determined by the DPPH• and ABTS+ methods. In addition, the total content of phenols was performed by the colorimetric method of Folin-Ciocalteu reagent. The results of the test of antioxidant activity showed that the ethanolic extract of pepper chivato (Capsicum baccatum L.) obtained by maceration had IC50 values of 315,0±1,0 μg/mL and 160,11 ± 0,20 μg/mL and were used the DPPH• and ABTS.+ techniques respectively, and a high phenolic content. The ethanolic extract of pepper chivato (Capsicum baccatum L.) is considered promising to design pharmaceutical and cosmetic products with antioxidant activity.
Keywords: Antioxidant activity, Capsicum baccatum, ethanolic extract.
INTRODUCCION
Los radicales libres son especies químicas que poseen un electrón desapareado en su orbital más externo (último orbital), lo que los hace altamente reactivos a las moléculas vecinas. En los seres vivos, los radicales libres provienen principalmente del oxígeno y del nitrógeno1,2. Estos radicales libres pueden reaccionar químicamente con lípidos, proteínas, carbohidratos y ácidos nucleicos, lo que causa alteraciones celulares que se pueden expresar en patologías, entre ellas enfermedades cardiovasculares (ECV) y otras enfermedades crónicas no transmisibles3-5. Ahora bien, los vegetales poseen un amplio contenido de compuestos fitoquímicos los cuales pueden ofrecer diferentes efectos biológicos en el organismo humano, dentro de los que se destaca la actividad antioxidante6,7. Así, se ha demostrado una relación inversa entre el consumo de frutas y vegetales y el riesgo de enfermedades cardiovasculares y cáncer1.
Colombia es un país que posee una gran diversidad de ecosistemas y microclimas, lo cual hace que su vegetación sea muy variada, enriquecida con especies endémicas y diversidad genética muy alta. Algunas de las plantas que se pueden encontrar poseen actividad biológica, de amplias perspectivas para la investigación y el desarrollo de nuevos productos 8-12.
El cultivo del ají es importante en la historia, tradición y cultura de Colombia y es, además, un producto agrícola con alta demanda mundial. Los tipos de ají que se producen actualmente son el tabasco, cayena, habanero, chivato y jalapeño13-15. Esta producción se realiza principalmente en los departamentos de Bolívar, Atlántico, Magdalena, Guajira y Valle del Cauca. De ellos, el Valle del Cauca y la Costa Atlántica, por sus condiciones climáticas, concentran la mayor cantidad de área cultivada, pues este producto se desarrolla de manera óptima entre los 0 y 1000 msnm. Las variedades de ajís pueden ser picantes y no picante13-16.
El ají chivato (Capsicum baccatum L.) es un arbusto que llega a los 2m de altura de la familia de las Solanáceas. Sus flores son solitarias pendulares y blancas, los frutos son bayas de color verde que cambian a amarillo, naranja o rojo brillante al madurar; alargados, cónicos, varían en tamaño, puede alcanzar hasta 20cm de longitud13. El fruto contiene una serie de amidas denominadas capsaicinoides (0,3 a 1%), entre las cuales destaca la capsaicina (8-metil-N-vanillil-6-nonenamida), esta es una oleorresina, a la que se le ha demostrado propiedades antioxidantes 17-23.
Por lo anteriormente descrito, la presente investigación tuvo como objetivo determinar la actividad antioxidante y el contenido fenólico del extracto etanólico de ají chivato (Capsicum baccatum L.) proveniente del municipio de Ovejas – Sucre (Colombia).
MATERIALES Y MÉTODOS
Recolección del material vegetal
Con base en los registros de las colecciones del Herbario Regional Catatumbo-Sarare (HECASE) de la Universidad de Pamplona, los frutos de las plantas de ají chivato (Capsicum baccatum L.) fueron recolectados en una vereda del municipio de Ovejas – Sucre (9°31′33″N 75°13′38″O). Se recolectaron 500 g de material en diferentes plantas por semana, en el periodo comprendido de junio a julio del 2020, para asegurar la colección de frutos frescos.
Obtención del extracto etanólico
Los frutos recolectados fueron lavados con agua y seleccionados para garantizar buen estado, seguidamente se pesaron, se eliminó la capa externa y se procedió a pesar nuevamente. Este material se secó a la temperatura ambiente (25 ºC) por 24 horas y luego se trocearon. La extracción consistió en macerar, en solución hidroalcohólica al 70%, durante 5 días a temperatura ambiente. Cada extracto fue filtrado en papel filtro común y concentrado en rotoevaporador R-210 (BUCHI) hasta que aparentemente todo el alcohol fue eliminado 24.
Determinación de fenoles totales
El contenido de fenoles totales se determinó por el método colorimétrico de Folin-Ciocalteu, se utilizó como reactivo una mezcla de ácidos fosfowolfrámico y fosfomolibdíco en medio básico, que se reducen al oxidar los compuestos fenólicos, originando óxidos azules de wolframio (W.O23) y molibdeno (Mo.O23). Se construyó una curva patrón usando como estándar ácido gálico entre 50 – 500 µg/mL. Se diluyó en etanol el extracto correspondiente a una concentración en la cual el contenido de fenoles se encontrará dentro del intervalo de la curva patrón. Los resultados se expresaron como mg de ácido gálico / 250 mL de muestra. Las lecturas de las absorbancias se realizaron a 760 nm en un espectrofotómetro UV visible Thermo Scientific™ GENESYS 10S 25-27.
Método del radical DPPH•
La actividad captadora de radicales libres DPPH• se determinó empleando el método descrito por Silva y col., con algunas modificaciones28. Para ello, 75 µL de muestra fueron adicionados a 150 µL de una solución metanólica de DPPH• (100 µg/mL) y se incubó a temperatura ambiente durante 30 min, luego de los cuales se determinó espectrofotométricamente la desaparición del radical DPPH• a 550 nm en lector de microplacas Multiskan Ex (Thermoscientific). Se utilizó ácido ascórbico como control positivo de captación de los radicales DPPH• (25 µg/mL). La IC50 se determinó evaluando varias concentraciones seriadas de la muestra mediante análisis de regresión lineal. Los resultados se expresaron como la media ± E.S.M del porcentaje de captación del radical DPPH• relativo al grupo control. Se calculó el porcentaje de inhibición (% Inh) usando la ecuación (1).
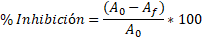
ecuación (1)
Donde A. y A. son los valores de absorbancia del blanco (solución de DPPH• en etanol) y la muestra (solución de DPPH• más antioxidante disueltos en etanol), respectivamente.
Método del radical ABTS+
El radical ABTS• se formó después de la reacción de ABTS 3,5 mM con 1,25 mM de persulfato potásico (concentración final). Las muestras fueron incubadas entre 2°C - 8 °C y en oscuridad de 16 h a 24 h. Una vez formado el radical ABTS• se diluyó con etanol hasta obtener una absorbancia de 0,7 ± 0,05 a 734 nm. A un volumen de 190 μL de la dilución del radical ABTS• se le adicionó 10 μL de la muestra en estudio y se incubó a temperatura ambiente durante 5 minutos, luego de transcurrido este tiempo se determinó espectrofotométricamente la desaparición del radical ABTS• a 734 nm en el lector de microplacas Multiskan Ex (Thermoscientific)6.
Análisis Estadístico
Todos los ensayos se realizaron por triplicado siguiendo los protocolos establecidos anteriormente. El análisis estadístico se realizó comprobando los supuestos de normalidad de datos para el empleo de modelos paramétricos (distribución normal, igualdad de varianza e independencia de datos). El análisis estadístico se orientó a comparar los valores de medios de los resultados obtenidos. Los resultados obtenidos fueron sometidos a análisis de varianza ANOVA, seguido de la prueba de Dunnet para determinación de diferencias significativas. Los datos se ordenaron empleando el programa MS Excel 365, y los análisis estadísticos se hicieron con el paquete GraphPad Prisma V 5.0.
RESULTADOS
Las sustancias fenólicas son reconocidas por su aporte a la actividad antioxidante de los materiales vegetales. Por lo que se evaluó el contenido de fenoles totales en los extractos, con el método de Folin-Ciocalteu, de los que se obtuvieron valores de 807,90±1,90 para el extracto etanólico de C. baccatum mg de ácido gálico/250 mL de muestra.
La actividad antioxidante del extracto etanólico del pimentón (Capsicum baccatum L.), se evaluó por los métodos de DPPH• y ABTS.+ y se alcanzaron valores de CI50 315,01±1,03 μg/mL y 160,11±0,20 μg/mL respectivamente. Estos resultados se expresaron como actividad antiradical o CI50, la que se define como la concentración del antioxidante que disminuye la absorción del radical a un 50 % de la cantidad inicial31.
DISCUSION
Las plantas son consideradas organismos fotosintéticos que están expuestos a ambientes muy oxidativos (radiación solar, oxígeno, entre otros), por lo cual, poseen un sistema antioxidante muy eficaz. Asimismo, se han reportado diversos metabolitos, en especial sustancias fenólicas como flavonoides, taninos y otras sustancias que actúan sinérgicamente para potenciar el efecto antioxidante como los tocoferoles, catequinas, ácidos orgánicos y carotenoides32,33.
El extracto etanólico de ají chivato (Capsicum baccatum L.), produjo una decoloración del radical DPPH• comparable con lo reportado por Zimmer y col., de un CI50 de 267,58 ± 29,08 μg/mL para el extracto etanólico del fruto18.
Nuestros resultados indican que el extracto etanólico del C. baccatum presenta un elevado contenido fenólico, el cual fue mayor a los reportados por Zimmer y col., de 180,08±3,76 mg GAE/g extracto para el extracto etanólico del fruto18. Esta diferencia puede estar correlacionada con el método de captura de electrones empleado para determinar la actividad antioxidante, y ratificado con estudios previos6,7,11,12. Se ha sugerido que el elevado contenido fenólico puede estar correlacionado con la actividad antioxidante mediante DDPH•.
Mejía y col.,34reportan que la serie de amidas denominadas capsaicinoides, presentes en porcentaje del 0,3 % a 1%, y entre las cuales destaca la capsaicina (amida vanílica del ácido isodecenoico), compuestos que contribuyen significativamente al mayor efecto antioxidante del género Capsicum.
Álvarez-Padilla y col,35 obtuvieron un contenido de fenoles totales de 1032 ± 95 mg ácido gálico/100 g muestra, en chile jalapeño, es similar a los reportados en el presente trabajo.
Granados y col,36evaluaron la actividad antioxidante in vitro del extracto etanólico de Capsicum annuum, resaltando los valores CI50 obtenidos para las técnica antiradicalarias de DPPH• (343,00 ± 0.25 μg/mL) y ABTS.+ (174,61 ± 0,10 μg/mL).
Torrenegra y col,37determinaron la actividad antioxidante mediante las técnicas de DPPH• (CI50 de 270,99±1,50 μg/mL) y ABTS.+ (CI50 de 137,95± 0,20 μg/mL), así como el contenido fenólico (1007,9±0,89 mg de ácido gálico/250 mL de muestra) del fruto de ají (Capsicum frutescens L.) proveniente del municipio de Ovejas (Sucre) – Colombia.
Las diferencias en los resultados encontrados por los diferentes investigadores podrían explicarse en parte por la diversidad con relación al lugar y condiciones de cultivo, de almacenamiento, y de procesamiento, además de las diferentes metodologías utilizadas en la medición de la capacidad antioxidante.36-38
En conclusión, debido a la alta actividad antioxidante mediante DDPH• y ABTS., así como el alto contenido de fenoles, el extracto etanólico de ají chivato (Capsicum baccatum L.) puede ser considerado como promisorio para diseñar productos farmacéuticos y cosméticos con actividad antioxidante.
Conflicto de intereses: Autores declaramos no tener conflicto de interés.
Agradecimientos
Los autores agradecen a la Universidad de Cartagena y a la Corporación Universitaria Rafael Núñez por facilitar espacio, recursos y tiempo de los investigadores.
REFERENCIAS BIBLIOGRAFICAS
1. Palomo I, Gutiérrez M, Astudillo L, Rivera C, Torres C, Guzmán L, Moore-Carrasco R, Carrasco G, Alarcón M. Efecto antioxidante de frutas y hortalizas de la zona central de Chile. Rev Chil Nutr, 2009; 36(2): 152.
2. Gutiérrez-Salinas J, Mondragón-Terán P, García-Ortíz L, Hernández-Rodríguez S, Ramírez-García S, Núñez-Ramos NR. Breve descripción de los mecanismos moleculares de daño celular provocado por los radicales libres derivados de oxígeno y nitrógeno. Rev Esp Méd Quir, 2014; 19: 446.
3. Narang S, Yadav A, Vaidya M. Free radicals vs Antioxidants: The deadly demons vs the friendly scavengers: A review. Asian J Pharmacy Life Sci, 2011; .(1): 95.
4. Gutiérrez-Salinas J, Morales-González JA. Producción de radicales libres derivados del oxígeno y el daño al hepatocito. Med Int Mex. 2004; 20: 287.
5. Gutiérrez-Salinas J. ¿Qué sabe usted acerca de radicales libres?. Rev Mex Cien Farm, 2006; 37: 69.
6. León G, Torrenegra M, Osorio M, Gil J. Extracción, caracterización y actividad antioxidante del aceite esencial de Plectranthus amboinicus L. Rev cubana Farm, 2015; 49(4): 708.
7. Granados C, Yáñez Y, Santafé G. Evaluación de la actividad antioxidante del aceite esencial foliar de Calycolpus moritzianus y Minthostachys mollis de Norte de Santander. Bistua, 2012; 10(1): 12.
8. Torrenegra M, Granados C, Osorio M, León G. Method comparison of hydrodistillation microwave radiation-assisted (MWHD) front hydrodistillation (HD) in the extraction of essential oil of Minthostachys mollis. Inf Tecnol, 2015; 26(1):117.
9. León G, Osorio MR, Martínez SR. Comparación de dos métodos de extracción del aceite esencial de Citrus Sinensis L. Rev Cuba Farm, 2015; 49(4):742.
10. Torrenegra M, Matiz G, León G, Gil J. Actividad antibacteriana in vitro de aceites esenciales frente a microorganismos implicados en el acné. Rev cubana Farm, 2015; 49(3): 512.
11. Granados C, Yáñez X, Acevedo D. Evaluación de la Actividad Antioxidante del Aceite Esencial Foliar de Myrcianthes leucoxyla de Norte de Santander (Colombia). Inf Tecnol, 2014; 25(3): 11.
12. Granados C, Santafé GG, Acevedo D. Composición química y evaluación de la actividad antioxidante del aceite esencial foliar de Eucalyptus camaldulensis de norte de Santander (Colombia). Rev U.D.C.A Act & Div Cient, 2015; 18(1): 235.
13. Mendoza R. Sistemática historia del ají CapsicumTourn. Universalia,2006; 11(02):80.
14. CORPOCAUCA. Análisis de agronegocios alianza productiva y comercial ají. 1-47(2008). URL: http://www.misionrural.net/observatorio/alianzas/productos/aji/7muni-valle/preinversion.pdf, consultado en diciembre de 2020.
15. Rocha-Ángulo JA, Rocha-Rocha TM, Albis-Arrieta AR. Drying of tabasco pepper (Capsicum frutescens) using air-forced dehydration. Prospect, 2016; 14(1): 89.
16. Rodríguez-Araujo EA, Bolaños-Benavides MM, Menjivar-Flores JC. Efecto de la fertilización en la nutrición y rendimiento de ají (Capsicum spp.) en el Valle del Cauca, Colombia. Acta Agronómica, 2010; 59(1): 55.
17. Yazdizadeh-Shotorbani N, Jamei R, Heidari R. Antioxidant activities of two sweet pepper Capsicum annuum L. varieties phenolic extracts and the effects of thermal treatment. Avicenna J Phytomed, 2013; 3(1): 25.
18. Zimmer AR, Leonardia B, Mirona D, Schapovala E, Rodrigues de Oliveirac J, Gosmanna G. Antioxidant and anti-inflammatory properties of Capsicum baccatum: From traditional use to scientific approach. J Ethnopharmacol,2012 139: 228.
19. Wahyunia Y, Ballestera AR, Sudarmonowatib E, Binoa RJ, Bovya AG. Metabolite biodiversity in pepper (Capsicum) fruits of thirty-two diverse accessions: Variation in health-related compounds and implications for breeding. Phytochemistry, 2011; 72(11–12): 1358.
20. Nascimento PL, Nascimento TC, Ramos NS, Silva GR, Gomes JE, Falcão RE, Silva T. “Quantification, antioxidant and antimicrobial activity of phenolics isolated from different extracts of Capsicum frutescens (Pimenta Malagueta)”. Molecules, 2014; 19(4): 5434.
21. Bijttebier S, Zhani K, D’Hondt E, Noten B, Hermans N, Apers S, Voorspoels S. “Generic characterization of apolar metabolites in red chili peppers (Capsicum frutescens L.) by orbitrap mass spectrometry”. J Agric Food Chem, 2014; 62(20): 4812.
22. Nascimento PL, Nascimento TC, Ramos NS, Silva GR, Camara CA, Silva TM, Moreira KA, Porto AL. Antimicrobial and antioxidant activities of Pimenta malagueta .Capsicum frutescens). Afr J Microbiol Res, 2013; 7(27): 3526.
23. Kappel VD, Costa GM, Scola G, Silva FA, Landell MF, Valente P, Souza DG, Vanz DC, Reginatto FH, Moreira JCF. Phenolic Content and Antioxidant and Antimicrobial Properties of Fruits of Capsicum baccatum L. var. pendulum at Different Maturity Stages. J Med Food, 2008; 11(2): 267.
24. Paula-Silva J, Martins-De Siqueira A. Acción antibacteriana de extractos hidroalcohólicos de Rubus urticaefolius. Rev Cubana Plant Med, 2000; 5(1): 26.
25. Singleton VL, Orthofer R, Lamuela-Raventos RM. Analysis of total phenols and other oxidation substrates and antioxidants by means of Folin Ciocalteu Reagent. Methods Enzymol. 1999; 299: 152.
26. Rojano BA, Vahos ICZ, Arbeláez AFA, Martínez AJM, Correa FBC, Carvajal LG. Polifenoles y actividad antioxidante del fruto liofilizado de palma naidi (açai colombiano) (Euterpe oleracea Mart). Rev Fac Nal Agr Medellín, 2011; 64: 6213.
27. Vásquez A, Cala M, Miranda I, Tafurt G, Martínez J, Stashenko E. Actividad antioxidante y contenido total de fenoles de los extractos etanólicos de Salvia aratocensis, Salvia Sochensis, Bidens reptons y Montanoa ovalifolia. Sci Technica, 2007; 13(33): 205.
28. Silva B, Andrade P, Valentao P, Ferreres F, Seabra R, Ferreira M. Quince (Cydonia oblonga Miller) Fruit (Pulp, Peel, and Seed) and Jam: Antioxidant Activity. J Agric Food Chem, 2004; 52: 4705.
29. Prior RL, Wu X, Schaich K. Standardized methods for the determination of antioxidant capacity and phenolics in foods and dietary supplements. J Agric Food Chem, 2005; 53: 4290.
30. Floegel A, Kim DO, Chung SJ, Koo SI, Chun OK. Comparison of ABTS/DPPH assays to measure antioxidant capacity in popular antioxidant-rich US foods. J Food Comp Anal, 2011; 24(7):1043.
31. Villanueva J, Condezo L, Asquieri E. Antocianinas, ácido ascórbico, polifenoles totales y actividad antioxidante, en la cáscara de camu-camu (Myrciaria dubia (H.B.K) McVaugh). Ciênc Tecnol Aliment Campinas, 2010; 30(1):151.
32. Álvarez E, Jímenez OJ, Posada CM, Rojano B, Gil J, García CM, Durango DL. Antioxidant activity and phenolic content of extracts from berries of two species of Vismia genus (Guttiferae). VITAE, 15(1), 165 (2008).
33. Morillas-Ruiz JM, Delgado-Alarcón JM. Análisis nutricional de alimentos vegetales con diferentes orígenes: Evaluación de capacidad antioxidante y compuestos fenólicos totales. Nutr clín diet hosp, 2012; 32(2): 8.
34. Mejía F. Aislamiento y Caracterización Fisicoquímica de la Capsaicina de Tres Variedades de Ají. Tesis Pontificia Universidad Católica del Ecuador. Pag 15. URL: http://repositorio.puce.edu.ec/bitstream/handle/22000/5728/T-PUCE-5882.pdf?sequence=1&isAllowed=y, Consultado en Junio de 2020.
35. Álvarez-Padilla E, de la Rosa LA, Amarowicz R, Shahidi F. Antioxidant activity of freshand processed Jalapeño and Serrano peppers. J Agric Food Chem. 2011;59(1):163-73.
36. Granados C, Pájaro N, León G. Actividad antioxidante y contenido fenólico del extracto etanólico de Capsicum annuum L. Revista Cubana de Farmacia. 2018;52(2):e78.
37. Torrenegra M, Granados C, León G. Actividad antioxidante del extracto etanólico de Capsicum frutescens L. Bistua: Revista de la Facultad de Ciencias Básicas.2019; 17(2):102-111.
38. León-Méndez G, Crisóstomo-Pérez T, González-Fegali M, Herrera-Barros A, Pájaro-Castro N, León-Méndez D. Frutas como fuentes de moléculas bioactivas. AVFT Archivos Venezolanos de Farmacología y Terapéutica. 2020; 39(2): 153-159.