Artículos

Esta obra está bajo una Licencia Creative Commons Atribución-SinDerivar 4.0 Internacional.
Recepción: 28 Enero 2021
Aprobación: 15 Febrero 2021
Publicación: 10 Junio 2021
DOI: https://doi.org/10.5281/zenodo.5227632
Resumen:
Antecedentes: Existe escasa información sobre la prevalencia de la coinfección bacteriana, y uso de antibióticos en pacientes hospitalizados por COVID-19. Este estudio evalúa la frecuencia de prescripción antibióticos intrahospitalario, de cultivos bacterianos y curso clínicos de los pacientes con COVID-19 según uso de antibióticos.
Métodos: Estudio retrospectivo, observacional de pacientes hospitalizados con COVID-19. Se uso el formulario de ISARIC-OMS para recopilar datos.
Resultados: Se incluyeron 145 pacientes, 95 hombres y 50 mujeres, con edad promedio 63.8±16.0 años. 79/145 (54.5%) pacientes recibieron antibióticos, 52/145 (35%) tuvieron muestras para cultivo y 49/145 (33.8%) fueron hemocultivo. Se aislaron bacterias patógenas en 7% de los pacientes. Los pacientes con antibiótico tenían mayor alteración de oxigenación, tomografía de tórax y marcadores inflamatorios, más ingreso a UCI, fallecimientos, y estancia hospitalaria prolongada.
Conclusión: Los resultados no respaldan el uso generalizado inicial de antibióticos en pacientes hospitalizados con COVID-19 sin aislamiento de microrganismos patógenos.
Palabras clave: SARS-CoV-2, COVID-19, coinfecciones bacterianas, neumonía, uso de antibióticos.
Abstract:
Background: There is little information on the prevalence of bacterial coinfection and use of antibiotics in hospitalized COVID-19 patients. The present study assesses the frequency of in-hospital antibiotic prescription, the bacterial cultures implementation and the clinical characteristics of patients with COVID-19 according to the use of antibiotics.
Methods: Retrospective, observational study of hospitalized patients with COVID-19. The ISARIC-WHO form was used for data collection.
Keywords: SARS-CoV-2, COVID-19, bacterial co-infections, pneumonia, antibiotic use.
Introducción
Para febrero del 2021 se han confirmado más de 100 millones de casos y más de 2 millones de muertes por COVID-19 en todo el mundo. Aunque la mayoría de las personas desarrollan una enfermedad leve-moderada o sin complicaciones, también se observa que una proporción importantes de pacientes desarrollan enfermedad grave que requiere hospitalización. Los datos de un estudio International Severe Acute Respiratory Infection Consortium (ISARIC) sobre características clínicas de los pacientes hospitalizados por COVID-19 en el Reino Unido indican que una alta proporción de los pacientes requirieron ingreso en unidades de alta dependencia o cuidados intensivos (17%, 3001/18183), y el 55% (9244/16849) recibió oxígeno de alto flujo en algún momento durante su ingreso1. El 16% de los pacientes (2670/16805) fueron tratados con ventilación no invasiva, mientras que el 10% (1658/16866) recibieron ventilación invasiva. Otro estudio en una serie de pacientes en la ciudad de New York indica que 14.2% de los pacientes hospitalizados ingresaron en la UCI y 12.2% recibieron soporte con ventilación mecánica invasiva2.
La prevalencia, incidencia y características de la coinfección bacteriana en pacientes infectados con el SARS-CoV-2 no se conocen bien y sigue siendo un tema de controversia. Por esto las recomendaciones de la OMS para el manejo clínico de los pacientes con COVID-19 hospitalizados propone realizar hemocultivos, así como recolección de muestras del tracto respiratorio superior para cultivos bacterianos, y comenzar solo en los casos graves tratamiento antimicrobiano de amplio espectro sin comprobación bacteriológica3.
Existe una preocupación global de que la pandemia de COVID-19 lleve al uso innecesario de antibióticos e incremente aún más la resistencia antimicrobiana, así como el riesgo de eventos adversos relacionados con el uso de antibióticos. Los datos publicados indican tasas altas de prescripción de antibióticos en relación con la infección por SARS-CoV-2 sin evidencia de apoyo de coinfección o sobreinfección bacteriana. Conocer entonces la proporción de pacientes con COVID-19 con coinfección bacteriana respiratoria aguda y los patógenos asociados es crucial para tratar a los pacientes con COVID-19 y ayudar a garantizar el uso responsable de antibióticos y minimizar las consecuencias negativas del uso excesivo.
Algunas revisiones sistemática y metaanálisis han informado sobre la proporción general de pacientes hospitalizados con el diagnostico de COVID-19 que presentan coinfección bacteriana confirmada y requirieron uso de agentes antimicrobianos4-6. En general la proporción de pacientes con COVID-19 con infección bacteriana asociada es 7% aproximadamente, y aumenta en el entorno de la UCI. A pesar de la baja tasa general de infecciones bacterianas, más del 70% de los pacientes reciben antibióticos, y la mayoría de ellos son agentes de amplio espectro. Por otra parte, se ha sugerido que los hallazgos de los marcadores inflamatorios y la gravedad del COVID-19 son los principales factores que influyen en la toma de decisión sobre el uso de antibióticos en estos pacientes7,8. Existe escasa información sobre los fundamentos usado por los médicos para la prescripción de antibióticos en pacientes hospitalizados con infección por SARS-CoV-2.
De nuestro conocimiento no existe información local sobre la prescripción de antibióticos en pacientes hospitalizados con COVID-19 y la prevalencia de infección bacteriana asociada, así como sobre las características de los pacientes que recibieron antibióticos intrahospitalarios. Por tanto, nuestro estudio buscó determinar la frecuencia de prescripción de antibióticos durante la hospitalización de pacientes con diagnóstico de COVID-19 y la frecuencia del uso de pruebas diagnósticas para determinar infección bacteriana asociada en el hospital privado Centro Médico de Caracas. También busca evaluar las características y el curso clínico intrahospitalario de los pacientes que recibieron o no antibióticos.
Métodos
Este es un estudio retrospectivo, observacional, de revisión de historias clínicas (serie de casos) de los pacientes hospitalizados con el diagnóstico clínico de COVID-19 en el Hospital Centro Médico de Caracas, Venezuela entre el 1 de marzo y el 15 de diciembre, 2020. El estudio fue sometido para su aprobación por el Comité de Bioética de la institución.
Recolección de datos
Para la recopilación de los datos se utilizó el formulario de informe de caso en papel (versión CORE en español del 23 de abril de 2020) desarrollado por el estudio ISARIC y la Organización Mundial de la Salud (OMS) para su uso en investigaciones del Protocolo "Clinical Characterization Protocol UK (CCP-UK)" (https://isaric.tghn.org/COVID-19-CRF/). Los datos se cargaron desde el ingreso y se recolectó la información sobre la clínica antes del ingreso hospitalario. Durante la hospitalización se evaluaron las medidas de gravedad de la enfermedad y los resultados de los análisis de laboratorio de rutina para COVID-19 en tres puntos temporales: el día uno de ingreso al hospital, día tres y día seis. Se realizó registro de los tratamientos intrahospitalario relevantes que recibieron los pacientes, el nivel de atención requerida (sala de hospitalización o UCI), desarrollo de síndrome de distrés respiratorio agudo (SDRA), así como los detalles del alta o muerte en el hospital y estancia hospitalaria.
Un equipo de médicos que había tratado a estos pacientes realizó la recopilación de los datos y completó el formulario extrayendo de los registros médicos el historial de exposición reciente, antecedentes pertinentes, síntomas clínicos, saturación de oxígeno por oximetría de pulso (SpO2), presión arterial de oxígeno (PaO2), fracción inspirada de oxígeno (FiO2) requerida, PaO2/FiO2, resultados de laboratorio, alteración en la tomografía de tórax (TC), tratamiento y los desenlaces clínicos. En 130 pacientes (90%) se realizó al menos una TC, y los datos se extrajeron después de que los estudios fueron revisados por un equipo de especialistas en imágenes.
Las pruebas de laboratorio (hematología, química sanguínea y marcadores inflamatorios) se realizaron de acuerdo con las necesidades clínicas de los pacientes. La toma de muestras para cultivos (hemocultivos o cultivo de otro tipo de muestras) también estuvo condicionada por las necesidades de los pacientes en cualquier momento del transcurso de la hospitalización. Los investigadores se comunicaron con los pacientes egresados por teléfono si algo no estaba claro o si faltaba información necesaria para el estudio en el registro médico.
Confirmación del diagnóstico de COVID-19
La confirmación diagnóstica de COVID-19 se basó en la detección de secuencias virales específicas mediante pruebas de amplificación de ácidos nucleicos (AAN), con el resultado positivo de la prueba reacción en cadena de la polimerasa por transcripción inversa en tiempo real (rRT-PCR) para el síndrome respiratorio agudo moderado a grave SARS-CoV-2. Las muestras de las vías respiratorias superiores (hisopados nasofaríngeos) fueron tomadas siguiendo las directrices estandarizadas por la OMS.
Criterios de hospitalización
El criterio más común de ingreso hospitalario para pacientes con COVID-19 fue la hipoxemia en aire ambiente (FiO. 0.21) y/o la presencia de infiltrados pulmonares compatibles con infección por COVID-19. Para el propósito de este artículo, una cama de la UCI se define como aquella con la capacidad de proporcionar ventilación mecánica y monitoreo continuo de signos vitales, con personal de enfermeras de cuidados críticos y supervisión de intensivistas. El ingreso a la UCI fue reservado con mayor frecuencia para pacientes con insuficiencia respiratoria aguda severa que requerían oxigenoterapia con cánula nasal de alto flujo o ventilación mecánica.
Análisis cualitativo y semicuantitativo de la TC de Tórax
En cada paciente, la TC de tórax se evaluó para determinar las siguientes características: a) presencia de opacidad en vidrio esmerilado; b) presencia de consolidado; c) número de lóbulos afectados donde estaban presentes la opacidad de vidrio esmerilado o de consolidado; e) grado de alteración de cada lóbulo pulmonar, además de la extensión global de la alteración pulmonar medida por una "puntuación de gravedad total".
La puntuación de gravedad de la TC fue calculada según los criterios de Pan y colaboradores para cada uno de los cinco lóbulos.. Para este análisis se usó la siguiente escala de puntuación: 0 (sin alteración), 1 (alteración <5%), 2 (alteración 5-25%), 3 (alteración 26-50%), 4 (51% - 75%), 5 (alteración >75%). La puntuación total en la TC fue la resultante de la suma de cada puntuación lobular individual (rango de puntuación posible, 0 a 25).
Análisis Estadístico
La estadística descriptiva incluyó las frecuencias en números y porcentajes para las variables categóricas y la media más desviación estándar (DS) para las numéricas. Para la comparación entre los pacientes que presentaron hiperglucemia o no se utilizó la prueba U de Mann-Whitney, la prueba χ2 o la prueba exacta de Fisher para comparar diferencias entre los dos grupos. Un valor de p de 0.05 o menos fue considerado estadísticamente significativo. Se utilizó el programa STATISTICA Versión 10 (StatSoft) para los análisis estadísticos.
Resultados
Un total de 145 pacientes se incluyeron en el estudio, 95 hombres y 50 mujeres, con una edad promedio 63.8±16.0 años. Entre ellos 6/145 pacientes fueron trasladados a otras instituciones por lo que los detalles del alta o muerte en el hospital se analizó en 139/145 (96%) pacientes. Del total de pacientes incluidos, a 79/145 (54.5%) se le prescribieron antibiótico durante la hospitalización y 66/145 (45.5%) no recibieron antibióticos. La figura 1 muestra el porcentaje de pacientes que recibieron antibióticos intrahospitalarios según el mes de ingreso a la institución. Con el curso del tiempo se observó una disminución progresiva en la prescripción de antibióticos en los pacientes ingresados con el diagnóstico clínico de COVID-19. Aproximadamente un tercio de los pacientes recibieron antibióticos en los últimos meses analizados.
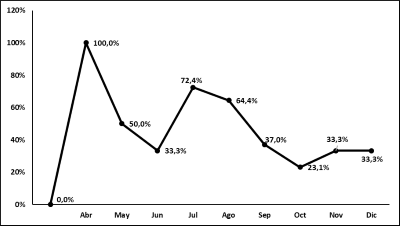
Figura 1.
Distribución porcentual de pacientes por mes de ingreso que recibieron antibiticos
De total de pacientes que les prescribieron antibióticos (tabla 1) 48/79 (61%) recibieron entre dos a tres medicamentos. En el grupo de paciente que recibieron antibióticos los medicamentos usados como primer antibiótico en orden decreciente de frecuencia fueron: Ceftriaxona 48/79 (60.76%), Piperacilina-Tazobactam 10/79 (12.66%) y Meropenem 8/79 (10.13%), Cefepime 3/79 (3.80%), Linezolid 3/79 (3.80%), Vancomicina 2/79 (2.53%), Levofloxacina 2/79 (2.53%), Ampicilina-Sulbactam 1/79 (1.27%), Metronidazol 1/79 (1.27%), Ciprofloxacina 1/79 (1.27%). Como segundo antibiótico fueron: Levofloxacina 14/48 (29.17%), Meropenem 12/48 (25.00%), Vancomicina 6/48 (12.50%), Linezolid 5/48 (10.42%), Cefepime 4/48 (8.33%), Amikacina 4/48 (8.33%), Metronidazol 1/48 (10.42%), Clindamicina 1/48 (10.42%), Piperacilina-Tazobactam 1/48 (10.42%). Como tercer antibiótico fueron: Linezolid 8/22 (36.36%), Vancomicina 6/22 (27.27%), Meropenem 3/22 (13.64%), Ceftriaxona 3/22 (13.64%), Metronidazol 1/22 (4.55%), Cancidas 1/22 (4.55%). El tiempo de duración del primero, segundo y tercer antibiótico fue 5.7 ± 2.8, 6.3 ± 3.3 y 7.2 ± 3.2, respectivamente.
Las características clínicas generales y principales desenlaces de los pacientes según el requerimiento o no de antibioticoterapia intrahospitalaria se muestran en la tabla 1 y la figura 2. En el grupo con requerimiento de antibióticos se observó una mayor proporción de pacientes con enfermedad grave-critica, SDRA, admisión a la UCI, fallecimientos y estancia hospitalaria más prolongada. Casi todos los pacientes (31/32) admitidos a la UCI requirieron antibióticos comparados con 43% (48/113) de los que no ingresaron a la UCI. Un tercio (25/74) de los pacientes que requirieron antibióticos fallecieron comparado con menos del 5% (3/65) de los que no requirieron la medicación. No se observaron diferencias en la edad, sexo, peso, talla, IMC, y duración de los síntomas previo al ingreso entre los grupos.
Características clínicas generales entre pacientes con y sin antibióticos

Definiciones: IMC; Índice de masa corporal; SDRA: Síndrome de distrés respiratorio agudo. Los datos se muestran como n (%) o media ± DE.
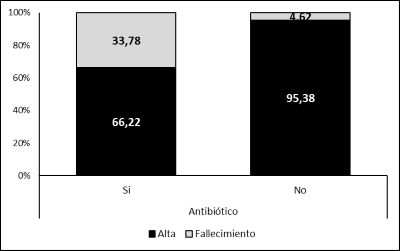
Figura 2
Mortalidad según uso de antibióticos en pacientes hospitalizados con COVID-19
Los datos se muestran en porcentaje †p<0.00001 (Si-Antibiótico vs No- Antibiótico)
La tabla 2 muestra los resultados de los signos vitales y oxigenación de ingreso y control en los dos grupos de pacientes. El grupo de pacientes que requirió antibióticos tenían valores más altos de temperatura y niveles más bajos de SpO2%, SpO2/FiO2, PaO2 y PaO2/FiO2 al ingreso y en la evaluación control, así como mayor requerimiento de oxígeno (FiO2) comparado con aquellos que no recibieron antibióticos.
Signos vitales y oxigenación de ingreso y control en pacientes con y sin antibióticos
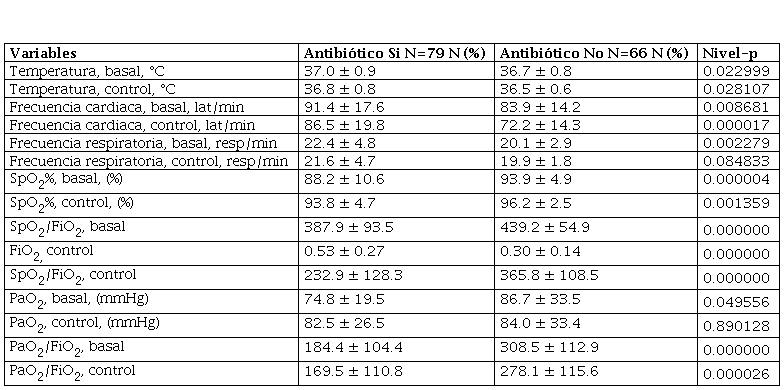
Definiciones: SpO2: saturación de oxígeno por oximetría de pulso; FiO2: fracción inspirada de oxígeno; PaO2: presión arterial de oxígeno. Los datos se muestran como media ± DE.
La Tabla 3 muestra los valores de algunas pruebas de laboratorio y marcadores inflamatorios de ingreso y control en los dos grupos de pacientes. El grupo de pacientes que requirió antibióticos tenían valores más elevados en las mediciones de ingreso y control del recuento total de leucocitos, neutrófilos e índice Neutrófilos/Linfocitos (N/L) y valores más bajos de hemoglobina, hematocrito y recuento de linfocitos.
Laboratorio de ingreso y control entre pacientes con y sin antibióticos
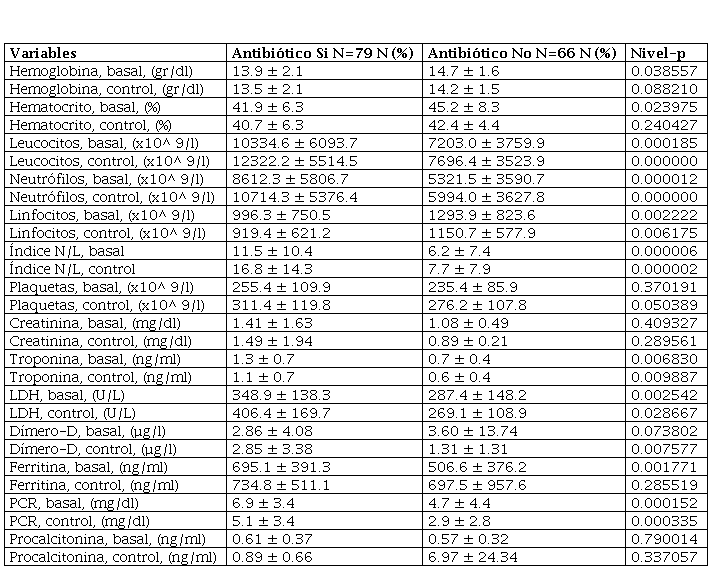
Definiciones: PCR: Proteína C reactiva; LDH: Lactato deshidrogenasa. Los datos se muestran como media ± DE.
Tambien se observaron niveles mas elevados de proteína C reactiva (PCR), Lactato deshidrogenasa (LDH), ferritina, troponina y dímero D en los pacientes con requerimientos de antibioticos. No se obsevo diferencia en los valores de plaquetas, creatinina y procalcitonina entre los grupos.
En un total de 52/145 pacientes (35%) se tomaron muestras para cualquier tipo de cultivo y 49/145 (33.8%) fueron hemocultivo. Del total de cultivos solo 19/52 (36.5%) fueron positivos. La figura 3 muestra los microorganismos aislados en los hemocultivos y otras muestras. Un total de 15 microorganismos fueros aislados en los hemocultivos, 5/15 fueron considerados patógenos (33.3%) y 10/15 contaminantes (66.7%). En los otros tipos de muestras se aislaron 9 microorganismos, 6/9 (66.7%) se consideraron patógenos y 3/9 (33.3%) contaminantes. En general la gran mayoría de los casos con crecimiento bacteriano fueron considerados como contaminados.
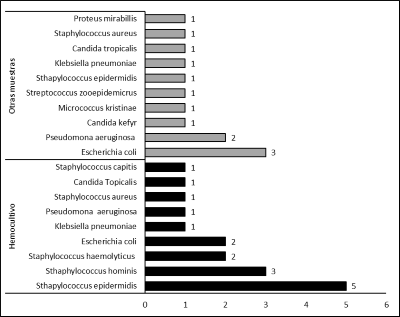
Figura 3.
Numero de microrganismos aislados en hemocultivo y otras muestras en pacientes hospitalizados con COVID-19
El porcentaje de pacientes con y sin cualquier tipo de cultivo bacteriano según uso de antibióticos se muestran en la figura 4. En aproximadamente la mitad de los pacientes que recibieron antibiótico se tomó algún tipo de muestra para cultivo (41/79) comparado con 17% (11/65) de los que no requirieron antibiótico. La proporción de cultivos positivos y negativos fue similar entre los grupos. Casi dos tercios de los pacientes que recibieron antibióticos tenían cultivos de cualquier muestra negativo y 70% hemocultivo negativo.
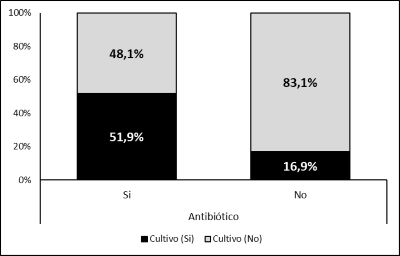
Figura 4.
Cultivo bacteriano según uso de antibióticos en pacientes hospitalizados con COVID-19
Los datos se muestran en porcentaje. †p<0.00001 (Si-Antibiótico vs No- Antibiótico)
Las alteraciones cuantitativas y cualitativas del parénquima pulmonar en la TC de tórax de los pacientes con y sin requerimientos de antibióticos se muestran en la Figura 5 y 6. El puntaje de gravedad en cada uno de los lóbulos pulmonares y total fue significativamente mayor en los pacientes que requirieron antibióticos (figura 5). También se observó en este grupo una mayor proporción (45/68) de pacientes con presencia de lesiones combinadas de vidrio deslustrado más consolidados, comparados con aquellos que no requirieron antibióticos en los que más del 50% tenían solo lesiones de tipo vidrio deslustrado (36/57).
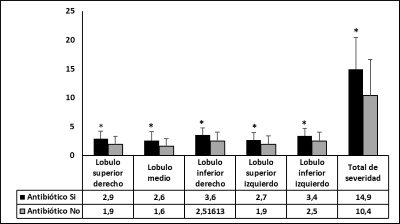
Figura 5
Puntaje de severidad por lóbulos pulmonares y total en la tomográfico de tórax según uso de antibióticos en pacientes hospitalizados con COVID-19
Los datos se muestran como media ± DE. *p<0.001 (Si-Antibiótico vs No- Antibiótico)
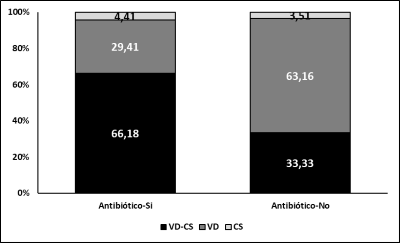
Figura 6.
Tipo de alteración predominante en la tomográfico en tórax según uso de antibióticos en pacientes hospitalizados con COVID-19
Definiciones: VD: Vidrio deslustrado; CS: Consolidados. Los datos se muestran en porcentaje *p= 0.001 (Si-Antibiótico vs No- Antibiótico)
Discusión
Los principales hallazgos de este estudio sobre prescripción de antibióticos durante la hospitalización en pacientes con COVID-19 fueron: a. aproximadamente la mitad de los pacientes hospitalizados por COVID-19 recibieron antibióticos durante su hospitalización; b. en aproximadamente un tercio de los pacientes hospitalizados con COVID19 se procesaron muestras para cultivo bacteriano y solo en un tercio de estas hubo aislamientos de microorganismos. La gran mayoría de los casos que hubo crecimiento bacteriano, fueron considerados como contaminantes; c. los pacientes a quienes se les prescribió antibiótico tenían mayor compromiso en los parámetros de oxigenación, requerimientos de oxígeno, TC de tórax y marcadores inflamatorios; d. los pacientes con requerimientos de antibióticos tenían mayor gravedad del COVID-19, mayor frecuencia de ingreso a la UCI, desarrollo de SDRA, estancia hospitalaria más prolongada y mayor proporción de fallecidos.
Diferentes estudios han reportado altas tasas de prescripción de antibióticos en pacientes hospitalizados con COVID-19 sin evidencia de apoyo de coinfección bacteriana1,4-6. El estudio ISARIC informó la prescripción de antibióticos en el 72% de los pacientes hospitalizados con COVID-191. Karami y col. en un estudio observacional retrospectivo en cuatro hospitales en los Países Bajos informaron que 1.2% de los pacientes hospitalizados con COVID-19 tuvieron una coinfección bacteriana documentada, mientras que 60.1% recibieron antibióticos10. Otro estudio retrospectivo en un centro de atención terciaria en Minnesota reporto el uso de tratamiento antimicrobiano en el 59% de todos los pacientes hospitalizados con tasas de 29%, 47% y 87% para los casos leves, moderados y graves, respectivamente11. Los datos de prevalencia de prescripción de antibióticos en pacientes hospitalizados con COVID-19 del presente estudio (54.5%) concuerdan con los reportados en la literatura previa e indican un uso elevado de antibióticos de amplio espectro en estos pacientes sin identificación previa de microrganismos patógenos y su susceptibilidad. También muestran claras diferencias en la prescripción de antibióticos entre los pacientes que están en la sala general y los que están en la UCI (97% vs 43%, respectivamente), lo que indica la importancia de la infección nosocomial en el entorno de UCI críticos y la necesidad de iniciativas continuas de prevención, control de infecciones y administración de antimicrobianos.
Una revisión sistemática y metaanálisis en 3834 pacientes con COVID-19 evaluó la frecuencia de coinfecciones y encontró que el 7% de los pacientes hospitalizados tenían una coinfección bacteriana confirmadas por laboratorio (IC 95%: 3-12%, n =2183, I2 =92.2%)5. El análisis de subgrupos del estudio mostro que el 4% de los pacientes hospitalizados fuera de la UCI tuvo una coinfección bacteriana, mientras que esta proporción aumentó a 14% en el entorno de la UCI5. Las bacterias más comunes fueron la neumonía por Micoplasma, Pseudomonas aeruginosa y Haemophilus influenzae. Otra revisión y metaanálisis reciente que incluyó 28 estudios primarios y 3338 pacientes con COVID-19, informo que la proporción general de pacientes con COVID-19 con coinfección bacteriana fue 6.9% (IC 95%: 4.3-9.5%) variando según la población de pacientes, desde 5.9% en pacientes hospitalizados hasta el 8.1% en pacientes críticos6. A pesar de una tasa baja general de infecciones bacterianas, más del 70% de los pacientes recibieron antibióticos, y la mayoría de ellos constituyeron agentes de amplio espectro como las fluoroquinolonas y las cefalosporinas de tercera generación (74% de los casos)6. Similares resultados fueron reportados en otra revisión indicando que 62/806 (8%) de los pacientes con COVID-19, experimentaron coinfección bacteriana/fúngica durante la admisión al hospital y 72% de los pacientes recibieron terapia antimicrobiana4. La mayoría de los estudios no lograron diferenciar el entorno en el que se realizó el muestreo (UCI versus no críticos). Todos estos resultados claramente indican que los antimicrobianos se administraban a una tasa mayor que el número de infecciones bacterianas confirmadas. Nuestros resultados coinciden con los estudios previos y muestran que en aproximadamente un 7% de los pacientes hospitalizados con COVID-19 se logró aislar bacterias patógenas, y en 54.5% se prescribieron antibióticos, indicando esto que el uso incrementado de antimicrobianos no coincidió con una confirmación de infección bacteriana asociada. Por otra parte, la baja frecuencia de cultivos realizados puede ser en parte explicada por la presencia frecuente de tos no productiva en pacientes con COVID-19, lo que limita la recolección de una muestra adecuada de esputo para análisis bacteriológico de rutina, así como los temores que rodean el contacto prolongado con el paciente y la generación de aerosoles al intentar inducir la toma de una muestra que pueda ser sometida a investigación microbiológica.
Seaton y col. realizaron un análisis multivariado de factores asociados con la prescripción de antimicrobianos en pacientes con COVID-19. Los resultados indican que la presencia de EPOC / enfermedad pulmonar crónica y una PCR ≥100 mg/l se asociaron con mayores probabilidades de recibir al menos un antibiótico7. Otros autores reportaron un uso mayor de terapia antimicrobiana de amplio espectro iniciada sin conocer el microrganismo patógeno y su susceptibilidad en pacientes con COVID-19 más severo8. También indicaron que los hallazgos de laboratorio al ingreso parecen ser diferente entre los regímenes de antibióticos, lo que sugiere que los marcadores inflamatorios influyeron en la decisión del médico sobre qué antimicrobiano iniciar. Por otra parte, se ha reportado un incremento en la prescripción de antibióticos con la gravedad de la enfermedad (tasas de 29%, 47% y 87% para los casos leves, moderados y graves, respectivamente)10.
Los resultados del presente estudio sugieren que la prescripción de antibióticos en nuestros pacientes hospitalizados con COVID19 pareciera estar determinada por la presencia de marcadores tradicionales que se utilizan para respaldar las decisiones sobre los antimicrobianos como signos vitales, gravedad de la enfermedad (gravedad del COVID-19, desarrollo de SDRA, admisión a UCI), mayor compromiso en los parámetros de oxigenación, requerimientos de oxígeno, puntuación de gravedad alta en la TC de tórax y mayor alteración de marcadores inflamatorios (recuento elevado de glóbulos blancos, PCR, ferritina, troponina y dímero D), así como la presencia de lesiones mixtas en la TC de tórax de vidrio deslustrado más consolidados. Los resultados también siguieren un uso menor de otros biomarcadores bacterianos específicos como la procalcitonina para respaldar la prescripción de antimicrobianos en los pacientes hospitalizados con COVID-19 al evidenciar valores similares tanto basal como control de este marcador en los pacientes con y sin antibióticos. Una posible solución para respaldar la prescripción de antimicrobianos y reducir su uso en COVID-19 seria estimular el mayor uso de biomarcadores bacterianos específicos, como la procalcitonina que respalda la diferenciación entre infección bacteriana y viral y el cese temprano de antibióticos en la infección bacteriana confirmada sin efecto sobre la mortalidad de los pacientes11,12.
Nuestro estudio tiene varias limitaciones que deben ser comentadas. Primero, es un estudio observacional retrospectivo realizado durante un brote, por lo que puede haber factores de confusión no medidos y los hallazgos podrían estar limitados por el tamaño de la muestra. No obstante, nuestros resultados concuerdan con los datos reportados en otras series en pacientes hospitalizados con COVID-19 y representan el primer análisis sobre la prescripción de antibióticos en nuestra población. Segundo, en todos los pacientes no se emplearon estudios de laboratorio para detectar la presencia de coinfección. Por lo tanto, las tasas de coinfección informadas pueden no representar las tasas absolutas que podrían haberse observado si las pruebas se hubieran utilizado ampliamente. Tercero, nuestro centro es un hospital privado de atención terciaria del área metropolitana de Caracas lo que puede limitar la validez externa a otro tipo de instituciones de salud como las de atención pública o el interior del país.
En conclusión, nuestros resultados muestran nuevas evidencias de que actualmente no hay pruebas suficientes para respaldar el uso generalizado de terapia antimicrobiana de amplio espectro en la mayoría de los pacientes hospitalizados con COVID-19, ya que la proporción de infecciones bacterianas en estos pacientes ha sido baja en diferentes series. La proporción de pacientes con prescripción de antibióticos, usualmente de amplio espectro, pareciera ser mayor en pacientes más graves y en aquellos que requieren un nivel de atención más alto. Dado que los antibióticos probablemente brindan un beneficio mínimo como tratamiento en COVID-19 y están asociados con potenciales consecuencias no deseadas, es prudente que los médicos prescriban estos medicamentos considerando criterios más estrictos para minimizar el uso de antimicrobianos innecesarios y/o inapropiados en pacientes con COVID-19.
Referencias
1. Docherty AB, Harrison EM, Green CA, Hardwick HE, Pius R, Norman L, et al. Features of 20 133 UK patients in hospital with covid-19 using the ISARIC WHO Clinical Characterisation Protocol: prospective observational cohort study. BMJ 2020 May 22;369:m1985.
2. Richardson S, Hirsch JS, Narasimhan M, Crawford JM, McGinn T, Davidson KW, et al. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area.. JAMA 2020 May 26;323(20):2052-2059.
3. World Health Organization. (2020). Clinical management of COVID-19: interim guidance, 27 May 2020. World Health Organization. License: CC BY-NC-SA 3.0 IGO. Available from: URL: https://apps.who.int/iris/handle/10665/332196.
4. Rawson TM, Moore LSP, Zhu N, Ranganathan N, Skolimowska K, Gilchrist M, et al. Bacterial and Fungal Coinfection in Individuals With Coronavirus: A Rapid Review To Support COVID-19 Antimicrobial Prescribing. Clin Infect Dis 2020 Dec 3;71(9):2459-2468.
5. Lansbury L, Lim B, Baskaran V, Lim WS. Co-infections in people with COVID-19: a systematic review and meta-analysis. J Infect 2020 Aug;81(2):266-275.
6. Langford BJ, So M, Raybardhan S, Leung V, Westwood D, MacFadden DR, et al. Bacterial co-infection and secondary infection in patients with COVID-19: a living rapid review and meta-analysis. Clin Microbiol Infect 2020 Dec;26(12):1622-1629.
7. Seaton RA, Gibbons CL, Cooper L, Malcolm W, McKinney R, Dundas S, et al. Survey of antibiotic and antifungal prescribing in patients with suspected and confirmed COVID-19 in Scottish hospitals. J Infect 2020 Dec;81(6):952-960.
8. Rothe K, Feihl S, Schneider J, Wallnöfer F, Wurst M, Lukas M, et al. Rates of bacterial co-infections and antimicrobial use in COVID-19 patients: a retrospective cohort study in light of antibiotic stewardship. Eur J Clin Microbiol Infect Dis 2021 Apr;40(4):859-869.
9. Pan F, Ye T, Sun P, Gui S, Liang B, Li L, et al. Time Course of Lung Changes at Chest CT during Recovery from Coronavirus Disease 2019 (COVID-19). Radiology 2020 Jun;295(3):715-721.
10. Stevens RW, Jensen K, O'Horo JC, Shah A. Antimicrobial prescribing practices at a tertiary-care center in patients diagnosed with COVID-19 across the continuum of care. Infect Control Hosp Epidemiol 2021 Jan;42(1):89-92.
11. Meier MA, Branche A, Neeser OL, Wirz Y, Haubitz S, Bouadma L, et al. Procalcitonin-guided Antibiotic Treatment in Patients With Positive Blood Cultures: A Patient-level Meta-analysis of Randomized Trials. Clin Infect Dis 2019 Jul 18;69(3):388-396.
12. de Jong E, van Oers JA, Beishuizen A, Vos P, Vermeijden WJ, Haas LE, et al. Efficacy and safety of procalcitonin guidance in reducing the duration of antibiotic treatment in critically ill patients: a randomised, controlled, open-label trial. Lancet Infect Dis 2016 Jul;16(7):819-827.
Notas de autor
catirasilva@gmail.com
