Cambios morfológicos del cálamo de las plumas remeras en crecimiento de palomas
Cambios morfológicos del cálamo de las plumas remeras en crecimiento de palomas
Ciencia y Agricultura, vol. 15, núm. 2, pp. 15-24, 2018
Universidad Pedagógica y Tecnológica de Colombia
Recepción: 22 Febrero 2018
Aprobación: 25 Abril 2018
Resumen: Las plumas se han utilizado para estudiar procesos de diferenciación celular y morfogénesis. existen pocos estudios histológicos en animales adultos que describan de manera secuencial la maduración de los componentes celulares durante el crecimiento; así que el objetivo de este trabajo fue describir las características histológicas de este proceso, abarcando los elementos celulares y sus relaciones anatómicas. Se obtuvieron plumas remeras de palomas, en las que se había inducido un proceso de regeneración, a los 8, 13, 18, 23 y 28 días de crecimiento. Se realizaron cortes histológicos teñidos con diferentes técnicas. Se demostró la presencia de la zona ramogénica, que tiende a disminuir de tamaño del día 8 al 28. en las crestas de la barba se observaron células de la barba, barbulares y de la placa axial, quedando cada cresta delimitada por la placa marginal. Las características celulares variaron de acuerdo con la región de las crestas, mostrando en la placa marginal transiciones de células escamosas a cuboides y nuevamente a escamosas, y, por otro lado, en la placa barbular de células cuboides a columnares y después a fusiformes. Se identificaron las células obscuras de la zona ramogénica, las cuales, por sus características tintoriales, parecen derivar de la papila dérmica. en conclusión, se realizó la caracterización histológica del cálamo y se describió, por primera vez, de manera secuencial en las diferentes etapas del crecimiento.
Palabras clave: crecimiento de la pluma, morfogénesis de la pluma, pluma, regeneración de la pluma.
Abstract: Feathers have been studied in processes of cellular differentiation and morphogenesis; however, only few histological studies in adult animals describe the maturation of the cellular components sequentially. Therefore, the objective of this work was to describe the histological characteristics, covering the cellular elements and their anatomical relationships. Pigeon feathers were withdrawn to induce regeneration, and samples were taken at different times: 8 (sprout time), 13, 18, 23, and 28 days. We prepared histological cuts using different staining techniques. We demonstrated the presence of a very marked ramogenic zone that tends to diminish from day 8 to 28. In the barb ridge, we observed the barb, barbule, and axial plate cells, with the marginal plate delimiting each barb ridge. The cellular characteristics varied according to the ridges region, showing in the marginal plate transitions from squamous to cuboidal and back to squamous cells; and, in the barbular plate, from cuboidal to columnar and then to fusiform cells. obscure cells from the ramogenic zone were identified as cells derived from the dermal papilla based on their staining. In conclusion, we characterized the histology of the calamus and, for the first time, described the different growth stages sequentially.
Keywords: feather, feather growth, feather regeneration, morphogenesis of the feather.
I. Introducción
las palomas son sumamente valiosas en investigación; sus plumas han sido utilizadas en estudios de diferenciación celular embrionaria, de interacciones celulares y de morfogénesis de las plumas (1, 2); además de servir como un modelo único para el estudio de organogénesis y de regeneración ectodérmica de órganos, por su capacidad de regenerarse en condiciones fisiológicas y en respuesta al desplume normal o inducido (3).
Los estudios realizados durante el proceso de morfogénesis de la pluma han servido de base para iniciar investigaciones en ingeniería de tejidos (4, 5), principalmente en medicina regenerativa, en donde se aplican conocimientos que permiten identificar las células que participan en el desarrollo, proliferación y crecimiento de los tejidos, incluyendo estudios moleculares y topobiológicos, que incluyen tamaño, expansión y forma celular; así como la arquitectura y disposición de los tejidos durante los procesos de organogénesis (6, 7). en el caso de la pluma, la mayoría de los estudios se han realizado empleando embriones o con animales jóvenes, principalmente en pollos, codorniz y pinzones, sin embargo, pocos se han realizado en animales adultos.
Aunque el proceso de morfogénesis de la pluma es muy complejo, se sabe que ocurre en la etapa embrionaria y durante la regeneración del plumaje, lo cual tiene como base la formación de pliegues epidérmicos dentro del folículo plumoso (cada pliegue se conoce como cresta de la barba), a partir de los cuales se van a originar los diferentes elementos de la pluma (5). una vez que se forma la pluma dentro del folículo, se realiza su crecimiento y maduración. estos eventos varían con la especie, localización geográfica, alimentación, factores fisiológicos, etc. (8, 9).
Como se sabe, la pluma presenta un cálamo, que se inserta en el folículo plumoso y se continúa con el raquis, en donde se insertan las barbas con sus bárbulas. Es el cálamo la estructura en donde se empieza a formar la pluma; externamente presenta una vaina, que va a formar el epitelio de la pluma,
A partir del cual se originan las crestas de la barba, que son las responsables de la ramificación de la pluma. De manera específica, en el espacio interno del cálamo se localiza el tejido mesenquimatoso que forma la papila, la cual queda rodeada por la pulpa; es a partir de estas dos estructuras que se liberan las moléculas inductoras de la regeneración de la pluma, estructuras que están delimitadas por el ombligo inferior y superior del cálamo (10, 11). Sin embargo, en los estudios que se han realizado durante la morfogénesis no se ha abarcado de manera sistemática la maduración de los componentes histológicos y sus interacciones durante la etapa de crecimiento de las plumas de animales adultos; es decir, hasta la fecha no se han realizado estudios comparativos dentro de la misma etapa, y pocos estudios relacionan las interacciones de los componentes celulares de la papila y la pulpa con el epitelio. Por ello, en este trabajo se describe la estructura histológica del cálamo de plumas remeras de palomas adultas y los cambios que ocurren durante las diferentes etapas de crecimiento.
II. Materiales y métodos
Se utilizaron diez palomas mensajeras (Columba livia), machos, adultos (entre 5 y 9 años de edad), que pertenecían a un criadero particular y se tenían confinadas en palomares. Las aves se alimentaron con concentrado a base de maíz amarillo, sorgo rojo y trigo y con agua limpia a libre acceso, y se mantuvieron a temperatura ambiente (20 a 25 ºc).
A. Toma de muestra
Para inducir su regeneración se hizo la extracción manual de algunas plumas, elegidas de manera aleatoria. Las plumas se dejaron crecer hasta que empezaron a brotar (día 8) y, posteriormente, a intervalos de 5 días se extrajo de cada ave una pluma en crecimiento, hasta cubrir el periodo de estudio (días 8, 13, 18, 23 y 28 a partir del día en que se extrajeron las plumas). Las muestras se fijaron en paraformaldehído al 4 % con buffer salino de fosfatos (PBS) a pH 7.4. Una vez fijadas las muestras, la región del cálamo fue disecada y se procedieron a realizar las preparaciones histológicas (11, 12, 13).
B. Preparaciones histológicas
Se empleó la técnica de inclusión en parafina de rutina, descrita por estrada et al. (14), la cual consistió de lavado de las muestras para eliminar el exceso de fijador, deshidratación con alcohol al 70
%, 80 %, 90 % y, finalmente, alcohol absoluto (100 %), con dos cambios en cada uno, aclaramiento con xileno y, para darle consistencia al tejido, se hizo la infiltración e inclusión en parafina a 60 °C. Posteriormente, se realizaron cortes transversales y longitudinales de 5-7 μm y se montaron en portaobjetos para su posterior tinción. Las técnicas de coloración empleadas fueron; Hematoxilina- eosina (H-e), Tricrómica de Gomori, Tricrómica de cason y Ácido Peryódico de Shiff (PAS). Asimismo, se realizó la histoquímica de chévremont-Frederic para corroborar el proceso de cornificación.
C. Observación de las preparaciones histológicas
La interpretación de las muestras se realizó en un microscopio carl Zeiss, modelo Axioscop Axio con los aumentos totales de 100´, 200´ y 400´. Finalmente, se tomaron fotografías con una cámara digital canon e05 1000D.
III. Resultados y discusión
En este estudio se caracteriza por primera vez el desarrollo histológico del cálamo durante el crecimiento de las plumas remeras de palomas mensajeras adultas. Así, se observó que el cálamo está constituido por una cavidad interna ocupada por tejido conectivo y limitada por una pared externa que, en los cortes transversales realizados cerca del ombligo inferior del cálamo y en los cortes longitudinales a nivel del eje del cálamo, está constituida por un tejido epitelial de revestimiento de tipo estratificado escamoso queratinizado; este epitelio presentó cambios morfológicos durante la etapa de crecimiento, para dar origen a la rama de la pluma, originando posteriormente sus elementos anatómicos, como vaina, barbas, bárbulas y raquis.
En las muestras del día 8 se observó, a nivel del estrato basal del epitelio, el inicio de la formación de algunos pliegues, mientras que hacia la región intermedia del epitelio se observó de manera dispersa la presencia de células finamente alargadas (fusiformes), dispuestas de manera vertical, las cuales presentaron mayor apetencia tintorial a H-e, Tricrómica de Gomori y chévremont- Frederic que el resto de las células del epitelio. Estas características histológicas coinciden con las de las células obscuras, observadas en la zona ramogénica en etapas posteriores del crecimiento de la pluma, y de donde se originarán las crestas de las barbas. Con las mismas tinciones, las células obscuras mostraron la misma coloración que las células de la papila dérmica, lo cual sugiere que se trata del mismo tipo celular. Las tinciones tricrómicas se utilizaron para diferenciar los tejidos epitelial y conectivo (Figs. 1 y 2).
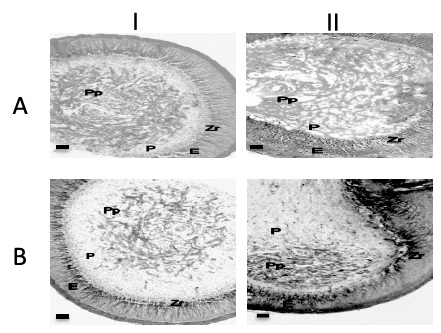
Fig. 1
Fig. 1. Componentes histológicos del filamento de la pluma a nivel del cálamo. Cortes del cálamo de las plumas remeras en los días 8 (I) y 28 (II) de crecimiento. A. Hematoxilina-eosina (I y II, cortes transversales). b. Tricrómica de Gomori (I, corte transversal y II, corte longitudinal). e. epitelio, Pp. Papila, P. Pulpa, Zr. Zona ramogénica. microscopio óptico. barra = 500 μm.
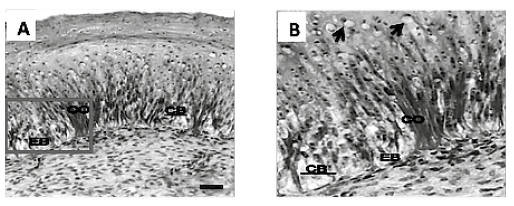
Fig. 2.
Fig. 2. corte transversal del cálamo a nivel del epitelio al día 23 de crecimiento. A. Se observan cambios morfológicos a nivel del estrato basal del epitelio (eb), como la formación de las crestas de la barba (cb) y entre estas se observa la presencia de las células obscuras (CO). B. Corresponde a la amplificación del área contenida en el recuadro. Las flechas señalan la presencia de posibles células adiposas. Tinción tricrómica de Gomori. microscopio óptico. barra = 250 μm.
Los cortes longitudinales permitieron observar adecuadamente los pliegues conocidos como crestas de las barbas en el epitelio. la región proximal del cálamo estuvo constituida por crestas pequeñas formadas por células de morfología no definida, mientras que en la región distal las crestas eran de mayor tamaño (datos no mostrados).
De los días 13 al 23 se observó, en los cortes transversales, un plegamiento marcado del estrato basal en la base del epitelio, lo que evidencia la formación de las crestas de las barbas. En el interior de cada cresta se observaron componentes celulares anidados, que darán origen, posteriormente, a las zonas de la barba (con las bárbulas) y a la placa axial. Las células del estrato basal y suprabasal, a nivel del ápice de la cresta, presentan un citoplasma claro o blanquecino. Entre cada pliegue se observaron las células obscuras. En los estratos intermedio y superficial del epitelio, entre los queratinocitos, fue posible apreciar una serie de espacios redondeados, pequeños, con núcleos desplazados hacia un extremo, coincidiendo con la apariencia normal de los adipocitos (Fig. 2). También se identificaron melanocitos que siempre permanecieron entre las células de las crestas (Fig. 3b, 3c y 3D).
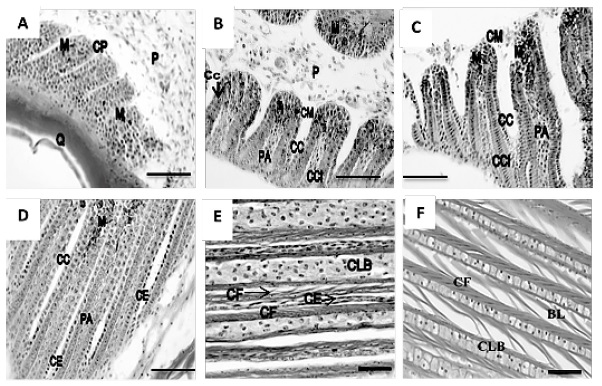
Fig. 3
Fig. 3. características morfológicas de las crestas de las barbas. A. región proximal del cálamo (Ácido Peryódico de Shiff); crestas pequeñas no diferenciadas (cP). b. Inicio de la región media del cálamo (Ácido Peryódico de Shiff); presencia de crestas de las barbas medianas (cm). c. región media del cálamo (Ácido Peryódico de Shiff); transición de crestas medianas a grandes. D. región distal del cálamo (Ácido Peryódico de Shiff); presencia de crestas grandes y alargadas. e y F. Zona de transición entre cálamo y raquis (H-e). células cuboides (cc). células cuboides de la placa barbular (cc). células columnares (ccl). células escamosas (ce). células fusiformes (cF). células de la bárbula (clb). bárbula (bl). epitelio (e). Pulpa (P). Placa axial (PA). Papila (Pp). Queratina (Q). melanocitos (m). microscopio óptico. barra = 250 μm (A, b, c y D). barra = 60 μm (e y F).
Los cortes longitudinales permitieron observar que, en todas las etapas de crecimiento, las crestas de las barbas, en la región proximal del cálamo, están constituidas por una masa de células con una morfología no definida (Fig. 3A); así como que a lo largo del cálamo las crestas empezaron a desarrollarse y crecer. en la placa marginal se identificaron células escamosas, conforme se alargaban las crestas; también se observaron células cuboides, y nuevamente se presentaron células escamosas en la región distal del cálamo. A nivel de la placa marginal, a partir del estrato intermedio, se dispuso otra capa de células cuboides que también presentó una transición a células columnares y que, finalmente, dieron origen a las placas barbulares (Fig. 3b, 3c). Tanto la placa marginal como las placas barbulares se observaron rodeando toda la cresta; ambos estratos de células se encontraron en la superficie lateral de la cresta, proximal y distalmente, separadas por un grupo de células que se disponen en el eje de la misma cresta; estas células formarán la placa axial (Fig. 3c).
Las muestras pertenecientes al día 28 mostraron que las crestas fueron disminuyendo en tamaño en toda la longitud del cálamo, tendiendo a desaparecer en el epitelio, y también disminuyó la presencia de las células obscuras en la zona ramogénica, quedando nuevamente un epitelio estratificado escamoso queratinizado. En esta etapa se observó la capa externa queratinizada muy unida al epitelio para formar la vaina (datos no mostrados).
Por otra parte, en la zona de transición, entre la región distal del cálamo y el raquis, se observaron completamente diferenciadas las crestas de las barbas, adquiriendo la estructura ramificada a partir de la barba. Al emerger de la vaina, las barbas desplegaron las bárbulas, que son estructuras alargadas formadas con células de morfología fusiforme, las cuales se expandieron externamente para formar la veleta o vano (Fig. 3e y 3F).
Con la técnica de chévremont-Frederic se detectó mayor cornificación, que se incrementó gradualmente conforme la pluma fue creciendo. Asimismo, se observó la presencia de melanocitos (Fig. 3c y 3D). con P.A.S. no se observó la presencia de glucógeno en las células de las crestas, por lo que no se pudo determinar el momento de inicio de su degeneración (datos no mostrados).
Tomando en consideración los hallazgos encontrados en los cortes histológicos realizados para describir la regeneración de las plumas, es importante destacar la formación de las crestas de las barbas, las cuales se desarrollan a partir del epitelio estratificado escamoso queratinizado que conforma la pared del filamento de la pluma. la formación de las crestas inicia en el epitelio, con la zona ramogénica, en donde se pudieron encontrar las células obscuras, de las cuales se piensa que son células epiteliales en degeneración o células mesenquimales infiltradas (3). Cada cresta se encontró perfectamente delimitada; en los cortes longitudinales se observaron dispuestas como pliegues en forma de columnas, y en los cortes transversales, como celdas. lo anterior concuerda con estudios previos realizados en pollos y pinzones por Alibardi (11, 13) y lin et al. (4). Nuestros resultados, considerando los días 8, 13, 18 y 23, muestran la presencia de crestas de diferentes tamaños, ya que se pudo detectar un alargamiento durante este periodo, encontrándose crestas de tamaño pequeño, mediano y grande, desde la región proximal hasta la región distal. en las crestas pequeñas se observó que las células mantienen una morfología similar, y en las crestas medianas y grandes se observaron estratos celulares bien definidos. Algunas de estas características coincidieron con lo reportado por Alibardi (12, 13), quien observó en la región basal de las crestas de las barbas que la epidermis permaneció poco diferenciada. A diferencia de lo señalado por este autor, en el sentido de que no se tiene el conocimiento de la organización celular en las crestas de la barba (11, 12), en este trabajo se encontraron crestas bien definidas y delimitadas en forma de pliegues (Fig. 3b, 3c y 3D).
Las características celulares de las crestas de las barbas coincidieron con los estudios realizados por Alibardi (11), Prum y Dyck (10), Sawyer et al. (15) y Yue et al. (16), quienes señalan que durante la formación de las crestas el estrato basal se dispone en la periferia de la región interna del cálamo, rodeando por completo las crestas, mientras que en el interior de estas, a partir del estrato celular intermedio, se forman las zonas medular y cortical, dividida en las placas laterales de las bárbulas y una placa axial. en la zona medular las placas laterales de las bárbulas se disponen en la cara proximal y distal de la cresta, unidas al eje que forma la zona medular y que va a originar la placa axial. en la placa marginal se observó la presencia de células escamosas que, conforme las crestas se alargaban, pasaron a ser células cuboides y nuevamente escamosas en la región distal del cálamo, desapareciendo completamente de la placa marginal al madurar las crestas de las barbas, permitiendo la liberación de las bárbulas; estos resultados coinciden con lo descrito por Alibardi (13).
En las placas barbulares se observó una transición celular de acuerdo con el tamaño de las crestas; en las crestas pequeñas se observó un epitelio simple cuboide, mientras que en las crestas medianas y grandes pasó a ser un epitelio columnar.
Esta transición, hasta donde se sabe, no ha sido reportada en las placas barbulares (Fig 3b y 3c). En los estudios de Alibardi (18), realizados en pinzón cebra, cerca de la zona de la barba, la placa barbular presentó un solo estrato de células barbulares de forma cuboide, y el resto del epitelio se observó diestratificado, con una morfología celular fusiforme. en este trabajo encontramos que en la placa axial, las células alargadas que la componen tendieron a desaparecer a nivel de las crestas ya ramificadas, lo cual coincide con lo reportado por bragulla y Hirschberg (17) y Prum (10), quienes las identifican como un tipo de células de apoyo que se caracterizan por presentar un proceso de lipogénesis y posterior desintegración, dejando solo las regiones queratinizadas unidas a las crestas, perdiéndose así su relación con las células barbulares y permitiendo la separación entre cada una de las células, para dar origen a las bárbulas. En este trabajo fueron las únicas células de apoyo que se percibieron claramente, aunque se han descrito otro tipo de células de apoyo, como las células de la cuña, que se localizan en la placa marginal de las crestas largas de las plumas en regeneración, pero estas son células que actúan como espaciadores de las crestas de la barba y participan en la cornificación (18).
A partir de nuestros resultados, postulamos que las células que inician la proliferación estuvieron alojadas en el epitelio de la región proximal, dando origen a crestas pequeñas que presentan un crecimiento hacia la región distal, realizándose una maduración próximo-distal del filamento de la pluma. El crecimiento, por lo tanto, abarcó, a nivel del epitelio, la presencia de la zona ramogénica, que dio origen a las crestas de las barbas. Asimismo, estas crestas presentaron cambios morfológicos en sus componentes celulares, iniciando con las modificaciones del estrato basal del epitelio, realizándose su plegamiento, formando la placa marginal, constituida de una capa de células cuboides en las crestas medianas. En las crestas más grandes se observaron células escamosas, cuboides y nuevamente escamosas, presentándose este epitelio a partir de la base de las crestas.
Esta transición no ha sido reportada, pero puede relacionarse con lo observado por chang et al. (4), quienes observaron a nivel del raquis y en las crestas de las barbas una diferenciación terminal, presentándose queratina, lo cual señala un proceso de apoptosis en las células con diferenciación terminal; las células de la placa marginal de las crestas cercanas al raquis crean espacios al morir, permitiendo que las células barbulares (bárbulas) de toda la rama se liberen. Nuestros resultados concuerdan con lo descrito por chang (4) y también nos hacen suponer que lo que observamos, principalmente la presencia de las células escamosas, en la base de las crestas de mayor tamaño, cerca de la zona de transición con el raquis, se debe al proceso de apoptosis que probablemente inicia en la base de la cresta; por lo tanto, se observa un epitelio simple con células escamosas, cuboides y nuevamente escamosas, permitiendo la separación de las células barbulares. La placa axial está presente en etapa temprana y desaparece en etapa tardía, dejando un espacio entre las placas barbulares. En cuanto a las células de la placa barbular, chang (4) menciona que las células se vuelven voluminosas, realizando un proceso de diferenciación terminal; en este proceso las células producen a o b queratinas y se convierten en corneocitos, similar a lo que ocurre en células epidérmicas de mamíferos. Cuando la b queratina es dominante y adquiere forma de andamio, las células se vuelven queratinocitos y van a formar las estructuras permanentes (como el pelo en los mamíferos). en la pluma, esto sucede en las células de la placa barbular que originarán las bárbulas. Con estos datos podemos decir que, en nuestro estudio, la transición de las células de la placa barbular se dio por la acumulación de queratina en el citoplasma, adquiriendo, inicialmente, una forma celular cuboide; posteriormente, columnar, y, finalmente, fusiforme. Así mismo, proponemos que las células de la barba desarrollan un proceso parecido al que sucede en los condrocitos, denominado oncosis, en el cual se da un hinchamiento de la célula, cariorrexis y cariolisis, que en el caso de las células de la barba dejan un vacío a todo lo largo del brazo de la barba, para hacer menos pesada la pluma (4, 19).
IV. Conclusiones
Se hizo la caracterización histológica del cálamo de las plumas remeras durante la etapa de crecimiento en palomas adultas. este estudio permitió identificar por primera vez de manera secuencial las diferentes etapas del crecimiento de la pluma en la base de las crestas. A nivel de la placa marginal en cualquiera de las etapas de crecimiento, se presentan células de morfología escamosa; las células presentaron morfología cuboide, y en la zona de transición entre el cálamo y raquis, las células son, nuevamente, de morfología escamosa. Ahora bien, a nivel de las placas barbulares, en las crestas pequeñas se observó un solo estrato celular de morfología cuboide; durante el alargamiento de estas crestas se presentaron células de morfología cuboide y columnar; mientras que en la zona de transición entre el cálamo y raquis las células son de morfología fusiforme. Finalmente, las células obscuras de la zona ramogénica se identificaron con base en sus características tintoriales, las cuales fueron similares a las células de la papila dérmica, lo cual permite considerar que podrían ser células que derivan de esta estructura.
Agradecimientos
A los Proyectos DGAPA-PAPIme Pe205717 (uNAm) y PIAPI 1602 (FeSc-uNAm), por el apoyo recibido para la realización de este trabajo.
Referencias
(1) lin J., luo J., redies c. Differential regional expression of multi- ple ADAms during feather bud formation. Developmental Dyna- mics. 2004; 231:741-749.
(2) Alibardi l. cell junctions during morphogenesis of feathers: ge- neral ultrastructure with emphasis on adherens junctions. Acta Zoologica (Stockholm). 2011; 92: 89-100. DoI: https://doi.org/10.1111/j.1463-6395.2010.00454.x.
(3) Alibardi l. ultraestructure of the feather follicle in relation to the formation of the rachis in pennaceous feathers. Anat Sci Int. 2010; 85: 79-91. DoI: https://doi.org/10.1007/s12565-009-0060-z.
chang cH., Yu m., Wu P., Jiang TX., Yu HS., Widelitz rb., et al. Sculpting skin appendages out of epidermal layers via tempo- rally and spatially regulated apoptotic events. J Invest Dermatol. 2004; 122: 1348-1355. DoI: https://doi.org/10.1111/j.0022-202X.2004.22611.x.
(5) lin SJ., Wideliz rb., Yue Z., li A., Wu X. Feather regeneration as a model for organogenesis. Develop Growth Differentiation. 2013; 55: 139-148. DoI: https://doi.org/10.1111/dgd.12024.
Gade Ne., Pratheesh mD., Nath A., Dubey PK., Amarpal G., Sha- rma T. Therapeutic potential of stem cell in veterinary practice. Vet World. 2012; 5(8): 499-507. DoI: https://doi.org/10.5455/vetworld.2012.499-507.
(7) Yap KK. modelling human development and disease: The role of animals, stem cells, and future perspectives. Australian Med Student J. 2012; 3(2): 8-10.
(8) Dawson A., Perrins cm., Sharp PJ., Wheeler D., Groves S. The involvement of prolactin in avian molt: the effects of gender and breeding success on the timing of molt in mute swans (Cygnus olor). General Comparative Endocrinol. 2009; 161(2): 267-270. DoI: https://doi.org/10.1016/j.ygcen.2009.01.016.
(9) Gienapp P., merilä JP. Genetic and environmental effects on a condition-dependent trait: feather growth in Siberian jays. J. Evol Biol. 2010; 23: 715-723. DoI: https://doi.org/10.1111/j.1420-9101.2010.01949.x.
(10) Prum ro., Dyck J. A hierarchical model of plumage: morpho- logy, development, and evolution. J Exp Zool (Mol Dev Evol). 2003; 298b: 73-90. DoI: https://doi.org/10.1002/jez.b.27.
(11) Alibardi l. cell organization of barb ridges in regenerating fea- thers of the quail: implications of the elongation of barb ridges for the evolution and diversification of feathers. Acta Zoologica (Stockholm). 2007; 88: 101-117. DoI: https://doi.org/10.1111/j.1463-6395.2007.00257.x.
(12) Alibardi l. cytological aspects of the differentiation of barb cells during the formation of the ramus of feathers. Int J Mor- phol. 2007; 25(1): 73-83. DoI: https://doi.org/10.4067/S0717-95022007000100010.
(13) Alibardi l. cell structure of barb ridges in down feathers and ju- venile wing feathers of the developing chick embryo: barb ridge modification in relation to feather evolution. Ann Anat. 2006; 88: 303-318. DoI: https://doi.org/10.1016/j.aanat.2006.01.011.
(14) estrada Fe., Peralta Zl., rivas mP. manual de Técnicas Histológicas. A.G.T. 1982.
(15) Sawyer rH., rogers l., Washington l., Glenn Tc., Knapp lW. evolutionary origin of the feather epidermis. Developmental Dynamics. 2005; 232: 256-267. DoI: https://doi.org/10.1002/dvdy.20291.
(16) Yue Z., Jiang TX., Widelitz rb., chuong c. m. Wnt3a gradient converts radial to bilateral feather symmetry via topological arrangement of epithelia. PNAS. 2006; 103(4): 951-955. DoI: https://doi.org/10.1073/pnas.0506894103.
(17) bragulla H., Hirschberg r. Horse hooves and bird feathers: Two model systems for studying the structure and development of highly adapted integumentary accessory organs the role of the dermo epidermal interface for the micro-architecture of complex epidermal structures. J Exp Zool (Mol Dev Evol). 2003; 298b: 140-151. 61.
(18) Alibardi l. Wedge cells during regeneration of juvenile and adult feathers and their role in carving out the branching pat- tern of barbs. Ann Anat. 2007; 189: 234-242. DoI: https://doi.org/10.1016/j.aanat.2006.11.008.
Van cS., Van DbW. morphological and biochemical as- pects of apoptosis, oncosis and necrosis. Anat Histol Embr- yol. 2002; 31: 214-223. DoI: https://doi.org/10.1046/j.1439-0264.2002.00398.x.