Goji Berry : propriedades nutricionais e benefícios para a saúde humana
Goji Berry: nutritional properties and benefits for human health
Goji Berry: propiedades nutricionales y beneficios para la salud humana
Goji Berry : propriedades nutricionais e benefícios para a saúde humana
Research, Society and Development, vol. 8, núm. 4, pp. 01-12, 2019
Universidade Federal de Itajubá

Este trabalho está sob uma Licença Internacional Creative Commons Atribuição 4.0.
Recepção: 16 Janeiro 2019
Revised: 30 Janeiro 2019
Aprovação: 31 Janeiro 2019
Publicado: 06 Fevereiro 2019
Resumo: O Lycium barbarum (Goji Bery) é uma planta pertencente à família Solanaceae, é utilizado como alimento funcional em diversos países da Ásia Oriental, Europa e América do Norte, é altamente nutritivo, possuindo oito aminoácidos essenciais, minerais, como ferro, zinco e selênio e ação antioxidante. O objetivo do artigo é investigar as possíveis propriedades nutricionais do Goji Berry e seus benefícios a saúde humana. Trata-se de uma revisão integrativa, após o levantamento dos artigos seguindo os critérios de inclusão pré-estabelecidos obteve-se um total de 13 estudos publicados nos últimos dez anos. A grande maioria (78%) dos estudos experimentais demostram efeitos positivos para o uso do Goji berry. No entanto, os efeitos adversos existem e dependendo do uso, pode ser considerado um risco para saúde pública, assim, deve-se ter cautela e orientação profissional quanto ao consumo seguro desse alimento, afim de evitar efeitos adversos, toxidades, alergias e consequências do seu consumo em demasiado, principalmente em mulheres gravidas, idosos e crianças.
Palavras-chave: Lycium Barbarum, Antioxidante, Propriedades terapêuticas..
Abstract: Lycium barbarum (Goji Bery) is a plant belonging to the family Solanaceae, is used as functional food in several countries of East Asia, Europe and North America, is highly nutritious, having eight essential amino acids, minerals such as iron, zinc and selenium and antioxidant action. The objective of the article is to investigate the possible nutritional properties of Goji Berry and its benefits to human health. It is an integrative review, after surveying the articles following the pre-established inclusion criteria, a total of 13 studies published in the last ten years were obtained. The great majority (78%) of the experimental studies show positive effects for the use of Goji berry. However, adverse effects exist and depending on the use, can be considered a risk to public health, therefore, caution and professional guidance regarding the safe consumption of this food must be taken, in order to avoid adverse effects, toxicity, allergies and consequences of their consumption on too much, especially in pregnant women, seniors and children.
Keywords: Lycium Barbarum, Antioxidant, Therapeutic Properties.
Resumen: El Lycium barbarum (Goji Bery) es una planta perteneciente a la familia Solanaceae, se utiliza como alimento funcional en diversos países de Asia Oriental, Europa y América del Norte, es altamente nutritivo, con ocho aminoácidos esenciales, minerales, como hierro, cinc y selenio y la acción antioxidante. El objetivo del artículo es investigar las posibles propiedades nutricionales del Goji Berry y sus beneficios a la salud humana. Se trata de una revisión integrativa, tras el levantamiento de los artículos siguiendo los criterios de inclusión preestablecidos, se obtuvieron un total de 13 estudios publicados en los últimos diez años. La gran mayoría (78%) de los estudios experimentales demuestran efectos positivos para el uso del Goji berry. Sin embargo, los efectos adversos existen y dependiendo del uso, puede considerarse un riesgo para la salud pública, por lo que debe tenerse precaución y orientación profesional en cuanto al consumo seguro de ese alimento, a fin de evitar efectos adversos, toxicidad, alergias y consecuencias su consumo en demasiado, principalmente en mujeres embarazadas, ancianos y niños.
Palabras clave: Lycium Barbarum, antioxidante, Propiedades terapéuticas.
1. Introdução
O Goji Berry (Lycium barbarum), pertencente à família botânica Solanaceae, é um fruto originado da região sudeste da Europa e Ásia, utilizado como alimento funcional em diversos países da Ásia Oriental, Europa e América do Norte. Caracteriza-se com 1 a 2 cm de comprimento, cor avermelhada, em forma elipsoide, possuem folhas verde-cinzas, sua arvore pode atingir até três metros de altura (Donno et al., 2014).
Segundo Song (2013), o Lycium barbarum é altamente nutritivo, contendo oito aminoácidos essenciais, minerais, como ferro, zinco e selênio. Rico em vitamina B1, B2, B6 e E, apresenta cerca de 500 vezes mais vitamina C do que a laranja. Além disso, possui atividade antioxidante, sendo atribuída a presença de compostos fenólicos, como taninos, flavonoides e outros compostos fenólicos simples, trazendo inúmeros benefícios como: a melhora do sistema imunológico; prevenção do câncer; redução de açúcar no sangue e lipídios, antienvelhecimento e aumento da fertilidade masculina (Ionica, Nour & Trandafir, 2012).
Pesquisas estão sendo desenvolvidas para confirmação dos benefícios dos componentes químicos e efeitos farmacológicos do fruto do Goji Berry, atualmente diversos componentes já foram identificados, como: hidratos de carbono, carotenoides, polissacarídeos, ácidos fenólicos (flavonoides, quinonas e cumarinas), cerebrosideos, aminoácidos (betaína), β-sitosterol, oligoelementos, vitaminas e outros componentes (Amagase & Farnsworth, 2011).
A possível ação benéfica dos compostos do Goji Berry a saúde humana acarretou o aumento de seu consumo pela população que busca uma alimentação funcional. Contudo, estudos mais aprofundados devem ser realizados para comprovação de seus efeitos positivos, assim como a identificação de efeitos adversos, toxidades, potencial alergênico e consequências do seu consumo em demasiado, principalmente em mulheres gravidas, idosos e crianças (Martins, Coimbra & Schlichting, 2014).
Este artigo teve por objetivo, investigar as propriedades nutricionais do Goji Berry e seus benefícios a saúde humana por meio de uma revisão bibliográfica integrativa.
2. Metodologia
Este estudo caracteriza-se como uma revisão bibliográfica integrativa. Segundo Mendes, Silveira & Galvão (2008), este tipo de revisão consiste na construção de uma análise da literatura, importante para discussões sobre métodos e resultados de pesquisas. O propósito inicial é obter um profundo entendimento de um determinado fenômeno baseando-se em estudos anteriores, de maneira sistemática e ordenada, contribuindo para o aprofundamento do conhecimento do tema investigado.
Para tanto realizou-se a seguinte sequência de busca: identificação do tema e seleção da hipótese, busca nas bases de dados eletrônicas, definição das informações a serem extraídas dos estudos selecionados, estabelecimento de critérios para inclusão e exclusão de estudo, interpretação dos resultados e apresentação da revisão/síntese do conhecimento.
De acordo com a temática: Goji Berry (Lycium Barbarum): propriedades nutricionais e benefícios para a saúde humana, elaborou-se a estratégia de busca utilizando-se as bases de dados: PubMed, Scielo e Cochrane, utilizando descritores indexados e cadastrados no banco de dados Descritores em Ciências da Saúde (DeCS) e Medical Subject Headings (MeSH).
A busca dos artigos foi realizada nos meses de março a maio de 2018 por meio dos descritores “Goji Berry,” Lycium barbarum”, “antioxidante”, “hepatoprotetor”, “resistência à insulina” e “potencial alergênico”, utilizados isoladamente em combinações na língua portuguesa e inglesa. Para guiar este estudo elaborou-se a seguinte questão: “Qual ou quais os potenciais benefícios do consumo regular de Goji Berry (Lycium barbarum) à saúde humana?
Os critérios de inclusão utilizados para a seleção dos artigos foram: pesquisas originais realizadas com seres humanos publicadas em inglês, português, que estivesse disponível na integra, publicadas entre os anos de 2006 a 2017, e que avaliassem as possíveis propriedades nutricionais e os benefícios do consumo regular de Gojy Berry. Foram excluídas pesquisas advindas de artigos de revisão e que não estivessem disponíveis na integra. Os detalhes da seleção dos estudos estão expostos no fluxograma logo abaixo (Figura 1).
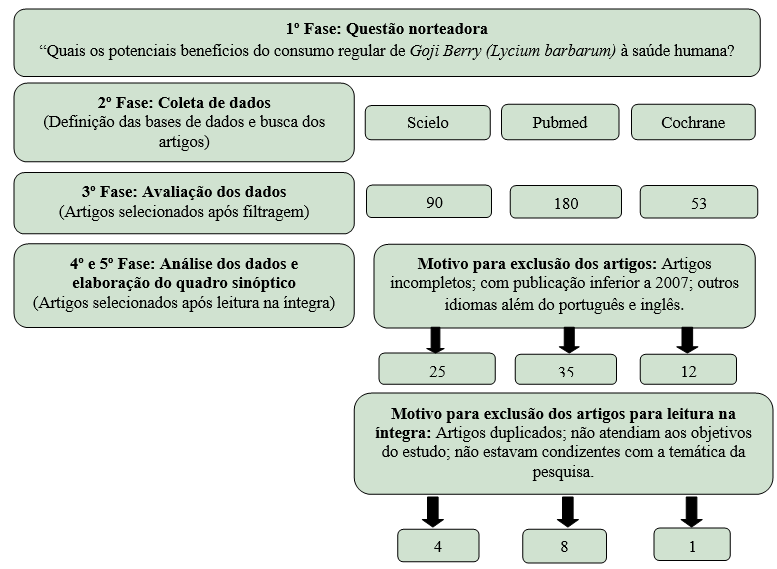
Figura 1.
Fluxograma de identificação, seleção e inclusão dos estudos da revisão integrativa.
Fonte: Dados da pesquisa,2018.
A amostra final foi constituída por 13 artigos científicos, selecionados pelos critérios de inclusão previamente estabelecidos.
3. Resultados e Discussão
Para a extração de dados dos artigos incluídos foram considerados: identificação de autores e ano da publicação, características do método abordado nos estudos, avaliação metodológica, intervenções estudadas e resultados encontrados. A apresentação dos dados e a discussão foram feitas de forma descritiva. Os artigos incluídos neste estudo estão apresentados na tabela 1.
| AUTOR E ANO | METODOLOGIA | RESULTADOS |
| AMAGASE & NANCE, 2008. | Ensaio clínico randomizado, duplo-cego e controlado com placebo. Examinou os efeitos gerais do Lycium barbarum consumida oralmente, como um suco padronizado, em adultos saudáveis por 14 dias. Medidas de peso corporal, índice de massa corporal, pressão arterial, taxa de pulso e acuidade visual foram avaliados antes e depois consumindo 120 mL de Goji berry/dia ou solução de controle de placebo. Os dados foram analisados estatisticamente por mudanças. dia 1 e dia 15. | Diferenças significativas entre o dia 1 e 15 dia foram encontradas no grupo que consumiram o Goji berry (n=16) para nível de energia, desempenho atlético, qualidade do sono, facilidade de despertar, capacidade de se concentrar em atividades, acuidade mental, calma e sentimentos de saúde, contentamento e felicidade. Também reduziu significativamente a fadiga, estresse, e melhoria da regularidade da função gastrointestinal. Em contraste, o grupo placebo (N=18) apresentaram apenas duas mudanças significativas (azia e felicidade). |
| AMAGASE, SOL & BOREK, 2009. | Estudo clínico randomizado, duplamente cego, controlado por placebo, durante 30 dias. Incluiu 50 adultos chineses saudáveis com idade 55-72 anos. Os marcadores antioxidantes constituíram-se de níveis sérios de superóxido dismutase, glutationa peroxidase, e níveis reduzidos de malondialdeído, observados na pré e pós intervenção com 120mL de goji berry ou placebo. | No grupo goji os marcadores antioxidantes aumentaram e malondialdeído reduzida significativamente, nos grupos pré e pós intervenção. E não foram observadas diferenças significativas entre os momentos pré e pós intervenção no grupo placebo. |
| WU et al. 2010. | Investigou-se a estrutura química dos polissacarídeos de Lycium Barbarum e sua modulação sobre o estresse oxidativo em ratos com alto teor de gordura. Os polissacarídeos continham principalmente xilose e glicose. Os ratos foram alimentados com dieta rica em gordura por 2 meses. | Os resultados mostraram que as atividades das enzimas antioxidantes do sangue e do fígado e o nível de GSH nos camundongos modelo diminuíram significativamente, e o nível de MDA aumentou significativamente (p<0,01) em comparação com ratinhos de controle normais. |
| AMAGASE & NANCE, 2011. | Dois ensaios clínicos separados aleatorizados, duplamente cegos e controlados com placebo foram realizados usando um suco de fruta padrão de goji e avaliado seus efeitos na taxa metabólica de repouso (RMR) e gasto de energia pós-prandial (PPEE) como medido por calorimetria indireta após a ingestão de bolus único de 3 doses de L. barbarum (30, 60 e 120 ml) e placebo; e circunferência da cintura e outras alterações morfométricas em um ensaio de intervenção de 14 dias (ingestão diária de 120 ml) nos indivíduos (idade = 34 anos, IMC = 29 kg / m (2)). | No ensaio da RMR um único bolo de L. barbarum aumentou o nível basal pós-dose PPEE 1 a 4 horas pós-dose de uma maneira dependente da dose e foi significativamente maior do que o grupo placebo em 10% a 1 hora após a ingestão de 120 ml (p <0,05 ). Em um ensaio da circunferencia da cintura de intervenção de 14 dias, L. barbarum diminuiu significativamente a circunferência da cintura em 5,5 ± 0,8 cm (n =15) em comparação com as medidas de préintervenção e o grupo placebo no dia 15 após a intervenção (p <0,01). Em contraste, as alterações no grupo de placebo (n = 14) de preintervenções foram 0,9 ± 0,8 cm, o que não foi estatisticamente significante. |
| BUCHELI et al. 2011. | Ensaio clínico randomizado, duplo-mascarado com 150 idosos de 65-70 anos. Dois grupos, foram avaliados durante 90 dias placebo e experimental, sendo que o segundo recebeu 13,7 g / d do leite da baga do goji berry. Depois foi analisado uma amostra de sangue para medir o nível de zeaxantina plasmática e a capacidade total antioxidante. | No grupo experimental o nível de zeaxantina plasmática e a capacidade antioxidante aumentou significativamente, e não alterou no grupo placebo. Não foi verificado eventos adversos nos dois grupos. |
| CHENG & HONG KONG, 2011. | Investigou-se efeitos de Lycium barbarum sobre lesões hepáticas induzidas pelo álcool em 36 ratos, divididos em grupos, controle, etanol e etanol + Lycium barbarum. Grupo etanol foram alimentados com7 g de etanol / kg de peso corporal por infusão gástrica, três vezes ao dia, durante 30 dias consecutivos. Grupo controle receberam o mesmo volume de solução salina fisiológica em vez de Etanol. E grupo etanol + Lycium barbarum foram alimentados com etanol (7 g / kg de peso corporal) e Lycium barbarum (300 mg / Kg de peso corporal / dia).A lesão hepática foi analisada pela alanina e aspartato amino transferase, o fígado gordo alcoólico foi avaliado pelos níveis lipídicos e o estresse oxidativo pelos marcadores antioxidantes. | No grupo etanol, houve uma elevação significativa de enzimas e lipídios no soro, aumento do nível de MDA e SOD, CAT, GSH-Px e GSH no fígado. LBP significativamenteLesão hepática melhorada, impediu a progressão do fígado gordo induzido pelo álcool eMelhorou as funções antioxidantes quando comparado com o grupo etanol. O exame histopatológico do fígado de rato revelou que a administração de LBP protegia o fígado do dano induzido pelo etanol. |
| LARRAMENDI et al. 2012. | Recrutou-se 30 indivíduos com alergias alimentares de plantas para fazerem uso às bagas de Goji durante 3 meses. Quatro pacientes relataram sintomas, seis tolerou as bagas e 20 nunca tentaram as bagas de Goji. Os pacientes foram submetidos a testes cutâneos com bagas de Goji, pele e planta, alimentos panalergenos como marcadores de reatividade cruzada entre alimentos não relacionados. | Os testes cutâneos para bagas de Goji foram positivos em 24 pacientes (77%): 5 pacientes sintomáticos e 19 pacientes assintomáticos. Positividade para as bagas de Goji foi associada com positividade à casca de pêssego e à proteína de transferência de lipídios não-especifico panalergen (LTP). Em todos os cinco casos, foi encontrada IgE específica contra bagas de goji. Várias reconhecidas 2 bandas (7 e 50 kDa) na imunotransferência. A inibição com LTP impediu a ligação da IgE à banda de 7 kDa, sugerindo o papel desse panalergeno na sensibilização para bagas de goji. |
| CARNÉS et al. 2013. | Investigou-se a frequencia de sensilbilação dos gens envolvidos com o alergismo as bagas de Goji Berry(GB). 566 indivíduos, com sintomas respiratórios ou cutâneos, foram submetidos à prova de pele com bagas de Goji Berry. | Trinta e três foram positivos (5,8%). 94% foram sensibilizados para outros alérgenos, IgE específica para GB, pêssego. Treze de 24 soros disponíveis (54,2%) tiveram IgE específica. 92,3% dos pacientes com GB positivos foram positivos para o pêssego. Sete indivíduoS reconheceram 8 bandas e seis reconhecidos na banda de 7 kDa. Banda identificada como LTP. |
| PREETHI et al. 2013. | Explorou-se os efeitos hipolipidêmicos do Lycium barbarum L. Solanaceae em pó no modelo de hiperlipidemia induzida por dieta de alta gordura. O extrato de frutos de L. barbarum em pó (250mg / kg e 500mg / kg) foi administrado a ratos Wistar albinos alimentados com uma dieta rica em gordura colesterol durante 45 dias. Os efeitos foram comparados com o medicamento padrão atorvastatina (10 mg / kg / dia, oral). Após 30 dias de tratamento, o perfil lipídico das amostras de sangue dos roedores experimentais foi avaliado. | O extrato em pó de L. barbarum mostrou uma redução significativa no colesterol total, triglicerídeos e níveis de lipoproteína-colesterol de baixa densidade em ambas as doses empregadas (p <0,05). No entanto, a redução nos níveis de lipoproteína-colesterol de baixa densidade foi significativa (p <0,05) apenas na dose de 500 mg / kg quando comparada ao grupo de fármaco padrão. O aumento nos níveis de lipoproteínas de alta densidade foi significativo somente em 250 mg / kg. |
| WANG et al. 2014. | Investigou-se se a Lycium barbarum P. impedia o fígado gordo por meio da ativação da proteína quinase ativada com monofosfato de adenosina (AMPK) e a supressão da proteína-1c de ligação ao elemento regulador de esterol (SREBP-1c). Os ratos machos C57BL / 6J foram alimentados com uma dieta rica em gordura, dieta rica em gordura ou dieta de 100 mg / kg de tratamento com Lycium barbarum P. durante 24 semanas. As células HepG2 foram tratadas com Lycium barbarum P. na presença de ácido palmítico. | Lycium barbarum P. melhorou as composições corporais e os perfis metabólicos lipídicos em rato alimentados com dieta rica em gordura, reduzindo significativamente o acúmulo hepático de triacilglicerol intracelular. Lycium barbarum P. atenuou a esteatose hepática. Além de poder ativar a fosforilação do AMPK, suprimir a expressão nuclear do SREBP-1c e diminuir a expressão de proteínas e mRNA de genes lipogênicos. Por fim, Lycium barbarum P. aumentou significativamente a proteína de desacoplamento-1 (UCP1) e a expressão do tecido adiposo marrom-ativado por proliferador de peroxissoma-1 (PGC-1) |
| YANG et al. 2014. | Investigou-se o mecanismo envolvido no eixo fosfatidilinositol 3-quinase (PI3K) / AKT / Nrf2 mediado por Lycium barbarum P. contra a resistência à insulina induzida por alto teor de gordura. As células HepG2 foram incubadas com Lycium barbarum P durante 12 horas na presença de palmitato. Os ratinhos C57BL / 6J foram alimentados com uma dieta rica em gordura suplementada com Lycium barbarum P durante 24 semanas. | Analisou-se a expressão do fator nuclear fator 2 (Nrf2), quinases Jun N-terminal (JNK) e glicogênio sintase quinase 3β (GSK3β) envolvidas na via de sinalização de insulina in vivo e in vitro. Lycium barbarum P induziu significativamente a fosforilação de Nrf2 através da sinalização PI3K / AKT, aumentou a expressão de desintoxicação e enzimas antioxidantes e reduziu os níveis de espécies reativas de oxigênio (ROS) através do eixo PI3K / AKT / Nrf2. E por último regulou os níveis de fosforilação de GSK3β e JNK através da sinalização PI3K / AKT. Finalmente, a Lycium barbarum P reverteu significativamente a expressão dos genes glicolônico e gluconegênico através da ativação de efeitos citoprotectores mediados por Nrf2 |
| XIA et al. 2014 | Foram investigados efeitos protetores do Lycium barbarum L. contra a hepatoxicidade por tetracloreto de carbono em fatias de fígado de peixes carpas in vitro e in vivo. In vitro: 03 grupos, antes, após e antes e depois da exposição ao tetracloreto de carbono, aos quais foram adicionais Lycium barbarum L.nas concentrações de0,1, 0,3 e 0,6 mg/mL, respectivamente. In vivo: 03 grupos, aos quais foram alimentados com dietas contendo Lycium barbarum L., nas concentrações de 0,1, 0,5 e 1%, durante 60 dias antes de uma injeção intraperitoneal de tetracloreto de carbono à 30% com volume de 0,05 mL/10 g de peso corporal. | In vitro o Lycium barbarum L. aumentou as enzimas antioxidantes suprimidas no pré e pré e pós tratamento. E in vivo, suplementação nas concentrações de0,5 e 1% reduziram significativamente os níveis de algumas enzimas marcadoras de toxicidade. E inibiu a redução das enzimas antioxidantes e aumentou o malondialdeído no tecido hepático. |
| HENRY et al. 2017. | Ensaio controlado randomizado duplo-mascarado que investigou o efeito do tratamento de Lycium barbarum (LB) nas funções da retina e estrutura de pacientes com Retinite pigmentosa (RT). Os particpantes foram alocados aleatoriamente para grupos de tratamento LB ou placebo com o fornecimento de LB ou placebo por 12 meses. Havia casos totais de 41 RP (22 em grupo LB e 19 em grupo placebo) completou a intervenção de 12 meses. | As taxas de conformidade para os grupos LB e placebo foram 89,8% ± 12,5% e 85,3% ± 7,7% respectivamente. Em comparação com o grupo placebo, não houve deterioração da acuidade visual de alto e baixo contraste no grupo LB (P <0,01). Além disso, algumas melhorias da resposta da haste escotópica e resposta do cone fotópico do ffERG foram obtidas em Grupo LB (P <0,05). Na medida óptico tomografia de coerência (OCT), observou-se um desbaste óbvio da espessura macular no grupo placebo, mas não encontrado no grupo LB (P <0,05). No entanto, não houve alterações na sensibilidade do campo visual central entre dois grupos. |
Os resultados apresentados demostram que a maioria (78%) dos estudos experimentais encontraram efeitos positivos para o uso do Goji berry. No entanto, os efeitos adversos existem e dependendo do uso, pode ser considerado um risco para saúde pública.
Xia et al. (2014), Cheng, Hon & Kong (2011) e Wang, et al. (2014), defendem em seus estudos o uso do Lycium barbarum (LBP) como agente hepatoprotetor, mas os experimentos foram realizados in vitro. Xin et al. (2011), destacam que LBP provocou, em seu ensaio in vitro, um típico pro-efeito protetivo sobre a cardiotoxicidade aguda induzida por doxorrubicina aguda (DOX) por meio da supressão do estresse oxidativo.
No ensaio clínico randomizado realizado com idosos, Bucheli et al. (2011), encontraram que o grupo experimental suplementado com leite da baga do goji berry aumentaram sua capacidade antioxidante. A desvantagem é que o mecanismo de ação de como ocorreu o aumento dos níveis de antioxidantes pelo uso da baga não foi descrito.
A atividade antioxidante do Lycium barbarum também é defendida por Amagese, Sol & Borek (2009), a eficácia antioxidante do Goji foi encontrada em adultos chineses que fizeram uso de 120 mL de goji berry por 30 dias. Em outro ensaio clínico com adultos humanos saudáveis fazendo uso durante 14 dias de 120 ml de suco de goji, Amagese & Nance (2011), encontraram aumento da taxa metabólica e redução da circunferência da cintura, em relação aos indivíduos controlados tratados com placebo. Khanal et al. (2010), usando o bagaço de goji na dieta não encontraram diferença significativa no peso corporal, mas observaram uma diminuição na gordura total.
Ainda de acordo com o estudo de Amagase & Nance (2011), o qual descreveu que tomar diariamente 120 ml do suco de goji berry por 14 dias, melhora atividade cerebral e digestão. O goji berry, é fonte de fibras que promovem efeito laxativo normal e podem tratar a constipação, o que pode ter ocasionado melhora no funcionamento intestinal.
Preethi et al. (2013), buscaram em seu experimento demostrar os efeitos hipolipidêmicos do Lycium barbarum L. In vitro, a suplementação do goji em pó durante 45 dias, associado a uma dieta rica em gordura, apresentou efeito anti-hiperlipidêmico.
Um outro fator positivo quanto ao uso do goji é seu efeito contra a resistência a insulina. Yang et al. (2014), suplementaram ratos durante 24 semanas. Assim como os outros estudos in vitro, os animais eram alimentados simultâneamente com uma dieta rica em gordura. E no final das 24 semanas os ratos não desenvolveram resistência devido a ativação da PI3K/AKT/Ntf2.
Os efeitos adversos do uso do goji encontrados nos estudos estão relacionados ao alergismo ocasionados pelas bagas. E o responsável pela alergia pode ser uma proteína de transferência de lipidios presente no goji e em muitas outras frutas.
Outro efeito avesso é abordado por Riviera et al. (2012), pacientes que fazem uso do anticoagulante varfarina devem evitar o uso do goji, pois aumenta o tempo atividade da protrombina (TAP) e seu derivado índice internacional normalizado, também conhecido como razão normalizada internacional ou RNI (>6).
Atualmente, estudos demostram que Lycium barbarum (LB) tem efeito neuroprotetivo na retina. Henry et al. (2017), investigaram o efeito do tratamento de goji nas funções da retina e estrutura de pacientes com retinite pigmentosa (RP) e observou melhorias (p <0,05) da resposta da haste escotópica e resposta do cone fotópico do ffERG. Concluiu que o tratamento com LB pode atrasar ou minimizar a deterioração da função visual em RP.
Estudos recentes também indicam que o Lycium barbarum tem efeito na inibição em células de cânceres. Hsu et al. (2017), determinaram o conteúdo de carotenóides em L. barbarum por cromatografia líquida de alta performance, espectrometria de massa, seguido da preparação de uma nanoemulsão carotenóide para avaliar o mecanismo de inibição em células de câncer de colo HT-2 e observou que a nanoemulsão carotenóide e o extracto foram eficazes para inibir o crescimento de células de câncer de cólon HT-29.
4. Consideracões finais
Goji berry tem alto poder antioxidante e consequentemente efeitos positivos, hipoglicêmico e hipolipidêmicos, na saúde humana, além de efeito neuroprotetivo na retina e inibidor de células de cânceres. Mas, seu uso deve ser controlado uma vez que pode causar efeitos colaterais desconhecidos e, em alguns casos, conduzir a quadro de intoxicação ou interação medicamentosa. Por exemplo, em indivíduos com alergias alimentares, o consumo de goji pode causar alergia e nas pessoas que fazem uso de varfarina é contraindicado. Apesar dos resultados apresentados nos estudos serem mais promissores do que desanimadores, faz-se necessários mais experimentos envolvendo seres-humanos.
Os estudos evidenciam efeitos benéficos do Goji Berry para a saúde humana, alcançando o objetivo do artigo, entretanto, é necessário a realização de mais estudos afim de se estabelecer padrões e quantidade máxima a ser ingerida, no intuito de se obter resultados positivos e evitar possíveis efeitos colaterais.
Referências
Amagase, H. & Farnsworth, N. R. (2011). A review of botanical characteristics, phytochemistry, clinical relevance in efficacy and safety of Lycium barbarum fruit (Goji). Food Research International, 44(1):1702–1717. Disponível em: https://www.sciencedirect.com/science/article/pii/S0963996911001840.
Amagase, H. & Nance, D. M. (2008). A randomized, double-blind, placebo-controlled, clinical study of the general effects of a standardized Lycium barbarum (goji) juice, GoChi™. The Journal of Alternative and Complementary Medicine, 14(4):403-12. Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/18447631.
Amagase, H. & Nance, D. M. (2011). Lycium barbarum increases caloric expenditure and decreases waist circumference in healthy overweight men and women: pilot study. Journal of the American College of Nutrition, 30(5):304-9, Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/22081616.
Amagase, H.; Sun, B. & Borek, C. (2009). Lycium barbarum (goji) juice improves in vivo antioxidant biomarkers in serum of healthy adults. Nutrition Research, 29(1):19-25. Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/19185773.
Bucheli, P. et al. (2011). Goji Berry Effects on Macular Characteristics and Plasma Antioxidant Levels. Optometry and vision Science, 88(2):257-62. Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/21169874.
Carnés, J. et al. (2013). Recently introduced foods as new allergenic sources: Sensitisation to Goji berries (Lycium barbarum). Food Chemistry, 137(1):130-5. Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/23200000.
Cheng, D.& Kong, H. (2011). The Effect of Lycium Barbarum Polysaccharide on Alcohol-Induced Oxidative Stress in Rats. Molecules,16(1):2542-50, Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/21415835.
Donno, D. et al. (2014). Goji berry fruit (Lycium spp.): antioxidant compound fingerprint and bioactivity evaluation. Journal of Functional Foods, 18(1):1070-85. Disponível em: https://www.sciencedirect.com/science/article/pii/S175646461400191.
Henry, C. et al. (2017). Cone rescue in retinitis pigmentosa by the treatment of Lycium barbarum (Random Clinical Trial). Annals of Eye Science, 2(1). Disponivel em: https://clinicaltrials.gov/ct2/show/NCT02244996.
Hsu, H. J. et al. (2017). Preparation of carotenoid extracts and nanoemulsions from Lycium barbarum L. and their effects on growth of HT-29 colon cancer cells. Nanotechnology, 28(13). Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/28266352.
Ionica, M. E.; Nour, V. & Trandafir, I. (2012). Polyphenols content and antioxidant capacity of goji fruits (Lycium chinense) as affected by the extraction solvents. South Western Journal of Horticulture, Biology and Environment, 3(2):121-9. Disponivel em: https://www.researchgate.net/publication/288802749_Polyphenols_content_and_antioxidant_capacity_of_goji_fruits_Lycium_chinense_as_affected_by_the_extraction_solvents.
Khanal, R. C. et al. (2010). Cranberry pomace partially ameliorates metabolic factors associated with high fructose feeding in growing Sprague–Dawley rats. Journal of Functional Foods, 2(4):284-91, Disponivel em: https://www.sciencedirect.com/science/article/pii/S1756464610000629.
Larramendi, C. H. et al. (2012). Goji Berries (Lycium barbarum): Risk of Allergic Reactions in Individuals With Food Allergy. Investig Allergol Clin Immunol, 22(5):345-50. Disponivel em: https://www.ncbi.nlm.nih.gov/pubmed/23101309.
Martins, G. S. G.; Coimbra, C. C. B. E. & Schlichting, C. L. R. (2014). Toxicidade do goji berry (lyciumbarbarum). Revista UNINGA Review, 20(1):87-91. Disponível em: http://revista.uninga.br/index.php/uningareviews/article/view/1561.
Mendes, K. D. S.; Silveira, R. C. C. P. & Galvão, C. M. (2008). Revisão integrativa: método de pesquisa para a incorporação de evidências na saúde e na enfermagem. Revista Enferm. Florianópolis, 17(4):758-64. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-07072008000400018.
Preethi, G. P. (2013). Evaluation of Hypolipidemic Effects of Lyciumbarbarum (goji Berry) in a Murine Model. Jornal of natural remedies, 13(1). Disponível em: http://www.informaticsjournals.com/index.php/jnr/article/view/110.
Rivera, C.A. et al. (2012). Probable interaction between Lycium barbarum (Goji) and warfarin. Pharmacotherapy, 32(3)3:50-3. Disponível em: https://www.ncbi.nlm.nih.gov/pubmed/22392461.
Xia, G. et al. (2014). Inhibitory effect of Lycium barbarum polysaccharides on cell apoptosis and senescence is potentially mediated by the p53 signaling pathway. Molecular medicine reports, 9(4):1237-41. Disponível em: https://www.ncbi.nlm.nih.gov/pubmed/24549741.
Apéndice
Porcentagem de contribuição de cada autor no manuscrito
Josiane da Rocha Silva Ferraz - 30%
Joyce Lopes Macedo - 25%
Daisy Jacqueline Sousa Silva - 25%
Lucas Vinicius Alves Sampaio - 20%
