Resumo: Diversos materiais do cotidiano possuem propriedades indicadoras ácido-base. Pensando nisso, este artigo tem como objetivo desenvolver um material de consulta sobre Indicadores ácido-base feitos a partir desses materiais, que possam ser usados pelo professor de Química no conteúdo de Ácidos e Bases para realizar a identificação destes, e dessa forma, poder contextualizar seu ensino com o cotidiano dos alunos, que muitas vezes associam os conteúdos da Química a algo de difícil compreensão e sem aplicações no dia a dia. Foram selecionadas 10 substâncias (uva roxa, açaí, azeitona preta, repolho roxo, feijão preto, flor jasmim-manga, flor minilacre, flor hibisco, cebola roxa e berinjela) para a preparação dos extratos, que foram feitos utilizando álcool etílico comum, encontrado em farmácias e mercados, por um período de 24 horas. Os extratos foram testados em quatro substâncias: ácido muriático comercial, soda cáustica comercial, vinagre e sabão. Todos os indicadores apresentam resultados satisfatórios, conseguindo identificar com distinção substâncias ácidas e básicas, o que permite inferir que podem ser usados como ferramenta de ensino pelo professor de Química.
Palavras-chave:Ensino de QuímicaEnsino de Química,Indicador ácido-baseIndicador ácido-base,Material de baixo custoMaterial de baixo custo,ExperimentaçãoExperimentação.
Abstract: Several everyday materials have acid-base indicator properties. This article aims to develop a reference material on acid-base indicators made from these materials, which can be used by the professor of Chemistry in the content of Acids and Bases to carry out the identification of these, and in this way, to be able to contextualize their teaching with the daily life of the students, who often associate the contents of Chemistry with something difficult to understand and without applications in everyday life. A total of 10 substances (purple grape, açaí, black olives, purple cabbage, black beans, jasmine-mango flower, minilacre flower, hibiscus flower, purple onion and eggplant) were selected for the preparation of the extracts, which were made using ethyl alcohol, found in pharmacies and markets, for a period of 24 hours. The extracts were tested on four substances: commercial muriatic acid, commercial caustic soda, vinegar and soap. All the indicators present satisfactory results, being able to identify with acid and basic substances distinction, which allows to infer that they can be used as a teaching tool by the professor of Chemistry.
Keywords: Chemistry Teaching, Acid-base indicators, Low cost material, Experimentation.
Resumen: Diversos materiales del cotidiano poseen propiedades indicadoras ácido-base. En este artículo se pretende desarrollar un material de consulta sobre Indicadores ácido-base hechos a partir de esos materiales, que puedan ser usados por el profesor de Química en el contenido de Ácidos y Bases para realizar la identificación de éstos, y de esa forma, poder contextualizar su enseñanza con el cotidiano de los alumnos, que muchas veces asocian los contenidos de la Química a algo de difícil comprensión y sin aplicaciones en el día a día. Se seleccionaron 10 sustancias (uva morada, açaí, aceituna negra, repollo morado, frijol negro, flor jazmín-manga, flor minilacre, flor hibisco, cebolla morada y berenjena) para la preparación de los extractos, que se hicieron utilizando alcohol etílico común, encontrado en farmacias y mercados, por un período de 24 horas. Los extractos se probaron en cuatro sustancias: ácido muriático comercial, sosa cáustica comercial, vinagre y jabón. Todos los indicadores presentan resultados satisfactorios, logrando identificar con distinción sustancias ácidas y básicas, lo que permite inferir que pueden ser usados como herramienta de enseñanza por el profesor de Química.
Palabras clave: Enseñanza de la Química, Indicador ácido-base, Material de bajo costo, Experimentación.
Indicadores ácido - base produzidos com materiais de baixo custo para uso no Ensino de Química
Acid-base indicators produced with low cost materials for use in Chemistry Teaching
Indicadores ácido-base producidos con materiales de bajo costo para uso en la Enseñanza de la Química

Recepção: 02 Junho 2019
Revised: 05 Junho 2019
Aprovação: 06 Junho 2019
Publicado: 07 Junho 2019
Diversas substâncias presentes em flores, frutos e vegetais podem agir como indicadores ácido-base. São essas substâncias que lhes conferem cor, aroma e sabor. Segundo Alkema (1952), apud Couto (1997), dentre as principais substâncias encontram-se os flavonoides, carotenoides e porfirinas. A Tabela 1 exemplifica esses corantes.
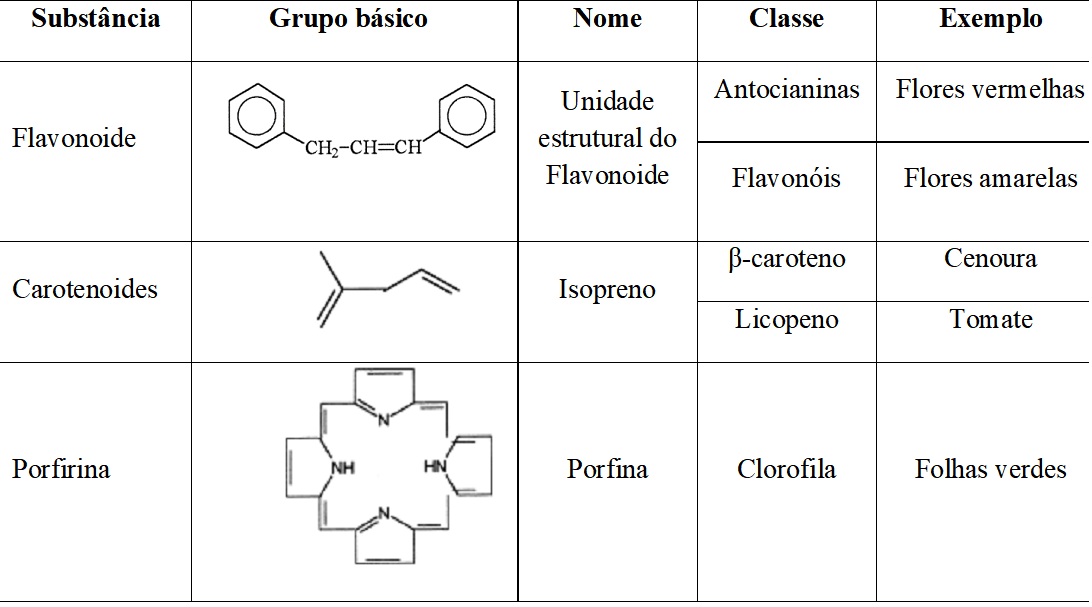
Soares (2001), citando estudos sobre mudança de coloração, referencia as afirmações de Geissman (1941), observando que compostos com pH variando entre ácidos e básicos que tinham essas substâncias adicionadas em seu meio apresentavam mudança de coloração. Mudanças de coloração semelhante foram estudadas por autores como Soares (2001).
Extratos naturais dessas substâncias indicadoras ácido-base podem ser amplamente usados e explorados didaticamente no ensino de química e ciências, tanto na parte de coleta e extração, quanto na parte de identificação das mudanças de coloração em função do pH em que se encontram. É possível a elaboração de aulas práticas no ensino de química tratando, por exemplo, da identificação de substâncias ácidas e básicas, processos de separação de mistura e soluções.
A ciência Química é tida por muitos estudantes como algo abstrato e de difícil entendimento. Fazer com que os alunos compreendam os conceitos químicos é tarefa árdua para o professor, pois muitas vezes este não dispõe de material didático ou mesmo de formação adequada para produzi-los. Segundo a Lei de Diretrizes e Bases da Educação LDB 9394/96, é essencial que o aluno conclua o ensino médio compreendendo conceitos técnicos e científicos e saiba, de forma clara, relacionar teoria e prática, não podendo, o ensino de química, ser resumido a apenas apresentação de conceitos sem a devida contextualização. Conforme os Parâmetros Curriculares Nacionais, no Ensino Médio “é importante apresentar ao aluno fatos concretos, observáveis e mensuráveis, uma vez que os conceitos que o aluno traz para a sala de aula advêm principalmente de sua leitura do mundo” (Brasil, 2000).
Com as devidas técnicas, é possível relacionar de forma simples e prática, conteúdos ministrados na disciplina de Química ao cotidiano do aluno, pois esta faz-se presente em todo lugar. Um dos conteúdos abordados na Química no ensino médio é o conceito de Ácido e Base. O aluno precisa compreender o que são essas substâncias, suas características, aplicabilidades e como identificá-las. E é no desenvolvimento de técnicas de identificação dessas substâncias para uso na Educação Básica que esse artigo irá focar: nos Indicadores ácido-base.
Muitas escolas não dispõem de recursos para uso do professor, impossibilitando a contextualização das teorias abordadas em sala de aula. Esse artigo tem como objetivo principal desenvolver um material de consulta sobre Indicadores ácido-base feitos a partir de materiais do cotidiano, que possam ser usados pelo professor de Química no conteúdo de Ácidos e Bases para realizar a identificação destes, seja pela simples mudança física que acontece ao adicionarmos indicadores a essas substâncias, ou para ser usado em processos como titulação ácido-base, por exemplo.
Há muito tempo o Ensino de Química tem sido bastante discutido e debatido por muitos pesquisadores em educação. Isso se deu porque, apesar deste componente curricular ser de extrema importância para formação do cidadão crítico, sua aprendizagem para muitos dos estudantes é difícil e incompreensível, afirma Carvalho, Batista e Ribeiro (2007), desse modo, é papel dos docentes buscarem novas metodologias para torná-la mais atrativa, vinculada com a realidade social dos educandos, tornando os conceitos explanados mais compreensíveis.
Estas novas metodologias devem estimular e despertar a curiosidade dos educandos para que eles possam se sentirem motivados na busca e construção do conhecimento. No entanto, observa-se que muitos professores apresentam certa dificuldade em aceitar as inovações e mudanças que o ensino necessita, e muitos estão enraizados à tendência pedagógica unicamente tradicionalista que ainda hoje é dominante nas escolas brasileiras.
O ensino de química possui um papel importante para formar o cidadão, sendo preciso mostrar a relevância de buscar mais metodologias que promovam o conhecimento sobre essa disciplina e sua ampla visão em relação a sociedade, com o intuito de despertar o interesse dos estudantes conduzindo-os a participarem de várias situações que envolva a química e sua vida, fazendo com que tomem atitudes sobre questões ambientais e tecnológicas (Quadros, Pena, Freitas & Carmo 2016).
Para tornar esse componente curricular mais atrativa e contextualizada defende-se que a aprendizagem de Química permita que os alunos compreendam a química e suas transformações que ocorrem no mundo a nossa volta de forma abrangente e integrada, para que possam ser julgados de acordo com os fundamentos teórico-práticos (Nunes & Adorni, 2010). Entretanto, nem sempre o docente está preparado para ministrar aulas de forma interdisciplinar e relacionar o conteúdo abordado em sala com a realidade dos alunos.
Conforme aponta Maldaner (2003, p. 105), a utilização da experimentação tem por objetivo
[...] aproximar os objetos concretos das descrições teóricas criadas, produzindo idealizações e, com isso, originando sempre mais conhecimento sobre esses objetos e, dialeticamente, produzindo melhor matéria prima, melhores meios de produção teórica, novas relações produtivas e novos contextos sociais e legais da atividade produtiva intelectual.” (p.105).
No entanto, alguns fatores colaboram para a carência de aulas práticas realizadas, como a falta do Laboratório de Ciência nas escolas, no qual Ribeiro (2013) aponta que somente 11% das instituições de ensino, pública ou privadas, possuem. A metodologia de utilizar matérias alternativos para realização de aulas práticas experimentais auxilia de forma expressiva na explicação teórica dos conceitos, potencializando a aprendizagem do aluno, tornando-a significativa (Delizoicov, Angotti & Pernambuco, 2002).
O nosso cotidiano está repleto de substâncias que apresentam sabor azedo, como suco de limão e vinagre, como também substâncias que apresentam sabor adstringente, a exemplo podemos citar o caju e a banana verdes. Peruzzo e Canto (2006) afirmam que esses dois sabores, azedo e adstringente, caracterizam dois grupos de substâncias, os ácidos e as bases, respectivamente.
Com o tempo logo se percebeu que classificar substâncias ácidas e básicas através do paladar era um procedimento um tanto perigoso. Foi a partir daí que químicos do passado perceberam que as substâncias ácidas, ou azedas, quando misturados ao suco de uva ou amora, deixavam essas substâncias avermelhadas. Por sua vez, as substâncias adstringentes, ou seja, básicas, deixavam os mesmos sucos com coloração azulada (Peruzzo & Canto, 2006).
Feito tais testes, Peruzzo e Canto (2006, p. 202) apontam o surgimento das definições operacionais de ácidos e bases:
Ácidos são substâncias que avermelham o suco de uva ou de amora.
Bases são substâncias que azulam o suco de uva ou de amora.
Por serem definições operacionais, são fundamentadas em observações experimentais, o que não envolve explicações dos processos que ocorrem a nível microscópico. Posteriormente surgiram novas definições para ácidos e bases, que abrangiam mais substâncias e fornecem explicações detalhadas do fenômeno, como a definição de Arrhenius (1884), de Brønsted-Lowry (1923) e de Lewis (1923). Como a este artigo tem por objetivo apresentar indicadores de pH para uso experimental, essas outras teorias não serão discutidas.
Os sucos citados anteriormente, uva e amora, são exemplo de indicadores ácido-base. Peruzzo e Canto (2006, p. 202) definem indicador ácido-base como sendo “uma substância que apresenta uma determinada coloração em meio ácido e outra em meio básico”. Na Figura 1 pode-se observar um exemplo de indicador ácido-base natural.
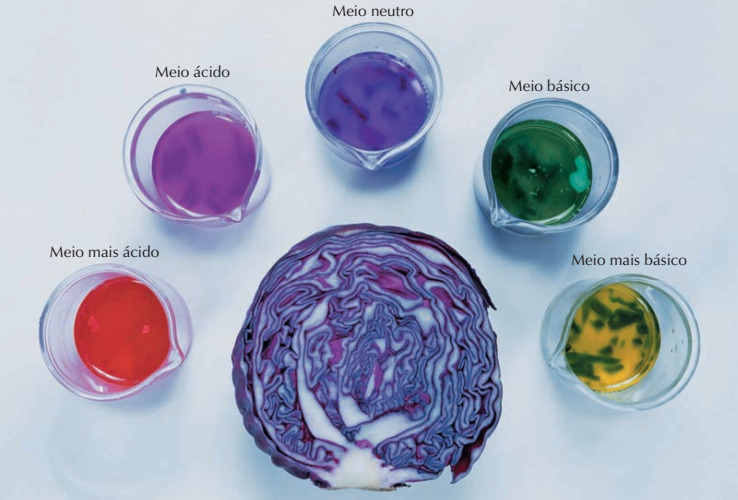
O indicador ácido-base da Figura 1 foi obtido do extrato do repolho-roxo, submetendo suas folhas picadas à água fervente e depois testado em diferentes concentrações de ácidos e bases. Pode-se observar que em meio ácido torna-se vermelho/róseo e em meio básico verde-amarelo.
Para a extração e preparação dos indicadores ácido-base buscaram-se diferentes tipos de flores, frutas, legumes e hortaliças que possam ser encontrados no cotidiano do professor e também do aluno. As espécies escolhidas foram: uva roxa, açaí, azeitona preta, repolho roxo, feijão preto, flor jasmim-manga, flor minilacre, flor hibisco, cebola roxa e berinjela. Adotou-se a extração alcóolica tendo em vista sua maior eficácia, utilizando álcool etílico 46,3° INPM, encontrado em mercantis e farmácia. A preparação dos extratos ocorreu conforme descrito na Tabela 2.
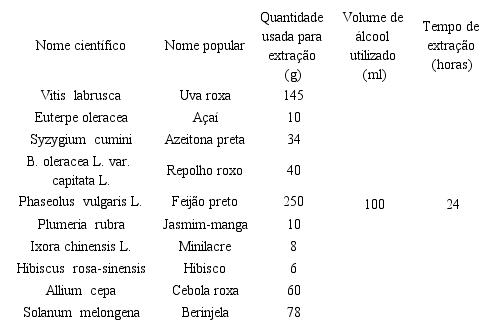
Após o processo descrito acima, realizou-se a filtração dos extratos utilizando-se funil e papel de filtro usado para coar café (ver Figura 2), armazenando-os em frascos de vidro. Em seguida prepararam-se algumas soluções para atestar a propriedade indicadora. Foram escolhidas algumas substâncias encontradas no dia-a-dia, tais como: ácido muriático comercial, soda cáustica comercial (base), vinagre (ácido) e sabão em barra (base).

Após o processo de filtração separaram-se quatro tubos de ensaio contendo as quatro soluções preparadas. Em cada tubo adicionou-se 2 ml de solução, em seguida acrescentou-se 1 ml do extrato. Repetiu-se o processo para os dez extratos.
Os extratos apresentaram bons resultados, sendo atestada a características de indicador ácido-base. Em caráter ácido a solução atingiu cores nos tons de vermelho, já em caráter básico, apresentaram-se cores nas tonalidades do verde ou amarelo. Testaram-se os dez extratos em cada solução (ácido muriático, soda cáustica, sabão e vinagre) e ambos apresentaram resultados bem semelhantes, embora alguns tenham ficado com colorações mais intensas ou mais suaves. A minilacre (Ixora chinensis L.), por exemplo, apresentou uma coloração bem suave, já o feijão preto (Phaseolus vulgaris L.) apresentou uma coloração bem acentuada. Observou-se também uma boa distinção entre o ácido muriático (ácido forte) e a soda cáustica (base forte). Na Figura 3 é possível observar as soluções com os indicadores e a coloração formada. Cada quarteto de tubos de ensaio contém as seguintes soluções, na ordem da esquerda para a direita: ácido muriático, vinagre, soda cáustica e sabão.

Observa-se também que apesar dos indicadores identificarem as substâncias ácidas e básicas apenas de forma qualitativa, é possível inferir através dos resultados apresentados quando uma substância é mais forte ou mais fraca. Nota-se um padrão, no qual os indicadores tendem a apresentar coloração vermelha para o ácido muriático (ácido forte) e uma coloração rósea para o vinagre (ácido fraco).
Este artigo possui como objetivo criar um material de consulta sobre indicadores ácido-base para que outros professores possam usar para contextualizarem suas aulas. Os extratos preparados a partir das espécies estudadas revelam-se promissores à utilização como recurso didático para auxiliar o professor em suas aulas, pois os indicadores naturais se mostraram eficazes na identificação de ácidos e bases, além de serem de fácil obtenção. Observou-se uma semelhança entre os indicadores: ácido apresenta coloração vermelho ou rosa e base coloração amarela ou verde, e também uma boa distinção entre os dois. É importante lembrar que os indicadores aqui apresentados possuem limitações, como determinar o pH de uma substância com exatidão. Eles podem ser usados com a finalidade de identificar tais substâncias de forma qualitativa e não quantitativamente.
Eduardo da Silva Firmino – 40%
Virna Pereira de Araújo – 30%
Caroline de Goes Sampaio – 10%
Ana Karine Portela Vasconcelos – 10%
Maria Cleide da Silva Barroso – 10%




