RESUMO
Introdução: Os avanços biotecnológicos em associação com a pressão para substituir a experimentação animal impulsionam o desenvolvimento de modelos in vitro mais fisiológicos e preditivos da resposta in vivo .
Objetivo: Discutir vantagens e limitações de modelos tridimensionais (3D) de cultura de células.
Método: Revisão da literatura na base PubMed utilizando os termos “ 3D culture ”, spheroid , organoid , “ organotypic culture ”, “ alternative model ”, microfluidic , organ-on-a-chip e biotechnology , individualmente e em diferentes combinações. A pesquisa abrangeu o período de 1971 a 2017.
Resultados: Ensaios tradicionais de cultura em monocamada, embora sejam amplamente utilizados, não reproduzem as interações célula-célula e célula-matriz extracelular, que criam gradientes físicos e químicos e controlam funções celulares, como sobrevivência, proliferação, diferenciação, migração e expressão de genes e proteínas. Modelos 3D de cultura de células são capazes de mimetizar um microambiente mais fisiológico. O número de publicações no período estudado reflete o crescente interesse científico no tema.
Conclusões: Embora os modelos 3D tenham inequivocamente contribuído para as áreas de bioengenharia, morfogênese, oncologia e toxicologia, muitos desafios permanecem. O custo elevado de alguns destes modelos, reproduzir as características mecânicas, espaciais e temporais dos tecidos, assim como a necessidade de desenvolver protocolos padronizados devem ser considerados.
Palavras chave: Cultura 3D, Modelo Alternativo, Esferoide Multicelular, Cultura Organotípica, Organoide.
ABSTRACT
Introduction: Biotechnological advances in association with the pressure to substitute animal experimentation impelled the development of in vitro models that are more physiological and predictive of in vivo response.
Objective: To discuss advantages and limitations of three-dimensional (3D) cell culture models.
Method: Review of the scientific literature at PubMed using the keywords “3D culture”, spheroid, organoid, “organotypic culture”, “alternative model”, microfluidic, organ-on-a-chip and biotechnology, individually and in different combinations. The search period was from 1971 to 2017.
Results: Traditional monolayer cell culture assays, although extensively used, do not reproduce the cell-cell and cell-extracellular matrix interactions that create physical and chemical gradients and that control cell functions, such as survival, proliferation, differentiation, migration, and protein and gene expression. 3D cell culture models are able to mimic more physiological microenvironment. The number of manuscripts published in this period reflects the scientific interest in the field.
Conclusions: Although 3D models have unequivocally contributed to the bioengineering, morphogenesis, oncology, and toxicology fields, many challenges remain. The high cost of some of these models, to reproduce the mechanical spatiotemporal features of the tissues, as wells as the lack of standard protocols should be taken into account. Here we discuss the advantages and limitations of some 3D cell culture models.
Keywords: 3D Culture, Alternative Model, Multicellular Spheroid, Organotypic Culture, Organoid.
ARTIGO
Modelos tridimensionais de cultura de células: aproximando o in vitro do in vivo
Three-dimensional cell culture: nearing the gap between in vitro and in vivo models
INCQS-FIOCRUZ
Recepção: 30 Setembro 2017
Aprovação: 23 Janeiro 2018
Desde a última década do século XX até hoje, o avanço tecnológico na área da biologia e da saúde foi imenso. Foram criadas ferramentas e metodologias que possibilitam a manipulação de moléculas de DNA e RNA e o desenvolvimento in vitro de tecidos e órgãos com características semelhantes às observadas in vivo . A capacidade de sequenciar o genoma de maneira rápida e eficiente foi grandemente ampliada desde 1995, ano da primeira publicação científica no tema, até 2001, quando os primeiros resultados do projeto genoma humano foram publicados1 , 2. Concomitantemente, o conhecimento adquirido nas últimas décadas sobre células-tronco derivadas da camada interna de blastocistos (células-tronco embrionárias), de tecidos adultos e as de pluripotência induzida (iPSC - induced Pluripotent Stem Cell ) tem trazido um avanço considerável na área da Medicina Regenerativa, que inclui a terapia celular e a bioengenharia3 , 4 , 5 , 6 , 7 , 8, com 6.205 ensaios clínicos utilizando células-tronco registrados até o momento (Fonte: https://clinicaltrials.gov). Ou seja, a área de Biotecnologia, definida como “qualquer aplicação tecnológica que utilize sistemas biológicos, organismos vivos, ou seus derivados, para fabricar ou modificar produtos ou processos para utilização específica”, pelo art. 2º do texto aprovado na Convenção sobre Diversidade Biológica, assinada durante a Conferência das Nações Unidas sobre Meio Ambiente e Desenvolvimento (Rio de Janeiro, 5 a 14 de junho de 1992) e aprovado pelo Decreto Legislativo nº 2 de 1994, tem se expandido continuamente. Sem dúvida, a biotecnologia abre enormes possibilidades, como criação de organismos sintéticos9 , 10 e mudança na forma de lidar com patologias causadas por mutações genéticas11 , 12. No entanto, é inquestionável que seu provável avanço nos próximos anos cria desafios éticos e regulatórios, que já vem sendo debatidos em países desenvolvidos11 , 13 , 14.
No Brasil, o debate avança de forma mais lenta para a aprovação de terapias celulares e comercialização de tecidos engenheirados a partir de células humanas. A polêmica da comercialização recai sobre § 4º do art. 199 da Constituição Federal que, apesar de aprovar a “remoção de órgãos, tecidos e substâncias humanas” incluindo a “coleta, processamento e transfusão de sangue e seus derivados”, restringe essas práticas a “fins de transplante, pesquisa e tratamento” vetando “todo tipo de comercialização”15. A legislação brasileira vigente ainda possui dispositivos como a Lei nº 9.434, de 4 de fevereiro de1997 e a Lei nº 11.105, de 24 de março de 2005 (Lei de Biossegurança), que dispõem, respectivamente, sobre a disposição gratuita de órgãos, tecidos ou partes do organismo e sobre a normativa de segurança e fiscalização das atividades que envolvam organismos geneticamente modificados (OGMs)16 , 17. A Agência Nacional de Vigilância Sanitária (Anvisa) vem avançando, de forma discreta, no desenvolvimento de diretrizes mais significativas na área. É o caso da Resolução da Diretoria Colegiada (RDC) no 9, de 14 de março de 2011 que: “Dispõe sobre o funcionamento dos Centros de Tecnologia Celular para fins de pesquisa clínica e terapia”18. Esta questão, por requerer um fórum específico, embora urgente e necessária, não será abordada mais amplamente neste espaço.
Novos produtos biotecnológicos na área da saúde requerem plataformas ou modelos que permitam avaliar sua eficácia e segurança antes de sua aplicação em testes clínicos. Em geral, os testes pré-clínicos envolvem modelos in vitro com cultura de células em monocamada, na sua maioria de linhagens celulares imortalizadas e comercialmente disponíveis, e modelos in vivo . Os testes in vivo , que utilizam animais de laboratório, são frequentemente inadequados em função de diferenças espécie-específicas. Além disso, como consequência da preocupação quanto à utilização de animais como modelo experimental, a política de substituição, redução e refinamento, denominada de política dos 3Rs ( Replacement, Reduction and Refinement ), foi introduzida na década de 1950. No Reino Unido, o National Centre for the Replacement, Refinement and Reduction of Animals in Research (NC3Rs – www.nc3rs.org.uk) foi criado tendo como missão encontrar soluções inovadoras para atingir os objetivos da política dos 3Rs, o que também impulsionou o desenvolvimento de métodos alternativos ao uso de animais19 , 20. O próprio avanço biotecnológico é propulsor do desenvolvimento de modelos alternativos reprodutíveis, mais próximos da biologia humana e, consequentemente, com maior poder preditivo.
Objetivou-se apresentar diversos tipos de modelos de cultivo tridimensional numa perspectiva histórica e discutir criticamente vantagens e limitações destes quanto ao seu poder preditivo e reprodutibilidade para implantação como alternativa ao uso de animais de experimentação. Em função da vasta literatura, não se pretendeu esgotar o assunto e, assim, informação complementar foi indicada.
Aqui apresentamos uma revisão narrativa da literatura sobre modelos de cultura tridimensional, sem esgotar o tema, dada a vastidão de artigos no assunto, o que reflete o grande interesse científico atual na área. O levantamento da literatura foi realizado através de consulta a base de dados PubMed (https://www.ncbi.nlm.nih.gov/pubmed), utilizando as expressões: “ 3D culture ”, spheroid , organoid , “ organotypic culture ”, “ alternative model ”, microfluidic , organ-on-a-chip e biotechnology , individualmente e em diferentes combinações, tais como: (a) “ 3D culture ” OR spheroid ; (b) “ 3D culture ” AND “ alternative model ” e (c) “ 3D culture ” AND biotechnology . A pesquisa abrangeu o período de 1971 a 2017 e os artigos foram selecionados por sua importância histórica e científica, levando-se em consideração, ainda, sua disponibilidade no portal Capes (www.periodicos.capes.gov.br) ou livre acesso. Dado o número de publicações no assunto (total de 5.497 no período determinado, utilizando apenas as palavras-chave spheroid ou “ 3D culture ”), foram selecionados artigos de revisão como fonte de consulta complementar. Informações complementares sobre biotecnologia foram obtidas na página do governo brasileiro com acervo de leis federais e a Constituição de 1988 (http://www4.planalto.gov.br/legislacao). Além disto, a página do NC3Rs (www.nc3rs.org.uk) foi consultada sobre a política de redução, substituição e refinamento do uso de animais em experimentação.
Culturas de células animais foram introduzidas no início do século XX como método de estudo e, após o isolamento da primeira linhagem de células tumorais humanas, as células HeLa, na década de 1950, foram crescentemente utilizadas21 , 22. Embora esta técnica tenha permitido inegáveis avanços na área de biologia celular e ainda seja amplamente utilizada, a partir do final do século XX e início do XXI, as limitações do modelo, em especial no que diz respeito a testes de novos fármacos, se tornaram evidentes. Numa cultura tradicional, em geral denominada de cultura bidimensional (2D), as células tendem a formar uma monocamada aderida a uma superfície de poliestireno modificado para favorecer a adesão, o que é obviamente um substrato não encontrado in vivo e que induz uma polarização artificial das células, não observada quando estas estão nos tecidos. In vivo , as células interagem entre si através de moléculas de adesão, principalmente da família das caderinas, e de complexos juncionais (desmossomos, junção íntima ou oclusiva e junção de adesão) que se ligam, na sua porção citoplasmática, a proteínas do citoesqueleto, através de moléculas adaptadoras23 , 24 , 25 , 26. Além disso, dependendo do tipo, as células se encontram: (a) imersas numa matriz extracelular de composição variada, que inclui diversos tipos de colágeno, fibras elásticas, diversas glicoproteínas, como fibronectina, laminina e vitronectina, além de proteoglicanos e glicosaminoglicanos ou (b) apoiadas numa lâmina basal formada predominantemente por laminina, além de colágeno IV e proteoglicanos. As células ligam-se à matriz extracelular via moléculas principalmente do tipo integrina, que também interagem, através de moléculas adaptadoras, ao citoesqueleto27 , 28 , 29. Estas interações célula-célula e célula-matriz extracelular criam forças mecânicas que organizam espacialmente tanto a matriz extracelular quanto os componentes celulares (citoesqueleto e organelas), modulando diversas propriedades celulares, como forma, diferenciação e migração26 , 30 , 31 , 32 , 33 , 34 , 35 , 36. Associadas a gradientes químicos gerados por difusão de fluídos, O2 e metabólitos celulares37 , 38 , 39 , 40, e pela associação de fatores de crescimento e quimiocinas a moléculas da matriz extracelular27 , 41 estas interações formam microambientes específicos, ou nichos, que regulam a homeostasia dos tecidos42 , 43 , 44 , 45. Tanto as interações celulares complexas quanto os gradientes físicos e químicos observados nos tecidos não são reproduzidos nas culturas em monocamada sobre plástico33 , 40 , 46 , 47 , 48 , 49 , 50 , 51 , 52 , 53 , 54. Além disso, possivelmente como resultado de sua adaptação às condições de cultura em monocamada, as células modificam o padrão de expressão gênica49 , 51 , 54 , 55 , 56. Portanto, não é surpreendente que, dependendo dos objetivos do estudo, os resultados observados com estes modelos in vitro muito frequentemente não sejam reproduzidos in vivo . De fato, os resultados instigantes do grupo da Dra. Mina Bissell57 , 58, obtidos a partir de cultivo de células em sistema tridimensional (3D), mudaram o panorama na área de oncologia, merecendo um editorial na revista Nature intitulado “ Goodbye flat biology? ”59 e o lançamento, pelo Instituto Nacional do Câncer nos Estados Unidos (NIC – National Cancer Institute ), de um programa de pesquisa, iniciado em outubro de 2003, com orçamento anual de US$ 400 milhões para modelos de cultura 3D60. Isto impulsionou o desenvolvimento de sistemas in vitro que buscam mimetizar a fisiologia e a histologia de órgãos e tecidos humanos, o que é refletido pelo aumento no número de publicações científicas sobre o assunto desde então51. Um levantamento no portal PubMed, utilizando os termos “ 3D culture ” OR spheroid resultou em 5.497 artigos publicados no período de 1971 a 2017. A análise ao longo do tempo indicou um grande aumento no número de artigos publicados a partir do início do século XX. De 1971 até 2000, a média foi de 37 artigos ao ano, passando para 261 artigos ao ano a partir de 2001. Somente em 2017 foram publicados 936 artigos, o que comprova o interesse no assunto e o impacto dos resultados obtidos com modelos in vitro tridimensionais.
Diversos sistemas de cultura, que propõem uma abordagem onde uma organização mais fisiológica, complexa e tridimensional das células ocorra, têm sido desenvolvidos, desde os primeiros relatos em 1971. Técnicas, denominadas de cultura 3D, culturas organotípicas ou culturas de organoides, incluem sistemas onde as células são cultivadas em moldes tridimensionais de composição variável, modelos em que células ou fragmentos de órgãos são mecanicamente sustentados ( Figura 1 ) e modelos de agregados em suspensão, denominados esferoides por seu aspecto arredondado ( Figura 2 ). Mais recentemente, sistemas microfabricados de cultura microfluídica ( microfluidics culture ) e os denominados de órgãos sobre chip ( organ-on-a-chip ) foram introduzidos.

Figura 1
Modelos de cultura de células e culturas organotípicas. (A) Modelo de cultura sobre biopolímero. As células são distribuídas em frascos de cultura cuja superfície foi recoberta com moléculas de matriz extracelular, como colágeno I e matrigel. (B) Modelo de cultura em molde de biopolímero natural ou sintético. As células são encapsuladas em gel de biopolímero, o que permite sua organização tridimensional mais fisiológica (C-D). Linhagens humanas de tumor de mama basal MDA-MB-231 (C) e luminal T-47D (D) foram encapsuladas em matrigel (cultivo 3D), formando, respectivamente, estruturas semelhantes a dutos ramificados (C) ou ácinos (D). Contraste de fase. Barras = 100 µm (C) e 50 µm (D). (E-F) Cultura sobre suporte mecânico. Órgãos ou fragmentos de órgãos (E) e células (F) são cultivados em inserto na interface líquido-ar.
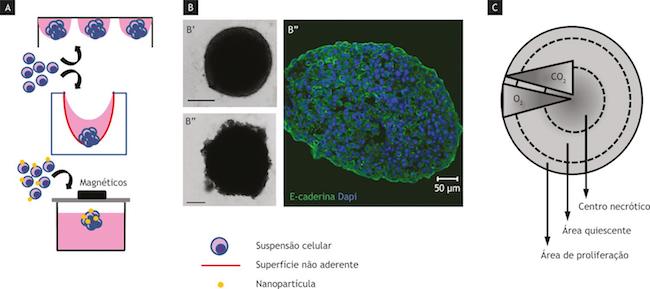
Figura 2
Modelo de cultura 3D do tipo esferoide multicelular. (A) Suspensão celular cultivada utilizando a técnica de gota pendente (acima), em frasco de cultura com superfície modificada para impedir a adesão (meio) e utilizando a técnica de levitação magnética, na qual as células são incubadas com nanopartícula e expostas a campo magnético. (B) Morfologia dos esferoides de fibroblasto humano (B’) e de linhagens humanas de tumor de mama luminal, MCF-7 (B’’) e basal MDA-MB-231 (B’’’). Notar a superfície irregular do esferoide de MDA-MB-231 quando comparado ao do de fibroblasto e a expressão da molécula de adesão E-caderina (em verde) nas células de MCF-7. Núcleos corados com DAPI (em azul). Contraste de fase (B’ e B’’’) e microscopia confocal (B’’). Barras = 50µm. (C) Esquema de esferoide mostrando gradiente de O2 e CO2 do centro para a periferia e as regiões de proliferação, quiescência e morte celular que podem ser observadas estão indicadas.
Os modelos que utilizam moldes procuram criar um ambiente que mimetize a matriz extracelular e, consequentemente, regule a organização espacial das células, sua migração, proliferação e diferenciação. Uma grande diversidade de substâncias, como moléculas de matriz extracelular, biopolímeros naturais, polímeros sintéticos ou híbridos, cerâmicas e metais, tem sido utilizada como molde49 , 51 , 53 , 61 , 62 , 63 , 64. Os diversos biomateriais variam na sua rigidez, porosidade e potencial biodegradável e a escolha do material depende tanto do tipo celular, quanto da aplicação do estudo. Fatores de crescimento podem ser incorporados, favorecendo a proliferação e a diferenciação das células cultivadas nestes moldes e tornando-os mais fisiológicos, ou seja, mais similares à matriz extracelular dos tecidos. A variedade de biomateriais e suas aplicações são objetos de revisões específicas49 , 51 , 53 , 63 , 64.
Os sistemas com matriz extracelular ou biopolímeros foram inicialmente propostos com o cultivo de células primárias (obtidas por dissociação de tecidos ex vivo ) ou linhagem estabelecida, em suspensão ou como agregados, sobre substrato de matriz extracelular, o que não constitui propriamente uma cultura 3D (Figura 1A). Ainda assim, verificou-se que este tipo de cultura favoreceu a proliferação e a diferenciação das células, permitindo que estas se associassem de forma mais fisiológica, mimetizando sua organização in vivo . Estes estudos contribuíram para o entendimento do impacto das interações célula-matriz extracelular nas propriedades celulares e como estas eram modificadas dependendo do tipo de substrato49 , 63 , 64 , 65 , 66 , 68.
Na tentativa de reconstituir um ambiente mais fisiológico, as células foram encapsuladas na matriz polimerizada, que forma um gel (Figura 1B). Neste ambiente tridimensional, em contato com moléculas da matriz extracelular, diferentes tipos celulares (tumorais e fibroblastos, entre outras) foram capazes de migrar de forma muito semelhante ao observado in vivo , o que o possibilitou investigar os detalhes da interação célula-matriz durante a migração69 , 70. Além disso, estes modelos permitem que as células se organizem de forma complexa. Por exemplo, células derivadas de glândulas mamárias formam estruturas semelhantes a dutos ramificados ou a ácinos71 , 72 (Figura 1C-D). Ou seja, num ambiente 3D, as células organizam-se espontaneamente formando estruturas histológicas complexas, que se assemelham às observadas nos órgãos dos quais derivam. Por este motivo, estas estruturas foram denominadas de organoides ( oides , do latim, significa semelhante). No entanto, alguns grupos de cientistas restringem o termo organoide a modelos 3D iniciados com células-tronco ou progenitores, que proliferam e se diferenciam, gerando uma progênie que forma estruturas histológicas semelhante à dos órgãos de origem63 , 73 , 74. Organoides de intestino ( mini-guts ) foram descritos em 2009 a partir de células com potencial de célula-tronco, isoladas das criptas do intestino delgado, que foram cultivadas em modelo 3D de matrigel. O sistema permitiu a proliferação e a diferenciação destas células que originaram as demais populações do epitélio intestinal (enterócitos, células caliciformes e células de Paneth) e formaram estruturas semelhantes às criptas e vilosidades intestinais75 , 76. Ou seja, o modelo foi capaz de revelar o potencial de diferenciação das células-alvo, confirmando sua identidade como célula-tronco intestinal. Organoides de cérebro ( mini-brains ) foram desenvolvidos a partir de uma adaptação do modelo de indução de neuroectoderma em corpos embrionários formados por células-tronco embrionárias77. Além de possibilitar a compreensão da morfogênese do tecido nervoso, estes organoides mostraram-se uma ferramenta importante na descrição de mecanismo patológico do vírus Zika e sua possível implicação no desenvolvimento de microcefalia78. Os exemplos acima mostram as potenciais aplicações deste sistema de cultura na compreensão da morfogênese dos tecidos e na modelagem de doenças e, portanto, não é de se estranhar que uma lista crescente de outros modelos, como de fígado, retina, pituitária, pulmão, pode ser encontrada na literatura científica63 , 73 , 74 , 79.
Culturas de órgãos e fragmentos de tecido foram introduzidas em meados do século XX e, como as condições de difusão de nutrientes e trocas gasosas não são ideais se os tecidos ficam imersos em meio líquido, as estratégias de cultura foram orientadas no sentido de favorecer estes processos. Assim, as culturas de órgãos utilizam um suporte que permite que os tecidos fiquem numa interface líquido-ar (Figura 1E). Inicialmente, os suportes foram montados com filtro microporoso aplicado sobre grade de metal, gel de colágeno ou esponja, mas, recentemente, insertos com membrana porosa, disponíveis comercialmente, são os suportes mais utilizados21 , 63 , 80 , 81. Este tipo de cultura mantém as características histológicas dos tecidos e trouxe avanços em várias áreas do conhecimento. Entre os vários tipos de cultura de órgãos, o modelo de cultura de timo fetal (FTOC, fetal thymus organ culture ) foi um dos mais amplamente utilizados, tendo contribuído de forma relevante na compreensão das etapas e mecanismos de diferenciação de linfócitos T80 , 81 , 82 , 83.
Este tipo de modelo com suporte mecânico foi mais recentemente adaptado para cultura de células que tradicionalmente se encontram em contato com o ar in vivo , como queratinócitos e epitélio respiratório (Figura 1F). As células são cultivadas sobre membrana porosa de inserto e expostas à interface líquido-ar. A superfície da membrana pode ser coberta por matriz extracelular e, ainda, este modelo permite cocultura com fibroblastos, que, imersos na matriz de colágeno, mimetizam o estroma subjacente. Queratinócitos derivados da epiderme, quando cultivados em meio líquido, formam uma monocamada, mas, ao serem expostos a uma interface líquido-ar, estratificam e diferenciam-se formando uma camada queratinizada63 , 84. De maneira similar, as células das vias aéreas condutoras cultivadas neste sistema se organizam de forma mais fisiológica, reproduzindo a morfologia do epitélio respiratório, ou seja, um epitélio pseudoestratificado cilíndrico ciliado, onde células caliciformes podem ser observadas85 , 86 , 87 , 88. O potencial destes sistemas de cultura, não só na compreensão de mecanismos de morfogênese e de propriedades biológicas dos epitélios, mas, sobretudo, como modelos alternativos para teste de novos fármacos e de citotoxicidade, é evidente. De fato, modelos de epiderme, como o Episkin (L’Oreal e Shanghai Episkin Biotechnology Ltd.), e de epitélio respiratório, como o EpiAirway™ (MatTek Corporation) e o MucilAir™ (Epithelix) estão comercialmente disponíveis atualmente.
O modelo de cultura 3D do tipo esferoide multicelular foi inicialmente desenvolvido como reagregados celulares para estudo de biologia do desenvolvimento nas décadas de 1940–195089 , 90 , 91. A partir da década de 1970, Sutherland et al.92 impulsionaram as pesquisas na área de oncologia, ao propor o modelo para estudo sistemático da resposta dos tumores à radioterapia e a drogas89 , 90. O modelo de esferoide multicelular baseia-se na capacidade de adesão homotípica célula-célula, quando sua adesão ao plástico dos frascos de cultura é impedida. De forma geral, os métodos (Figura 2A) como a técnica de cultura em gota pendente, o cultivo em superfícies não aderentes89 , 90 , 91 , 93 , 94 e, mais recentemente, o método de levitação magnética (MLM – magnetic levitation method ), no qual as células são cultivadas com nanopartículas e mantidas em cultura com campo magnético95, permitem a formação de agregados celulares arredondados (Figura 2B). O tamanho dos esferoides varia em função do número de células cultivadas e do tipo celular. Além disso, diferenças na capacidade de estabelecer adesões célula-célula influenciam a formação dos esferoides, que podem ser mais frouxos, com uma superfície irregular, ou mais firmes (Figura 2B)33 , 54 , 89 , 90. O modelo permite o cocultivo de diferentes tipos celulares e é interessante que nestes esferoides as células se organizam espontaneamente, depositam matriz extracelular e formam microambientes específicos89 , 90 , 91 , 96 , 97. Em função da difusão da periferia, em contato com o meio de cultura, para o centro do esferoide, um gradiente químico de O2 e de nutrientes e metabólitos celulares se estabelece ao longo do raio do esferoide (Figura 2C). Essa difusão pode ser melhorada com o uso de biorreatores53. Deve ser dito que diversos tipos de biorreatores estão hoje disponíveis, mas nem todos serão igualmente adequados.
A concentração de O2 no centro do esferoide correlaciona-se inversamente com o tamanho do mesmo e, embora variações sejam observadas, em geral os esferoides de diâmetro acima de 500 µm desenvolvem apoptose e necrose das células localizadas na região central em função da hipóxia. Esta zona central é circundada por uma região de células quiescentes e, mais externamente, pode-se formar uma zona de proliferação, presente nos esferoides de células tumorais, mas praticamente ausente naqueles formados por células não transformadas54 , 89 , 90 , 91 , 93 , 94 , 97 , 98 , 99 , 100 , 101 , 102.
A hipóxia central e as diversas regiões formadas tornam o modelo especialmente vantajoso na área de oncologia por se assemelhar a nódulos tumorais não vascularizados54 , 103. Por outro lado, o modelo também pode favorecer o estudo de mecanismos de angiogênese, quando coculturas com células endoteliais são estabelecidas101 , 104 , 105 , 106. Digno de nota, a integração das células endoteliais no modelo de esferoide de cardiomiócitos murinos promoveu sobrevivência das células, sugerindo que houve melhora na difusão das moléculas presentes no meio de cultura105. O modelo vem sendo utilizado, com discernimento e menor frequência em função do possível desenvolvimento de necrose central, na área de bioengenharia tecidual106 , 107 , 108.
A semelhança dos esferoides com nódulos tumorais avascularizados impulsionou sua aplicação em testes com quimioterápicos e novos fármacos. Diversos ensaios mostraram que enquanto células tumorais em monocamada foram sensíveis à ação de diversos quimioterápicos, quando cultivadas em modelo de esferoide mostraram-se resistentes. Por outro lado, algumas drogas mostraram-se eficazes somente quando as células se encontravam em ambiente 3D54 , 103 , 109 , 110. Como resultado dessas diferenças, ensaios de alto desempenho com modelo de esferoide para triagem de fármacos antitumorais ( high-throughput screening assay ) têm sido cada vez mais frequentes54 , 103 , 111 , 112 , 113 , 114 , 115. Concomitantemente, novas ferramentas de análise têm sido desenvolvidas116 , 117 , 118, o que reforça o potencial deste modelo na área de oncologia.
A ausência de vasos sanguíneos na maioria dos modelos 3D tem impacto sobre o transporte de fluidos e pequenas moléculas119 , 120. Com o objetivo de tornar mais fisiológico os modelos 3D de cultura de células, técnicas que possibilitam criar um controle espacial dos fluídos, denominadas de microfluídica ( Microfluidic techniques ), têm sido desenvolvidas. O controle do fluxo de fluídos permite regular os gradientes químicos e, consequentemente, a formação de microambientes específicos. O controle espacial é a base da técnica e os modelos mais sofisticados envolvem equipes multidisciplinares para a criação de canais padronizados de tamanho micrométrico ( micropatterning ) em moldes de biopolímero53 , 119 , 120 , 121.
A microfluídica, aliada à cultura de células 3D, possibilitou o cultivo de órgãos em chips , onde os microcanais preenchidos com meios de cultura interligam cavidades de formatos específicos que mimetizam os órgãos de onde as células são retiradas122. As células são cultivadas nessas cavidades específicas e a interação entre os diferentes tipos celulares, que formam os órgãos sobre o chip , ocorre por meio dos microcanais. Essa comunicação possibilita o estudo toxicológico sistêmico123, pois a microfluídica permite a interligação de câmaras que mimetizam órgãos diferentes, os chamados “ body-on-a-chip ”124 , 125 , 126. Somado a esse sistema sobre chip , forças mecânicas podem ser empregadas ao substrato onde as células são cultivadas de modo a gerar estímulos que mimetizem o observado in vivo, como, por exemplo, a contração cardíaca e o movimento de inspiração e expiração pulmonar127 , 128. Esses estímulos mecânicos modulam o comportamento celular tornando o sistema mais fisiológico129. O potencial destes modelos na área de bioengenharia e de substituição de experimentação animal é inegável.
Não restam dúvidas de que os modelos 3D de cultura de células, por mimetizarem melhor as condições in vivo , trouxeram grandes avanços em diversas áreas do conhecimento, o que inclui influência do microambiente em diversas propriedades celulares (expressão de genes e proteínas, proliferação, morte, migração e diferenciação), morfogênese, modelagem de doenças e ensaios de citotoxicidade para avaliação de novos fármacos46 , 47 , 48 , 49 , 50 , 51 , 53 , 54 , 55 , 63 , 64 , 73. Além disso, esses sistemas abrem a possibilidade de serem realizados estudos personalizados, com o cultivo de células extraídas de tecidos ex vivo (culturas primárias) em sistemas mais fisiológicos. Assim, cada indivíduo teria suas próprias células cultivadas em diferentes modelos e sua resposta celular seria testada frente a drogas a serem estudadas para o desenvolvimento de medicamentos ou terapias específicas para o indivíduo em questão74 , 120 , 130 , 131 , 132 , 133.
A grande maioria destes modelos permite fácil manipulação, teste rápido de hipóteses e análises em tempo real, quando comparados a modelos in vivo . Portanto, estes sistemas são candidatos a métodos alternativos ao uso de animais em experimentação. De fato, em algumas áreas, como na de citotoxicidade de cosméticos, modelos in vitro 3D estão sendo utilizados em substituição ao teste in vivo , erradicado em vários países. No entanto, mesmo nesta área, algumas limitações do modelo devem ser consideradas, como veremos.
A escolha do modelo, que deve levar em conta vários fatores, como o tipo celular e a aplicação do estudo é fundamental na reprodutibilidade dos resultados. Por exemplo, células epiteliais de revestimento podem formar múltiplas camadas ou não, mas encontram-se apoiadas sobre membrana basal e apresentam uma polarização baso-apical. Por outro lado, alguns tipos celulares encontram-se imersos em uma matriz extracelular com características próprias. Exemplificando, osteoblastos estão associados a uma matriz rígida por associação de cristais de hidroxiapatita com moléculas de colágeno I, num processo denominado de mineralização da matriz. Ou seja, o tipo de molde pode ter impacto nos resultados obtidos. Como vimos, os componentes da matriz extracelular incluem uma grande variedade de moléculas, que se associam entre si e ligam fatores de crescimento e citocinas, criando microambientes específicos. As diferenças na composição da matriz alteram sua organização tridimensional, suas propriedades mecânicas e o gradiente químico27 , 29 , 32. Não só, mas a polimerização de alguns componentes da matriz pode criar diferenças estruturais que impactam as propriedades celulares. Por exemplo, diferenças no diâmetro das fibrilas e na porosidade da matriz de colágeno I derivada de rabo de rato ou de derme de bovino tiveram impacto na migração de linhagens celulares tumorais134. O grupo de Tatiana Coelho-Sampaio mostrou que o pH altera o padrão de polimerização da laminina, o que, por sua vez, modifica o comportamento de diversos tipos celulares68 , 135 , 136. A variação na polimerização destes biopolímeros também ocorre em função de diferenças na sua extração, como no caso do matrigel, que é comercialmente disponível, mas que varia de lote para lote na sua propriedade de induzir tubulogênese, o que certamente tem impacto na reprodutibilidade dos resultados54 , 137. Ou seja, ainda é desafiador reproduzir, nas condições de cultura, as propriedades mecânicas, a porosidade, a elasticidade e o gradiente químico da matriz extracelular dos tecidos. Mesmo no caso dos órgãos engenheirados, os modelos de órgãos em chip , mimetizar a proporção de massa e volume ou determinar os vários tipos celulares que serão incluídos são desafios que vão além da microfluídica e da engenharia de arcabouços que mimetizem órgãos138. Ou seja, é necessária a padronização dos modelos, com critérios bem definidos, para reduzir a variação nos resultados. Além disso, o custo deve ser levado em conta, assim como a ausência de métodos controlados de avaliação em larga escala dos efeitos obtidos53 , 54.
A utilização dos modelos 3D de cultura em substituição ao uso de animais em experimentação deve levar em consideração ainda que mesmo os modelos mais complexos representam somente parcialmente as características dos órgãos e tecidos. Ou seja, o microambiente é mais simples do que o observado in vivo e, portanto, diversos mecanismos fisiopatológicos não são reproduzidos. In vivo , diversos sistemas interagem e, portanto, o microambiente é mais complexo, com contribuição de células do sistema linfohematopoiético e nervoso, além do vascular, já abordado. Macrófagos, células dendríticas, apresentadoras de antígeno, e linfócitos, entre outras, compõem o microambiente, mas estão ausentes na grande maioria dos modelos, comprometendo a avaliação de efeitos inflamatórios e de hipersensibilidade47 , 63. Finalmente, os sistemas de cultura desenvolvidos até o momento, além das limitações espaciais, têm limitação temporal, pois são sistemas que mimetizam eventos de curta duração, enquanto in vivo os eventos se sucedem, ou seja, progridem47.
A busca por modelos in vitro alternativos ao uso de animais de laboratório, em consonância com a política dos 3Rs, e que, ao mesmo tempo permitam alcançar resultados reprodutíveis e preditivos dos obtidos em ensaios clínicos, é imperativa. Neste sentido, sistemas de cultura 3D de células, que mimetizam a complexidade dos tecidos, têm sido desenvolvidos. De forma geral, permitem interações célula-célula e entre estas e a matriz extracelular, depositada pelas próprias células ou derivadas de matriz natural ou sintética, o que leva a uma organização morfológica das células e regula suas propriedades biológicas. Além disto, gradientes físicos e químicos podem se formar nestes modelos, o que também contribui para a modulação do comportamento das células. A escolha do modelo deve levar em conta não só o tipo de tecido-alvo, mas também o efeito que se objetiva averiguar, pois as vantagens, assim como as limitações, são próprias de cada modelo. O próprio aspecto inovador dos modelos de cultura 3D acompanha-se de desafios a sua validação como modelo substitutivo aos ensaios clássicos. Um aspecto fundamental, que é a reprodutibilidade dos resultados, depende da harmonização de protocolos, da padronização de métodos de cultivo em diferentes laboratórios, das boas práticas em métodos in vitro , da realização de ensaios multilaboratoriais, da automação dos métodos de análise e de avaliações de vias de efeito adverso, como recomendado por organizações internacionais, como a Organização para Cooperação e Desenvolvimento Econômico (OECD – Organisation for Economic Co-operation and Development ). Apesar desses desafios, os sistemas de cultura 3D são um passo na direção de modelos mais próximos da complexidade dos tecidos e, portanto, são bons candidatos a modelos alternativos ao uso de animais de experimentação.
Os autores agradecem às Dras. Anneliese Fortuna de Azevedo Freire da Costa, PhD, atualmente no Instituto de Traumato-Ortopedia, Rio de Janeiro, RJ, Brasil e Araci Maria da Rocha Rondon, PhD, do Instituto de Bioquímica Médica da Universidade Federal do Rio de Janeiro, RJ, Brasil, pela colaboração na realização de culturas 3D com linhagens humanas de tumor de mama. Os autores agradecem ainda a Profa. Tatiana Lobo Coelho-Sampaio pelas informações a respeito do comportamento biológico de diferentes linhagens celulares cultivadas sobre matriz de laminina.
O trabalho foi financiado pelas agências de governo, Capes, Faperj e CNPq. Os autores declaram não ter conflito de interesses.
* E-mail: idrossi@hucff.ufrj.br

Figura 1
Modelos de cultura de células e culturas organotípicas. (A) Modelo de cultura sobre biopolímero. As células são distribuídas em frascos de cultura cuja superfície foi recoberta com moléculas de matriz extracelular, como colágeno I e matrigel. (B) Modelo de cultura em molde de biopolímero natural ou sintético. As células são encapsuladas em gel de biopolímero, o que permite sua organização tridimensional mais fisiológica (C-D). Linhagens humanas de tumor de mama basal MDA-MB-231 (C) e luminal T-47D (D) foram encapsuladas em matrigel (cultivo 3D), formando, respectivamente, estruturas semelhantes a dutos ramificados (C) ou ácinos (D). Contraste de fase. Barras = 100 µm (C) e 50 µm (D). (E-F) Cultura sobre suporte mecânico. Órgãos ou fragmentos de órgãos (E) e células (F) são cultivados em inserto na interface líquido-ar.

Figura 2
Modelo de cultura 3D do tipo esferoide multicelular. (A) Suspensão celular cultivada utilizando a técnica de gota pendente (acima), em frasco de cultura com superfície modificada para impedir a adesão (meio) e utilizando a técnica de levitação magnética, na qual as células são incubadas com nanopartícula e expostas a campo magnético. (B) Morfologia dos esferoides de fibroblasto humano (B’) e de linhagens humanas de tumor de mama luminal, MCF-7 (B’’) e basal MDA-MB-231 (B’’’). Notar a superfície irregular do esferoide de MDA-MB-231 quando comparado ao do de fibroblasto e a expressão da molécula de adesão E-caderina (em verde) nas células de MCF-7. Núcleos corados com DAPI (em azul). Contraste de fase (B’ e B’’’) e microscopia confocal (B’’). Barras = 50µm. (C) Esquema de esferoide mostrando gradiente de O2 e CO2 do centro para a periferia e as regiões de proliferação, quiescência e morte celular que podem ser observadas estão indicadas.
