RELATO DE EXPERIÊNCIA
Farmacovigilância em tuberculose: experiência-piloto de um Centro de Referência do Rio de Janeiro, Brasil
Pharmacovigilance in tuberculosis: pilot experience of a Reference Center of Rio de Janeiro, Brazil
Farmacovigilância em tuberculose: experiência-piloto de um Centro de Referência do Rio de Janeiro, Brasil
Vigilância Sanitária em Debate, vol. 7, núm. 1, pp. 71-75, 2019
INCQS-FIOCRUZ
Recepção: 28 Janeiro 2018
Aprovação: 13 Fevereiro 2019
RESUMO
Introdução: Farmacovigilância é um conjunto de atividades que tem por objetivo identificar, avaliar, compreender e prevenir possíveis eventos adversos (EA) ao uso de medicamentos através da detecção precoce dos problemas de segurança relacionados a esses produtos.
Objetivo: Descrever a experiência do projeto-piloto de Farmacovigilância em Tuberculose realizado no Centro de Referência Professor Hélio Fraga da Escola Nacional de Saúde Pública (ENSP) da Fundação Oswaldo Cruz (Fiocruz), no período de julho de 2013 a fevereiro de 2014.
Resultados: Foram avaliadas 15 notificações e os principais EA encontrados foram: poliartralgia (dois); neuropatia periférica (um); dor articular (cinco), sendo um desses com insônia; artralgia (dois); alteração da acuidade visual (um); diarreia (três); vômitos, cefaleias, dor articular e náuseas (um). As variáveis analisadas foram: Gravidade, Não graves, Providências adotadas e Medicamentos suspeitos.
Gravidade: 11 eram efeitos clinicamente importantes e, dentre estes, um foi notificado como incapacidade persistente ou significante; Não graves: quatro notificações descritas; Providências adotadas: quatro notificações com interrupção do medicamento suspeito e em quatro houve redução da dose e em sete houve manutenção da dose; Medicamentos suspeitos; o Levofloxacino foi o medicamento mais prescrito aos pacientes e suspeito de causar EA.
Conclusões: Os resultados mostraram que alguns medicamentos utilizados no tratamento da tuberculose resistente são mais propensos de causarem EA. Existe a necessidade de adotar medidas para que os medicamentos sejam objetos de atenção permanente.
Palavras chave: Farmacovigilância+ Eventos Adversos+ Notivisa.
ABSTRACT
Introduction: Pharmacovigilance is a set of activities that aims to identify, evaluate, understand and prevent possible adverse events (AE) in the use of drugs through the early detection of safety related problems.
Objective: To describe the experience of the pilot project of Pharmacovigilance in Tuberculosis carried out at the Professor Hélio Fraga Reference Center – ENSP/ Fiocruz, Brazil from July 2013 to February 2014.
Results: We evaluated 15 reports where the main AE found were: Polyarthralgia (2); Peripheral neuropathy (1); Joint pain (5), one of these with insomnia; arthralgia (2); change in visual acuity (1); diarrhea (3); vomiting, headache, joint pain and nausea (1). The analyzed variables were: Severity, Non-serious, Adopted procedures and Suspicious drugs: Severity = eleven were clinically important and, among them, one was reported as persistent or significant disability. Non-severe = four notifications described. Proceedings adopted = four reports with interruption of the suspected drug; in four the dose was reduced and in seven the dosage was maintained. Suspected medicines = Levofloxacin was the most prescribed drug suspected of causing AE.
Conclusions: The results showed that some drugs used in the treatment of resistant tuberculosis are more likely to cause AE. There is a need to adopt measures where medicines are the object of permanent attention.
Keywords: Pharmacovigilance, Adverse Events, Notivisa.
INTRODUÇÃO
A Agência Nacional de Vigilância Sanitária (Anvisa) define a Farmacovigilância como a ciência e atividades relativas à identificação, avaliação, compreensão e prevenção de efeitos adversos ou quaisquer problemas relacionados ao uso de medicamentos 1.
As reações adversas a medicamentos (RAM) foram definidas, segundo a Organização Mundial da Saúde (OMS), como toda resposta nociva e não intencional a um medicamento, que ocorre em função de doses normalmente utilizadas no homem para profilaxia, diagnóstico ou tratamento de doença ou para modificação da função fisiológica 2.
O Brasil ocupa a 20ª posição na lista de países com maior carga de tuberculose (TB), 69 mil pessoas foram diagnosticadas e 1.077 desenvolveram a forma mais grave da doença, tuberculose multidroga resistente, no ano de 2015 e o coeficiente de incidência de 2014, segundo o Boletim Epidemiológico 2016, é de 34,2 casos por 100 mil habitantes. A expectativa é que, com o aumento da cobertura da Estratégia de Saúde da Família, a realização do Tratamento Diretamente Observado e a melhoria gradativa dos indicadores, as metas internacionais propostas sejam alcançadas em 2035, ano estabelecido pela OMS na Estratégia Global pelo fim da TB 3, 4.
Diante do elevado número de casos de TB ao longo dos anos e do uso de múltiplos fármacos pelos pacientes, no ano de 2013 um projeto-piloto de farmacovigilância em TB idealizado pelo Programa Nacional de Controle da Tuberculose (PNCT) e pela Anvisa tinha como objetivo incentivar a notificação das RAM antituberculose e implementar a farmacovigilância específica em TB no Brasil.
Três Centros de Referência foram eleitos para participarem do projeto-piloto. Estas unidades de saúde estão localizadas em Manaus (Amazonas), Belo Horizonte (Minas Gerais) e Rio de Janeiro (RJ). Entre eles, o Centro de Referência Professor Hélio Fraga (CRPHF), criado em 1984 e localizado em Curicica no Rio de Janeiro, possui como identidade finalística atuar na área de Pneumologia Sanitária, em especial no controle da TB e outras micobacterioses.
O principal objetivo do projeto-piloto foi o de estimular a notificação de reações adversas aos medicamentos antituberculosos e implementar a farmacovigilância específica em TB no Brasil de maneira que esta atividade se torne uma rotina nos serviços de saúde.
MÉTODO
Trata-se de um estudo descritivo, realizado no Centro de Referência Professor Hélio Fraga (CRPHF) da Fundação Oswaldo Cruz (Fiocruz), Rio de Janeiro, Brasil. Por se tratar de uma referência terciária, o CRPHF atende a pacientes com Tuberculose multidroga resistente (TBMDR) e Tuberculose Extensivamente Resistente (TBXDR), além de outras micobacterioses.
Em julho de 2013, foi realizada uma capacitação para o Projeto-piloto de Farmacovigilância em TB no CRPHF em que os profissionais do PNCT, consultores do projeto de Inovação no Controle da Tuberculose (InCo-TB) e técnicos da Anvisa, foram os responsáveis pelo treinamento dos profissionais médicos, enfermeiros, farmacêuticos e técnicos de farmácia 5.
Na ocasião, foram apresentados o Formulário de Notificação de Eventos Adversos (FNEA) de pacientes em uso de medicamentos para TB elaborado de acordo com as variáveis do Sistema de Notificações em Vigilância Sanitária (Notivisa) – sistema informatizado desenvolvido pela Anvisa para receber notificações de incidentes, eventos adversos (EA) e queixas técnicas (QT) – e o Guia de Notificação de Reações Adversas em TB. Foram realizadas também a apresentação do Notivisa e a capacitação para cadastro de usuários e notificação de EA no sistema 6.
O FNEA para pacientes em uso de medicamentos para TB, já impresso, estava disponível nos consultórios de atendimento e era preenchido manualmente pelo profissional médico, no ato da consulta, ao identificar a reação adversa ocorrida no paciente. Posteriormente este formulário devidamente preenchido era entregue no serviço de farmácia para que a reação adversa fosse notificada no Notivisa em tempo oportuno. A coleta das reações adversas (RA) teve início em outubro de 2013 com término em fevereiro de 2014. Quatro profissionais do serviço de farmácia possuíam senha de acesso ao Notivisa, com os seguintes perfis: dois profissionais como técnicos com permissão de envio (a notificação realizada pode ser encaminhada diretamente para o Sistema Nacional de Vigilância Sanitária – SNVS) e dois profissionais como técnicos sem permissão de envio (a notificação é recebida pelo Gestor Notivisa da instituição para aprovação até seu encaminhamento para o SNVS).
No período de outubro a dezembro de 2013 e no ano de 2014, nos meses de janeiro e fevereiro, 512 e 228 pacientes, utilizaram pelo menos um dos seis medicamentos suspeitos de causarem RA, respectivamente.
O protocolo do trabalho foi analisado e aprovado pelo Comitê de Ética em Pesquisa da Escola Nacional de Saúde Pública Sergio Arouca – Fiocruz do Rio de Janeiro no dia 05 de outubro de 2018, sob o parecer n o 2.943.979 e CAAE n o 98760818.7.0000.5240.
RESULTADOS
Nos cinco meses de análise do projeto-piloto realizado, 740 pacientes utilizaram pelo menos um dos seis medicamentos suspeitos de causarem RA.
Ao todo, 15 EA foram notificados durante o projeto, sendo nove no período de outubro a dezembro de 2013 e seis no período de janeiro a fevereiro de 2014.
Destes, nove eram relacionados a pacientes do sexo feminino e seis do sexo masculino com uma variação de idade entre 18 e 64 anos; sete pacientes eram brancos, quatro pardos e quatro pretos. Dos 15 pacientes atendidos que relataram os EA, um era fumante, um era diabético, um tinha hipertireoidismo e um, incontinência urinária.
Os principais EA descritos foram: poliartralgia (dois); neuropatia periférica (um); dor articular (cinco), sendo um desses com insônia; artralgia (dois); alteração da acuidade visual (um); diarreia (três); vômitos, cefaleias, dor articular e náuseas (um).
As notificações de EA foram separadas pelas variáveis: Gravidade, Providências adotadas e Medicamentos suspeitos ( Quadro).
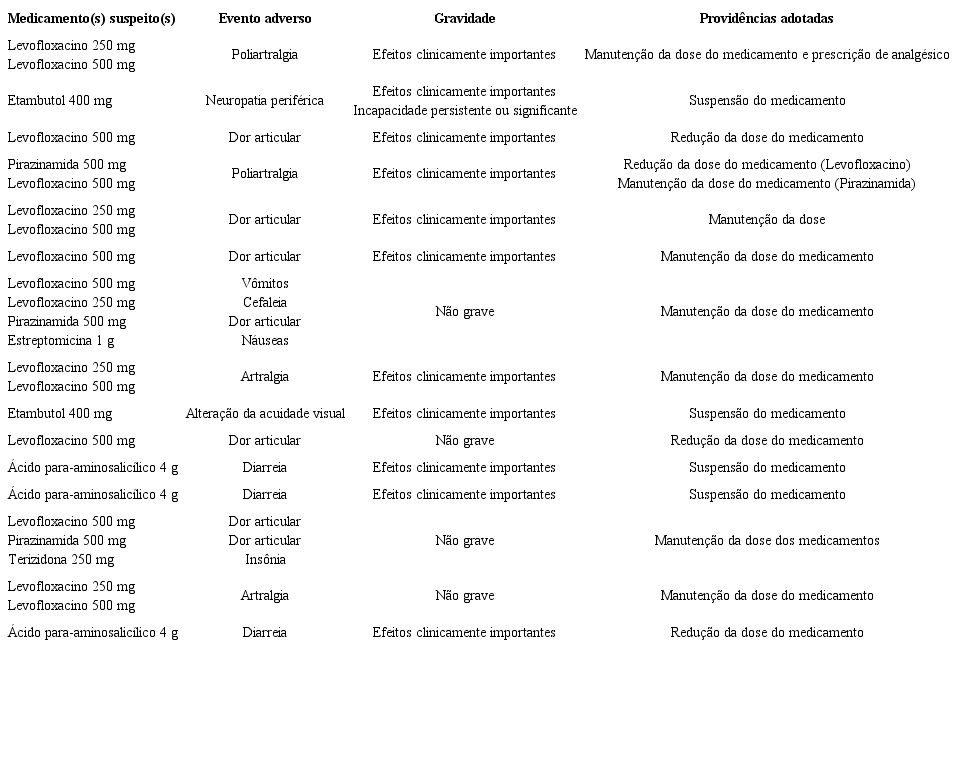
-
Gravidade: 11 eram efeitos clinicamente importantes e, dentre estes, um foi notificado como incapacidade persistente ou significante.
-
Não graves: foram descritas quatro notificações.
-
Providências adotadas: em quatro notificações houve a interrupção do medicamento suspeito; em quatro houve redução da dose e em sete houve manutenção da dose do medicamento (dentre estes um com prescrição de analgésico).
-
Medicamentos suspeitos: dentre os medicamentos antituberculosos e antimicrobianos suspeitos de causar EA, o Levofloxacino foi o mais prescrito.
Os EA foram associados a sete medicamentos regularmente prescritos entre antituberculosos e antimicrobianos. Dentre estes, o Levofloxacino foi o mais prescrito e o EA de maior gravidade foi a diminuição de força muscular e alteração da marcha.
DISCUSSÃO
Apesar de os medicamentos utilizados para o tratamento da TB combaterem o micro-organismo causador da doença de forma eficaz, efeitos colaterais podem ocorrer durante o uso, sejam eles pelo próprio princípio ativo ou pelos seus metabólitos 7. Esses efeitos colaterais podem acontecer durante o tratamento, ao longo das consultas clínicas de acompanhamento, de forma leve e temporária, o que pode levar os pacientes a não considerarem importante o relato destes efeitos aos profissionais que os acompanham 7.
Dos estudos realizados fora do Brasil, temos como exemplo o ocorrido em outubro de 2012, com o apoio da Organização Fundo Global no Marrocos, país situado no norte da África, para a organização de uma estratégia nacional de implementação da Farmacovigilância no Programa Marroquino de Controle da Tuberculose. Neste país, a TB também é um problema de saúde pública com uma incidência de 83,5 casos em 105 mil habitantes, dados do ano de 2011. Os casos de TB resistente representam 1,3% do total 8.
Apesar de ser um estudo para demonstrar um modelo eficiente de Farmacovigilância para tuberculose sensível no Marrocos, o relato torna-se importante quando verificamos o acréscimo do número de notificações de RA e a lista gerada a partir destas notificações após a implementação do modelo. As reações listadas com maior frequência foram as seguintes: aumento das enzimas hepáticas, colestase, icterícia, artralgia, acne, edema de membros inferiores, prurido, erupções cutâneas e vômitos.
O exemplo ocorrido no Marrocos enfatiza a necessidade da parceria com um Programa de Saúde Pública que tenha como escopo a gestão eficiente de medicamentos e as atividades de Farmacovigilância, evitando assim possíveis fatalidades 8.
Em Buenos Aires, um estudo realizado entre 2007 e 2014 no Hospital Parmenio Piñero para TB sensível tinha entre os objetivos, descrever e analisar a frequência dos efeitos adversos dos medicamentos antituberculose 9.
Dos 562 casos de TB relatados, 109 (19%) pacientes apresentaram RA, sendo um total de 242 EA: 39% eram hepáticos e 36% gastrointestinal e em 7% dos casos o tratamento teve que ser suspenso.
Um outro ponto levantado, refere-se à ausência de conteúdo sobre sistemas de vigilância na formação acadêmica, além da escassez de recursos para implementá-los. Apesar de os profissionais conhecerem o sistema de Farmacovigilância (61%), poucos haviam recebido treinamento (8%) e apenas 29% utilizaram a notificação para relatar os EA. Estes foram tidos como obstáculos que dificultaram a geração de informações de qualidade que são importantes na avaliação das políticas de saúde referentes a Farmacovigilância 9.
No presente estudo, embora seja para os esquemas especiais da TB e o número de notificações no período apresentado de cinco meses tenha sido pequeno considerando a média mensal de pacientes atendidos (165), as variáveis analisadas permitiram importantes subsídios para avaliação da Farmacovigilância em TB.
Do somatório dos pacientes tratados com os medicamentos suspeitos citados neste estudo para os esquemas especiais da TB no serviço de farmácia (740), de outubro de 2013 a fevereiro de 2014, 15 pacientes apresentaram EA relacionados às drogas. Com relação à gravidade, 73% tiveram efeitos clinicamente importantes e 27% tiveram efeitos não graves. Já relacionado as providências adotadas, em 27% dos casos houve suspensão dos medicamentos, 27% houve redução da dose e em 46% houve manutenção da dose do medicamento devido aos efeitos colaterais.
Dentre as nove mulheres e seis homens que tiveram EA relacionados aos medicamentos para TB, 46% eram brancos, 27%, pardos e 27% eram pretos.
Dos EA descritos, 33% tiveram dores articulares, 20% tiveram diarreia e 13% tiveram poliartralgia no período analisado.
Este resultado evidencia a necessidade da consolidação desta prática de notificação de EA com o envolvimento da equipe multidisciplinar. Pelo fato do uso simultâneo de múltiplos fármacos durante o tratamento, que tem duração de dezoito a vinte e quatro meses no caso de esquemas especiais e, eventualmente, a ocorrência da necessidade de internações, se faz necessário o controle do uso, monitoramento e vigilância dos EA aos medicamentos para TB.
Um estudo realizado recentemente no Brasil sobre Farmacovigilância como ferramenta de gerenciamento de risco reforça que a vigilância dos fármacos, ao ser realizada, faz com que seja possível a identificação dos riscos associados ao uso dos medicamentos, sendo portanto a Farmacovigilância uma ferramenta de extrema importância para se manejar os riscos associados aos medicamentos e, desta forma, garantir a segurança do paciente 10.
No último dia 10 de dezembro de 2018, com o objetivo de contribuir para a avaliação de segurança dos medicamentos, foi lançado um novo sistema pela Anvisa para notificação de EA relacionados a medicamentos e vacinas, o VigiMed. O VigiMed é uma versão adaptada do sistema utilizado pela OMS e as notificações cadastradas no Brasil serão enviadas para o sistema mundial que é gerenciado por este órgão. Dentre as vantagens do VigiMed, a disponibilização de funcionalidades mais modernas para avaliação das notificações pela Farmacovigilância, a ausência de cadastro prévio e a facilidade de geração de informações para tomada de decisão e divulgação ao público externo são os destaques apresentados 11, 12.
Desta forma, os registros de EA relacionados a vacinas e aos medicamentos deverão ser realizados por este sistema e não mais pelo Notivisa. O Notivisa continuará a ser utilizado para registro e processamento das notificações de incidentes, QT e EA associados ao uso de outros produtos e serviços sob vigilância sanitária. Além do Brasil, outros 120 países adotaram o mesmo procedimento 11.
Sendo assim, para que o monitoramento do uso e das RA aos medicamentos para TB ocorra, é necessário um aprimoramento na gestão da qualidade dos serviços onde os medicamentos sejam objetos de atenção permanente, evitando os erros de prescrição, dispensação e administração e o uso irracional, contribuindo, desta forma, para evitar ou diminuir os EA.
CONCLUSÕES
A Farmacovigilância é um tema amplamente divulgado, mas na realidade ainda precisa se tornar prática em muitos lugares. Através da plataforma on-line para recebimento de notificações, o Notivisa possui uma significativa contribuição como ferramenta para registro de notificações relacionadas a produtos de vigilância sanitária. Somado a isso, em dezembro de 2018 foi lançado um novo sistema pela Anvisa para notificação de EA relacionados a medicamentos e vacinas, o VigiMed, que tem como objetivo contribuir para avaliação de segurança dos medicamentos. Contudo, mesmo com a experiência deste projeto-piloto, percebe-se a necessidade de uma modificação profunda na cultura brasileira, de modo a incentivar os profissionais de saúde a incluir esta prática nas rotinas das instituições em que fazem parte pois, mesmo com o tema relacionado à RA ainda ser frequente, constatou-se que não é suficiente conhecer acerca da eficácia dos medicamentos, mas é de extrema importância elucidar as consequências de seu uso e os efeitos colaterais que podem ocorrer 12.
REFERÊNCIAS
.Brasil. Lei Nº 9.782, de 26 de janeiro de 1999. Define o Sistema Nacional de Vigilância Sanitária, cria a Agência Nacional de Vigilância Sanitária e dá outras providências. Diário Oficial da União. 27 jan 1999.
.Capucho HC. Monitoramento e avaliação farmacoterapêutica: o medicamento fez efeito? Qual? In: Organização Pan-Americana de Saúde – OPAS, Organização Mundial da Saúde – OMS, organizadores. Uso racional de medicamentos: fundamentação em condutas terapêuticas e nos macroprocessos da assistência farmacêutica. Brasília, DF: Organização Pan-Americana de Saúde-Representação Brasil; 2016. p. 1-7.
.World Health Organization – WHO. The safety of medicines in public health programmes. Geneva: World Health Organization; 2006.
.Ministério da Saúde (BR). Brasil livre da tuberculose: plano nacional pelo fim da tuberculose como problema de saúde pública. Brasília, DF: Ministério da Saúde; 2017.
.Rocha JL, Silva CHL, Cyriaco CSS, Cury MEC, Oliveira MG, Gasparotto MS et al. Farmacovigilância em tuberculose: relato de uma experiência no Brasil. Vigil Sanit Debate. 2015;3(2):131-5. https://doi.org/10.3395/2317-269x.00270
.Agência Nacional de Vigilância Sanitária – Anvisa. Notivisa: sistema de notificações em vigilância sanitária. Brasília, DF: Agência Nacional de Vigilância Sanitária; [acesso 12 jul 2017]. Disponível em: http://www.anvisa.gov.br/hotsite/notivisa/apresenta.htm
.Vieira DEO, Gomes M. Efeitos adversos no tratamento da tuberculose: experiência em serviço ambulatorial de um hospital-escola na cidade de São Paulo. J Bras Pneumol. 2008;34(12):1049-55. https://doi.org/10.1590/S1806-37132008001200010
.Tanani DS, Serragui S, Hammi S, Moussa LA, Soulaymani A, Soulaymani R et al. National strategy for the integration of pharmacovigilance in the moroccan TB control program. Pan Afr Med J. 2017;26:48. https://doi.org/10.11604/pamj.2017.26.48.7394
.Chiareli J, Marconi AM, Pistani ML, Waingarten S, Knopoff EG. Sistema de farmacovigilancia: conocimiento y actitudes de los médicos del primer nivel de atención y tasa de notificación de efectos adversos para medicación antituberculosis. Rev Am Med Resp. 2017;17(2):156-61.
.Valeriano TGC, Comarella L. Farmacovigilância como ferramenta de gerenciamento de riscos visando à segurança do paciente. Rev Saude Des. 2015;8(4):60-74.
.Instituto Brasileiro para Segurança do Paciente – IBES. Novo sistema registra eventos adversos de medicamentos e vacinas. São Paulo: IBES; 2018[acesso 22 jan 2019]. Disponível em: https://www.segurancadopaciente.com.br/qualidade-assist/novo-sistema-registra-eventos-adversos-de-medicamentos-e-vacinas/
.Agência Nacional de Vigilância Sanitária – Anvisa. VigiMed. Brasília, DF: Anvisa; [acesso 22 jan 2019]. Disponível em: http://portal.anvisa.gov.br/vigimed
Autor notes
* E-mail: ericafernandesfarma@gmail.com
Declaração de interesses
Os autores informam não haver qualquer potencial conflito de interesse com pares e instituições, políticos ou financeiros deste estudo.
