REVISÃO
Nanomedicamentos: regulamentação e controle de qualidade
Nano drugs: regulation and quality control
Nanomedicamentos: regulamentação e controle de qualidade
Vigilância Sanitária em Debate, vol. 9, núm. 2, pp. 138-151, 2021
INCQS-FIOCRUZ
Recepção: 26 Agosto 2020
Aprovação: 04 Janeiro 2021
Financiamento
Fonte: CAPES
Número do contrato: 001
Financiamento
Fonte: FAPERJ
Número do contrato: 02/2019
RESUMO
Introdução: A utilização dos conhecimentos oriundos da nanotecnologia na indústria farmacêutica tem propiciado a produção de novos medicamentos com características terapêuticas e toxicológicas próprias. Medicamentos de liberação controlada e que atuam diretamente em seus locais de ação, reduzindo seus potenciais efeitos colaterais, têm sido produzidos às custas desta tecnologia. Com tamanhos comparáveis aos de entidades biológicas e propriedades únicas, esta nova classe de medicamentos, os nanomedicamentos, apesenta ainda algumas lacunas que dificultam sua regulação.
Objetivo: Avaliar estas lacunas, seus impactos nas áreas de regulamentação e qualidade e as novas abordagens de regulamentação que estão em estudo.
Método: Foi realizado um levantamento de dados nas bases de dados eletrônicas MEDLINE (PubMed) e SciELO, buscando artigos originais indexados, em português ou em inglês ou espanhol, a partir de 2002 até 2020. Foram utilizados termos de busca relevantes nas três línguas (“nanomedicamento”, “regulação de nanomedicamentos”, “nanocarreadores”, “nanomedicina”, “medicamentos com nanotecnologia”, “qualidade e segurança pelo procedimento” e “vigilância sanitária de nanomedicamentos”).
Resultados: Os trabalhos selecionados descrevem o atual momento da regulamentação e do controle da qualidade desses nanoprodutos, bem como evidenciam os problemas que ainda requerem maior compreensão.
Conclusões: A nanotecnologia aplicada à formulação e à fabricação de medicamentos constitui indubitavelmente um grande avanço para a saúde. No entanto, existem vários pontos que ainda requerem maior desenvolvimento e que impactam os marcos regulatórios para o registro, a eficácia e a segurança desses produtos.
Palavras chave: Medicamentos+ Controle de qualidade+ Nanotecnologia+ Vigilância Sanitária.
ABSTRACT
Introduction: The use of knowledge from nanotechnology in the pharmaceutical industry has led to the production of new drugs with their own therapeutic and toxicological characteristics. Controlled-release drugs that act directly on their action places, reducing their potential side effects, have been produced at the expense of this technology. With sizes comparable to those of biological entities and unique properties, this new class of drugs, the nanodrugs still presents some gaps that hinder its regulation.
Objective: To evaluate these gaps, their impacts in the regulation and quality areas and the new regulation approaches under study.
Method: A data survey was carried out in the electronic databases MEDLINE, PubMed and SCIELO, searching for original indexed articles, in Portuguese or in English, since 2002 until 2020. Relevant search terms in both languages were used (“Nanomedication”, “nanomedicine regulation”, “nanocarriers”, “nanomedicine”, “nanotechnology drugs”, “quality and safety by the procedure” and “nanomedicine health surveillance”).
Results: The selected works describe the current moment of regulation and quality control of these nanoproducts, as well as highlight the problems that still require greater understanding.
Conclusions: Nanotechnology applied to the formulation and manufacture of drugs is undoubtedly a great advance for health. However, there are several points that still require further development and that impact the regulatory frameworks for the registration, effectiveness and safety of these products.
Keywords: Drugs, Quality control, Nanotechnology, Health Surveillance.
INTRODUÇÃO
A indústria farmacêutica tem procurado desenvolver novas formas farmacêuticas capazes de atingir diretamente seus alvos biológicos e aí promoverem a liberação controlada de seus princípios ativos medicamentosos, já que a liberação da dose correta do medicamento no sítio de ação produziria medicamentos mais eficazes, mais seguros e com menos efeitos colaterais1 . Por isso, a indústria vem investindo em tecnologias que favoreçam a otimização de produtos que permitam o transporte de maiores cargas de medicamentos, o aumento do tempo de circulação do fármaco em sua forma íntegra no organismo, o aumento da biodisponibilidade de medicamentos pouco solúveis em água, o direcionamento e a liberação do fármaco no local desejado, a facilidade de permear várias barreiras biológicas, de interagir com os alvos biológicos selecionados e, consequentemente, minimizar os efeitos colaterais e aumentar a eficácia. Ou seja, procura-se aumentar a biodisponibilidade do medicamento ao se alterar sua farmacocinética2 , 3 , 4 , 5 .
Para isto, a tecnologia que tem sido mais amplamente empregada é a utilização de nanopartículas tecnologicamente controladas (ou modificadas) produzidas com o uso da nanotecnologia, ou seja, com a habilidade de medir, desenhar e manipular materiais nos níveis atômico, molecular ou supramolecular com o objetivo de se entender, criar e aplicar sistemas e estruturas com funções específicas próprias de suas dimensões de aproximadamente 1 a 100 nanômetros6 . Produtos farmacêuticos obtidos com o uso desta tecnologia, os nanomedicamentos, apresentam propriedades físicas, químicas e biológicas que diferem do mesmo material em escala habitual7 . No caso da indústria farmacêutica, esta definição é deficiente, pois não aborda questões importantes como as implicações científicas, legais, ambientais, regulatórias e éticas pois se baseia apenas no tamanho da partícula, ignorando a complexidade de suas interações com o meio exterior e especialmente com os organismos vivos7 .
Em geral, os nanomedicamentos se caracterizam pela redução do tamanho das partículas medicamentosas de baixa solubilidade até as dimensões nanométricas e posterior conjugação com carreadores apropriados que exercem papel fundamental para sua eficácia terapêutica. Nos nanomedicamentos, diferentemente dos medicamentos habituais, as propriedades físico-químicas e morfológicas dos carreadores interferem nas características farmacológicas dos nanoprodutos8 , 9 .
Os nanomedicamentos são definidos como formas farmacêuticas que contêm um ou mais fármacos em escala nanométrica ou como insumos farmacêuticos que estão associados a um adjuvante em escala nanométrica2 , 9 , 10 . Estes possuem ação farmacológica específica visando modular funções metabólicas e fisiológicas e podendo ser usados com finalidades profilática, curativa, paliativa ou para fins de diagnóstico10 . Hoje se sabe que mais de 20 propriedades dos nanomateriais são capazes de influenciarem seus efeitos sobre a saúde e seus riscos ambientais11 , 12 , 13 , 14 .
Portanto, o conhecimento abrangente de como os nanomedicamentos se comportam em um sistema biológico exige a participação de várias disciplinas, dentre as quais; a fisiologia, a anatomia, a patologia, a genética, a bioquímica, a físico-química e a nanotoxicologia. De fato, as características genéticas, as epigenéticas e a existência de eventuais patologias no organismo, bem como as propriedades físicas e físico-químicas dos nanomateriais, influenciam as interações com componentes celulares (proteínas, membranas, fosfolipídios, vesículas e organelas) e consequentemente afetam sua farmacocinética e farmacodinâmica4 , 7 , 10 , 15 .
Atualmente, a busca de diretrizes para a regulamentação e a qualidade desta nova classe de medicamentos envolve uma série de lacunas e é um desafio de âmbito mundial, uma vez que as principais agências regulamentadoras internacionais, como a Food and Drug Administration (FDA), dos Estados Unidos da América, e a European Medicines Agency (EMA), não possuem uma regulamentação harmonizada para seus registros e liberação2 , 16 .
Sendo assim, este artigo pretendeu discutir as principais lacunas no conhecimento vigente, bem como algumas diretrizes que estão sendo propostas pelos organismos reguladores dos maiores produtores de nanomedicamentos no mundo.
MÉTODO
Bases de dados consultadas e estratégias de busca
Para este estudo, foram consultadas as bases de dados eletrônicas Medical Literature Analysis and Retrieval System Online (MEDLINE), do PubMed, e Scientific Electronic Library Online (SciELO). Todos os trabalhos científicos originais indexados desde 2002 até 2020, quando se iniciou a discussão do uso da nanotecnologia na área da saúde, foram inicialmente considerados. Foram utilizados de forma individualizada os seguintes termos de busca em todas as bases de dados e suas versões em inglês e espanhol: “nanomedicamento”, “regulação de nanomedicamentos”, “nanocarreadores”, “nanomedicina”, “medicamentos com nanotecnologia”, “qualidade e segurança pelo procedimento” e “vigilância sanitária de nanomedicamentos”.
Critérios de inclusão/exclusão dos artigos
Foram incluídos os trabalhos científicos com foco nas tecnologias aplicadas a medicamentos e aqueles que apontavam as lacunas científicas ainda existentes. Além desses, as legislações cabíveis e os documentos oficiais de agências reguladoras que abordavam diretrizes e definições sobre nanomedicamentos e controle de qualidade que ainda estavam em vigor no período de busca e disponíveis nos seus respectivos portais eletrônicos foram incluídos no material de análise deste trabalho. A única restrição foi em relação ao idioma de divulgação dos trabalhos, sendo incluídos apenas aqueles publicados em português, inglês e espanhol.
Foram desconsiderados trabalhos científicos sem acesso online na íntegra e os trabalhos científicos duplicados. Além disso, foram excluídos aqueles que não abordavam conceitos, os que apresentavam apenas a rota sintética do nanomedicamento, os que abordavam temática diferente do objeto deste estudo e, ainda, os que possuíam dados inconsistentes, como artigos que careciam de qualidade intelectual com redução de conteúdo e com pouca profundidade, quando comparados com o restante da literatura.
Procedimentos da revisão
O levantamento dos dados bibliográficos foi feito por dois autores/pesquisadores, com base nos critérios de inclusão estabelecidos e, em momento posterior, em um confrontamento sobre os achados, houve compatibilidade do material encontrado por ambos os pesquisadores. A primeira etapa de seleção das produções foi realizada mediante a leitura e a análise dos títulos e resumos de todos os artigos identificados. Após essa triagem inicial, procedeu-se à leitura na íntegra dos estudos selecionados, a qual possibilitou a exclusão de outros textos por não abordarem o assunto desta revisão.
RESULTADOS E DISCUSSÃO
O levantamento bibliográfico localizou 1.011 trabalhos científicos publicados. Destes, 546 foram excluídos por estarem presentes em mais de uma base de dados, sendo registrados, assim, de forma duplicada. Ao se aplicar os outros critérios de exclusão acima relacionados nos títulos e resumos, foram excluídos 238, restando apenas 227 trabalhos científicos para serem lidos na íntegra pelos pesquisadores. Após essa segunda avaliação, apenas 108 trabalhos foram selecionados e utilizados como base teórica para a elaboração do presente trabalho. Todos foram incluídos nas referências deste artigo.
A Figura 1 apresenta o fluxograma com as etapas de identificação, seleção e inclusão dos artigos científicos.
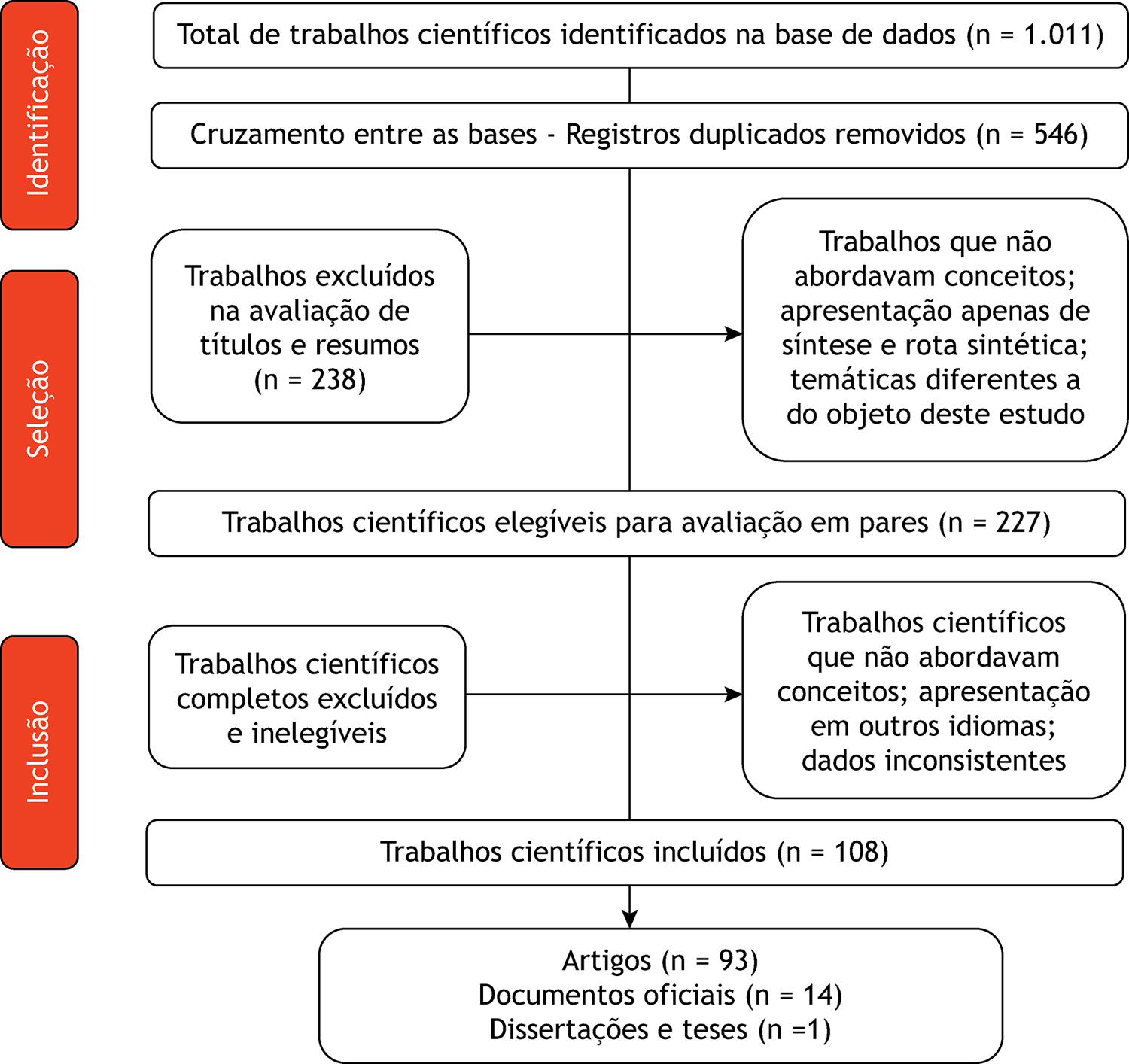
Figura 1
Fluxograma da identificação, seleção e inclusão dos trabalhos científicos revisados.
Fonte: Elaborada pelos autores, 2020.
Nanocarreadores e nanomedicamentos
A maior parte dos nanomedicamentos envolve a utilização de nanocarreadores que podem ser entendidos como nanoestruturas biocompatíveis e inertes, associadas ou envoltas por uma substância farmacologicamente ativa (medicamento), capazes de a transportarem e a direcionar a um alvo específico do organismo, executando sua liberação, geralmente controlada12 .
Dados têm mostrado que várias nanopartículas possuem as qualidades requeridas pela indústria para um bom carreador, ou seja: aumentar a eficácia e a tolerância local e sistêmica (evitar reações por corpo estranho), proteger as células sadias, diminuir a toxicidade e produzir menores efeitos colaterais secundários16 , 17 , 18 , 19 .
Sendo assim, uma grande variedade de nanocarreadores vem sendo utilizada no desenvolvimento de nanomedicamentos que têm sido classificados em nanopartículas derivadas de lipídeos, poliméricas, derivadas do carbono e materiais inorgânicos20 . A diversidade de nanocareadores disponíveis, cada um com propriedades características, exige que sua escolha siga alguns parâmetros, como: o tipo de doença e a população-alvo, o tipo de fármaco a ser utilizado, a rota de administração, as barreiras biológicas a serem ultrapassadas, os sítios-alvo, a cinética de liberação e a dose pretendida. As propriedades características de cada tipo têm sido objeto de várias publicações5 , 8 , 9 , 14 , 16 , 21 , 22 , 23 , 24 , 25 , 26 , 27 .
No entanto, é importante considerar que o contato dessas nanopartículas com o meio biológico pode resultar em modificações significativas de suas características físico-químicas e, consequentemente, de suas propriedades fármaco e toxicológicas. Estas modificações são, em sua maioria, determinadas por processos superficiais tais como adsorção de proteínas, coagulação etc. Outro fator importante relacionado ao uso dos nanocarreadores é o conhecimento das frações incorporadas e liberadas do fármaco nos estudos de bioequivalência. De fato, a farmacologia tradicional sustenta que a droga livre (não ligada) é a forma biologicamente ativa, logo a simples determinação da concentração total do fármaco pode induzir a erros significativos na interpretação dos mecanismos de transporte e nas relações farmacocinéticas/farmacodinâmicas28 , 29 .
Atualmente existem no mercado internacional pouco mais de 60 nanomedicamentos dos quais 13 utilizam lipossomas; 22 nanomateriais poliméricos e 27 nanomateriais inorgânicos. Uma visão geral da atual disponibilidade mercadológica e do uso de nanomedicamentos na clínica médica, bem como sua diversidade, classificação farmacêutica e os benefícios do uso da escala nanométrica, pode ser encontrada em alguns estudos12 , 16 , 30 , 31 , 32 , 33 , 34 .
Devido às características que os diferenciam dos medicamentos tradicionais, os nanomedicamentos apresentam diferentes toxicidades e efeitos colaterais. Acredita-se que estas diferenças ocorram devido aos nanocarreadores, mas ainda são necessários mais estudos para confirmação desta suspeita. Alergias, hipersensibilidade e imunossupressão têm sido atribuídas ao uso de certos nanomedicamentos35 , 36 .
Diante dos benefícios potenciais obtidos com o uso da nanotecnologia, a indústria farmacêutica tem sido incentivada a utilizá-la principalmente para a produção de nanomedicamentos voltados para o tratamento de doenças como: Alzheimer37 , síndrome da imunodeficiência adquirida37 , 38 , 39 , malária40 , 41 , Parkinson42 , tuberculose43 e os cânceres, uma vez que seus tratamentos ainda acarretam muitos efeitos colaterais e a eficácia desejada nem sempre é alcançada44 , 45 , 46 , 47 , 48 , 49 , 50 , 51 , 52 , 53 , 54 , 55 , 56 , 57 . Isto porque os nanomedicamentos possuem um conjunto de parâmetros vantajosos, como a menor dose recomendada e maior dose máxima tolerada (MTD, do inglês maximum tolerated dose ) quando comparadas a medicamentos não nanoformulados. Além disso, os nanomedicamentos podem ser direcionados mais efetivamente para os tecido-alvo por meio dos mecanismos de direcionamento passivo, via efeito de permeabilidade e retenção aumentados (EPR) e/ou ativo, feito através do uso de ligantes específicos capazes de aumentarem a interação entre o nanofármaco e receptores das células dos tecidos-alvo, como os receptores de células cancerosas58 .
Além disso, vários estudos focam na obtenção de maiores eficiências dos antibióticos59 , 60 e antioxidantes61 no tratamento de leishmaniose62 , da dependência química63 , de intoxicação por metais64 , na periodontia65 , na psoríase20 e em úlceras66 .
Regulação de nanomedicamentos
O uso da nanotecnologia na medicina, por ser um campo do conhecimento novo, ainda comporta várias dúvidas que limitam ou dificultam a regulação dos nanomedicamentos. Estas lacunas vão desde a falta de uma definição internacional única para esse tipo de material até o desconhecimento da possibilidade de comprometimento das funções cerebrais resultantes da permeação da barreira hematoencefálica; da acumulação sistêmica das nanoparticulas em determinados órgãos; de seu potencial de genotoxicidade; do efeito da variação da morfologia sobre as propriedades físico-químicas e de suas interações biológicas e eficácia terapêutica; da diferença de comportamento in vitro e in vivo e mesmo entre animais e humanos; da necessidade de desenvolvimento de novos métodos analíticos para monitorização da eficácia e da segurança dos nanomedicamentos; dos impactos ambientais e das diferenças entre as características farmacocinéticas dos nanomedicamentos e daquelas determinadas por normas padronizadas para pequenas moléculas67 , 68 .
A dificuldade que essas lacunas têm trazido para a proposição de normas e guias regulatórios tem permitido que ainda hoje a indústria farmacêutica utilize os estudos toxicológicos dos insumos farmacêuticos ativos (IFA) já registrados e tradicionalmente comercializados para produzir os dados requeridos nos processos de registro dos nanomedicamentos, desconsiderando quaisquer diferenças entre os comportamentos in vivo e in vitro58 .
Por exemplo, desprezam-se estudos farmacocinéticos que mostrem que parâmetros importantes, como o tempo de meia-vida, a área sob a curva de absorção e a depuração das nanoformulações, difiram consideravelmente quando comparados com as formulações tradicionais. Em geral, os nanomedicamentos permanecem por mais tempo no organismo e, consequentemente, permitem a redução do número de doses administradas, mas, em casos de intoxicação ou de efeitos adversos, sua eliminação dos diversos compartimentos biológicos ocorre de forma mais lenta, podendo até ocasionar a morte58 .
Outros exemplos envolvem a diferença nos comportamentos in vivo e in vitro de um mesmo fármaco quando produzido em nanoescala e em escala convencional, a falta de regulamentação para a avaliação de alguns efeitos tóxicos causados pelos nanomedicamentos, como, por exemplo, os efeitos sobre o sistema imune; a inexistência de um método padrão consensual para medir a bioequivalência de uma droga nova em comparação com a droga de referência já existente no mercado, dentre outros. Neste aspecto, enquanto o FDA preconiza o uso do método clássico para determinação dos parâmetros farmacocinéticos (área sob a curva ou concentração máxima no plasma), a agência europeia (EMA) exige informações bem mais detalhadas do estudo de bioequivalência. O mesmo cenário se propaga e magnifica para os medicamentos considerados genéricos e os similares36 , 68 .
Outra lacuna importante é a interação destes nanomedicamentos com o meio ambiente. Dentre as incertezas que precisam ser sanadas para permitir uma avaliação de riscos ambientais resultantes do descarte de nanomedicamentos mais completa podem ser citadas: a inexistência de dados de farmacocinética; a exposição e potenciais riscos ambientais; a existência de dados experimentais contraditórios sobre os efeitos no meio ambiente e nos organismos; as incertezas sobre a relação físico-química e toxicidade; a falta de dados ecotoxicológicos para muitos nanomateriais e as incertezas sobre como avaliar a dose do nanoproduto. Neste particular o US National Research Council criou um sistema próprio para avaliação de risco ambiental69 , 70 .
Em relação aos nanossimilares e aos nanogenéricos, a Comunidade Econômica Europeia, por exemplo, reconhece que testes biológicos devem ser também requisitados no registro dessas formulações, demonstrando a complexidade na regulação de tais produtos. Mesmo assim, tais resultados nem sempre podem ser transferidos de uma espécie para outra71 , 72 .
Como pode ser depreendido, a multiplicidade dos fatores que influenciam o efeito biológico de um nanomedicamento faz com que as exigências regulatórias para esta classe sejam mais complexas, pois alterações podem ser observadas mesmo entre diferentes lotes do mesmo produto. Como grande parte desses nanoprodutos são de liberação controlada e esta propriedade depende das características físico-químicas dos carreadores, estudos detalhados dessas características são requisitos fundamentais para que os órgãos reguladores possam exercer suas atividades regulatórias com total segurança. Este é ainda um campo pouco conhecido e aberto para novas pesquisas73 , 74 .
O FDA, por exemplo, relacionou os fatores que considera importantes para avaliação de um novo nanomedicamento. São eles: caracterização adequada da estrutura do nanomaterial e suas funções; complexidade da nanoestrutura; conhecimento dos mecanismos pelos quais as propriedades físico-químicas do nanomaterial impactam seus efeitos biológicos (por exemplo, efeito do tamanho das partículas nos parâmetros farmacocinéticos); entendimento dos mecanismos de liberação in vivo tendo como base as propriedades físico-químicas do nanomaterial; predição da liberação in vivo baseada nos resultados obtidos in vitro; estabilidade física e química; maturidade da nanotecnologia utilizada na produção e no controle (incluindo os métodos analíticos); impacto potencial de alterações no processo de produção sobre a qualidade do nanofármaco; estado físico-químico do nanoproduto depois da administração; rota de administração; dissolução, biodisponibilidade, distribuição, biodegradação, acumulação e sua predição baseada em estudos físico-químicos e em animais75 .
Estas exigências são várias e constituem ainda hoje um desafio a ser cumprido, pois determinados requisitos, como, por exemplo, a estrutura química de algumas drogas, particularmente das drogas complexas não biológicas (NBCD), não pode ser cumprida. Isto porque as NBCD não possuem estruturas homomoleculares, mas sim uma mistura complexa de estruturas semelhantes que não podem ser isoladas, quantificadas ou descritas através da análise físico-química. Por esta razão, suas qualidades são altamente dependentes de seus processos de produção76 , 77 .
Em vista disto, várias instituições têm optado por produzirem manuais e guias para orientar a indústria farmacêutica no desenvolvimento de nanomedicamentos. Ou seja, procura-se normatizar os processos de produção. Dentre elas temos a European Chemical Agency (ECHA), a Organização para a Cooperação e o Desenvolvimento Econômico (OECD), o International Conference on Harmonization (ICH), a EMA, o Scientific Committee on Emerging and Newly Idetified Risks (SCENIHR) e o FDA22 , 75 , 78 , 79 .
Sob a chancela do programa Registration, Evaluation, Authorization and Restriction of Chemical Substances (REACH), instituído pela Comunidade Econômica Europeia em 2006, e no intuito de suprir estas carências, a União Europeia patrocinou entre 2013 e 2017 um projeto de pesquisa pioneiro denominado NANoREG framework for the safety assessment of nanomaterials , objetivando a elaboração de conteúdo científico para auxiliar os órgãos reguladores na implementação de normas e controle da qualidade de produtos que utilizam a nanotecnologia em seu processo de fabricação80 , 81 . Este projeto é constituído de um estudo colaborativo de mais de 50 instituições de diversos países como: Austrália, Estados Unidos, Japão, Canadá, Brasil, China e Coreia do Sul.
Além de disponibilizar para os legisladores um conjunto de ferramentas para avaliação de riscos e instrumentos de tomada de decisão, incluindo a exposição, o monitoramento e o controle para um grupo de nanomateriais já utilizados, este projeto propõe o desenvolvimento de ensaios que analisem os impactos sobre o ambiente e a saúde humana dos nanomateriais mais utilizados pelas indústrias82 .
Os objetivos centrais deste projeto originaram um compêndio de protocolos norteadores para regulação dos nanomateriais produzido por grupos multidisciplinares e multinacionais. Esses protocolos orientam como se avaliar os riscos e a toxicidade dos nanoprodutos, bem como fornecem os dados científicos obtidos para que os órgãos legisladores e fiscalizadores possam elaborar procedimentos para monitorar e controlar a qualidade dessa nova classe de produtos. O acesso ao material produzido pode ser feito através do sítio eletrônico do projeto83 .
O projeto NaNOREG foi posteriormente continuado com a aprovação do H2020 ( Ensuring the safe and sustainable develpment and application of nanotechnologies ), ProSafe initiative (www.h2020-prosafe.eu) e dos projetos NanoReg2, NanoRoadMap e GoNanoBioMat que se propõem a promoverem estudos multidisciplinares no sentido de melhor entender os impactos dessa tecnologia na saúde humana e do ambiente, a complexidade destas formulações e propor metodologia para regulação, avaliação da qualidade e da similaridade81 , 84 .
Outros grupos, como as agências reguladoras dos Estados Unidos, Japão e mesmo da Comunidade Econômica Europeia, se uniram para a criação de documentos comuns norteadores para toda a comunidade farmacêutica73 . Porém o maior desafio ainda é o estabelecimento de ensaios suficientemente sensíveis e específicos para detectarem baixas concentrações das nanopartículas e diferenciar as formas livres das agregadas, assim como as formas metabolizadas e as não metabolizadas85 , 86 .
De fato, até o presente, as agências reguladoras têm trabalhado de maneira diferenciada, cada uma a seu modo. Um exemplo interessante destas diferenças é descrito por Rocco et al.77 , que compararam os procedimentos adotados pelo FDA e pela EMA no registro de produtos contendo o acetado de glatiramer, uma droga complexa não biológica (NBDC) constituído por uma mistura heterogênea de polipeptídios sintéticos77 . Esta substância foi inicialmente registrada sob o nome de Copaxone e posteriormente com outras denominações (Glatopa, Copemyl e outros). Nos Estados Unidos, o Copaxone foi identificado como produto original e os demais como genéricos e, como tal, para registro, foi exigido testes de equivalência farmacêutica e bioequivalência. No entanto, a demonstração de equivalência farmacêutica é aplicada quando os produtos contêm a mesma substância ativa, o que não é possível demonstrar através de testes físico-químicos ou biológicos para o glatiramer. Na Europa, a EMA adotou um procedimento híbrido, registrando inicialmente como genérico, mas solicitando uma série de estudos comparativos adicionais. Além disto, deixou a critério das autoridades reguladoras nacionais a possibilidade de substituição entre estes produtos77 .
No Brasil, a Agência Nacional de Vigilância Sanitária Brasileira (Anvisa) ainda não elaborou regulamentação específica, apenas instituiu o Comitê Interno de Nanotecnologia (CIN) em 2013 e, em 2014, publicou um documento intitulado: Diagnóstico Institucional de Nanotecnologia da Agência Nacional de Vigilância Sanitária, em que ressalta alguns temas sujeitos a atuação regulatória da agência. A proposta defende ainda a elaboração de um inventário de nanoprodutos existentes no mercado de consumo no Brasil, sendo que cerca de 637 produtos registrados na Anvisa se utilizam das nanotecnologias87 .
No entanto, a atual regulação dos nanomedicamentos ainda não é adequada e exige melhoria contínua, especialmente na área ambiental68 , 88 . Porém, alguns produtos já foram desenvolvidos e estão sendo amplamente comercializados. Diante disso, a International Standard Organization (ISO) publicou recentemente a ISO/TR 22019:2019, intitulada: Nanotechnologies- Considerations for performing toxicokinetic studies with nanomaterials . Este documento descreve os princípios básicos para estudos relevantes em toxicocinética de nanomateriais89 .
Qualidade dos nanomedicamentos
Até o advento dos nanoprodutos, a qualidade de um medicamento era determinada através de alguns ensaios físico-químicos, químicos e/ou biológicos. No entanto, com a influência de outros fatores puramente físicos ou físico-químicos sobre o comportamento farmacocinético/dinâmico, houve a necessidade de se introduzir novos testes laboratoriais, que não eram comuns em um laboratório farmacêutico, o que exigiu o consequente treinamento do pessoal envolvido. A importância desses fatores é tão marcante que atualmente se sabe que o entendimento das relações entre as propriedades físico-químicas, a performance e a segurança de um nanomedicamento são os primeiros passos para o controle da qualidade do produto78 , 79 .
Observa-se que mesmo pequenas alterações das propriedades físico-químicas ou da morfologia das nanopartículas podem ter significativos efeitos sobre a eficácia terapêutica e a segurança biológica do nanoproduto. A variabilidade desses fatores tem impacto sobre a produção dos nanomedicamentos, podendo causar diferenças de comportamento biológico entre lotes do mesmo produto e suas bioequivalências, aspectos importantes particularmente para os produtos nanossimilares e nanogenéricos73 . Como consequência, acredita-se que, devido a esta complexidade de fatores intervenientes na ação farmacológica de um nanofármaco, a substituição de um nanoproduto por seu similar é difícil, senão impossível71 . Por estas razões, produtos teoricamente similares e/ou biossimilares produzidos utilizando-se diferentes tipos de nanocarreadores ou formas de nanoencapsulação que não possuam estudos de equivalência farmacêutica e bioequivalência têm sido registrados como produtos novos31 , 90 , 91 .
Uma discussão interessante sobre equivalência farmacêutica e bioequivalência, que envolve biossimilaridade e genéricos, para medicamentos complexos obtidos por nanotecnologia e por biotecnologia e como as agências reguladoras têm conduzido alguns registros pode ser encontrado em Hussaarts et al.92 .
A influência de múltiplos fatores sobre os efeitos medicamentosos traz consigo a dificuldade de se predizer as interações entre os nanomedicamentos e os sistemas biológicos e dificulta a elaboração de normas, padrões e ferramentas para avaliar os riscos93 .
O impacto destas propriedades sobre o comportamento farmacológico fez com que o uso das farmacopeias nacionais, como código e regulador da qualidade, deixou de atender às peculiaridades desses nanoprodutos31 , 73 . Em muitos casos, ainda hoje os nanomedicamentos estão sendo produzidos e comercializados utilizando as mesmas normas de boas práticas de fabricação aplicáveis aos medicamentos formulados em escala tradicional31 .
Como consequência dessas limitações, novos métodos mais sofisticados e robustos devem ser desenvolvidos e aplicados tanto no controle de matéria prima quanto no produto acabado31 . Assim, os fatores importantes nesse contexto que devem ser considerados no controle do processo de fabricação, da qualidade e da similaridade de nanomedicamentos são mostrados na Figura 2 .
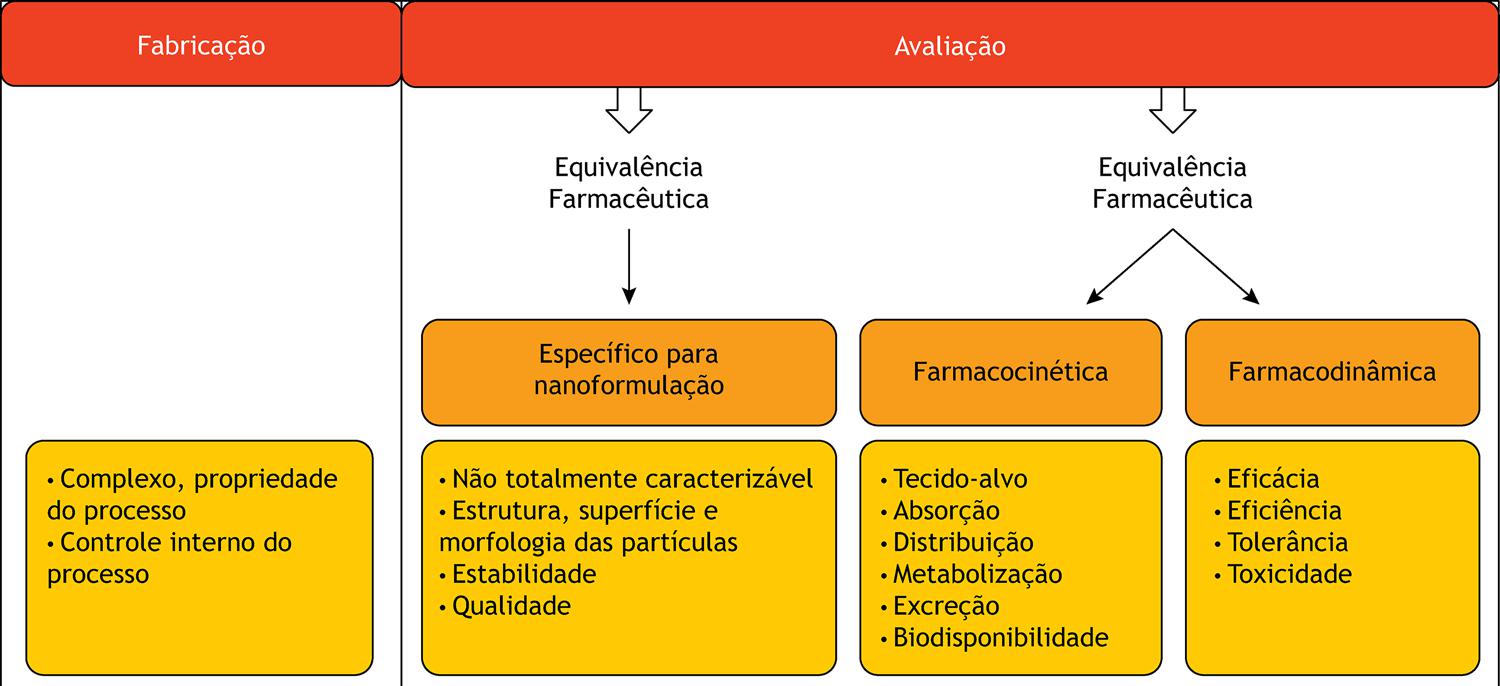
Figura 2
Fatores necessários para o controle do processo de fabricação, da qualidade e da similaridade de nanomedicamentos.
Fonte: Adaptado31.
Novas abordagens
As etapas atuais de um planejamento para a produção de nanomedicamentos ou de nanocarreadores2 ocorrem da seguinte forma: produção de nanomedicamento <-> caracterização físico-química <-> biocompatibilidade e nanotoxicologia <-> farmacocinética e farmacodinâmica <-> controle do processo e produção2 .
No entanto, a complexidade das interações entre os nanomateriais e os organismos resulta no entendimento apenas parcial dos riscos associados a seus usos e tem criado novos desafios para o controle de seus efeitos adversos potenciais ao homem e ao meio ambiente. Além disto, desde a introdução dos nanomedicamentos no mercado, os custos do desenvolvimento, a produção, a qualidade e a segurança têm sido fatores preocupantes e muitas vezes determinantes do sucesso ou não de um empreendimento. Devido a isto, em contraposição à abordagem tradicional da qualidade, algumas novas abordagens integradoras têm sido dirigidas ao processo de produção no sentido de garantirem a qualidade, reduzirem seus custos e diminuírem os riscos associados ao uso destes produtos94 .
Já no ano de 2000, o FDA propôs uma iniciativa denominada Quality by Design (QbD) ou qualidade baseada no processo para ser utilizada na produção de medicamentos e especialmente de nanomedicamentos. Em 2009, a International Conference on Harmonizatin of Technical Requirements for Registration of Pharmaceuticals for Human Use (ICH Q8) recomendou a adoção desta abordagem pela indústria farmacêutica.
As principais etapas deste processo são mostradas na Figura 3 . Embora este conceito não seja novo, esta abordagem, em contraposição ao modelo até então usual, propõe a construção da qualidade durante todo o processo de produção78 , 95 , 96 .
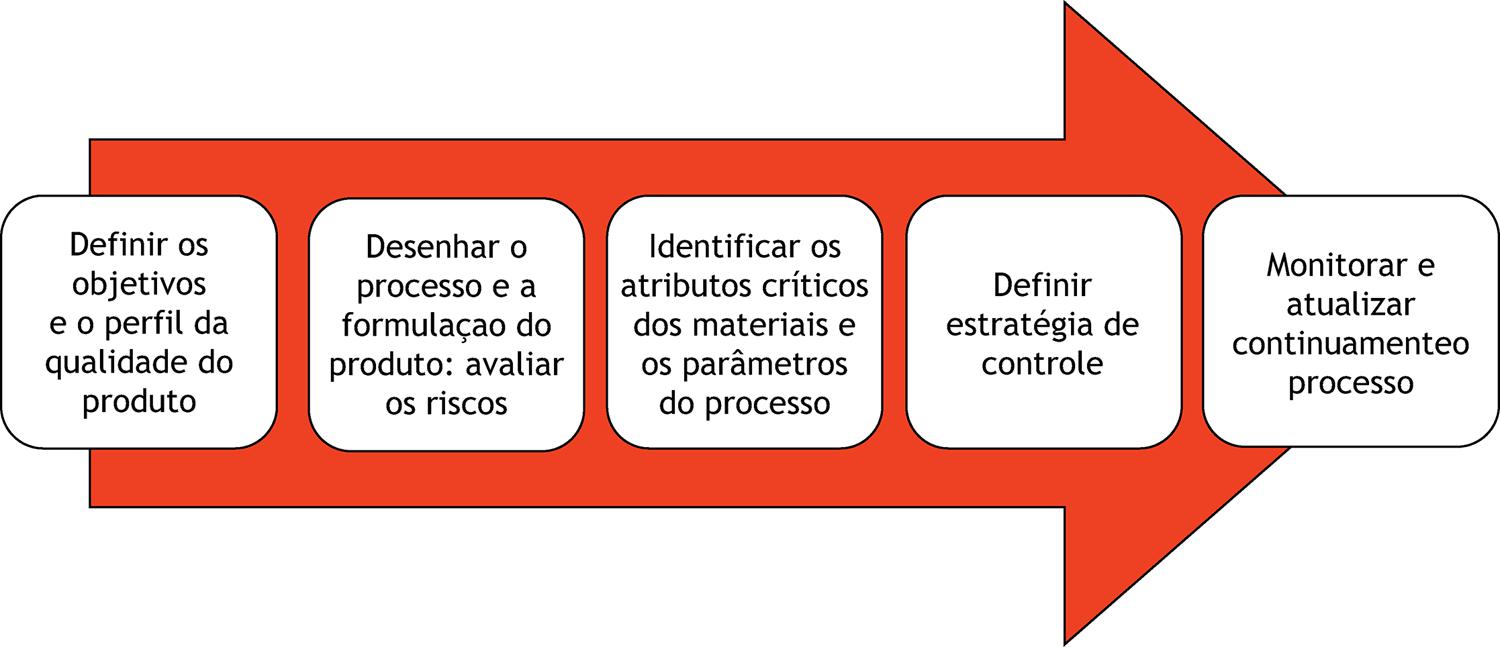
Figura 3
Principais etapas de um processo de Quality by Design .
Fonte: Modificado97.
Esta ferramenta pode ser entendida como uma abordagem sistemática aplicada durante a concepção e a produção de um medicamento de modo que consistentemente assegure a qualidade pré-definida ao final do processo com base nos conhecimentos científicos atuais e na gestão dos riscos ocupacionais97 .
Isto envolve a definição do perfil da qualidade pretendida do produto, a concepção do produto e dos processos de produção, a identificação dos atributos críticos para a qualidade, dos parâmetros do processo e das fontes de variabilidade e o controle do processo de produção de modo que se obtenha produtos com a qualidade consistente97 .
Esta metodologia exige o estabelecimento de uma série de atributos críticos para a qualidade, para o processo e para a produção. Dentre os 20 atributos críticos adotados para a qualidade dos nanomedicamentos, ressaltam-se: o tamanho das nanopartículas, a heterogeneidade de tamanho (índice de polidispersidade), a eficiência no encapsulamento, o potencial zeta e a quantidade do fármaco liberada78 . Um exemplo detalhado da aplicação da metodologia QbD na produção de um nanomedicamento pode ser encontrado em Raina et al.98 .
No Brasil, a Anvisa, por meio da Resolução de Diretoria Colegiada (RDC) n° 301, de 21 de agosto de 2019, incorporou este conceito em seu texto sobre as Boas Práticas de Fabricação de Medicamentos99 .
Mais recentemente, outra proposta tem ganho bastante atenção especialmente na Europa: a Safe-by-Design (SbD), ou segurança baseada no processo ( Figura 4 )27 , 100 . Este conceito de segurança baseada no processo aplicado aos nanomedicamentos, busca eliminar ou reduzir e controlar os perigos à saúde a partir dos riscos potenciais identificados à luz dos conhecimentos atuais e minimizá-los desde os estágios iniciais do processo de concepção do produto. Esta abordagem é utilizada no projeto GoNanoBioMat, financiado pela Comunidade Econômica Europeia, mas ainda não foi incluído nas normas produzidas pelo International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH), EMA ou FDA.
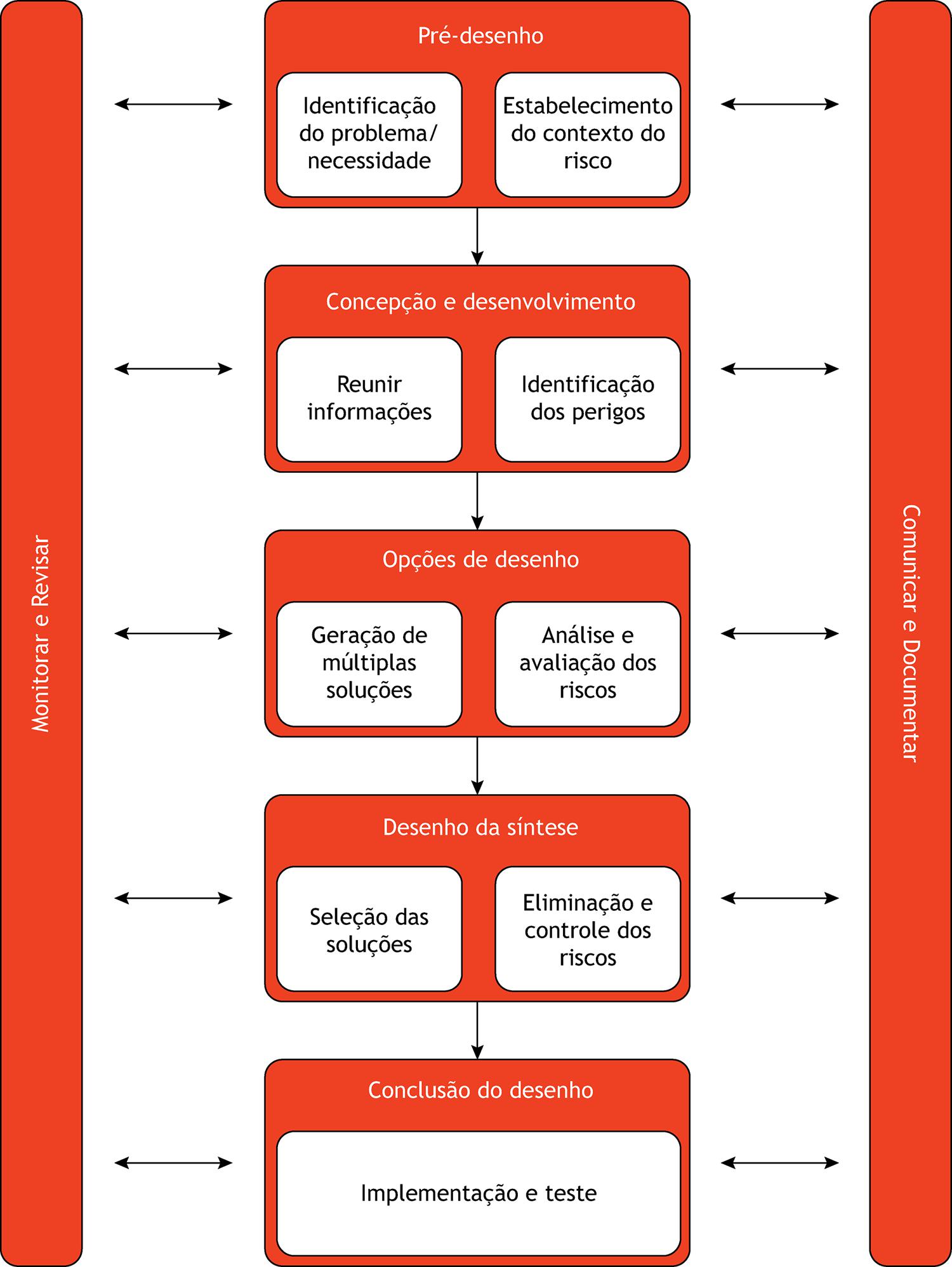
Figura 4
Etapas constituintes do processo Safe by Design .
Fonte: Adaptado104.
Neste conceito procura-se antever e reduzir os riscos e as incertezas relacionadas à segurança da saúde humana e do meio ambiente tendo como base a segurança e os requerimentos de eficácia. Considera a segurança como uma propriedade fundamental, assim como aquelas de natureza física ou química, advinda das características e efeitos biológicos e ambientais do nanomaterial. Ou seja, envolve a integração das etapas de identificação dos perigos e gerenciamento dos riscos às etapas iniciais do processo de delineamento e produção dos nanomedicamentos e se baseia em três pilares: 1 – nanobiomateriais seguros para a saúde humana e o meio ambiente; 2 – produção segura e controlada para garantir a segurança e a qualidade, eliminando os riscos ocupacionais e a produção de resíduos e 3 – uso e ciclo de vida seguros (transporte e estocagem seguras para garantirem a segurança e a qualidade dos nanobiomateriais) definindo rotas de reciclagem e de disposição final27 , 101 , 102 .
Esta abordagem tem sido utilizada nos projetos NaNOReg, NaNOReg 2, GoNanoBioMat e CALIBRATE, todos financiados pela Comunidade Econômica Europeia102 , 106 .
Mais recentemente se introduziu o conceito de Abordagem Segura da Inovação ( Safe Innovation Approach ou SIA), que acrescenta ao SbD o conceito de preparação regulatória, ou seja, além de utilizar todos os critérios da metodologia SbD, adiciona uma atitude proativa junto aos órgãos reguladores facilitando o desenvolvimento de normas reguladoras e a aprovação final dos produtos, como mostrado na Figura 5105 .
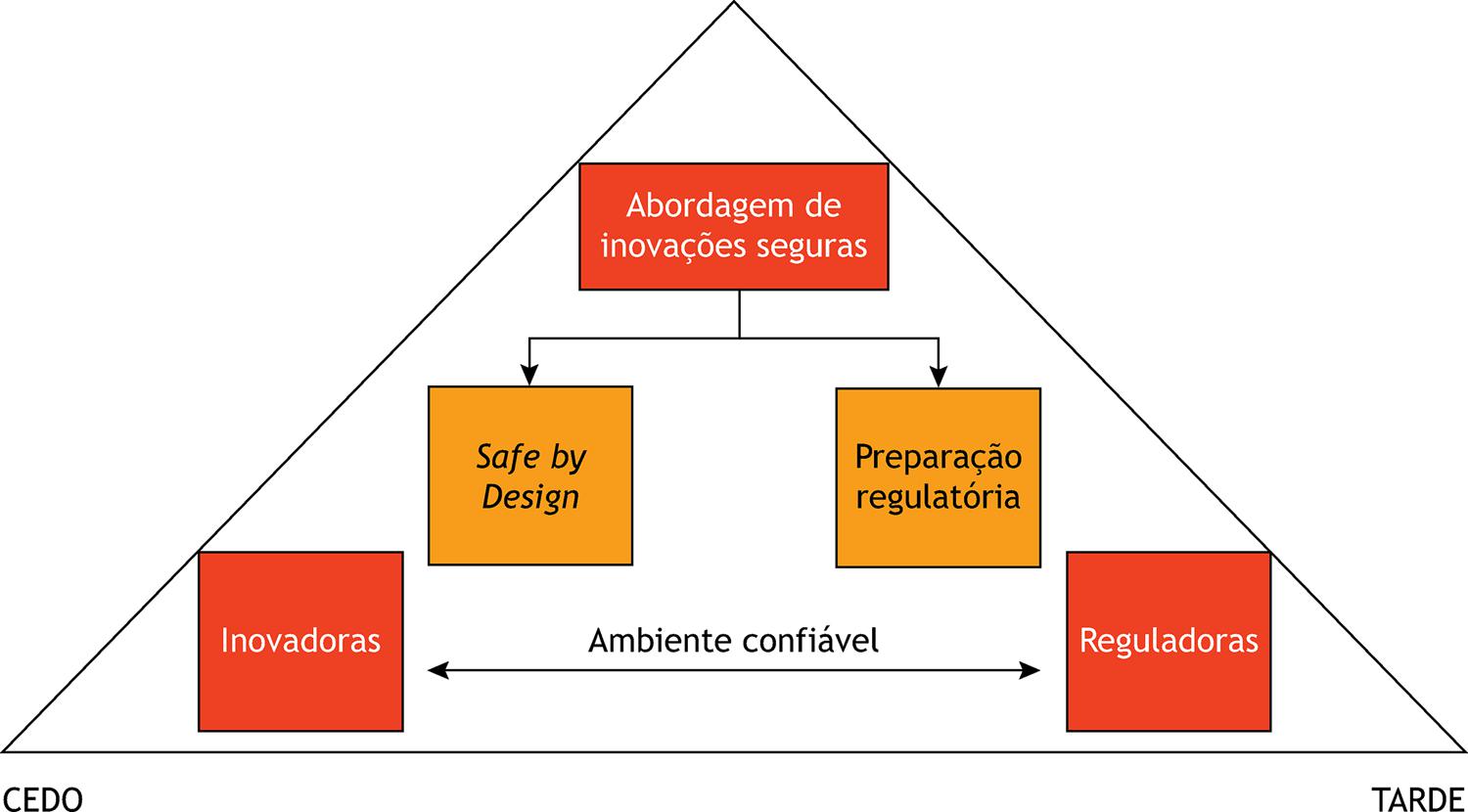
Figura 5
Representação conceitual do Abordagem Segura da Inovação (SAI).
Fonte: Adaptado106.
Estes procedimentos ainda estão em fase exploratória e, sendo uma área relativamente nova, necessitam de mais estudos27 . Estas abordagens exigem a produção de nanomateriais mais seguros quanto aos riscos e às incertezas relacionadas à saúde humana e à segurança ambiental. Mesmo assim algumas incertezas que se originam das alterações das propriedades físico-químicas das nanopartículas em contato com material biológico (adsorção, agregação, efeito corona etc.) ainda persistem e são capazes de afetarem suas toxicidades e suas funções27 , 100 , 104 .
Em 2016, o FDA publicou um guia para a indústria denominado Safety consideration for product design to minimize medication error , com recomendações aplicáveis a drogas e produtos biológicos107 .
CONCLUSÕES
Com o desenvolvimento industrial, as tecnologias utilizadas para a produção de medicamentos sofreram modificações na tentativa de se aumentar a eficácia, reduzir os custos e as doses administradas aos pacientes, assim como os efeitos adversos associados a alguns insumos farmacêuticos ativos. Desta forma, os nanomedicamentos foram projetados para atingirem diretamente o local específico da patologia com menor dose recomendada e maior dose máxima tolerada, tendo menos efeitos adversos para o indivíduo.
Porém, esta tecnologia trouxe consigo uma série de fatores que aumentaram em muito a complexidade das interações dos nanomedicamentos com os organismos vivos, exigindo uma adequação das normas regulamentadoras para os processos de produção, controle da qualidade, testes toxicológicos específicos e para o registro, constituindo uma grande preocupação mundial e uma prioridade para as autoridades sanitárias.
Sendo assim, grupos de reguladores de diversos países estão estabelecendo parcerias e projetos para discutirem e exporem os conhecimentos para conseguirem estabelecer normas para a produção, avaliação de eficácia, controle do processo produtivo e da qualidade de nanomedicamentos, assim como a proteção do profissional envolvido na fabricação e do consumidor final, e também do meio ambiente. No entanto, existem vários pontos que ainda requerem maior desenvolvimento, como a questão da bioequivalência e equivalência farmacêutica para os nanomedicamentos produzidos. Essa construção coletiva impacta diretamente os marcos regulatórios para o registro, a eficácia e a segurança desses produtos, porém ainda não consegue responder completamente as lacunas no conhecimento como apresentadas neste trabalho.
Assim, apesar da nanotecnologia associada a medicamentos estar no centro das pesquisas mundiais, ainda persistem inúmeras dúvidas a serem sanadas. A tendência atual é a de se regular os processos produtivos de modo a aumentar sua segurança, garantir a reprodutibilidade, a qualidade, a eficácia e diminuir os possíveis riscos de seus produtos. No entanto, isto ainda exige domínio de uma série de variáveis e o preenchimento de várias lacunas sendo um campo aberto para a pesquisa.
Agradecimentos
O presente trabalho foi realizado com o apoio da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior, Brasil (CAPES) – Código de Financiamento nº 001, do Programa INOVA/Fiocruz – Edital Geração do conhecimento 2019, do projeto Edital FAPERJ nº 02/2019 – Programa Redes de Pesquisa em Nanotecnologia no Estado do Rio de Janeiro.
REFERÊNCIAS
1. Barata-Silva C, Hauser-Davis RA, Silva ALO, Moreira JC. Desafios ao controle da qualidade de medicamentos no Brasil. Cad Saúde Colet. 2017;25(3):362-70. http://doi.org/10.1590/1414-462x201700030075
2. Soares S, Sousa J, Pais A, Vitorino C. Nanomedicine: principles, properties, and regulatory issues. Front Chem. 2018;6(360):1-15. http://doi.org/10.3389/fchem.2018.00360
3. Oberdörster G, Oberdörster E, Oberdörster J. Nanotoxicology: an emerging discipline evolving from studies of ultrafine particles. Environ Health Perspect. 2005;113(7):823-39. http://doi.org/10.1289/ehp.7339
4. Kim BY, Rutka JT, Chan WC. Nanomedicine. N Engl J Med. 2010;363(25):2434-43. http://doi.org/10.1056/NEJMra0912273
5. Jesus S, Schmutz M, Som C, Borchard G, Wick P, Borges O. Hazard assessment of polymeric nanobiomaterials for drug delivery: what can we learn from literature so far. Front Bioeng Biotechnol. 2019;7:1-37. http://doi.org/10.3389/fbioe.2019.00261
6. Bawa R. PharmaMedDevice 2007. Issues in nanodrug delivery and personalized medicine. IDrugs. 2007;10(7):455-8.
7. Nel AE, Mädler L, Velegol D, Xia T, Hoek EM, Somasundaran P et al. Understanding biophysicochemical interactions at the nano-bio interface. Nat Mater. 2009;8(7):543-57. http://doi.org/10.1038/nmat2442
8. Gil PR, Hühn D, Mercato LL, Sasse D, Paarak WJ. Nanopharmacy: inorganic nanoscale devices as vectors and active compounds. Pharmacol Res. 2010;62(2):115-25. http://doi.org/10.1016/j.phrs.2010.01.009
9. Weissig V, Pettinger TK, Murdock N. Nanopharmaceuticals (part 1): products on the market. Int J Nanomedicine. 2014;9:4357-73. http://doi.org/10.2147/IJN.S46900
10. Monopoli MP, Aberg C, Salvati A, Dawson KA. Biomolecular coronas provide the biological identity of nanosized materials. Nat Nanotechnol. 2012;7(12):779-86. http://doi.org/10.1038/nnano.2012.207
11. Ossa D. Quality aspects of nano-based medicines SME workshop: focus on quality for medicines containing chemical entities London. Amsterdam: European Medicines Agency; 2014[acesso 2 out 2018]. Disponível em: http://www.ema.europa.eu/docs/en_GB/document_library/Presentation/2014/04/W500165444.pdf
12. Caixeta AV. Nanomedicamentos e nanocarreadores de drogas para o uso terapêutico de câncer [especialização]. Goiânia: Pontifícia Universidade Católica de Goiás; 2013[acesso 1 out 2018]. Disponível em: http://www.cpgls.pucgoias.edu.br/8mostra/Artigos/SAUDE%20E%20BIOLOGICAS/Nanomedicamentos%20e%20Nanocarreadores%20de%20drogas%20para%20o%20usoterap%C3%AAutico%20de%20C%C3%A2ncer.pdf
13. Falleiros JPB, Brandil AL, Fonseca ARA. Aplicações da nanotecnologia no diagnóstico e tratamento de câncer. Nucleus. 2011;8(1):151-70. http://doi.org/10.3738/nucleus.v8i1.453
14. Gubala V, Johnston LJ, Liu Z, Krug H, Moore CJ, Ober CK et al. Engineered nanomaterials and human health part 1: preparation, functionalization and characterization (IUPAC Technical Report). Pure Appl Chem. 2018;90(8):1283-324. http://doi.org/10.1515/pac-2017-0101
15. Albanese A, Tang PS, Chan WC. The effect of nanoparticle size, shape, and surface chemistry on biological systems. Annu Rev Biomed Eng. 2012;14:1-16. http://doi.org/10.1146/annurev-bioeng-071811-150124
16. Jabir NR, Tabrez S, Ashraf GM, Shakil S, Damanhouri GA, Kamal MA. Nanotechnology-based approaches in anticancer research. Int J Nanomedicine. 2012;7:4391-408. http://doi.org/10.2147/IJN.S33838
17. Pavon LF, Okamoto OK. Aplicações de recursos nanobiotecnológicos em câncer. Einstein. 2007;5(1):74-7.
18. Jain KK. Advances in the field of nanooncology. BMC Med. 2010;8:1-11. http://doi.org/10.1186/1741-7015-8-83
19. Feitosa JPM. Funcionalização covalente e não covalente de nanotubos de carbono [dissertação]. Fortaleza: Universidade Federal do Ceará; 2009.
20. Pradhan M, Alexander A, Singh MR, Singh D, Saraf S, Saraf S et al. Understanding the prospective of nano-formulations towards the treatment of psoriasis. Biomed Pharmacother. 2018;107:447-63. http://doi.org/10.1016/j.biopha.2018.07.156
21. Akhter S, Ahmad I, Ahmad MZ, Ramazani F. Nanomedicines as cancer therapeutics: current status. Curr Cancer Drug Targets. 2013;13(4):262-78. http://doi.org/10.2174/1568009611313040002
22. Som C, Schmutz M. Guidelines for implementing a safe-by-design approach for medicinal polymeric nanocarriers. St Gallen: Empa; 2019.
23. Patra JK, Das G, Fraceto LF, Campos EVR, Rodriguez-Torres MP, Acosta-Torres LS et al. Nano based drug delivery systems: recent developments and future prospects. J Nanobiotechnol. 2018;16(1):71- 83. http://doi.org/10.1186/s12951-018-0392-8
24. Weissig V, Guman-Villanueva D. Nanopharmaceuticals (part 2): products in the pipeline. Int J Nanomedicine. 2015;10:1245-57. http://doi.org/10.2147/IJN.S65526
25. Ulku Y, Burcu GB. The importance of nanotechnology and drug carrier systems in pharmacology. GSC Biol Pharm Sci. 2020;10(2):14-23. http://doi.org/10.30574/gscbps.2020.10.2.0018
26. Farjadian F, Ghasemi A, Gohari O, Roointan A, Karimi M, Hamblin MR. Nanopharmaceuticals and nanomedicines currently on the market: challenges and opportunities. Nanomedicine (Lond). 2019;14(1):1-12. http://doi.org/10.2217/nnm-2018-0120
27. Yan L, Zhao F, Wang J, Zu Y, Gu Z, Zhao Y. A safe by design strategy towards safer nanomaterials in nanomedicine. Adv Mater. 2019;31:1-33. http://doi.org/10.1002/adma.201805391
28. Stern ST, Zou P, Skoczen S, Xie S, Liboiron B, Harasym T et al. Prediction of nanoparticle prodrug metabolismo by pharmacokinetic modeling of biliary excretion. J Control Release. 2013;172(2):558-67. http://doi.org/10.1016/j.jconrel.2013.04.025
29. Zhao F, Meng H, Yan L, Wang B, Zhao Y. Nanosurface chemistry and dose govern the bioaccumulation and toxicity of carbon nanotubes, metal nanomaterials and quantum dots in vivo. Sci Bull. 2015;60(1):3-20. http://doi.org/10.1007/s11434-014-0700-0
30. World Health Organization – WHO. Cancer: fact sheet 297. Geneva: World Health Organization; 2018[acesso 1 out 2018]. Disponível em: http://www.who.int/mediacentre/factsheets/fs297/en/
31. Tinkle S, Mcneil SE, Mühlebach S, Bawa R, Borchard G, Barenholz YC. Nanomedicines: addressing the scientific and regulatory gap. Ann N Y Acad Sci. 2014;1313:35-56. http://doi.org/10.1111/nyas.12403
32. Anselmo AC, Mitagrotri S. Nanoparticles in the clinic. Bioeng Transl Med. 2016;1(1):10-29. http://doi.org/10.1002/btm2.10003
33. Anselmo AC, Mitagrotri S. Nanoparticles in the clinic: an update. Bioeng Transl Med. 2019;4(3):1-19. http://doi.org/10.1002/btm2.10143
34. Yan L, Zhao F, Wang J, Zu Y, Gu Z, Zhao Y. A Safe-by-Design strategy towards safer nanomaterials in nanomedicines. Adv Mater. 2019;31(45). http://doi.org/10.1002/adma.201805391
35. Brand W, Noorlander CW, Giannakou C, Jong WH, Kooi MW, Park MVDZ et al. Nanomedicinal products: a survey on specific toxicity and side effects. Int J Nanomedicine. 2017;12:6107-29. http://doi.org/10.2147/IJN.S139687
36. Giannakou C, Park MVDZ, Jong WH, Loveren HV, Vandebriel RJ, Geertsma RE. A comparison in immunotoxic effects of nanomedicinal products with regulatory immunotoxicity testing requirement. Int J Nanomedicine. 2016;11:2935-52. http://doi.org/10.2147/IJN.S102385
37. Roy U, Drozd V, Durygin A, Rodriguez J, Barber P, Atluri V et al. Characterization of nanodiamond-based anti-HIV drug delivery to the brain. Sci Rep. 2018;8:1-12. http://doi.org/10.1038/s41598-017-16703-9
38. Shao J, Kraft JC, Li B, Yu J, Freeling J, Koehn J et al. Nanodrug formulations to enhance HIV drug exposure in lymphoid tissues and cells: clinical significance and potential impact on treatment and eradication of HIV/AIDS. Nanomedicine (Lond). 2016;11(5):545-64. http://doi.org/10.2217/nnm.16.1
39. Roy U, Ding H, Kanthikeel SP, Raymond AD, Atluri V, Yndart A et al. Preparation and characterization of anti-HIV nanodrug targeted to microfold cell of gut-associated lymphoid tissue. Int J Nanomedicine. 2015;10:5819-35. http://doi.org/10.2147/IJN.S68348
40. Ibrahim S, Tagami T, Ozeki T. Effective-loading of platinum-chloroquine into PEGylated neutral and cationic liposomes as a drug delivery system for resistant malaria parasites. Biol Pharm Bull. 2017;40(6):815-23. http://doi.org/10.1248/bpb.b16-00914
41. Guo J, Waknine-Grinberg JH, Mitchell AJ, Barenholz Y, Golenser J. Reduction of experimental cerebral malaria and its related proinflammatory responses by the novel liposome-based ß-methasone nanodrug. Biomed Res Int. 2014;2014:1-8. http://doi.org/10.1155/2014/292471
42. Azeem A, Ahmad FJ, Khar RK, Talegaonkar S. Nanocarrier for the transdermal delivery of an antiparkinsonian drug. AAPS PharmSciTech. 2009;10(4):1093-103. http://doi.org/10.1208/s12249-009-9306-2
43. Helal-Neto E, Pinto SR, Portilho FL, Costa MD, Pereira JX, Nigro F et al. Development and biological evaluation of a new nanotheranostic for tuberculosis. Drug Deliv Transl Res. 2018;9(1):97-105. http://doi.org/10.1007/s13346-018-0577-6
44. Babu A, Templeton AK, Munshi A, Ramesh R. Nanodrug delivery systems: a promising technology for detection, diagnosis, and treatment of cancer. AAPS PharmSciTech. 2014;15(3):709-21. http://doi.org/10.1208/s12249-014-0089-8
45. Liu L, Ye Q, Lu M, Chen ST, Tseng HW, Lo YC et al. A new approach to deliver anticancer nanodrugs with reduced off-target toxicities and improved efficiency by temporarily blunting the reticuloendothelial system with intralipid. Sci Rep. 2017;7(1):1-13. http://doi.org/10.1038/s41598-017-16293-6
46. Huang Y, Cole SPC, Cai T, Cai Y. Applications of nanoparticle drug delivery systems for the reversal of multidrug resistance in cancer (review). Oncol Lett. 2016;12(1):11-5. http://doi.org/10.3892/ol.2016.4596
47. Zhao R, Zheng G, Fan L, Shen Z, Jiang K, Guo Y et al. Carrier-free nanodrug by co-assembly of chemotherapeutic agent and photosensitizer for cancer imaging and chemo-photo combination therapy. Acta Biomaterialia. 2018;70:197-210. http://doi.org/10.1016/j.actbio.2018.01.028
48. Hare JI, Lammers T, Ashford MB, Puri S, Storm G, Barry ST. Challenges and strategies in anti-cancer nanomedicine development: an industry perspective. Adv Drug Deliv Rev. 2017;108:25-38. http://doi.org/10.1016/j.addr.2016.04.025
49. Allahverdiyev AM, Parlar E, Dinparvar S, Bagirova M, Abamor ES. Current aspects in treatment of breast cancer based of nanodrug delivery systems and future prospects. Artif Cells Nanomed Biotechnol. 2018;46(Supl.3):S755-62. http://doi.org/10.1080/21691401.2018.1511573
50. Xiong W, Li L, Wang Y, Yu Y, Wang S, Gao Y et al. Design and evaluation of a novel potential carrier for a hydrophilic antitumor drug: auricularia auricular polysaccharide-chitosan nanoparticles as a delivery system for doxorubicin hydrochloride. Int J Pharm. 2016;511(1):267-75. http://doi.org/10.1016/j.ijpharm.2016.07.026
51. Xu Z, Kleinstreuer C. Direct nanodrug delivery for tumor targeting subject to shear-augmented diffusion in blood flow. Med Biol Eng Comput. 2018;56(11):1949-58. http://doi.org/10.1007/s11517-018-1818-z
52. Millard M, Yakavets I, Zorin V, Kulmukhamedova A, Marchal S, Bezdetnaya L. Drug delivery to solid tumors: the predictive value of the multicellular tumor spheroid model for nanomedicine screening. Int J Nanomedicine. 2017;12:7993-8007. http://doi.org/10.2147/IJN.S146927
53. Zhang J, Tang H, Liu Z, Chen B. Effects of major parameters of nanoparticles on their physical and chemical properties and recent application of nanodrug delivery system in targeted chemotherapy. Int J Nanomedicine. 2017;12:8483-93. http://doi.org/10.2147/IJN.S148359
54. Zhang N, Zhang J, Wang P, Liu X, Huo P, Xu Y et al. Investigation of an antitumor drug-delivery system based on anti-HER2 antibody-conjugated BSA nanoparticles. Anticancer Drugs. 2018;29(4):307-22. http://doi.org/10.1097/CAD.0000000000000586
55. Kapse-Mistry S, Govender T, Srivastava R, Yergeri M. Nanodrug delivery in reversing multidrug resistance in cancer cells. Front Pharmacol. 2014;5:1-22. http://doi.org/10.3389/fphar.2014.00159
56. Bregoli L, Movia D, Gavigan-Imedio J, Lysaght J, Reynolds J, Prina-Mello A. Nanomedicine applied to translational oncology: a future perspective on cancer treatment. Nanomedicine. 2016;12(1):81-103. http://doi.org/10.1016/j.nano.2015.08.006
57. Li C, Lin J, Wu P, Zhao R, Zou J, Zhou M et al. Small molecule nanodrug assembled of dual-anticancer drug conjugate for synergetic cancer metastasis therapy. Bioconjug Chem. 2018;29(1):3495-502. http://doi.org/10.1021/acs.bioconjchem.8b00657
58. Alphandéry E, Grand-Dewyse P, Lefèvre R, Mandawala C, Durand-Dubief M. Cancer therapy using nanoformulated substances: scientific, regulatory and financial aspects. Expert Rev Anticancer Ther. 2015;15(10):1233-55. http://doi.org/10.1586/14737140.2015.1086647
59. Ahmed S, Govender T, Khan I, Rehman NU, Ali W, Muhammad S et al. Experimental and molecular modeling approach to optimize suitable polymers for fabrication of stable fluticasone nanoparticles with enhanced dissolution and antimicrobial activity. Drug Des Devel Ther. 2018;12:255-69. http://doi.org/10.2147/DDDT.S148912
60. Sikwl DR, Kalhapure RS, Rambharose S, Vepuri S, Soliman M, Mocktar C et al. Polyelectrolyte complex of vancomycin as a nanoantibiotic: preparation, in vitro and in silico studies. Mater Sci Eng C Mater Biol Appl. 2016;63:489-98. http://doi.org/10.1016/j.msec.2016.03.019
61. Weissig V, Guzman-Villanueva D. Nanocarrier-based antioxidant therapy: promise or delusion? Expert Opin Drug Deliv. 2015;12(11):1783-90. http://doi.org/10.1517/17425247.2015.1063611
62. Mehrizi TZ, Ardestani MS, Khamesipour A, Hoseini MHM, Mosaffa N, Anissian A et al. Reduction toxicity of amphotericin B through loading into a novel nanoformulation of anionic linear globular dendrimer for improve treatment of Leishmania major. J Mater Sci Mater Med. 2018;29(8). http://doi.org/10.1007/s10856-018-6122-9
63. Goonoo N, Bhaw-Luximon A, Ujoodha R, Jhugroo A, Hulse GK, Jhurry D. Naltrexone: a review of existing sustained drug delivery systems and emerging nano-based systems. J Control Release. 2014;183:154-66. http://doi.org/10.1016/j.jconrel.2014.03.046
64. Yadav A, Flora SJS. Nano drug delivery systems: a new paradigm for treating metal toxicity. Expert Opin Drug Deliv. 2016;13(6):831-41.
65. Madi M, Pavlic V, Samy W, Alagl A. The anti-inflammatory effect of locally delivered nano-doxycycline gel in therapy of chronic periodontitis. Acta Odontol Scand. 2018;76(1):71-6. http://doi.org/10.1080/00016357.2017.1385096
66. Mohamed EA, Hashim IIA, Yusif RM, Shaaban AAA, El-Sheakh AR, Hamed MF et al. Polymeric micelles for potentiated antiulcer and anticancer activities of naringin. Int J Nanomedicine. 2018;13:1009-27. http://doi.org/10.2147/IJN.S154325
67. Foulkes R, Man E, Thind J, Yeung S, Joy A, Hoskins C. The regulation of nanomaterials and nanomedicines for clinical application: current and future perspectives. Biomat Sci. 2020;8(1):4653-64. http://doi.org/10.1039/D0BM00558D
68. Bhardwaj V, Kaushik A, Khatib ZM, Nair M, Mcgoron AJ. Recalcitrant issues and new frontiers in nano-pharmacology. Front Pharmacol. 2019;10:1-9. http://doi.org/10.3389/fphar.2019.01369
69. Louie SM, Ma R, Lowry GV, Gregory KB, Apte SC, Lead JR. Transformations of nanomaterials in the environment. Environ Sci Technol. 2012;46(13):6893-9. http://doi.org/10.1021/es300839e
70. European Chemicals Agency – Reach. Characterisation of dose [concentration]-response for environment. In: European Chemicals Agency – Reach. Guidance on information requirements and chemical safety assessment. Helsinki: European Chemicals Agency; 2008[acesso 15 jun 2020]. p. 2-65. Disponível em: http://echa.europa.eu/documents/10162/13632/information_requirements_r10_en.pdf/bb902be7-a503-4ab7-9036-d866b8ddce69
71. Flühmmann B, Ntai I, Borchard G, Simoens S, Mühlebach S. Nanomedicines: the magic bullets reaching their target? Eur J Pharm Sci. 2019;128:73-80. http://doi.org/10.1016/j.ejps.2018.11.019
72. Muhlebach S. Regulatory challenges of nanomedicines and their follow-on version: a generic or similar approach. Adv Drug Dellivery Rev. 2018;131:122-31. http://doi.org/10.1016/j.addr.2018.06.024
73. Sainz V, Conniot J, Matos I, Peres C, Zupancic E, Moura L et al. Regulatory aspects on nanomedicines. Biochem Biophys Res Commun. 2015;468(3):504-10. http://doi.org/10.1016/j.bbrc.2015.08.023
74. Farjadian F, Ghjasemi A, Gohari O, Roointan A, Karimi M, Hamblin MR. Nanopharmaceuticals and nanomedicines currently on the market: challenges and opportunities. Nanomedicine (Lond). 2019;14(1):93-126. http://doi.org/10.2217/nnm-2018-0120
75. US Food & Drug Admistration – FDA. Drug products, including biological products that contain nanomaterials. Silver Spring: US Food & Drug Admistration; 2017[acesso 4 jul 2020]. Disponível em: http://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm588857.pdf
76. Schellekens H, Stegemann S, Weinstein V, Vlieger JSB, Flühmann B, Mühlebach S et al. How to regulate nonbiological complex drugs and they follow-on versions: points to consider. AAPS J. 2014;16(1):15-21. http://doi.org/10.1208/s12248-013-9533-z
77. Rocco P, Eberini I, Musazzi UM, Franzè S, Minghetti P. Glatiramer acetate: a complex drug beyond biologics. Eur J Pham Sci. 2019;133:8- 14. http://doi.org/10.1016/j.ejps.2019.03.011
78. European Medicines Agency – EMA. Pharmaceutical development Q8 (R2). Amsterdam: European Medicines Agency; 2009.
79. Grossman JH, Crist RM, Clogston JD. Early development challenges for drug products containing nanomaterials. AAPS J. 2017;19(1):92-102. http://doi.org/10.1208/s12248-016-9980-4
80. Gottardo S, Crutzen H, Jantunen P. NANoReg framwork for the safety assessment of nanomaterials. Brussels: European Commision; 2017.
81. Zielinska A, Costa B, Ferreira MV, Miguéis D, Louros JMS, Durazzo A et al. Nannotoxicology and nanosafety: Safety-by-Design and testing at a glance. Int J Environ Res Public Health. 2020;17(13):1-23. http://doi.org/10.3390/ijerph17134657
82. Silva ACC. Nanotecnologia em diagnóstico e terapia no Brasil [mestrado]. São Paulo: Universidade de São Paulo; 2015.
83. Gottardo S, Crutzen H, Jantunen P. Nanoreg framework for the safety assessment of nanomaterials. Brussels: European Commission; 2017[acesso 26 abr 2020]. Disponível em: http://publications.jrc.ec.europa.eu/repository/bitstream/JRC105651/kjna28550enn.pdf
84. Organization for Economic Co-operation and Development – OECD. Report of the scientific conference: science based support for regulation of manufactured nanomaterials. Paris: Organization for Economic Co-operation and Development; 2016[acesso 4 ago 2020]. Disponível em: www.oecd.org
85. Kwong GA, Radu CG, Hwang K, Shu CJ, Ma C, Koya RC et al. Modular nucleic acid assembled p/MHC microarrays for multiplexed sorting of antigen-specific T cells. J Am Chem Soc. 2009;131:9695-703. http://doi.org/10.1021/ja9006707
86. Nel AE, Madler L, Velegol D, Xia T, Hoek EMV, Somasundaran P et al. Understanding biophysicochemical interactions at the nano-bio interface. Nat Mater. 2009;8(7):543-57. http://doi.org/10.1038/nmat2442
87. Oliveira LPS, Marinho ME, Fumagali EO. Nanomedicamentos e os desafios da Anvisa diante da inexistência de um marco regulatório no Brasil. Amazon Res Env Law. 2015;3(3):36-51. http://doi.org/10.14690/2317-8442.2015v33166
88. Schwirn K, Voelker D, Galert W, Quik J, Tietjen L. Environmental risk assessment of nanomaterials in the light of new obligations under the REACH regulations: with challenges remain and how to approach them? Integr Environ Assess and Manag. 2020;16(5):706-17. http://doi.org/10.1002/ieam.4267
89. International Standard Organization – ISO. ISO/TR 22019:2019 nanotechnologies: considerations for performing toxicokinetic studies with nanomaterials. Geneva: International Standard Organization; 2019.
90. Borchard G, Flühmann B, Mühlebach S. Nanoparticle iron medicinal products: requirements for approval of intended copies of non-biological complex drugs (NBCD) and the importance of clinical comparative studies. Regul Toxicol Pharmacol. 2012;64(2):324-8. http://doi.org/10.1016/j.yrtph.2012.08.009
91. Schellekens H, Klinger E, Mühlebach S. The therapeutic equivalence of complex drugs. Regul Toxicol Pharmacol. 2011;59(1):176-83. http://doi.org/10.1016/j.yrtph.2010.09.021
92. Hussaarts L, Mühlebach S, Shah VP, Mcneil S, Borchard G, Flühmann B et al. Equivalence of complex drug products: advances, in challenges for current regulatory frameworks. Ann N Y Acad Sci. 2017;1407(1):39-49. http://doi.org/10.1111/nyas.13347
93. Accomasso L, Cristallini C, Giachino C. Risk assessment and risk minimization in nanomedicine: a need for predictive, alternative, and 3Rs strategies. Front Pharmacol. 2018;9:1-7. http://doi.org/10.3389/fphar.2018.00228
94. Mukhopadhyay S, Nautiyal J, Bhatt J, Durgapal S. Nanotoxicology: assessment of toxicological properties of nanomaterial. J Nanomed Res. 2017;6(2):1-2. http://doi.org/10.15406/jnmr.2017.06.00149
95. Bastogmne T. Quality by design of nanopharmaceuticals: a state of the art. Nanomedicine. 2017;13(7):2151-7. http://doi.org/10.1016/j.nano.2017.05.014
96. Dahmash EZ, Al-KhattawI A, Iyire A, Al-Yami H, Dennison TJ, Mohammed AR. Quality by design (QbD) based process optimisation to develop functionalised particles with modified release properties using novel dry particle coating technique. Plos One. 2018;13(11):1-20. http://doi.org/10.1371/journal.pone.0206651
97. Yu LX. Pharmaceutical quality by design: product and process development, understanding, and control. Pharm Res. 2008;25(4):781-90. http://doi.org/10.1007/s11095-007-9511-1
98. Raina H, Kaur S, Jinda AB. Development of efavirenz loaded solid lipid nanoparticles: risk assessment, quality by design based optimization and physicochemical characterization. J Drug Deli Sci Tech. 2017;39:180-91. http://doi.org/10.1016/j.jddst.2017.02.013
99. Agência Nacional de Vigilância Sanitária – Anvisa. Resolução RDC Nº 301, de 21 de agosto de 2019. Dispõe sobre as diretrizes gerais de boas práticas de fabricação de medicamentos. Diário Oficial União. 22 ago 2019.
100. Kraegeloh A, Suarez-Merino B, Sluijters T, Micheletti C. Implementing a Safe-by-Design for nanomaterial development and safe innovation: why we need a comprehensive approach. Nanomaterials (Basel). 2018;8(4):1-12. http://doi.org/10.3390/nano8040239
101. Jacobs U, De Vries M. Design for values in nanotechnology. In: Hoven J, Vermaas PE, Poel I, editores. Handbook of ethics and technological design. Dordrecht: Springer Science; 2013. p.1-19
102. Schmutz M, Borges O, Jesus S, Borchard G, Perale G, Zinn M et al. A methodological Safe-by-Design approach for the development of nanomedicines. Front Bioeng Biotechnol. 2020;8:1-7. http://doi.org/10.3389/fbioe.2020.00258
103. Australian Safety and Compensation Council – ASCC. Guidance of the principles of safe by design for work. Camberra: Australian Government; 2006.
104. Cobaleda-Siles M, Guillamon AP, Delpivo C, Vázquez-Campos S, Puntes VF. Safer by design strategies. J Phys Conf Ser. 2017;838:1-10. http://doi.org/10.1088/1742-6596/838/1/012016
105. Soeteman-Hernandez LG, Apostolova MD, Bekker C, Dekkers S, Grafström RC, Groenewold M et al. Safe innovation approach: towards an agile system for dealing with innovations. Mat Today Commun. 2019;20:1-47. http://doi.org/10.1016/j.mtcomm.2019.100548
106. Poel I, Robaey Z. Safe-by-Design: from safety to responsibility. Nanoethics. 2017;11:297-306. http://doi.org/10.1007/s11569-017-0301-x
107. US Food and Drug Administration – FDA. Safety consideration for product design to minimize medication error. Silver Spring: US Food and Drug Administration; 2016[acesso 15 jul 2020]. Disponível em: http://www.gmp-compliance.org/guidemgr /files/UCM331810.pdf
Autor notes
Barata-Silva C, Moreira JC – Concepção, planejamento (desenho do estudo), aquisição, análise, interpretação dos dados e redação do trabalho. dos Santos LMG, Vicentini Neto SA, Magalhães CD, Jacob SC – Concepção, planejamento (desenho do estudo) e redação do trabalho. Todos os autores aprovaram a versão final do trabalho.
* E-mail: cristianebarata@hotmail.com
Declaração de interesses
Os autores informam não haver qualquer potencial conflito de interesse com pares e instituições, políticos ou financeiros deste estudo.
