REVISÃO
A influência da microbiota de doadores e do armazenamento do enxerto no transplante de córnea
Influence of donor microbiota and of graft storage on corneal transplantation
A influência da microbiota de doadores e do armazenamento do enxerto no transplante de córnea
Vigilância Sanitária em Debate, vol. 10, núm. 1, pp. 44-54, 2022
INCQS-FIOCRUZ
Recepção: 30 Dezembro 2020
Aprovação: 21 Julho 2021
Resumo
Introdução: O transplante de córneas é o principal tratamento para pessoas que apresentam distúrbios de curvatura ou transparência da córnea. No Brasil, não há protocolo unificado para meios de preservação, tempo de armazenamento e antibióticos utilizados. A preocupação é a de que patógenos possam ser transferidos aos receptores de transplantes.
Objetivo: Realizar o levantamento da microbiota ocular de doadores de córneas a fim de verificar uma possível correlação com infecções em receptores e, dessa forma, auxiliar na melhoria de metodologias e protocolos de armazenamento de córneas.
Método: Foi conduzido a partir de revisão da literatura, nas bases de dados PubMed, SciELO e nos portais: periódicos da CAPES, Anvisa, Ministério da Saúde e ABTO, entre 2018 e 2020.
Resultados: Estudos baseados em cultivo de microrganismos trazem Staphylococcus coagulase negativa (SCN) de 30% a 100% das amostras isoladas de conjuntivas. Em menor quantidade estão Streptococcus, Corynebacterium e Propionibacterium . Bactérias Gram-negativas aparecem em número inferior, representadas pelos gêneros Haemophilus, Neisseria, Pseudomonas, Enterobacter, Escherichia, Proteus e Acinetobacter . Já as técnicas independentes de cultivo trazem Pseudomonas como a principal colonizadora da conjuntiva. Também apresentam uma diversidade maior de colonizadores, mostrando um potencial campo de estudos, no qual a superfície ocular pode ter uma diversidade muito maior de espécies e potenciais agentes patogênicos. Os principais meios de preservação utilizados no Brasil levam os antimicrobianos gentamicina e estreptomicina em sua composição, porém estudos têm mostrado que as bactérias presentes nos meios de preservação são resistentes a esses antibióticos.
Conclusões: Os dados apontam para a necessidade de reavaliação da eficiência desses meios de preservação na descontaminação das córneas para transplante.
Palavras-chave: Microbiota+ Transplante de Córnea+ Meio de Preservação+ Resistência a Antimicrobianos.
Abstract
Introduction: Corneal transplantation it is the main treatment for people who have corneal curvature or transparency disorders. In Brazil, there is no unified protocol on the means of preservation, storage time and antibiotics used. The concern is that pathogens are transferred to transplant recipients, causing eye infections after transplantation.
Objective: Examine ocular microbiota of corneal donors, to verify a possible correlation with infections in recipients and thus assist in improving corneal storage methodologies and protocols.
Method: Literature review conducted in PubMed, SciELO and the following websites: CAPES Journals, Anvisa, Brazilian Ministry of Health and ABTO, between 2018 and 2020.
Results: Studies based on microorganism’s cultivation show coagulase negative Staphylococcus in 30% to 100% of samples isolated from conjunctiva. In lesser quantities are Streptococcus, Corynebacterium and Propionibacterium . Gram-negative bacteria appear in much lower numbers, represented by the genera Haemophilus, Neisseria, Pseudomonas, Enterobacter, Escherichia, Proteus and Acinetobacter . On the other hand, results based on independent cultivation techniques bring Pseudomonas as the main colonizer of the conjunctiva. Also, they have a much greater diversity of colonizers, showing a potential field of study. The ocular surface may have a much greater diversity of species and potential pathogens than was expected. The main means of preservation used in Brazil contain the antimicrobials gentamicin and streptomycin in their composition; however, several studies have shown that bacteria present in the means of preservation are resistant to these antibiotics.
Conclusions: These data point to the need for a reassessment of the efficiency of these means of preservation in decontaminating corneas for transplantation.
Keywords: Microbiota, Corneal Transplantation, Mean of Preservation, Antibiotic Resistance.
INTRODUÇÃO
O ano de 2020 trouxe novos desafios na área da saúde, impactando diretamente a disponibilidade e os serviços de doação de órgãos. No dia 11 de março de 2020, a Organização Mundial da Saúde (OMS) declarou a pandemia de SARS-CoV-2. O Brasil, durante o período da pandemia, por falta de direcionamento de estratégias do governo federal coordenadas com os estados e municípios brasileiros, atingiu, em abril de 2021, a triste marca de 400 mil mortes, de acordo com os dados divulgados pelo portal do Ministério da Saúde 1 . Essa tragédia refletiu, também, na diminuição da taxa de doação e transplantes no país. O número de transplantes de córnea no primeiro semestre de 2020 caiu 44,3%, comparado ao mesmo período do ano passado 2 .
O número de doadores se mostra insuficiente quando comparado ao número de pacientes que aguardam em filas de transplante. Um levantamento realizado em 2019 estimou a necessidade anual de transplantes de córnea no Brasil em 18.765, já o número de transplantes realizados foi 14.943 3 . Porém, com a pandemia, esse número ficou ainda pior, já que ocorreu a diminuição do número de doadores. De acordo com o levantamento da Agência Brasileira de Transplantes de Órgãos (ABTO), os pacientes ativos em lista de espera para transplante de córnea, nos primeiros seis meses de 2020, já eram mais de 12 mil 2 . A possibilidade de utilização de córneas de doadores que contraíram COVID-19 ainda está sendo discutida. Como há um elevado número de pessoas infectadas, a viabilidade das córneas estocadas de doadores não infectados por COVID-19 é ainda mais importante. A perda ou inviabilidade dos tecidos se torna uma preocupação na medida em que ficam indisponíveis, sendo a contaminação microbiológica um dos principais motivos de descarte de córneas em bancos de olhos 4 . Ao contrário da maior parte dos medicamentos utilizados na oftalmologia, dos quais se espera que aumentem a eficácia ao longo de anos de estudos, os antimicrobianos têm a eficácia diminuída pelo aumento da resistência de microrganismos 5 . Por esse motivo, é de extrema importância que se conheça o microbioma ocular, a fim de identificar a relação de proteção formada pela própria microbiota comensal 6 , entendimento da fisiopatologia de diversas doenças oftalmológicas 7 e identificar possíveis patógenos, responsáveis por infecções pós-transplante.
À medida que se compreende a relação complexa que se dá entre os microrganismos que compõem a microbiota ocular, é possível formular ações mais específicas de prevenção ou de tratamento. Como prevenção às infecções, antibióticos são utilizados junto aos meios de preservação usados em protocolos de armazenamento. Eles são adicionados no intuito de realizar a descontaminação das córneas, porém essas soluções não têm se mostrado 100% eficientes. No Brasil, os principais antimicrobianos utilizados em meios de preservação são a gentamicina e a estreptomicina 8 , mas estudos já mostram que diversas espécies bacterianas apresentam resistência a esses antibióticos 9 , 10 .
Até o momento, não há um protocolo que uniformize a utilização de meios de preservação, antimicrobianos mais eficientes, temperatura e tempo de estocagem de córneas. A realização de estudos comparando esses métodos se mostra necessária, pois o aprimoramento da metodologia poderá resultar em uma perda menor de material, assim como evitar que microrganismos do doador, ou que cresceram junto aos meios de preservação de córneas, sejam transmitidos aos receptores, já que isso pode causar endoftalmites graves e, até mesmo, a perda do globo ocular.
Este artigo de revisão teve como objetivo realizar levantamento sobre a microbiota ocular de doadores de córnea para verificar uma possível correlação com infecções pós-transplante, a fim de auxiliar futuros estudos sobre metodologias e protocolos de armazenamento de córneas no Brasil.
MÉTODO
Este trabalho foi realizado a partir de uma revisão da literatura, nas bases de dados: PubMed, Scientific Electronic Library Online (SciELO), Portal de Periódicos da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), Portal da Agência Nacional de Vigilância Sanitária (Anvisa), Ministério da Saúde e Associação Brasileira de Transplante de Órgãos (ABTO), no período compreendido entre 2018 e 2020. Os três primeiros portais citados foram utilizados para a busca de artigos científicos nacionais e internacionais, a partir das seguintes palavras-chave: “cornea transplant”, “corneal storage media”, “corneal preservation”, “eye banking”, “ocular microbiome”, “eye infections”. Para a busca de dados relacionados à COVID-19, por se tratar de uma literatura escassa até o momento da pesquisa, além dos portais anteriores, foram realizadas buscas no Google Acadêmico, utilizando as palavras-chave “SARS-CoV-2 corneal infection” e “COVID-19”. Os portais da Anvisa, do Ministério da Saúde e da ABTO foram utilizados para a coleta de dados livres, publicados pelo governo brasileiro e pela ABTO. Para a seleção de artigos, foram utilizados inicialmente critérios como o interesse para o tema e a data de publicação, a partir da leitura dos títulos. Após a leitura dos títulos dos artigos, notou-se que alguns deles se repetiram nas diferentes bases e que outros não preenchiam os critérios deste estudo. Após uma pré-seleção, foi avaliada a bibliografia utilizada no estudo, se estava atualizada, o delineamento dos experimentos e a relevância acerca do tema. Foram considerados artigos publicados em português, espanhol e inglês. Os textos foram então selecionados para leitura do resumo e excluídos os que não diziam respeito ao propósito deste estudo. Na seleção final, 87 artigos foram utilizados para a elaboração deste trabalho, sete deles da PubMed, quatro da SciELO, 68 selecionados a partir de buscas no Portal de Periódicos da CAPES e oito do Google Acadêmico. A partir da leitura completa dos artigos, foram retiradas as informações que conduziram à escrita deste trabalho.
RESULTADOS E DISCUSSÃO
Transplantes de córnea no Brasil
A córnea é a interface entre o olho e o ambiente externo. Além da função de proteção, é a principal superfície de refração do olho 11 . Quando a sua qualidade está comprometida, podem ocorrer diversos transtornos na visão, incluindo a sua perda completa. Dentre as principais causas da cegueira estão: catarata (51%), glaucoma (8%), degeneração macular relacionada à idade (5%), cegueira infantil e opacidade da córnea (4%), erros refrativos não corrigidos e tracoma (3%), retinopatia diabética (1%) e causas indeterminadas (21%) 12 . Pesquisas mostram que as doenças de córneas representam as principais causas das cegueiras reversíveis no mundo 12 , 13 e o transplante de córneas vem a ser um importante tratamento para recuperar a visão.
O Sistema Único de Saúde (SUS) brasileiro é responsável por coordenar o sistema de transplantes, que deve ser disponibilizado a toda população do país sem custos, universalizando o acesso aos transplantes e ao tratamento. A Política Nacional de Transplantes está disciplinada na Lei nº 9.434, de 4 de fevereiro de 1997, e Lei nº 10.211, de 23 de março de 2001. Os transplantes podem ser realizados por instituições públicas ou privadas, porém o procedimento deve ser gratuito, conforme disposto em lei.
O Ministério da Saúde divulga dados sobre o número total de transplantes realizados no país. Porém, apesar de o SUS coordenar o sistema de transplantes, não disponibiliza um banco de dados centralizado para acompanhamento após a realização dos procedimentos, dificultando a estimativa do número de transplantes de córneas bem-sucedidos.
A ABTO trouxe em sua última divulgação os dados de transplantes de córnea de janeiro a junho de 2020, onde foram realizados 3.963 transplantes, pouco mais da metade dos transplantes realizados no mesmo período do ano de 2019, 7.112 2 . A série histórica completa da ABTO 3 , com dados de 2012 a 2019, mostra a Região Sudeste com o maior número de transplantes de córnea em 2019, 7.558, sendo São Paulo o estado com o maior número de transplantes realizados (69,4%). Já a Região Sul realizou, no mesmo ano, 2.209 transplantes de córnea, e o Rio Grande do Sul representou 32,2% ( Figura 1 ).
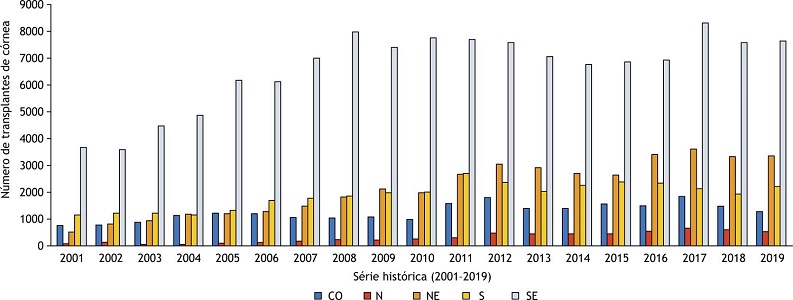
Figura 1
Série histórica do número de transplantes de córnea realizados no Brasil entre 2001 e 2019, nas seguintes Regiões: Centro-Oeste (CO); Norte (N); Nordeste (NE); Sul (S) e Sudeste (SE).
Fonte: Elaborada pelos autores, 2020, a partir de dados divulgados pelo Ministério da Saúde (2001 a 2017) e pela Associação Brasileira de Transplante de Órgãos (2012 a 2019).
O Rio Grande do Sul teve o maior número de transplantes realizados entre os anos 2011 e 2012, 918 e 882 transplantes de córnea, respectivamente ( Figura 2 ). Desde então, não tem mais atingido o número de transplantes realizados nos anos citados, tendo, em 2019, realizado 727 transplantes.
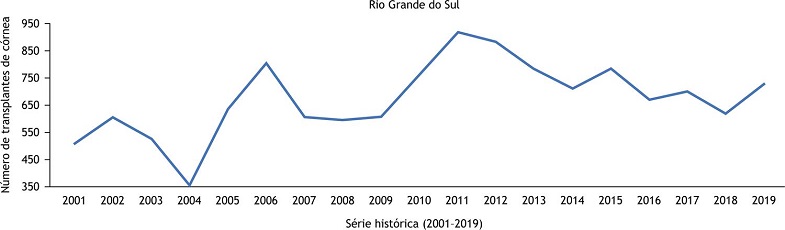
Figura 2
Série histórica do número de transplantes de córnea realizados no Rio Grande do Sul, entre 2001 e 2019.
Fonte: Elaborada pelos autores, 2020, a partir de dados divulgados pelo Ministério da Saúde (2001 a 2017) e pela Associação Brasileira de Transplante de Órgãos (2012 a 2019).
Apesar de o transplante de córneas ser o transplante de tecidos mais realizado no mundo 14 , a demanda de doações não está sendo suprida, principalmente pelo número insuficiente de doadores 15 . Os números da ABTO chamam atenção, no primeiro semestre de 2020 dentre os potenciais doadores de órgão do Rio Grande do Sul, apenas 31,56% foram realizados, ou seja, de 301 potenciais doadores, apenas 110 doadores efetivos e, desses, 95 cujos órgãos foram transplantados. Na lista de espera para doações de córnea encontram-se 12.234 pacientes ativos, os números variam muito por Estado. Em São Paulo existem 2.984 pacientes em lista de espera, já no Rio Grande do Sul, este número cai para 201. Segundo o Ministério da Saúde, dentre os motivos para o baixo número de efetivação nas doações está a negativa familiar (43%) manifestada em entrevistas com os familiares, porém, em 31% dos casos, os familiares não chegam a ser entrevistados. Os motivos para a não realização das entrevistas não foram divulgados pelo Ministério da Saúde, assim como não foram divulgados dados discriminando os tipos de doação.
Devido ao número insuficiente de doadores de córnea e às listas de espera, os Bancos de Olhos acabam tendo um papel fundamental não só na captação, mas principalmente, em dar boas condições de armazenamento e conservação para posterior efetivação dos transplantes 16 . Estudos indicam que, mesmo após a autorização para doação, uma grande parcela das córneas é descartada e não há a efetivação do transplante. Em estudo realizado no estado do Paraná, entre os anos de 2011 e 2015, 45,6% das córneas doadas foram descartadas por diversos motivos e, no Brasil, esse número correspondeu a 29,5% 17 . Dentre os motivos do descarte estão, em maior número, a sorologia positiva, a viabilidade e a qualidade da córnea e, em menor número, a contaminação do tecido ocular.
Microbiota da superfície ocular humana
A microbiota normal é definida como as espécies de microrganismos presentes na maioria dos indivíduos avaliados, em uma localização particular 18 . A conjuntiva, assim como margens da pálpebra e lágrimas, apresenta uma quantidade muito menor de espécies microbianas quando comparada a outras mucosas, como a superfície da mucosa oral. Mesmo em menor número, a superfície ocular está continuamente exposta ao ambiente e a diferentes espécies de microrganismos 19 . O desequilíbrio na microbiota normal ou a inserção de espécies transitórias pode ter como consequência o aparecimento de algumas doenças 20 .
A microbiota da superfície ocular pode ser alterada por diversos fatores: ambientais, doenças, uso de antibióticos 21 , 22 , dentre outros. A síndrome do olho seco tem sido constantemente associada às condições inflamatórias da superfície ocular 23 , pois a lubrificação realizada pela lágrima, que contém compostos antimicrobianos 24 , contribui para que poucas espécies de microrganismos se estabeleçam na mucosa ocular.
Estudos baseados em métodos dependentes de cultivo têm mostrado uma predominância de bactérias Gram-positivas presentes na conjuntiva humana, especialmente Staphylococcus coagulase negativa (SCN), isoladas em 20% a 80% dos swabs de conjuntiva e em 30% a 100% dos swabs de pálpebras; assim como os gêneros Streptococcus, Corynebacterium e Propionibacterium ( P. acnes ) 18 , 19 , 22 , 25 , 26 , 27 , 28 e, com menor ocorrência, S. aureus, Micrococcus sp., Bacillus sp. Enterococcus sp., Lactobacillus sp. 19 . Também, embora em menor número, bactérias Gram-negativas, tais como: Haemophilus sp., Neisseria sp. 22 , Pseudomonas aeruginosa, Enterobacter sp, Escherichia coli, Proteus sp. e Acinetobacter sp. 19 , 29 , 30 , 31 , 32 , assim como alguns grupos de fungos 19 . Já nas pálpebras e/ou lágrimas podem ser encontrados, em maior frequência, SCN, como também Propionibacterium sp. , Corynebacterium sp., S. aureus, Micrococcus sp. e Streptococcus sp. Novamente, em menor número, bactérias Gram-negativas, tais como: Moraxella sp., Pseudomonas sp., Neisseria sp. e Proteus sp. 19 .
Nos últimos anos, houve uma intensificação da utilização de métodos de identificação independentes de cultivo, como a reação em cadeia da polimerase (PCR) e o sequenciamento utilizando o gene 16S rRNA. Através dessa nova abordagem, outros gêneros estão sendo identificados como possíveis colonizadores da conjuntiva ocular 20 . Dentre os gêneros encontrados por pesquisadores através de técnicas independentes de cultivo e não citados acima, estão: Millisia, Anaerococcus, Finegoldia, Simonsiella, Veillonella20 , Bradyrhizobium, Brevundimonas, Aquabacterium, Sphingomonas, Streptophyta e Methylobacterium33 .
No mesmo estudo, Dong et al. 28 apresentaram 12 gêneros bacterianos constituindo o microbioma da conjuntiva, ordenados por frequência: Pseudomonas sp. (20%), Propionibacterium (20%), Bradyrhizobium (16%), Corynebacteria (15%), Acinetobacter (12%), Brevundomonas (5%), Staphylococcus (4%), Aquabacterium (2%), Sphingomonas (1%) e Streptococcus (1%). O gênero Pseudomonas é citado por outros estudos dentre os microrganismos mais abundantes da conjuntiva, por técnicas independentes de cultivo. Lee et al. 23 encontraram Pseudomonas, Elizabethkingia, Corynebacterium, Staphylococcus, Delftia, Propionibacterium e Streptococcus representando 63,6% das sequências. Novamente, Pseudomonas sp. foi a sequência mais abundante nos estudos de Zhou et al. 34 , seguido por Bradyrhizobium sp. e Acinetobacter sp.
A frequência de espécies apresentadas por métodos independentes de cultivo, nesses estudos, surpreende na medida em que o gênero Pseudomonas aparece em elevada frequência, e não mais SCN, como em resultados apresentados por técnicas dependentes de cultivo. Bactérias Gram-negativas são as menos abundantes por isolamento e identificação de gêneros bacterianos por métodos dependentes de cultivo. Os diferentes locais do olho apresentam microbiota diferenciada onde Pseudomonas sp. se mostrou mais frequente, nas pálpebras e na conjuntiva, porém não é tão frequentemente encontrada na superfície ocular 35 .
A metodologia de análise dependente de cultivo, acaba favorecendo microrganismos com crescimento mais rápido e menos fastidiosos 33 , 36 , 37 . Os meios de cultivo, assim como as condições de crescimento fazem uma seleção de espécies, o que não ocorre em métodos independentes de cultivo. Estima-se que apenas 1% dos microrganismos sejam cultiváveis por técnicas de rotina 38 . Além da metodologia, condições ambientais, sazonalidade e faixa etária podem ser fatores importantes na diferença dos dados apresentados 21 , 22 , 34 . Nos estudos avaliados, não houve diferença estatística na microbiota ocular entre homens e mulheres, mas essa diferença aparece entre faixas etárias avaliadas 28 , 33 .
A introdução de técnicas independentes de cultivo e de análises de metagenômica mostrou uma microbiota ocular mais parecida com a da pele, e não com a de outras mucosas, como a boca e garganta 39 . Estudos inferem que o microbioma ocular pode ter se desenvolvido como resultado de interações físicas entre a pele nas margens das pálpebras ou os dedos com a superfície ocular 31 , 40 , assim como partículas de poeira, água, pólen etc. É importante definir quais os microrganismos são transitórios e possíveis causadores de distúrbios na composição do microbioma e quais são comensais e contribuem para a manutenção desse equilíbrio 20 .
Microbiota relacionada a infecções oculares
Apesar de ser conhecido que a microbiota normal auxilia na proteção do olho, algumas espécies presentes na conjuntiva contribuem com o aparecimento de doenças infecciosas e autoimunes do olho, tais como: ceratite, conjuntivite, endoftalmite e síndrome do olho seco 19 . Por esse motivo, é importante conhecer e distinguir a microbiota comensal da microbiota transitória. Mesmo com o aumento de estudos utilizando técnicas mais sensíveis, não há consenso sobre quantos filotipos realmente contribuem para o equilíbrio microbiano ocular e compõem a microbiota normal, assim como não se sabe exatamente qual a relação da adição ou exclusão de espécies 20 .
Até 82% das endoftalmites pós-cirúrgicas em pacientes que reverteram cataratas podem ser causadas pela microbiota ocular 41 . Bactérias são os principais agentes causadores de endoftalmites e os patógenos Gram-positivos responsáveis por 60% a 80% das infecções agudas, sendo SCN o microrganismo mais comumente isolado 6 , 42 , 43 e, em menor quantidade, cocos Gram-positivos e P. acnes43 . Em estudos que avaliaram 55 casos de endoftalmite acometidos após transplante de córnea, 44 foram de origem bacteriana com cultura comprovada, sendo o mesmo microrganismo isolado do receptor e do doador em 56,8% dos casos 44 . Esses dados ressaltam a importância de se compreender e monitorar a distribuição de microrganismos e infecções oculares e a sua resistência a antimicrobianos para melhor adequar o tratamento pré, peri e pós-operatório 6 . O aumento da incidência de infecções fúngicas pós-transplantes de córneas também aponta para a necessidade de revisão de métodos de seleção de material 45 .
Bactérias Gram-negativas são muito comuns na superfície ocular de pessoas que utilizam lentes de contato 46 , sendo que o gênero Pseudomonas aparece dentre as bactérias mais abundantes 47 , assim como aparece, também, na microbiota da superfície de pessoas saudáveis, em análises realizadas através de técnicas independentes de cultivo. Outros gêneros bacterianos, incluindo bactérias Gram-positivas, também são relatados como presentes no microbioma de usuários de lentes de contato, são eles: Methylobacterium, Lactobacillus e Acinetobacter e, em menor número, Haemophilus, Streptococcus, Staphylococcus e Corynebacterium spp 47 . Sabe-se que o risco de infecções em usuários de lentes de contato é aumentado pela falta de contato com o filme lacrimal e de proteínas antimicrobianas presentes nele, mas também pela fricção mecânica na superfície ocular que, hoje se sabe, não é estéril, ao contrário, apresenta uma grande quantidade de microrganismos.
Em estudo avaliando Gram ou culturas positivas em doadores de tecidos de córnea relacionados com casos de infecção pós-transplante, de 46 resultados positivos, 42 isolados foram por bactérias, dois por Candida , um por Acanthamoeba e um por levedura de brotamento inespecífica. Dentre as espécies bacterianas, 11 foram por SCN, oito foram por P. acne s e, em menor número, Enterococcus faecalis, E. coli, Peptostreptococcus anaerobius, P. aeruginosa, Streptococcus viridans . Porém, foi possível correlacionar a infecção no receptor da córnea, apenas para Candida48 . Os resultados encontrados pelos autores corroboram com outros estudos, já citados, nos quais há prevalência dessas espécies em métodos dependentes de cultivo, porém, deve-se levar em consideração as limitações implicadas pela metodologia. O estudo também apresentou dez culturas positivas, apenas com resultados de coloração de Gram, não tendo os gêneros ou espécies sido identificados e não sendo possível correlacionar os agentes com infecções posteriores. Outros estudos de caso também relataram a transmissão de Candida sp. do doador para o hospedeiro 45 , 49 , 50 .
Farrel et al. 9 avaliaram 446 tecidos de córnea, e 14,1% dos crescimentos em cultura foram positivos. As espécies mais abundantes foram: Streptococcus (41%), Propionibacterium (23%) e Staphylococcus (22%), sendo a maior parte das espécies resistentes à gentamicina 9 . Apesar de o artigo não relacionar as espécies encontradas às endoftalmites nos receptores, os autores inferiram que conhecer os agentes patogênicos serve para selecionar antibióticos para uso na cirurgia e, também, no período pós-operatório, assim como para modificar os meios de preservação em bancos de olhos, já que a maior parte das espécies encontradas era resistente à gentamicina.
Os estudos que relacionam os agentes infecciosos presentes em doadores às endoftalmites em receptores foram todos desenvolvidos com técnicas que utilizam o cultivo de microrganismos. A maior parte dos estudos não encontra correlação entre doador e receptor, corroborando com os dados já mencionados 51 , 52 . No entanto, os isolados de amostras oculares não são necessariamente os agentes causadores de infecções oculares, já que ocorre simultaneamente a presença de diversas bactérias na superfície ocular 53 . Técnicas dependentes de cultivo, apesar de menos precisas, ainda são as mais utilizadas, pelo baixo valor da análise e pela facilidade em se obter resultados, já que técnicas mais robustas dependem de sequenciamento e análises de bioinformática.
A presença de agentes patogênicos na cultura aumenta a probabilidade de endoftalmites em até 1%, já para fungos, poderia chegar a 1,23%, sendo que a identificação precoce do agente infeccioso permitiria a antecipação de um tratamento agressivo, o que poderia prevenir danos ou sequelas, como submeter o paciente a uma nova cirurgia 48 . Lembrando que as técnicas mais comumente utilizadas poderiam estar subestimando as espécies presentes 7 , portanto os agentes infecciosos não estariam aparecendo nas avaliações dos contaminantes. A diferença entre os resultados obtidos em cultura convencional e exames de biologia molecular poderia afetar resultados clínicos 53 .
Apesar da grande presença de bactérias como agentes patogênicos, o alto índice de infecções pelo novo SARS-CoV-2 se faz importante nesta discussão. Em setembro de 2020, os números chamam atenção: são quase 30 milhões de casos de COVID-19 e quase um milhão de mortos no mundo 54 . Atualmente as córneas afetadas por SARS-CoV-2 estão sendo descartadas, devido a sua alta transmissibilidade e possível presença na conjuntiva, podendo ocasionar infecção aos receptores 55 . Alguns estudos indicam uma baixa frequência de implicações preocupantes para a doação de tecidos da córnea, porém alguns casos relatados na China e Singapura demonstraram pacientes com sintomas oculares, como conjuntivites predominantemente em pacientes com doença sistêmica grave 56 , 57 , 58 , 59 , podendo ser detectado na lágrima ou secreções conjuntivais. Contudo, Ang et al. 60 e Desautels et al. 55 argumentaram que os sintomas oculares podem ter sido causados pelos ventiladores utilizados no tratamento.
Atualmente não há evidências de que o vírus SARS-CoV-2 possa infectar tecidos corneanos mais profundos em pacientes com COVID-19, mas os estudos ainda são baseados em observações em animais e in vitro61 , assim como ainda não se pode inferir que haja uma carga viral considerável no estroma e endotélio corneano, que possa causar riscos significativos aos receptores 62 , 63 . Ainda que Xia et al. 59 sugeriram que o SARS-CoV-2 possa ser transmitido através do olho, o estudo foi baseado em um número muito baixo de observações. Um estudo recente, publicado em agosto de 2020, avaliou cinco doadores de córneas quanto à expressão viral. Os epitélios corneano e conjuntival expressam ACE2, DC-SIGN/DC-SIGNR e TMPRSS2, sugerindo que a superfície ocular é uma rota potencial para a transmissão de SARS-CoV-2 e que o risco de transmissão viral com o transplante de córnea não pode ser descartado devido à presença de ACE2 no epitélio e endotélio da córnea 64 . A priori , suspeitava-se que o vírus se alojava superficialmente, portanto seria possível fazer a esterilização local com solução de Iodopovidona após a excisão do doador 65 , 66 , porém estudos recentes já demonstram resultados contrários. Claramente são necessários mais estudos para inferir se as córneas de doadores positivados para COVID-19 podem ou não ser utilizadas.
Seleção de córnea e meios de preservação
No Brasil, a Resolução n° 67, de 30 de setembro de 2008, da Anvisa, regulamenta as contraindicações na utilização de córneas doadas, tais como morte por sepse, soropositivos para HIV, hepatite viral aguda. Também diagnóstico positivo para raiva e outras doenças associadas a microrganismos, com o intuito de não transferir patógenos aos receptores. Mesmo em doadores em que a causa mortis ou o seu histórico não são contraindicados para a doação de córneas, a presença de microrganismos em olhos enucleados é inevitável, portanto, a avaliação do material é importantíssima para que os microrganismos não sejam levados do enxerto para o interior do olho receptor. Como controle da contaminação, o material enucleado recebe banho de imersão em colírio e, após, o material é armazenado em soluções contendo antibióticos. Estudos nos quais foram analisadas a conjuntiva de doadores mostraram uma contaminação de 40% a 100% antes de qualquer tratamento e preservação da córnea 25 , porém, mesmo após este tratamento, as córneas não se tornaram estéreis, podendo ainda carregar algum tipo de microrganismo.
No Brasil, a temperatura de armazenamento, assim como o tempo, são definidos pela Anvisa na Resolução nº 67/2008, que indica o armazenamento em refrigeradores com controle de temperatura de 2ºC a 8ºC. Essa metodologia é a mais difundida no mundo e a única utilizada na América do Norte 67 , e é relativamente eficiente e facilmente reproduzida em bancos de olhos. Já na maior parte dos bancos de olhos europeus, utilizam-se temperaturas de armazenamento das córneas, de 31ºC a 37ºC. Essa temperatura ofereceria vantagens quando comparada ao armazenamento a 4ºC, pois os microrganismos são metabolicamente mais ativos em temperaturas mais altas, aumentando a eficiência dos antimicrobianos e também o tempo de armazenamento pela viabilidade de células endoteliais 4 , 67 .
O tempo de armazenamento dos órgãos determina a metodologia escolhida. Para períodos mais longos, de até 48 dias, a temperatura recomendada é de 31ºC a 37ºC, já para períodos curtos, até 14 dias, a temperatura recomendada é de 4ºC 68 . Na maior parte do mundo, são utilizados períodos menores de armazenamento, por ter uma necessidade constante de doações, ou seja, a demanda é maior do que a quantidade de córneas disponíveis para doação. Isso explicaria a frequente utilização de temperaturas de armazenamento a 4ºC. O interessante em se utilizar períodos mais longos de armazenamento seria a possibilidade de fortalecer os testes de diagnósticos de patógenos, possíveis causadores de infecções, antes da realização do transplante 69 , porém, um problema de estocar córneas por um período mais longo pode vir a ser as possíveis alterações sofridas na composição do meio de estoque 70 .
Um estudo realizado na Nova Zelândia comparando meios de preservação de córneas mostrou o Optisol-GS com um tempo de estocagem ideal médio de 3,5 dias 71 , contrariando informações dos fabricantes, para os quais o tempo de utilização indicado é de até 14 dias. No Brasil, os meios de preservação de médio prazo utilizados são Optisol-GS (Bausch & Lomb, EUA) e o Eusol-C (Al.Chi.Mia, Itália), o tempo de preservação endotelial da córnea, para ambos, é de 14 dias, e 64% dos Bancos de Olhos no país utilizam soluções de preservação com gentamicina e estreptomicina 8 . Já na Europa, os antimicrobianos utilizados junto às soluções de armazenamento são, com mais frequência: penicilina, estreptomicina e anfotericina B 67 .
A utilização da estreptomicina junto à gentamicina, com o intuito de aumentar o espectro antimicrobiano contra bactérias contaminantes e diminuir a possibilidade do desenvolvimento de endoftalmites, foi introduzida no Optisol GS. Um problema da utilização do Optisol GS ou Optisol G, que tem somente gentamicina em sua composição, no Brasil, seria a temperatura de armazenamento utilizada, que é de 4ºC. A gentamicina e estreptomicina sofrem um decréscimo em sua atividade a 4ºC, quando comparada a 37ºC, além disso, seria necessário deixar a córnea em solução de estoque em temperatura ambiente por 3 h, antes da refrigeração 43 . Ainda, antes de realizar o procedimento cirúrgico, seria necessário deixar, mais uma vez, a córnea em temperatura ambiente, por cerca de 1 h 72 . Apesar disso, há relatos de que, após a introdução do meio Optisol GS, houve um decréscimo de 77% das endoftalmites causadas por bactérias, em comparação com fungos e um aumento de 3,4 vezes de endoftalmites, causadas por fungos quando o tempo de estocagem das córneas foi superior a 4 dias 73 .
A gentamicina se tornou um antibiótico amplamente utilizado nos meios de preservação de córneas em todo o mundo 10 , porém um estudo realizado ainda em 1991 mostrou que bactérias resistentes à gentamicina já eram encontradas nas córneas estocadas, mesmo que essas nem sempre estivessem relacionadas a infecções pós-transplante 9 . Embora o número comprovado de infecções pós-operatórias seja baixo, Eastlund 10 sugeriu que esses dados sejam pouco estudados, já que os pacientes que apresentam um quadro de infecção pós-operatório nem sempre retornam ao hospital ou ao profissional responsável pelo transplante. Há também a dificuldade de efetivar o isolamento do microrganismo presente na córnea do doador para comparar com o microrganismo causador da infecção pós-transplante. Esse acompanhamento é realizado em poucos casos, portanto esse dado poderia estar sendo subestimado. As contraindicações do uso de córneas de pacientes com morte por sepse, ventilação mecânica ou outra enfermidade, citadas na Resolução n° 67/2008, são justamente para evitar que patógenos sejam transmitidos junto com o tecido, como já foi comprovado por diversos estudos de caso 73 , 74 , 75 , 76 , 77 , 78 .
Os gêneros Streptococcus, Propionibacterium e Staphylococcus, assim como os difteróides, resistentes à gentamicina, são comumente encontrados nos meios de preservação 10 . Em estudo avaliando a cultura de córneas em meios de preservação com gentamicina e estreptomicina, foi relatado crescimento de microrganismos em 72,5% das amostras 25 , mostrando a ineficiência dos meios de preservação, quanto a descontaminação das córneas. O mesmo estudo mostrou que, dos 76 isolados identificados, 81,6% são bactérias Gram-positivas, por ordem de frequência: SCN, em 44,8% dos casos, Corynebacterium sp., em 19,7%, S. aureus , em 15,8% e Bacillus sp., em 1,3%. Lembrando que SCN é o microrganismo mais comumente isolado em endoftalmites 71 , 79 . Outro estudo, baseado em meios de preservação somente com gentamicina, apresentou 81% dos isolados sendo Streptococcus , 60% sendo Propionibacterium e 71% sendo Staphylococcus resistentes a esse antibiótico. O mesmo estudo mostrou que todos os isolados foram sensíveis à vancomicina 9 . Assim como um estudo de caso relatado por Khokhar et al. 80 indicou que a espécie Alcaligenes faecalis , resistente à vancomicina, foi responsável por infecção na córnea transplantada 80 .
Em estudo realizado no Hospital de Clínicas de Porto Alegre/RS, entre os anos de 2001 a 2003, analisando a positividade em halos doadores córneo-esclerais, preservados em Optisol GS, dos 63 halos analisados, 11 apresentaram culturas positivas e, desses, quatro foram por Staphylococcus epidermidis , um por S. aureus , um por Serratia sp e um por P. aeruginosa , todas resistentes à gentamicina 52 . Baer et al. 81 , ainda em 1988, encontraram S. viridans resistentes a esse antibiótico e relataram três casos de endoftalmites causadas por este patógeno 81 . Assim como em um estudo publicado por Fong et al. 82 , no qual não foram eliminados estafilococos, estreptococos e fungos. Para Broniek et al. 83 , a gentamicina não foi eficaz em inibir a replicação bacteriana durante o armazenamento da córnea, em estudo realizado com cultura bacteriana em córneas armazenadas em meio Eusol-C.
O tempo de armazenamento das córneas se mostra determinante no aumento do risco de contaminação 73 . Segundo alguns estudos, o risco de contaminação aumenta após 5 dias de armazenamento 84 , 85 , apesar de os meios de preservação como o Optisol-GS manterem as córneas com células endoteliais viáveis por até 14 dias a 4ºC 86 . A recomendação da Eye Bank Association of America (EBAA) é de que a enucleação do bulbo ocular seja realizada, preferencialmente, nas primeiras 6 h após o óbito. Já o reimplante tem como recomendação ideal que seja realizado em até 4 dias após a enucleação. Estudos comparando diferentes combinações de antibiótico e antifúngicos se mostram necessários, visando uma melhor efetividade na descontaminação de córneas para doação. Cada vez mais, ocorrem casos de bactérias resistentes a antimicrobianos, mesmo na comunidade onde as córneas para doação normalmente são capturadas. O aumento da resistência a antimicrobianos se torna um desafio, não só no tratamento de doenças causadas por microrganismos, mas também na descontaminação de órgãos para doação.
CONCLUSÕES
Os estudos baseados em técnicas independentes de cultivo mostram que há uma diversidade muito maior de bactérias que colonizam o globo ocular do que se pensava existir. Assim como que as bactérias presentes em maior frequência são do gênero Pseudomonas e não SCN, como nos resultados de estudos baseados em crescimento em meios de cultivo. Os antibióticos presentes nos meios de cultivo utilizados no Brasil, gentamicina e estreptomicina, já se mostram controversos, na medida em que muitas espécies bacterianas isoladas dos meios de preservação e de infecções pós-transplante são resistentes à gentamicina e algumas, resistentes à gentamicina e à estreptomicina. Há necessidade de se rever os antimicrobianos utilizados nos meios de preservação, seja por sua eficiência ou pelo grupo-alvo a ser atingido, já que estudos indicam a presença de uma grande quantidade de bactérias Gram-negativas no bioma ocular, pode levar ao desenvolvimento de um protocolo unificado para utilização no Brasil.
REFERÊNCIAS
Ministério da Saúde (BR). Painel coronavírus Brasil. Brasília: Ministério da Saúde; 2020[acesso 12 set 2020]. Disponível em: https://covid.saude.gov.br/
Associação Brasileira de Transplante de Órgãos – ABTO. Registro brasileiro de transplante: dados numéricos da doação de órgãos e transplantes realizados por estado e instituição no período: janeiro/junho 2020. São Paulo: Associação Brasileira de Transplante de Órgãos; 2020[acesso 12 set 2020]. Disponível em: https://site.abto.org.br/wp-content/uploads/2020/08/rbt-1sem-final-leitura.pdf
Associação Brasileira de Transplante de Órgãos – ABTO. Registro brasileiro de transplante: dimensionamento dos transplantes no Brasil e em cada estado (2012-2019). São Paulo: Associação Brasileira de Transplante de Órgãos; 2019[acesso 12 set 2020]. Disponível em: http://www.abto.org.br/abtov03/Upload/file/RBT/2019/RBT-2019-leitura.pdf
Gruenert AK, Rosenbaum K, Geerling G, Fuchsluger TA. The influence of donor factors on corneal organ culture contamination. Acta Ophthalmol. 2017;95(7):733-40. http://doi.org/10.1111/aos.13402
Ta CN, Chang RT, Singh K, Egbert PR, Shriver EM, Blumenkranz MS et al. Antibiotic resistance patterns of ocular bacterial flora. Ophthalmology. 2003;110(10):1946-51. http://doi.org/10.1016/s0161-6420(03)00735-8
Grzybowski A, Brona P, Kim SJ. Microbial flora and resistance in ophthalmology: a review. Graefes Arch Clin Exp Ophthalmol. 2017;255(5):851-62. https://doi.org/10.1007/s00417-017-3608-y
Petrillo F, Pignataro D, Lavano MA, Santella B, Folliero V, Zannella C et al. Current evidence on the ocular surface microbiota and related diseases. Microorganisms. 2020;8(7):1-13. https://doi.org/10.3390/microorganisms8071033
Pereira MLM, Santos AMC, Passos MC. Análise comparativa entre os bancos de olhos brasileiros: da preservação à distribuição da córnea doada. Rev Bras Oftalmol. 2002;61(3):169-72.
Farrell PL, Fan JT, Smith RE, Trousdale MD. Donor cornea bacterial contamination. Cornea. 1991;10(5):381-6. https://doi.org/10.1097/00003226-199109000-00004
Eastlund T. Bacterial infection transmitted by human tissue allograft transplantation. Cell Tissue Bank. 2006;7(3):147-66. https://doi.org/10.1007/s10561-006-0003-z
Niederkorn JY. Cornea: window to ocular immunology. Curr Immunol Rev. 2011;7(3):328-35. https://doi.org/10.2174/157339511796196593
Pascolini D, Mariotti SP. Global estimates of visual impairment: 2010. Br J Ophthalmol. 2012;96(5):614-8. https://doi.org/10.1136/bjophthalmol-2011-300539
Cruz GKP, Azevedo IC, Carvalho DPSRP, Vitor AF, Santos VEP, Ferreira Júnior MA. Clinical and epidemiological aspects of cornea transplant patients of a reference hospital. Rev Latino-Am Enfermagem. 2017;25:1-9. https://doi.org/10.1590/1518-8345.1537.2897
Robaei D, Watson S. Corneal blindness: a global problem. Clin Experiment Ophthalmol. 2014;42(3):213-4. https://doi.org/10.1111/ceo.12330
Gain P, Jullienne R, He Z, Aldossary M, Acquart S, Cognasse F et al. Global survey of corneal transplantation and eye banking. JAMA Ophthalmol. 2016;134(2):167-73. https://doi.org/10.1001/jamaophthalmol.2015.4776
Santos CG, Pacini KM, Adán CBD, Sato EH. Motivos do descarte de córneas captadas pelo banco de olhos do Hospital São Paulo em dois anos. Rev Bras Oftalmol. 2010;69(1):18-22. https://doi.org/10.1590/S0034-72802010000100004
Freitas RA, DellʼAgnolo CM, Melo WA, Andrade L, Pimentel RR, Pelloso SM et al. Do donated corneas become transplanted corneas? The causes of discard in southern Brazil. Cornea. 2019;38(4):419-25. https://doi.org/10.1097/ICO.0000000000001856
Kugadas A, Gadjeva M. Impact of microbiome on ocular health. Ocul Surf. 2016;14(3):3420-9. https://doi.org/10.1016/j.jtos.2016.04.004
Willcox MDP. Characterization of the normal microbiota of the ocular surface. Exp Eye Res. 2013;117:99-105. https://doi.org/10.1016/j.exer.2013.06.003
Huang Y, Yang B, Li W. Defining the normal core microbiome of conjunctival microbial communities. Clin Microbiol Infect. 2016;22(7):7-12. https://doi.org/10.1016/j.cmi.2016.04.008
Zegans ME, Van Gelder RN. Considerations in understanding the ocular surface microbiome. Am J Ophthalmol. 2014;158(3):420-2. https://doi.org/10.1016/j.ajo.2014.06.014
Miller D, Iovieno A. The role of microbial flora on the ocular surface. Curr Opin Allergy Clin Immunol. 2009;9(5):466-70. doi:10.1097/ACI.0b013e3283303e1b
Lee SH, Oh DH, Jung JY, Kim JC, Jeon CO. Comparative ocular microbial communities in humans with and without blepharitis. Invest Ophthalmol Vis Sci. 2012;53(9):5585-93. https://doi.org/10.1167/iovs.12-9922
McDermott AM. Antimicrobial compounds in tears. Exp Eye Res. 2013;117:53-61. https://doi.org/10.1016/j.exer.2013.07.014
Araújo MEXS, Scarpi MJ. Microbiota bacteriana da conjuntiva de doadores de córnea. Arq Bras Oftalmol. 2004;67(6):927-33. https://doi.org/10.1590/S0004-27492004000600016
Hamelin J, Fromin N, Tarnawski S, Teyssier-cuvelle S, Aragno M. nifH gene diversity in the bacterial community associated with the rhizosphere of Molinia coerulea, an oligonitrophilic perennial grass. Environ Microbiol. 2002;4(8):477-81. https://doi.org/10.1046/j.1462-2920.2002.00319.x
Tilman D, Cassman KG, Matson PA, Naylor R, Polasky S. Agricultural sustainability and intensive production practices. Nature. 2002;418(6898):671-7. https://doi.org/10.1038/nature01014
Doan T, Akileswaran L, Andersen D, Johnson B, Ko N, Shrestha A et al. Paucibacterial microbiome and resident DNA virome of the healthy conjunctiva. Invest Ophthalmol Vis Sci. 2016;57(13):5116-26. https://doi.org/10.1167/iovs.16-19803
Campos MS, Silva LQC, Rehder JR, Lee MB, O’Brien T, McDonnell PJ. Anaerobic flora of the conjunctival sac in patients with AIDS and with anophthalmia compared with normal eyes. Acta Ophthalmol (Copenh). 2009;72(2):241-5. https://doi.org/10.1111/j.1755-3768.1994.tb05023.x
Elander TR, Goldberg MA, Salinger CL, Tan JR, Levy B, Abbott RL. Microbial changes in the ocular environment with contact lens wear. CLAO J. 1992;18(1):53-5.
Graham JE, Moore JE, Jiru X, Moore JE, Goodall EA, Dooley JSG et al. Ocular pathogen or commensal: a PCR-based study of surface bacterial flora in normal and dry eyes. Investig Opthalmology Vis Sci. 2007;48(12):5616-23. https://doi.org/10.1167/iovs.07-0588
Hsu HY, Lind JT, Tseng L, Miller D. Ocular flora and their antibiotic resistance patterns in the midwest: a prospective study of patients undergoing cataract surgery. Am J Ophthalmol. 2013;155(1):36-44. https://doi.org/10.1016/j.ajo.2012.06.024
Dong Q, Brulc JM, Iovieno A, Bates B, Garoutte A, Miller D et al. Diversity of bacteria at healthy human conjunctiva. Investig Opthalmology Vis Sci. 2011;52(8):5408-13. https://doi.org/10.1167/iovs.10-6939
Zhou Y, Holland MJ, Makalo P, Joof H, Roberts CH, Mabey DCW et al. The conjunctival microbiome in health and trachomatous disease: a case control study. Genome Med. 2014;6(11):1-10. https://doi.org/10.1186/s13073-014-0099-x
Ozkan J, Willcox M, Wemheuer B, Wilcsek G, Coroneo M, Thomas T. Biogeography of the human ocular microbiota. Ocul Surf. 2019;17(1):111-8. https://doi.org/10.1016/j.jtos.2018.11.005
Woo PCY, Lau SKP, Teng JLL, Tse H, Yuen KY. Then and now: use of 16S rDNA gene sequencing for bacterial identification and discovery of novel bacteria in clinical microbiology laboratories. Clin Microbiol Infect. 2008;14(10):908-34. https://doi.org/10.1111/j.1469-0691.2008.02070.x
Burns DG, Camakaris HM, Janssen PH, Dyall-Smith ML. Combined use of cultivation-dependent and cultivation-independent methods indicates that members of most haloarchaeal groups in an Australian crystallizer pond are cultivable. Appl Environ Microbiol. 2004;70(9):5258-65. https://doi.org/10.1111/j.1469-0691.2008.02070.x
Amann RI, Ludwig W, Schleifer KH. Phylogenetic identification and in situ detection of individual microbial cells without cultivation. Microbiol Rev. 1995;59(1):143-69. https://doi.org/10.1128/mr.59.1.143-169.1995
Grice EA, Kong HH, Renaud G, Young AC, Bouffard GG, Blakesley RW et al. A diversity profile of the human skin microbiota. Genome Res. 2008;18(7):1043-50. https://doi.org/10.1101/gr.075549.107
Berry M, Harris A, Lumb R, Powell K. Commensal ocular bacteria degrade mucins. Br J Ophthalmol. 2002;86(12):1412-6. https://doi.org/10.1136/bjo.86.12.1412
Speaker MG, Milch FA, Shah MK, Eisner W, Kreiswirth BN. Role of external bacterial flora in the pathogenesis of acute postoperative endophthalmitis. Ophthalmology. 1991;98(5):639-50. https://doi.org/10.1016/s0161-6420(91)32239-5
Gray ND, Miskin IP, Kornilova O, Curtis TP, Head IM. Occurrence and activity of archaea in aerated activated sludge wastewater treatment plants. Environ Microbiol. 2002;4(3):158-68. https://doi.org/10.1186/1471-2180-12-140
Durand ML. Endophthalmitis. Clin Microbiol Infect. 2013;19(3):227-34. https://doi.org/10.1111/1469-0691.12118
Kloess PM, Stulting RD, Waring GO, Wilson LA. Bacterial and fungal endophthalmitis after penetrating keratoplasty. Am J Ophthalmol. 1993;115(3):309-16. https://doi.org/10.1016/s0002-9394(14)73580-9
Tsui E, Fogel E, Hansen K, Talbot EA, Tammer R, Fogel J et al. Candida interface infections after descemet stripping automated endothelial keratoplasty. Cornea. 2016;35(4):456-64. https://doi.org/10.1097/ico.0000000000000778
Boost M, Cho P, Wang Z. Disturbing the balance: effect of contact lens use on the ocular proteome and microbiome. Clin Exp Optom. 2017;100(5):459-72. https://doi.org/10.1111/cxo.12582
Zhang H, Zhao F, Hutchinson DS, Sun W, Ajami NJ, Lai S et al. Conjunctival microbiome changes associated with soft contact lens and orthokeratology lens wearing. Investig Opthalmology Vis Sci. 2017;58(1):128-36. https://doi.org/10.1167/iovs.16-20231
Garg S, Said B, Farid M, Steinert RF. Prevalence of positive microbiology results from donor cornea tissue in different methods of corneal transplantation. Cornea. 2013;32(2):137-40. https://doi.org/10.1097/ICO.0b013e3182542368
Villarrubia A, Cano-Ortiz A. Candida keratitis after descemet stripping with automated endothelial keratoplasty. Eur J Ophthalmol. 2014;24(6):964-7. https://doi.org/10.5301/ejo.5000499
Koenig SB, Wirostko WJ, Fish RI, Covert DJ. Candida keratitis after descemet stripping and automated endothelial keratoplasty. Cornea. 2009;28(4):471-3. https://doi.org/10.1097/ICO.0b013e31818ad9bc
Gomes JAP, Dana MR, Dua HS, Goren MB, Laibson PR, Cohen EJ. Positive donor rim culture in penetrating keratoplasty. Cornea. 1995;14(5):457-62.
Borowsky CM, Wallau AD, Reetz A, Kwitko S, Rymer S, Locatelli CI. Contaminação de halos doadores córneo-esclerais em ceratoplastia penetrante no Hospital de Clínicas de Porto Alegre. Arq Bras Oftalmol. 2008;71(1):13-7. https://doi.org/10.1590/S0004-27492008000100003
Eguchi H, Hotta F, Kuwahara T, Imaohji H, Miyazaki C, Hirose M et al. Diagnostic approach to ocular infections using various techniques from conventional culture to next-generation sequencing analysis. Cornea. 2017;36(Supl.1):S46-S52. https://doi.org/10.1097/ICO.0000000000001338
World Helth Organization – WHO. WHO coronavirus disease (COVID-19) dashboard. Geneva: World Helth Organization; 2020[acesso 12 set 2020]. Disponível em: https://covid19.who.int/
Desautels JD, Moshirfar M, Martheswaran T, Shmunes KM, Ronquillo YC. Risks posed to corneal transplant recipients by COVID-19-affected donors. Ophthalmol Ther. 2020;9(3):371-9. https://doi.org/10.1007/s40123-020-00254-w
Wu P, Duan F, Luo C, Liu Q, Qu X, Liang L et al. Characteristics of ocular findings of patients with coronavirus disease 2019 (COVID-19) in Hubei Province, China. JAMA Ophthalmol. 2020;138(5):575-8. https://doi.org/10.1001/jamaophthalmol.2020.1291
Guan W, Ni Z, Hu Y, Liang W, Ou C, He J et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020;382(18):1708-20. https://doi.org/10.1056/NEJMoa2002032
Seah IYJ, Anderson DE, Kang AEZ, Wang L, Rao P, Young BE et al. Assessing viral shedding and infectivity of tears in coronavirus disease 2019 (COVID-19) patients. Ophthalmology. 2020;127(7):977-9. https://doi.org/10.1016/j.ophtha.2020.03.026
Xia J, Tong J, Liu M, Shen Y, Guo D. Evaluation of coronavirus in tears and conjunctival secretions of patients with SARS-CoV-2 infection. J Med Virol. 2020;92(6):589-94. https://doi.org/10.1002/jmv.25725
Ang M, Moriyama A, Colby K, Sutton G, Liang L, Sharma N et al. Corneal transplantation in the aftermath of the COVID-19 pandemic: an international perspective. Br J Ophthalmol. 2020;104(11):1477-81. https://doi.org/10.1136/bjophthalmol-2020-317013
Belser JA, Rota PA, Tumpey TM. Ocular tropism of respiratory viruses. Microbiol Mol Biol Rev. 2013;77(1):144-56. https://doi.org/10.1128/MMBR.00058-12
Bayyoud T, Iftner A, Iftner T, Bartz-Schmidt KU, Rohrbach JM, Ueffing M et al. Absence of severe acute respiratory syndrome-coronavirus-2 RNA in human corneal tissues. Cornea. 2020;40(3):342-7. https://doi.org/10.1097/ICO.0000000000002479
Chaurasia S, Sharma N, Das S. COVID-19 and eye banking. Indian J Ophthalmol. 2020;68(6):1215-6. https://doi.org/10.4103/ijo.IJO_1033_20
Roehrich H, Yuan C, Hou JH. Immunohistochemical study of SARS-CoV-2 viral entry factors in the cornea and ocular surface. Cornea. 2020;39(12):1556-62. https://doi.org/10.1097/ICO.0000000000002509
Kampf G, Todt D, Pfaender S, Steinmann E. Persistence of coronaviruses on inanimate surfaces and their inactivation with biocidal agents. J Hosp Infect. 2020;104(3):246-51. https://doi.org/10.1016/j.jhin.2020.01.022
Eye Bank Association of America – EBAA. Procedures manual. Washington: Eye Bank Association of America; 2019[acesso 12 set 2020]. Disponível em: https://restoresight.org/wp-content/uploads/2019/11/EBAA-ProcMan-October-2019.pdf
Armitage WJ. Preservation of human cornea. Transfus Med Hemotherapy. 2011;38(2):143-7. https://doi.org/10.1159/000326632
Jeng BH. Preserving the cornea: corneal storage media. Curr Opin Ophthalmol. 2006;17(4):332-7. https://doi.org/10.1097/01.icu.0000233950.63853.88
Frueh BE, Böhnke M. Prospective, randomized clinical evaluation of optisol vs organ culture corneal storage media. Arch Ophthalmol. 2000;118(6):757-60. https://doi.org/10.1001/archopht.118.6.757
Engelmann K, Ventura AS, Drexler D, Staude HJ. A sensitive method for testing the quality of organ culture media and of individual medium components in a cornea bank. Graefes Arch Clin Exp Ophthalmol. 1998;236(4):312-9. https://doi.org/10.1007/s004170050084
Patel HY, Brookes NH, Moffatt L, Sherwin T, Ormonde S, Clover GM et al. The New Zealand national eye bank study 1991-2003. Cornea. 2005;24(5):576-82. https://doi.org/10.1097/01.ico.0000155035.55751.b2
Lass JH, Gordon JF, Sugar A, Norden RA, Reinhart WJ, Meyer RF et al. Optisol containing streptomycin. Am J Ophthalmol. 1993;116(4):503-4. https://doi.org/10.1016/S0002-9394(14)71413-8
Hassan SS, Wilhelmus KR. Eye-banking risk factors for fungal endophthalmitis compared with bacterial endophthalmitis after corneal transplantation. Am J Ophthalmol. 2005;139(4):685-90. https://doi.org/10.1016/j.ajo.2004.12.016
Gandhi SS, Lamberts DW, Perry HD. Donor to host transmission of disease via corneal transplantation. Surv Ophthalmol. 1981;25(5):306-10. https://doi.org/10.1016/0039-6257(81)90156-9
Leveille AS, McMullan FD, Cavanagh HD. Endophthalmitis following penetrating keratoplasty. Ophthalmology. 1983;90(1):38-9. https://doi.org/10.1016/S0161-6420(83)34601-7
Seedor JA, Stulting RD, Epstein RJ, Nay RE, Dreizen NG, Waring 3rd GO et al. Survival of corneal grafts from donors supported by mechanical ventilation. Ophthalmology. 1987;94(2):101-8. https://doi.org/10.1016/S0161-6420(87)33490-6
Spelsberg H, Reinhard T, Sengler U, Daeubener W, Sundmacher R. Organ-cultured corneal grafts from septic donors: a retrospective study. Eye (Lond). 2002;16(5):622-7. https://doi.org/10.1038/sj.eye.6700145
Robert PY, Camezind P, Drouet M, Ploy MC, Adenis JP. Internal and external contamination of donor corneas before in situ excision: bacterial risk factors in 93 donors. Graefes Arch Clin Exp Ophthalmol. 2002;240(4):265-70. https://doi.org/10.1007/s004170100322
Ciulla TA, Starr MB, Masket S. Bacterial endophthalmitis prophylaxis for cataract surgery. Ophthalmology. 2002;109(1):13-24. https://doi.org/10.1016/S0161-6420(01)00899-5
Khokhar DS, Sethi HS, Kumar H, Sudan R, Sharma N, Nayak N. Postkeratoplasty endophthalmitis by Alcaligenes faecalis: a case report. Cornea. 2002;21(2):232-3. https://doi.org/10.1097/00003226-200203000-00024
Baer JC, Verinder S, Nirankari MD, Dean S, Glaros MD. Streptococcal endophthalmitis from contaminated donor corneas after keratoplasty. Arch Ophthalmol. 1988;106(4):517-20. https://doi.org/10.1001/archopht.1988.01060130563037
Fong LP, Gladstone D, Casey TA. Corneo-scleral rim cultures: donor contamination a case of fungal endophthalmitis transmitted by K-Sol stored cornea. Eye (Lond). 1988;2(Pt.6):670-6. https://doi.org/10.1038/eye.1988.123
Broniek G, Langwińska-Wośko E, Sybilska M, Szaflik J, Szaflik JP, Wróblewska M. Prevalence of bacteria and fungi in samples of cornea preservation fluid. Arch Med Sci. 2018;14(3):541-6. https://doi.org/10.5114/aoms.2016.58927
Pels E, Vrensen GF. Microbial decontamination of human donor eyes with povidone-iodine: penetration, toxicity, and effectiveness. Br J Ophthalmol. 1999;83(9):1019-26. https://doi.org/10.1136/bjo.83.9.1019
Antonios SR, Cameron JA, Badr IA, Habash NR, Cotter JB. Contamination of donor cornea: postpenetrating keratoplasty endophthalmitis. Cornea. 1991;10(3):217-20. https://doi.org/10.1097/00003226-199105000-00006
Kanavi MR, Javadi MA, Chamani T, Fahim P, Javadi F. Comparing quantitative and qualitative indices of the donated corneas maintained in Optisol-GS with those kept in Eusol-C. Cell Tissue Bank. 2015;16(2):243-7. https://doi.org/10.1007/s10561-014-9466-5
Autor notes
Reali C - Concepção, planejamento (desenho do estudo), aquisição, análise, interpretação dos dados e redação do trabalho. Pagnussato F, Geimba MP – Concepção, planejamento (desenho do estudo), aquisição, análise e interpretação dos dados. Todos os autores aprovaram a versão final do trabalho.
Os autores informam não haver qualquer potencial conflito de interesse com pares e instituições, políticos ou financeiros deste estudo.
* E-mail: catiuscar@gmail.com
