ARTIGO
Análise das notificações de queixas técnicas e das medidas preventivas de fiscalização sanitária, aplicadas durante a pandemia da COVID-19 no Brasil
Analysis of notifications of technical complaints and preventive health inspection measures applied during the COVID-19 pandemic in Brazil
Análise das notificações de queixas técnicas e das medidas preventivas de fiscalização sanitária, aplicadas durante a pandemia da COVID-19 no Brasil
Vigilância Sanitária em Debate, vol. 11, pp. 1-11, 2023
INCQS-FIOCRUZ
Recepção: 02 Maio 2022
Aprovação: 02 Maio 2023
RESUMO
Introdução: O consumo de medicamentos falsificados, não registrados e fora do padrão é um grave problema de saúde pública, sendo fundamental conhecer as ações legais de fiscalização sanitária durante a pandemia no Brasil.
Objetivo: Analisar as notificações de queixas técnicas e as medidas preventivas de fiscalização sanitária, aplicadas durante a pandemia da COVID-19, no Brasil.
Método: Estudo descritivo, quantitativo, retrospectivo com dados das notificações de queixas técnicas e das medidas determinadas pela Agência Nacional de Vigilância Sanitária (Anvisa), no intervalo de 2019 a junho de 2021. As notificações foram obtidas por meio da Lei de Acesso à Informação, enquanto as medidas preventivas foram coletadas no portal da Anvisa, com a validação dos dados no site da imprensa nacional.
Resultados: Foram registradas 25.088 notificações de queixas técnicas de medicamentos e 562 medidas, sendo 314 com elevado potencial de causar sérios danos à saúde, incluindo óbito. A maioria dos produtos não registrados alegam propriedades farmacêuticas relativas à imagem corporal, à imunidade ou ditos “naturais” ou da Medicina Tradicional Chinesa. Dentre as medidas, 63,3% estavam voltadas para propaganda irregular e comércio eletrônico de medicamentos suspeitos. Em cerca de 59,3% das medidas, as empresas não tinham o Cadastro Nacional de Pessoa Jurídica na Receita Federal, o que dificulta a responsabilização legal do infrator. Quanto às ações de fiscalização, as mais frequentes foram: apreensão (322), inutilização (305) e proibição (376). Quanto às medidas de proibição, as mais citadas se relacionam à pós-produção no ciclo produtivo, incluindo distribuição, comercialização e uso. Observa-se que a frequência observada de medicamentos segundo a classificação de risco é significativamente diferente para as várias ações fiscalizatórias (p < 0,001).
Conclusões: Faz-se necessário desenvolver estratégias voltadas à prevenção, detecção e resposta às práticas irregulares/ilícitas, mediante revisão do marco regulatório e do modelo de atuação; maior responsabilização das empresas; mecanismos de rastreabilidade; ações fiscalizatórias efetivas e aprimoramento das medidas adotadas pela Anvisa para proteger a saúde da população.
Palavras chave: Vigilância de Produtos Comercializados+ farmacovigilância+ vigilância Sanitária+ apreensão de Produtos.
ABSTRACT
Introduction: The consumptio of falsified, unregistered, and substandard medicines is a serious public health problem, and it is essential to know the legal enforcement actions related that were taken during the pandemic in Brazil.
Objective: To Analyze notifications of technical complaints and preventive health measures applied during the Covid-19 pandemic in Brazil.
Method: Descriptive, quantitative, retrospective study with data from notifications of technical complaints and measures determined by the National Health Surveillance Agency (Anvisa), from 2019 to June 2021.
Results: 25,088 notifications of technical complaints about medicines and 562 measures were identified. 314 were classified as class I risk, with high potential to cause serious injury to health, including death. Most unregistered products claim pharmaceutical properties regarding body image, immunity, or information as being “natural” or Traditional Chinese Medicine (TCM). There were 63.3% of actions for advertising and irregular commerce of medicines on the internet. There were 333 measures (59.3%) with an unknown/non-existent company associated, making it impossible to legally hold the offender responsible. The type of enforcement activities the most frequent were: seizure (322), destruction (305) and prohibition (376). The most cited stages of the chain related to post-production, included distribution, commercialization and use. It was observed that the frequency of risk classification of medicines is significantly different with enforcement actions (p < 0.001).
Conclusions: It is important to: develop strategies aimed at preventing, detecting, and responding to irregular/illegal practices, by reviewing the legal regulatory and the framework; and have greater corporate accountability, traceability mechanisms, effective inspection actions and improvement of the measures adopted by Anvisa to protect the population’s health.
Keywords: Post-Market Product Surveillance, pharmacovigilance, health Surveillance, products Retention.
INTRODUÇÃO
A Organização Mundial da Saúde (OMS) 1 alertou por meio de estudo realizado entre 2013–2017 sobre o impacto na economia e na saúde pública do consumo de produtos médicos fora do padrão, falsificados e não registrados. Nesse estudo, foram identificadas mais de 1,5 mil notificações, sendo os antimaláricos e antibióticos os mais relatados, configurando um problema mundial que afeta todos os sistemas regulatórios e traz sérias consequências à saúde e prejuízos econômicos aos países 2. A OMS propõe que sejam desenvolvidas ações que possam prevenir, detectar e responder de forma efetiva à comercialização de produtos farmacêuticos fora do padrão, falsificados e não registrados 2.
No Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) coordena o sistema regulatório e, dentre suas atribuições, é responsável pelo controle sanitário de medicamentos no país, incluindo autorização/registro, monitoramento e fiscalização, podendo aplicar medidas que interrompam o risco, como apreensão ou proibição da fabricação, propaganda e comercialização de produtos potencialmente nocivos à saúde da população 3.
A Anvisa registra e investiga as notificações de queixas técnicas (QT) de produtos, entendidas como qualquer relato de suspeita de irregularidade sanitária de um produto relacionado à sua qualidade, segurança ou eficácia na pós-comercialização 4, 5. Todos os produtos falsificados, os não registrados pela autoridade reguladora nacional (ARN) e aqueles que estão fora das especificações ou do padrão estabelecido compõem o universo das notificações de QT. Embora os medicamentos fora do padrão estejam regularizados, podem apresentar algum problema nos parâmetros de qualidade ou falhas nos processos produtivos como fabricação, embalagem, armazenamento ou transporte 2, 6. Neste sentido, a Anvisa entende como produto irregular todo aquele que esteja fora dos padrões ou que não observe a legislação sanitária e demais normas estabelecidas pela Agência 7.
No processo de triagem e investigação das QT, há a avaliação e a classificação de acordo com o grau de risco, considerando sua natureza, extensão e gravidade 4, 8. As notificações de Classe I (alto risco de causar sérios danos à saúde, incluindo óbito) recebem prioridade absoluta frente às demais, sendo as medidas preventivas voltadas à intervenção imediata na transmissão do risco sanitário. Mesmo que as demais classes tenham menor prioridade de análise, também é importante mencionar que a de Classe de Risco II envolve a situação na qual existe alta probabilidade de que o uso ou a exposição a um medicamento possa causar agravo temporário à saúde ou reversível por tratamento medicamentoso. E a de Classe de Risco III caracteriza-se como uma situação na qual existe baixa probabilidade de que o uso ou a exposição a um medicamento possa causar consequências adversas à saúde 8, 9.
A adoção das ações de fiscalização é priorizada conforme o grau de risco classificado na etapa da triagem e tem por base o arcabouço jurídico da década de 1970, como a Lei nº 6.360, de 23 de setembro de 1976 10, a Lei nº 6.437, de 20 de agosto de 1977 11, e as resoluções decorrentes, como a Resolução da Diretoria Colegiada (RDC) nº 55, de 17 de março de 2005 8.
Martins e Galato 12 identificaram que, no universo de todas as notificações recebidas pela Agência, no período de 2012 a 2017, houve predomínio das notificações de medicamentos (38,5%), com 46.818 QT, 1.919 dossiês de investigação e 851 medidas preventivas em que ao menos uma ação de fiscalização foi determinada pela Anvisa. Hall et al. 13também estudaram o controle sanitário de medicamentos falsificados, não registrados ou fora do padrão no contexto americano, identificando 3.045 medicamentos num universo de 21.120 recalls reportados pela Food and Drug Administration (FDA) no período entre junho de 2012 e dezembro de 2014 13.
Além disso, uma vez declarada a pandemia do COVID-19 14 e tendo sido aplicadas pela Anvisa 15as excepcionalidades aos requisitos específicos das boas práticas de fabricação (BPF) e de importação de medicamentos e insumos farmacêuticos, tornou-se ainda mais prioritário monitorar o comportamento dos medicamentos no mercado, bem como verificar possíveis alterações no perfil das QT e das ações de fiscalização no período.
Assim, este artigo objetivou analisar as notificações de QT e as medidas preventivas de fiscalização sanitária, aplicadas durante a pandemia da COVID-19, no Brasil.
MÉTODO
Trata-se de um estudo descritivo, baseado em dados da Anvisa, referentes às notificações de QT e às medidas preventivas de fiscalização sanitária, no período de 1 o de janeiro de 2019 a 30 de junho de 2021.
O acesso aos dados das notificações de QT por ano foi realizado por meio da Lei de Acesso à Informação (LAI), utilizando a plataforma eletrônica Fala.BR 16, o sistema eletrônico integrado de ouvidoria e o acesso à informação (https://falabr.cgu.gov.br), sendo informado, oficialmente pela Anvisa, em setembro/outubro de 2021.
As notificações de QT passam pelo processo de triagem, investigação e, se comprovada a irregularidade, se aplica uma medida preventiva publicada no Diário Oficial da União (DOU) (www.gov.br/imprensanacional/pt-br), por meio de Resolução Específica (RE). Segundo o regimento interno da Anvisa 17, a resolução é um instrumento que expressa a decisão administrativa para fins de autorização, homologação, certificação, cancelamentos, interdição e aplicação de penalidades previstas na legislação sanitária. Nesta pesquisa, a resolução foi considerada como publicação da tomada de decisão da Anvisa 17 para vigência imediata de medidas de recolhimento, apreensão, proibição, suspensão de produtos potencialmente nocivos à saúde no mercado.
Os dados das medidas preventivas (RE) foram coletados diretamente no portal da Anvisa, no qual é possível, desde o final de 2018, a consulta, a identificação e a extração de informações sobre produtos irregulares no mercado 18.
Os tipos de irregularidades extraídas das publicações foram: medicamento não registrado, medicamento fora do padrão, medicamento falsificado, empresa sem autorização de funcionamento (AFE) e propaganda irregular de medicamentos, incluindo controlados com retenção de receita e cancelamento de registro.
Para melhor compreensão e análise das informações contidas nas medidas, adotou-se os seguintes conceitos da legislação sanitária referentes às ações de fiscalização determinadas pela Anvisa:
-
Apreensão e inutilização – ação destinada aos produtos falsificados, empresas sem autorização de funcionamento e produtos não registrados – Lei nº 6.360/1976 10 e Lei nº 9.782, de 26 de janeiro de 1999 3.
-
Proibição – ação determinada para falsificados, empresas sem autorização de funcionamento e produtos não registrados – Lei nº 9.782/1999 3 e Lei nº 6.437/1977 11.
-
Suspensão da importação, fabricação, distribuição, comercialização e uso de medicamentos/insumos – ações tomadas para produtos fora das especificações ou parâmetros de qualidade; com resultado insatisfatório na análise fiscal; produtos em contrariedade com o registro – Lei nº 6.360/1976 10 e Lei nº 9.782/1999 3.
-
Recolhimento de produtos – retirada ou remoção de produtos fora do padrão ou sem registro no mercado – Lei nº 6.360/1976 10e RDC nº 55/2005 8. Cabe destacar que há informações publicadas sobre o recolhimento voluntário realizado pelas empresas.
-
Suspensão/proibição/adequação da publicidade – ação realizada sobre a divulgação irregular dos produtos em diferentes mídias – Lei nº 6.360/1976 10 e Lei nº 9.782/1999 3.
É importante destacar que uma medida preventiva não se limita a uma única ação de fiscalização, podendo envolver mais de uma decisão técnica, variando conforme o caso investigado, as infrações sanitárias cometidas e os riscos potenciais envolvidos. Além disso, as medidas contra medicamentos fora do padrão se referem à parte dos produtos irregulares que tiveram suspensão ou recolhimento determinados pela Anvisa.
Foram identificadas 601 medidas preventivas de medicamentos emitidas pela Anvisa entre janeiro de 2019 e junho de 2021, excluídas 39 resoluções que se encontravam revogadas ou parcialmente revogadas, vencidas ou inativas. Foram incluídas no estudo somente as resoluções ativas, totalizando 562 medidas para análise e realizadas a verificação e a confirmação destas no portal da imprensa nacional. Houve medidas que não informavam quais os produtos e traziam termos como “todos” ou “vários”, sendo contabilizado apenas uma unidade do produto, nestes casos.
Os seguintes dados foram coletados: número da resolução; tipo de irregularidade; classificação de risco; identificação da empresa responsável pela irregularidade, podendo ser fabricante, marketplace, distribuidora, transportadora ou comerciante; medicamentos e websites; indicações ou alegações terapêuticas e ações legais (medidas) de fiscalização determinadas pela Anvisa.
Os dados foram inseridos em planilhas do Microsoft Excel® e analisados no programa Jamovi® v.3 de estatística descritiva, neste caso sendo apresentadas as variáveis numéricas em medidas de tendência central e dispersão e as variáveis categóricas em números absolutos e proporções. Para determinar se houve mudança no perfil das medidas preventivas durante o período observado, foi adotado o Teste do Qui-quadrado para comparar proporções, considerando-se significativo os valores de p < 0,05.
Foram respeitados todos os aspectos éticos da pesquisa com dados secundários, neste caso a Resolução do Conselho Nacional de Saúde n° 510 de 7 de abril de 2016 19, sendo que as análises e as opiniões são de total responsabilidade dos autores, não representando necessariamente a posição oficial da agência reguladora.
RESULTADOS
No período analisado, foram registradas 25.088 notificações de QT de medicamentos, sendo 6.328 em 2019, 5.860 em 2020 e 12.900 até junho de 2021, incluindo vacinas ( Figura 1). É possível observar que no primeiro semestre de 2021 houve um aumento de 120% das notificações, quando comparado com todo ano de 2020.
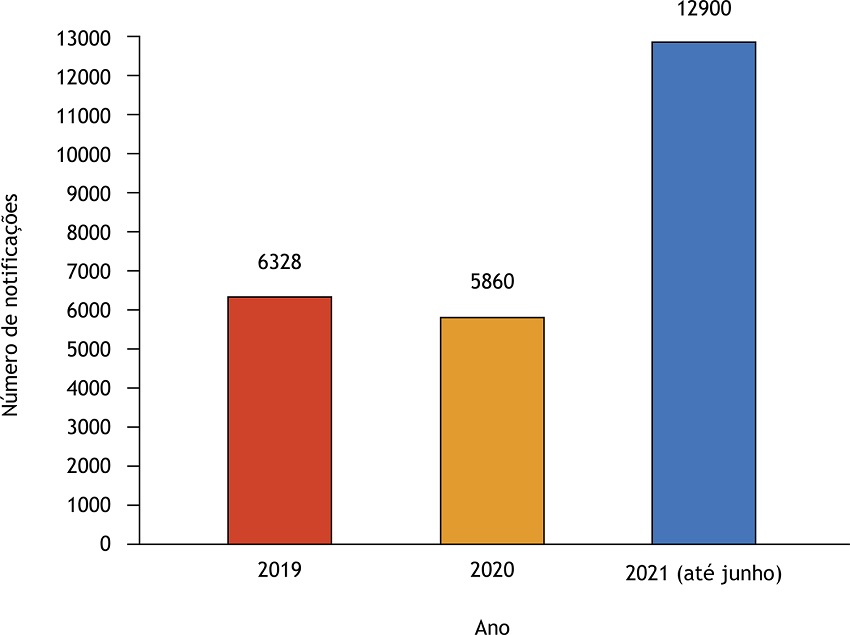
Figura 1
Número de notificações de queixas técnicas de medicamentos registradas pela Anvisa, entre janeiro de 2019 a junho de 2021 (N = 25.088).
Fonte: Dados disponibilizados pela Anvisa, por meio da Lei de Acesso à Informação (LAI), 2021.
No universo das 562 medidas preventivas de fiscalização analisadas, 169 foram publicadas em 2019; 256 em 2020 e 138 até junho de 2021. Tais medidas envolveram um ou mais medicamentos (máximo de 69 em cada medida), totalizando aproximadamente 2.035 produtos irregulares (média 3,6; SD 7,4: mediana 1,0), com média de 678 produtos potencialmente nocivos dispostos ao consumo a cada ano. Em 37,9% das medidas preventivas, não havia o número do Cadastro Nacional de Pessoa Jurídica (CNPJ) da Receita Federal.
A Tabela 1 mostra os tipos de irregularidades segundo a classificação do risco sanitário, sendo 339 (60,3%) medidas de supostos medicamentos não registrados na Anvisa, 166 (29,5%) medicamentos fora do padrão e 33 (5,9%) medidas motivadas pelos falsificados. Com relação ao risco, 314 medidas estavam relacionadas a produtos classificados como Risco I (55,9%), 156 Risco II (27,7%) e 92 Risco III (16,4%). Note-se que a maioria dessas medidas foram classificadas como Risco I (p < 0,001).

Quanto às indicações ou alegações terapêuticas dos medicamentos não registrados, alguns alegam propriedades farmacêuticas relativas à imagem corporal, como emagrecedores e anabolizantes; ao aumento da imunidade ou trazem informações que buscam confundir o consumidor como sendo “produtos naturais” ou da Medicina Tradicional Chinesa (MTC).
Na análise das 339 medidas contra medicamentos não registrados, 336 trouxeram o registro de que estavam sendo comercializados em redes sociais, plataformas de comércio eletrônico ou farmácias online sem exigência de receita médica válida, dentre outros canais da internet.
A frequência das ações legais de fiscalização determinadas nas medidas preventivas por ano é apresentada na Tabela 2.
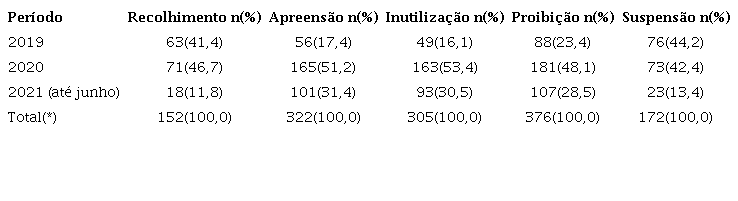
*a somatória dos itens é superior ao número de observações, pois uma mesma medida preventiva pode ter várias ações de fiscalização.
Com relação à Tabela 2, analisando detalhadamente o recolhimento, destacam-se os medicamentos fora do padrão ou desvios de qualidade. Nesses casos, a maior parte ocorreu de forma voluntária pela empresa, representando 44 (69,8%), 54 (76%) e 14 (77,8%) dos recolhimentos, respectivamente, nos anos de 2019, 2020 e 2021 (até junho). A contaminação por impurezas, conhecidas como “nitrosaminas”, representaram um terço (44/152) das medidas de recolhimento, sendo a maioria classificada como Risco II.
Dentre as ações de proibição, detalhadas na Figura 2A, destacam-se as proibições de comercialização, uso, distribuição e propaganda. Já na Figura 2B, entre as ações de suspensão, destacam-se as suspensões de comercialização, distribuição e uso.
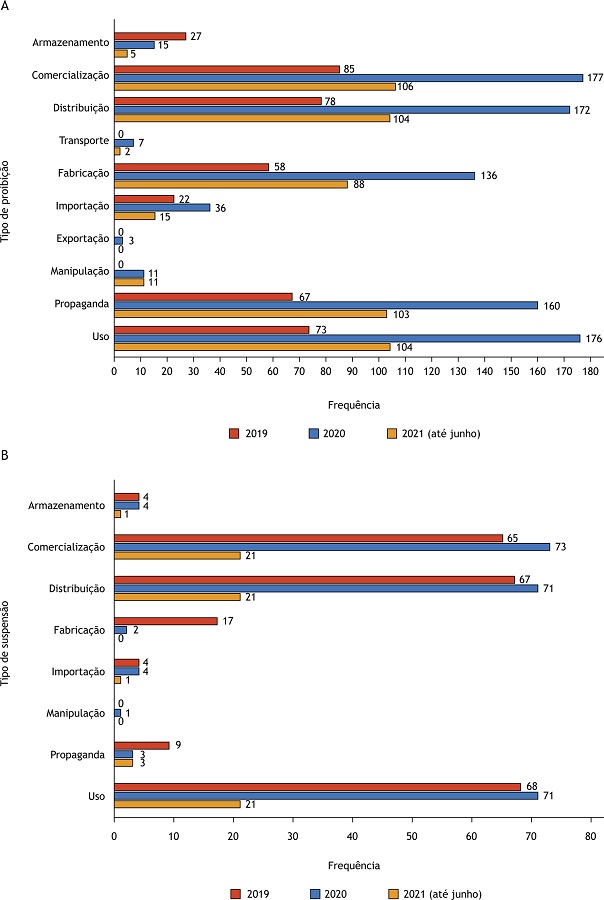
Figura 2
(A) Distribuição das ações de proibição de medicamentos por etapa da cadeia produtiva determinadas pela Anvisa, entre janeiro de 2019 e junho de 2021. (n = 376); (B) Frequência das ações de suspensão de medicamentos por etapa da cadeia produtiva determinada pela Anvisa, entre janeiro de 2019 e junho de 2021 (n = 172).
Fonte: Portal da Anvisa, 2021 17.
A Figura 2B, por sua vez, mostra que, de forma semelhante às proibições, as suspensões mais comuns são de uso, comercialização e distribuição e representam 160 (93,0%), 159 (92,4%) e 159 (92,4%) no período do estudo, respectivamente.
A Tabela 3 exibe a relação entre as ações de fiscalização determinadas pela Anvisa e a classificação do risco sanitário. Nota-se que há uma diferença significativa entre as frequências das ações de fiscalização e os riscos envolvidos. O recolhimento e a suspensão foram significativamente maiores para os medicamentos de menor risco (II e III) e as ações relacionadas à apreensão, inutilização e proibição significativamente mais frequentes para os produtos de maior risco (Risco I).
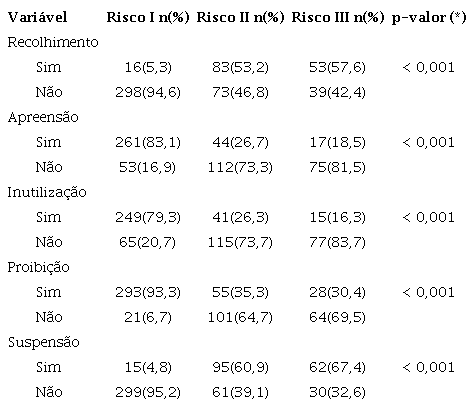
* Teste do Qui-quadrado.
DISCUSSÃO
Analisar as notificações de QT e as medidas preventivas faz parte de uma estratégia global da própria OMS 1 que possibilita monitorar os casos de medicamentos irregulares no mercado e conhecer as ações de fiscalização desenvolvidas pela Anvisa para proteger a saúde da população. Pode-se constatar que no universo dos medicamentos irregulares, há o predomínio dos medicamentos não registrados que são divulgados e comercializados na internet.
Os achados da presente pesquisa demonstram que houve aumento nas notificações de QT e das medidas preventivas no Brasil, acompanhando a tendência mundial, conforme relatório da OMS e dados da Organização Internacional de Polícia Criminal (Interpol) 1, 20. O quantitativo de medicamentos irregulares envolvidos nas ações fiscalizatórias teve um aumento na média anual de 255% em relação aos números apresentados em período anterior (2012–2017) conforme analisado por Martins e Galato 12. Corroborando estes achados, Rojas-Cortés 21 destacou que a taxa de detecção no Brasil é bastante elevada, sendo um dos países que mais identifica medicamentos falsificados, não registrados ou fora do padrão na América Latina 21. Além disso, um estudo 22 corrobora ao constatar que algumas preparações magistrais apresentavam nomes comerciais que induzem ações terapêuticas, como: cápsulas para fumante, imunidade de leão, cápsula de controle emocional, da beleza etc. 22.
Nesse intervalo, houve a implantação do Vigimed em 2019/2020, associado à ampla disseminação do papel da Anvisa e das ações de fiscalização junto à população pela imprensa e mídias sociais, durante a pandemia da COVID-19. A implantação do Vigimed e a pandemia podem estar relacionados ao aumento de notificações no período, corroborado pelo estudo envolvendo idosos de Souza et al. 23. Segundo esta pesquisa 23, o uso de cloroquina e as vacinas para a COVID-19 tiveram um papel importante no aumento significativo de notificações.
Ainda, durante a pandemia foi observada a ampliação do acesso e do comércio eletrônico de produtos médicos em escala mundial em função das medidas de isolamento/restrição social, tornando-se uma preocupação para todos os sistemas regulatórios 24.
Reforçando o papel importante da vigilância sanitária junto às mídias sociais, Soares et al. 25 descreveram o papel desta agência em um município do Nordeste e destacaram as ações realizadas no âmbito da gestão e planejamento; no controle do risco sanitário; na própria regulação; no monitoramento dos casos suspeitos e confirmados da doença e em situações relacionadas ao não cumprimento do isolamento social em primeiro momento e, como abordado anteriormente, no processo de informação, comunicação e educação para a saúde.
Em relação à pandemia, Palácio e Takenami 26 destacaram que houve inúmeras barreiras para alcançar a população por meio da educação em saúde. Segundo os autores, estas barreiras estão relacionadas a diversas situações que vão desde o desenvolvimento tecnológico até as dificuldades voltadas à adoção de medidas de higiene ou mesmo divulgação de fake news. Estes aspectos levantam a importância da atuação da vigilância sanitária na prevenção de agravos à saúde.
Apesar destas ações internas, a Anvisa suspendeu as inspeções internacionais em março de 2020, devido à pandemia de COVID-19. A medida foi tomada para evitar a propagação do vírus e proteger a saúde dos funcionários e das empresas envolvidas nas inspeções. A suspensão das inspeções internacionais afetou as atividades regulatórias da Anvisa e a aprovação de novos medicamentos e produtos para a saúde, já que muitos processos dependem dessas inspeções. Nesse sentido, a Anvisa intensificou as ações de fiscalização como alternativa para manter a segurança e a eficácia dos produtos em circulação no mercado 27. Cassano e Areda 28 abordaram o tema relacionado à flexibilização das BPF e alertaram sobre “a responsabilidade tanto das empresas quanto das autoridades sanitárias que, juntas, devem buscar assegurar a qualidade dos medicamentos disponibilizados à população 29” (p. 50).
Nesse sentido, é fundamental refletir sobre a quantidade de medidas identificadas sem empresa responsável ou CNPJ inexistente, o que dificulta a responsabilização legal do infrator, seja quem for na cadeia produtiva. A falta de identificação do infrator, por meio do CNPJ, pode se dar tanto por uma possível incompletude dos dados na notificação de QT, mas principalmente por empresas irregulares, muitas vezes representadas por sites de venda online.
É preciso considerar ainda a elevada subnotificação de QT, uma vez que o modelo de atuação da fiscalização sanitária no âmbito federal é predominantemente do tipo passivo-reativo, ou seja, o processo tem início após a notificação da QT ou a denúncia registrada e tem limitada capacidade de investigação, análise fiscal e aplicação efetiva de penalidades 1, 29. Alguns estudos 24, 30consideram que os sistemas regulatórios de medicamentos, as agências de polícia e o poder judiciário devem ser ágeis e atuarem de forma integrada e proativa frente às irregularidades identificadas, buscando proteger a população do consumo de produtos irregulares no Brasil.
Pontua-se aqui as ações de educação em saúde para profissionais de saúde e população para que possam suspeitar de qualquer sinal de impureza, contaminação ou vedação inadequada, entre outros problemas. Se algo parecer suspeito, devem saber como notificar à Agência, antes que qualquer outro dano à saúde possa, de fato, acontecer 31, 32.
Apesar da ausência de algumas informações, como constatado anteriormente, observou-se um avanço importante nas RE da Anvisa, quando da disponibilidade de informações sobre a classificação de risco. No estudo de Martins e Galato 12, os autores não disponibilizaram a classificação de risco porque esta informação era inconstante na ocasião do estudo. No entanto, para esta pesquisa, foi possível verificar uma maior frequência de medidas preventivas relacionadas às situações classificadas como de alto risco (Risco I). Da mesma forma, a maioria dos estudos internacionais 21, 33, 34, 35 sobre as restrições, as proibições e os recolhimentos de medicamentos irregulares se concentram na classificação de alto risco, com maior potencial de causar danos graves à saúde, incluindo óbitos. Ressalta-se que a Anvisa utiliza a classificação internacional de risco, praticada internacionalmente por países como EUA, Reino Unido, Canadá e Portugal, como forma de estabelecer prioridades para tomada de decisão 21, 33, 34, 35.
Embora seja visível a melhoria na qualidade das informações das medidas sanitárias, não é possível estabelecer a quantidade de produtos efetivamente apreendidos, inutilizados e recolhidos do mercado, sendo difícil a análise com mais informações sobre os 2.035 medicamentos irregulares identificados nesta pesquisa.
Também houve dificuldade em estabelecer um perfil no processo decisório de ação de fiscalização quanto ao tipo de suspensão e proibição, considerando as etapas da cadeia produtiva. Algumas medidas trazem todas as etapas, outras, somente algumas, sendo mais frequentes as que têm maior proximidade com o consumidor final, como distribuição e uso. Rojas-Cortes 21 comprovou “a hipótese de que a cadeia de suprimentos é mais vulnerável em seu nó final” 21(p. 7), o que facilita a penetração de fármacos não registrados e falsificados. “À medida que um medicamento se move em direção ao paciente ao longo do ciclo de vida do produto, o número de controles regulatórios diminui, enquanto o número de partes interessadas e transações aumenta” 21(p. 7).
Nesse sentido, pode-se inferir que as medidas que apresentam maior risco tendem a ser mais severas, como apreensão e inutilização, geralmente relacionadas a produtos falsificados ou produtos sem registro na Anvisa. As ações determinadas apresentam uma proporção significativamente diferente em relação ao risco envolvido. Neste sentido, como a maioria dessas medidas foi classificada como Risco I e, considerando que se desconhece a composição e origem dos produtos, a sua retirada do mercado deve ser imediata.
A RDC n° 55/2005 8determina que é obrigação do detentor do registro do medicamento fora do padrão notificar e recolher todos os lotes dos produtos na cadeia produtiva enquadrados no Risco I e II, porém, identifica-se que nem todas as medidas estudadas apresentam a determinação do recolhimento. Observa-se que não há uma padronização das ações legais de fiscalização, o que reforça os achados do estudo de Yamamoto 36, destacando que a ausência de informações detalhadas sobre os esforços realizados para remover ou corrigir o produto irregular serve como importante estratégia de transparência e proteção à saúde da população 28. Neste sentido, é importante que a Anvisa determine e aplique critérios claros para a fiscalização e para as ações legais, o que poderia ser realizado por meio de um quadro de especialistas com base nas recomendações da OMS 1 e de outras agências internacionais.
Quanto aos medicamentos fora do padrão/desvios de qualidade, houve um aumento dos recolhimentos voluntários por parte das empresas, provavelmente resultado do fortalecimento e amadurecimento do sistema regulatório brasileiro 20. Dentre os motivos para esse aumento, pode-se apontar alerta internacional de contaminação por impurezas conhecidas como “nitrosaminas”, compostos químicos potencialmente cancerígenos 37. Desde então, numa atuação proativa, a Anvisa estabeleceu regras e implantou o programa de monitoramento de nitrosaminas, com o objetivo de aprofundar as investigações com análise laboratorial na classe dos antagonistas de receptores da angiotensina II, as “sartanas”, produtos utilizados para controle de pressão alta, envolvendo a participação voluntária do setor produtivo para o enfrentamento do problema 37. Representaram um terço (44/152) das medidas de recolhimento, sendo a maioria classificada como Risco II. Ao final de 2019, a Anvisa publicou uma medida preventiva em razão da presença desta impureza no insumo farmacêutico ativo (IFA) (Resolução Específica RE nº 3.210/2019), desencadeando uma série de recolhimentos voluntários por parte das empresas regulares 37. De forma semelhante, Pinto et al. 38 observaram que as ações mais frequentes de inspeções da Anvisa permitiram um maior número de apreensões e, entre essas, destacam-se aquelas relacionadas à deficiência de boas práticas, à falta de registro ou à contaminação por nitrosamidas, como referido anteriormente.
Um fator limitante a uma maior adesão por parte das empresas ao recolhimento voluntário, encontra-se na obrigatoriedade da Anvisa para autuar e instaurar o processo administrativo sanitário (PAS), independentemente do tipo de recolhimento, segundo a Lei nº 6.437/1977 11 e a RDC n° 55/2005 8. Em outros países, por exemplo, nos EUA, o recolhimento voluntário corresponde a mais de 90% dos recalls de medicamentos fora do padrão, sendo incentivado, supervisionado e avaliado pela autoridade regulatória 13, 31. Entretanto, Nagaich e Sadhna 30 afirmaram que a extensa lista de recalls no site da FDA/EUA evidencia que muitas indústrias ainda não seguem de forma eficiente, as normas de BPF emitidas pela agência americana.
No Brasil, importantes iniciativas têm se mostrado promissoras, como o Vigimed e a implantação do Sistema Nacional de Controle de Medicamentos (SNCM), que possibilitarão a rastreabilidade em toda a cadeia de medicamentos, dificultando a inserção de medicamentos falsificados no mercado, por exemplo 28, 39.
Neste sentido, Martins e Teixeira 40 propuseram algumas iniciativas para fortalecer as ações de controle e fiscalização de medicamentos como:
1) a revisão do modelo de gestão do risco dos medicamentos na pós-comercialização/uso; 2) fortalecimento do trabalho em rede entre os serviços de saúde para monitoramento e comunicação; 3) análise sistêmica das notificações e integração entre os sistemas de informação; e 4) implantação efetiva do sistema de rastreabilidade dos produtos, pois dificulta a entrada dos irregulares no mercado.
Uma limitação importante consiste nas poucas informações disponibilizadas nas medidas preventivas, mesmo havendo dupla verificação de cada uma, tanto no portal da imprensa nacional, como no da Anvisa. Não foi possível relacionar as ações de fiscalização com as classes terapêuticas, dos principais medicamentos suspeitos de irregularidades. Ademais, os dados do ano de 2018 não foram incluídos devido à incompatibilidade das informações no antigo portal 18da Agência, havendo reformulação da página em 2019.
CONCLUSÕES
Este estudo trouxe evidências sobre um problema mundial de saúde pública, atualizando informações sobre as QT e as medidas preventivas de fiscalização relacionadas aos medicamentos falsificados, não registrados ou fora do padrão no Brasil.
Houve aumento significativo de notificações de QT no período estudado, sendo crescente também o percentual de recolhimento voluntário realizado pela empresa detentora do registro.
Constata-se que as ações de fiscalização para o recolhimento e a suspensão dos medicamentos potencialmente nocivos caíram progressivamente ao longo dos anos em quantidade relativa ao total de medidas sanitárias, sendo que as ações de apreensão, inutilização e proibição cresceram.
Para combater a comercialização de medicamentos irregulares na internet, a Anvisa implantou no final de 2021 um projeto-piloto de monitoramento com a utilização de uma ferramenta de inteligência artificial que rastreia e notifica tais produtos no ambiente virtual (Epinet – Microsoft Power BI).
Recomenda-se maior alinhamento com as estratégias sugeridas pela OMS em âmbito mundial para fortalecer o sistema regulatório nacional na vigilância pós-comercialização de medicamentos irregulares. Além de ampliação da capacidade de prevenção, detecção e resposta aos produtos fora do padrão, falsificados e não registrados, com atualização do marco regulatório e do modelo de atuação; maior responsabilização das empresas; uso de tecnologias que ampliem a detecção e integração com a farmacovigilância; implantação dos mecanismos de rastreabilidade; ações de comunicação do risco aos profissionais de saúde e a população; ações fiscalizatórias efetivas com supervisão do recolhimento destes produtos do mercado e melhoria da qualidade das informações das medidas preventivas adotadas pela Anvisa para proteger a saúde da população.
REFERÊNCIAS
World Health Organization – WHO. A study on the public health and socioeconomic impact of substandard and falsified medical products. Geneva: World Health Organization; 2017[acesso 12 jul 2019]. Disponível em: https://www.who.int/publications/i/item/9789241513432
World Health Organization – WHO. Organization global surveillance and monitoring system for substandard and falsified medical products. Geneva: World Health Oganization; 2017[acesso 22 ago 2019]. Disponível em: https://www.who.int/medicines/regulation/ssffc/publications/GSMSreport_EN.pdf?ua=1
Brasil. Lei No 9.782, de 26 de janeiro de 1999. Define o Sistema Nacional de Vigilância Sanitária, cria a Agência Nacional de Vigilância Sanitária, e dá outras providências. Diário Oficial União. 27 jan 1999.
Agência Nacional de Vigilância Sanitária – Anvisa.Diretrizes para investigação de queixas técnicas de medicamentos e aplicação de processo administrativo sanitário. Brasília: Agência Nacional de Vigilância Sanitária; 2010[acesso 20 dez 2021]. Disponível em: https://www.anvisa.gov.br
Chieffi AL. Características de uma boa notificação de suspeita de queixa técnica de medicamentos. São Paulo: Centro de Vigilância Sanitaria; 2013.
Centro de Vigilância Sanitária – CVS. Apresentação.São Paulo: Centro de Vigilância Sanitária; 2021[acesso 20 dez 2021]. Disponível em: https://www.cvs.saude.sp.gov.br/apresentacao.asp?te_codigo=30
Agência Nacional de Vigilância Sanitária – Anvisa. Produtos irregulares: o que são e como identificá-los: cosmetovigilancia. Brasília: Agência Nacional de Vigilância Sanitária; 2019[acesso 8 dez 2021]. Disponível em: http://antigo.anvisa.gov.br/resultado-de-busca?p_p_id=101&p_p_lifecycle=0&p_p_state=maximized&p_p_mode=view&_101_struts_action=%2Fasset_publisher%2Fview_content&_101_returnToFullPageURL=http%3A%2F%2Fantigo.anvisa.gov.br%2Fresultado-de-busca%3Fp_auth%3DQii
Agência Nacional de Vigilância Sanitária – Anvisa. Resolução RDC N° 55, de 17 de março de 2005. Regulamenta o recolhimento de medicamentos, que possibilite o acompanhamento pelos órgãos do Sistema Nacional de Vigilância Sanitária e pela sociedade Brasília. Diário Oficial União. 18 mar 2005.
Agência Nacional de Vigilância Sanitária – Anvisa.Guia prático para identificação de medicamentos irregulares no mercado. Brasília: Agência Nacional de Vigilância Sanitária; 2010.
Brasil. Lei N o 6.360, de 23 de setembro de 1976. Dispõe sobre a vigilância sanitária a que ficam sujeitos os medicamentos, as drogas, os insumos farmacêuticos e correlatos, cosméticos, saneantes e outros produtos, e dá outras providências. Diário Oficial União. 24 set 1976.
Brasil. Lei N o 6.437, de 20 de agosto de 1977. Configura infrações à legislação sanitária federal, estabelece as sanções respectivas, e dá outras providências. Diário Oficial União. 21 ago 1977.
Martins MAF, Galato D. Irregularidades dos medicamentos comercializados no Brasil: uma análise das notificações e das medidas sanitárias de 2012 a 2017. Vigil Sanit Debate. 2018;6(4):23-33. https://doi.org/10.22239/2317-269x.01165
Hall K, Stewart T, Chang J, Freeman MK.Characteristics of FDA drug recalls: a 30-month analysis. Am J Heal Pharm. 2016;73(4):235-40. https://doi.org/10.2146/ajhp150277
World Health Oganization – WHO. Director-general’s opening remarks at the media briefing on COVID-19: 11 March 2020. Geneva: World Health Oganization; 2020[acesso 17 mar 2022]. Disponível em: https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---11-march-2020
Agência Nacional de Vigilância Sanitária – Anvisa. Resolução RDC N o 392 de 26 de maio de 2020.Define os critérios e os procedimentos extraordinários e temporários para a aplicação de excepcionalidades a requisitos específicos das boas práticas de fabricação e de importação de medicamentos e insumos farmacêuticos. Diário Oficial União. 28 maio 2020.
Controladoria-Geral da União (BR). Fala.BR: plataforma integrada de ouvidoria e acesso a informação: consultar manifestação. Brasília: Controladoria-Geral da União; 2022[acesso 17 mar 2022]. Disponível em: https://falabr.cgu.gov.br/publico/Manifestacao/DetalharManifestacaoPublico
Agência Nacional de Vigilância Sanitária – Anvisa. Resolução RDC Nº 585, de 10 de dezembro de 2021. Aprova e promulga o regimento interno da Agência Nacional de Vigilância Sanitária – Anvisa e dá outras providências. Diário Oficial União. 15 fev 2021.
Agência Nacional de Vigilância Sanitária – Anvisa. Consultas. Brasília: Agência Nacional de Vigilância Sanitária; 2018[acesso 9 dez 2021]. Available from: https://consultas.anvisa.gov.br/#/dossie/
Ministério da Saúde (BR). Resolução Nº 510,de 7 de abril de 2016. Dispõe sobre as normas aplicáveis a pesquisas em ciências humanas e sociais cujos procedimentos metodológicos envolvam a utilização de dados diretamente obtidos com os participantes ou de informações identificáveis ou que possam acarretar riscos maiores do que os existentes na vida cotidiana. Dário Oficial União. 8 abr 2016.
.International Criminal Police Organization – Interpol. Pharmaceutical crime operations. Lyon: International Criminal Police Organization; 2021[acesso 9 dez 2021]. Disponível em: https://www.interpol.int/en/Crimes/Illicit-goods/Pharmaceutical-crime-operations
Rojas-Cortés R. Substandard, falsified and unregistered medicines in Latin America, 2017-2018. Rev Panam Salud Publica. 2020;44:1-10. https://doi.org/10.26633/RPSP.2020.125
Nagaich U, Sadhna D. Drug recall: an incubus for pharmaceutical companies and the most serious drug recall of history. Int J Pharm Investig. 2015;5(1):1-7. https://doi.org/10.4103/2230-973X.147222
Souza BG, Rezende CP, Detoni KB, Capucho HC, Rosa MB, Carmo Júnior NM, Nascimento MMG. Eventos adversos a medicamentos entre idosos no Brasil antes e após o início da pandemia da COVID-19. Vigil Sanit Debate. 2022;10(3):13-21. https://doi.org/10.22239/2317-269x.02045
Mackey TK, Aung P, Liang BA. Illicit Internet availability of drugs subject to recall and patient safety consequences. Int J Clin Pharm. 2015;37:1076-85. https://doi.org/10.1007/s11096-015-0154-8
Ferreira VES, Mesquita JMC, Parente PD, Costa Filho LG, Lima MGF, Aguiar AM. O agir da vigilância sanitária frente à COVID-19 e o necessário exercício da intersetorialidade. Rev Pol Públicas. 2021;20(Supl.):58-70. https://doi.org/10.36925/sanare.v20i0.1508
Palácio MAV, Takenami I. Em tempos de pandemia pela COVID-19: o desafio para a educação em saúde. Vigil Sanit Debate. 2020;8(2):10-5. https://doi.org/10.22239/2317-269X.01530
Agência Nacional de Vigilância Sanitária – Anvisa. Relatório inspeção internacional de fabricantes de insumos farmacêuticos ativos (riifa_2020): período da revisão 2020. Brasília: Agência Nacional de Vigilância Sanitária; 2021[acesso 5 abr 2023]. Disponível em: https://www.gov.br/anvisa/pt-br/centraisdeconteudo/publicacoes/certificacao-e-fiscalizacao/manuais-e-orientacoes/relatorio-inspecao-internacional-de-fabricantes-de-insumos-farmaceuticos-ativos-riifa-2020#:~:text=Todas%20as%20inspe%C3%A7%C3%B5es%20internacionais%20agendadas,%2D2019%2Dcom%2Dficha
Cassano AO, Areda CA. A flexibilização de requisitos brasileiros de boas práticas de fabricação durante a pandemia da COVID-19 sob uma perspectiva comparada. Vigil Sanit Debate. 2020;8(3):44-51. https://doi.org/10.22239/2317-269x.0171
Ji Y, Ying H, Farber MS, Yen J, Dews P, Miller RE et al. A Distributed, collaborative intelligent agent system approach for proactive postmarketing drug safety surveillance. IEEE Trans Inf Technol Biomed. 2010;14(3):826-37. https://doi.org/10.1109/TITB.2009.2037007
Nayyar GML, Breman JG, Mackey TK, Clark JP, Hajjou M, Littrell M et al. Falsified and substandard drugs: stopping the pandemic. Am J Trop Med Hyg. 2019;100(5):1058-65. https://doi.org/10.4269/ajtmh.18-0981
Wang B, Gagne JJ, Choudhry NK. The epidemiology of drug recalls in the United States. Arch Intern Med. 2012;172(14):1110-1. https://doi.org/10.1001/archinternmed.2012.2013
Terrie YC. Overview of the fda’s drug-recall process. U.S. Pharmacist. 17 set 2019[acesso 30 ago 2020]. Disponível em: https://www.uspharmacist.com/article/overview-of-the-fdas-drugrecall-process
Almuzaini T, Sammons H, Choonara I. Quality of medicines in Canada: a retrospective review of risk communication documents (2005–2013). BMJ Open. 2014;4(10):1-9. https://doi.org/10.1136/bmjopen-2014-006088
Almuzaini T, Sammons H, Choonara I. Substandard and falsified medicines in the UK: a retrospective review of drug alerts (2001–2011). BMJ Open. 2013;3:1-9. https://doi.org/10.1136/bmjopen-2013-002924
Eissa ME. Drug recall monitoring and trend analysis: a multidimensional study. Glob J Qual Saf Healthc. 2019;2(2):34-9. https://doi.org/10.4103/JQSH.JQSH_3_19
Yamamoto C, Monteiro E, Batista C. Grounded theory: avaliação das causas de recolhimento de medicamentos irregulares pela Agência Nacional de Vigilância Sanitária. Anais 4º Seminário Internacional de Pesquisa e Estudo Qualitativos; 2009, Rio Claro, Brasil. São Paulo: Sociedade de Estudos e Pequisa Qualitativa; 2009.
Agência Nacional de Vigilância Sanitária – Anvisa. Anvisa lança programa de monitoramento de nitrosaminas. Brasília: Agência Nacional de Vigilância Sanitária; 2020[acesso 17 mar 2022]. Disponível em: http://antigo.anvisa.gov.br/resultado-de-busca?p_p_id=101&p_p_lifecycle=0&p_p_state=maximized&p_p_mode=view&p_p_col_id=column-1&p_p_col_count=1&_101_struts_action=%2Fasset_publisher%2Fview_content&_101_assetEntryId=6037353&_101_type=content&_101_groupId=2
Pinto NN, Resende KA, Couto RO. Insumos farmacêuticos ativos irregulares no Brasil: análise descritiva de 2011 a 2019. Vigil Sanit Debate. 2021;9(1):61-70. https://doi.org/10.22239/2317-269x.0145
Melo VAZC, Beteto AL, Gregis C, Rebelo F, Curado V, Rodrigues A et al. Rastreabilidade na cadeia de medicamentos brasileira. Bol Inst Saúde. 2020;21(1):211-23.
Martins MAF, Teixeira APCP. Desafios e perspectivas na vigilância sanitária pós-comercialização/uso. Vigil Sanit Debate. 2019;7(4):3-9. https://doi.org/10.22239/2317-269X.01425
Autor notes
* E-mail: josivan.padro@gmail.com
Declaração de interesses
Os autores informam não haver qualquer potencial conflito de interesse com pares e instituições, políticos ou financeiros deste estudo.
