Artículos de investigación
Rasgos morfológicos de semillas y germinación de Peltogyne mexicana (Fabaceae): única especie de Peltogyne en México
Seed morphological traits and germination of Peltogyne mexicana (Fabaceae): unique Peltogyne species in Mexico
Rasgos morfológicos de semillas y germinación de Peltogyne mexicana (Fabaceae): única especie de Peltogyne en México
Acta botánica mexicana, núm. 131, e2208, 2024
Instituto de Ecología A.C., Centro Regional del Bajío
Recepción: 04 Mayo 2023
Recibido del documento revisado: 20 Septiembre 2023
Aprobación: 01 Diciembre 2023
Publicación: 06 Marzo 2024
Resumen
Antecedentes y Objetivos: Peltogyne mexicana es la única especie del género Peltogyne en México, pero sus poblaciones naturales están sometidas a procesos de fragmentación, siendo necesarias estrategias de conservación. La propagación en vivero puede contribuir a conservar la especie, pero deben desarrollarse estrategias adecuadas de manejo del germoplasma. En esto es importante conocer las características morfológicas de las semillas y su germinación. Los objetivos de este trabajo fueron: (1) caracterizar la variación intrapoblacional de algunos rasgos morfológicos (cualitativos y morfométricos) de las semillas de P. mexicana, y (2) analizar la influencia del tamaño en la germinación.
Métodos: Se describieron y caracterizaron rasgos como el color, forma, largo, ancho, grosor y peso de las semillas de P. mexicana. Se examinó la relación entre los rasgos con un análisis de correlación de Pearson y se probó la variación intrapoblacional con un análisis de varianza. También se analizó la influencia del tamaño en la germinación mediante regresión logística y la función de Weibull, en todos los casos a un nivel de significancia de 5%.
Resultados clave: Las semillas de P. mexicana son de color rojo obscuro con forma ovoide. Existe una variación intrapoblacional alta en sus rasgos. El ancho es el rasgo con menor variación, el peso es el que más varía. Todos los rasgos se correlacionan significativamente entre sí, pero el largo y el peso tienen el mayor grado de asociación. La germinación se relaciona significativamente con el peso de las semillas. La probabilidad de germinación aumenta a medida que el peso también se incrementa. Tasas altas de germinación se presentan en semillas con un peso de 0.65 g y la germinación ocurre con mayor frecuencia entre los 11.20 días.
Conclusiones: Los rasgos morfológicos de las semillas de P. mexicana varían intrapoblacionalmente. El peso de la semilla influye en la germinación.
Palabras clave: Conservación+ ecología de semillas+ especies amenazadas+ madera preciosa+ palo morado+ vivero forestal.
Abstract
Background and Aims: Peltogyne mexicana is the only species of the genus Peltogyne in Mexico, but its natural populations are subject to fragmentation processes and conservation strategies are needed. Nursery propagation can contribute to the conservation of the species, but appropriate germplasm management strategies must be developed. It is important to know the morphological characteristics of the seeds and their germination. The objectives of this work were: (1) to characterize the intrapopulation variation of some morphological traits (qualitative and morphometric) of P. mexicana seeds, and (2) to analyze the influence of size on germination.
Methods: Traits such as color, shape, length, width, thickness, and weight of seeds of individuals of P. mexicana were described and characterized. The relationship between traits was examined with a Pearson correlation analysis and intrapopulation variation was tested with an analysis of variance. The influence of size on germination was also analyzed using logistic regression and the Weibull function, in all cases at a significance level of 5%.
Key results: The seeds of P. mexicana are dark red with an ovoid shape. There is a high intrapopulation variation in traits. Width is the trait with the least variation, weight varies the most. All traits are significantly correlated with each other, but length and weight have the highest degree of association. Germination is significantly related to seed weight. The probability of germination increases as weight also increases. High germination rates occur for seeds weighing 0.65 g and germination occurs most frequently at 11.20 days.
Conclusions: Seed morphological traits of P. mexicana vary intrapopulationally. Seed weight influences germination.
Key words: Conservation, seed ecology, threatened species, precious wood, purpleheart, forest nursery.
Introducción
Peltogyne mexicana Martínez (palo morado como comúnmente se le conoce en México) pertenece a la familia Fabaceae y de las 24 especies aceptadas del género Peltogyne Vogel (WFO, 2023) es la única con representatividad en México; además, endémica al estado de Guerrero (Sotuyo, 2014). Es considerada una especie arbórea de madera preciosa de la selva mediana subperennifolia, cuya distribución natural actualmente está limitada a los municipios Chilpancingo, Juan R. Escudero (Tierra Colorada) y Acapulco (Sotuyo, 2014). Durante varias décadas ha sido aprovechada para la elaboración de muebles y artesanías por la calidad de su madera (alta densidad y finura de grano) y por la coloración púrpura de su duramen (Navarro-Martínez et al., 2005; Sotuyo, 2014). Peltogyne mexicana está catalogada como especie amenazada por la NOM-059-SEMARNAT-2010 (SEMARNAT, 2010) y como especie en peligro de extinción por la Unión Internacional para la Conservación de la Naturaleza (Machuca Machuca et al., 2022). A pesar de su importancia forestal, ecológica y social, no hay evidencia de un registro oficial de su aprovechamiento y tampoco hay antecedentes que constaten acciones gubernamentales para su conservación, especialmente por la fragmentación creciente de su hábitat debido a la deforestación, tala clandestina y presión urbana (Sotuyo, 2014).
Para las especies forestales vulnerables, como P. mexicana, la propagación en vivero es una alternativa importante para la conservación in situ de esos recursos genéticos. Esta actividad permite impulsar proyectos de plantaciones forestales de enriquecimiento, reforestación o restauración ecológica, lo cual es crucial para repoblar o acelerar los procesos de recuperación de los hábitats fragmentados de poblaciones de árboles con algún grado de amenaza (Calixto Valencia et al., 2022). La iniciativa de propagar en vivero a P. mexicana plantea retos importantes. En general, no existe evidencia que documente protocolos para su propagación. Esto tiene sentido considerando que es una especie amenazada, por lo que los vacíos de información sobre su biología, ecología o silvicultura son un común denominador, como sucede con otros taxones silvestres en la misma circunstancia (Rivera-Martin et al., 2013; Romero-Saritama y Pérez Ruíz, 2016), incluyendo algunas de sus congéneres que tienen un área más grande de distribución natural como Peltogyne paniculata Benth. (Rivera-Martin et al., 2013; Mosquera Mena y Ruíz Flórez, 2015) y P. purpurea Pittier (Barrace et al., 2003).
En este sentido, en P. mexicana es necesario generar información para cada uno de los aspectos relacionados con la propagación en vivero. Por ejemplo, el conocimiento de la ecología de sus semillas es un aspecto que amerita atención porque esta información ayudaría a definir estrategias para el manejo adecuado de su germoplasma (Rivera-Martin et al., 2013), ya que muchas especies arbóreas tropicales, dentro de un mismo taxón y a nivel de individuos, suelen presentar una variación alta en la morfología de sus semillas (color, forma, tamaño, peso) por condicionantes genéticos, ambientales y fisiológicos que afectan el éxito reproductivo de las fuentes parentales y, consecuentemente, la formación y desarrollo de las semillas (Souza et al., 2015; Lozano et al., 2016; Romero-Saritama y Pérez Ruiz, 2016). De modo que conocer estas características morfológicas es útil para formular directrices para la manipulación de las semillas desde su recolección hasta su uso en vivero. En este sentido, para garantizar mayores tasas de germinación en los programas de propagación sexual, también es relevante comprender el papel funcional de algunos rasgos, como es el caso del tamaño, de lo cual se tiene evidencia de su influencia en los procesos de germinación en varias especies de árboles tropicales (Baraloto et al., 2005; Romero-Saritama y Pérez Ruiz, 2016; Deb y Sundriyal, 2017).
Al respecto, en algunas especies se ha encontrado una relación positiva entre el tamaño de las semillas y la germinación. Por ejemplo, la tasa de germinación de Beilschmiedia assamica Meisn. (Lauraceae), Canarium strictum Roxb. (Burseraceae), Dipterocarpus macrocarpus Vesque (Dipterocarpaceae), Ostodes paniculata Blume (Euphorbiaceae) (Deb y Sundriyal, 2017), Swietenia macrophylla King (Meliaceae) (Pramono et al., 2019) y Enterolobium contortisiliquum (Vell.) Morong (Fabaceae) (Trindade-Lessa et al., 2015) incrementa entre más grande o pesada es la semilla. Sin embargo, en contraparte, también hay especies como Coulteria platyloba (S. Watson) N. Zamora (Leguminosae), Dalbergia congestiflora Pittier (Fabaceae), Mimosa benthamii J.F. Macbr. (Mimosaceae) y Pithecellobium acatlense Benth. (Mimosaceae), en las que la germinación es independiente del tamaño o peso de las semillas (González-Vélez et al., 2020).
Ante esa discrepancia en la respuesta de germinación, aún siguen siendo necesarios más estudios para comprender el papel especie-específico del peso o tamaño de las semillas, como lo sugieren Gelviz-Gelvez et al. (2020). Desde un enfoque que derive en implicaciones prácticas, los objetivos de este estudio son: (1) caracterizar la variación intrapoblacional de algunos rasgos morfológicos (cualitativos y morfométricos) de las semillas de P. mexicana, y (2) analizar la influencia del tamaño en la germinación. Los resultados pueden contribuir a desarrollar estrategias adecuadas de manejo del germoplasma desde su recolección hasta su uso en vivero para la producción de planta de P. mexicana, lo cual es fundamental para establecer bases que contribuyan a su conservación en futuros proyectos.
Materiales y Métodos
Características de la especie
Peltogyne mexicana es un árbol monoico de 15-20 m de altura con un tronco de 30-60 cm de diámetro. Sus flores son blancas y numerosas, están dispuestas en inflorescencia de tipo panícula terminal y axilar. La floración ocurre entre los meses de julio a agosto con un traslape en los procesos de fructificación que suceden entre julio y febrero, que es cuando los frutos alcanzan su madurez. Los frutos son vainas dehiscentes que contienen una semilla, rara vez dos. Tras la apertura de las vainas, las semillas permanecen unidas por el funículo y su diseminación ocurre entre marzo y abril, primariamente por gravedad. En ocasiones la semilla se dispersa secundariamente por el viento cuando esta aún mantiene partes de la vaina. La semilla en su morfología externa suele ser obovoide (Navarro-Martínez, 2001).
Recolección de semillas
En abril de 2021, se recolectaron semillas de 10 árboles localizados en la localidad Tierra Colorada, municipio Juan R. Escudero, Guerrero, México, en las coordenadas 17°10'04''N, 99°31'34''O, a 317 m s.n.m. La recolección se realizó mediante un muestreo dirigido, procurando cubrir las condiciones fisiográficas incluyendo principalmente la exposición geográfica y la pendiente del terreno. La población estudiada tiene una densidad de 27 árboles/ha. El criterio para la selección de los árboles se basó en la disponibilidad de semillas, complementario a algunas características fenotípicas sobresalientes como fuste limpio y recto, copa de tamaño grande, ausencia visible de plagas y enfermedades (Fig. 1). En promedio, los individuos tienen una altura de 15 m y un diámetro normal de 40 cm. La semilla recolectada, separada por árbol, se transportó en costales de polipropileno para su posterior separación del fruto, limpieza y secado dentro de un invernadero.

Figura 1:
Ejemplar adulto de Peltogyne mexicana Martínez seleccionado como fuente semillera en la localidad de Tierra Colorada, municipio Juan R. Escudero, Guerrero, México.
Caracterización cualitativa y morfométrica de las semillas
La caracterización cualitativa consistió en describir el color de la cubierta seminal y la forma de las semillas. El color se determinó con cartas de colores Munsell® únicamente en una muestra de 50 semillas. Para la forma se calculó el índice de redondez (IR) mediante la relación entre el largo y ancho de las semillas; por lo tanto, si IR=1 es esférica, IR>1 es alargada u oblonga, e IR<1 es ovoide más larga que ancha (Aguirre-Dugua et al., 2012). Para la caracterización morfométrica, las dimensiones se determinaron con un calibrador digital Mitutoyo® Digimatic CD-4” AX (Mitutoyo America Corporation, Aurora, Illinois, EUA). El largo de las semillas se midió desde el extremo hilar hasta el extremo calazal, el ancho se midió en la porción media y más ancha de la semilla, y el grosor en el centro del pleurograma presente en ambos costados de la semilla (Fig. 2). El peso se registró con una báscula digital con precisión de 0. 01 g (iBalance® i2001, MyWeigh® (HBI International, Phoenix, Arizona, EUA)). Además de los datos de largo y ancho de las semillas previamente registrados para calcular la redondez, se midió el grosor (mm) y el peso (g), como parte de las evaluaciones sugeridas por Romero-Saritama y Pérez Ruiz (2016) para caracterizar los rasgos morfológicos de las semillas. Estas mediciones (largo, ancho, grosor y peso) se realizaron en una muestra aleatoria de 500 semillas (50 por cada uno de los 10 árboles). Al momento de la evaluación, la semilla presentaba una humedad de 7-9%, estimada mediante la metodología descrita por Viveros Viveros et al. (2015) que consiste en la determinación en muestras de 5 g de semillas enteras secadas dentro de recipientes en un horno de secado a 103 °C durante 17 h.

Figura 2:
Rasgos morfológicos evaluados en semillas de Peltogyne mexicana Martínez en la localidad de Tierra Colorada, municipio Juan R. Escudero, Guerrero, México.
Prueba de germinación en vivero
Para analizar la influencia del tamaño de las semillas en la germinación se estableció, a partir de las recomendaciones de Willan (1991), un ensayo de germinación en condiciones de vivero. El vivero se localiza en la comunidad La Bajada, municipio Coyuca de Catalán, Guerrero (18°19'11.81''N, 100°40'18.10''O; 254 m s.n.m.). Durante el ensayo que duró 15 días, la temperatura mínima promedio fue de 20 °C y la máxima de 38 °C, mientras que la humedad relativa osciló entre 40 y 90% (datos registrados con un Hobo® MX2304 (Onset Computer Corporation, Bourne, Massachusetts, EUA). Para este ensayo de germinación, se utilizó una muestra de 100 semillas sin signos aparentes de plagas o enfermedades. La siembra se realizó el 12 de mayo de 2021. Se emplearon charolas de plástico con volumen de 180 ml por cavidad y se utilizó un sustrato compuesto por 70% de turba de musgo Sphagnum (peat moss), 15% de perlita y 15% de vermiculita. El diseño experimental fue completamente al azar considerando como repetición una semilla, a la cual de manera individual se le registró su peso (g) previo a sembrarse. La siembra se realizó a una profundidad similar a la longitud de la semilla (1-2 cm) y se aplicaron riegos cada tercer día a saturación.
Se hicieron conteos diarios durante 15 días para monitorear la germinación. La germinación se consideró como evento ocurrido una vez que se observó la emergencia de los cotiledones en la superficie del sustrato, esto por tratarse de una prueba de germinación de vivero con semillas enterradas en condiciones naturales. Los conteos se hicieron desde la emergencia de la primera plántula hasta la fase de estabilización; es decir, cuando ya no se tuvo registro de emergencia en días consecutivos. Se registró la fecha de emergencia de cada plántula para obtener el número de días para germinar después de la siembra.
Análisis de datos
Con excepción del color y la forma, las variables morfométricas (con 500 observaciones) se sometieron a un análisis estadístico, incluyendo el registro de medidas de tendencia central y de dispersión de cada una de ellas (largo, ancho, grosor y peso fresco). Se calcularon los coeficientes de correlación lineal entre las variables usando el método de Pearson y de Spearman (Chock, 2010). Por otra parte, con la finalidad de probar la variación intrapoblacional en los rasgos morfológicos entre los individuos, se realizó un análisis de varianza (ANOVA) de una sola vía, previa validación de los supuestos de normalidad y homogeneidad de la varianza mediante las pruebas de Shapiro-Wilk y Levene, respectivamente. En todos los casos se usó un nivel de significancia de 5%.
Los resultados del ensayo de germinación se evaluaron como eventos independientes entre sí con una distribución binomial: 1 para semillas germinadas y 0 para las no germinadas. Los valores de ocurrencia se modelaron en una regresión logística como una función del peso de las semillas, el cual fue registrado al momento de la siembra y este fue el criterio de diferenciar tamaños. El ajuste de la regresión logística se hizo con la función glm del paquete ‘stats’ disponible en el programa de análisis de datos R v. 4.3.0 (R Core Team, 2021). Los coeficientes de dicha regresión y sus límites de confianza ((1-95%) se calcularon mediante la simulación de Monte Carlo con 10,000 permutaciones, usando la función MCMClogit del paquete ‘MCMCpack’ de R versión 4.3.0 (Martin et al., 2011). Finalmente, se usó la función de densidad de Weibull de dos parámetros para: (1) conocer la distribución de frecuencias, (2) determinar el peso ideal de germinación y, (3) el número de días transcurridos (posterior a la siembra) en los que la probabilidad de germinación se maximiza.
Y su función acumulada es
La fórmula usada para encontrar el peso ideal de las semillas, así como el día con la mayor probabilidad de emergencia fue la siguiente:
En las tres ecuaciones, c es el parámetro de forma y b el parámetro de escala. Estos parámetros se estimaron por el método de máxima verosimilitud usando el paquete ‘MASS’ (Venables y Ripley, 2002) de R v. 4.3.0.
Resultados
Caracterización cualitativa y morfométrica de las semillas
Las semillas de P. mexicana del área de estudio presentan una cubierta seminal de color rojo obscuro (10R 3/3 - 3/4) y disponen de un pleurograma cerrado en el extremo hilar en ambos costados, y en su parte interna tiene un color rojo muy obscuro (10R 2.5/2). Las semillas tienen una forma ovoide según el IR con un valor promedio de 0.64 ± 0.04 (Fig. 3). Al correlacionar las variables morfométricas, se observó que los coeficientes de determinación, tanto de Pearson como de Spearman eran débiles (r≤0.43) en la mayoría de los casos. No obstante, todas las asociaciones fueron positivas y estadísticamente significativas. La mayor asociación lineal se observó entre el peso y la longitud con un coeficiente de Pearson igual a 0.74 y un coeficiente de Spearman igual a 0.71 (Fig. 4). Las medidas de tendencia central y dispersión para las variables estudiadas se detallan en el Cuadro 1.

Figura 3:
Morfología externa de semillas de Peltogyne mexicana Martínez en la localidad de Tierra Colorada, municipio Juan R. Escudero, Guerrero, México.
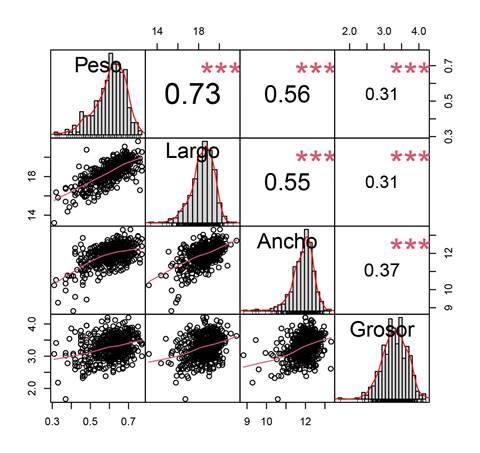
Figura 4:
Análisis de correlación de Pearson entre características de tamaño (largo, ancho y grosor) y el peso de semillas de Peltogyne mexicana Martínez recolectadas en la localidad de Tierra Colorada, municipio Juan R. Escudero, Guerrero, México (N = 500; α = 0.05).
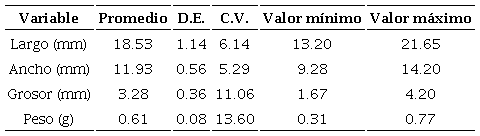
De las variables registradas, la anchura de las semillas exhibió el menor porcentaje de variabilidad al mostrar un coeficiente de variación igual a 5.29%. En contraste, la variable peso mostró el coeficiente de variación más elevado con un valor de 13.60% (Cuadro 1). Por otro lado, al contrastar los rasgos morfométricos de las semillas entre los individuos proveedores de semillas (árboles), se observaron diferencias significativas (p<0.05) (Cuadro 2).
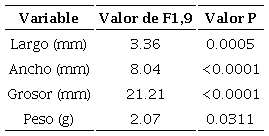
Por otra parte, el modelo logístico reveló que la germinación se asocia significativamente con el peso de las semillas (p=0.0252; Cuadro 3). El coeficiente de regresión reveló que la probabilidad de germinación experimenta un aumento de nueve unidades por cada 100 mg que aumenta el peso de las semillas (Cuadro 3). Por el contrario, a medida que el peso de las semillas se aproxima al valor mínimo (0.31 g), la probabilidad del evento de germinación se vuelve incierta (Fig. 5).

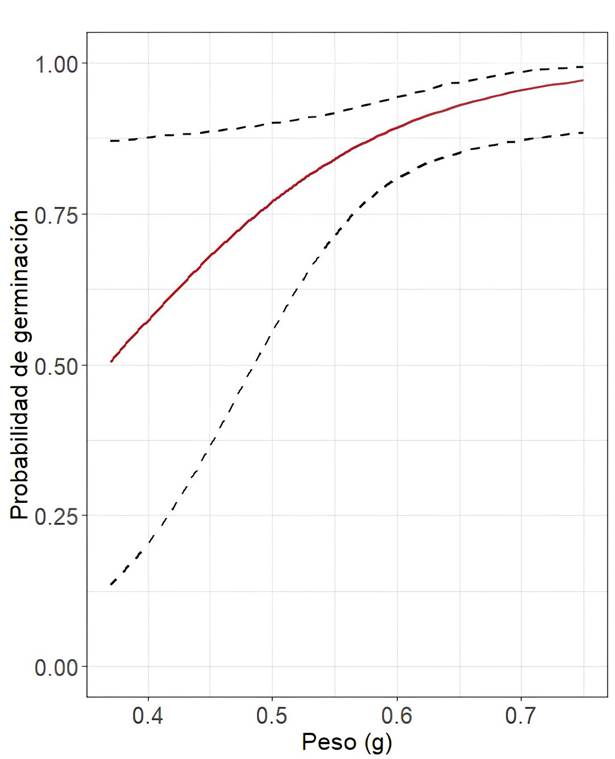
Figura 5:
Probabilidad de germinación y emergencia de Peltogyne mexicana Martínez en función del peso de la semilla. La línea sólida indica valores predichos de probabilidad estimados a partir del ajuste de un modelo logístico, las líneas punteadas representan los límites de confianza al 95% de la probabilidad estimada.
El modelo de Weibull, por su lado, indicó que las semillas con un peso cercano a 0.65 ± 0.068 g (desviación estándar) son las que presentan mayores posibilidades de germinación en comparación con las demás (Fig. 6A). Además, esta función confirmó que la probabilidad de germinación aumenta proporcionalmente al incremento en el peso de las semillas. Sin embargo, cuando el peso se acerca a 0.80 g, la probabilidad parece disminuir (Fig. 6A), aunque es importante mencionar que el declive en la curva de densidad podría atribuirse a la presencia limitada de semillas con pesos superiores a 0.70 g. El vértice de la curva de Weibull sugirió que el día 11±2 días (desviación estándar), es cuando la probabilidad de germinación de las semillas se maximiza (Fig. 6B).
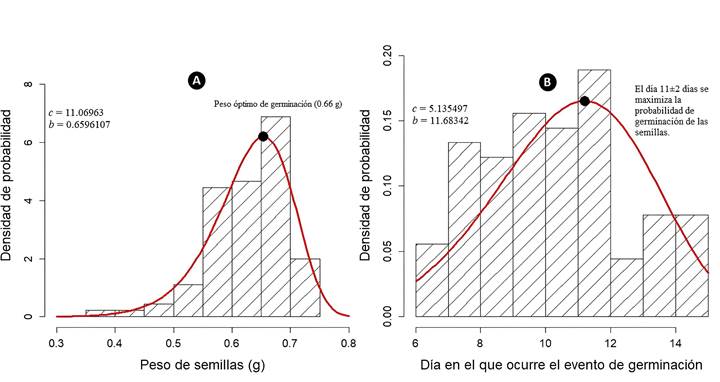
Figura 6:
A. distribución de la probabilidad de germinación/emergencia en función del peso de la semilla; B. distribución de la probabilidad de los días en el que ocurre el evento de germinación/emergencia de Peltogyne mexicana Martínez estimados a partir del ajuste del modelo de Weibull. En ambas gráficas c es el parámetro de forma y b es el parámetro de escala.
Finalmente, se propone una categorización preliminar de las semillas de P. mexicana tomando en cuenta la correspondencia estadística entre el peso de las semillas y la tasa de germinación (en especial cuando el peso es 0.70 g (Figs. 6A, 7)). En el primer percentil se agrupan las semillas con un peso entre 0.37 y 0.60 g, en el segundo, las que pesan entre 0.60 y 0.67 g y en el tercero, cuyos pesos fluctúan entre 0.67 y 0.75 g. Las tasas de germinación observadas de manera empírica para el primer grupo, segundo y tercero fueron 78.6%, 94.9% y 94.1%, respectivamente.
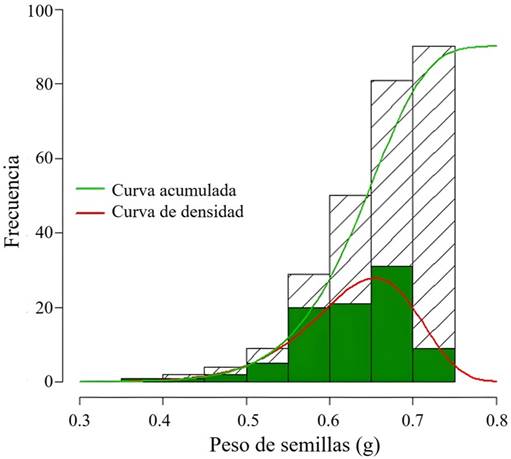
Figura 7:
Distribución de los pesos de las semillas de Peltogyne mexicana Martínez, de acuerdo con las características de la muestra analizada en el área de estudio (N = 500).
Discusión
Las características de color y forma de las semillas de P. mexicana coinciden con las de otras especies del mismo género, como P. paniculata (Salazar et al., 2000; Barrace et al., 2003) y P. purpurea (Salazar et al., 2000; Rivera-Martin et al., 2013). El color y tamaño son rasgos morfológicos distintivos del grado de madurez fisiológica de las semillas (Bareke, 2018) y en algunas especies como Pinus cembroides Zuccarini y P. orizabensis (D.K. Bailey) D.K. Bailey & F.G. Hawksworth, el color de las semillas varía entre procedencias y tiene influencia en la germinación (Hernández-Anguiano et al., 2018). Aunque es común encontrar variación intraespecífica en los rasgos morfológicos de las semillas, como se ha observado en diferentes especies tropicales, tanto a nivel de poblaciones como de individuos (Romero-Saritama, 2016; Calixto Valencia et al., 2022), este estudio no fue la excepción, siendo patente la variación entre individuos en el tamaño y el peso de la semilla, particularmente el peso mostró la mayor variabilidad (Cuadro 1, 2). Turner (2004) reporta que en árboles tropicales el peso de las semillas varía hasta seis ordenes de magnitud. La variación en el tamaño o peso de las semillas es una condición característica en varias especies de la familia Fabaceae, como ejemplifican García Azpeitia et al. (2022) con semillas de Prosopis laevigata (Humb. & Bonpl. ex Willd.) M. C. Johnst.
Para el caso del género Peltogyne, se reportan diferencias en las dimensiones de las semillas según la especie. Por ejemplo, las semillas de P. paniculata miden 12-16 mm de largo (Rivera-Martin et al., 2013); en cambio, los resultados de este estudio muestran que las semillas de P. mexicana son más grandes porque superan los valores reportados en su congénere (Cuadro 1). En este mismo sentido, las semillas de P. mexicana son hasta tres veces más pesadas que las de P. paniculata cuyo valor aproximado es de 0.28 g de peso fresco. Este contraste en peso se explica, para el caso de P. mexicana, con la relación positiva que mostraron la longitud y el peso (Fig. 4). En semillas, el tamaño usualmente se correlaciona con el peso porque la masa es una propiedad volumen-dependiente (Turner, 2004).
Las variaciones en el tamaño o peso de las semillas son aspectos en los que se ha centrado mayor atención (Baskin y Baskin, 2014), por su estrecho vínculo con los procesos de germinación y emergencia (Norden et al., 2009). Los resultados de este estudio se suman a la evidencia experimental, ratificando que para P. mexicana el peso de sus semillas influye en la germinación (Cuadro 3, Fig. 5). Para la especie estudiada, los resultados muestran que entre más pesada es la semilla, su potencial de germinación es mayor (Fig. 5). Sin embargo, la regla no se cumple a cabalidad debido a que la capacidad germinativa disminuye cuando el peso es >0.70 g, lo que puede atribuirse, como se mencionó con anterioridad, a la poca disponibilidad de semillas con ese peso.
La relación positiva registrada en P. mexicana entre el tamaño de las semillas y la germinación coincide con la reportada en especies como Beilschmiedia assamica, Canarium strictum, Dipterocarpus macrocarpus, Ostodes paniculata (Deb y Sundriyal, 2017), Swietenia humilis Zucc. (Calixto Valencia et al., 2022), S. macrophylla (Pramono et al., 2019) y Enterolobium contortisiliquum (Trindade-Lessa et al., 2015), pero a su vez contrasta con la respuesta mostrada en otros taxones cuyas semillas de menor tamaño o peso tienden a germinar mejor (Murali, 1997), aunque incluso hay taxones, como Coulteria platyloba, Dalbergia congestiflora, Mimosa benthamii, Pithecellobium acatlense, en los que la germinación es independiente del peso o tamaño de las semillas (González-Vélez et al., 2020). Esta divergencia de respuestas ha sido difícil de explicar debido a que las variaciones en el tamaño o peso de las semillas y sus repercusiones en la germinación o emergencia son un efecto coyuntural de condicionantes genéticos (Khurana y Singh, 2001; Norden et al., 2009), ambientales o fisiológicos que afectan el éxito reproductivo de cada fuente parental y consecuentemente la formación y tasa de desarrollo de las semillas (Bareke, 2018).
Un ejemplo de la influencia por factores ambientales es aportado por García Azpeitia et al. (2022) con un estudio en Prosopis laevigata, quienes atribuyen a las diferencias en la disponibilidad de nutrientes o fertilidad del suelo, la variación en el tamaño de las semillas en una población de dicha especie. Asimismo, también hay evidencia de la influencia de factores como la posición de las semillas en el fruto. Este aspecto ha sido corroborado en varias fabáceas, aunque mayormente en plantas herbáceas (Baskin y Baskin, 2014). Sin embargo, por ejemplo, hay evidencia de una especie arbórea, E. contortisiliquum, en la que la posición de las semillas en el fruto (proximal, central o distal) no representa diferencias en la germinación (Lessa et al., 2014). Para P. mexicana, quizá esto último no tenga relevancia porque al parecer es frecuente que los frutos contengan solo una semilla (según se observó al procesar los frutos recolectados qua aún contenían la semilla en su interior) al igual que P. purpurea (Salazar et al., 2000) y P. paniculata (Rivera-Martin et al., 2013).
Por otro lado, las diferencias en las respuestas de germinación se asocian con el efecto de factores como las condiciones y necesidades particulares de temperatura, luz y humedad, el grado de madurez fisiológica (Baskin y Baskin, 2014; Bareke, 2018), la presencia de algún mecanismo de latencia (Baskin y Baskin, 2014; Romero-Saritama, 2016; Luna-Nieves et al., 2019), el tipo de sustancias de reservas (Soriano et al., 2011) o el propio tamaño del embrión o endospermo (Romero-Saritama, 2016), los cuales pueden simultáneamente afectar la germinación cuando las semillas ya son independientes de la planta madre. En este sentido, basados en un meta-análisis con 1037 especies tropicales, Norden et al. (2009) proponen que gran parte de la relación del tamaño o peso de las semillas con la germinación se atribuye a condicionantes biofísicas entre el embrión, la absorción de agua, el grosor de la cubierta seminal y el grado de impermeabilidad de la cubierta.
En resumen, las respuestas de germinación encontradas en P. mexicana y la similitud o diferencia de estas en comparación con las de otras especies forestales, resalta la importancia de realizar estudios para comprender el papel especie-específico del peso o tamaño de las semillas (Gelviz-Gelvez et al., 2020). Esto es particularmente importante por las implicaciones prácticas de dicha información, ya que los datos aportan información útil para desarrollar las estrategias adecuadas de manejo de las semillas de P. mexicana, porque, por ejemplo, con los resultados se tiene identificado el peso idóneo con los que se tiene una tasa más alta de germinación.
Adicionalmente, con base en el ajuste del modelo Weibull, P. mexicana tiene una mayor tasa de germinación entre los 10 y 12 días después de la siembra, bajo las condiciones del ensayo (Fig. 6B). Este tiempo es menor que el de P. paniculata cuya germinación, en condiciones de laboratorio, ocurre entre los 14 y 19 días (Rivera-Martin et al., 2013). En P. purpurea se reporta que la germinación inicia entre los cinco y ocho días (Mosquera Mena y Ruíz Flórez, 2015). Es posible que estas diferencias se deban a las características intrínsecas de cada especie, como anteriormente se mencionó, pero tampoco se descarta que también estén implicadas desviaciones de tipo experimental, como ocurre al comparar ensayos en condiciones de laboratorio con los de condiciones naturales, ya sean estos últimos en campo o vivero.
En conclusión, los rasgos morfológicos de las semillas de P. mexicana varían a nivel intrapoblacional. El peso de la semilla afecta la capacidad germinativa. Finalmente, debido a la amplia variación en el peso de las semillas, se sugiere una clasificación preliminar de tres categorías según los análisis de distribución de pesos (Fig. 7), de modo que en correspondencia al esquema de clasificación propuesto por Baskin y Baskin (2014), las semillas de P. mexicana pueden considerarse como monomórficas por presentar un pico unimodal con distribución normal o sesgada.
Agradecimientos
Se agradece a Cenobio Calixto por las facilidades otorgadas en su predio para el establecimiento del ensayo en vivero.
Literatura citada
Aguirre-Dugua, X., L. E. Eguiarte, A. González-Rodríguez y A. Casas. 2012. Round and large: morphological and genetic consequences of artificial selection on the gourd tree Crescentia cujete by the Maya of the Yucatan Peninsula, Mexico. Annals of Botany 109(7): 1297-1306. DOI: https://doi.org/10.1093/aob/mcs068
Baraloto, C., P. M. Forget y D. E. Goldberg. 2005. Seed mass, seedling size and neotropical tree seedling establishment. Journal of Ecology 93(6): 1156-1166. DOI: https://doi.org/10.1111/j.1365-2745.2005.01041.x
Bareke, T. 2018. Biology of seed development and germination physiology. Advance in Plants & Agriculture Research 8(4): 336-346. DOI: https://doi.org/10.15406/apar.2018.08.00335
Barrace, A., J. Beer, D. H. Boshier, J. Chamberlain, J. Cordero, G. Detlefsen, B. Finegan, G. Galloway, M. Gómez, J. Gordon, M. Hands, J. Hellin, C. Hughes, M. Ibrahim, D. Kass, R. Leakey, F. Mesén, M. Montero, C. Rivas, E. Somarriba, J. Stewart y T. Pennington. 2003. Árboles de Centroamérica: un manual para extensionistas. Oxford Forestry Institute/Centro Agronómico Tropical de Investigación y Enseñanza. Turrialba, Costa Rica. 1079 pp.
Baskin, C. C. y J. M. Baskin. 2014. Seeds: Ecology, Biogeography, and Evolution of Dormancy and Germination. Ed. 2. Elsevier. San Diego, USA. 1586 pp. DOI: https://doi.org/10.1016/B978-0-12-080260-9.X5000-3
Calixto Valencia, C. G., V. M. Cetina Alcalá, C. Ramírez Herrera, M. Á. López López, G. Ángeles-Pérez, A. Equihua Martínez y E. Basave Villalobos. 2022. Características morfométricas, reproductivas y germinativas del germoplasma de Swietenia humilis Zucc. en Guerrero. Revista Mexicana de Ciencias Forestales 13(72): 148-172. DOI: https://doi.org/10.29298/rmcf.v13i72.1250
Chok, N. S. 2010. Pearson’s versus Spearman’s and Kendall’s correlation coefficients for continuous data. Master’s Thesis. Graduate School of Public Health, University of Pittsburgh. Pittsburgh, PA, USA. 43 pp.
Deb, P. y R. C. Sundriyal. 2017. Effect of seed size on germination and seedling fitness in four tropical rainforest tree species. Indian Journal of Forestry 40(4): 313-322. DOI: https://doi.org/10.54207/bsmps1000-2017-6jbcpr
García Azpeitia, L., G. J. Labrada-Delgado, E. Montalvo-González y S. Loza-Cornejo. 2022. Caracteres morfométricos y anatómicos de frutos y semillas de Prosopis laevigata (Fabaceae) en Lagos de Moreno, Jalisco, Mexico. Acta Botanica Mexicana 129: e2057. DOI: https://doi.org/10.21829/ABM129.2022.2057
Gelviz-Gelvez, S. M., N. P. Pavón, J. Flores, F. Barragán y H. Paz. 2020. Germination of seven species of shrubs in semiarid central Mexico: Effect of drought and seed size. Botanical Sciences 98(3): 464-472. DOI: https://doi.org/10.17129/BOTSCI.2537
González-Vélez, G., A. R. Andrés-Hernández, G. Valdez-Eleuterio, N. Álvarez-Quiroz, D. Martínez-Moreno y S. P. Rivas-Arancibia. 2020. Germinación de semillas de seis especies arbóreas maderables de una selva baja caducifolia en Puebla, México. Agrociencia 54(2): 227-240.
Hernández-Anguiano, L. A., J. López-Upton, C. Ramírez-Herrera y A. Romero-Manzanares. 2018. Variación en germinación y vigor de semillas de Pinus cembroides y Pinus orizabensis. Agrociencia 52(8): 1161-1178.
Khurana, E. y J. S. Singh. 2001. Ecology of seed and seedling growth for conservation and restoration of tropical dry forest: a review. Environmental Conservation 28(1): 39-52. DOI: https://doi.org/10.1017/S0376892901000042
Lessa, B. F. da T., J. P. N. de Almeida, C. L. Pinheiro, F. C. B. Nogueira y S. Medeiros Filho. 2014. Germinação e crescimento de plântulas de Enterolobium contortisiliquum (Vell.) Morong em função da localização da semente no fruto e regimes de temperatura. Bioscience Journal 30(5): 1474-1483.
Lozano, E. C., M. A. Zapater, C. Mamani, C. B. Flores, M. N. Gil y S. S. Sühring. 2016. Efecto de pretratamientos en semillas de Enterolobium contortisiliquum (Fabaceae) de la Selva Pedemontana Argentina. Boletín de la Sociedad Argentina de Botánica 51(1): 79-87. DOI: https://doi.org/10.31055/1851.2372.v51.n1.14414
Luna-Nieves, A. L., J. A. Meave, E. J. González, J. Cortés-Flores y G. Ibarra-Manríquez. 2019. Guiding seed source selection for the production of tropical dry forest trees: Coulteria platyloba as study model. Forest Ecology and Management 446: 105-114. DOI: https://doi.org/10.1016/j.foreco.2019.05.020
Machuca Machuca, K., E. Martínez Salas y M.-S. Samain. 2022. Peltogyne mexicana. The IUCN Red List of Threatened Species 2022: e.T200749596A200816012. DOI: https://doi.org/10.2305/IUCN.UK.2022-1.RLTS.T200749596A200816012.en
Martin, A. D., K. M. Quinn y J. H. Park. 2011. MCMCpack: Markov chain Monte Carlo in R. Journal of Statistical Software 42(9): 1-21. DOI: https://doi.org/10.18637/jss.v042.i09
Mosquera Mena, R. A. y L. Á. Ruíz Flórez 2015. Evaluación del desarrollo en vivero de Peltogyne purpurea Pittier (Nazareno). Revista de Investigación Agraria y Ambiental 6(2): 261-274. DOI: https://doi.org/10.22490/21456453.1422
Murali, K. S. 1997. Patterns of seed size, germination and seed viability of tropical tree species in Southern India. Biotropica 29(3): 271-279. DOI: https://doi.org/10.1111/j.1744-7429.1997.tb00428.x
Navarro-Martínez, J. 2001. Contribución al conocimiento de Palo Morado (Peltogyne mexicana Martínez), una especie amenazada de Guerrero, México. Tesis de maestría. División de Ciencias Forestales, Universidad Autónoma Chapingo. Chapingo, Estado de México, México. 208 pp.
Navarro-Martínez, J., A. Borja-de la Rosa y R. Machuca-Velasco. 2005. Características tecnológicas de la madera de palo morado (Peltogyne mexicana Martínez) de Tierra Colorada, Guerrero, México. Revista Chapingo Serie Ciencias Forestales y del Ambiente 11(1): 73-82.
Norden, N., M. I. Daws, C. Antoine, M. A. Gonzalez, N. C. Garwood y G. Chave. 2009. The relationship between seed mass and mean time to germination for 1037 tree species across five tropical forests. Functional Ecology 23(1): 203-210. DOI: https://doi.org/10.1111/j.1365-2435.2008.01477.x
Pramono, A. A., D. Syamsuwida y K. P. Putri. 2019. Variation of seed sizes and its effect on germination and seedling growth of mahogany (Swietenia macrophylla). Biodiversitas Journal of Biological Diversity 20(9): 2576-2582. DOI: https://doi.org/10.13057/biodiv/d200920
R Core Team. 2021. R: A language and environment for statistical computing. R Foundation for Statistical Computing. Vienna, Austria. http://www.R-project.org/
Rivera-Martin, L. E., M. C. Peñuela-Mora, E. M. Jiménez R. y M. del P. Vargas J. 2013. Ecología y silvicultura de especies útiles amazónicas: Abarco (Cariniana micrantha Ducke), Quinilla (Manilkara bidentata (A. DC.) A. Chev.) y Violeta (Peltogyne paniculata Benth.). Universidad Nacional de Colombia (Sede Amazonia)-Instituto Amazónico de Investigaciones. Leticia, Colombia. 180 pp.
Romero-Saritama, J. M. 2016. Caracterización morfofisiológica de semillas de especies leñosas distribuidas en dos zonas secas presentes en el Sur del Ecuador. Ecosistemas 25(2): 93-100. DOI: https://doi.org/10.7818/ECOS.2016.25-2.12
Romero-Saritama, J. M. y C. Pérez Ruíz. 2016. Rasgos morfológicos de semillas y su implicación en la conservación ex situ de especies leñosas en los bosques secos tumbesinos. Ecosistemas 25(2): 59-65. DOI: https://doi.org/10.7818/ECOS.2016.25-2.07
Salazar, R., C. Soihet y J. Mendez. 2000. Manejo de semillas de 100 especies forestales de America Latina. Volumen I. Centro Agronómico Tropical de Investigación y Enseñanza. Turrialba, Costa Rica. 204 pp.
SEMARNAT. 2010. NORMA Oficial Mexicana NOM-059-SEMARNAT-2010. Protección ambiental-Especies nativas de México de flora y fauna silvestres-Categorías de riesgo y especificaciones para su inclusión, exclusión o cambio-Lista de especies en riesgo. Secretaría del Medio Ambiente y Recursos Naturales. Diario Oficial de la Federación. Cd. Mx., México. http://dof.gob.mx/nota_detalle.php?codigo=5173091&fecha=30/12/2010 (consultado diciembre de 2022).
Soriano, D., A. Orozco-Segovia, J. Márquez-Guzmán, K. Kitajima, A. Gamboa-de Buen y P. Huante. 2011. Seed reserve composition in 19 tree species of a tropical deciduous forest in Mexico and its relationship to seed germination and seedling growth. Annals of Botany 107(6): 939-951. DOI: https://doi.org/10.1093/aob/mcr041
Sotuyo, S. 2014. El palo morado (Peltogyne mexicana), una leguminosa maderable con futuro incierto y parientes lejanos. Revista Digital Universitaria 15(4): 1-8.
Souza, M. L., R. R. Solar y M. Fagundes. 2015. Reproductive strategy of Copaifera langsdorffii (Fabaceae): more seeds or better seeds? Revista de Biología Tropical 63(4): 1161-1167.
Trindade-Lessa, B. F., J. Paulo Nobre-de Almeida, C. Lobo-Pinheiro, F. Melo-Gomes y S. Medeiros-Filho. 2015. Germination and seedling growth of Enterolobium contortisiliquum as a function of seed weight and temperature and light conditions. Agrociencia 49(3): 315-327.
Turner, I. M. 2004. The ecology of trees in the Tropical Rain Forest. Cambridge University Press. Cambridge, UK. 298 pp. DOI: https://doi.org/10.1017/CBO9780511542206
Venables, W. N. y B. D. Ripley. 2002. Modern Applied Statistics with S. Springer. New York, USA. DOI: https://doi.org/10.1007/978-0-387-21706-2
Viveros Viveros, H., J. D. Hernández Palmeros, M. V. Velasco García, R. Robles Silva, C. Ruiz Montiel, A. Aparicio Rentería, M. J. Martínez Hernández, J. Hernández Villa y M. L. Hernández Hernández. 2015. Análisis de semilla, tratamientos pregerminativos de Enterolobium cyclocarpum (Jacq.) Griseb. y su crecimiento inicial. Revista Mexicana de Ciencias Forestales 6(30): 52-65.
WFO. 2023. World Flora Online. http://www.worldfloraonline.org/ (consultado abril de 2023).
Willan, R. L. 1991. Guía para la manipulación de semillas forestales. Estudio FAO Montes (20/2). Centro de Semillas Forestales de DANIDA. Roma, Italia. https://www.fao.org/3/ad232s/ad232s00.htm#TOC (consultado marzo de 2023).
Contribución de autores
Financiamiento
Notas de autor
6Autor para la correspondencia: celi86_2@hotmail.com
