Artículos de investigación
Delimitación de especies del complejo Cercocarpus fothergilloides (Rosaceae)
Species boundaries among the Cercocarpus fothergilloides complex (Rosaceae)
Delimitación de especies del complejo Cercocarpus fothergilloides (Rosaceae)
Acta botánica mexicana, no. 131, e2310, 2024
Instituto de Ecología A.C., Centro Regional del Bajío
Received: 23 January 2024
Revised document received: 23 February 2024
Accepted: 03 May August 2024
Funding
Funding source: El Consejo Nacional de Humanidades, Ciencias y Tecnologías
Contract number: 926811
Funding statement: El Consejo Nacional de Humanidades, Ciencias y Tecnologías de México apoyó con una beca (número de beca 926811)
Resumen
Antecedentes y Objetivos: Cercocarpus (Dryadoideae, Rosaceae) es un género endémico del centro-oeste de Estados Unidos de América y México. Tres revisiones taxonómicas reconocen de seis a 21 especies, las cuales han sido delimitadas principalmente con base en caracteres morfológicos foliares, y están agrupadas en los complejos C. ledifolius, C. betuloides, C. montanus y C. fothergilloides. El complejo Cercocarpus fothergilloides incluye cuatro taxones endémicos de México, que presentan variación morfológica y podrían reconocerse más especies. Los objetivos de este trabajo fueron identificar y delimitar las especies del complejo C. fothergilloides, determinar si hay correlación de los caracteres con respecto a la latitud y longitud, además de describir la anatomía y arquitectura foliar.
Métodos: Cuantificamos 13 caracteres morfológicos foliares y florales, y ocho anatómicos de la hoja. Utilizamos dos Análisis Discriminantes Canónicos (ADCs) para examinar los datos morfo-anatómicos cuantitativos. Con los caracteres cuantitativos más importantes del ADC y diez caracteres cualitativos morfo-anatómicos y de arquitectura foliar, realizamos un análisis de agrupamiento para reconocer grupos. Efectuamos un análisis de correlación entre los caracteres con latitud y longitud.
Resultados clave: El número de venas secundarias, la longitud de la lámina, de los pedicelos en fruto, del estilo y del fruto fueron los caracteres morfológicos que permitieron diferenciar a las especies. Las características anatómicas del grosor de la hoja y la cutícula, el alto del parénquima en empalizada y de la epidermis, así como la profundidad de la cripta distinguieron a los taxones. El análisis de agrupamiento diferenció siete grupos. No hubo correlación entre la mayoría de los caracteres con latitud y longitud.
Conclusiones: El complejo Cercocarpus fothergilloides comprende siete entidades, y tres de ellas son nuevas. Todas se distinguen por combinaciones de caracteres morfológicos, anatómicos y de arquitectura foliar.
Palabras clave: Análisis de correlación+ Análisis Discriminante Canónico+ delimitación de especies+ Dryadoideae+ morfometría.
Abstract
Background and Aims: Cercocarpus (Dryadoideae, Rosaceae) is an endemic genus to the central-western United States of America and Mexico. Three taxonomic revisions recognize six to 21 species, which have been delimited mainly based on morphological foliar characters and are grouped into the complexes C. ledifolius, C. betuloides, C. montanus and C. fothergilloides. The Cercocarpus fothergilloides complex includes four taxa endemic to Mexico, but present morphological variation and more species could be recognized. The aims of this work were to identify and delimit the species of the fothergilloides complex, establish if the characters correlate with latitude and longitude as well as describe the anatomy and leaf architecture.
Methods: We quantified 13 foliar and floral morphological characters and eight anatomical ones of the leaf. We used two Canonical Discriminant Analyzes (CDAs) to examine the quantitative morpho-anatomical data. With the most important quantitative characters from the CDA and ten qualitative morpho-anatomical and leaf architecture ones, we performed a clustering analysis to recognize groups. A correlation analysis between characters and latitude and longitude was performed.
Key results: The number of secondary veins, the length of the lamina, the fruit pedicel, the style and the fruit were the morphological characters that allowed differentiating species. Anatomical characteristics such as the thickness of the leaf and cuticle, the height of the palisade parenchyma and epidermis, as well as the depth of the crypt distinguished the taxa. The cluster analysis differentiated seven species. There was not a correlation between most characters with latitude and longitude.
Conclusions: The Cercocarpus fothergilloides complex comprises seven species and three of these are new. The species are distinguished by combinations of morphological, anatomical and leaf architecture characters.
Key words: Canonical Discriminant Analysis, correlation analysis, Dryadoideae, morphometry, species delimitation.
Introducción
Cercocarpus Kunth (Dryadoideae, Rosaceae) es un género endémico del centro-oeste de Estados Unidos de América y México (Henrickson y Vanden Heuvel, 2014). Las plantas habitan el bosque de Quercus, bosque de coníferas, bosque mesófilo de montaña y matorral xerófilo (Martin, 1950; Rzedowski y Calderón de Rzedowski, 2005). Cercocarpus agrupa árboles y arbustos con hojas simples, flores carentes de pétalos, con hipantio tubular abierto en un limbo deciduo con cinco sépalos, el gineceo es unicarpelar con un óvulo y su fruto es un aquenio con estilo acrescente similar a una cola (Martin, 1950; Henrickson y Vanden Heuvel, 2014).
En México se registran 9-12 especies de Cercocarpus (Vanden Heuvel, 2002; Villaseñor, 2016), pero en general el número reconocido varía de un autor a otro. Schneider (1905b) aceptó diez especies agrupadas en los complejos C. betulaefolius, C. ledifolius y C. fothergilloides. Por su parte, Rydberg (1913) registró 21 sin dividirlas en complejos. Más tarde, Martin (1950) propuso seis con 11 variedades en tres complejos. Lis (1992) reconoció diez taxones y ocho variedades agrupadas en los complejos C. betuloides, C. montanus, C. ledifolius y C. fothergilloides. Este último es endémico de México e incluye C. fothergilloides Kunth, C. mojadensis C.K. Schneid., C. pringlei (C.K. Schneid.) Rydb. y C. macrophyllus C.K. Schneid. Este complejo se caracteriza por presentar hojas con textura coriácea, venas prominentes en el envés y tricomas en las anteras, tiene las hojas más grandes del género y el mayor número de flores por inflorescencia (Martin, 1950). En todas las revisiones, dentro del complejo C. fothergilloides, se reconocen cuatro especies.
En sistemática, la delimitación taxonómica es un debate recurrente. Una especie es un grupo de individuos con características morfológicas comunes que no muestran formas intermedias con otros taxones cuando crecen en simpatría (Mallet, 1995). Esta es la unidad fundamental de la taxonomía (de Queiroz, 2005). Sin embargo, su identificación y delimitación es difícil en muchos casos (Duminil y Di Michele, 2009), por ejemplo, cuando encontramos complejos de especies. Hay tres escenarios que los producen (Freudenstein et al., 2017; Pinheiro et al., 2018): en el primero, la formación de linajes está acompañada por poca variación morfológica; en el segundo, hay modificaciones morfológicas sin cambios genéticos, mientras que el tercero implica surgimiento de especies morfológicamente diferentes a partir de una población ancestral (Freudenstein et al., 2017). El complejo C. fothergilloides muestra poca variabilidad genética (Vanden Heuvel y Linder, 2001; Vanden Heuvel, 2002), pero mucha diversidad morfológica (Martin, 1950). La principal fuente de información para separar especies en Cercocarpus ha sido la morfología foliar; son pocos los caracteres florales empleados en trabajos taxonómicos porque presentan elevada variación y sobrelape morfológico entre los taxones (Martin, 1950). Lis (1992) estudió la arquitectura foliar de los taxones reconocidos por Martin (1950) y encontró que los patrones de venación ayudan a identificar y diferenciar taxones; sin embargo, revisó poco material y no resolvió los problemas taxonómicos del complejo C. fothergilloides. Por su parte, otros autores han documentado que la anatomía es útil en la delimitación taxonómica (Zamora-Natera y Terrazas, 2012; Pacheco-Seixasa et al., 2019) y para describir nuevos taxones de angiospermas (Ceja-Romero et al., 2009). Por lo tanto, esperamos que en el complejo C. fothergilloides, la morfología, anatomía y arquitectura foliar aporten información para el reconocimiento y circunscripción de las entidades taxonómicas. Si los caracteres están asociados a la distribución, entonces podríamos explicar su variación. Los objetivos de este trabajo fueron delimitar a las especies del complejo C. fothergilloides mediante caracteres morfológicos, anatómicos y de arquitectura foliar, y determinar si hay correlación de dichos caracteres con respecto a latitud y longitud. Además, describir la anatomía y arquitectura foliar de los taxones agrupados en el complejo C. fothergilloides.
Materiales y Métodos
Identificación de taxones putativos
En la revisión de especímenes depositados en las colecciones científicas consultadas, identificamos las cuatro especies del complejo C. fothergilloides. En la determinación de especies incluimos los trabajos de Schneider (1905a, b), Rydberg (1913), Martin (1950) y Lis (1992). Además, encontramos tres morfoespecies que no pudieron ser identificadas o relacionadas con ninguna de las especies reconocidas previamente. En el Cuadro 1 está la lista de taxones estudiados en este trabajo, los nombres de los estados donde se distribuyen fueron abreviados de acuerdo con INEGI (2020).

Caracteres morfológicos cuantitativos
Se revisaron y fotografiaron 104 especímenes del complejo Cercocarpus fothergilloides (Apéndice 1). El material incluyó ejemplares herborizados depositados en los herbarios ENCB (Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional), FCME (Facultad de Ciencias, Universidad Nacional Autónoma de México (UNAM)), IBUG (Instituto de Botánica, Universidad de Guadalajara), IEB (Centro Regional del Bajío, Instituto de Ecología, A.C.), MEXU (Instituto de Biología, UNAM) y UAMIZ (Departamento de Biología, Universidad Autónoma Metropolitana Iztapalapa) (acrónimos citados de acuerdo con Thiers, 2022). También se incluyó material obtenido de recolectas en campo, e imágenes de los tipos nomenclaturales depositados en JSTOR Global Plants (JSTOR, 2022). Trece caracteres vegetativos y florales, de posible importancia taxonómica, fueron cuantificados (Cuadro 2, Fig. 1). Para cada uno de los caracteres se efectuaron hasta diez mediciones por ejemplar, con el programa ImageJ v. 1.52a (Abràmoff et al., 2004; Rasband, 2019).
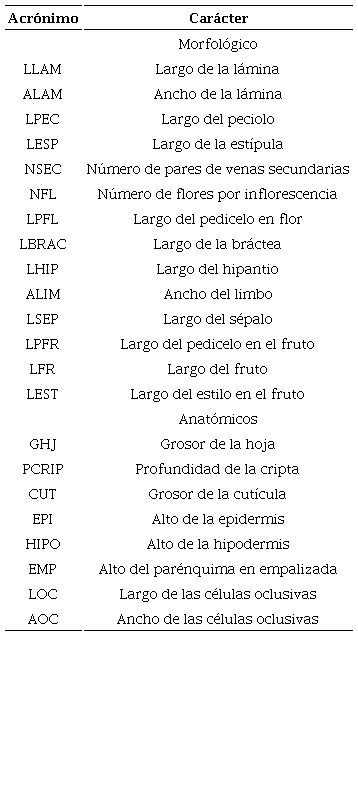
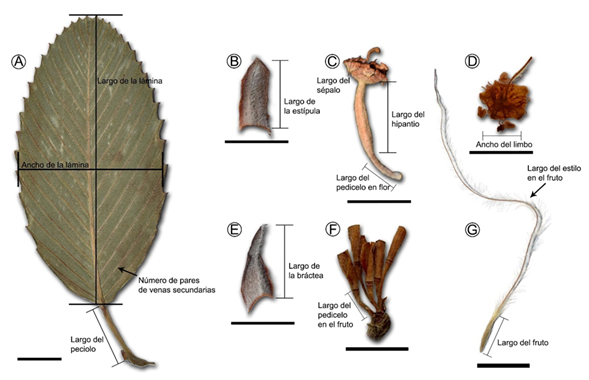
Figura 1:
Algunos caracteres morfológicos cuantitativos incluidos en los Análisis Discriminantes Canónicos. Las flechas y líneas indican cómo se midió cada carácter. A. hoja de Cercocarpus macrophyllus C.K. Schneid.; B. estípula de Cercocarpus sp. 1; C. flor de C. mojadensis C.K. Schneid.; D. limbo de Cercocarpus sp. 1; E. bráctea de Cercocarpus sp. 1; F. inflorescencia de Cercocarpus sp. 2; G. fruto de C. macrophyllus C.K. Schneid. Escala: 1 cm en A, F, G y 0.5 cm en B-E.
Caracteres anatómicos cuantitativos
Se examinaron 25 especímenes provenientes de recolectas de campo y ejemplares depositados en los herbarios FCME, IBUG y MEXU (Apéndice 2). Se tomando muestras de hoja de los ejemplares se hirvieron durante 10-20 min en una parrilla eléctrica (AR-300 Fabricantes Feligneo, Zapopan, México) con agua corriente. Una vez hidratadas, se cortaron y se utilizó solamente el tercio medio de la lámina. Estos pedazos se colocaron en NaOH al 20% hasta obtener una coloración uniforme. Posteriormente, fueron colocados en etilendiamina al 50% durante 72 h.
Los fragmentos de hojas se insertaron en una zanahoria para darles soporte y poder realizar los cortes a 50 μm en un micrótomo de rotación (RM2125 Leica, Wetzlar, Alemania). La mitad de los cortes fueron aclarados con cloro al 50%. La tinción se realizó con safranina-verde rápido y el montaje en resina sintética (Ruzin, 1999).
Las fotografías de los cortes se obtuvieron con un microscopio (BX51 Olympus, Tokio, Japón) y las mediciones fueron realizadas con el programa Image Pro-plus v. 7.1 (Image Pro-plus, 2019). Al final, se analizaron ocho caracteres (Cuadro 2, Fig. 2).
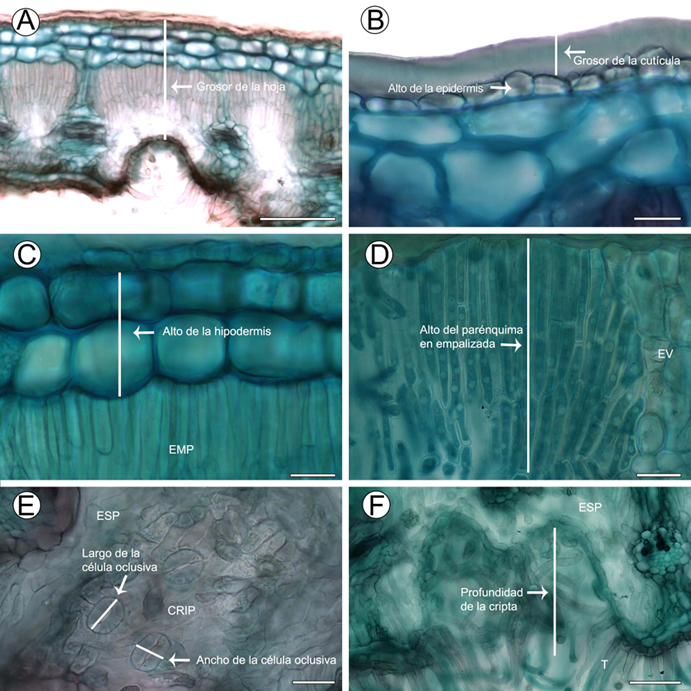
Figura 2:
Caracteres anatómicos cuantitativos incluidos en los Análisis Discriminantes Canónicos. Las flechas y líneas indican cómo medimos cada carácter. A. hoja de Cercocarpus macrophyllus C.K. Schneid.; B. detalle de la cutícula y epidermis de Cercocarpus pringlei (C.K. Schneid.) Rydb.; C. hipodermis de C. mojadensis C.K. Schneid.; D. parénquima en empalizada de C. macrophyllus C.K. Schneid.; E. aparatos estomáticos de C. fothergilloides Kunth; F. cripta de C. fothergilloides. Abreviaciones. EMP=parénquima en empalizada. ESP=parénquima esponjoso. EV=extensión de la vaina. CRIP=cripta. T=tricomas. Escala: 100 μm en A, 20 μm en B-E, 50 μm en F.
Caracteres cualitativos
Se construyó una matriz de caracteres morfológicos foliares y florales, anatómicos y de arquitectura foliar con base en la revisión de los ejemplares de herbario que están sintetizados en el Cuadro 3. El análisis de la arquitectura foliar implicó identificar y describir los patrones de venación. Se utilizó el segundo tercio de la hoja con la vena media, una región intercostal y el margen (Martínez-Cabrera et al., 2007). Las hojas se colocaron en NaOH al 20% durante 24 h a temperatura ambiente y 1 h en la estufa (ED26 Binder, Tuttlingen, Alemania) a 60 °C. Posteriormente, se aclararon en cloro al 50% hasta que tuvieron una coloración uniforme para después enjuagar con agua corriente.

La deshidratación del tejido se hizo con diferentes concentraciones de alcohol (50%, 70%, 96%), cada uno por 24 h. Después, se dejaron en solución aclaradora durante 72-94 h (Martínez-Cabrera et al., 2007). Pasado ese tiempo, se lavaron en alcohol al 96% por 30 min, posteriormente, fueron colocadas en alcohol al 96% durante 24 h. La tinción se realizó con safranina por 1 h. Por último, las muestras estuvieron en xilol durante 24 h para finalmente montarlas en resina sintética (Ruzin, 1999).
Análisis estadísticos
Se realizaron dos Análisis Discriminantes Canónicos (ADCs) con los programas R (R Core Team, 2018) y SAS® v. 2.8 (SAS Institute Inc., 2018). El primer ADC analizó los caracteres morfológicos vegetativos y florales; el segundo los caracteres anatómicos. Las variables dependientes fueron las cuatro especies del complejo C. fothergilloides y las tres morfoespecies. Las variables independientes fueron los caracteres cuantitativos.
Los caracteres morfológicos y anatómicos se analizaron por separado para determinar la capacidad de cada uno para discriminar a las especies. Los gráficos se generaron en el programa RStudio v. 1.2.5033 (RStudio Team, 2019) mediante la paquetería ggplot2. Los datos se transformaron con logaritmo natural para cumplir con los supuestos paramétricos (Hair et al., 1999). Se incluyó el análisis de distancias cuadradas de Mahalanobis para determinar si había diferencias significativas entre los centroides de los grupos (especies). Con base en los ADCs, el programa SAS realizó un Análisis Discriminante Clasificatorio (ACC). Para clasificar las variables cuantitativas a partir de grupos conocidos, las observaciones se catalogan en los grupos ya establecidos con base en la similitud de sus características (Sánchez et al., 2013; 2020). Del ACC se obtiene un porcentaje de clasificación que indica cuántas observaciones se ubicaron en cada grupo.
El análisis de agrupamiento se realizó en el programa STATISTICA v. 7.0 (StaSoft, 2004). Este incluyó a los 25 individuos analizados con anatomía foliar, que representan los grupos recuperados por los análisis discriminantes. Para ello, se hizo una matriz de datos con el promedio de los caracteres cuantitativos con mayor aporte en la discriminación de grupos en los ADCs. Además, se incluyeron diez caracteres cualitativos (Cuadro 3). La matriz de similitud se realizó con base en Distancias Euclidianas. El dendograma se construyó con el Método de Agrupamiento en Pares no Ponderados utilizando Promedios Aritméticos (UPGMA) y se buscó la distancia mínima en la cual se pudieran recuperar las descritas del complejo C. fothergilloides (Sánchez et al., 2020).
Se ejecutó un análisis de correlación de Pearson entre los caracteres cuantitativos con mayor contribución en los ADCs con respecto a la latitud y la longitud, ya que ambas distancias se han utilizado para explicar la variación morfo-anatómica con respecto a la distribución geográfica (Terrazas et al., 2008; Ramírez-Diaz, 2016). Los registros que carecían de latitud y longitud fueron georreferenciados con Google Earth Pro v. 7.3 (Google Inc., 2020). Los análisis de correlación se realizaron en el programa PAST v. 3.16 (Hammer et al., 2001). El coeficiente de correlación estimó el grado de covariación lineal entre las variables cuantitativas. Una correlación alta tuvo coeficientes >0.7.
Descripción de la morfología, arquitectura y anatomía foliar
La descripción morfológica de la hoja, su arquitectura y anatomía se realizaron con base en la terminología de Metcalfe y Chalk (1950), Hickey (1973), Cutler et al. (2008) y Ellis et al. (2009). Las descripciones de la arquitectura y anatomía fueron hechas con base en la lista de caracteres utilizada por Mortenson (1973) y Lis (1992).
Resultados
Con base en la información de los trabajos consultados y la revisión de ejemplares, reconocimos siete taxones: C. fothergilloides, C. macrophyllus, C. mojadensis, C. pringlei, Cercocarpus sp. 1, Cercocarpus sp. 2 y Cercocarpus sp. 3. La revisión de literatura y de los ejemplares de herbario permitió generar la lista de caracteres cuantitativos y la matriz cualitativa (Cuadros 2, 3). Estos caracteres se evaluaron con los análisis estadísticos.
Análisis discriminante con caracteres morfológicos
La tres primeras funciones del ADC explicaron 67.3%, 18.4% y 9.6% de la variación (95.3%) (lambda de Wilks p<0.05). La variación de las dos primeras funciones se muestra en la Figura 3A y fue posible reconocer cinco grupos con los extremos de la variación traslapados entre ellos.
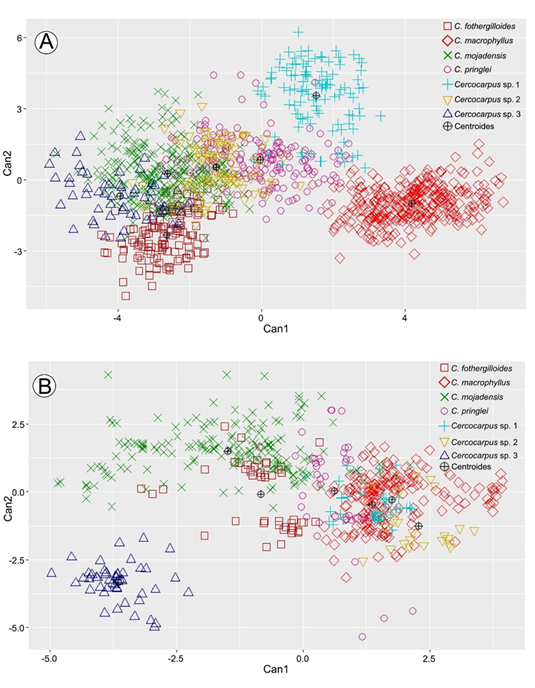
Figura 3:
Gráficas de los Análisis Discriminantes Canónicos. A. dos primeras funciones del ADC de los caracteres morfológicos; B. dos primeras funciones del ADC de los caracteres anatómicos. Abreviaciones. Can1=primera función canónica. Can2=segunda función canónica.
Los coeficientes canónicos mostraron que, en la primera función el número de pares de venas secundarias (NSEC) y largo de la lámina (LLAM) fueron los caracteres con mayor contribución (Cuadro 4). Cercocarpus macrophyllus, Cercocarpus sp. 1 y C. pringlei se separaron en los valores positivos de la primera función al presentar hojas más largas y mayor número de pares de venas secundarias (Figs. 3A, 4A, B). Por su parte, en los valores negativos se encontraron C. fothergilloides, C. mojadensis, Cercocarpus sp. 2 y Cercocarpus sp. 3, ya que estas tienen hojas de menor tamaño y menos número de venas secundarias.
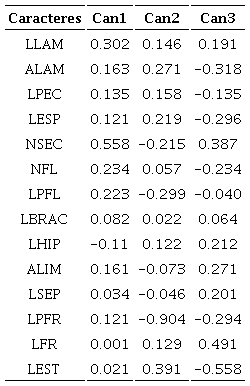

Figura 4:
Diagramas de caja y bigotes de los once caracteres con mayor carga en los Análisis Discriminantes Canónicos. El primer y tercer cuartil se representan por la caja. La mediana se indica por la línea adentro de la caja. Los bigotes indican los valores mínimos y máximos de cada variable.
En la segunda función, la longitud del pedicelo en el fruto (LPFR) y el estilo en el fruto (LEST) tuvieron la mayor contribución (Cuadro 4). Cercocarpus macrophyllus se agrupó en los valores negativos de la segunda función por presentar pedicelos más largos en el fruto, mientras que C. fothergilloides y Cercocarpus sp. 3 estuvieron en los valores negativos de la segunda función por tener pedicelos de al menos 1 mm en los frutos (Fig. 4C). Entre los valores negativos y positivos se agruparon C. mojadensis, C. pringlei y Cercocarpus sp. 2, las cuales presentan estilos de mayor longitud en los frutos maduros.
Por último, en la tercera función, largo del fruto (LFR) y ancho de la lámina (ALAM) fueron los caracteres con mayor aporte para discriminar grupos (Cuadro 4, Apéndice 3). Cercocarpus mojadensis, C. pringlei y Cercocarpus sp. 2 se traslaparon en los extremos de variación (Fig. 3A).
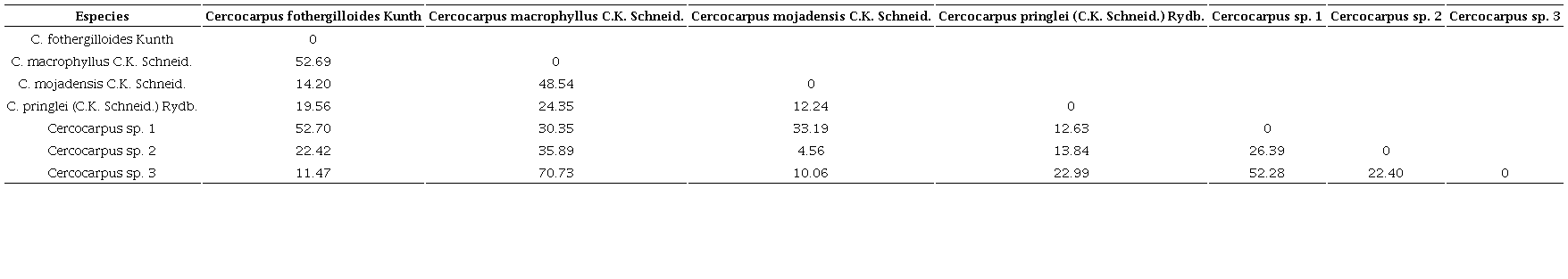
Las distancias cuadradas de Mahalanobis (D2) mostraron diferencias significativas (p<0.05) entre los siete taxones. Las especies menos distantes fueron C. mojadensis y Cercocarpus sp. 2. En contraste, las más alejadas fueron C. macrophyllus y Cercocarpus sp. 3 (Cuadro 5). El porcentaje de clasificación de C. macrophyllus, Cercocarpus sp. 2, C. fothergilloides y Cercocarpus sp. 1 superó el 85% (Cuadro 6). Por el contrario, C. mojadensis, C. pringlei y Cercocarpus sp. 3 presentaron bajos porcentajes de clasificación.

Análisis discriminante con caracteres anatómicos
La tres primeras funciones del ADC explicaron 56.09%, 29.58% y 8.13% de la variación, que en total sumó 93.8% (lambda de Wilks p<0.05). El gráfico de las dos primeras funciones (Fig. 3B) separó cuatro grupos con amplia variación.
Los coeficientes canónicos mostraron que en la primera función el grosor de la hoja (GHJ) y alto de la hipodermis (HIPO) mostraron la mayor contribución (Cuadro 7). En los valores negativos de la primera función canónica se agruparon Cercocarpus sp. 3, C. mojadensis y C. fothergilloides estas presentaron hojas más gruesas e hipodermis más altas (Fig. 4G-H), mientras que C. macrophyllus, C. pringlei, Cercocarpus sp. 1 y Cercocarpus sp. 2 se agruparon en los valores positivos, al tener hojas más delgadas (Fig. 4G).
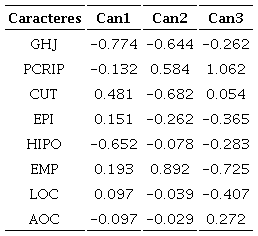
En la segunda función, grosor de la cutícula (CUT) y alto del parénquima en empalizada (EMP) fueron los caracteres con mayor importancia (Cuadro 7). En los valores negativos de la segunda función canónica se separó Cercocarpus sp. 3, taxón que presentó las cutículas más gruesas (Fig. 4I). En los valores positivos se discriminó C. mojadensis por tener el parénquima en empalizada más alto.
Mientras que, en la tercera función, la profundidad de la cripta (PCRIP) fue el carácter con mayor contribución (Cuadro 7, Apéndice 3). Cercocarpus fothergilloides y C. mojadensis se traslaparon en los extremos de variación. En los valores negativos y positivos de la segunda función canónica fueron incapaces de distinguir entre C. macrophyllus, C. pringlei, Cercocarpus sp. 1 y Cercocarpus sp. 2.
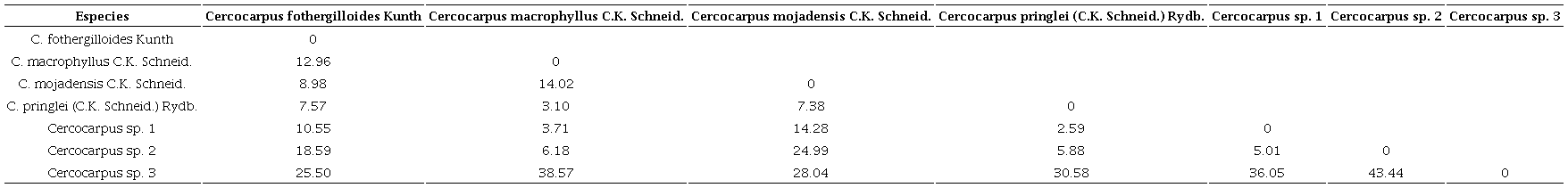
No obstante, las distancias cuadradas de Mahalanobis (D2) resultaron significativas (p<0.05) entre todas. Cercocarpus pringlei y Cercocarpus sp. 1 fueron las menos distantes. En el otro extremo, las más alejadas fueron Cercocarpus sp. 3 y Cercocarpus sp. 2. (Cuadro 8). Cercocarpus fothergilloides y Cercocarpus sp. 2 tuvieron un porcentaje de clasificación mayor del 85% (Cuadro 9) y Cercocarpus sp. 3 registro una clasificación correcta de 100%. En C. macrophyllus, C. mojadensis, C. pringlei y Cercocarpus sp. 1, el porcentaje de clasificación fue bajo (Cuadro 9).

Análisis de agrupamiento
Establecimos un umbral en la distancia mínima en la que se separaron las cuatro especies descritas del complejo C. fothergilloides. De esta forma, a cinco unidades de Distancia Euclidiana (Fig. 5) recuperamos siete grupos que corresponden a C. fothergilloides, C. macrophyllus, C. mojadensis, C. pringlei, Cercocarpus sp. 1, Cercocarpus sp. 2 y Cercocarpus sp. 3.
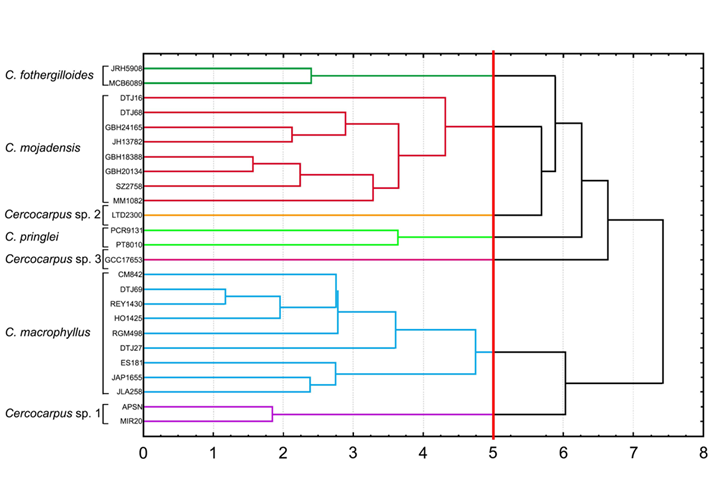
Figura 5:
Dendrograma obtenido mediante el UPGMA que combina los caracteres cuantitativos morfológicos y anatómicos, además de caracteres cualitativos del complejo Cercocarpus fothergilloides Kunth. El análisis distingue siete especies al hacer un corte de cinco Distancias Euclidianas (línea roja).
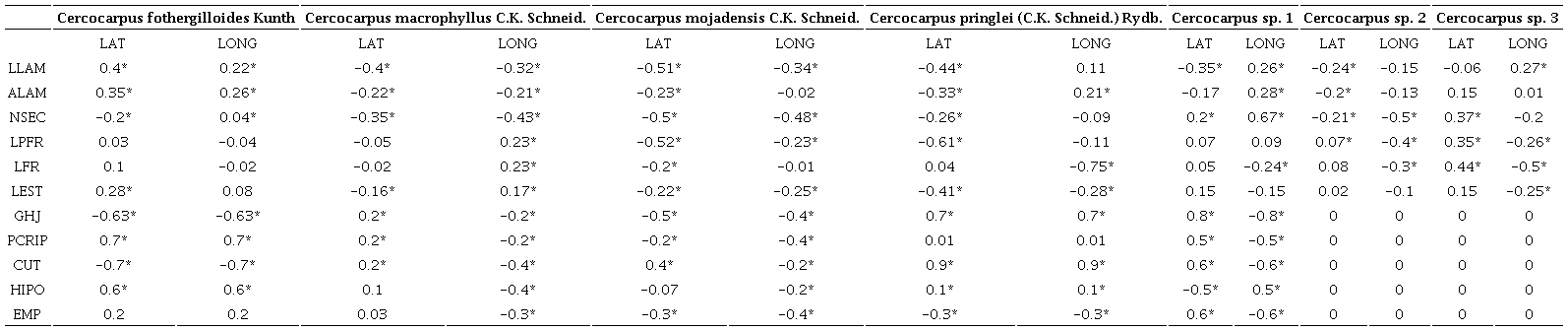
Análisis de correlación con variables geográficas
El análisis de correlación mostró que la profundidad de la cripta (PCRIP) y grosor de la cutícula (CUT) tuvieron altos coeficientes de correlación con la latitud y longitud en C. fothergilloides. Mientras que en C. pringlei fueron el grosor de la hoja (GHJ) y CUT. Por último, el GHJ tuvo correlación positiva con la latitud y negativa con la longitud en Cercocarpus sp. 1 (Cuadro 10).
Descripciones de arquitectura y anatomía foliar
Cercocarpus Kunth, Nov. Gen. Sp. 6: 233-234, pl. 559. 1823.
TIPO: Cercocarpus fothergilloides Kunth.
Hojas simples, alternas o en braquiblastos; pecioladas, láminas nanofilas, microfilas, notofilas y mesofilas, suborbiculares, elípticas, ovadas u obovadas; margen dentado, rara vez entero, crenado, aserrado, frecuentemente revoluto; vena primaria recta, venación secundaria pinnada, craspedódroma, a veces eucamptódroma, venación terciaria percurrente, con venas de cuarto y quinto orden, aréolas bien desarrolladas y vénulas presentes o ausentes; dientes con venación secundaria; hojas hipostomáticas, estomas en criptas, isolaterales, en vista superficial células epidérmicas no isodiamétricas, con paredes anticlinales y periclinales rectas, con tricomas en la superficie abaxial, especialmente en las criptas, tricomas unicelulares, estomas anomocíticos; en sección transversal, hojas 100-630 μm de grosor, adaxial y abaxialmente con cutícula lisa, epidermis simple, la adaxial de menor altura, estomas por encima del nivel de la epidermis, hipodermis adaxial 2-3 estratos, con menor número de estratos y discontinua en la superficie abaxial; mesofilo heterogéneo, parénquima en empalizada ocupando la mayor parte de la lámina, empalizada adaxial 2-3 estratos, continuo, empalizada abaxial 1 estrato, de menor grosor, discontinuo, con células más pequeñas, esponjoso con células braciformes, con amplios espacios intercelulares, especialmente cerca de las criptas, haces vasculares colaterales o anficribales, con vainas de parénquima, en las venas secundarias extensiones de la vaina proyectadas hacia la hipodermis adaxial, en las venas de órdenes superiores extensiones de la vaina orientadas hacia la superficie adaxial y abaxial, a veces colenquimatosas hacia la superficie abaxial; vena media plana o con una depresión adaxialmente, ligeramente proyectada a cóncava abaxialmente, cutícula de mayor grosor que en la lámina, epidermis abaxial con células papilosas, epidermis adaxial sin papilas, colénquima anular por debajo de la epidermis abaxial, con parénquima rodeando el haz, haz en forma de arco o cerrado, xilema y floema con crecimiento secundario, xilema con vasos solitarios o en grupos 2-3, radios de paredes primarias o secundarias, a veces con fibras de paredes gruesas, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor frecuentemente con cristales y sobre éste algunas fibras; taninos en epidermis, hipodermis, mesofilo, haces vasculares o en toda la hoja, cristales prismáticos o drusas, principalmente en las extensiones de la vaina, floema, mesofilo y colénquima.
Cercocarpus fothergilloides Kunth, Nov. Gen. Sp. 6: 233-234 pl. 559. 1824.
TIPO: MÉXICO. Crescit prope urbem Mexici, alt. 2106 m, Floret Aprili, F. W. H. A. von Humboldt y A. J. A. Bonpland s.n. (holotipo: P-00135175!).
Hojas con estípulas, 2.1-5.1 mm de largo, angostamente deltadas, ápice atenuado, glabras en ambas superficies; peciolos 2.3-6.1 mm de largo, seríceos, glabrescentes; láminas nanofilas a microfilas, 0.9-3.1 cm × 0.5-1.8 cm, estrechamente elípticas, a veces obovadas (Figs. 6A, B), ápice agudo u obtuso, base cuneada, margen aserrado, no revoluto, haz lustroso, seríceo en hojas jóvenes, glabrescente con la edad, envés más claro que el haz, seríceo en hojas jóvenes y maduras, venación secundaria craspedódroma, con 5-7(-9) pares de venas, venación de tercer orden percurrente mixta, con venas de cuarto orden, aréolas bien desarrolladas, vénulas sin ramificar, a veces ausentes (Figs. 7A, B), venación marginal ausente, a veces en arcos o incompleta; hojas en sección transversal, 129-371 μm de grosor, criptas 100-278 μm de profundidad, cutícula 2-8.4 μm, epidermis adaxial 5-10 μm de alto, hipodermis adaxial con 2-3 estratos, 24-70 μm de altura, hipodermis abaxial con 1-2 estratos, parénquima en empalizada adaxial con 2 estratos (Fig. 8A), 58-96 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media plana a ligeramente cóncava adaxialmente, ligeramente proyectada abaxialmente (Fig. 9A), colénquima 3-4 estratos, tejido vascular en un haz con xilema arreglado en semicírculos, con vasos solitarios, a veces en grupos de 2, fibras de paredes gruesas, con 8-13 radios de parénquima, rara vez lignificados, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de pocos estratos de células colapsadas; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos o drusas abundantes en extensiones de la vaina y parénquima en vena media escasos o ausentes en mesofilo.

Figura 6:
Variación foliar del complejo Cercocarpus fothergilloides. A-B. Cercocarpus fothergilloides Kunth; C-F. C. macrophyllus C.K. Schneid.; G-L. C. mojadensis C.K. Schneid.; M-O. C. pringlei (C.K. Schneid.) Rydb.; P-Q. Cercocarpus sp. 1.; R-S. Cercocarpus sp. 2.; T-U. Cercocarpus sp. 3. Escala: 1 cm.
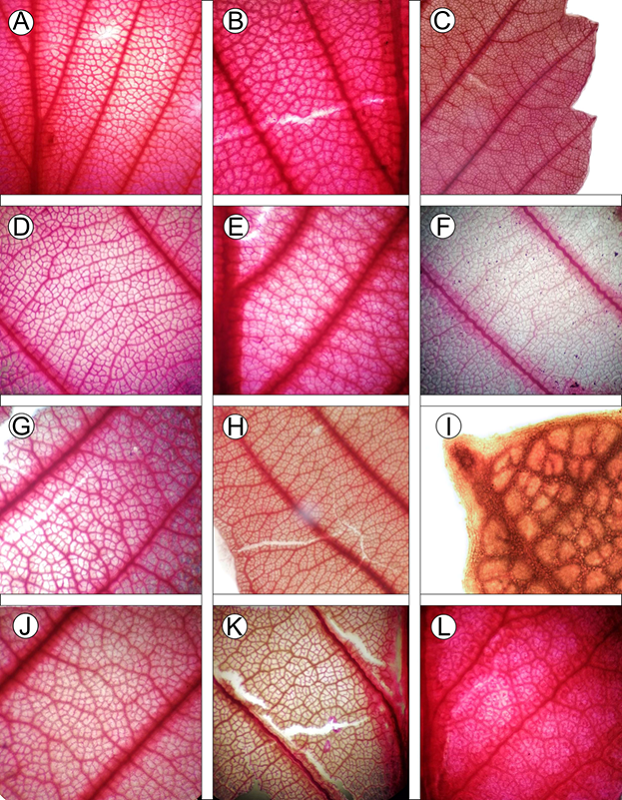
Figura 7:
Fragmentos de hojas aclaradas mostrando las características de la arquitectura foliar del complejo C. fothergilloides. A-B. C. fothergilloides Kunth; C-D. C. macrophyllus C.K. Schneid.; E-F. C. mojadensis C.K. Schneid.; G-H. C. pringlei (C.K. Schneid.) Rydb.; I-J. Cercocarpus sp. 1; K. Cercocarpus sp. 2; L. Cercocarpus sp. 3.
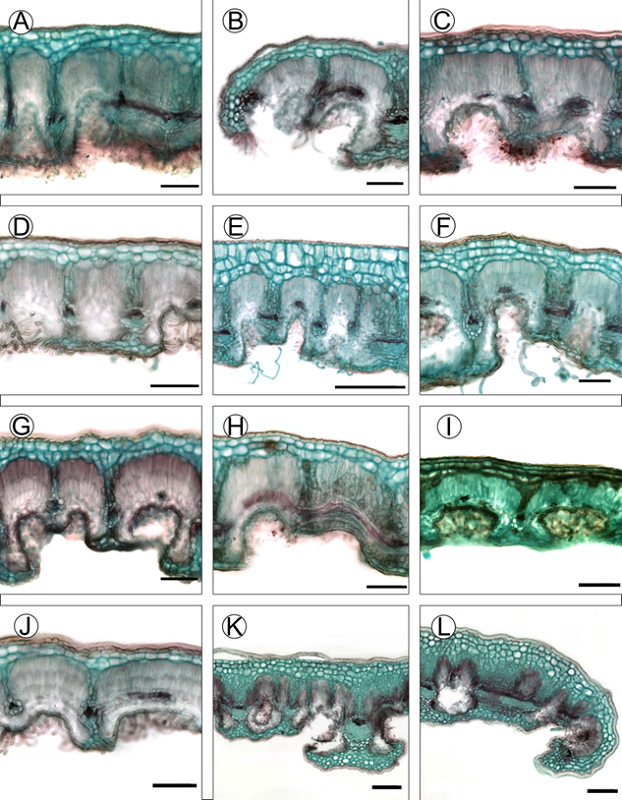
Figura 8:
Características anatómicas de la lámina de las especies del complejo C. fothergilloides. A-B. C. fothergilloides Kunth; C-D. C. macrophyllus C.K. Schneid.; E-F. C. mojadensis C.K. Schneid.; G-H. C. pringlei (C.K. Schneid.) Rydb.; I. Cercocarpus sp. 1; J. Cercocarpus sp. 2; K-L. Cercocarpus sp. 3. Escalas: 100 μm en A-D y F-J; 200 μm en K-L.
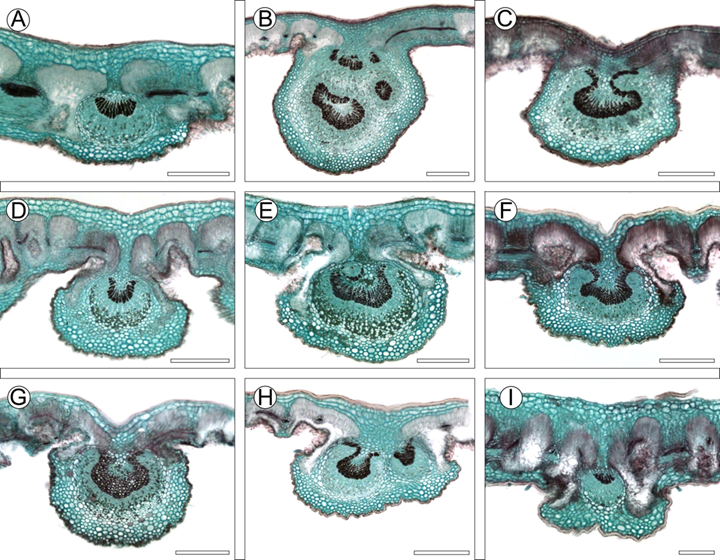
Figura 9:
Características anatómicas de la vena media de las especies del complejo C. fothergilloides. A. C. fothergilloides Kunth; B-C. C. macrophyllus C.K. Schneid.; D-E. C. mojadensis C.K. Schneid.; F. C. pringlei (C.K. Schneid.) Rydb.; G. Cercocarpus sp. 1; H. Cercocarpus sp. 2; I. Cercocarpus sp. 3. Escalas: 300 μm en A-H y 200 μm en I.
Distribución: Oaxaca, Puebla, Tlaxcala y Veracruz.
Notas taxonómicas: Lis (1992) reportó que Cercocarpus fothergilloides tiene hojas rómbicas. Sin embargo, no observamos individuos con esa característica. Hasta ahora, C. fothergilloides ha sido mal entendida y esto se ve reflejado en los ejemplares herborizados. Observamos que el material de C. mojadensis y Cercocarpus sp. 3 estaba bajo el nombre de C. fothergilloides. Martin (1950) reportó que esta especie se distribuye en Puebla y probablemente en Oaxaca. Rzedowski y Calderón de Rzedowski (2005) registraron a C. fothergilloides en Coahuila y Nuevo León; no obstante, esas recolectas corresponden a C. mojadensis.
Cercocarpus macrophyllus C.K. Schneid., Ill. Handb. Laubholzk. 1: 530 (1905). 1905.
TIPO: MÉXICO. Veracruz, Orizaba, 11.I.1892, J. G. Smith 199 (holotipo: MO-1940029 foto!).
Hojas con estípulas, 2.2-10 mm de largo, angostamente deltadas, ápice atenuado, glabras en el haz, pilosas o seríceas en el envés; peciolos (4.6-)7-25 mm de largo; láminas microfilas, notofilas a mesofilas, (4.1-)5.2-14 × (2-)2.5-7.4 cm, estrechamente ovadas, elípticas o ampliamente elípticas (Fig. 6C-F), ápice agudo u obtuso, base cuneada u obtusa, margen aserrado, no revoluto, haz lustroso, piloso en las hojas jóvenes, glabrescente con la edad, envés más claro, en hojas jóvenes tomentuloso en la porción intercostal y seríceo sobre las venas, glabrescente con la edad, rara vez tomentuloso; venación secundaria craspedódroma, con (9-)10-18(-21) pares de venas, venación de tercer orden percurrente mixta, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas sin ramificar, a veces ausentes (Fig. 7C-D), venación marginal en arcos, incompleta o ausente; hojas en sección transversal, 100-242 μm de grosor, criptas 29-151 μm de profundidad, cutícula 1-14 μm, epidermis adaxial 4-12 μm de alto, hipodermis adaxial 1-2 estratos, 9-51 μm de alto, hipodermis abaxial 2-3 estratos, parénquima en empalizada adaxial con 2-3 estratos (Fig. 8C-D), 38-118 μm de alto, esponjoso poco desarrollado, con espacios intercelulares, haces vasculares colaterales o anficribales; vena media con una ligera a una marcada depresión adaxialmente, convexa-redondeada abaxialmente (Fig. 9B-C), colénquima 3-7 estratos, el tejido vascular en un haz con el xilema arreglado en forma de omega u ovalado, vasos solitarios o en grupos de 2, fibras de paredes gruesas, abundantes radios (30-43), lignificados o de parénquima, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de pocos estratos de células colapsadas, frecuentemente con pocas fibras sobre el floema; taninos en epidermis, hipodermis, parénquima en empalizada, haces vasculares y colénquima; cristales prismáticos o drusas en extensiones de la vaina, mesofilo, colénquima, parénquima, radios y floema no conductor en vena media, escasos o ausentes.
Distribución: Aguascalientes, Ciudad de México, Coahuila, Colima, Durango, Estado de México, Guanajuato, Guerrero, Hidalgo, Jalisco, Michoacán, Nayarit, Nuevo León, Oaxaca, Puebla, Querétaro, San Luis Potosí, Sinaloa, Tamaulipas, Veracruz y Zacatecas.
Notas taxonómicas: Lis (1992) mencionó que C. macrophyllus tiene venación semicaspedródoma, aunque no observamos este carácter en ningún individuo.
Cercocarpus mojadensis C.K. Schneid., Mitt. Deutsch. Dendrol. Ges. 14: 126. 1905.
TIPO: MÉXICO. Coahuila, Sierra Mojada, 19.IV.1892, M. E. Jones 134 (holotipo: MO-1940032!).
Hojas con estípulas, 1.4-8.3 mm de largo, angostamente deltadas, ápice atenuado, glabras en el haz, piloso-vilosas en el envés, peciolos 2.2-9.9 mm de largo, pilosos y tomentosos; láminas nanofilas a microfilas, 1.3-4.9 cm × 0.9-2.9 cm, obovadas, ovadas, a veces elípticas hasta anchamente elípticas, rara vez suborbiculares (Fig. 6G-L), margen crenado, crenado-aserrado, revoluto, ápice obtuso, base cuneada, obtusa, haz lustroso, piloso en hojas jóvenes, glabrescente con la edad, envés blanquecino, tomentoso a tomentuloso, a veces viloso en las venas, en hojas jóvenes y maduras, venación secundaria craspedódroma, con 4-8(-9) pares de venas, venación de tercer orden percurrente mixta, a veces percurrente alterna, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas sin ramificar, rara vez con una ramificación o ausentes (Fig. 7E, F), venación marginal en arcos, incompleta o ausente; hojas en sección transversal, 162-555 μm de grosor, criptas 56-397 μm de profundidad, cutícula 1-13 μm, epidermis adaxial 5-16 μm de alto, hipodermis 1-3 estratos, 21-140 μm de alto, hipodermis abaxial 2-3 estratos, parénquima en empalizada adaxial 2-3 estratos (Fig. 8E, F), 62-179 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media plana adaxialmente, convexa-redonda, convexa-alargada abaxialmente (Fig. 9D, E), epidermis abaxial con células papilosas, colénquima 3-6 estratos, el tejido vascular en un haz con el xilema arreglado en forma de U, poco profunda, con vasos solitarios o en grupos de 2-3, fibras de paredes gruesas, radios abundantes (13-24), de parénquima o lignificados, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de varios estratos de células colapsadas; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos y drusas en extensiones de la vaina, mesofilo, colénquima y parénquima en vena media, rara vez ausentes en el mesofilo.
Distribución: Chihuahua, Coahuila, Durango, Hidalgo, Nuevo León, Querétaro, San Luis Potosí, Tamaulipas y Zacatecas.
Notas taxonómicas: Lis (1992) reportó que C. mojadensis tiene hojas con margen aserrado, aunque en el presente trabajo también observamos que es crenado. Además, mencionó que las vénulas están ausentes, pero en este estudio reportamos vénulas.
Cercocarpus pringlei (C.K. Schneid.) Rydb., N. Amer. Fl. 22(5): 420. 1913.
TIPO: MÉXICO. Oaxaca, La Hoya Canyon, 2.XI.1894, 1676 m, C. G. Pringle 6140 (lectotipo: MO-1940037! (designado por Martin, 1950); isolectotipos: GH, NY, RM, UC, US).
Hojas con estípulas, 1.7-8.2 mm de largo, oblongo-deltadas, ápice atenuado, glabras en el haz, vilosas en el envés; peciolos 1.6-19 mm de largo, pilosos y tomentosos; láminas microfilas a notofilas, 2.1-7.1(-8.4) × 1.2-4.1 cm, obovadas, a veces elípticas (Fig. 6M, O), ápice obtuso, base cuneada, a veces obtusa, margen crenado, crenado-aserrado hacia el ápice, revoluto, haz lustroso, piloso en hojas jóvenes, glabrescente en las maduras, envés blanquecino, tomentoso en la porción intercostal, viloso sobre las venas en hojas jóvenes y maduras, venación secundaria craspedródoma hacia el ápice, eucamptódroma en la base (Fig. 7HH, con 6-12(-13) pares de venas, venación de tercer orden percurrente mixta, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas sin ramificar (Fig. 7G, H), venación marginal en arcos, a veces ausente; hojas en sección transversal, 163-246 μm de grosor, criptas 52-167 μm de profundidad, cutícula 2-18 μm, epidermis adaxial 6-14 μm de alto, hipodermis adaxial 1-2 estratos, 20-55 μm de alto, hipodermis abaxial con 1-2 estratos, parénquima en empalizada adaxial 3 estratos (Fig. 8G, H), 49-113 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media plana o con una depresión adaxialmente, cóncava-redondeada abaxialmente (Fig. 9F), colénquima 5-7 estratos, tejido vascular en un haz con el xilema arreglado en forma de omega poco profundo, vasos solitarios, fibras de paredes gruesas, radios abundantes (~26), de parénquima o lignificados, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor con varios estratos; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos en extensiones de la vaina y parénquima en vena media, ausentes en mesofilo, rara vez con drusas.
Distribución: Oaxaca y Puebla.
Notas: Lis (1992) reportó que C. pringlei presenta venación secundaria craspedódroma y eucamptódroma, la cual observamos en los individuos examinados. De acuerdo con el mismo autor, el orden de venación superior es de cuarto orden. No obstante, también encontramos venas de quinto orden.
Cercocarpus sp. 1
Hojas con estípulas, 3.5-13.8 mm de largo, oblongo-deltadas, ápice atenuado, glabras en el haz, vilosas en el envés; peciolos 4.7-15 mm de largo, pilosos y tomentosos; láminas microfilas a notofilas, (2.9-)3.9-8.5 × (1.6-)2.1-5.3 cm, elípticas, ovadas, estrechamente ovadas (Fig. 6P, Q), ápice obtuso, a veces agudo, base obtusa, margen aserrado, revoluto, haz lustroso, piloso en hojas jóvenes, glabrescente en las maduras, envés blanquecino, en hojas jóvenes y maduras tomentoso en porción intercostal, piloso sobre las venas, venación secundaria craspedódroma (Fig. 7I), con 8-14 pares de venas, venación de tercer orden percurrente mixta, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas sin ramificar, rara vez con una ramificación o ausentes (Fig. 7J), venación marginal ausente o en arcos, a veces incompleta; hojas en sección transversal, 113-200 μm de grosor, criptas 38-123 μm de profundidad, cutícula 3-8 μm, epidermis adaxial 7-14 μm, hipodermis adaxial 2 estratos, 23-49 μm de alto, hipodermis abaxial 2 estratos, parénquima en empalizada adaxial 2 estratos (Fig. 8I), 51-108 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media con una depresión en la superficie adaxial, convexa-redondeada abaxialmente (Fig. 9G), cutícula mayor que en la lámina, epidermis abaxial con células papilosas, colénquima 3-6 estratos el tejido vascular en un haz con el xilema en forma de omega, vasos solitarios o en grupos de 2, fibras de paredes gruesas, radios abundantes (~20), de parénquima o lignificados, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de pocos estratos de células colapsadas; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos y drusas en extensiones de la vaina, mesofilo, parénquima y floema colapsado en vena media, abundantes o escasos.
Distribución: Guerrero y Oaxaca.
Notas taxonómicas: El material de Cercocarpus sp. 1 fue identificado como Cercocarpus macrophyllus; pero, a diferencia de esta especie Cercocarpus sp. 1 presentó hojas tomentosas en el envés y pedicelos de hasta 5 mm de largo. Cercocarpus sp. 1 también fue confundida con C. pringlei. Ambas especies presentan distribución geográfica parapátrica en los límites entre Oaxaca y Guerrero. Las hojas de Cercocarpus sp. 1 son ovadas, obtusas y agudas; su rango de distribución se extiende hacia el noroeste de Guerrero. En contraste, las hojas en C. pringlei son obovadas, cuneadas y obtusas. Su distribución es opuesta, en dirección hacia el sur y sureste de Oaxaca y Puebla. Además, Cercocarpus sp. 1 no presentó venación eucamptódroma en la base de las hojas.
Cercocarpus sp. 2
Hojas con estípulas, 3.4-8.9 mm de largo, oblongo-deltadas, ápice atenuado, glabras en el haz y envés; peciolos 2.4-8.9 mm de largo, pilosos y tomentosos; láminas microfilas, 1.4-4.6 × 1.0-3.1 cm, elípticas, obovadas (Fig. 6R, S), ápice obtuso, a veces agudo, base obtusa, a veces cuneada, margen aserrado, revoluto, haz lustroso, piloso en hojas jóvenes, glabrescente en las maduras, en hojas jóvenes y maduras envés blanquecino, tomentoso en la porción intercostal, viloso sobre las venas, venación secundaria craspedódroma, con 5-9 pares venas, venación de tercer orden percurrente mixta, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas ramificadas una vez, a veces sin ramificar (Fig. 7K), venación marginal incompleta, en arcos o ausente; hojas en sección transversal, 123-195 μm de grosor, criptas 36-145 μm de profundidad, cutícula 5-13 μm, epidermis adaxial 9-14 μm de alto, hipodermis 1-2 estratos, 16-36 μm de alto, hipodermis abaxial 2 estratos, parénquima en empalizada adaxial 2-3 estratos (Fig. 8J), 61-85 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media plana adaxialmente, convexa-redonda abaxialmente (Fig. 9H), colénquima 3-4 estratos, tejido vascular en un haz con el xilema arreglado en forma de omega, vasos solitarios o en grupos de 2, radios abundantes (~20), de parénquima o lignificados, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de varios estratos de células colapsadas; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos o drusas, escasos en extensiones de la vaina, mesofilo y parénquima en vena media.
Distribución: Coahuila y Nuevo León.
Notas taxonómicas: Las variantes morfológicas de Cercocarpus mojadensis del material herborizado procedente de Coahuila y Nuevo León tuvieron hojas ovadas a elípticas con el envés viloso en las venas y tomentoso entre ellas. Además, presentaron vénulas una vez ramificadas y pedicelos de hasta 7 mm de largo; estos especímenes correspondieron a Cercocarpus sp. 2.
Cercocarpus sp. 3
Hojas con estípulas, 1.3-3.5 mm de largo, deltadas, ápice atenuado, glabras en el haz, hírtulas en el envés, con tricomas en el margen; peciolos 2.7-8.5 mm de largo, tomentosos e hírtulos; láminas nanofilas a microfilas, 1.1-3.3 × 0.6-1.9 cm, elípticas, algunas veces suborbiculares (Fig. 6T, U), ápice obtuso, redondeado, a veces mucronado, base obtusa, rara vez cuneada, margen crenado o entero, revoluto (Fig. 8L), haz lustroso, densamente piloso en hojas jóvenes, glabrescente en las maduras, envés blanquecino, densamente tomentosos en hojas jóvenes, tomentoso en hojas maduras, venación secundaria craspedódroma, con 5-7 pares de venas, venación de tercer orden percurrente alterna, con venas de cuarto y quinto orden, aréolas bien desarrolladas, vénulas ausentes (Fig. 7L), venación marginal en arcos, incompleta o ausente; hojas en sección transversal, 487-630 μm de grosor, criptas 84-371 μm de profundidad, cutícula 10-28 μm, epidermis 7-19 μm de alto, hipodermis adaxial 3-4 estratos (Fig. 8K), 76-167 μm de alto, hipodermis abaxial 2 estratos, parénquima en empalizada adaxial 2 estratos, 77-106 μm de alto, esponjoso desarrollado, con espacios intercelulares, haces vasculares colaterales; vena media plana adaxialmente, convexa-alargada abaxialmente (Fig. 9I), colénquima 5-6 estratos, tejido vascular en un haz con el xilema en forma de semicírculo, vasos solitarios, con 5-6 radios de parénquima, floema conductor con tubos cribosos y células acompañantes turgentes, floema no conductor de pocos estratos de células colapsadas, fibras sobre el floema; taninos en epidermis, hipodermis, mesofilo, haces vasculares y colénquima; cristales prismáticos o drusas en extensiones de la vaina, parénquima y floema colapsado en vena media, rara vez con drusas en mesófilo.
Distribución: Puebla y Veracruz.
Notas taxonómicas: Cercocarpus sp. 3 se distingue de C. fothergilloides por sus hojas ovadas a suborbiculares con el envés viloso, además de tener margen entero o crenado vs. serrado.
Discusión
Caracteres morfológicos cuantitativos
Por sí solos, los caracteres cuantitativos tuvieron una capacidad limitada para distinguir a todas las especies del complejo Cercocarpus fothergilloides (Fig. 3); reflejo de esto es que el porcentaje de clasificación fue bajo en C. mojadensis (Cuadro 6). No obstante, las distancias cuadradas de Mahalanobis fueron significativas (Cuadro 5).
En Rosaceae y en otras angiospermas, los caracteres cuantitativos han permitido delimitar taxones (Eriksen, 1997; Sosa et al., 2012; Vásquez-Cruz et al., 2017). Sin embargo, en el complejo C. fothergilloides las especies presentaron una gran variación y hubo traslape de estos caracteres en los individuos. Nuestros resultados corroboran lo que Martin (1950) mencionó; los caracteres de un taxón ocasionalmente aparecen en otros. Aunque las características cuantitativas presentan variación, la combinación de estas con los caracteres cualitativos permiten distinguir las especies.
El ADC de la variación morfológica recuperó cinco grupos (Fig. 3A). El número de venas secundarias y el largo de la lámina formaron dos grupos. Cercocarpus fothergilloides, C. mojadensis, Cercocarpus sp. 2 y Cercocarpus sp. 3 tuvieron láminas de menos de 4 cm de largo, con menos de 10 pares de venas secundarias (Fig. 4A, B). Por el contrario, en C. macrophyllus, C. pringlei y Cercocarpus sp. 1, las hojas midieron más de 4 cm de largo y al menos en una hoja por individuo, hubo más de 10 pares de venas secundarias (Fig. 4A, B). Martin (1950) señaló la importancia taxonómica del número de venas secundarias y este estudio muestra que la longitud de la lámina también lo tiene.
Los caracteres florales con mayor peso fueron la longitud del pedicelo en el fruto y del estilo. Históricamente, las características de la flor no han sido la principal fuente de información en la delimitación de especies de Cercocarpus (Rydberg, 1913; Martin, 1950). Con hasta 1.2 cm, C. macrophyllus registró los pedicelos más largos en fruto (Fig. 4C). Cercocarpus sp. 2 tuvo un valor de hasta 0.7 cm, mientras que C. mojadensis presentó flores sésiles y pedicelos en fruto de hasta 0.5 cm. Por otro lado, el largo del estilo formó dos grupos. Cercocarpus macrophyllus, Cercocarpus sp. 2, C. pringlei y C. mojadensis presentaron estilos de más de 6 cm de largo. En contraste, Cercocarpus sp. 1, C. fothergilloides y Cercocarpus sp. 3 tuvieron estilos ≥6 cm (Fig. 4D).
Los resultados obtenidos en el presente estudio resaltan la importancia de la morfología floral como evidencia para delimitar las especies. Martin (1950) indicó que el número de flores es útil para delimitar al complejo C. fothergilloides porque tiene el mayor número de flores por inflorescencia (hasta 11) en comparación con los otros grupos. Sin embargo, dicho carácter carece de valor entre las especies de Cercocarpus. Por el contrario, en otros grupos de Rosaceae se han utilizado caracteres florales como el largo del estilo, número de flores y estambres para delimitar especies (Boza Espinoza et al., 2019). De igual forma, este trabajo mostró que los caracteres florales pueden aportar información.
Caracteres anatómicos cuantitativos
El análisis de los caracteres anatómicos cuantitativos resolvió cuatro grupos (Fig. 3B). Los coeficientes canónicos del grosor de la hoja y la hipodermis fueron los más altos (Cuadro 7). Cercocarpus sp. 3, C. mojadensis y C. fothergilloides tuvieron las hojas más gruesas. En el otro extremo, C. macrophyllus, C. pringlei, Cercocarpus sp. 1 y Cercocarpus sp. 2 presentaron hojas más delgadas (Fig. 4G). En C. mojadensis y Cercocarpus sp. 3 se encontraron las hipodermis más gruesas, mientras que C. fothergilloides, C. macrophyllus, C. pringlei y Cercocarpus sp. 1 tuvieron hipodermis más delgadas y con altura similar (Fig. 4H). El extremo inferior de este carácter fue observado en Cercocarpus sp. 2 que presentó la hipodermis más delgada de todas las especies (16-36 μm). En Rosaceae, particularmente en Polylepis Ruiz & Pav., se ha reportado que la anatomía foliar presenta mucha variación y sobreposición de caracteres entre especies (Simpson, 1979). No obstante, el grosor de la cutícula y del parénquima en empalizada ha proporcionado información taxonómica en Potentilla L. (Faghir et al., 2011). Aunque no tuvieron los coeficientes más altos, esos caracteres también resultaron importantes en el complejo C. fothergilloides.
Por último, la morfología y la anatomía discriminaron a Cercocarpus sp. 2 (Fig. 3), pero hubo diferencia en la agrupación: la morfología la asoció con C. mojadensis, mientras que la anatomía la relacionó con el grupo de C. macrophyllus, C. pringlei y Cercocarpus sp. 1. Ambas fuentes de evidencia nos permitieron reconocer a Cercocarpus sp. 2 como una especie diferente.
Análisis de agrupamiento
La combinación de caracteres cuantitativos y cualitativos separó siete grupos que representan a las cuatro especies conocidas del complejo C. fothergilloides y tres grupos que constituyen el mismo número de morfoespecies (Fig. 5). Este trabajo, al igual que en otras familias, muestra que los análisis de similitud son una herramienta útil para separar y delimitar especies (Chitchak et al., 2018; Finot et al. 2018; Sánchez et al. 2020).
El tipo de indumento en el envés de las hojas maduras fue distintivo entre todas las especies analizadas. Abaxialmente las hojas seríceas son características de C. fothergilloides (Fig. 6A), mientras que C. mojadensis presenta hojas tomentosas. En contraste, C. macrophyllus tiene envés glabro (Fig. 6D, E). En Cercocarpus pringlei (Fig. 6M, O), Cercocarpus sp. 1 (Fig. 6P, Q) y Cercocarpus sp. 2 (Fig. 6R, S) observamos pubescencia mixta, es decir que sus hojas son tomentosas entre las venas y vilosas o pilosas sobre ellas. La venación secundaria permitió distinguir a C. pringlei, al ser eucamptódroma en la base de las hojas (Fig. 7H).
Las vénulas también contribuyeron en el reconocimiento taxonómico; por ejemplo, Cercocarpus sp. 2 presentó vénulas con una ramificación (Fig. 7K). Resultados similares se han encontrado en otros grupos de angiospermas en los que el patrón de venación contribuye a delimitar especies (Andrés-Hernández y Terrazas, 2009; Martínez-Cabrera et al., 2011; de Souza Lima et al., 2019; Vila Nova de Lima et al., 2019). La importancia de los tipos de venación concuerda con lo registrado por Lis (1992), ya que este carácter ayudó a separar especies en el complejo C. fothergilloides.
Los caracteres anatómicos cualitativos también fueron informativos. El contorno de la vena media ayudó a distinguir algunas especies. La vena media de C. fothergilloides y Cercocarpus sp. 3 fue plana adaxialmente y ligeramente convexa abaxialmente (Fig. 9A, I). Mientras que en C. macrophyllus hubo una depresión ligera a marcada adaxialmente, abaxialmente fue convexo-redonda (Fig. 9B, C). Este carácter también se ha utilizado para delimitar especies de Eriosema (DC.) Desv. (Pacheco Seixas et al., 2019). La evidencia encontrada en el presente estudio mostró que la forma de la vena media puede contribuir a separar algunas especies del complejo C. fothergilloides.
Análisis de correlación con variables geográficas
Ninguno de los caracteres morfológicos se correlacionó significativamente con la latitud y longitud. No obstante, algunas características anatómicas tuvieron correlación con las variables de distribución geográfica. El grosor de la hoja y la cutícula, así como la profundidad de la cripta fueron los caracteres más correlacionados con la latitud y longitud (Cuadro 10). Se ha descrito que los caracteres anatómicos varían en diferentes condiciones climáticas (Mortenson, 1973). Las cutículas gruesas se han atribuido a ambientes xerófitos con poca disponibilidad de agua. Asimismo, criptas más profundas podrían asociarse con hojas más gruesas (op. pers.). Se ha propuesto que las criptas más profundas facilitan la difusión de CO2 en hojas gruesas (Hassiotou et al., 2009).
Cercocarpus mojadensis y Cercocarpus sp. 2 habitan en ambientes similares, por lo que esperaríamos que tuvieran características similares en la cutícula y altura del parénquima en empalizada. Cercocarpus mojadensis presentó parénquima en empalizada grueso (Fig. 4J), característico de zonas con alta luminosidad (Mortenson, 1973; Cutler et al., 2008). No obstante, en Cercocarpus sp. 2 el parénquima en empalizada fue de menor altura (Fig. 4J). Estos resultados sugieren que no toda la variación presente en las especies del complejo C. fothergilloides está relacionada con su distribución geográfica.
Conclusiones
El complejo Cercocarpus fothergilloides incluye cuatro especies descritas y tres morfoespecies que presentan diferencias significativas en su morfología y anatomía. El número de venas secundarias, longitud de la lámina, los pedicelos en fruto, del estilo y el fruto fueron los caracteres morfológicos que permitieron diferenciar a las especies. Las características anatómicas importantes para separar taxones del complejo C. fothergilloides son: el grosor de la hoja y la cutícula, alto del parénquima en empalizada y la epidermis. La combinación de estos con los atributos cualitativos en el análisis de agrupamiento, que incluyó arquitectura foliar, permitió distinguir a C. fothergilloides, C. macrophyllus, C. mojadensis, C. pringlei, Cercocarpus sp. 1, Cercocarpus sp. 2 y Cercocarpus sp. 3.
Agradecimientos
Agradecemos a los curadores de los siguientes herbarios: ENCB, FCME, IBUG, IEB, MEXU y UAMIZ por las facilidades otorgadas para consultar sus colecciones. Se agradece especialmente a María del Rosario García y Laura Calvillo por la ayuda en la extracción de hojas de los ejemplares de MEXU. Alicia Rojas brindó apoyo técnico para obtener los cortes anatómicos y las hojas aclaradas. Arturo Castro y Gerald Matus Hernández Barón ayudaron en la recolección de hojas en campo. Rosa María Fonseca y Pablo Carrillo proporcionaron hojas de Cercocarpus sp. 1. y C. pringlei, respectivamente. Agradecemos a los dos revisores anónimos por sus comentarios que ayudaron a mejorar el manuscrito.
Literatura citada
Abràmoff, M. D., P. J. Magalhães y S. J. Ram. 2004. Image processing with Image J. Biophotonics International 11: 36-42.
Andrés-Hernández, A. R. y T. Terrazas. 2009. Leaf architecture of Rhus s.str. (Anacardiaceae). Feddes Repertorium 120(5-6): 293-306. DOI: https://doi.org/10.1002/fedr.200911109
Boza Espinoza, T. E., H. R. Quispe-Melgar y M. Kessler. 2019. Taxonomic reevaluation of the Polylepis sericea complex (Rosaceae), with the description of a new species. Systematic Botany 44(2): 324-334. DOI: https://doi.org/10.1600/036364419X15562052252225
Ceja-Romero, J., A. Espejo-Serna y A. R. López-Ferrari. 2009. Una nueva especie de Sisyrinchium (Iridaceae) del estado de Guanajuato, México. Acta Botanica Mexicana 87: 83-90. DOI: https://doi.org/10.21829/abm87.2009.1083
Chitchak, N., P. Traiperm, G. Staples, P. Rattanakrajang y P. Sumanon. 2018. Species delimitation of some Argyreia (Convolvulaceae) using phenetic analyses: insights from leaf anatomical data reveal a new species. Botany 96(4): 217-233. DOI: https://doi.org/10.1139/cjb-2017-0108
Cutler, D. F., T. Botha y D. W. Stevenson. 2008. Plant anatomy and applied approach. Blackwell Publishing. Malden, USA. 312 pp.
de Queiroz, K. 2005. A unified concept of species and its consequences for the future of taxonomy. Proceedings of the California Academy of Sciences 56(18): 196-215.
de Souza Lima, M. P., A. Soares, J. L. Ribeiro de Sousa, M. Santos Carvalho, J. M. Padovani Porto y F. Tavares Braga. 2019. Leaf architecture of Rubiaceae Juss. from caatinga vegetation in Brazil. Biota Neotropica 19(1): e20170473. DOI: https://doi.org/10.1590/1676-0611-BN-2017-0473
Duminil, J. y M. Di Michele. 2009. Plant species delimitation: a comparison of morphological and molecular markers. Plant Biosystems 143(3): 528-542. DOI: https://doi.org/10.1080/11263500902722964
Ellis, B., D. C. Daly, L. J. Hickey, K. R. Johnson, J. D. Mitchell, P. Wilf y S. L. Wing. 2009. Manual of leaf architecture. Cornell University Press. Ithaca, USA. 190 pp.
Eriksen, B. 1997. Morphometric analysis of Alaskan members of the genus Potentilla sect. Niveae (Rosaceae). Nordic Journal of Botany 17(6): 621-630. DOI: https://doi.org/10.1111/j.1756-1051.1997.tb00358.x
Faghir, M. B., F. Attar y B. Ertter. 2011. Foliar anatomy of the genus Potentilla L. (Rosaceae) in Iran and its taxonomic implication. Iranian Journal of Science & Technology 35(3): 243-256. DOI: https://doi.org/10.22099/IJSTS.2011.2149
Finot, V. L., R. J. Soreng, L. M. Giussani y R. G. Muñoz. 2018. A multivariate morphometric delimitation of species boundaries in the South American genus Nicoraepoa (Poaceae: Pooideae: Poeae). Plant Systematics and Evolution 304: 679-697. DOI: https://doi.org/10.1007/s00606-018-1499-y
Freudenstein, J. V., M. B. Broe, R. A. Folk y B. T. Sinn. 2017. Biodiversity and the species concept-lineages are not enough. Systematic Biology 66(4): 644-656. DOI: https://doi.org/10.1093/sysbio/syw098
Google Inc. 2020. Google Earth Pro v. 7.3. https://www.google.com/intl/es-419/earth/ (consultado enero de 2020).
Hair, J. F., R. E. Anderson, R. L. Tatham y W. C. Black. 1999. Análisis multivariante. Pearson Prentice Hall. Madrid, España. 832 pp.
Hammer, Ø., D. A. T. Harper y P. D. Ryan. 2001. PAST: Paleontological Statistics Software Package for Education and Data Analysis. Palaeontologia Electronica 4: 1-9. https://palaeo-electronica.org/2001_1/past/issue1_01.htm (consultado marzo de 2020).
Hassiotou, F., J. R. Evans, M. Ludwig y E. J. Veneklaas. 2009. Stomatal crypts may facilitate diffusion of CO2 to adaxial mesophyll cells in thick sclerophylls. Plant, Cell & Environment 32(11): 1596-1611. DOI: https://doi.org/10.1111/j.1365-3040.2009.02024.x
Henrickson, J. y B. D. Vanden Heuvel. 2014. Cercocarpus Kunth. In: Comité Editorial de Flora of North America (eds.). Flora of North America, Magnoliophyta: Picramniaceae to Rosaceae, vol. 9. Oxford University Press. New York, USA. http://floranorthamerica.org/Cercocarpus (consultado mayo de 2022).
Hickey, L. J. 1973. Classification of the Architecture of Dicotyledonous Leaves. American Journal of Botany 60(1): 17-33. DOI: https://doi.org/10.1002/j.1537-2197.1973.tb10192.x
Image Pro-plus. 2019. Image Pro-plus ver. 7.1. Media Cybernetics. Inc. Bethesda, EUA. https://www.mediacy.com/78-products/image-pro-plus (consultado agosto de 2019).
INEGI. 2020. Catálogo Único de Claves de Áreas Geoestadísticas Estatales, Municipales y Localidades. Instituto Nacional de Estadística y Geografía (INEGI). https://www.inegi.org.mx/app/ageeml/# (consultado enero de 2024).
JSTOR. 2022. JSTOR Global Plants. https://plants.jstor.org/ (consultado mayo de 2022).
Lis, R. A. 1992. Leaf architectural survey of Cercocarpus (Rosaceae) and its systematic significance. International Journal of Plant Sciences 153(2): 258-272. DOI: https://doi.org/10.1086/297030
Mallet, J. 1995. A species definition for the modern synthesis. Trends in Ecology & Evolution 10(7): 294-299. DOI: https://doi.org/10.1016/0169-5347(95)90031-4
Martin, F. L. 1950. A revision of Cercocarpus. Brittonia 7: 91-111. DOI: https://doi.org/10.2307/2804932
Martínez-Cabrera, D., T. Terrazas y H. Ochoterena. 2007. Leaf architecture of Hamelieae (Rubiaceae). Feddes Repertorium 118(7-8): 286-310. DOI: https://doi.org/10.1002/fedr.200711140
Martínez-Cabrera, D., F. Zavala-Chávez y T. Terrazas. 2011. Estudio morfométrico de Quercus sartorii y Q. xalapensis (Fagaceae). Revista Mexicana de Biodiversidad 82(2): 551-568. DOI: https://doi.org/10.22201/ib.20078706e.2011.2.459
Metcalfe, C. R. y L. Chalk. 1950. Anatomy of the dicotyledons: leaves, stem and wood in relation to taxonomy, with notes on economic uses, Vol. I. Oxford University Press. Londres, UK. 724 pp.
Mortenson, T. H. 1973. Ecological variations in the leaf anatomy of selected species of Cercocarpus. Aliso 8(1): 19-48. DOI: https://doi.org/10.5642/aliso.19730801.14
Pacheco Seixas, D., A. P. Fortuna-Perez y T. M. Rodrigues 2019. Leaf anatomical features of the Eriosema campestre Benth. (Leguminosae, Papilionoideae, Phaseoleae) complex and potential taxonomic implications. Flora 253: 107-115. DOI: https://doi.org/10.1016/j.flora.2019.03.011
Pinheiro, F., M. V. Dantas-Queiroz y C. Palma-Silva. 2018. Plant species complexes as models to understand speciation and evolution: a review of South American studies. Critical Reviews in Plant Sciences 37(1): 1-27. DOI: https://doi.org/10.1080/07352689.2018.1471565
Ramírez-Diaz, C. M. 2016. Anatomía y arquitectura foliar del género Tilia en México. Tesis de licenciatura. Facultad de Ciencias, Universidad Nacional Autónoma de México. Cd. Mx., México. 51 pp.
Rasband, W. S. 2019. ImageJ ver. 1.52a. U. S. National Institutes of Health. Bethesda, EUA. https://imagej.nih.gov/ij/index.html (consultado agosto de 2019).
R Core Team. 2018. R: a language and environment for statistical computing. R Foundation for Statistical Computing. Vienna, Austria. http://www.R-project.org/ (consultado enero de 2020).
RStudio Team. 2019. RStudio: Integrated Development for R. RStudio, PBC. Boston, EUA. https://www.rstudio.com/products/rstudio/ (consultado enero de 2023).
Ruzin, S. E. 1999. Plant Microtechnique and Microscopy. Oxford University Press. New York, USA. 322 pp.
Rydberg, P. A. 1913. Rosaceae. In: Glenson, H. A., H. W. Rickett, D. P. Rogers, F. W. Pennell y E. P. Killip (eds.). North American Flora, vol. 22, part. 5. The New York Botanical Garden. New York, USA. Pp. 389-480.
Rzedowski, J. y G. Calderón de Rzedowski. 2005. Rosaceae. In: Rzedowski, J. y G. Calderón de Rzedowski (eds.). Flora del Bajío y de Regiones Adyacentes 135. Instituto de Ecología, A.C., Pátzcuaro, México. 157 pp. DOI: https://doi.org/10.21829/fb.113.2005.135
Sánchez, D., S. Arias y T. Terrazas. 2013. Análisis morfométrico de las especies de Echinocereus sección Triglochidiati (Cactaceae) en México. Brittonia 65: 368-385. DOI: https://doi.org/10.1007/s12228-012-9285-6
Sánchez, D., D. Gómez-Quintero, O. Vargas-Ponce, P. Carillo-Reyes y P. Dávila-Aranda. 2020. Species delimitation in the Echinocereus pulchellus complex (Cactaceae). Brittonia 72(4): 433-452. DOI: https://doi.org/10.1007/s12228-020-09632-x
SAS Institute Inc. 2018. SAS Studio 3.8: User’s Guide. Cary: SAS Institute Inc. https://support.sas.com/downloads/package.htm?pid=1924 (consultado enero de 2020).
Schneider, C. K. 1905a. Gattung Cercocarpus Kunth. IIllustriertes Handbuch der Laubholzkunde 14: 125-129.
Schneider, C. K. 1905b. Beitrag zur Kenntnis der Arten und Formen der Gattung Cercocarpus Kunth. Mitteilungen der Deutschen Dendrologischen Gesellschaft 14: 125-129.
Simpson, B. B. 1979. A revision of the genus Polylepis (Rosaceae: Sanguisorbeae). Smithsonian Contributions to Botany 43: 1-62. DOI: https://doi.org/10.5479/si.0081024X.43.1
Sosa, M., A. Panseri y M. Dematteis. 2012. Morphometric analysis of Stemodia hyptoides and S. stricta (Plantaginaceae). Plant Systematics and Evolution 298: 1315-1323. DOI: https://doi.org/10.1007/s00606-012-0638-0
StaSoft Inc. 2004. STATISTICA (Data analysis software system) ver. 7.0. StaSoft Inc. Oklahoma, USA. https://www.statistica.com/en/ (consultado marzo de 2020).
Terrazas, T., S. Aguilar-Rodríguez y L. López-Mata. 2008. Wood anatomy and its relation to plant size and latitude in Buddleja L. (Buddlejaceae). Interciencia 33(1): 46-50.
Thiers, B. 2022+. Index Herbariorum: a global directory of public herbaria and associated staff. New York Botanical Garden’s Virtual Herbarium. http://sweetgum.nybg.org/science/ih/ (consultado mayo de 2022).
Vanden Heuvel, B. D. 2002. Molecular systematics of Cercocarpus H.B.K. (Rosaceae). Tesis de doctorado. Faculty of the Graduate School, The University of Texas at Austin. Austin, USA. 256 pp.
Vanden Heuvel, B. D. y C. R. Linder. 2001. A molecular phylogeny for Cercocarpus H.B.K. (Rosaceae) using the external transcribed spacer of the nuclear ribosomal repeat. In: McArthur, E. D. y D. J. Fairbanks (comps.). Shrubland ecosystem genetics and biodiversity: proceedings. Department of Agriculture, Forest Service, Rocky Mountain Research Station. Colorado, USA. Pp. 89-94.
Vásquez-Cruz, M., A. P. Vovides y V. Sosa. 2017. Disentangling species limits in the Vauquelinia corymbosa complex (Pyreae, Rosaceae). Systematic Botany 42(4): 835-847. DOI: https://doi.org/10.1600/036364417X696519
Vila Nova de Lima, R. G., L. Ferreira Lima, A. Cândida Ferreira, J. Silva Araújo y C. Silvia Zickel. 2019. Leaf morphoanatomy of Diploon Cronquist (Sapotaceae Juss.). Biota Neotropica 19(1): e20180600. DOI: https://doi.org/10.1590/1676-0611-BN-2018-0600
Villaseñor, J. L. 2016. Checklist of the native vascular plants of Mexico. Revista Mexicana de Biodiversidad 87(3): 559-902. DOI: https://doi.org/10.1016/j.rmb.2016.06.017
Zamora-Natera, J. F. y T. Terrazas. 2012. Anatomía foliar y del pecíolo de cuatro especies de Lupinus (Fabaceae). Revista Mexicana de Biodiversidad 83(3): 687-697. DOI: https://doi.org/10.22201/ib.20078706e.2012.83.3269
Apéndices
Apéndice 1: Ejemplares representativos de Cercocarpus Kunth en los que examinamos la morfología. Las coordenadas entre paréntesis indican que fueron calculadas.
Cercocarpus fothergilloidesKunth
MÉXICO. Oaxaca, Distrito Coixtlahuaca, municipio Villa Tepelmeme de Morelos, cerro Paraje Ladrón, 18°6'39.82''N, 97°18'26.68''W, 2100 m, 17.IX.1994, A. Salinas y E. Martínez-Correa 7903 (MEXU). Puebla, municipio Caltepec, cerro Yeltepec, al NE de la Compañía, (18°13'42.7''N, 97°30'24.02''W), 2070 m, 1.VIII.1984, P. Tenorio y C. Romero 6753 (IEB, MEXU); cerro Viejo, (18°8'44.4''N, 97°20'53.27''W), 1900 m, 7.VI.1991, A. Valiente-Banuet et al. 857 (MEXU). Municipio Chalchicomula de Sesma, 9.93 km al ESE de Santiago Tenango, 18°58'49.8''N, 97°33'10.1''W, 2859 m, 10.VI.2011, C. H. Ramos et al. 2894 (MEXU). Municipio de Chapulco, 7 km antes de llegar a Nicolás Bravo, carretera Azumbilla - Lagunas de San Bernardino, (18°35'40.03''N, 97°16'32.76''W), 2570 m, 28.IX.1989, M. Cházaro et al. 6089 (MEXU). Municipio Nicolás Bravo, 5 mi NE of Chapulco, (18°39'52.3''N, 97°22'7''W), 2270 m, 21.VIII.1975, G. Holstein et al. 20049 (MEXU). Municipio Palmar de Bravo, cerro Tepoxtla de San Miguel Esperilla, (18°42'42.3''N, 97°31'11.3''W), 2580 m, 28.XI.1991, P. Tenorio 18248 (MEXU). Municipio Zapotitlán, lado NE en la cima del cerro Canocua, al NE de San Francisco Xochiltepec, 18°16'16.4''N, 97°27'0.1''W, 2419 m, 28.V.2007, I. Rosas et al. 3060 (MEXU); San Francisco Xochiltepec, (18°15'14.9''N, 97°27'3.5''W), 2270 m, 13.VII.1991, A. Valiente-Banuet et al. 989 (MEXU). Veracruz de Ignacio de la Llave, municipio Acultzingo, Ojo de Agua de Arriba, (18°44'32.5''N, 97°19'3.9''W), 2400 m, 15.VI.2013, J. E. Rivera-Hernández et al. 5908 (MEXU).
Cercocarpus macrophyllusC.K. Schneid.
MÉXICO. Aguascalientes, municipio Calvillo, 6 km al N del Temazcal, (22°2'15.87''N, 102°44'17.85''W), 2250 m, 31.X.1987, G. García 3242 (IEB); barranca El Pilar (Sierra Fría), 22°4'49''N, 102°43'48''W, 2442 m, 23.X.2008, J. Martínez-Ramírez 1316 (IEB); parte alta de barranca Los Pilares, 22°3'57.82''N, 102°44'10.33''W, 2560 m, 21.V.2010, J. Martínez-Ramírez 1667 (IEB); sierra del Laurel, ca. 10 mi SE of Calvillo (2-3 hours by horse from Rancho de Los Adobes), (21°45'16''N, 102°43'34.2''W), 2000 m, 4.XI.1959, R. McVaugh y W. N. Koelz 165 (ENCB). Ciudad de México, Coyoacán, Ciudad Universitaria, UNAM, Jardín Botánico Exterior, (19°19'0''N, 99°11'5''W), 2330 m, 14.IV.1995, R. Bye 19536 (MEXU). Coahuila de Zaragoza, municipio Arteaga, Sierra de las Vigas, cañón de Jamé, Rancho El Tirol, aprox. 12 km al NE de Jamé, (25°23'7.62''N, 100°34'24.49''W), 2400-2600 m, 8.V.1995, M. A. Carranza y J. Encinas 2158 (IEB, MEXU). Municipio Saltillo, Sierra Catana, 40 km SW de Saltillo, (25°19'1.75''N, 101°11'50.65''W), 1582 m, 29.VII.1992, J. A. Villarreal et al. 6494 (MEXU). Colima, municipio Minatitlán, Lagunitas, 5 km antes de El Terrero, entre el límite con el estado de Jalisco, (22°19'33.51''N, 103°54'38.81''W), 2000 m, 9.V.1986, F. J. Santana-Michel 2953 (IBUG, IEB). Durango, municipio Pueblo Nuevo, alrededor de 75 km al S de El Salto, 23°39'8.1''N, 105°44'33.1''W, 2505 m, 4.VII.2019, D. Trujillo-Juárez et al. 69 (IBUG). Municipio San Dimas, 4 km al NE de Revolcaderos, (23°37'52.55''N, 105°50'9.64''W), 1900 m, 26.VI.1982, P. Tenorio et al. 634 (ENCB, MEXU). Hidalgo, municipio Zimapán, al NE de Las Trancas, 2 km NE por la desviación a Nicolás Flores, 20°48'2.3''N, 99°15'14''W, 2189 m, 19.IV.2014, D. Trujillo-Juárez et al. 27 (MEXU). Jalisco, municipio Tolimán, km 12 camino El Sauz - Lagunillas, cerca del límite con Colima, (19°28'54.61''N, 103°58'40.92''W), 2100 m, 29.XII.1988, J. A. Pérez de la Rosa et al. 1655 (IBUG, MEXU); Lagunitas, (19°32'12.46''N, 103°58'41.11''W), 1800-1900 m, 15.I.1991, E. Salcedo et al. 181 (IBUG, IEB). Municipio Yahualica de González Gallo, La Yesca - La Tinaja, (21°13'27.48''N, 102°59'30.13''W), 1800-1900 m, 24.I.1993, L. J. Arellano 258 (IBUG). Nuevo León, municipio General Zaragoza, San Antonio Peña Nevada, (23°50'4.76''N, 99°53'39.91''W), 2800 m, 18.V.1978, G. B. Hinton et al. 17339 (ENCB, IEB). Oaxaca, provincia de Oaxaca, Mixteca Alta Javejia, II.1840, H. Galeotti 3070 (MEXU). Distrito Etla, municipio San Felipe Tejalápam, Salinas del Puente León, 17°2'54.2''N, 96°55'12.1''W, 2215 m, 17.I.2012, C. Cervantes-Morales 842 (MEXU). Distrito Juxtlahuaca, municipio San Juan Mixtepec, Tierra Blanca, a 4 km de San Juan Mixtepec, (17°16'12.55''N, 97°50'32.35''W), 2300 m, 6.I.1989, J. Reyes 1430 (MEXU). Municipio San Pedro Nodón, 4 km de San Pedro Nodón, (17°46'40.5''N, 97°5'58.9''W), 1887 m, 17.XI.2004, O. Téllez et al. 17912 (FCME). Querétaro, municipio Peñamiller, Molinitos de Orozco, (21°10'33.94''N, 99°59'10.41''W), 2280 m, 13.XII.1977, S. Zamudio 2603 (ENCB, IEB, MEXU). Tamaulipas, municipio Hidalgo, Los Caballos, (24°0'2.64''N, 99°28'12.3''W, 1700 m), V.1984, F. González-Medrano et al. 14046 (MEXU). Veracruz de Ignacio de la Llave, municipio Camerino Z. Mendoza, predio San Tila, paraje La Cuesta, 18°48'5.4''N, 97°9'25.9''W), 1968 m, 6.III.2013, J. L. Flores-Nicanor 100 (MEXU). Municipio Huayacocotla, camino al Tine, cerca de Huayacocotla, (20°33'26.31''N, 98°29'18.23''W), 2000 m, 10.III.1972, R. Hernández 1590 (ENCB, MEXU). Municipio de Orizaba, Orizaba, mountain side, 11.I.1982, J. G. Smith 199 (MO). Municipio Papantla, Tenixtepec, (19°0'47.63''N, 97°8'26.99''W), 1900 m, 2.XI.1992, H. Oliva y H. García 1425 (IBUG). Municipio Zongolica, cerca de Apanga y de la carretera en construcción a Xochitla, 18°38'0''N, 96°58'22''W, 1582 m, 8.IV.2000, A. Rincón y C. Durán 1343 (MEXU). Zacatecas, municipio Tlaltenango de Sánchez Román, al NW de Jalpa sobre la brecha a Sánchez-Román, ca. del km 37, (21°42'48.72''N, 103°9'38.42''W), 2450 m, 1.XI.1976, R. Guzmán-Mejía 498 (ENCB, IBUG).
Cercocarpus mojadensis C.K. Schneid.
MÉXICO. Chihuahua, municipio Jiménez, ca. 20 (air) km ENE of Cd. Jiménez, upper slopes of Sierra de Chupaderos, (27°11'53.36''N, 104°42'58.8''W), 1677 m, 2.X.1973, J. Henrickson 13782 (MEXU). Coahuila de Zaragoza, municipio Arteaga, sierra de Las Vigas, cañón de Jamé, rancho El Tirol., aprox. 12 km al NE de Jamé, (25°23'7.62''N, 100°34'24.49''W), 2400 m, 8.V.1995, M. A. Carranza y J. Encinas 2153 (MEXU). Municipio Ocampo, minas San Francisco, 160 km al NW de Múzquiz, (28°22'35.42''N, 102°34'32.06''W), 1600 m, 8.III.1971, F. Brizuela 754 (ENCB). Municipio Parras, Sierra de Parras, (25°23'55.28''N, 102°13'3.42''W, 1972 m, 14.V.1973, M. C. Johnston et al. 11000 (MEXU). Municipio Sierra Mojada, Sierra Mojada, 19.IV.1892, M. E. Jones 134 (MO). Municipio Villa de Acuna, serranías del Burro, Rancho El Bonito, on slope between canyons El Bonito and La Pantera in shrub woodland, 29°1'30''N, 102°7'30''W, 1722 m, 19.IX.1977, D. H. Riskind et al. 2193 (MEXU). Durango, municipio Nombre de Dios, San José de La Parilla, (23°44'3.58''N, 104°6'29.4''W), 2258 m, 12.II.1987, J. C. Sánchez 465-b (IEB, MEXU); 2 km al O de San José de La Parilla, 23°44'12.3''N, 104°8'13.08''W, 2274 m, 2.VII.2019, D. Trujillo-Juárez et al. 68 (IBUG). Hidalgo, municipio Cardonal, 26 km al NE de Ixmiquilpan, pasando el Cardonal hacia la barranca de Tolantongo, 1 km al E de la localidad de El Cubo, 20°37'6.4''N, 99°1'42.6''W, 2074 m, 17.III.2014, D. Trujillo-Juárez et al. 16 (MEXU). Municipio Zimapán, twenty mi N of Zimapán, (20°51'28.49''N, 99°14'5.06''W, 2383 m), 14.IV.1947, F. A. Barkley 1330 (ENCB). Nuevo León, municipio Galeana, cerro El Gallo, (24°51'57.28''N, 100°4'56.4''W), 1900 m, 21.II.1990, G. B. Hinton et al. 20134 (IEB, MEXU); Santa Clara de González, Santa Clara, 9 km al S del entronque Galeana - San Roberto, rumbo a Dr. Arroyo, (24°39'28''N, 100°2'16''W), 1900 m, 15.V.1985, F. González-Medrano et al. 14627 (IEB, MEXU), 14663 (MEXU); Santa Clara, (24°38'39.25''N, 100°2'32.79''W), 2050 m, 20.III.1983, G. B. Hinton et al. 18388 (ENCB, IBUG, IEB, MEXU). Municipio Rayones, E of road leading from Rayones to Galeana, 13.6 mi from middle of bridge across Río Pilon, 24°55'45''N, 100°3'45''W, 1500 m, 9.IV.1994, T. F. Patterson et al. 7476 (MEXU). Municipio Santiago, near San Isidro, (25°21'28.28''N, 100°17'51.55''W), 1800 m, 12.V.1994, G. B. Hinton et al. 24165 (IEB, MEXU). Querétaro, municipio Cadereyta de Montes, 10 km al E de Maconí, (20°50'30.05''N, 99°29'55.5''W), 2000 m, 26.III.1985, R. Fernández 2862 (ENCB, IEB); ladera NE de la Sierra Peña Azul, 6.5 km al SW de Vizarrón, (20°47'17.26''N, 99°44'16.85''W), 2410 m, 30.IV.1978, S. Zamudio 2758 (IBUG, IEB, MEXU). Municipio Querétaro, 6 km al NW de La Luz, en terrenos de la hacienda Raspiño, (20°53'40.21''N, 100°28'10.21''W), 2300 m, 23.IX.1994, J. Rzedowski 52517 (IEB). Municipio Tolimán, 14 km al NW de Tolimán, sobre el camino a El Derramadero, (20°58'0.5''N, 100°1'1.7''W), 2200 m, 9.IX.1990, J. Rzedowski 50137 (IEB). Tamaulipas, municipio Miquihuana, 15 km al N de La Perdida, (23°37'42.16''N, 99°52'21.63''W), 1700 m, 18.IV.1976, F. González-Medrano et al. 8769 (ENCB, MEXU); camino al cañón del Soldado por la brecha a la Marcela, (23°38'50.96''N, 99°51'33.72''W), 1900 m, 16.V.1986, M. Martínez 1082 (MEXU). Zacatecas, municipio Concepción del Oro, al sureste de Mazapil, 26.6 km al este de San Tiburcio, 24°8'27''N, 101°13'47''W, 2133 m, 10.IV.2014, J. A. Encina et al. 3774 (MEXU).
Cercocarpus pringlei (C.K. Schneid) Rydb.
MÉXICO. Oaxaca, La Hoya canyon, 1676 m, 2.XI.1894, C. G. Pringle 6140 (MEXU); Oaxaca, II.1934, J. R. Bruff 1257 (MEXU). Municipio San Juan Achiutla, 1.5 km al N de San Juan Achiutla por el camino a Santa María Nduayaco, 17°22'33''N, 97°30'30''W, 1840 m, 31.X.2018, P. Carillo-Reyes et al. 9131 (IBUG). Municipio San Pedro y San Pablo Teposcolula, 500 m al S del juego de pelota del cerro de Pueblo Viejo, (17°29'58.33''N, 97°28'17.37''W), 2348 m, 4.II.2006, A. García-Mendoza y S. Franco 8292 (MEXU). Distrito Teposcolula, municipio San Pedro y San Pablo Tequixtepec, 1.6 km E of highway 125 on the road to Guadalupe Cuautepec at km 85 from Tehuacán on highway 125, (18°3'23.4''N, 97°41'42.06''W), 1960 m, 18.X.1985, B. Bartholomew et al. 3069 (MEXU). Distrito de Teposcolula, municipio San Pedro Yucunama, Mixteca Alta, 3 km al E de Yucunama, (17°34'13.14''N, 97°27'37.43''W), 2630 m, 17.II.1982, A. García-Mendoza 857 (FCME, MEXU). Distrito Juxtlahuaca, municipio San Sebastián Tecomaxtlahuaca, solo 5 km de la desviación a San Sebastián Tecomaxtlahuaca, (17°19'19''N, 98°3'24.26''W, 1900 m), 24.IV.1996, J. I. Calzada 20983 (MEXU); Sabino Solo, a 4.5 km de San Sebastián Tecomaxtlahuaca, carretera hacia San Martín Duraznos, 17°19'30.2''N, 98°3'28.7''W, 1595 m, 9.III.1997, J. I. Calzada 21787 (IBUG, MEXU); a 5 km de San Sebastián Tecomaxtlahuaca, laderas de Sabino Solo, (17°19'35.02''N, 98°3'10.28''W), 1800 m, 21.III.1998, J. I. Calzada 22491 (MEXU). Municipio Santa Catarina Ixtepeji, between Oaxaca and Valle Nacional 19 km N of highway 190, (17°11'16.16''N, 96°36'8.5''W), 2560 m, 22.X.1985, B. Bartholomew et al. 3274 (MEXU). Distrito Cuicatlán, municipio Santiago Nacaltepec, 2 km al NO de Cieneguilla, brecha a Santa María Tejotepec, (17°28'33''N, 96°57'18''W), 2075 m, 25.I.1995, A. Salinas y E. Martínez-Correa 8089 (MEXU); 158.3 km de la carretera Tehuacán - Cuicatlán, 17°33'44.7''N, 96°56'47.3''W, 1787 m, 15.XI.2004, O. Téllez et al. 17618 (FCME). Distrito Santiago Juxtlahuaca, municipio Santos Reyes Tepejillo, 8 km al N de Santos Reyes Tepejillo, entrada por La Cruz Río Boquerón, (17°28'49.96''N, 97°54'1.49''W, 1824 m), 14.II.1995, J. I. Calzada 19698 (MEXU). Distrito de Huajuapan, municipio Zapotitlán Palmas, 10 km al NO de Huajuapan, (17°51'22.39''N, 97°49'9.42''W), 2000 m, 16.II.1988, A. García-Mendoza et al. 3610 (MEXU). Puebla, municipio Caltepec, cerro El Capulín, SW de Los Membrillos, (18°9'12.17''N, 97°30'45.95''W), 2000 m, 8.XI.1984, P. Tenorio y C. Romero 8010 (IEB, MEXU). Municipio Molcaxac, cañada de Mamacla, (18°44'55.25''N, 97°58'39.73''W), 1900 m, 20.XII.1982, R. Medina y A. Valiente 419 (ENCB, MEXU, UAMIZ).
Cercocarpus sp. 1
MÉXICO. Guerrero, municipio Chilapa de Álvarez, a 16 km de Tixtla por la carretera a Tlapa, (17°35'49.39''N, 99°18'21.24''W), 1790 m, 6.II.1981, J. L. Contreras 779 (FCME). Municipio Chilpancingo de Los Bravo, 6.5 mi W of Chilpancingo on road above and SW of village of Amojileca, (17°33'43.55''N, 100°46'22.48''W), 1850 m, 3.XII.1966, W. R. Anderson y C. W. Laskowski 4343 (ENCB); along road from Chilpancingo W toward Omilte 10.4 mi W of Chilpancingo, (17°34'9.96''N, 99°36'21.93''W), 1840 m, 27-28.VII.1968, W. R. Anderson y C. Anderson 4953 (ENCB); Colonia México, 1250 m, 19.I.2014, R. Castro 17993 (FCME); cañada de Atzizintla, al N de Chilpancingo, 1200 m, 28.XII.1967, J. Chavelas-Polito 2888 (ENCB); aprox. 1 km al SW de Ixtemalco por el camino Chilpancingo - San Vicente, (17°30'59.93''N, 99°36'1.04''W), 2100 m, 8.I.1984, A. Peláez s.n. (FCME, IBUG). Municipio Eduardo Neri, Tlapangalapa, (17°43'36.6''N, 99°27'33.6''W), 1582 m, 21.II.2010, DIAAPROY S.A. de C.V. 70469 (MEXU). Municipio Taxco de Alarcón, Tlamacazapa, 3 km antes del poblado, entrando vía Taxco, (18°29'39.93''N, 99°31'18.69''W), 1900 m, 28.I.1998, F. Terán y P. Lara 406 (FCME, MEXU); Palo de Chicharrón, carretera Juliantla - Tlamacazapa (0.5 km de la carretera Juliantla - Tlamacazapa), (18°30'52.75''N, 99°33'40.51''W), 1800 m, 26.VII.1988, F. Terán et al. 444 (FCME, MEXU). Municipio Zitlala, Topiltepec (reserva campesina), (17°39'16.84''N, 99°14'10.9''W, 1700 m), 14.II.1996, C. Miranda 20 (FCME). Oaxaca, distrito de Huajuapan, municipio San Pedro y San Pablo Tequixtepec, paraje Horno de Pan, 200 m al este de la desviación de Cuautepec, 2022 m, 30.XI.1999, E. Cruz-Cruz 419 (MEXU).
Cercocarpus sp. 2
MÉXICO. Coahuila de Zaragoza, municipio Arteaga, ca. 25 mi southeast of Saltillo above Rancho Chapultepec, ca. 4 mi N of Huachichil, (25°17'19.18''N, 100°46'22.48''W), 2200 m, 16.V.1949, R. McVaugh 10551 (ENCB, MEXU). Municipio General Cepeda, Sierra de la Concordia, 10 km al N de ejido la Casita, 25°13'55''N, 101°25'27''W, 2150 m, 23.X.1996, J. A. Encina y J. Zavala 373 (MEXU). Municipio Saltillo, Sierra Zapalinamé, Las Vacas, 2100 m, VI.1942, E. Lyonnet 3543 (IEB, MEXU); cañón de San Lorenzo, 5-6 mi southeast of Saltillo, (25°19'59.25''N, 100°59'26.39''W), 2200 m, 28.V.1951, R. McVaugh 12349 (ENCB). Nuevo León, municipio Aramberri, El Salitre, 1465 m, 26.III.1994, G. B. Hinton et al. 24060 (MEXU). Municipio Galeana, road to summit of cerro Potosí, ca. 3.6 mi from Dieciocho de Marzo, (24°52'50.05''N, 100°11'47.19''W, 2430 m), 18.V.1982, L. J. Dorr y T. L. Atkins 2300 (MEXU); Cerro Potosí, 15 km al NW de Galeana, (24°52'10.61''N, 100°13'49.06''W), 2600 m, 23.V.1982, R. Sánchez-Silva 100 (MEXU). Municipio Iturbide, about 3 mi above Iturbide, on road to Galeana, (24°43'57.47''N, 99°55'51.33''W), 2600 m, 18.V.1949, R. McVaugh y R. L. Wilbur 10574 (MEXU). Municipio Santiago, San Isidro, (25°21'28.28''N, 100°17'51.55''W), 1800 m, 12.V. 1994, G. B. Hinton et al. 24164 (MEXU).
Cercocarpus sp. 3
MÉXICO. Puebla, municipio Aljojuca, cerro al E de Aljojuca, (19°5'32.17''N, 97°30'46.6''W), 2650 m, 21.IV.2005, J. L. Contreras 8272 (MEXU). Municipio Guadalupe Victoria, en el cerro de la Derrumbada Roja, (19°17'49.1''N, 97°27'13''W), 2700 m, 6.XI.1977, M. Cházaro 721 (ENCB). Veracruz de Ignacio de la Llave, municipio Perote, cerro de Tenextepec, 19°28'3''N, 97°16'33''W, 2660 m,19.XI.1997, G. Castillo- Campos et al. 16583 (IEB, MEXU); loc. cit., 28.IV.1998, G. Castillo-Campos y S. Avendaño 17653 (IEB, MEXU).
Apéndice 2
Ejemplares representativos de Cercocarpus Kunth en los cuales examinamos las características anatómicas y de arquitectura foliar. Las coordenadas entre paréntesis indican que fueron calculadas. Los códigos entre paréntesis son los mostrados en la Figura 5.
Cercocarpus fothergilloides Kunth
MÉXICO. Oaxaca, municipio de Chapulco, 7 km antes de llegar a Nicolás Bravo, carretera Azumbilla - Lagunas de San Bernardino, (18°35'40.03''N, 97°16'32.76''W), 2570 m, 28.IX.1989, M. Cházaro et al. 6089 (MEXU) (MCB6089). Veracruz de Ignacio de la Llave, municipio Acultzingo, Ojo de Agua de Arriba, 15.VI.2013, J. E. Rivera-Hernández et al. 5908 (MEXU) (JRH5908).
Cercocarpus macrophyllusC.K. Schneid.
MÉXICO. Durango, municipio Pueblo Nuevo, alrededor de 75 km al S de El Salto, 23°39'8.1''N, 105°44'33.1''W, 2505 m, 4.VII.2019, D. Trujillo-Juárez et al. 69 (IBUG) (DTJ69). Hidalgo, municipio Zimapán, al NE de Las Trancas, 2 km NE por la desviación a Nicolás Flores, 20°48'2.3''N, 99°15'14''W, 2189 m, 19.IV.2014, D. Trujillo-Juárez et al. 27 (MEXU) (DTJ27). Jalisco, municipio Tolimán, km 12 camino El Sauz - Lagunillas, cerca del límite con Colima, (19°28'54.61''N, 103°58'40.92''W), 2100 m, 29.XII.1988, J. A. Pérez de la Rosa et al. 1655 (IBUG) (JAP1655); Lagunitas, (19°32'12.46''N, 103°58'41.11''W), 1800-1900 m, 15.I.1991, E. Salcedo et al. 181 (IBUG) (ES181). Municipio Yahualica de González Gallo, La Yesca - La Tinaja, (21°13'27.48''N, 102°59'30.13''W), 1800-1900 m, 24.I.1993, L. J. Arellano 258 (IBUG) (JLA258). Oaxaca, distrito Etla, municipio San Felipe Tejalapam, Salinas del puente León, 17°2'54.2''N, 96°55'12.1''W, 2215 m, 17.I.2012, C. Cervantes-Morales 842 (MEXU) (CM843). Distrito Juxtlahuaca, municipio San Juan Mixtepec, Tierra Blanca, a 4 km de San Juan Mixtepec, (17°16'12.55''N, 97°50'32.35''W), 2300 m, 6.I.1989, J. Reyes 1430 (MEXU) (REY1430). Veracruz de Ignacio de la Llave, municipio Papantla, Tenixtepec, (19°0'47.63''N, 97°8'26.99''W), 1900 m, 2.XI.1992, H. Oliva y H. García 1425 (IBUG) (HO1425). Zacatecas, municipio Tlaltenango de Sánchez Román, al NW de Jalpa sobre la brecha a Sánchez-Román, ca. del km 37, (21°42'48.72''N, 103°9'38.42''W), 2450 m, 1.XI.1976, R. Guzmán-Mejía 498 (IBUG) (RGM498).
Cercocarpus mojadensis C.K. Schneid.
MÉXICO. Chihuahua, municipio Jiménez, ca. 20 (air) km ENE of Ciudad Jiménez, upper slopes of Sierra de Chupaderos, (27°11'53.36''N, 104°42'58.8''W), 1677 m, 2.X.1973, J. Henrickson 13782 (MEXU) (JH13782). Durango, municipio Nombre de Dios, 2 km al O de San José de La Parilla, 23°44'12.3''N, 104°8'13.08''W, 2274 m, 2.VII.2019, D. Trujillo-Juárez et al. 68 (IBUG) (DTJ68). Hidalgo, municipio Cardonal, 26 km al NE de Ixmiquilpan, pasando el Cardonal hacia la barranca de Tolantongo, 1 km al E de la localidad de El Cubo, 20°37'6.4''N, 99°1'42.6''W, 2074 m, 17.III.2014, D. Trujillo-Juárez et al. 16 (MEXU) (DTJ16). Nuevo León, municipio Galeana, Santa Clara, (24°38'39.25''N, 100°2'32.79''W), 2050 m, 20.III.1983, G. B. Hinton et al. 18388 (IBUG, MEXU) (GBH18388); cerro El Gallo, (24°51'57.28''N, 100°4'56.4''W), 21.II.1990, G. B. Hinton et al. 20134 (MEXU) (GBH20134). Municipio Santiago, near San Isidro, (25°21'28.28''N, 100°17'51.55''W), 1800 m, 12.V.1994, G. B. Hinton et al. 24165 (MEXU) (GBH24165). Querétaro, municipio Cadereyta de Montes, ladera NE de la Sierra Peña Azul, 6.5 km al SW de Vizarrón, (20°47'17.26''N, 99°44'16.85''W), 2410 m, 30.IV.1978, S. Zamudio 2758 (IBUG, MEXU) (SZ2758). Tamaulipas, municipio Miquihuana, camino al cañón del Soldado por la brecha a la Marcela, (23°38'50.96''N, 99°51'33.72''W), 1900 m, 16.V.1986, M. Martínez 1082 (MEXU) (MM1082).
Cercocarpus pringlei (C.K. Schneid) Rydb.
MÉXICO. Oaxaca, municipio San Juan Achiutla, 1.5 km al N de San Juan Achiutla por el camino a Santa María Nduayaco, 17°22'33''N, 97°30'30''W, 1840 m, 31.X.2018, P. Carrillo-Reyes et al. 9131 (IBUG) (PCR9131). Puebla, municipio Caltepec, Cerro El Capulín, SW de Los Membrillos, (18°9'12.17''N, 97°30'45.95''W), 2000 m, 8.XI.1984, P. Tenorio y C. Romero 8010 (MEXU) (PT8010).
Cercocarpus sp. 1
MÉXICO. Guerrero, municipio Chilpancingo de Los Bravo, aprox. a 1 km al SW de Ixtemalco por el camino Chilpancingo-San Vicente, (17°30'59.93''N, 99°36'1.04''W), 2100 m, 8.I.1984, A. Peláez s.n. (IBUG) (APSN). Municipio Zitlala, Topiltepec (reserva campesina), (17°39'16.84''N, 99°14'10.9''W, 1700 m), 14.II.1996, C. Miranda 20 (FCME) (MIR20).
Cercocarpus sp. 2
MÉXICO. Nuevo León, municipio Galeana, road to summit of cerro Potosí, ca. 3.6 mi from Dieciocho de Marzo, (24°52'50.05''N, 100°11'47.19''W, 2430 m), 18.V.1982, L. J. Dorr y T. L. Atkins 2300 (MEXU) (LTD2300).
Cercocarpus sp. 3
MÉXICO. Veracruz de Ignacio de la Llave, municipio Perote, cerro de Tenextepec, 19°28'3''N, 97°16'33''W, 2660 m, 28.IV.1998, G. Castillo-Campos y S. Avendaño 17653 (MEXU) (GCC17653).
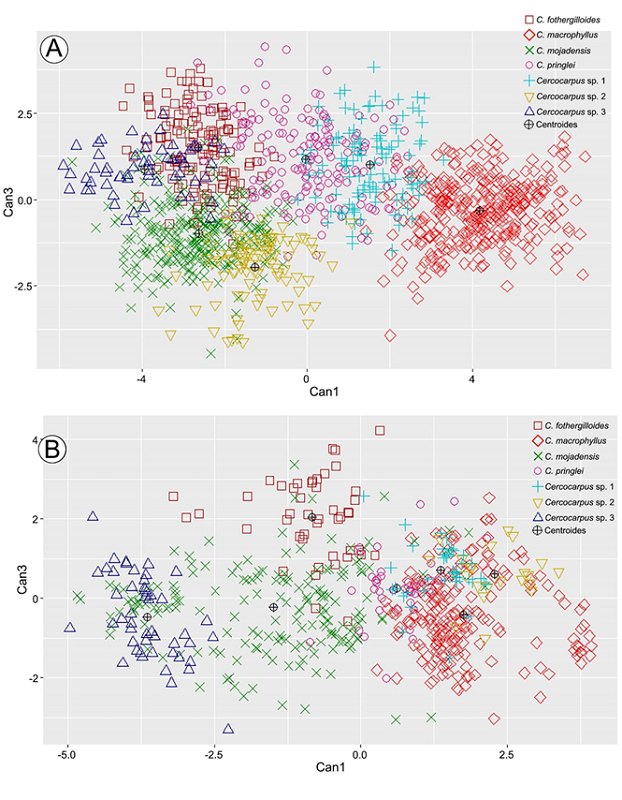
Apéndice 3:
Figura que muestra las gráficas de los ADCs. A. primera y tercera función del ADC de los caracteres morfológicos; B. primera y tercera función del ADC de los caracteres anatómicos. Abreviaciones. Can1=primera función canónica. Can3=tercera función canónica.
Contribución de autores
Financiamiento
Author notes
6Autor para la correspondencia: dianatrujillo2311@gmail.com
