Ensayos
Los Deltochilina (Coleoptera: Scarabaeinae), un grupo indicador biogeográfico en el sureste de México
The Deltochilina (Coleoptera: Scarabaeinae), a biogeographical indicator group in southeastern Mexico
Los Deltochilina (Coleoptera: Scarabaeinae), un grupo indicador biogeográfico en el sureste de México
Acta zoológica mexicana, vol. 38, e2457, 2022
Instituto de Ecología A.C.
Recepción: 15 Octubre 2021
Aprobación: 13 Diciembre 2022
Publicación: 26 Diciembre 2022
Resumen: Se utilizaron como indicadores biogeográficos siete especies de Deltochilina (Anomiopus cirulito, Canthon triangularis, C. lituratus, C. edmondsi, C. morsei, C. angustatus y C. lucreciae), para ejemplificar la influencia de la fauna sudamericana en la diversidad tropical mexicana, buscando explicar por qué México, al sur del Istmo de Tehuantepec, es cada vez más Neotropical. La escala temporal empleada es del fin del Pleistoceno a la época actual y se consideraron tres niveles de información: 1) Penetración con presencia mínima, 2) Penetración con poblaciones marginales y 3) Penetración con poblaciones establecidas. Se ofrecen ejemplos de invasores foráneos que han tenido éxito en lugares ganaderos, sin desplazar a ninguna especie autóctona. Los fenómenos naturales que han condicionado la distribución actual de las especies indicadoras seleccionadas se corresponden con procesos geológicos y macroclimáticos, que influyeron en la composición y los movimientos de las horobiotas a nivel continental. La tendencia de Deltochilini de Centro y Sudamérica por invadir México ha sido muy intensa, empleando el Puente Panameño o incluso el puente inter-Caribe para dispersarse, avanzando con las selvas y, su número supera a las especies incipientes de penetración reciente, de cualquier otro borde de México.
Palabras clave: Escarabajos coprófagos, Deltochilini, Región Neotropical, diversidad tropical mexicana, Istmo de Tehuantepec, fauna sudamericana, nuevos registros.
Abstract: Seven Deltochilina species (Anomiopus cirulito, Canthon triangularis, C. lituratus, C. edmondsi, C. morsei, C. angustatus and C. lucreciae) were used as biogeographic indicators, to exemplify the influence of South American fauna in Mexican tropical diversity, seeking to explain why Mexico, south of the Isthmus of Tehuantepec, is increasingly Neotropical. The time scale used is from the end of the Pleistocene to the present time and three levels of information were considered: 1) Penetration with minimal presence, 2) Penetration with marginal populations and 3) Penetration with established populations. Examples of foreign invaders that have successfully established in livestock areas, without displacing any native species, are provided in this study. The natural phenomena that have conditioned the current distribution of the selected indicators correspond to geological and macroclimatic processes, which influenced the composition and movements of horobiota at the continental level. The tendency of Deltochilini from Central and South America to invade Mexico has been very intense, using the Panamanian Bridge or even the inter-Caribbean bridge to disperse, advancing with the jungle and, their number exceeds the incipient species of recent penetration, of any other border of Mexico.
Key words: Dung beetles, Deltochilini, Neotropical Region, mexican tropical diversity, Isthmus of Tehuantepec, south American fauna, new records.
Introducción
La medición es un proceso básico de la ciencia, y en el campo de la Biología medir es una actividad habitual. Hay cosas que pueden medirse y otras que no: existen cosas mensurables y cosas que no son susceptibles de medición, ya que no se dispone de una escala o de una unidad que permita este tipo de registros. Además de razones puramente técnicas, medir otorga valor, sitúa en el medio ambiente, así como en el medio humano y, ayuda a comparar fenómenos que tienen una magnitud similar. En el fondo, siempre estamos midiendo, incluso el campesino que estima que en su campo hay el doble de frutos (incluso solamente muchos frutos) ya está midiendo. Como es imposible saber qué pasa con todos los conjuntos de seres vivos, usamos a los escarabajos copronecrófagos como un indicador biológico (Favila & Halffter, 1997; Arellano et al., 2005; Escobar et al., 2007; Halffter et al., 2007) y biogeográfico (Halffter & Morrone, 2017), cuyo comportamiento y número refleja el de la comunidad, ayudando a descifrar acontecimientos actuales o pasados, relacionados con el estudio de un ambiente.
Para incorporar a los artrópodos como auxiliares en el diagnóstico de las comunidades naturales, se ha propuesto elegir grupos indicadores que deben reunir atributos básicos (Brown, 1991), siendo los coleópteros Scarabaeoidea recomendados para comparar ambientes terrestres en el tiempo y el espacio, debido a su notable riqueza específica y diversidad de hábitos (Halffter & Favila, 1993; Schuster et al., 2000; Morón, 2014). Una gran proporción de especies de Scarabaeidae tienen distribución geográfica y ecológica restringida y con frecuencia se les puede considerar como entidades endémicas. Además de todas las consideraciones ecológicas y evolutivas que se puedan desarrollar a partir de estos hechos, esta característica es muy valiosa para seleccionar a varias especies como indicadores biogeográficos, ya que los fenómenos naturales que han condicionado su distribución espacial y aislamiento, se corresponden con procesos geológicos y macroclimáticos, acaecidos en tiempos pasados, que influyeron en la composición y los movimientos de las horobiotas a nivel continental (Liebherr, 1988; Morón, 2006; Morrone, 2009).
Un concepto introducido por Halffter desde los primeros trabajos sobre la Zona de Transición Mexicana (ZTM), es el de patrón de distribución, que hace referencia a la distribución actual de un cenocrón. En cuanto a su origen y penetración en la ZTM, se distinguen cinco patrones. Uno de ellos, es el patrón de distribución Neotropical Típico, que lo integran especies que tienen un origen sudamericano-neotropical. Halffter (2017) propuso dividir estos elementos neotropicales según su penetración mínima, media o amplia, según la antigüedad relativa de su penetración y también, por su éxito en la colonización de la parte tropical de la ZTM.
Con este trabajo, se aportan ejemplos de cada tipo de penetración con los cuales se busca tener una idea más concreta, de la influencia de la fauna sudamericana en la diversidad tropical mexicana. Como instrumento de trabajo se consideran a los escarabajos coprófagos de la tribu Deltochilini (Scarabaeidae, Scarabaeinae) Lacordaire, 1856 (ex Canthonini) (Tarasov & Génier, 2015; Tarasov & Dimitrov, 2016), como indicadores biogeográficos y la escala temporal empleada es del fin del Pleistoceno (~ en el 10,000 a. C.) a la época actual (Antropoceno). La selección a priori de esta subtribu de escarabajos es debido a que: 1) en general ha sido bien estudiada en cuanto a su taxonomía, biología, comportamiento y ecología (Halffter, 1961; Rivera-Cervantes & Halffter, 1999); 2) es un grupo filogenéticamente bien definido (Tarasov & Génier, 2015; Tarasov & Dimitrov, 2016); 3) forman un gremio funcional y taxonómicamente bien definido; 4) se ha estandarizado un método simple para su colecta usando trampas de caída (Lobo et al., 1988); y 5) existe una hipótesis bien aceptada sobre su llegada en dos oleadas de Sudamérica a Norte América (Halffter, 1964; 1974; 1976; Kohlmann & Halffter, 1990).
Materiales y métodos
Para desarrollar este estudio fueron considerados los tres niveles de información propuestos por Halffter (2017), que surgen de datos de colectas puntuales ejercidos por los autores, datos de especímenes de la colección Gonzalo Halffter Salas (GHSC) y algunos datos de literatura, de los cuales se aporta la cita:
Primer nivel, “Penetración con presencia mínima”: se reúnen especies con presencia única, puntual o muy restringida en México en los grandes manchones de selva lluviosa del sureste (independientemente de si en otro lugar son abundantes), pues el propósito es buscar puntos de posible penetración en México.
Segundo nivel, “Penetración con poblaciones marginales”: se reúnen líneas de especies con penetración media en el sureste mexicano, que son muy recientes y marginales, pero que siguen teniendo éxito reproductivo.
Tercer nivel, “Penetración con poblaciones establecidas”: se reúnen líneas de especies con penetración amplia, las cuales han formado poblaciones incipientes, pero ya estables o que tienden a ello.
Cabe mencionar que en este estudio no se consideraron dos grupos de especies invasoras recientes: los grupos subhyalinus y viridis del género Canthon, subgénero Glaphyrocanthon, por ser más numerosos y antiguos (Mioceno).
Todas las especies revisadas se encuentran depositadas en la colección Gonzalo Halffter Salas (GHSC), Coatepec, Veracruz (donada al INECOL, como legado del Dr. Gonzalo Halffter), con excepción de la especie Canthon (Glaphyrocanthon) edmondsi, de la cual únicamente se cuenta con los datos obtenidos de la literatura. Las fotografías de las Figuras 1-8 fueron tomadas por F. Escobar-Hernández usando una cámara Leica DMC 2900, integrada a un microscopio Leica Z16 AP0A; las imágenes multifocales fueron procesadas con el software Leica Application Suite ver. 4.7. Las figuras fueron editadas con el software Corel Photo-Paint 11® por S. L. Rivera-Gasperín.

Figuras 1-8
1) Vista dorsal de Canthon triangularis; 2) Etiquetas de colecta de Canthon triangularis; 3) Vista dorsal de Anomiopus cirulito; 4) Vista dorsal de Canthon lituratus; 5) Vista dorsal de Canthon morsei; 6) Vista lateral de Canthon morsei; 7) Vista dorsal de Canthon angustatus; 8) Vista dorsal de Canthon lucreciae. Escala= 2 mm. (Fotos ©F. Escobar-Hernández).
Resultados
Penetración con presencia mínima de Canthon triangularis (Drury, 1770) (Figs. 1, 2). Se reporta por primera vez la presencia de Canthon triangularis (Drury, 1770) en la Estación de Biología Tropical Los Tuxtlas, Veracruz, México, colectada de forma fortuita en las instalaciones de la estación, sin haber ejercido un esfuerzo para su colecta o un muestreo formal. Esta especie es abundante y está ampliamente distribuida en el noreste de Sudamérica, de Bolivia hacia el norte, incluyendo Brasil, las Guayanas, Venezuela y Colombia (Medina et al., 2001). Material examinado: MÉXICO: Veracruz. Los Tuxtlas-Estación Biológica Tropical. 9-IX-1992 G. Halffter col. 18°35.11´ N, 95°04.45´ O.
Penetración con presencia mínima de Anomiopus cirulitoCano, 2018 (Fig. 3). Se registran dos capturas de esta especie en la selva de Nueva Betania, Palenque, Chiapas, México, por Escobar-Hernández et al. (2019). Anteriormente, Anomiopus cirulito se conocía únicamente en la selva de la Reserva de la Biosfera Maya, Departamento de Petén, Guatemala (Cano, 2018). Anomiopus es un género típicamente sudamericano (con 61 especies), con sólo otra especie en Centroamérica: Anomiopus panamensis (Paulian, 1939) de Panamá y Costa Rica (también presente en Colombia) (Canhedo, 2006).
Penetración con presencia mínima de Canthon (Canthon) lituratus (Germar, 1813) (Fig. 4). Navarrete y Halffter (2008a) registraron una sola captura de esta especie, atraída con una trampa de caída cebada con excremento humano, en la Selva Lacandona (Reserva de la Biósfera Montes Azules, Chiapas, México). Es una especie de amplia distribución en Sudamérica, cuyo límite de distribución norte estaba registrado hasta Costa Rica, con un límite máximo de altitud de 1,000 m (Solís & Kohlmann, 2002; Navarrete & Halffter, 2008b).
Penetración con poblaciones marginales de Canthon (Glaphyrocanthon) edmondsiRivera-Cervantes y Halffter, 1999. Rivera-Cervantes y Halffter (1999), consideran a los Canthon (Glaphyrocanthon) de México como un grupo aislado e importante que se distingue de los otros Canthon. Pero hay una excepción, hasta el momento Canthon (Glaphyrocanthon) edmondsi no encaja con ninguno de los grupos del subgénero. Es una especie considerada del interior de la selva y, en su momento, junto con Rivera-Cervantes se estudiaron 53 ejemplares colectados en la Estación de Biología Tropical Los Tuxtlas, Veracruz (cerca de Catemaco), así como un lote colectado en Rancho Grande, Estado de Aragua, Venezuela. Actualmente no se cuenta con el material, por lo cual no fue posible obtener una fotografía.
Penetración con poblaciones establecidas de Canthon (Canthon) morsei Howden, 1966 (Figs. 5, 6). Se trata de una especie asociada a bosques tropicales perennifolios que ha sido colectada en los estados de Jalisco, Estado de México, Veracruz y Chiapas. Ha sido señalada por Padilla-Gil y Halffter (2007) como una especie con penetración limitada en México. Material examinado adicional: (1 ♂) MÉXICO: Veracruz, Estación de Biología Tropical Los Tuxtlas, UNAM, 18-IX-76. Trampa hígado de pollo. M. A. Morón, R. Terrón cols., depositado en la Colección Halffter, Xalapa, Veracruz, México (GHSC). (1 ♀) MÉXICO: Chiapas, Laguna de Miramar, 14/15-X-1976. Cebo pescado. V. y G. Halffter cols., (GHSC). MÉXICO: Chiapas, Palenque, 26-V-1965, G. y V. Halffter cols., (GHSC). MÉXICO: Chiapas, Palenque. Área del templo de las inscripciones, selva perennifolia, trampa con excremento humano, noche, 19-V-93, G. y V. Halffter cols., (GHSC). GUATEMALA: Izabal, Cayuga Gruta de Silvino, 20-VIII-1969, S. & J. Peck cols., (GHSC).
Penetración con poblaciones establecidas de Canthon (Glaphyrocanthon) angustatus Harold, 1867 (Fig. 7). Esta especie no se considera dentro del grupo de C. (Gl.) subhyalinus, ya que realmente solo hay una convergencia ecológica. Es una especie que puede ser frecuente, es coprófaga, diurna, de selva, igualmente asociada al excremento de los monos Alouatta palliata (Gray, 1849) y A. pigra Lawrence, 1933. En México se ha colectado en el estado de Chiapas, en la Selva Lacandona cerca de la frontera con Guatemala, por los autores del presente estudio; en la Reserva de Montes Azules por Howden y Young (1981), Solís y Kohlmann (2002), Chamé-Vázquez y Gómez y Gómez (2005), Navarrete y Halffter (2008b); y en Palenque por Halffter y Halffter (2009). En Veracruz se ha colectado en Las Choapas por Sánchez-Huerta et al. (2019); también se distribuye en Perú, Ecuador, Colombia, Panamá, Costa Rica, Nicaragua, Guatemala y Belice (Chamé-Vázquez & Gómez y Gómez, 2005).
Penetración con poblaciones establecidas de Canthon (Canthon) lucreciaeHalffter & Halffter, 2009 (Fig. 8). Es una especie endémica de la Depresión Central de Chiapas, con un rango de altitud entre los 600 y 700 m y, aunque su distribución está totalmente localizada, es una especie abundante. A diferencia de los otros elementos que mencionamos, C. (Canthon) lucreciae es una especie de ambiente antropizado y, por lo tanto, sus orígenes son diferentes al de otras especies de selva, y sus afinidades difieren de las especies de ambiente exclusivamente tropical, como las encontradas en países centroamericanos. Se le ha emparentado con Canthon (Canthon) indigaceus chevrolati Harold, 1868, un linaje tropical de antigüedad media, pero no de selva (Halffter & Halffter, 2009).
Penetración con poblaciones establecidas de Digitonthophagus gazella (Fabricius, 1787). Caso excepcional, por tratarse de una especie invasora. Para mencionar los dos ejemplos más espectaculares de invasores, aunque provienen de procesos muy distintos, están los casos de D. gazella y de Euoniticellus intermedius (Reiche, 1848). Desde 1972 fueron introducidos en Texas, EUA, provenientes de los continentes africano y asiático. Se reprodujeron en la estación del College Station, Texas, y posteriormente fueron liberados por el Departamento de Agricultura de los Estados Unidos (USDA) para el control de exceso de boñigas (Fincher, 1981). Actualmente, ambas especies están presentes en la mayoría de los estados mexicanos y en casi todo el continente americano. Digitonthophagus gazella tiene éxito colonizando la mayor parte de los lugares ganaderos, sin desplazar a ninguna especie autóctona. Este invasor ha ocupado un nicho que estaba vacío, el que debieron ocupar escarabajos asociados a grandes vertebrados antes de la extinción de la mayor parte de estos mamíferos y antes de la llegada del ganado europeo. Es un caso en el cual podemos decir que “lo necesario llegó a tiempo”. Una característica intrínseca que ha ayudado a esta especie invasora a ser buena colonizadora y ha permitido su expansión (y por la cual hoy podemos considerarla como indicadora biogeográfica), es que es una especie que se ve favorecida por las perturbaciones antropogénicas como la ganadería, pues al contrario de las especies nativas, el disturbio les proporciona una condición ideal para desarrollarse.
Digitonthophagus gazella es muy abundante en pastizales y potreros ganaderos, pues sus hábitos son coprófagos, con una fuerte atracción hacia el excremento bovino y, por el contrario, en las selvas su éxito es nulo o extremadamente menor. Por ejemplo, no ha sido colectado en lugares de selva como la Reserva de la Biosfera de Montes Azules, Chiapas (Sánchez-Hernández et al., 2018) y en Palenque presenta una penetración mínima hacia la selva, sin embargo, es bien sabido que abunda en pastizales de ganado bovino muy próximos a esta zona arqueológica.
En México se ha establecido en localidades áridas, semiáridas, tropicales y subtropicales, dispersándose de norte a sur siguiendo tres frentes de penetración principales: llanuras del Golfo de México (Nuevo León, Tamaulipas, Veracruz, Yucatán), Altiplano Mexicano (Coahuila, Durango, Hidalgo) y llanuras del Pacífico (Chiapas, Guerrero, Jalisco, Nayarit, Oaxaca) (Morón et al., 1988; 1998; Montes de Oca et al., 1994; Kohlmann, 1994; Montes de Oca & Halffter, 1998; Verdú et al., 2007; Arellano et al., 2008; Basto-Estrella et al., 2014; Moctezuma, 2021). Los principales sistemas montañosos representan para esta especie una barrera natural (Kohlmann, 1994), lo cual impide una invasión a estas áreas, sin embargo, ha continuado su distribución por las costas llegando al norte de Centroamérica y Sudamérica (Miranda et al., 1990; Kohlmann, 1994; Noriega, 2002; Solís & Kohlmann, 2002; Álvarez-Bohle et al., 2009; Pablo-Cea et al., 2017).
Discusión
La tribu Deltochilini cuenta con una gran riqueza de especies en Sudamérica, por lo cual, Halffter (1974) ha sugerido que tiene una distribución gondwánica antigua, pues hasta el período Cretácico, México era solo una península del continente norteamericano, sin embargo, con la emersión del Puente Panameño jugó un papel de corredor para el encuentro de las faunas laurásicas y gondwánicas. Así, Centroamérica y Norteamérica fueron pobladas desde Sudamérica por elementos de Deltochilini durante dos probables grandes eventos de dispersión.
La primera oleada de dispersión pudo ocurrir durante el Mioceno (antes de la interrupción del Puente Panameño y de la formación del Altiplano), en la cual algunos linajes alcanzaron la actual Altiplanicie Mexicana. Estos linajes que participaron en el primer evento de dispersión tuvieron una notable especiación en Estados Unidos de América y en México, seguida en algunos casos por expansión secundaria, pues solo hasta el Mioceno, pudieron formarse las barreras fisiográficas para la formación de islas virtuales que propiciaron la diferenciación y el origen in situ de especies propiamente mexicanas. En algunos de estos linajes apenas es posible identificar sus afinidades sudamericanas a nivel de género.
La segunda oleada de dispersión pudo ocurrir desde el Plioceno hasta el Antropoceno (época actual) cuando se restableció el Puente Panameño, lo cual representó la conexión del continente norteamericano con Sudamérica y Centroamérica. En este segundo evento de dispersión algunos grupos no pudieron superar la elevación del Altiplano y se dispersaron dicotómicamente por las costas del Pacífico y del golfo de México. Los grupos que participaron en esta segunda oleada de distribución (que son los linajes de distribución moderna), tienen mucho más marcadas sus afinidades con el norte de Sudamérica, aunque también ha habido especiación in situ. Estos linajes constituyen el patrón de distribución Neotropical Típico, integrado luego de la consolidación del Puente Panameño con especies cercanas a las del norte de Sudamérica, ahora distribuidas en las tierras bajas tropicales de México, o algunas que representan el patrón montañoso Mesoamericano, compuesto por taxones que evolucionaron en el Núcleo Centroamericano, presentando frecuentemente expansiones hacia el norte, y cuya afinidad más importante es la antigua América del Sur (Halffter, 1964; 1974; 1976; Kohlmann & Halffter, 1990). La expansión del área de distribución de muchos de los Deltochilini sudamericanos y otros Scarabaeinae, que comparten la misma historia biogeográfica, fue facilitada ciertamente por la coexistencia con la megafauna de mamíferos que desde entonces ha desaparecido (Padilla-Gil & Halffter, 2007; Halffter & Morrone, 2017).
Es sorprendente la cantidad de especies provenientes de Centro y Sudamérica que entran a México a través de las selvas del suroeste. No son individuos ocasionales. Este patrón de dispersión de Sur a Norte, que permite explicar la historia biogeográfica de los Deltochilini, también se ha evidenciado en otros trabajos entomofaunísticos, por ejemplo, el realizado por Cancino-López et al. (2021) para estudiar la diversidad de Neuroptera del volcán Tacaná. En dicho trabajo se menciona que “existe una fuerte afinidad con los dominios del Pacífico y Mesoamérica, lo que respalda una relación evidente de la fauna de América Central y del Sur. La fauna de neurópteros del volcán Tacaná es predominantemente Neotropical con algunas especies de afinidad Neártica y otras de amplia distribución en las Américas. Probablemente, la fauna de Neuroptera es diferente en las porciones del Sur de la Zona de Transición Mexicana, debido a una disminución en el número de especies y linajes de origen norteño, y al efecto del Istmo de Tehuantepec que funciona como una barrera para la entomofauna en general”.
Aún si hemos cometido errores para determinar cuáles especies son recientes, aquí tomamos como ejemplo muchos casos (ocho con la especie indo-africana). Consideramos que, a partir del Plioceno, después del restablecimiento del Puente Panameño, la tendencia de Deltochilini de Centro y Sudamérica de invadir México, o al menos sus partes cálidas, ha sido muy intensa y varias veces superior al movimiento de origen opuesto (fauna Neártica que se dispersa hacia la región Neotropical) (Halffter, 1964; 1974; 1976; Kohlmann & Halffter, 1990). Además de los continuos movimientos a través del Puente Panameño, existe la conexión ocasional vía el puente inter-Caribe, que se comunica con la costa del Golfo de México (el caso de C. edmondsi), o bien, un equivalente ocasional, aunque una suma de ocasiones puede crear cierta certeza. Al respecto, la presencia de C. triangularis es interesante debido a que, la fecha de su captura en México (9 septiembre 1992) sigue por pocos días al paso del huracán de categoría cinco “Andrew”, fenómeno meteorológico que por sus violentos vientos podría explicar la presencia del escarabajo en territorio mexicano, considerando esto como una hipótesis (Fig. 9).
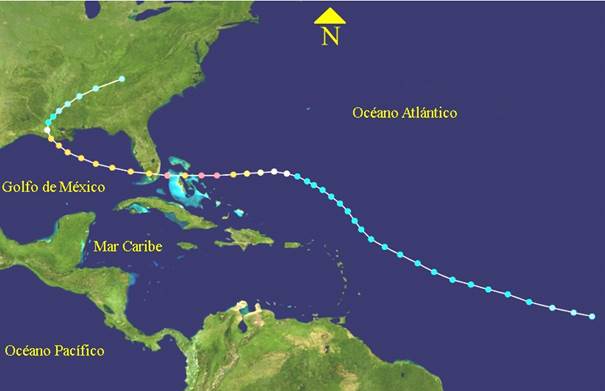
Figura 9
Trayectoria del Huracán Andrew, 16-28-agosto-1992. Tomado de: WikiProject Tropical cyclones/Tracks, tracking data from the National Hurricane Center.
Aunque las especies que se han presentado en este estudio difieren en algunos aspectos, por ejemplo, su abundancia relativa, todas ellas tienen en común que, 1) son elementos con origen en Centro y Sudamérica bien marcado, son poco numerosos y por lo general de penetración reciente, muchas veces incipiente u ocasional, 2) son en su gran mayoría, elementos de selva perennifolia o subcaducifolia, que están avanzando con la selva, y 3) su abundancia es baja, pudiéndose encontrar desde uno o dos individuos por colecta, hasta algunas decenas. Pero el número en las condiciones aquí citadas supera a las especies incipientes de penetración reciente, de cualquier otro “borde” de México.
Literatura citada
Álvarez-Bohle, M. C., Damborsky, M. P., Bar, M. E., Ocampo, F. C. (2009) Records and distribution of the Afro Asian species Digitonthophagus gazella (Coleoptera: Scarabaeidae: Scarabaeinae) in Argentina. Revista de la Sociedad Entomológica Argentina, 68, 373-376.
Arellano, L., Favila, M. E., Huerta, C. (2005) Diversity of dung and carrion beetles in a disturbed Mexican tropical montane cloud forest and on shade coffee plantations. Biodiversity and Conservation, 14, 601-615.
Arellano, L., León-Cortes, J. L., Halffter, G. (2008) Response of dung beetle assemblages to landscape structure in remnant natural and modified habitats in southern Mexico. Insect Conservation and Diversity, 1 (4), 253-262. https://doi.org/10.1111/j.1752- 4598.2008.00033.x
Basto-Estrella, G. S., Rodríguez-Vivas, R. I., Delfín-González, H., Reyes-Novelo, E. (2014) Dung beetle (Coleoptera: Scarabaeinae) diversity and seasonality in response to use of macrocyclic lactones at cattle ranches in the Mexican Neotropics. Insect Conservation and Diversity , 7 (1), 73-81. https://doi.org/10.1111/icad.12035
Brown, Jr. K. S. (1991) Conservation of Neotropical environments: insects as indicators. Pp. 350-404. En: Collins, N. M., Thomas, J. A. (Eds.). The conservation of insects and their habitats. Academic Press, London.
Cancino-López, R. J., Martins, C. C., Contreras-Ramos, A. (2021) Neuroptera diversity from Tacaná Volcano, Mexico: species composition, altitudinal and biogeographic pattern of the fauna. Diversity, 13 (11), 537. https://doi.org/10.3390/d13110537
Canhedo, V. L. (2006) Revisão taxonômica do gênero Anomiopus Westwood, 1842 (Coleoptera, Scarabaeidae, Scarabaeinae). Arquivos de Zoologia do Estado de São Paulo, 37 (4), 349-502. https://doi.org/10.11606/issn.2176-7793.v37i4p349-502
Cano, E. B. (2018) A new Anomiopus Westwood (Coleoptera: Scarabaeidae: Scarabaeinae) from the Mayan Biosphere Reserve, Petén, Guatemala. Insecta Mundi, 0659, 1-9.
Chamé-Vázquez, E. R., Gómez y Gómez, B. (2005) Primer registro de Canthon angustatus Harold, 1867 en México (Coleoptera: Scarabaeoidea). Acta Zoológica Mexicana (nueva serie), 21 (3), 159-160. https://doi.org/10.21829/azm.2005.2131981
Escobar, F., Halffter, G., Arellano, L. (2007) From forest to pasture: an evaluation of the influence of environment and biogeography on the structure of beetle (Scarabaeinae) assemblages along three altitudinal gradients in the Neotropical region. Ecography, 30 (2), 193-208. https://doi.org/10.1111/j.0906-7590.2007.04818.x
Escobar-Hernández, F., Rivera-Gasperín, S. L., Arellano, L. (2019) First record of the genus Anomiopus Westwood (Coleoptera: Scarabaeidae: Scarabaeinae) in Mexico. The Coleopterists Bulletin, 73 (4), 1105-1107. https://doi.org/10.1649/0010-065X-73.4.1105
Favila, M. E., Halffter, G. (1997) The use of indicator groups for measuring biodiversity as related to community structure and function. Acta Zoológica Mexicana (nueva serie) , (72), 1-25. https://doi.org/10.21829/azm.1997.72721734
Fincher, G. T. (1981) The potential value of dung beetles in pasture ecosystems. Journal of the Georgia Entomological Society, 16, 316-333.
Halffter, G. (1961) Monografía de las especies norteamericanas del género Canthon Hoffsg. (Coleoptera, Scarabaeidae). Ciencia México, 20, 225-320.
Halffter, G. (1964) La entomofauna americana, ideas acerca de su origen y distribución. Folia Entomológica Mexicana, 6, 1-108.
Halffter, G. (1974) Eléments anciens de l’entomofaune neotropicale: ses implications biogéographiques. Quaestiones Entomologicae, 10, 223-262.
Halffter, G. (1976) Distribución de los insectos en la Zona de Transición Mexicana: relaciones con la entomofauna de Norteamérica. Folia Entomológica Mexicana , 35, 1-64.
Halffter, G. (2017) La zona de transición mexicana y la megadiversidad de México: del marco histórico a la riqueza actual. Dugesiana, 24 (2), 77-89. https://doi.org/10.32870/dugesiana.v24i2.6572
Halffter, G., Favila, M. E. (1993) The Scarabaeinae (Insecta: Coleoptera) an animal group for analysing, inventorying and monitoring biodiversity in tropical rainforest and modified landscapes. Biology International, (27), 15-21.
Halffter, G., Morrone, J. J. (2017) An analytical review of Halffter’s Mexican transition zone, and its relevance for evolutionary biogeography, ecology and biogeographical regionalization. Zootaxa, 4226 (1), 1-46. https://doi.org/10.11646/zootaxa.4226.1.1
Halffter, G., Pineda, E., Arellano, L., Escobar, F. (2007) Instability of copronecrophagous beetle assemblage (Coleoptera: Scarabaeinae) in a mountains tropical landscape. Environmental Entomology, 36 (6), 1397-1407. https://doi.org/10.1603/0046-225X(2007)36[1397:IOCBAC]2.0.CO;2
Halffter, V., Halffter, G. (2009) Nuevos datos sobre Canthon (Coleoptera: Scarabaeinae) de Chiapas, México. Acta Zoológica Mexicana (nueva serie) , 25 (2), 397-407. https://doi.org/10.21829/azm.2009.252646
Howden, H. F., Young, O. P. (1981) Panamanian Scarabaeinae: taxonomy, distribution, and habits (Coleoptera, Scarabaeidae). Contributions of the American Entomological Institute, 18, 1-204.
Kohlmann, B. (1994) A preliminary study of the invasion and dispersal of Digitonthophagus gazella (Fabricius, 1787) in Mexico (Coleoptera: Scarabaeidae). Acta Zoológica Mexicana (nueva serie) , (61), 35-42. https://doi.org/10.21829/azm.1994.61611666
Kohlmann, B., Halffter, G. (1990) Reconstruction of a specific example of insect invasion waves: the cladistic analysis of Canthon (Coleoptera: Scarabaeidae) and related genera in North America. Quaestiones Entomologicae , 26 (1), 1-20.
Liebherr, J. K. (1988) Zoogeography of Caribbean insects. Cornell University Press, London, 285 pp.
Lobo, J. M., Martín-Piera, F., Veiga, C. M. (1988) Las trampas pitfall con cebo, sus posibilidades en el estudio de las comunidades coprófagas de Scarabaeoidea (Col.). I. Características determinantes de su capacidad de captura. Revue d'Écologie et de Biologie du Sol, 25, 77-100.
Medina, C. A., Lopera-Toro, A., Vítolo, A., Gill, B. (2001) Escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) de Colombia. Biota Colombiana, 2 (2), 131-144.
Miranda, C. H. B., Nascimento, Y. A., Bianchin, A. (1990) Desenvolvimento de um programa entregado de controle dos nematódeos e a mosca-dos-chifres na região dos cerrados. Fase 3. Potencial de Onthophagus gazella no enterrio de fezes bovinas. EMBRAPA-Gado de Corte, Pesquisa em Andamento, 42, 1-5.
Moctezuma, V. (2021) Spatial autocorrelation in a Mexican dung beetle ensemble: implications for biodiversity assessment and monitoring. Ecological Indicators, 125, 107548. https://doi.org/10.1016/j.ecolind.2021.107548
Montes de Oca, E., Halffter, G. (1998) Invasion of Mexico by two dung beetles previously introduced into the United States. Studies in Neotropical Fauna Environment, 33 (1), 37-45. https://doi.org/10.1076/snfe.33.1.37.2174
Montes de Oca, E., Anduaga, S., Rivera, E. (1994) Presence of the exotic dung beetle Euoniticellus intermedius (Reiche) in northern Mexico. The Coleopterists Bulletin , 48 (3), 244.
Morón, M. A. (2006) Patrones de distribución de la familia Scarabaeidae (Coleoptera). Pp. 271-293. En: Morrone, J. J., Llorente-Bousquets, J. (Eds.). Componentes bióticos principales de la entomofauna mexicana. Facultad de Ciencias, UNAM, México.
Morón, M. A. (2014) Los escarabajos lamelicornios como indicadores ecológicos y biogeográficos. Pp. 309-326. En: González-Zuarth, C. A., Vallarino, A., Pérez-Jiménez, J. C., Low-Pfeng, A. M. (Eds.). Bioindicadores: guardianes de nuestro futuro ambiental. El Colegio de la Frontera Sur (ECOSUR) e Instituto Nacional de Ecología y Cambio Climático (INECC), México.
Morón, M. A., Deloya, C., Delgado-Castillo, L. (1988) Fauna de coleópteros Melolonthidae, Scarabaeidae y Trogidae de la Región de Chamela, Jalisco, México. Folia Entomológica Mexicana , (77), 313-378.
Morón, M. A., Deloya, C., Ramírez, C. A., Hernández-Rodríguez, S. (1998) Fauna de Coleóptera Lamellicornia de la región de Tepic Nayarit, México. Acta Zoológica Mexicana (nueva serie) , (75), 73-116. https://doi.org/10.21829/azm.1998.75751708
Morrone, J. J. (2009) Evolutionary biogeography. An integrative approach with case studies. Columbia University Press, New York, 301 pp.
Navarrete, D., Halffter, G. (2008a) Nuevos registros de escarabajos copro-necrófagos (Coleoptera: Scarabaeidae) para México y Chiapas. Acta Zoológica Mexicana (nueva serie) , 24 (1), 247-250. https://doi.org/10.21829/azm.2008.241637
Navarrete, D., Halffter, G. (2008b) Dung beetle (Coleoptera: Scarabaeidae: Scarabaeinae) diversity in continuous forest, forest fragments and cattle pastures in a landscape of Chiapas, Mexico: the effects of anthropogenic changes. Biodiversity and Conservation , 17, 2869-2898. https://doi.org/10.1007/s10531-008-9402-8
Noriega, J. A. (2002) First report of the presence of the genus Digitonthophagus (Coleoptera: Scarabaeidae) in Colombia. Caldasia, 24 (1), 213-215.
Pablo-Cea, J. D., Velado-Cano, M. A., Fuentes, R., Cruz, M., Noriega, J. A. (2017) First report of Digitonthophagus gazella (Fabricius, 1787) and new records for Euoniticellus intermedius (Reiche, 1849) (Coleoptera: Scarabaeidae Latreille, 1802) in El Salvador. Acta Zoológica Mexicana (nueva serie) , 33 (3), 527-531. https://doi.org/10.21829/azm.2017.3331154
Padilla-Gil, D. N., Halffter, G. (2007) Biogeography of the areas and Canthonini (Coleoptera: Scarabaeidae) of dry tropical forests in Mesoamerica and Colombia. Acta Zoológica Mexicana (nueva serie) , 23 (1), 73-108. https://doi.org/10.21829/azm.2007.231559
Rivera-Cervantes, L. E., Halffter, G. (1999) Monografía de las especies mexicanas de Canthon del subgénero Glaphyrocanthon (Coleoptera: Scarabaeidae: Scarabaeinae). Acta Zoológica Mexicana (nueva serie) , (77), 23-150. https://doi.org/10.21829/azm.1999.77771693
Sánchez-Hernández, G., Gómez, B., Delgado, L., Rodríguez-López, M. E., Chamé-Vázquez, E. R. (2018) Diversidad de escarabajos copronecrófagos (Coleoptera: Scarabaeidae: Scarabaeinae) en la Reserva de la Biosfera Selva El Ocote, Chiapas, México. Caldasia , 40 (1), 144-160. https://doi.org/10.15446/caldasia.v40n1.68602
Sánchez-Huerta, J. L., Moctezuma, V., Halffter, G. (2019) Nuevo registro de distribución de Canthon angustatus Harold en Veracruz, México. Southwestern Entomologist, 44 (1), 353-355. https://doi.org/10.3958/059.044.0143
Schuster, J. C., Cano, E. B., Cardona, C. (2000) Un método sencillo para priorizar la conservación de los bosques nubosos de Guatemala usando Passalidae (Coleoptera) como organismos indicadores. Acta Zoológica Mexicana (nueva serie) , (80), 197-209. https://doi.org/10.21829/azm.2000.80801900
Solís, A., Kohlmann, B. (2002) El género Canthon (Coleoptera: Scarabaeidae) en Costa Rica. Giornale Italiano di Entomologia, 10 (50), 1-68.
Tarasov, S., Dimitrov, D. (2016) Multigene phylogenetic analysis redefines dung beetles relationships and classification (Coleoptera: Scarabaeidae: Scarabaeinae). BMC Evolutionary Biology, 16 (1), 257. https://doi.org/10.1186/s12862-016-0822-x
Tarasov, S., Génier, F. (2015) Innovative Bayesian and parsimony phylogeny of dung beetles (Coleoptera, Scarabaeidae, Scarabaeinae) enhanced by ontology-based partitioning of morphological characters. PLoS ONE, 10, e0116671. https://doi.org/10.1371/journal.pone.0116671
Verdú, J. R., Moreno, C. E., Sánchez-Rojas, G., Numa, C., Galante, E., Halffter, G. (2007) Grazing promotes dung beetle diversity in the xeric landscape of a Mexican Biosphere Reserve. Biological Conservation, 140 (3-4), 308-317. https://doi.org/10.1016/j.biocon.2007.08.015
Notas de autor
*Autor corresponsal: Sara Lariza Rivera-Gasperín. zaralariza@gmail.com
