Artículos originales
Bioprospección de receptores de insulina a partir de ARN mensajero en Brevicoryne brassicae L. (Hemiptera: Aphididae)
Bioprospecting of insulin receptors from messenger RNA in Brevicoryne brassicae L. (Hemiptera: Aphididae)
Bioprospección de receptores de insulina a partir de ARN mensajero en Brevicoryne brassicae L. (Hemiptera: Aphididae)
Acta zoológica mexicana, vol. 38, e3812513, 2022
Instituto de Ecología A.C.
Recepción: 24 Marzo 2022
Aprobación: 28 Junio 2022
Publicación: 25 Julio 2022
Financiamiento
Fuente: CONACyT
Nº de contrato: 1000540
Resumen: La supresión de moléculas de ácido ribonucleico mensajero (ARNm) mediante ARN interferente (ARNi) se ha propuesto como método de control de insectos plagas. El ARNi impide el desarrollo morfológico y funcional de los insectos y se considera altamente específico. En este estudio se buscaron receptores de insulina (InR) en Brevicoryne brassicae L. (Hemiptera: Aphididae) a partir del ARNm de pulgones, como primer paso para el diseño posterior de ARNi dirigido a la supresión de InR. A partir del ácido desoxirribonucleico complementario (ADNc) y mediante PCR anidada, se amplificó la región correspondiente a InR con dos pares de cebadores diseñados para Nilaparvata lugens (Homoptera: Delphacidae). No se logró identificar InR, en su lugar se predice la presencia de la proteína receptora Dip2A de unión a folistatina (FS) debido a que comparten regiones proteicas similares con los InR, involucradas en la traducción de señales en los insectos. Se sugiere continuar con la búsqueda de InR específicos para el pulgón, así como posibles cebadores para regiones de Dip2A, para lograr un ARNi altamente específico.
Palabras clave: Pulgón de la col, ARNi, Brassica, plaga, áfidos, insulina.
Abstract: Suppression of messenger ribonucleic acid (mRNA) molecules by RNA interference (RNAi) has been proposed as a method for controlling insect pests. RNAi impedes the morphological and functional development of insects and is considered highly specific. In this study, insulin receptors (InR) were searched for in Brevicoryne brassicae L. (Hemiptera: Aphididae) from aphid mRNA, as a first step for further design of RNAi targeting InR suppression. From complementary deoxyribonucleic acid (cDNA) and by means of nested PCR, the region corresponding to InR was amplified with two pairs of primers designed for Nilapavata lugens (Homoptera: Delphacidae). InRs could not be identified. However, the presence of the follistatin-binding receptor protein Dip2A (FS) was predicted from the regions of similarity with the InRs that are involved in signal translation in insects. We recommend continuing the search for aphid specific InRs, as well as possible primers for Dip2A regions, to identify a highly specific RNAi.
Key words: Cabbage aphid, RNAi, Brassica, pest, aphids, insulin.
Introducción
El método de control poblacional de insectos con ácido ribonucleico interferente (ARNi), consiste en sintetizar ARN de doble cadena (ARNds) e introducirlo en la célula para suprimir ARN mensajero (ARNm) (Christiaens et al., 2020). La técnica del ARNi se basa en el mecanismo de respuesta inmune de células eucariotas, que se desencadena ante la presencia de material genético exógeno (ARN o ADN) de patógenos (Nandety et al., 2015; Cooper et al., 2019). El ARNds sintetizado e incorporado en el citoplasma de las células se fragmenta y se crean cadenas de ARN de una sola hebra que se empalman al ARNm objetivo, lo que impide su traducción a proteínas en los ribosomas (Darrington et al., 2017).
La técnica del ARNi se propone como posible método para el control de diversos insectos plagas de plantas cultivadas (Mamta & Rajam, 2017), ya que se ha demostrado que impide el crecimiento y desarrollo de especies de insectos de diferentes órdenes (Ding et al., 2017). Unas de las ventajas de la técnica del ARNi, es que es altamente específico y representa una alternativa ante los métodos de control convencionales como los insecticidas. Sin embargo, la eficacia del ARNi depende de varios factores, entre ellos el conocimiento y selección de ARNm objetivo a suprimir (Guan et al., 2018), aspecto que en la mayoría de los insectos plaga aún se tiene poco conocimiento. Un primer paso en el uso de la técnica del ARNi, es ubicar el ARNm codificante de una proteína particular involucrada en el crecimiento y desarrollo de los insectos.
Para algunas especies de insectos se tiene conocimiento de su genoma o evidencia de la presencia de genes potencialmente blancos de ARNi (Luan et al., 2013; Koo et al., 2020). Sin embargo, con frecuencia no se dispone de esta información para especies de insectos que se consideran plagas regionalmente. Este es el caso del pulgón cenizo de la col, Brevicoryne brassicae (Linnaeus, 1758) (Hemiptera: Aphididae), el cual es una plaga en la región de Los Altos de Chiapas (México) y su control hasta ahora se hace mediante el uso de insecticidas, cuyos costos económicos y sociales son significativos (Santiago-Lastra & Perales-Rivera, 2007). Aunque hay estudios genéticos con poblaciones de esta especie en la región (Leal-Aguilar et al., 2008; Ruíz-Montoya & Núñez-Farfán, 2013), hasta ahora no se han investigado métodos de control alternativos como el uso de ARNi, en parte por la falta de conocimiento del genoma o de la presencia de ARNm codificante de una proteína estructural fundamental. El ensayo de cebadores inespecíficos puede ser una alternativa cuando se carece de la información de genes potencialmente blancos de ARNi en la especie de interés.
En este estudio se optó por ensayar con proteínas receptoras de insulina (InR) para desarrollar la técnica del ARNi en B. brassicae. Estas proteínas son estructurales (Nässel & Broeck, 2016) y se encuentran en diversas especies de insectos incluyendo los pulgones (Shan-Shan et al., 2016), participan en procesos fisiológicos como el crecimiento, el desarrollo y la fecundidad (Liu et al., 2020). Las receptores de insulina producen señales de traducción, que reclutan y fosforilizan a dos principales proteínas adaptadoras: IRS (sustrato receptor de la insulina) (Olivares & Arellano, 2008) y Shc (proteína con dominio fosfotirosina) (Ding et al., 2017), encargadas de organizar complejos moleculares que liberan diferentes vías de señalización como la PI3K/Akt (fosfatidilinositol 3-quinasa) para regular el ciclo celular y diversos eventos metabólicos (Nässel & Broeck, 2016). Otra ruta es MAPK (proteínas quinasas activadas por mitógenos), que regulan la transcripción y expresión de proteínas en las células (Ding et al., 2017). Estudios recientes han mostrado que en Apis mellifera (Linnaeus, 1758) (Hymenoptera: Apidae), Nilaparvata lugens (Stål, 1854) (Hemiptera: Delphacidae) y Acyrthosiphon pisum (Harris, 1776) (Hemiptera: Aphididae), presentan dos tipos de InR, que son producidas por dos genes distintos InR1 e InR2 (Azevedo & Hartfelder, 2008; Shan-Shan et al., 2016; Zhao et al., 2019). En contraste, en insectos del orden Diptera como Drosophila melanogaster (Meigen, 1830) y Aedes aegypti (Meigen, 1818), se ha identificado un solo gen InR1 (Garofalo, 2002; Ding et al., 2017). Es posible que los receptores de insulina se encuentren en todas las especies de insectos y que presenten diferencias que permitan una alta especificidad del ARNi.
La supresión de InR con la técnica de ARNi, experimentada en los insectos Toxoptera citricida (Kirkaldy, 1907) y Nilaparvata lugens (Stål, 1854), impide la transición de un estadio ninfal a otro (Ding et al., 2017) y un desarrollo normal de las alas (Xu et al., 2015). Por lo que la presencia de receptores de insulina es crucial para el crecimiento, desarrollo y supervivencia de los insectos (Nässel & Broeck, 2016). Por lo tanto, los InR pueden ser blancos ideales para llevar a cabo la técnica del RNAi en insectos plagas (Joga et al., 2016), en los que los estudios genómicos son insuficientes. En este estudio se reporta la bioprospección de InR en Brevicoryne brassicae o pulgón cenizo de la col, con el uso de cebadores inespecíficos diseñados para insectos del mismo orden: Nilaparvata lugens y Toxoptera citricida.
El pulgón cenizo de la col, B. brassicae, es considerado plaga del cultivo de crucíferas (Cruciferae), y se distribuye en prácticamente todas las regiones templadas del mundo (Blackman & Eastop, 2000; Ruíz et al., 2013). En México el cultivo de crucíferas es básico en zonas de alta marginación, forman parte de la dieta básica de los productores y les permite generar ingresos económicos. Brevicoryne brassicae ha sido objeto de diversos estudios para entender su adaptación local a las plantas hospederas y la plasticidad fenotípica como limitante de la adaptación (Núñez-Farfán et al., 2003; Ruíz-Montoya & Núñez-Farfán, 2013), no obstante, no se han desarrollado estudios para ofrecer estrategias nuevas de control menos nocivos que los insecticidas. Con la finalidad de aportar conocimiento para generar medios de control alternativos, el presente trabajo se llevó a cabo con los objetivos de: (1) identificar ARNm que codifique proteínas de InR en B. brassicae con cebadores inespecíficos, (2) reconocer regiones y dominios de InR de B. brassicae con herramientas bioinformáticas, y (3) comparar entre secuencias de InR reportadas para especies de insectos y la obtenida para B. brassicae, para valorar similitud o especificidad. Los resultados permitirán identificar en B. brassicae regiones de InR potencialmente útiles para el diseño de cebadores altamente específicos para la implementación de la técnica del ARNi, como posible método de control del pulgón, una alternativa más amigable con el medio ambiente, la salud de los productores y de quienes consumen el cultivo.
Materiales y métodos
Obtención de especímenes de B. brassicae. Los ejemplares ápteros (sin alas) de B. brassicae utilizados para la generación de las colonias fueron colectados en plantas de col cultivadas en campo abierto del municipio de San Cristóbal de Las Casas, Chiapas, México, e identificados inicialmente por caracteres morfológicos mediante claves taxonómicas (Blackman & Eastop 2000).
Se cultivaron 10 plantas de Brassica oleracea var. capitata (col o repollo) hasta la etapa de pre-floración para el desarrollo del pulgón (ver información suplementaria; Fig. S1). Las plantas fueron colocadas dentro de cámaras de estructura metálica cubiertas con tela organza de maya fina, rígida y transparente (100 % poliamida; ver información suplementaria; Fig. S2), para evitar el ingreso de otros insectos como parasitoides, depredadores u otras especies de pulgones, sin fertilizar y regadas en días alternos en invernadero, con temperatura y humedad relativa ambientales: Temperatura media anual, 17.25 oC; precipitación anual 700 mm y fotoperiodo de 13 ± 4 °C y 12 h de luz. Por cada planta cultivada se colocó un pulgón áptero (madre) (información suplementaria; Fig. S1 a y b). Una vez que el pulgón depositó al menos una ninfa, la madre se retiró y se permitió el libre desarrollo de la ninfa por 30 días hasta obtener varios individuos mediante reproducción asexual (partenogénesis).
Extracción de ARN total y síntesis de ADN complementario. En un tubo de microcentrífuga de 1.5 ml se colocaron 30 individuos entre adultos y ninfas de una clona de 13 generaciones para la extracción de ARN total. El ARN total se extrajo mediante el uso de TRIZOL™ Plus RNA Purification Kit (Invitrogen, Carlsbad, CA, EUA) de acuerdo con las instrucciones del fabricante. El ARN se cuantificó mediante Nanodrop ND-2000 (Thermo scientific, Wilmington, DE, EUA), a 260 nm de absorbancia. La pureza de ARN se evaluó a partir de la relación de absorbancia a OD260/280 y OD260/230. Luego se verificó la integridad del ARN mediante electroforesis en gel de agarosa (NORGEN) al 1 %.
El ácido desoxirribonucleico complementario (ADNc) de una sola hebra se sintetizó a partir de 7 µl de ARN total libre de ADN a una concentración de 500 ng/µl, usando PrimeScript 1st strand cDNA Synthesis Kit (Takara Bio) de acuerdo con las instrucciones del fabricante. El volumen de reacción fue 10 µl compuesto de 7 µl de ARN, 0.5 µl de PrimeScript RT Enzyme Mix I, 0.5 µl de Oligos dT, 0.5 µl (200 pmol) Random 6 mers, 1 µl de 5X PrimeScript Buffer y 0.5 µl de agua libre de RNAsas. La reacción de PCR por transcripción inversa (RT-PCR) se realizó en un termociclador BIO-RAD T100TM. La temperatura de incubación de la reacción en un primer paso fue de 37 °C por 15 minutos, 85 °C por 5 segundos y se dejó incubar por 20 minutos a 4 °C. El ADNc obtenido se confirmó mediante PCR con el par de cebadores (COIBF y COIBR) correspondientes al gen mitocondrial (ADNmt) Citocromo Oxidasa I (COI o gen coxI) (Hebert et al., 2004) como control positivo (Cuadro 1). Esta reacción de PCR consistió en 20 µl de volumen de reacción que contenía: 6 µl de Master Mix 10x PCR (Thermo Scientific), 5 µl de ADNc, 2 µl de cada cebador y 5 µl de agua libre de nucleasas. Las condiciones de reacción fue la siguiente: 1 minuto a 94 °C, 45 segundos a 94 °C, 45 segundos a 52 °C, 1 minuto a 72 °C, y 72 °C por 6 minutos, posteriormente se verificó la integridad de los productos de PCR mediante electroforesis y gel de agarosa al 2 % (NORGEN). El ADNc se almacenó a < 80 °C para análisis posteriores.

Amplificación de InR y purificación de productos de PCR. Mediante PCR se amplificaron regiones de posibles proteínas receptoras de insulina (InR) en B. brassicae, usando ADNc como molde con dos pares de cebadores (NIInR1F NIInR1R y NIInR2F, NIInR2R) reportados por Lin et al. (2018) y diseñados para Nilaparvata lugens, y dos pares reportados para Toxoptera citricidus (InR1-F, InR1-R y InR2-F, InR2-R) (Ding et al., 2017). El volumen final de reacción de PCR fue de 15 µl, conteniendo: 6 µl de Master Mix 10x PCR (Thermo Scientific), 4 µl de ADNc, 1 µl de cada cebador y 3 µl de agua libre de nucleasas. Las condiciones de reacción fueron las siguiente: 3 minutos a 95 °C, 30 segundos a 95 °C, 30 segundos a 55.4 °C, 2 minutos a 72 °C y 72 °C por 5 minutos, posteriormente se verificó el fragmento correspondiente a los productos de PCR mediante electroforesis y gel de agarosa al 2 %. Los cebadores utilizados se muestran en la Cuadro 1, e incluye el tamaño esperado del producto y eficiencia de amplificación.
Para incrementar la concentración de producto amplificado se realizó una PCR semianidada con un volumen de reacción de 15 µl por cada muestra, se usaron las mismas cantidades de la primera reacción y el producto de la primera PCR se utilizó como ADN molde. Los productos amplificados de la segunda PCR se purificaron en gel de agarosa con Zymoclean TM Gel DNA Recovery Kit de acuerdo con instrucciones del fabricante, se diluyó en 30 µl de agua grado molecular y se cuantificó la concentración de material genético recuperado mediante el uso de NanoDrop 2000 Thermo Scientific™ a 260/280 nm de absorbancia. De cada muestra recuperada, incluyendo el control positivo (gen coxI o COI), se prepararon diluciones de 20 µl a una concentración promedio de 20 ng/µl para la secuenciación de ADN mediante el método de Sanger en Macrogen (Seúl, Corea del Sur). En total se mandaron 21 muestras procedentes de un lote de 30 individuos (nueve muestras correspondientes al par de cebadores NIInR1F, nueve muestras del par NIInR2F-NIInR2R y tres muestras de producto amplificado del control positivo).
Identificación molecular de amplicones de PCR. Se utilizó el Software BioEdit (Hall, 2011) para la alineación de secuencias amplificadas (secuencias problema) en B. brassicae y eliminar los extremos para evitar regiones de baja calidad (baja señal o indefinición de nucleótidos). Previo al alineamiento, las secuencias antisentido se sometieron a la interfaz del Software Reverse Complement para convertirlas a su complemento inverso (disponible en: https://www.bioinformatics.org/sms/index.html) y se confirmó manualmente. Para determinar el grado de identidad de los productos amplificados con las secuencias de InR ya reportadas en la base de datos del GenBank, se realizó nuevamente un alineamiento de todas las secuencias problemas (sentido y complemento inverso) en MEGA opción MUSCLE (Edgar, 2004), luego se sometieron a la herramienta Nucleotide BLAST (Basic Local Alignment Search Tool) de la base de datos del NCBI (National Center for Biotechnology Information) mediante la opción de búsqueda no redundante (disponible en: https://blast.ncbi.nlm.nih.gov/Blast.cgi). Posteriormente, todas las secuencias sentido amplificadas con cebadores de InR se analizaron con el software Expasy (Duvaud et al., 2021) con la ayuda de la herramienta Translate (disponible en: https://web.expasy.org/translate/), para la traducción de secuencias de nucleótidos a proteínas de acuerdo con los marcos de lecturas de cada una de las secuencias. Las secuencias deducidas de proteínas se analizaron con la herramienta BLASTp para comparar secuencias de aminoácidos contra una base de proteínas, y PSI-BLAST para la búsqueda de proteínas de homólogos lejanos (Altschul et al., 1997). Las secuencias problemas previamente traducidas a proteínas se colocaron dentro de la interfaz gráfica del software PSORTII y WoLF PSORT (programa informático para la predicción de sitios de localización de proteínas en las células) para identificar el sitio predictivo de anclaje de las proteínas en las células (Horton et al., 2007) (disponible en: https://psort.hgc.jp/).
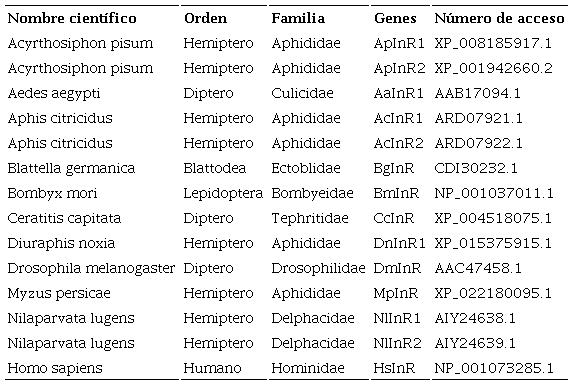
Regiones y dominios en InR in silico. En la base de datos del NCBI se buscaron secuencias de proteínas de InR de diferentes especies de insectos, sin información disponible para B. brassicae (Cuadro 2). Se incluyó una secuencia de InR de Homo sapiens similar a la de los insectos, por ser un organismo en el que la función y estructura de InR ha sido ampliamente estudiada, y eventualmente ese conocimiento puede ser de ayuda para comprender las rutas metabólicas del InR en insectos. La identificación de dominios se realizó en el Software SMART-EMBL (disponible en: http://smart.embl-heidelberg.de/help/smart_about.shtml), y se recuperó la secuencia del dominio presente en todas las secuencias de insectos y en la de H. sapiens, este dominio corresponde a la tirosina quinasa (TyrKc). El alineamiento se realizó usando el programa BioEdit (Hall, 2011) opción alineamiento múltiple de secuencias bajo el método Neighbor-Joining (Saitou & Nei, 1987), y se corroboró con el Software MEGA versión 7.0.26 opción MUSCLE (Edgar, 2004). El árbol filogenético se realizó con el programa MEGA bajo el método de máxima verosimilitud (ML, del inglés maximum likelihood) basado en el modelo Jones, Taylor y Thornton (JTT), y un bootstrap de 1,000 réplicas. Es importante hacer notar que las secuencias de B. brassicae obtenidas se excluyeron de este análisis debido a que no correspondieron a secuencias de InR reportadas para otros insectos
Resultados
Integridad de ARN total y obtención de ADNc. El ARN total se obtuvo de manera eficaz mediante el método de Trizol (Fig. 1). Se observaron dos bandas que probablemente corresponden a ARN de las subunidades 28S y 18S. Se obtuvo ADNc de buena calidad que permitió la amplificación exitosa del amplicón correspondiente a COI (Fig. 2).
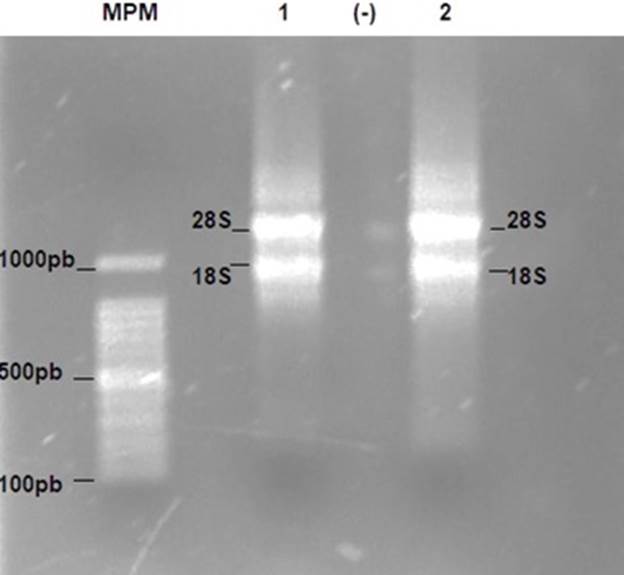
Figura 1
Integridad del ARN total de Brevicoryne brassicae visualizado en gel de agarosa al 1 % (tinción bromuro de etidio). MPM = marcador de peso molecular 100-1,000 pb (1kb Ladder Promega), carril 1 y 2 corresponde a = muestra de ARN, carril (-) = control negativo sin ARN. 28S = Subunidad mayor ribosomal, 18S = subunidad menor ribosomal.
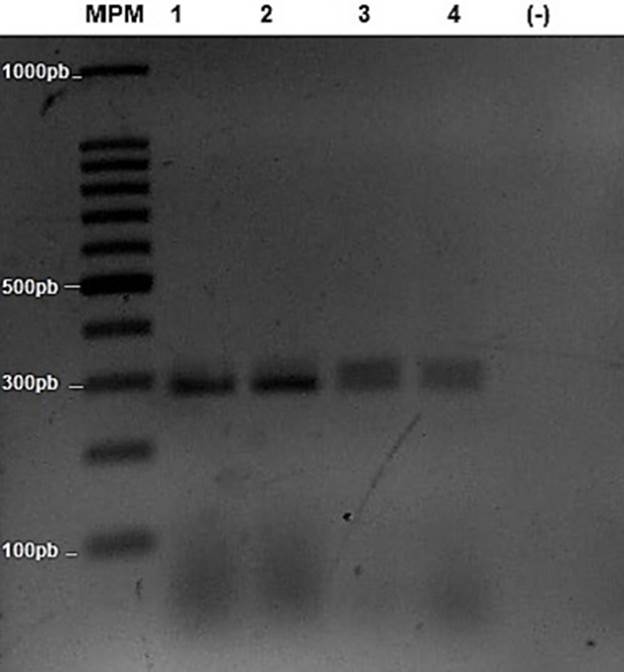
Figura 2
Amplificación del fragmento correspondiente a citocromo oxidasa subunidad I (COI) en Brevicoryne brassicae. Fragmento de 300 pb visualizado en gel de agarosa al 2 % y teñido con bromuro de etidio. MPM = marcador peso molecular de 100-1,000 pb (1Kb Ladder Promega), carriles 1, 2, 3, 4 = producto de amplificación correspondiente a COI, carril (-) corresponde al = control negativo sin ADNc.
Amplificación de InR. Los cebadores de InR de T. citricida no amplificaron ninguna región en el ADNc del pulgón. Los cebadores de N. lugens rindieron producto durante la PCR. En la primera reacción de PCR sólo se logró producto con el par de cebadores NIInR2F y NIInR2R. Sin embargo, la activad fue tenue y poco definida, con un tamaño inferior al reportado. En la segunda reacción de PCR (PCR semianidada) se obtuvo producto con los dos pares de cebadores. Para el par NIInR1F y NIInR1R, fueron bandas bien definidas y con un tamaño similar al reportado. Con los cebadores NIInR2F y NIInR2R se obtuvo el mismo resultado que en la primera PCR (Fig. 3). La secuencia de ADN obtenida a partir de estos fragmentos fue analizada por las herramientas bioinformáticas previamente mencionadas.
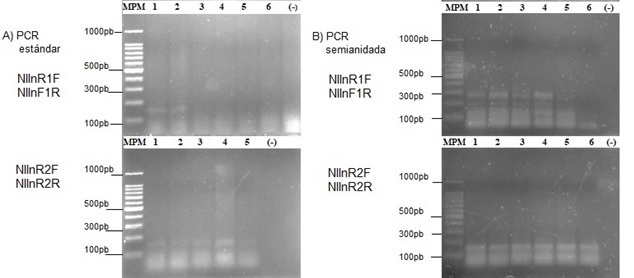
Figura 3
Amplificación de InR en Brevicoryne brassicae. A) PCR estándar: MPM = marcador de peso molecular 100-1,000pb (1kb Ladder Promega), los carriles 1, 2, 3, 4, 5, 6 corresponden a = muestras de producto de amplificación usando los oligonucleótidos NlInR1F-NIInF1R y NIInR2F-NIInR2R, carril (-) muestra el = control negativo sin ADNc. B) PCR semianidada.
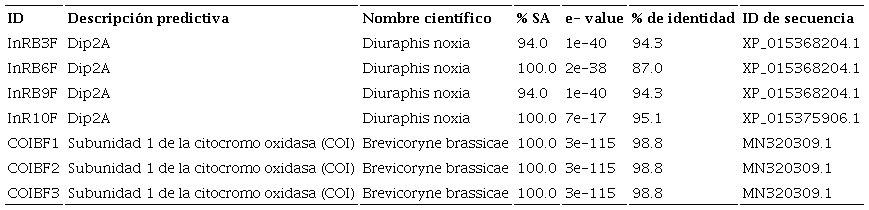
Identificación in silico de InR en Brevicoryne brassicae. Únicamente cuatro muestras (InRB3F, InRB6F, InRB9F e InRB10F), amplificadas con el par de cebadores NIInR1F y NIInR1R y tres muestras (COIB1F, COIB2F y COIB3F) con cebadores de gen coxI (cebadores COIBF y COIBR), tuvieron una secuencia susceptible de analizar, el resto tenían baja señal de lectura. El tamaño final de todas las secuencias, una vez editadas, fue de 200 pares de bases (pb) y se analizaron solo secuencias con sentido forward (Cuadro S1). El análisis BLASTp identificó tres secuencias correspondientes a proteínas de tipo 2 con interacción al disco homólogo A (Dip2A) con porcentajes altos de identidad con función receptora a folistatina (FSTL1) (Cuadro 3), y en la cuarta muestra una posible proteína asociada con la proliferación inducida por señales con dominio PDZ que, debido al tamaño de la secuencia amplificada, no predijo una proteína en específico. El control positivo presentó 98.8 % de identidad con el gen citocromo oxidasa subunidad 1 (Cuadro 3). Ambas proteínas, Dip2A y PDZ, están presentes en membrana con función de señalización intracelular. El análisis PSI-BLAST identificó las mismas proteínas que BLASTp. Los Software PSORTII y WoLF PSORT predijeron que las secuencias correspondientes a proteínas Dip2A tuvieron 66.7 % de anclaje en regiones extracelulares y en pared celular (Cuadro 4).

Análisis filogenético de InR. Se recuperaron 14 secuencias de InR para 10 especies de insectos de cuatro órdenes y siete familias, y una secuencia correspondiente a H. sapiens (Cuadro 2), ya que en humanos se han estudiado ampliamente los receptores de insulina. Con el programa SMART se predijo la estructura de proteínas receptoras de insulina en las 14 secuencias recuperadas en el GenBank (Fig. 4). No se obtuvo ningún resultado con la secuencia obtenidas de B. brassicae. En la mayoría de las secuencias correspondiente a insectos se observó una región furina, tres dominios a fibronectina tipo III, una región helicoidal transmembrana y un dominio catalítico del tipo tirosina quinasa (TyrKc) (Fig. 4). El alineamiento con los programas BioEdit y MEGA mostró que el dominio TyrKc es el mejor conservado en todas las especies analizadas. El análisis de agrupación con base en el dominio TyrKc se realizó descartando la secuencia de B. brassicae por carecer de estructura. La agrupación mostró el porcentaje de cambios genéticos que van de 0.0 a 0.39 %. Los cambios genéticos menores correspondieron a grupos de especies que pertenecen a una misma familia (pulgones, por ejemplo). Los grupos tuvieron un soporte > 50 % con base en bootstrap (Fig. 5).

Figura 4
Estructura arquitectónica predictiva de la proteína receptora de insulina para especies de insectos (ver Cuadro 1), compuesta de ~1400 aminoácidos. FU = Región furina, FN3 = Dominio fibronectina tipo III, RT = Región helicoidal transmembrana, TyrKc = Dominio catalítico del tipo tirosina quinasa.
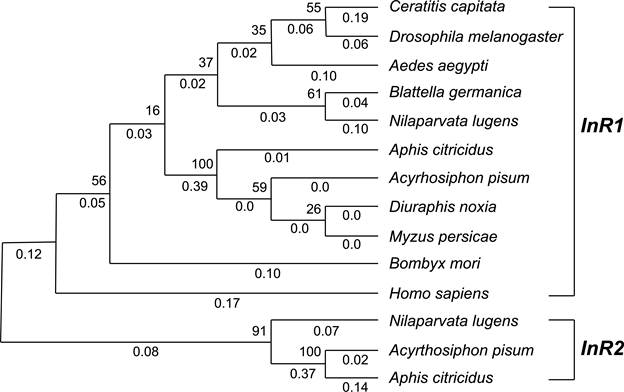
Figura 5
Agrupación de especies de insectos y Homo sapiens con base en la región tirosina quinasa de receptores de insulina. InR1 = Gen receptor de insulina de tipo 1, InR2 = Gen receptor de insulina del tipo 2, por el método de Neighbor-Joining. Los valores enteros corresponden a porcentaje de robustes con base en Bootstrap (1,000 repeticiones). Los valores decimales corresponden a cambios genéticos calculados con el método de máxima verosimilitud (ML, del inglés maximum likelihood) y el modelo evolutivo Jones, Taylor y Thornton (JTT).
Discusión
Fue posible la obtención de ARN total, así como su traducción a moléculas de ADNc. Se observaron claramente los ARN ribosomales correspondientes a 28S y 18S de células eucariotas (Dinkova & Sánchez de Jiménez, 2010). Estas son subunidades con altas concentraciones de ARN mensajeros (ARNm) y con posibles plegamientos terciarias como las proteínas (Yusupova et al., 2001; Noller, 2005). La clara presencia del ARN de las subunidades, además de la ausencia de bandas de mayor tamaño en el gel de electroforesis, sugieren que no hubo contaminación con ADN y ni enzimas degradadoras de ARN (RNAsas) que pudieran degradar el ARN durante y posterior a su extracción (Hernández et al., 1994).
La amplificación de COI a partir de ADNc indicó una buena integridad de la síntesis por transcriptasa inversa. El tamaño de la región COI amplificado en el ADNc de B. brassicae fue de alrededor de 200 pares de bases (pb), el cual está dentro del intervalo esperado (Hebert et al., 2004). El análisis de similitud de secuencias de ADN obtenida mostró 100 % de identidad con secuencias del gen coxI reportado en la base de datos de GeneBank para B. brassicae. Por lo que el ADNc pudo ser utilizado como molde para amplificar receptores de insulina en B. brassicae usando cebadores inespecíficos.
La búsqueda de receptores de insulina (InR) en ARNm de B. brassicae con cebadores inespecíficos, diseñados para otras especies, no permitió la amplificación de fragmentos correspondientes a InR. Sin embargo, se logró la identificación de regiones presentes en otras proteínas receptoras de membrana como Dip2A y PDZ, debido muy probablemente a la inespecificidad de los cebadores con respecto al ADN del pulgón (Restrepo et al., 2012).
La primera reacción de PCR para la obtención del InR de B. brassicae produjo poco producto lo que impidió la visualización del mismo en geles de agarosa 2 %, resultado similar al de Artemia (Han et al., 2018). Con la PCR semianidada, con el par de cebadores inespecíficos NIInR1F y NIInR1R se logró visualizar bandas definidas y con tamaños similares a lo reportado para InR en N. lugens (Lin et al., 2018). Por otra parte, la falta de producto con los cebadores InR1-F, InR1-R, InR2-F, InR2-R, NIInR2F y NIInR2R, probablemente se debió a la alta variación nucleotídica presente en el ADNc del pulgón respecto a los cebadores (Hernández et al., 1994).
as secuencias identificadas como proteína Dip2A y la correspondiente a un posible dominio PDZ exclusivo de proteínas transmembrana (Ponting, 1997), se han reportado en especies cercanas a B. brassicae como Myzus persicae (Hemiptera: Aphididae) Sulzer, 1776 (XM_022326326.1), Diuraphis noxia (Hemiptera: Aphididae) Kurdjumov, 1913 (XM_015512719.1) y Acyrthosiphon pisum (Hemiptera: Aphididae) Harris, 1776, XM_008191702.3), todos considerados insectos plagas de importancia agrícola con alta presencia en cultivos del género Brassica (Santiago-Lastra & Perales-Rivera, 2007), cereales (Nicholson et al., 2015) y cultivos de la familia Fabaceae (Sandhi & Reddy, 2020).
En este estudio no se logró evidenciar la presencia de proteínas receptoras de insulina en el pulgón cenizo de la col. Consideramos que esto puede deberse a que se utilizaron cebadores inespecíficos. Sin embargo, encontramos secuencias que sugieren la presencia de proteínas receptoras a folistatina (FSTL1), conocidas como Dip2A, que comparte con InR las mismas rutas de señalización en cuanto a la inducción de la proliferación y diferenciación celular (Ouchi et al., 2010; Tanaka et al., 2010). Por otra parte, se ha demostrado que tanto los InR y Dip2A presentan dominios del tipo tirosina quinasa (TyrKc), que son activadas por la vía de las P13K/Akt (fosfatidilinositol 3-quinasa) y participan en el trasporte de glucosa y otros eventos metabólicos (Ouchi et al., 2010; Vázquez-Jiménez et al., 2017). En específico, la proteína Dip2A actúa como receptora de folistatina (FSTL1) en la membrana celular, y pertenece a la superfamilia de factores de crecimiento transformante beta (TGF-β) (Ouchi et al., 2010), la cual está involucrada en varios procesos biológicos como la proliferación, diferenciación y muerte celular en diversos insectos (Tanaka et al., 2010; Ishimaru et al., 2016). Mientras que los InR son activados por hormonas de insulina en la membrana celular, y son los encargados de organizar complejos moleculares para desencadenar cascadas de señalización intracelular que participan en la síntesis de lípidos, proteínas, proliferación y diferenciación celular (Jensen & Meyts, 2009; Nässel & Broeck, 2016).
Actualmente hay trabajos que evidencian la presencia de múltiples InR en diversos ordenes de insectos que responden a la presencia de la hormona de la insulina o a hormonas similares a ésta (Smykal et al., 2020). En este estudio se identificó de forma in silico la presencia de InR producto de dos genes en 10 especies de insectos, con variaciones entre sus secuencias. Cabe resaltar que la secuencia de H. sapiens, difiere notablemente de las secuencias de insectos, lo que sugiere que es posible un desarrollo de ARNi altamente específico, aun cuando se compartan dominios como el de tirosina quinasa (TyrKc). Asimismo, hay diferencias nucleotídicas entre secuencias de insectos, que posiblemente predice regiones del dominio tirosina quinasa que son diferentes entre especies (Defferrari et al., 2018), por lo que la síntesis potencial de ARNi a partir de receptores de insulina puede llegar a ser altamente específico, por lo tanto ARNi se anticipa como una buena alternativa de control de insectos plaga.
En conclusión, con un par de cebadores inespecíficos de InR se logró identificar proteínas involucradas en la proliferación y diferenciación celular como Dip2A. Con lo que se cubre el primer paso para la síntesis de ARNi; sin embargo, se sugiere continuar con la búsqueda de InR específicos para el pulgón, así como posibles cebadores para regiones de Dip2A, y lograr un ARNi altamente específico. El diseño de cebadores puede acelerarse en cuanto sea posible tener la secuenciación y ensamble del genoma completo de Brevicoryne brassicae.
Agradecimientos
Se agradece a Maricela García Bautista y Anahí Canedo Téxon por el apoyo técnico y asesoría durante la fase experimental de laboratorio y bioinformática de este trabajo, de igual manera agradecemos a Remy Benoit Marie Vandame y a su equipo de trabajo por el acceso a equipo y reactivos de laboratorio. HUCM agradece al CONACyT por la beca 1000540 para estudios de posgrado. Este trabajo fue parcialmente financiado con fondos de la federación a través de proyecto “Ecología Evolutiva y Conservación” de El Colegio de la Frontera Sur.
Literatura citada
Altschul, S., Madden, T., Schäffer, A., Zhang, J., Zhang, Z., Miller, W., Lipman, D. (1997) Gapped BLAST and PSI-BLAST: a new generation of protein database search programs. Nucleic Acids Research, 25 (17), 3389-3402. https://doi.org/10.1093/nar/25.17.3389
Azevedo, S. V., Hartfelder, K. (2008) The insulin signaling pathway in honey bee (Apis mellifera) caste development-differential expression of insulin-like peptides and insulin receptors in queen and worker larvae. Journal of Insect Physiology, 54 (6), 1064-1071. https://doi.org/10.1016/j.jinsphys.2008.04.009
Blackman, R. L., Eastop, V. F. (2000) Aphids on the world’s crops, an identification and information guide. Second Edition, Wiley, Chichester, England, 251 pp.
Christiaens, O., Whyard, S., Vélez, A. M., Smagghe, G. (2020) Double-stranded RNA technology to control insect pests: current status and challenges. Frontiers in Plant Science, 11 (451), 1-10. https://doi.org/10.3389/fpls.2020.00451
Cooper, A. M. W., Silver, K., Zhang, J., Park, Y., Zhu, K. Y. (2019) Molecular mechanisms influencing efficiency of RNA interference in insects. Pest Management Science, 75, 18-28. https://doi.org/10.1002/ps.5126
Darrington, M., Dalmay, T., Morrison, N. I., Chapman, T. (2017) Implementing the sterile insect technique with RNA interference-a review. Entomologia Experimentalis et Applicata, 164 (3), 1-21. https://doi.org/10.1111/eea.12575
Defferrari, M. S., Da Silva, S. R., Orchard, I., Lange, A. B. (2018) A Rhodnius prolixus insulin receptor and its conserved intracellular signaling pathway and regulation of metabolism. Frontiers in Endocrinology, 9 (745), 1-17. https://doi.org/10.3389/fendo.2018.00745
Ding, B. Y., Shang, F., Zhang, Q., Xiong, Y., Yang, Q., Niu, J. Z., Smagghe, G., Wang, J. J. (2017) Silencing of two insulin receptor genes disrupts nymph-adult transition of alate brown citrus aphid. International Journal of Molecular Sciences, 18 (2), 2-14. https://doi.org/10.3390/ijms18020357
Dinkova, T. D., Sánchez de Jiménez, E. (2010) The ribosome: what we learned from its structure. Educación Química, 21 (1), 93-95. https://doi.org/10.1016/S0187-893X(18)30079-X
Duvaud, S., Gabella, C., Lisacek, F., Stockinger, H., Ioannidis, V., Durinx, C. (2021) Expasy, the Swiss bioinformatics resource portal, as designed by its users. Nucleic Acids Research , 49, 216-227. https://doi.org/10.1093/nar/gkab225
Edgar, R. C. (2004) MUSCLE: Multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Research , 32 (5), 1792-1797. https://doi.org/10.1093/nar/gkh340
Garofalo, R. S. (2002) Genetic analysis of insulin signaling in Drosophila. Trends in Endocrinology and Metabolism, 13 (4), 156-162. https://doi.org/10.1016/S1043-2760(01)00548-3
Guan, R. B., Li, H. C., Miao, X. X. (2018) Prediction of effective RNA interference targets and pathway-related genes in lepidopteran insects by RNA sequencing analysis. Insect Science, 25, 356-367. https://doi.org/10.1111/1744-7917.12437
Hall, T. (2011) BioEdit: An important software for molecular biology. GERF Bulletin of Biosciences, 2 (1), 60-61.
Han, J. E., Kathy, F. J., Tang, J. H. K. (2018) Use of beta-tubulin gene for phylogenetic analysis of the microsporidian parasite Enterocytozoon hepatopenaei (EHP) and development of a nested PCR as its diagnostic tool. Aquaculture, 495, 899-902. https://doi.org/10.1016/j.aquaculture.2018.06.059
Hebert, P. D. N., Penton, E. H., Burns, J. M., Janzen, D. H., Hallwachs, W. (2004) Ten species in one: DNA barcoding reveals cryptic species in the neotropical skipper butterfly Astraptes fulgerator. Proceedings of the National Academy of Sciences of the United States of America, 101 (41), 14812-14817. https://doi.org/10.1073/pnas.0406166101
Hernández, A., Martín, P., Torres, A., Salido, E. (1994) Análisis del RNA: Estudio de la expresión génica. Nefrología, 14 (2), 145-162.
Horton, P., Park, K. J., Obayashi, T., Fujita, N., Harada, H., Adams-Collier, C. J., Nakai, K. (2007) WoLF PSORT: Protein localization predictor. Nucleic Acids Research , 35, 585-587. https://doi.org/10.1093/nar/gkm259
Ishimaru, Y., Tomonari, S., Matsuoka, Y., Watanabe, T., Miyawaki, K., Bando, T., Tomioka, K., Ohuchi, H., Noji, S., Mito, T. (2016) TGF-β signaling in insects regulates metamorphosis via juvenile hormone biosynthesis. Proceedings of the National Academy of Sciences of the United States of America , 113 (20), 5634-5639. https://doi.org/10.1073/pnas.1600612113
Jensen, M., De Meyts, P. (2009) Molecular mechanisms of differential intracellular signaling from the insulin receptor. Vitamins and Hormones, 80, 51-75. https://doi.org/10.1016/S0083-6729(08)00603-1
Joga, M. R., Zotti, M. J., Smagghe, G., Christiaens, O. (2016) RNAi efficiency, systemic properties, and novel delivery methods for pest insect control: What we know so far. Frontiers in Physiology, 7 (553), 1-14. https://doi.org/10.3389/fphys.2016.00553
Koo, J., Chereddy, S. C., Palli, S. R. (2020) RNA interference-mediated control of cigarette beetle, Lasioderma serricorne. Archives of Insect Biochemistry and Physiology, 104 (4), 1-11. https://doi.org/10.1002/arch.21680
Leal-Aguilar, K., Ruiz-Montoya, L., Perales, H., Morales, H. (2008) Phenotypic plasticity of Brevicoryne brassicae in responses to nutritional quality of two related host plants. Ecological Entomology, 33, 735-741. https://doi.1111/j.1365-2311.2008.0103.x
Lin, X., Xu, Y., Jiang, J., Lavine, M., Lavine, L. C. (2018) Host quality induces phenotypic plasticity in a wing polyphenic insect. Proceedings of the National Academy of Sciences of the United States of America , 115 (29), 7563-7568. https://doi.org/10.1073/pnas.1721473115
Liu, Y. K., Luo, Y. J., Deng, Y. M., Li, Y., Pang, X. Q., Xu, C. D., Wang, S. G., Tang, B. (2020) Insulin receptors regulate the fecundity of Nilaparvata lugens (Stål). Journal of Asia-Pacific Entomology, 23 (4), 1151-1159. https://doi.org/10.1016/j.aspen.20200.09.011
Luan, J. B., Ghanim, M., Liu, S. S., Czosnek, H. (2013). Silencing the ecdysone synthesis and signaling pathway genes disrupts nymphal development in the whitefly. Insect Biochemistry and Molecular Biology, 43 (8), 740-746. https://doi.org/10.1016/j.ibmb.2013.05.012
Mamta, B., Rajam, M. V. (2017) RNAi technology: a new platform for crop pest control. Physiology and Molecular Biology of Plants, 23 (3), 487-501. https://doi.org/10.1007/s12298-017-0443-x
Nandety, R. S., Kuo, Y-W., Nouri, S., Falk, B. W. (2015) Emerging strategies for RNA interference (RNAi) applications in insects. Bioengineered, 6 (1), 8-19. https://doi.org/10.4161/21655979.2014.979701
Nässel, D. R., Broeck, J. V. (2016) Insulin/IGF signaling in Drosophila and other insects: factors that regulate production, release and post-release action of the insulin-like peptides. Cellular and Molecular Life Sciences, 73, 271-290. https://doi.org/10.1007/s00018-015-2063-3
Nicholson, S. J., Nickerson, M. L., Dean, M., Song, Y., Hoyt, R. P., Rhee, H., Kim, C., Puterka, G. J. (2015) The genome of Diuraphis noxia, a global aphid pest of small grains. BMC Genomics, 16 (429), 1-16. https://dx.doi.org/10.1186/s12864-015-1525-1
Noller, H. F. (2005) RNA structure: Reading the ribosome. Science, 309 (5740), 1508-1514. https://doi.org/10.1126/science.1111771
Núñez, F. J., Fornoni, J., Ruiz, M. L., Valverde, P. L. (2003) La evolución de la plasticidad fenotípica. Revista Especializada en Ciencias Químico-Biológicas, 6 (1), 16-24.
Olivares, J. A., Arellano, A. (2008) Bases moleculares de las acciones de la insulina. Revista de Educación Bioquímica, 27 (1), 9-18. Disponible en: https://www.medigraphic.com/pdfs/revedubio/reb-2008/reb081c.pdf (consultado el 5 marzo 2022).
Ouchi, N., Asaumi, Y., Ohashi, K., Higuchi, A., Sono-Romanelli, S., Oshima, Y., Walsh, K. (2010) DIP2A functions as a FSTL1 receptor. Journal of Biological Chemistry, 285 (10), 7127-7134. https://dx.doi.org/10.1074/jbc.M109.069468
Ponting, C. P. (1997) Evidence for PDZ domains in bacteria, yeast, and plants. Protein Science, 6, 464-468. https://doi.org/10.1002/pro.5560060225
Restrepo, J., Ortiz, L., Cardona, X., Olivera, M. (2012) Evaluación de la sensibilidad y especificidad del diagnóstico molecular del Staphylococcus aureus en leche de vacas afectadas por mastitis. Biosalud, 11 (2), 40-51. Disponible en: http://www.scielo.org.co/pdf/biosa/v11n2/v11n2a05.pdf (consultado el 3 junio 2022).
Ruíz, J. A., Bravo, M. E., Ramírez, O. G., Báez, G. A. D., Álvarez, C. M., Ramos, G. J. L., Nava, C. U., Byerly, M. K. F. (2013) Plagas de importancia económica en México: aspectos de su biología y ecología. Libro Técnico Núm. 2. INIFAP-CIRPAC-Campo Experimental Centro Altos de Jalisco. Tepatitlán de Morelos, Jalisco, 447 pp.
Ruíz-Montoya, L., Núñez, F. J. (2013) Testing local host adaptation and phenotypic plasticity in a herbivore when alternative related host plants occur sympatrically. PLoS ONE, 8 (11), 1-9. https://doi.org/10.1371/journal.pone.0079070
Saitou, N., Nei, M. (1987) The neighbor-joining method: a new method for reconstructing phylogenetic trees. Molecular Biology and Evolution, 4 (4), 406-425. https://doi.org/10.1093/oxfordjournals.molbev.a040454
Sandhi, R. K., Reddy, G. V. P. (2020) Biology, ecology, and management strategies for pea aphid (Hemiptera: Aphididae) in pulse crops. Journal of Integrated Pest Management, 11 (1), 1-20. https://doi.org/10.1093/jipm/pmaa016
Santiago-Lastra, J. A., Perales-Rivera, H. R. (2007) Producción campesina con alto uso de insumos industriales: El cultivo de repollo (Brassica oleracea var. Capitata) en Los Altos de Chiapas. Ra Ximhai, 3 (2), 481-507. https://doi.org/10.35197/rx.03.03.2007.03.js
Shan-Shan, G., Meng, Z., Tong-Xian, L. (2016) Insulin-related peptide 5 is involved in regulating embryo development and biochemical composition in pea aphid with wing polyphenism. Frontiers in Physiology , 7 (31), 1-13. https://doi.org/10.3389/fphys.2016.00031
Smykal, V., Pivarci, M., Provaznik, J., Bazalova, O., Jedlicka, P., Luksan, O., Horak, A., Vaneckova, H., Benes, V., Fiala, I., Hanus, R., Dolezel, D. (2020) Complex evolution of insect insulin receptors and homologous decoy receptors, and functional significance of their multiplicity. Molecular Biology and Evolution , 37 (6), 1775-1789. https://doi.org/10.1093/molbev/msaa048
Tanaka, M., Murakami, K., Ozaki, S., Imura, Y., Tong, X. P., Watanabe, T., Sawaki, T., Kawanami, T., Kawabata, D., Fujii, T., Usui, T., Masaki, Y., Fukushima, T., Jin, Z. X., Umehara, H., Mimori, T. (2010) DIP2 disco-interacting protein 2 homolog A (Drosophila ) is a candidate receptor for follistatin-related proteinfollistatin-like 1 - Analysis of their binding with TGF-β superfamily proteins. FEBS Journal, 277, 4278-4289. https://doi.org/10.1111/j.1742-4658.2010.07816.x
Vázquez-Jiménez, J. G., Roura-Guiberna, A., Jiménez-Mena, L. R., Olivares-Reyes, J. A. (2017) El papel de los ácidos grasos libres en la resistencia a la insulina. Gaceta Médica de México, 153, 852-863. https://doi.org/10.24875/GMM.17002714
Xu, H-J., Xue, J., Lu, B., Zhang, X-C., Zhuo, J-C., He, S-F., Ma, X-F., Jiang, Y-Q., Fan, H-W., Xu, J-Y., Ye, Y. X., Pan, P. L., Li, Q., Bao, Y. Y., Nijhout, H. F., Zhang, C. X. (2015) Two insulin receptors determine alternative wing morphs in planthoppers. Nature, 519, 464-467. https://doi.org/10.1038/nature14286
Yusupova, G. Z., Yusupov, M. M., Cate, J. H. D., Noller, H. F. (2001) The path of messenger RNA through the ribosome. Cell, 106, 233-241. https://doi.org/10.1016/S0092-8674(01)00435-4
Zhao, Y., Huang, G., Zhang, W. (2019) Mutations in NlInR1 affect normal growth and lifespan in the brown planthopper Nilaparvata lugens. Insect Biochemistry and Molecular Biology , 115, 103-246. https://doi.org/10.1016/j.ibmb.2019.103246
Notas de autor
*Autor corresponsal: Lorena Ruiz-Montoya. lruiz@ecosur.mx
Declaración de intereses
